Ana´lisis cuantitativo de insulina mediante
Anuncio

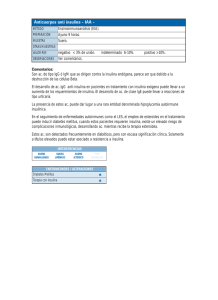
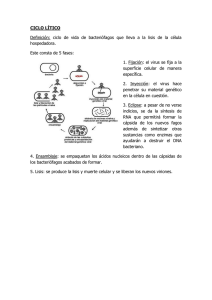
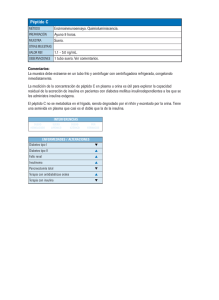
Clinical Chemistry 59:9 1349–1356 (2013) Endocrinologı́a y metabolismo Análisis cuantitativo de insulina mediante cromatografı́a de lı́quidos y espectrometrı́a de masas en tándem en un laboratorio clı́nico de alta capacidad Zhaohui Chen,1 Michael P. Caulfield,1 Michael J. McPhaul,1 Richard E. Reitz,1 Steven W. Taylor,1 y Nigel J. Clarke1* ANTECEDENTES: Las concentraciones de insulina en circulación reflejan la cantidad de insulina endógena producida por el páncreas y puede supervisarse para controlar la resistencia insulı́nica. La insulina se mide habitualmente mediante análisis inmunoquimioluminimétricos (ICMA). Desafortunadamente, las diversas reacciones cruzadas de los diferentes anticuerpos de ICMA han conducido a la variabilidad en los resultados de los análisis. En contraste, los métodos basados en cromatografı́a de lı́quidos y espectrometrı́a de masas en tándem (LC-MS/MS) pueden proporcionar una alternativa altamente especı́fica al inmunoanálisis. MÉTODOS: Se extrajo la insulina del suero del paciente y se la redujo para liberar la cadena B de la insulina. La posterior resolución del péptido se alcanzó mediantecromatografı́adelı́quidos(LC)juntoconespectrometrı́a de masas MS) de triple cuadrupolo. Se utilizó la supervisión de reacción seleccionada de las transiciones de cadena B para la cuantificación. Se utilizó insulina humana recombinante como calibrador y se comparó con el patrón de referencia del National Institute for Biological Standards and Control (Instituto Nacional de Control y Normas Biológicas, NIBSC). Se utilizó insulina bovina y una cadena B de la insulina humana con marcado radioactivo estable (13C/15N) y se compararon como patrones internos. RESULTADOS: El análisis de LC-MS/MS que se describe en el presente se validó de acuerdo con las directrices de CLIA (Enmiendas de Mejora de Laboratorios Clı́nicos) con un lı́mite de detección de 1.8 IU/ml (10.8 pmol/l) y un lı́mite de cuantificación de 3 IU/ml (18.0 pmol/ l). Se realizó una correlación entre el análisis de LCMS/MS y un análisis de ICMA aprobado por la Administración de Medicamentos y Alimentos de los EE. UU. (FDA) para las muestras de los pacientes y la re- 1 Quest Diagnostics Nichols Institute, San Juan Capistrano, CA. * Dirigir correspondencia para estos autores a: Quest Diagnostics Nichols Institute, 33068 Ortega Hwy, San Juan Capistrano, CA, 92675. Fax 949-728-4872; correo electrónico: [email protected]. gresión de Deming demostró una buena concordancia. Se estableció un intervalo de referencia para el análisis. CONCLUSIONES: Se desarrolló y validó de forma correcta un análisis de insulina de LC-MS/MS cuantitativo, simple y de alta capacidad certificado por patrón del NIBSC. © 2013 American Association for Clinical Chemistry La detección de individuos con prediabetes y diabetes puede realizarse al medir las concentraciones de glucosa en ayunas, glucohemoglobina e insulina en ayunas, y las concentraciones de glucosa luego de una carga glucémica por vı́a oral. Cada uno de estos métodos es eficaz pero todos presentan inconvenientes. Las concentraciones de glucosa en ayunas que no se encuentran dentro de los intervalos de referencia reflejan un estado fisiológico en el cual ya se ha presentado la diabetes temprana. Los incrementos en la hemoglobina A1C pueden reflejar las últimas etapas de prediabetes o diabetes sintomática. La prueba oral de tolerancia a la glucosa puede identificar la resistencia insulı́nica más temprano pero involucra una prueba dinámica más complicada y no siempre es tributaria del entorno de pruebas clı́nicas. Se ha sugerido la medición de insulina en suero en ayunas dado que puede proporcionar una prueba rápida y de fácil acceso para complementar otras metodologı́as existentes. De hecho, diversos estudios han demostrado mayores concentraciones de insulina en ayunas en pacientes con prediabetes, incluso en ausencia de aumentos de glucosa y hemoglobina A1C en ayunas (1–5 ). En un número limitado de casos, se ha sugerido la utilidad de las mediciones de insulina en ayunas para detectar la resistencia insulı́nica temprana (2, 6 ). Recibido para la publicación el 20 de noviembre de 2012; aceptado para la publicación el 26 de abril de 2013. Previously published online at DOI: 10.1373/clinchem.2012.199794 1349 Las técnicas inmunológicas se han usado ampliamente para la cuantificación de la insulina, inicialmente a través del radioinmunoanálisis y más recientemente mediante análisis inmunoquimioluminimétricos (ICMA)2 disponibles en el mercado en plataformas automatizadas (7 ). Sin embargo, aún no se ha establecido un método de referencia internacional para la insulina. El mayor obstáculo en el establecimiento de tal método surge de la variabilidad en los valores de la insulina medidos en comparación con diferentes inmunoanálisis y plataformas. Los valores medidos pueden diferir por un factor de 2 para el mismo patrón de insulina humana de la OMS (7 ). Las diferencias en los resultados de las diversas plataformas de ICMA con frecuencia están causadas por las diferentes reacciones cruzadas de los anticuerpos utilizados del análisis. Asimismo, los autoanticuerpos o anticuerpos heterófilos presentes en la muestra del paciente pueden causar sesgos en las concentraciones de insulina informadas. Los análisis de péptidos y proteı́nas basados en espectometrı́a de masas (MS) se han desarrollado recientemente como importantes estrategias alternativas para el análisis clı́nico de biomoléculas (8 ), incluida la insulina. Debido a que la insulina está presente en la sangre humana en concentraciones muy bajas, la mayorı́a de los métodos de MS anteriormente desarrollados para la detección y cuantificación de polipéptidos han dependido de las metodologı́as de captura inmunológica (9 –15 ). Sin embargo, las recientes mejoras en la sensibilidad de la MS niegan la necesidad del enriquecimiento basado en anticuerpos sin comprometer la alta especificidad. En consecuencia, el método que hemos desarrollado no requiere anticuerpos de captura mientras aún proporciona un análisis altamente especı́fico y sensible para la insulina humana a través del análisis de control selectivo de reacción (SRM) en un espectómetro de masas de triple cuadrupolo. La insulina humana madura (peso molecular, 5808 Da) consta de 2 cadenas peptı́dicas (A y B) ligadas por 2 enlaces disulfuro. Las cadenas A (peso molecular 2377 Da) y B (peso molecular, 3431 Da) de insulina pueden separase mediante el uso de agentes reductores adecuados. Se ha estudiado ampliamente la cadena B de la insulina; sin embargo, no se ha desarrollado un análisis cuantitativo para el péptido (12, 16, 17 ). Nuestro objetivo fue el de desarrollar un análisis para la cuantificación de las concentraciones de insulina total en el 2 Abreviaturas no estándar: ICMA, análisis inmunoquimioluminimétricos; MS, espectrometrı́a de masas; SRM, control de la reacción seleccionada; LC-MS/MS, cromatografı́a de lı́quidos y espectrometrı́a de masas en tándem; TCEP, tris-(2carboxietil)-fosfina; NIBSC, Instituto Nacional de Control y Normas Biológicas; IS, estándar interno; FDA, Administración de Medicamentos y Alimentos de los EE. UU; SPE, extracción en fase sólida; LOD, lı́mite de detección; LOQ, lı́mite de cuantificación. 1350 Clinical Chemistry 59:9 (2013) suero humano mediante la cuantificación de la cadena B luego de la reducción y liberación de la molécula intacta. En el presente, informamos la validación de este análisis y los estudios del intervalo de referencia para respaldar la medición clı́nica de alta capacidad de la insulina mediante cromatografı́a de lı́quidos y espectrometrı́a de masas en tándem (LC-MS/MS). Materiales y métodos PATRONES Y REACTIVOS Se utilizó agua, acetona, etanol, isopropanol y acetonitrilo de calidad HPLC de Burdick and Jackson; el metanol y la solución inhibidora de la adhesión tris-(2carboxietil)-fosfina (TCEP) fueron de Thermo Fisher Scientific. El ácido fórmico de alta pureza fue de Fluka. El patrón de insulina humana de la OMS (código: 66/ 304) fue del National Institute for Biological Standards (Instituto Nacional de Control y Normas Biológicas, NIBSC). La insulina humana recombinante fue de Millipore. La insulina bovina (⬎95% de pureza) y la solución de base de 1.5 mol/l Tris (Trizma) fueron de Sigma. La cadena B de la insulina con marcado isotópico totalmente sintética fue de Anaspec (consulte la Fig. 1 de los Datos complementarios que acompañan la versión en lı́nea de este informe en http://www. clinchem.org/content/vol59/issue9). El suero humano Hypo-Opticlear tratado sin insulina fue de los laboratorios Biocell. Todos los componentes proteicos se caracterizaron completamente mediante electroforesis en gel, HPLC y MS por parte de los fabricantes. El análisis de aminoácidos estuvo a cargo de AAA Service Laboratory Inc. para confirmar el contenido proteico antes del uso. PREPARACIÓN DE CALIBRADORES, CONTROLES Y PATRONES INTRENOS Se preparó una solución matriz del patrón de insulina humana (insulina humana recombinante excepto indicación en contrario) a 1 IU/ml (6 mol/l) en 0.2% de solvente de ácido fórmico y se almacenó a ⫺80 °C hasta su uso. Inmediatamente antes del análisis, se descongeló la solución matriz y se diluyó una parte en el suero humano tratado sin insulina a una concentración final de 4000 IU/ml (24 nmol/l). Las diluciones se realizaron posteriormente a fin de generar una serie de calibración a concentraciones de 5.0, 10, 15, 25, 50, 100, 200 y 300 IU/ml (30.0 –1800 pmol/l). Las reservas de QC internas se realizaron mediante el uso de insulina humana recombinante de Millipore, disuelta en 0.2% de ácido fórmico y almacenada a ⫺80 °C. La concentración de insulina de estas reservas se verificó mediante análisis de aminoácidos antes de la dilución. Se realizaron cinco determinaciones durante Análisis cuantitativo de la insulina Figura 1. Ejemplo de cromatogramas en el suero de un paciente (40.6 IU/ml o 243.6 pmol/l). El tiempo de retención real es 4.8 min. RT: tiempo de retención; AA: área; SN: relación señal ruido; BP: pico de base; NL: mayor normalizado; TIC: corriente total de iones un perı́odo de 6 meses con un coeficiente de variación (CV) del 3%. Los controles de QC (8, 16, 40 y 80 IU/ml o 48 – 480 pmol/l) se realizaron al agregar suero humano tratado Hypo-Opticlear a las concentraciones objetivo y luego almacenarlas en partes a ⫺80 °C. Los controles y calibradores de QC de insulina recién hechos se evaluaron mediante comparación con el material de referencia de NIBSC. Cada parte de QC se usó solo una vez después del descongelamiento para evitar los ciclos de congelamiento y descongelamiento. Los patrones internos (IS) se prepararon en 0.2% de ácido fórmico a una concentración de 10 mol/l. Se agregó insulina bovina (350 pmol) al suero durante la extracción (antes de la reducción) y se agregó la cadena B humana con marcado isotópico (115 pmol) al extracto reducido antes de la CL. APROBACIÓN DE LOS PARTICIPANTES DEL ESTUDIO EN HUMANOS Las muestras de suero se obtuvieron de participantes del estudio sanos luego del consentimiento informado y se almacenaron a ⫺80 °C hasta su uso [aprobación n.o 1085473 de Western Institutional Review Board (Junta de Revisión Institucional Occidental)]. El uso de muestras desechadas anónimas en estos estudios estuvo bajo la revisión del Western Institutional Review Board y se consideró eximido. OBTENCIÓN DE MUESTRAS CLÍNICAS Excepto indicación en contrario, la sangre se obtuvo en tubos de preparación de suero sin separación (tapón rojo) y se permitió la coagulación. El suero obtenido se Clinical Chemistry 59:9 (2013) 1351 proceso inmediatamente y se almacenó a ⫺80 °C hasta el análisis. PREPARACIÓN DE LAS MUESTRAS El suero del paciente se descongeló y se mezcló en vórtex, y se mezclaron enérgicamente 150 l con 350 l de etanol básico (85% etanol, 15% base Tris) y se permitió la incubación durante 60 min a ⫺20 °C. El precipitado obtenido se granuló mediante centrifugación durante10 min a 5200 g. Luego, se mezcló el supernadante clarificado (250 l) con 20 l de solución inhibidora de TCEP (Thermo Fisher Scientific), que se usó conforme a las indicaciones del fabricante para liberar las cadenas A y B de la insulina mediante la reducción de sus enlaces disulfuro. CROMATOGRAFÍA ANALÍTICA Y PREPARATIVA AUTOMATIZADA La separación analı́tica de la cadena B de la insulina de los componentes de la matriz antes de espectometrı́a de masas se realizó mediante TurboFlow Aria TLX-4 (Thermo Fisher), un sistema de cromatografı́a de lı́quidos en lı́nea completamente automatizado. Las 4 columnas en este sistema de cromatografı́a de lı́quidos se operan en paralelo y facilitan el alto rendimiento. Se llevo a cabo la preparación y el enriquecimiento de las muestras mediante extracción en fase sólida (SPE) en lı́nea mediante una columna Oasis HLB tipo cartucho (2.1 ⫻ 20 mm, 25 m) (Waters) (consulte la Fig. 2 complementaria en lı́nea). La resolución cromatográfica se realizó con una columna Magic C4 (2.1 ⫻ 50 mm, 5 m, 300 Å) (Bruker- Michrom). Para las columnas analı́ticas y de SPE, utilizamos el mismo solvente A (agua, 0.2% ácido fórmico) y B (acetonitrilo, 0.2% ácido fórmico). Después de la inyección del extracto (225 l) a 4 ml/min, se lavó el cartucho con solvente B al 12% durante otros 60 s. A continuación, se realizó el retrolavado de los analitos fuera del cartucho de extracción con un gradiente escalonado de solvente B al 35% a 0.8 ml/min y volvió a centrarse la atención en la columna analı́tica mediante una válvula T con una proporción de flujo de 3:1 entre las bombas de elución (0.6 ml/min) y de carga (0.2 ml/min), respectivamente. Finalmente, la resolución de los analitos se realizó con un gradiente lineal rápido de 12% a 42% del solvente B a 0.5 ml/min durante 3 min. ADQUISICIÓN Y PROCESAMIENTO DE DATOS Se utilizó un espectómetro de masas de triple cuadrupolo TSQ Vantage (ThermoFisher) interconectado al sistema TLX-4 con una sonda ESI como detector de MS/MS. Los datos se obtuvieron mediante SRM en modo de iones positivos bajo las siguientes condiciones: voltaje de ionización: 4800 V; presión del gas de impulsión: 50 (unidades arbitrarias); presión del gas auxiliar: 25 (unidades arbitrarias); temperatura capilar: 1352 Clinical Chemistry 59:9 (2013) 250 °C. El ajuste de los instrumentos en Xcalibur incluyó el modo de exploración positivo con el filtro Chrom activado y configurado en 10; amplitud de la exploración: 0.5 m/z; tiempo de exploración: 0.1 s; gas de colisión: 1.5 mTorr; y la amplitud de ambos valores máximos Q1 y Q3 configurada en 0.7. La naturaleza distintiva de la secuencia de aminoácidos para la cadena B de la insulina se confirmó al realizar una búsqueda mediante la herramienta BLAST (Basic Local Alignment Search Tool, herramienta de búsqueda de alineaciones locales básicas) (18 ) (http:// blast.ncbi.nlm.nih.gov/Blast.cgi). En este análisis, consideramos el tiempo de retención y la proporción de las transiciones de masas (1:1, con una tolerancia del ⫾20%) para admitir la identificación de la cadena B. Para el análisis cuantitativo, se utilizó el pico isotópico más intenso del ion MH5⫹5 de la cadena B de la insulina [m/z 686.9 (0.2)] como ion precursor (consulte la Fig. 3 complementaria en lı́nea). Las transiciones a b14⫹2 [768.5 (0.2)] y a y13⫹2 [753.2 (0.2)] de la cadena B de la insulina, con óptimas energı́as de colisión de 21 y 19 V, respectivamente, se supervisaron mediante SRM para mejorar la selectividad. Las correspondientes transiciones para los IS fueron de 680.8 (0.2) a 768.5 (0.2), 738.3 (0.2) para la insulina bovina y de 688.1 (0.2) a 768.5 (0.2), 756.0 (0.2) para la cadena B de la insulina humana con marcado isotópico. Para mejorar la sensibilidad, se resumieron las áreas de valor máximo de cada transición para cada péptido. Se utilizó la proporción del área de valor máximo del analito respecto del IS (excepto indicación en contrario, se empleó la cadena B de la insulina humana con marcado isotópico como IS) para calcular las concentraciones de la curva estándar. Se utilizó un modelo lineal (1/x) para la generación de la curva estándar mediante regresión lineal. Los resultados se informaron como la concentración de insulina (IU/ml o pmol/l; 1 IU/ml ⫽ 6 pmol/l). Las herramientas de software utilizadas fueron TSQ Vantage 2.0.0, Tune Master V 2.0.0, Xcalibur V 2.0.7. SP1, LC Quan V 2.5.6. SP1 y XReport 2.0.7. Se utilizó SP1 y ARIA OS V 1.6.1 (ThermoFisher) para la adquisición y el procesamiento de datos. COMPARACIÓN DEL MÉTODO El método de LC-MS/MS se comparó con una plataforma comercial (Beckman Access® ICMA) aprobada por la Administración de Medicamentos y Alimentos de los EE. UU. (FDA) [limite de detección (LOD) 0.13 IU/ml; lı́mite de cuantificación (LOQ) 0.3 IU/ml] para la medición de la insulina en pacientes (n ⫽ 89). Las muestras de estos pacientes fueron descartes sin identificación presentados anteriormente para análisis clı́nicos de rutina. Las concentraciones medidas cubrieron los intervalos de referencia de la insulina humana previstos y los excedieron de concentraciones bajas a Análisis cuantitativo de la insulina Figura 2. Comparación del método (regresión de Deming) de LC-MS/MS y la plataforma de ICMA aprobada por la FDA en 89 muestras de pacientes. concentraciones muy altas de insulina. La correlación de los 2 métodos se evaluó mediante el uso de la regresión de Deming. DETERMINACIÓN DEL INTERVALO DE REFERENCIA Se determinó un intervalo de referencia para el análisis de LC-MS/MS mediante el uso de suero obtenido en tubos de tapón rojo de 97 voluntarios sanos seleccio- nados cuidadosamente (51 mujeres, 46 hombres de entre 18 a 65 años de edad, empleados de Quest Diagnostics y ajenos a la firma). Se utilizaron los siguientes criterios de inclusión: adultos aparentemente sanos, ambulatorios, no medicados que viven en la comunidad. Los criterios de exclusión fueron los siguientes: cualquier trastorno endocrino, glucosa en ayunas ⬎100 mg/dl (⬎5.55 mmol/l) e insulina libre más alta Clinical Chemistry 59:9 (2013) 1353 Figura 3. Un intervalo de referencia para la insulina determinado mediante LC-MS/MS para 97 donantes sanos. de lo normal (⬎20 IU/ml o 120 pmol/l) detectada por la plataforma de ICMA actual. TIPO DE MUESTRA Y ESTABILIDAD Se evaluaron seis tipos de tubos de obtención de muestras (para suero con tapón rojo simple, tubos separadores de suero, plasma EDTA, plasma con heparina sódica, plasma con heparina de litio y plasma con citrato de sodio) con muestras extraı́das de 10 individuos y se analizaron mediante el análisis de LC-MS/MS. La estabilidad de la muestra se evaluó en el suero a lo largo del tiempo con los siguientes intervalos de temperatura: congelado ultrabajo (⫺60.0 a ⫺90.0 °C), congelado (⫺10.0 a ⫺30.0 °C), refrigerado (2.0 a 8.0 °C) y temperatura ambiente (18.0 a 26.0 °C). La estabilidad del congelamiento y descongelamiento se evaluó mediante el uso de muestras de suero de 10 pacientes individuales. Se obtuvo una muestra inicial sin congelamiento (ciclo 0) y 5 muestras adicionales estuvieron sujetas a los ciclos de congelamiento y descongelamiento de repetición (1–5 ). La estabilidad de la muestra se completó al evaluar la diferencia media entre el valor inicial y el valor temporal/de temperatura de la muestra dentro de un intervalo aceptable del 80% al 120%. Resultados EFICACIA DEL PATRÓN INTERNO Se prefirió inicialmente la cadena B de la insulina marcada para el análisis dado que es quı́micamente una correspondencia para la cadena B endógena. El péptido 1354 Clinical Chemistry 59:9 (2013) marcado se agregó a todas las muestras extraı́das, QC y calibradores conforme a la descripción en Materiales y métodos antes del análisis en el sistema de LC-MS/MS y se utilizó para normalizar los resultados de la espectometrı́a de masas cuantitativa. Sin embargo, a fin de corregir la posibilidad de la reducción incompleta de la insulina, también utilizamos insulina bovina inalterada como IS indirecto agregado al inicio de la preparación de la muestra para justificar cualquier pérdida de procedimiento durante los procesos de extracción y reducción. La Fig. 1 muestra los cromatogramas de SRM correspondientes a la cadena B de la insulina bovina coeluı́da, humana endógena y humana con marcado isotópico, respectivamente. Ambos IS demostraron consistencia en la respuesta de la señal a lo largo del tiempo y la regresión de Deming de 51 pacientes sugirió la misma idoneidad (consulte la Fig. 4 complementaria en lı́nea). Finalmente, elegimos la insulina bovina como el IS predeterminado dado que presenta una intensidad superior de valor máximo y costo además de corregir la posibilidad de la reducción incompleta. El beneficio de la utilización de un IS está demostrada en la Fig. 5 complementaria en lı́nea. Se observó la correlación de los resultados de LC-MS/MS con los resultados del análisis de ICMA mediante regresión de Deming para mejorar de forma considerable la curva, con una reducción de 1.36 (sin IS) a 1.07 (IS bovino). RENDIMIENTO DEL ANÁLISIS Las especificaciones del rendimiento analı́tico se resumen en la Tabla 1. El análisis demuestra una relación lineal dentro del lı́mite de declaración obligatoria de 5 a 300 IU/ml (30 –1800 pmol/l), con R2 de 0.9989. Determinamos el LOQ de la insulina mediante el análisis de 6 muestras diferentes a concentraciones próximas al LOQ previsto [1.25, 2.5, 5, 10, 15 y 25 IU/ml (1 IU/ ml ⫽ 6 pmol/l)] y la posterior evaluación de la reproducibilidad intranalı́tica en 7 series. La menor concentración que arrojó un rendimiento aceptable fue 3 IU/ml (18 pmol/l), para la cual el IC de 95% para el CV se mantuvo por debajo del 20%. Se midió un blanco 14 veces y los cocientes de área obtenidos se calcularon nuevamente para establecer un LOD (4 SD de la concentración cero) de 1.8 IU/ml (10.8 pmol/l) para la insulina y un lı́mite de blanco (2 SD de la concentración cero) de 1.4 IU/ml (8.4 pmol/l) para la insulina en suero tratado. La confirmación la identificación de la cadena B de la insulina se estableció como se describe en Métodos. Las proporciones de transición de masas fuera de los lı́mites de tolerancia definidos se encontraron en ⬍3% de las muestras de pacientes. No se observó arrastre detectable para las concentraciones por debajo de 500 IU/ml (3000 pmol/l). La precisión y exactitud intranalı́ticas para QC se generaron me- Análisis cuantitativo de la insulina Tabula 1. Rendimiento del análisis de LC-MS/MS para la insulina. LOBa Sensibilidad Precisión LOD 1.4 IU/ml (8.4 pmol/l) 1.8 IU/ml (10.8 pmol) 3.0 IU/ml (18.0 pmol) Insulina en suero tratado, IU/ml (pmol/l) % CV interanalı́tico, exactitud (n ⴝ 8) % CV intranalı́tico, exactitud (n ⴝ 8) 8 (48) 14.0, 91.3 7.0, 80.0 12 (72) 10.2, 91.2 7.9, 92.2 20 (120) 10.0, 87.0 6.0, 86.5 40 (240) 7.5, 87.7 4.0, 87.6 7.1, 96.3 3.0, 92.1 80 (480) Recuperación a LOQ Insulina en suero, IU/ml (pmol/l) % recuperación media (SD) (n ⴝ 3) 8 (48) 93.8 20 (120) 113.3 48 (288) 99.4 LOB, lı́mite de blanco. diante el análisis de 8 reproducciones. Los CV variaron del 3.0% al 7.9%, con una exactitud intranalı́tica que varió del 80% al 92%. La variación intranalı́tica durante 5 dı́as varió del 7.1% al 14.0% y la exactitud intranalı́tica varió del 87% al 96%. El rendimiento del análisis también se evaluó mediante experimentos de enriquecimiento y recuperación en el suero del paciente y se detectó una recuperación general del 94% al 113% en el intervalo medido (Tabla 1). COMPARACIÓN DEL MÉTODO Para hacer referencia al análisis, realizamos un análisis de correlaciones entre el análisis de LC-MS/MS y un análisis de ICMA aprobado por la FDA mediante la utilización de 89 descartes de pacientes sin identificación en todo el intervalo de concentración de la insulina de 3 a 180 IU/ml (18 a 1080 pmol/l). La regresión de Deming de este estudio demostró una buena concordancia entre el nuevo método de LC-MS/MS y el análisis de ICMA (y ⫽ 1.15x ⫺ 0.89) (Fig. 2). DETERMINACIÓN DEL INTERVALO DE REFERENCIA En esta investigación, usamos muestras de 97 donantes sanos cuidadosamente seleccionados para realizar un estudio de intervalo de referencia (Fig. 3). Se demostró que los datos fueron no gausianos. Los datos del porcentil 95 se usaron para establecer un intervalo de referencia de ⬍13.7 IU/ml (82.2 pmol/l). QC DEL ANÁLISIS Utilizamos procedimientos de QC conforme a las reglas de Westgard en el análisis para determinar las series correctas en comparación con las incorrectas, ası́ como para identificar los sesgos en los datos atribuibles a los problemas analı́ticos. Se evaluaron los controles de QC desde 2 fuentes diferentes. La primera fueron controles de TDM/inmunoanálisis Bio-Rad, muestras de suero de QC con concentraciones conocidas de insulina. El segundo tipo de muestra de QC fue una reserva de suero interna con baja concentración de insulina que preparamos al determinar la concentración de insulina luego de combinar el suero de una amplia población de donantes. Los márgenes para los controles Bio-Rad y suero de QC interno se determinaron para cada lote nuevo. Los márgenes de trabajo para los QC se establecieron al medir algunas observaciones de 50 –70 por nivel y en varias reproducciones durante 5 dı́as. Los resultados se analizaron estadı́sticamente para obtener los valores medios (16.1, 46.5 y 189.5 IU/ml o 96.6, 279 y 1137 pmol/l) y los CV para cada nivel de QC (17.4%, 12.4% y 8.2%, respectivamente). Estos datos se utilizaron posteriormente para definir los lı́mites de SD 2 y 3 para la aceptabilidad del QC. Durante el análisis de las muestras, se probaron todos los niveles de QC al inicio de cada análisis con varias reproducciones de los QC intercaladas en todo el análisis y, de ese modo, se asociaron las muestras de pacientes. TIPO DE MUESTRA Y ESTABILIDAD Se realizó la validación del análisis de insulina para el suero humano obtenido en tubos con tapón rojo simples. Una comparación de concentraciones de insulina determinada en la sangre obtenida en diferentes tipos de tubos demostró que la heparina sódica y de litio arrojaron resultados equivalentes y; por lo tanto, son tipos de muestras aceptables (no se muestran datos). Clinical Chemistry 59:9 (2013) 1355 Las condiciones de almacenamiento de las muestras se evaluaronentérminosdelareproducibilidadenlacuantificación a lo largo del tiempo y las mediciones aceptables estuvieron comprendidas entre ⫾20% del dı́a 0 (consulte la Fig. 6 complementaria en lı́nea). La insulina en el suero de los pacientes fue estable durante al menos 86 dı́as a ⫺80 °C. Sin embargo, a ⫺20 °C se observó que las concentraciones de insulina medidas en una porción de las muestras de suero se redujeron después del almacenamiento de las muestras durante 35 dı́as. La insulina fue estable en suero durante solo 1 dı́a a temperatura ambiente. Además, las concentraciones de insulina en algunas muestras parecieron disminuir el segundo dı́a de almacenamiento a temperaturas refrigeradas, como lo indica el aumento de SD, mientras que las muestras de otros pacientes demostraron una estabilidad ejemplar. Después de analizar los resultados de estabilidad, se determinó que las muestras del análisis de insulina de LC-MS/MS debı́an almacenarse y enviarse congeladas a ⫺20 °C o una temperatura inferior para el corto plazo (menos de 1 mes). El almacenamiento a más largo plazo debe ser a ⫺80 °C o una temperatura inferior. Finalmente, los datos indican que las concentraciones de insulina no sufrieron alteraciones en los 5 ciclos de congelamiento y descongelamiento (consulte la Fig. 6 complementaria en lı́nea). ESTUDIOS DE INTERFERENCIA Llevamos a cabo estudios de interferencia mediante la realización de exámenes del suero tratado de diferentes fuentes ası́ como las pruebas de más de 100 muestras de pacientes para buscar interferencias no especı́ficas. También se investigaron los efectos de los diferentes grados de hemólisis, lipemia y bilirrubina (leve, moderada o grave) en la exactitud de las mediciones de la insulina. Los efectos de la hemólisis, lipemia y bilirrubina en las determinaciones de la insulina se evaluaron al agregar diferentes concentraciones de insulina en muestras de pacientes con hemólisis, lipemia y bilirrubina baja, media y alta. Se utilizó un nivel de aceptación del 80% al 120% de recuperación para evaluar si el análisis se vio afectado de forma adversa por la interferencia. No se observó dependencia entre las concentraciones de insulina y el nivel de lipemia o concentración de bilirrubina. En contraste, hubo recuperaciones no aceptables de insulina de suero totalmente hemolizado. Por lo tanto, la hemólisis constituyó un criterio para el rechazo de la muestra (no se muestran datos). Análisis La aplicación de HPLC interconectada con la MS para el análisis de proteı́nas y péptidos en el entorno de laboratorio clı́nico siempre ha representado un gran desafı́o en comparación con los inmunoanálisis automatizados actuales basados en anticuerpos. La insulina demostró no 1356 Clinical Chemistry 59:9 (2013) ser una excepción a esta observación. Primero, cualquier nuevo análisis debe proporcionar una excelente selectividad y especificidad independientemente de la complejidad del suero humano. Segundo, el intervalo usual de concentración de insulina en la sangre humana es bastante bajo; algunos inmunoanálisis tienen menores LOQ hasta de 2 IU/ml, equivalente a 1.8 fmol de insulina en 150 l de suero que utilizamos para nuestro análisis. Tercero, cualquier análisis que vaya a utilizarse de forma habitual en un laboratorio clı́nico debe ser simple y altamente reproducible ası́ como sólido y capaz de adaptar un elevado número de muestras. Cada serie de LC demora ⬍8 min y al realizar la multiplexación del análisis, pueden obtenerse los datos para cada muestra en 2 min. En promedio, una placa de 96 pocillos demora ⬍4 h en ejecutarse. El rendimiento en la preparación de las muestras está determinado por los pasos de extracción y reducción e incubación (aproximadamente 2 h). Por lo tanto, hemos desarrollado un método de LC-MS/MS que cumple con todos los criterios para el uso habitual en un laboratorio clı́nico. Una caracterı́stica distintiva del análisis de insulina de LC-MS/MS es la uniformidad y armonización de la norma para la insulina del NIBSC y la insulina humana recombinante sintetizada. La mención al reactivo de referencia de la OMS como criterio de referencia adquirido directamente del NIBSC con una actividad biológica designada de 3 IU por frasco deberı́a ayudar a evitar los problemas de estandarización que han plagado los inmunoanálisis basados en anticuerpos actualmente disponibles, cada uno de los cuales utiliza sus propias normas de trabajo desarrolladas por los fabricantes. El análisis se ha validado y cumple con la polı́tica interna conforme a las directrices 88 493.1253 de CLIA, con un LOD de 1.8 IU/ml (10.8 pmol/l) y un menor LOQ de 3 IU/ml (18.0 pmol/l). Para confirmar la aplicabilidad de este análisis, se realizó una correlación entre el análisis de LC-MS/MS y un análisis de ICMA aprobado por la FDA, y la regresión de Deming obtenida demostró una buena concordancia entre ambos métodos en el intervalo de concentración menor. También se estableció un nuevo intervalo de referencia para el análisis de LC-MS/MS. La metodologı́a para este análisis involucra la reducción de la insulina inalterada y la medición de la cadena B libre. Este método proporciona información valiosa para la distinción de la insulina endógena de los análogos de la insulina terapéutica. Todas las formas sintéticas comerciales de insulina tienen alteraciones que afectan los aminoácidos C-terminal en la cadena B. Los filtros de masa de SRM usados proporcionan detalles estructurales moleculares que confirman la autenticidad de la señal de la cadena B de la insulina medida, mientras que ignoran los análogos sintéticos, habitualmente detectados como insulina con el uso de Análisis cuantitativo de la insulina métodos inmunológicos (inédito). Asimismo, el requisito de que los inmunoanálisis no reconozcan la proinsulina también se lleva a cabo por la selectividad del método de cuantificación basado en SRM (19 ). plido con los siguientes 3 requerimientos: (a) contribuciones significativas a la concepción y el diseño, la adquisición de datos o el análisis e interpretación de estos; (b) redacción o revisión del artı́culo en relación con su contenido intelectual; y (c) aprobación final del artı́culo publicado. Conclusión Declaración de los autores o posibles conflictos de interés: Tras la presentación del manuscrito, todos los autores completaron el formulario de declaración del autor. Declaraciones o posibles conflictos de interés: Se desarrolló y validó de forma correcta un análisis de insulina cuantitativo, simple y de alta capacidad con cromatografı́a de lı́quidos y espectrometrı́a de masas en tándem certificado por patrón del NIBSC conforme a las directrices de CLIA. El método combina la especificidad molecular con el rendimiento cuantitativo y el análisis estandarizado y proporciona intervalos de referencia, lo que convierte a este método en un candidato para considerar como método de referencia para las pruebas de insulina (19, 20 ). Contribuciones de los autores: Todos los autores confirmaron que han contribuido al contenido intelectual de este documento y han cum- Empleo o liderazgo: Z. Chen, Quest Diagnostics; M.P. Caulfield, Quest Diagnostics; M.J. McPhaul, Quest Diagnostics Nichols Institute; R.E. Reitz, Quest Diagnostics Nichols Institute; S.W. Taylor, Quest Diagnostics; N.J. Clarke, Quest Diagnostics. Papel del consultor o asesor: No se declara. Propiedad de acciones: Z. Chen, Quest Diagnostics; M.P. Caulfield, Quest Diagnostics; R.E. Reitz, Quest Diagnostics; N.J. Clarke, Quest Diagnostics. Honorarios: No se declara. Financiamiento de la investigación: No se declara. Testimonio de expertos: No se declara. Patentes: Z. Chen, Quest Diagnostics, 20120164741 (solicitud); N.J. Clarke, Quest Diagnostics, 20120164741 (solicitud). Papel del patrocinador: No se declaró ningún patrocinador. Referencias 1. Dankner R, Chetrit A, Shanik MH, Raz I, Roth J. Basal-state hyperinsulinemia in healthy normoglycemic adults is predictive of type 2 diabetes over a 24-year follow-up: a preliminary report. (La hiperinsulinemia basal en adultos normoglucémicos sanos indica diabetes tipo 2 durante un seguimiento de 24 horas: un informe preliminar). Diabetes Care 2009;32:1464 – 6. 2. Johnson JL, Duick DS, Chui MA, Aldasouqi SA. Identifying prediabetes using fasting insulin levels. (Identificación de la prediabetes mediante la utilización de niveles de insulina en ayunas). Endocr Pract 2010;16:47–52. 3. Wang H, Shara NM, Calhoun D, Umans JG, Lee ET, Howard BV. Incidence rates and predictors of diabetes in those with prediabetes: the Strong Heart Study. (Tasas de incidencia y predictores de la diabetes en aquellas personas con prediabetes: el estudio Strong Heart Study). Diabetes Metab Res Rev 2010;26:378 – 85. 4. Drzewoski J, Czupryniak L. Concordance between fasting and 2-h post-glucose challenge criteria for the diagnosis of diabetes mellitus and glucose intolerance in high risk individuals. (Acuerdo entre criterios de discusión sobre glucosa en ayunas y dos horas luego de la ingesta para el diagnóstico de la diabetes mellitus y la intolerancia glucémica en individuos con alto riesgo). Diabet Med 2001;18:29 –31. 5. Kim SH, Abbasi F, Reaven GM. Impact of degree of obesity on surrogate estimates of insulin resistance. (Impacto del grado de obesidad en estimaciones indirectas de resistencia insulı́nica). Diabetes Care 2004;27:1998 –2002. 6. Dankner R, Chetrit A, Shanik MH, Raz I, Roth J. Basal state hyperinsulinemia in healthy normoglycemic adults heralds dysglycemia after more than two decades of follow up. (La hiperinsulinemia basal en adultos normoglucémicos sanos anuncia disglucemia luego de un segui- 7. 8. 9. 10. 11. 12. miento durante más de dos décadas). Diabetes Metab Res Rev 2012;28:618 –24. Manley SE, Stratton IM, Clark PM, Luzio SD. Comparison of 11 human insulin assays: implications for clinical investigation and research. (Comparación de 11 análisis de insulina humana: repercusiones en la investigación clı́nica y la investigación). Clin Chem 2007;53:922–32. Hoofnagle AN, Wener MH. The fundamental flaws of immunoassays and potential solutions using tandem mass spectrometry. (Las principales fallas de los inmunoanálisis y posibles soluciones mediante el uso de espectometrı́a de masas en tándem). J Immunol Methods 2009;347:3–11. Kippen AD, Cerini F, Vadas L, Stocklin R, Vu L, Offord RE, Rose K. Development of an isotope dilution assay for precise determination of insulin, C-peptide, and proinsulin levels in non-diabetic and type II diabetic individuals with comparison to immunoassay. (Desarrollo de un análisis de dilución isotópica para la determinación precisa de los niveles de insulina, péptido-C y proinsulina en individuos no diabéticos y diabéticos de tipo II mediante comparación en inmunoanálisis). J Biol Chem 1997;272:12513–22. Stocklin R, Vu L, Vadas L, Cerini F, Kippen AD, Offord RE, Rose K. A stable isotope dilution assay for the in vivo determination of insulin levels in humans by mass spectrometry. (Un análisis de dilución isotópica estable para la determinación in vivo de los niveles de insulina en humanos mediante espectometrı́a de masas). Diabetes 1997;46:44 –50. Darby SM, Miller ML, Allen RO, LeBeau M. A mass spectrometric method for quantitation of intact insulin in blood samples. (Un método de espectometrı́a de masas para la cuantificación de la insulina inalterada en muestras de sangre). J Anal Toxicol 2001;25:8 –14. Thevis M, Thomas A, Delahaut P, Bosseloir A, Schanzer W. Qualitative determination of synthetic analogues of insulin in human plasma by immunoaffinity purification and liquid chromatography-tandem mass spectrometry for doping control purposes. (Determinación cualitativa de análogos sintéticos de insulina en plasma humano mediante purificación por inmunoafinidad y cromatografı́a de lı́quidos y espectrometrı́a de masas en tándem con propósitos de análisis de dopaje). Anal Chem 2005;77:3579 – 85. 13. Rodriguez-Cabaleiro D, Van Uytfanghe K, Stove V, Fiers T, Thienpont LM. Pilot study for the standardization of insulin immunoassays with isotope dilution liquid chromatography/tandem mass spectrometry. (Estudio piloto para la estandarización de los inmunoanálisis de insulina con cromatografı́a de lı́quidos y espectrometrı́a de masas en tándem de dilución isotópica). Clin Chem 2007;53:1462–9. 14. Van Uytfanghe K, Rodriguez-Cabaleiro D, Stockl D, Thienpont LM. New liquid chromatography/ electrospray ionisation tandem mass spectrometry measurement procedure for quantitative analysis of human insulin in serum. (Nuevo procedimiento de medición mediante cromatografı́a de lı́quidos/ionización por electronebulización y espectometrı́a de masas en tándem para el análisis cuantitativo de la insulina humana en suero). Rapid Commun Mass Spectrom 2007;21: 819 –21. 15. Hess C, Thomas A, Thevis M, Stratmann B, Quester W, Tschoepe D y cols. Simultaneous determination and validated quantification of human insulin and its synthetic analogues in human blood serum by immunoaffinity purification and liquid chromatography-mass spectrometry. (Determinación simultánea y cuantificación validada de la insulina humana y sus análogos sintéticos en suero de sangre humana mediante purifi- Clinical Chemistry 59:9 (2013) 1357 cación por inmunoafinidad y cromatografı́a de lı́quidos y espectrometrı́a de masas). Anal Bioanal Chem 2012;404:1813–22. 16. Thevis M, Thomas A, Schanzer W. Mass spectrometric determination of insulins and their degradation products in sports drug testing. (Determinación de espectometrı́a de masas de insulinas y sus productos de degradación en pruebas de antidopaje deportivas). Mass Spectrom Rev 2008; 27:35–50. 17. Thieme D, Hemmersbach P, Thevis M, Thomas A, 1358 Clinical Chemistry 59:9 (2013) Schanzer W. Insulin. (Insulina). En: Thieme D, Hemmersbach P, ed. Handbook of experimental pharmacology. (Manual de farmacologı́a experimental). Berlı́n: Springer-Verlag; 2010. p 209 –26. Vol. 195. 18. Altschul SF, Gish W, Miller W, Myers EW, Lipman DJ. Basic local alignment search tool. (Herramienta de búsqueda de alineación local básica). J Mol Biol 1990;215:403–10. 19. Miller WG, Thienpont LM, Van Uytfanghe K, Clark PM, Lindstedt P, Nilsson G y cols. Toward stan- dardization of insulin immunoassays. (Hacia la estandarización de los inmunoanálisis de insulina). Clin Chem 2009;55:1011– 8. 20. Marcovina S, Bowsher RR, Miller WG, Staten M, Myers G, Caudill SP y cols. Standardization of insulin immunoassays: report of the American Diabetes Association Workgroup. (Estandarización de los inmunoanálisis de insulina: informe del grupo de trabajo de la Asociación Americana de la Diabetes). Clin Chem 2007;53: 711– 6.