guía de estudio - CiberEsquina
Anuncio

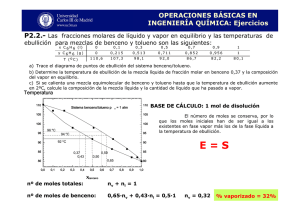
Procesos Químicos [240] Página 1 de 21 UNIVERSIDAD NACIONAL ABIERTA VICERRECTORADO ACADÉMICO ÁREA: Ingeniería CARRERA: Ingeniería Industrial GUÍA DE ESTUDIO MATERIAL INSTRUCCIONAL COMPLEMENTARIO NOMBRE: Procesos Químicos Código: 240 U.C.: 3 CARRERA: Ingeniería Industrial SEMESTRE: Código: 280 VI AUTORA: MSc Belkis Velásquez Ing. Thais Linares COMITÉ TÉCNICO: Lic. Freddy Herradas(Evaluador Educacional) DISEÑO ACADÉMICO Dra. Egleé Arellano de Rojas(Diseñadora Instruccional) Nivel Central Caracas, Octubre de 2006 Versión preliminar Procesos Químicos [240] Página 2 de 21 INDICE II. Objetivo de la asignatura 3 III. Propósito de la presente guía 3 IV. Conceptos Básicos de Procesos Químicos 3 V. Síntesis de Procesos Químicos 4 V.1 Síntesis de caminos de reacción 5 V.2 Primera selección de caminos de reacción 7 V.3 Procesos de Separación 11 VI. Análisis de Procesos Químicos 13 VI.1 Diagramas de bloque de proceso (DBP) 13 VI.2 Diagramas de flujo de proceso (DFP) 14 VI.3 Normas de Ingeniería 16 VII. Bibliografía 22 Procesos Químicos [240] Página 3 de 21 II. OBJETIVO DE LA ASIGNATURA El objetivo de la asignatura es: “Aplicar los conceptos básicos y las herramientas para la resolución de problemas de balance de masa y energía más frecuentes en los procesos químicos a escala industrial”. La sinopsis de contenido para esta asignatura que responde a este objetivo se resume en los siguientes aspectos: Introducción a los Cálculos de Procesos Químicos, Principios de Balance de Materia y Energía en Estado Estacionario con y sin Reacciones Químicas y Procesos Industriales Químicos. III. PROPÓSITO DE LA PRESENTE GUÍA El propósito de esta guía de estudio es mostrar aspectos de la asignatura que corresponden al objetivo 6 de la unidad 6 PROCESOS QUÍMICOS ORIENTADOS A LA INDUSTRIA: “Representar de manera conceptual los procesos y balances de materia y/o energía a nivel industrial través del diseño de una planta piloto”, por lo cual se pretende facilitar la integración de contenidos y comprender la utilidad de los conocimientos relacionados en esta asignatura IV. CONCEPTOS BÁSICOS DE PROCESOS QUÍMICOS ¿Qué es un proceso químico? Un proceso químico es una serie de cambios en secuencia producidos por reacciones químicas y/o una serie de cambios físico-químicos, dirigidos a la obtención de productos según especificaciones dadas. Un proceso químico puede describirse según un diagrama de flujo y de acuerdo con los balances de masa y energía y además, las especificaciones para las corrientes y equipos involucrados. Los tipos de industria donde están presentes los procesos químicos más comunes son: petrolera, metalúrgica, petroquímica, textil, gasífera, alimentos, farmacéutica, cosmetológica, de pinturas y fertilizantes. Las industrias petrolera, farmacéutica y petroquímica producen la mayor cantidad de materias primas para las otras industrias y operan a gran escala (3 000 TM/día) con pequeños márgenes de ganancia por unidad porque la utilidad reside en la escala de producción o economía de escala. Las otras industrias generan productos Procesos Químicos [240] Página 4 de 21 terminados cuya escala de producción puede ser mediana o pequeña, pero el margen de ganancia unitario es mayor. Aunque las industrias farmacéutica y cosmetológica son de pequeña capacidad, su rentabilidad por unidad es acorde con la producción, por ejemplo un colirio medicinal de 20 ml puede costar unos 40 000 Bs. Entonces existe una relación entre la capacidad de una industria, el margen de ganancia del producto y los requerimientos de espacio de la planta industrial. Por ejemplo, la industria petrolera debe ubicarse lejos de zonas pobladas por razones de riesgos de seguridad y de protección ambiental, sin embargo, una industria cervecera puede ubicarse en una ciudad como Caracas o una empresa de cosméticos ya que su impacto en términos cualitativos es mediano y existen otras ventajas como creación de empleos y tratamiento de efluentes que permiten su existencia en grandes urbes. Actividad 1: Dé ejemplos de tipos de industrias de su entorno habitacional con distintas capacidades y su ubicación, relacionando los factores ambientales (ruido, seguridad industrial, contaminación) y considerando la normativa legal existente. V. SÍNTESIS DE PROCESOS QUÍMICOS El desarrollo de un proceso químico a escala industrial requiere habilidades y destrezas en síntesis y análisis. La síntesis se relaciona con la creación de productos con propiedades deseadas, mientras el análisis con la comprensión de cómo son los productos y cómo trabajan o funcionan. La síntesis de procesos químicos puede describirse en varios problemas sencillos, cuyas soluciones se integran para resolver el problema total. Estos problemas sencillos pueden ser: . . . . . • Síntesis del camino de reacción • Localización de especies • Tecnología de Separación • Selección de la operación de separación • Integración de soluciones. Veamos cada uno con detalle: Síntesis del camino de reacción: Gran cantidad de procesos industriales comerciales comprenden la transformación química de los materiales, por lo cual el examen de la química del proceso es el primer paso para el desarrollo del mismo. Existen varios caminos de reacción para la obtención de un producto y generalmente el camino desarrollado a nivel de laboratorio no es el más Procesos Químicos [240] Página 5 de 21 económico de implementar a escala industrial. El químico y el ingeniero de procesos industriales deben trabajar juntos durante el descubrimiento de caminos de reacción competitivos. Localización de especies: Las reacciones químicas de cada camino de reacción son como elementos aislados que deben conectarse para establecer una relación entre las materias primas y los productos. Las reacciones rara vez son específicas, aunque las condiciones para su desarrollo sí lo son, ya que subproductos, reactantes y/o productos pueden salir del reactor. Durante la localización de las especies se determina la ruta de cada una, desde su fuente a su destino, con la ayuda de reglas simples. Tecnología de Separación: Al finalizar la localización de especies resulta que diferentes materiales en la misma fuente deben asignarse a destinos diferentes. Esta asignación implica una separación de materiales y el beneficio de aprovechar las diferencias en las propiedades que causan que el material se comporte de manera distinta en algún ambiente diferente. Selección de la operación de separación: Los materiales pueden ser separados unos de otros de diferentes maneras, aprovechando las distintas combinaciones de diferencias de propiedades. Entonces se debe determinar el método de separación que mejor se ajusta a un problema de proceso en particular (destilación, extracción, secado, humidificación). Integración de soluciones: Durante la selección de operaciones de separación, se escoge una secuencia de operaciones para cada corriente de proceso: materias primas, reacciones químicas, separaciones y productos deseados. Se debe considerar en el costo del proceso la necesidad de minimizar recursos externos de calor, refrigeración, agua y materias primas mediante disposición apropiada de equipos y emparejando tareas. La selección de un camino de reacción y de la localización de especies está determinada en parte por la facilidad de separación de los productos de la reacción; la selección del fenómeno de separación está influenciada por la facilidad con que pueda implementarse la integración más tarde y así sucesivamente. Estos pasos en la síntesis de procesos se enlazan unos a otros e interactúan fuertemente. Procesos Químicos [240] Página 6 de 21 V.1 Síntesis del camino de reacción: Continuamente la ciencia química realiza innovaciones impactantes en los procesos y por lo tanto, en los caminos de reacción con significado práctico antes que complicadas rutas propias de investigaciones científicas que, aunque puedan conducir a la obtención de distinciones y premios para los científicos, no llegan a trascender a la comunidad ni a la sociedad. Estrategia De Síntesis Molecular Sabemos por cursos anteriores que los enlaces químicos que unen a los átomos en moléculas, originan las propiedades físicas y químicas de las estructuras moleculares. Por ello debe conocerse las características de estos enlaces para predecir las posibilidades de que ocurran y las propiedades de los compuestos. Ejemplo De Caminos De Reacción Cuando hay varios caminos para la obtención de un producto: ¿Cuál es el óptimo? Los caminos pueden incluso cruzarse y al coincidir se alcanza el producto deseado. Como ejemplo tomemos la obtención de fenol, la cual se puede hacer por 5 vías: Sulfonación: el benceno más ácido sulfúrico produce ácido sulfónico de 1. benceno. El ácido sulfónico se convierte en peróxido de sodio bajo condiciones de reacción del hidróxido de sodio fundido (mayor de 300° C), esta fusión se lleva a cabo en agua y se filtra el sulfato de sodio producido. Esta ruta es poco atractiva por la generación de soluciones salinas. 2. Proceso catalítico de clorinación: en fase vapor el benceno puede ser catalíticamente clorinado (200° C) y convertido en fenol (500° C). Este es un proceso conveniente en un esquema de fase vapor a alta presión. 3. Proceso de hidroperóxido de cumeno: comienza con la oxidación de fase vapor del cumeno, seguido por acidificación para formar fenol y acetona. Si el cumeno es un subproducto de otro proceso y existe un mercado adicional para la acetona, este camino podría ser atractivo comercialmente. 4. Clorobenceno: en una solución de hidróxido de sodio a 5000 psi y 350 ° C, el clorobenceno se convierte a peróxido de sodio, el cual debe ser acidificado para producir fenol. Este es un camino comercial actual para producir fenol. 5. Oxidación de tolueno: el tolueno puede ser parcialmente oxidado usando un catalizador de sales de cobalto para producir ácido benzoico, el cual en presencia de catalizadores de sales de cobre y magnesio, se puede oxidar a fenol y dióxido de carbono. Este esquema de proceso en fase de vapor es preferido al de clorinación descrito. Procesos Químicos [240] Página 7 de 21 Se demuestra que el diseño de caminos o rutas de reacción es importante para evitar gastos innecesarios en la implantación de procesos químicos en la industria Recomendaciones de Interés para el Diseño de Caminos de Reacción Identifique la estructura molecular del compuesto químico deseado. Si el producto final es una mezcla compleja, determine la estructura de la composición característica. Basándose en analogías estructurales, identifique los compuestos químicos que pueden servir de punto de partida para la síntesis de los productos deseados o que pueden aparecer como productos intermedios en dicha síntesis Identifique las materias primas que pueden servir de fuente de los compuestos de partida para la síntesis de los procesos deseados Diseñe los caminos de reacción que puedan servir para la construcción de las moléculas deseadas Descarte los caminos impracticables por razones cinéticas o termodinámicas Una vez calculada la diferencia en $ entre materias primas y productos comerciales, desprecie aquellos cuyo valor no sea rentable. V.2 Primera selección del camino de reacción: Es de suma importancia el análisis económico en la síntesis del proceso. También es de considerar la variable del factor ambiental, aunque al final el interés es el desarrollo de síntesis de procesos químicos que tengan un gran beneficio económico. La eficiencia de un proceso se mide por: Beneficio anual = Beneficio bruto - Costo anual de amortización, mantenimiento, servicios, mano de obra y otros factores. Beneficio bruto = Valor del producto manufacturado-Costo anual de materias primas El beneficio bruto es una función del camino de reacción y puede estimarse con bastante aproximación. Análisis De Producción Y Consumo EJEMPLO: Caso de la producción de cloruro de vinilo a partir de cloro y etileno. En primer lugar se analizan la estequiometría de las reacciones: Reacción 1. C2H4 (etileno) + Cl2 (cloro) = C2H4Cl2 (dicloroetano) Reacción 2. C2H4Cl2 (dicloroetano) = C2H3Cl (cloruro de vinilo) + HCl (ácido clorhídrico) Procesos Químicos [240] Página 8 de 21 Se observa la generación de ácido clorhídrico como subproducto en la misma proporción que el cloruro de vinilo deseado. Si no hay salida conveniente para el HCl, podría ser útil la siguiente reacción: Reacción 3. 2HCl + ½ O2 = Cl2 + H2O Ahora se construye la siguiente tabla: En las columnas se colocan las especies de la reacción (productos y reactantes). Cada fila corresponde a cada reacción del esquema propuesto y se coloca el número correspondiente proporcional al coeficiente estequiométrico de la reacción balanceada: positivo para los productos y negativos para los reactantes. Así, todos los números pueden ser multiplicados por una constante y representar aún la estequiometría de la reacción. La fila final se obtiene por la suma algebraica de producción y consumo. En este caso se obtiene una tabla como la Tabla 1. TABLA 1 Reacción Etileno 1 2 3 neta -1(2) -2 Cloro -1(2) +1 -1 Especies Dicloro Cloruro De vinilo etano +1(2) -1(2) +1(2) 0 +2 HCl Oxígeno Agua +1(2) -2 0 -1/2 -1/2 +1 +1 Neto = + Producción/ -consumo/(n) Ajuste de la reacción por su factor de multiplicación Para obtener el precio por unidad de mol - libra se multiplica el peso molecular de cada especie involucrada en la reacción por el precio por libra. Así construimos la siguiente Tabla 2 TABLA 2 Especies Etileno Cloro Cloruro de vinilo Peso Molecular 28 70 62 X $ / libra 0.03 0.04 0.05 = $ / libra mol 0.84 2.80 3.10 Para obtener el beneficio bruto de este camino de reacción, se considera primero que por cada mol de cloruro de vinilo producido, se consumen un mol de etileno y ½ de cloro. Entonces: Beneficio bruto = 3.1 -0.84 -1/2 (2.80) = $0.86/ libra -mol de cloruro de vinilo. Como conclusión los productos tienen más valor que las materias primas por lo cual es un camino de reacción potencialmente rentable. Procesos Químicos [240] Página 9 de 21 Localización de especies Una vez que se han seleccionado varios caminos de reacción potenciales, se debe enfocar la atención a la disponibilidad y ubicación de la materia prima y disposición de productos y reactantes no convertidos. Los procesos de separación que vienen después, deben considerar estos aspectos y además el factor costo, el cual debe ser reducido del beneficio bruto calculado a partir del análisis costobeneficio anteriormente ejemplificado. Entonces, el balance de masa es la herramienta que definirá la localización de especies. Veamos un ejemplo: EJEMPLO: Dióxido de azufre por oxidación directa La reacción por oxidación directa para obtener dióxido de azufre es: S + O2 = SO2 Para mantener la temperatura baja en el quemador, el oxígeno es disuelto por una cantidad de gas inerte frío antes de alimentarlo al quemador (dilución previa antes de entrar al quemador). La mezcla debería ser un 70% molar en inerte y 30 % molar en oxígeno y se usa aire como la fuente de oxígeno. Se proponen dos localizaciones de especies: LOCALIZACIÓN 1 Aire: 100 moles O2 230 moles N2 S + O2 = SO2 N2 como gas inerte 100 moles S Separador 100 moles SO2 230 moles N2 LOCALIZACIÓN 2 N2 como gas inerte Aire: 100 moles O2 230 moles N2 230 moles de SO2 100 moles O2 Separador 230 moles N2 S + O2 = SO2 SO2 como gas inerte Enfriador 100 moles SO2 100 moles S En la primera localización, el aire y el azufre reaccionan directamente para producir una mezcla de dióxido de azufre y nitrógeno. Estos son separados para recuperar el SO2 producto. En la segunda localización el nitrógeno y el oxígeno se separan primero y el oxígeno puro es mezclado con el reflujo de SO2 frío para proveer la alimentación Procesos Químicos [240] Página 10 de 21 de oxígeno diluida al quemador. Este concepto elimina el paso de purificación del dióxido de azufre de la primera localización. Ambas localizaciones satisfacen tanto los requerimientos teóricos referentes a la dilución de la alimentación del quemador como los balances de masa. Las diferencias importantes entre ellas consisten en a) la dificultad de la separación b) la tolerancia a cambios incontrolados en la alimentación. Veamos estas diferencias en detalle: a) Diferencias en la separación: la localización 1 requiere la separación de una mezcla de N2 (punto de ebullición -320° F) y SO2 (punto de ebullición 14° F). Estas especies exhiben una gran diferencia en sus puntos de ebullición, uno tiende a gas y el otro a líquido por lo cual la separación será relativamente fácil. La localización 2 requiere la separación de N2 (punto de ebullición -320° F) y O2 (punto de ebullición -270 ° F) en nitrógeno y oxígeno puros. Los dos son gases y son mucho más difíciles de separar, aún cuando hay procesos comerciales para separar estas mezclas. b) Tolerancia a cambios en la alimentación: existe la posibilidad que ocurran cambios repentinos en el flujo y calidad de la alimentación, lo cual puede resultar en un exceso de oxígeno yo de azufre en el quemador. La localización 2 requiere que los flujos de alimentación sean perfectamente estequiométricos para obtener SO2 puro, mientras que la localización 1 tiene las unidades de separación en una posición que le permite amortiguar estas perturbaciones. Actividad 2: ¿Cuál localización de especies seleccionaría usted de acuerdo a lo planteado en el caso anterior? ¿Por qué? Enunciados de interés en el Manejo de Energía Las corrientes de fluidos a altas temperaturas deben usarse para generación de vapor, para realizar trabajo directamente o para tareas de calefacción Las corrientes a alta presión deben usarse para realizar trabajo directamente La calefacción o disipación de calor debe hacerse preferiblemente entre fluidos de proceso Los intercambiadores más efectivos son aquellos donde los fluidos fríos y calientes circulan en contracorriente Procesos Químicos [240] Página 11 de 21 Enunciados de interés en el Transporte de Materiales El transporte de fluido debe hacerse en cascada de presiones minimizando altibajos El transporte de sólidos debe hacerse en cascada de energía potencia (altura) usando la fuerza de gravedad y minimizando altibajos En la medida de lo posible debe evitarse el transporte de materiales en más de una fase En el caso en que el transporte de materiales requiera la coexistencia de dos o más fases por una etapa o tramo del trayecto, la segregación de las fases debe hacerse tan pronto como se pueda V. 3 Procesos De Separación Una vez que se ha definido el camino de la reacción química y el flujo de materiales, ahora se debe enfocar la atención en la tecnología para lograr la separación de las fases. Al examinar las propiedades físicas y químicas de los materiales se puede predecir el comportamiento de los mismos ante cambios bruscos de presión, temperatura, solubilidad ya que unas especies pueden cambiar a gas o sólido mientras otras permanecen en líquido, una especie puede flotar mientras otra se hunde, algunas pueden pasar a través de membranas cuando se alteran las condiciones a través de lo que llamaremos agente de separación. A continuación se muestran tablas (Tabla 3 y Tabla 4) que resumen una variedad de fenómenos de separación: TABLA 3 PROCESOS DE SEPARACIÓN MECÁNICA Fase de la Agente de Fases de los Nombre Propiedad Ejemplo alimentación separación productos Reducción Tamaño Recuperación de la del sólido de presión; mayor al catalizadores Filtración medio Líquido+sólido tamaño del en Líquido+Sólido filtrante poro del suspensión medio filtrante Diferencia ¿? Líquido+Sólido Líquido+Sólido de Centrifugado Fuerza u otro líquido u otro líquido densidad y (sedimentación centrífuga inmiscible inmiscible tamaño Carga de Remoción de las polvo en las Precipitación Gas+Sólidos Campo Gas+Sólidos partículas electrostática Finos eléctrico Finos chimeneas sólidas de gas. finas Procesos Químicos [240] Página 12 de 21 TABLA 4 PROCESOS DE SEPARACIÓN POR EQUILIBRIO Nombre Destilación Absorción Flotación Fase de la alimentación Líquido y/o vapor Gas Agente de separación Calor Líquido no volátil Fases de los productos Propiedad Líquido + vapor Diferencia de Separación volatilidad de petróleo (Pto. De crudo evaporación) Líquido + vapor Mezcla de Surfactantes;burbujas Dos sólidos de aire ascendente Sólidos pulverizados Solubilidad selectiva Tendencia de surfactantes a absorber a una de las especies sólidas Ejemplo Remoción de CO2 y H2S del gas natural por absorción en etanolaminas Industria de minerales; recuperación de oro de minerales anfitriones Actividad 3: investigue sobre tecnologías de separación a fin de enriquecer las tablas anteriores con mayor información y/o completar espacios en blanco. Enunciados de interés en el análisis de procesos de separación Al usar destilación, es conveniente remover si es posible el producto con el calor de vaporización más alto, para reducir las cargas de enfriamiento calentamiento de unidades subsecuentes. Se puede usar absorción gaseosa para remover trazas de un componente en una corriente gaseosa Utilice centrifugación para concentrar un sólido en un lodo Procesos Químicos [240] Página 13 de 21 VI. ANÁLISIS DE PROCESOS QUÍMICOS VI.1 Los Diagramas De Bloque Del Proceso (DBP) Los DBP son esquemas de los procesos químicos. En la fase de ingeniería conceptual de un proyecto de ingeniería, se elaboran los DBP para tener una visión general del proceso completo: entradas y salidas y las reacciones químicas que existen en él. Básicamente hay dos tipos de Diagramas de Bloques 1) DBP: representa un proceso simple 2) Diagrama de bloque de la planta: representa un complejo químico que involucra diferentes procesos químicos. Elaboración de DBP: - Las operaciones se representan por bloques - Los flujos principales se representan con flechas que indiquen la dirección de la corriente - El flujo va de izquierda a derecha - Las corrientes de gas o los livianos se dibujan por el tope de los bloques - Las corrientes de líquidos y sólidos se trazan por el fondo de los bloques - Se debe suministrar información mínima del proceso (flujo molar o másico, % de conversión, materias primas, productos, reactantes, reacciones involucradas) - Si hay cruces de líneas las horizontales son continuas y las verticales se parten - Debe contener un balance de masa simplificado (flujo de entrada y de salida) Este diagrama (DBP) no muestra los detalles en el bloque. Cada bloque en el diagrama representa un proceso o muchos, en realidad cada bloque consiste en varios equipos. EJEMPLO DBP de producción de benceno El tolueno y el hidrógeno son alimentados a un reactor que tiene una conversión del 75 % en tolueno. La corriente de salida va a una sección de separación donde se separan gases de líquidos. Los líquidos de fondo son sometidos a otro proceso de separación donde por el tope sale el benceno (producto deseado) y por el fondo el tolueno que va a recirculación. El diagrama omite información específica pero da una idea general del proceso y se aprecia en la figura 1. Procesos Químicos [240] Página 14 de 21 Fig. 1 Diagrama de Bloque de Proceso de Producción de Benceno VI.2 Los Diagramas de Flujo del Proceso (DFP) Este diagrama de flujo contiene información mucho más detallada que los DBP y necesaria para el diseño de un proceso químico. Estos diagramas pueden variar de acuerdo a la compañía de ingeniería de consulta o proyectista de ingeniería. Los DFP se elaboran con una serie de símbolos de equipos, tuberías y condiciones de operación aceptados internacionalmente y contienen la siguiente información: - Balances de masa y energía del proceso (pueden estar en la misma hoja o en anexos si el diagrama es complicado) - Dimensiones de los equipos mayores de procesos y de instrumentación y control - Los recipientes como reactores, separadores, tanques y equipos como bombas e intercambiadores de calor. - Flujos, composiciones, presión y temperatura - Las corrientes de alimentación se muestran del lado izquierdo y las de producto se muestran del lado derecho Procesos Químicos [240] Página 15 de 21 EJEMPLO DFP de Producción del Benceno TK-101 P-101/B E-101 H-101 R-101 C-101A/B E-102 V-101 V-103 E-103 E-106 T-101 V-102 P-102 A/B E-106 Almacén Bomba Precal. Horno Reactor Compr. Enfriad. Separad. Separad. Calent. Rehervidor Torre Tambor Enf. Tolueno Tolueno Alm. Alm. Gas Salida HP LP Entrada Benceno Reflujo Reflujo Producto Reciclo Reactor Torre Fig. 2 Diagrama de Flujo de Proceso de Producción de Benceno Es conveniente señalar que todas las corrientes deben estar identificadas, enumeradas y deben indicar temperatura, presión, componentes y flujos. Además se debe mostrar las corrientes de servicio sin indicar de dónde provienen y las corrientes de residuos y los lazos básicos de control. Procesos Químicos [240] Página 16 de 21 Se debe tomar en cuenta: -Todas las reacciones químicas que ocurren en el proceso -Las corrientes que contienen materiales inertes, reactivos no consumidos, catalizadores, solventes, inhibidores de corrosión y otros. VI.3 Normas De Ingeniería Las normas de ingeniería reglamentan la fabricación, inspección, pruebas, embarque, procedimientos de reparación y mantenimiento de los diferentes equipos de ingeniería utilizados normalmente en plantas industriales. Todas estas normas son reconocidas en el ámbito internacional y cada una de ellas se especializa en un área de la ingeniería y afines. Existen normas internacionales y nacionales. Las normas internacionales son ASME, API, ANSI, NFPA e ISA y las nacionales: las de PDVSA y COVENIN A continuación se describirán brevemente las normas internacionales: Sociedad Americana de Ingenieros Mecánicos ASME, organización Premium internacional que promueve el arte, la ciencia y la práctica de ingeniería mecánica en todo el mundo. Esta sociedad es autora del código ASME sobre calderas y recipientes a presión, que involucra un cuerpo de normas técnicas que abarcan entre otros aspectos las fases de diseño, materiales, procesos de fabricación y pruebas sobre estos equipos. Instituto Americano del Petróleo API, es la principal asociación para la industria petrolera mundial, con más de cuatrocientas compañías asociadas alrededor de este organismo. API organiza seminarios, talleres, publicaciones periódicas para discutir los problemas y avances de la industria. Esta sociedad es autora del código API que regula y normaliza lo relativo a crudos, gases y derivados del petróleo. Instituto Nacional Estadounidense de Estándares (American National Standard Institute) ANSI se encarga del estudio, pruebas, publicaciones sobre tuberías, bombas y afines. Esta sociedad ha elaborado el código ANSI sobre tuberías, bombas y conexiones, es decir, un cuerpo de normas técnicas que abarcan las fases de diseño, materiales, procesos de fabricación y pruebas sobre estos equipos. Las normas ANSI por ser altamente confiables han sido asimiladas por otras normas internacionales como las ASME y así se encuentran referenciadas como ASME/ANSI Asociación para la Protección Nacional del Fuego NFPA es reconocida internacionalmente y dicta las normas a seguir en lo relativo a seguridad y protección contra incendios. Esta asociación se encarga de realizar actividades de difusión e información sobre seguridad, protección industrial y protección contra incendios. Destaca además su acción en el dictado de las normas para sistemas Procesos Químicos [240] Página 17 de 21 eléctricos, sistemas de instrumentación y control, sistemas contra incendios y normas de seguridad industrial en general . Estandares de Asociación de Industrias ISA se encarga de las normativas específicas de la identificación de los equipos correspondientes a los sistemas de instrumentación y control Las normas nacionales más importantes son: Comisión Venezolana de Normas Industriales COVENIN: creada en 1958, es el organismo encargado a escala nacional de programar y coordinar las actividades de Normalización y Control de Calidad. Para llevar a cabo el trabajo de elaboración de normas, COVENIN instala comités y comisiones técnicas de normalización, donde participan organizaciones gubernamentales, no gubernamentales, usuarios y fabricantes del área específica. Petróleos de Venezuela Sociedad Anónima PDVSA: a través de la filial INTEVEP, se han elaborado un conjunto de manuales contentivos de las normas y reglamentos fundamentados en leyes venezolanas e internacionales, que se deben cumplir en el diseño, fabricación, inspección, pruebas, transporte, embarque, procedimientos de reparación, mantenimiento y seguridad de los diferentes equipos relacionados con la industria petrolera y petroquímica en Venezuela. Se puede resumir la identificación de equipos como aparece en la figura 3. Área Asignada en la planta XX-YZZ A/B Identificador del tipo de equipo Número Asignado al equipo Indicador de unidades paralelas Fig. 3 NORMAS PARA LOS DFP IDENTIFICACIÓN DE EQUIPOS Ejemplo: B-101 B101 A/B Primera bomba del proceso Primera bomba del proceso con unidad paralela Procesos Químicos [240] Página 18 de 21 Cada pieza de los equipos principales debe ser identificada por un número y/o unas letras que indican el tipo de equipo (XX-YZZ A/B) XX Identifica el tipo de equipo (compresor, reactor, separador…) Y Indica en cuál área de la planta está ubicado el equipo ZZ es el número designado para cada equipo de una clase A/B Indica la existencia de unidades paralelas o de respaldo TABLA 5 Normativa sobre la Identificación de equipos (según normas ISA) XX Equipo E H K P R TK V Intercambiadores de calor ( Heat exchanger) Hornos o Calentadores de fuego directo Compresores o turbinas (compressor or turbines) Bombas (pumps) Reactores Tanques de almacenamiento (Storage Tank) Recipientes a presión (Vessel) TABLA 6 Normativa sobre la Identificación de los servicios (según normas ASME) Descripción Parámetros Código lps Vapor de baja presión 3-5 barg (sat) mps Vapor de media presión 10-15 barg (sat) hps Vapor de alta presión 40-50 barg(sat) htm Medio de transferencia de calor Hasta 400 º C cw Agua de enfriamiento 30º C retorna 45º C wr Agua de río 25º C retorna >35º C rw Agua refrigerada 5º C retorna >15º C rb Refrigerante -45º C retorna 0º C cs Agua de desechos químicos(alto DQO) Procesos Químicos [240] Página 19 de 21 ss Agua de desechos sanitarios (alto DBO) el Energía eléctrica ng Gas natural fg Gas combustible fo Aceite combustible fw Agua para sistemas contra incendios 220,440 o 660 Voltios Es conveniente reiterar en este momento, que las corrientes de servicio no se indican de dónde provienen sino que se requieren y cuál tipo de servicio brinda. Ejemplos de corrientes de servicio: Código Descripción Parámetros lps ---4bar ---290 º F (145 º C) mps ---12 bar---375 º F (190 º C) hps ---4bar ---500 º F (260 º C) En los Diagramas de Flujo de Proceso (DFP) se requiere incluir como mínimo la siguiente información: TABLA 7 Información Mínima de un DFP Tipo de Equipo Descripción Dimensiones, T y P de diseño, Torres Material de construcción El dibujo debe indicar: bandejas o relleno, nº de bandejas y/o relleno Intercambiadores Tipo de intercambiador, T y P de diseño, servicios, material Recipientes Dimensiones, T y P de diseño , material, Servicios. Bombas Caudal, caída de presión Compresores Caudal, caída de presión Hornos Carga térmica, material Procesos Químicos [240] Página 20 de 21 En los Diagramas de Flujo de Proceso deben mostrarse las necesidades de: ►Electricidad, ►Compresores de aire, ►Enfriadores de aire, ►Refrigeradores de agua, ►Vapor, ►Gas inerte, ►Aguas tratadas, ►Aguas para el sistema contra incendios, ►Combustible, ►Demanda química de oxígeno (DQO) y ►Demanda biológica de oxígeno (DBO). En las corrientes del proceso se debe incluir la siguiente información • • • Composición molar • Composición másica Flujo molar total de la corriente (Kmol/h) 3 Flujo volumétrico total de la corriente (m /h) • Flujo molar de cada componente (Kmol/h) • Flujo másico de cada componente (Kmol/h) ¾ Porcentaje de vapor de la corriente ¾ Propiedades físicas importantes (densidad, viscosidad) ¾ Data termodinámica (entalpía, capacidad calórica) ¾ Nombre de la corriente Ejercicio Resuelto Haga el siguiente link para ver el ejercicio resuelto Estigmaterol a partir de concha de plátano. ..\Estigmasterol a partir de Concha de platano.ppt Procesos Químicos [240] Página 21 de 21 VII. BIBLIOGRAFÍA Consultada por el autor: • B. Blanco, L. Oropeza(2005) Guía de Procesos Químicos UCV • R. Turton y otros (1998) Síntesis and Design of Chemical Processes. Editorial Prentice Hall Obligatoria para el estudiante • Felder R., Rousseau R. (1991) Principios Elementales de los Procesos Químicos. Editorial Addison Wesley. Complementaria • Himmelblau D. (1997) Principios Básicos y Cálculos en Ingeniería Química. Sexta edición. Editorial Prentice Hall. • CD Rom del texto Himmelblau D. Principios Básicos y Cálculos en Ingeniería Química(1997). Sexta edición. Editorial Prentice Hall. • Austin G. (2000) Manual de Procesos Químicos en la Industria. Primera edición en español. Mc Graw Hill. Tomos I, II y III. • Journal of Industrial Engineering ( disponible en biblioteca de nivel central) • Manual de Ingeniería de Proyectos de PDVSA • Manual de Ingeniería de Proyectos de Pequiven