- Ninguna Categoria
quinasa cdc2. - Universidad de Antioquia
Anuncio
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el
sistema ciclina - quinasa cdc2.
Grupo de Biomatemáticas Universidad de Antioquia
Departamento de Matemáticas
Universidad de Antioquia
c 2008. Reproducción permitida bajo los
Copyleft términos de la licencia de documentación libre GNU.
Introducción
El modelo
Resultados
Apéndice
Referencias
Contenido
1
Introducción
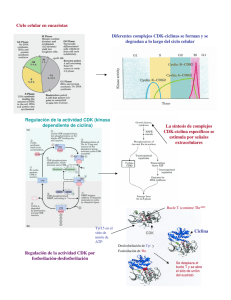
El ciclo celular
Supuestos
2
El modelo
Motivación
Descripción
3
Resultados
Soluciones numéricas
4
Apéndice
5
Referencias
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
2 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
El ciclo celular
Serie de eventos que conducen a la replicación de las células eucariotas.
Las células eucariotas contienen su información genética encerrada dentro de
una doble membrana (envoltura nuclear).
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
3 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
El ciclo celular
Serie de eventos que conducen a la replicación de las células eucariotas.
Las células eucariotas contienen su información genética encerrada dentro de
una doble membrana (envoltura nuclear).
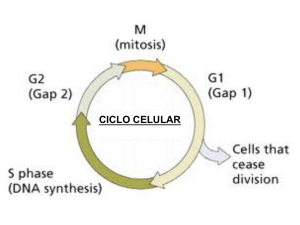
Fases del ciclo celular:
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
3 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
El ciclo celular
Serie de eventos que conducen a la replicación de las células eucariotas.
Las células eucariotas contienen su información genética encerrada dentro de
una doble membrana (envoltura nuclear).
Fases del ciclo celular:
Intefase: la célula crece, almacena nutrientes para la mitosis y duplica su
DNA.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
3 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
El ciclo celular
Serie de eventos que conducen a la replicación de las células eucariotas.
Las células eucariotas contienen su información genética encerrada dentro de
una doble membrana (envoltura nuclear).
Fases del ciclo celular:
Intefase: la célula crece, almacena nutrientes para la mitosis y duplica su
DNA.
Fase mitótica: la célula se divide en dos células distintas (“células hijas”).
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
3 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
El ciclo celular
Serie de eventos que conducen a la replicación de las células eucariotas.
Las células eucariotas contienen su información genética encerrada dentro de
una doble membrana (envoltura nuclear).
Fases del ciclo celular:
Intefase: la célula crece, almacena nutrientes para la mitosis y duplica su
DNA.
Fase mitótica: la célula se divide en dos células distintas (“células hijas”).
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
3 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
El ciclo celular
Serie de eventos que conducen a la replicación de las células eucariotas.
Las células eucariotas contienen su información genética encerrada dentro de
una doble membrana (envoltura nuclear).
Fases del ciclo celular:
Intefase: la célula crece, almacena nutrientes para la mitosis y duplica su
DNA.
Fase mitótica: la célula se divide en dos células distintas (“células hijas”).
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
3 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Supuestos
Se asume la existencia de un mecanismo universal que regula los procesos
bioquı́micos del ciclo celular.
Varios de estos procesos son desencadenados por la activación periódica de
proteı́nas quinasas.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
4 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Supuestos
Se asume la existencia de un mecanismo universal que regula los procesos
bioquı́micos del ciclo celular.
Varios de estos procesos son desencadenados por la activación periódica de
proteı́nas quinasas.
Las proteinas quinasas (enzimas) modifican a otras proteı́nas (sustratos),
mediante fosforilación/desfosforilación, activándolas o desactivándolas.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
4 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Supuestos
Se asume la existencia de un mecanismo universal que regula los procesos
bioquı́micos del ciclo celular.
Varios de estos procesos son desencadenados por la activación periódica de
proteı́nas quinasas.
Las proteinas quinasas (enzimas) modifican a otras proteı́nas (sustratos),
mediante fosforilación/desfosforilación, activándolas o desactivándolas.
Ejemplo de este mecanismo de desencadenamiento: embriones de anfibios a
temprana edad de desarrollo.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
4 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Supuestos
Se asume la existencia de un mecanismo universal que regula los procesos
bioquı́micos del ciclo celular.
Varios de estos procesos son desencadenados por la activación periódica de
proteı́nas quinasas.
Las proteinas quinasas (enzimas) modifican a otras proteı́nas (sustratos),
mediante fosforilación/desfosforilación, activándolas o desactivándolas.
Ejemplo de este mecanismo de desencadenamiento: embriones de anfibios a
temprana edad de desarrollo.
Las ciclinas (proteı́nas) controlan las fases del ciclo celular mediante la
regulación de las quinasas dependientes de ciclina (cyclin-dependent kinases,
CDKs).
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
4 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Supuestos
Se asume la existencia de un mecanismo universal que regula los procesos
bioquı́micos del ciclo celular.
Varios de estos procesos son desencadenados por la activación periódica de
proteı́nas quinasas.
Las proteinas quinasas (enzimas) modifican a otras proteı́nas (sustratos),
mediante fosforilación/desfosforilación, activándolas o desactivándolas.
Ejemplo de este mecanismo de desencadenamiento: embriones de anfibios a
temprana edad de desarrollo.
Las ciclinas (proteı́nas) controlan las fases del ciclo celular mediante la
regulación de las quinasas dependientes de ciclina (cyclin-dependent kinases,
CDKs).
La acumulación de ciclina activa el ciclo celular:
ciclina =⇒ quinasa cdc2 =⇒ mitosis =⇒ degradación de quinasa (reset)
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
4 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Supuestos
Se asume la existencia de un mecanismo universal que regula los procesos
bioquı́micos del ciclo celular.
Varios de estos procesos son desencadenados por la activación periódica de
proteı́nas quinasas.
Las proteinas quinasas (enzimas) modifican a otras proteı́nas (sustratos),
mediante fosforilación/desfosforilación, activándolas o desactivándolas.
Ejemplo de este mecanismo de desencadenamiento: embriones de anfibios a
temprana edad de desarrollo.
Las ciclinas (proteı́nas) controlan las fases del ciclo celular mediante la
regulación de las quinasas dependientes de ciclina (cyclin-dependent kinases,
CDKs).
La acumulación de ciclina activa el ciclo celular:
ciclina =⇒ quinasa cdc2 =⇒ mitosis =⇒ degradación de quinasa (reset)
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
4 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Motivación
¿Cuál es el mecanismo molecular por medio del cual la activación de la
quinasa cdc2 ocurre de una manera periódica?
En huevos de anfibios:
acumulación de ciclina =⇒ activación quinasa cdc2 =⇒ degradación de quinasa
|
{z
}
“oscilador mı́nimo del ciclo celular”
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
5 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Motivación
¿Cuál es el mecanismo molecular por medio del cual la activación de la
quinasa cdc2 ocurre de una manera periódica?
En huevos de anfibios:
acumulación de ciclina =⇒ activación quinasa cdc2 =⇒ degradación de quinasa
|
{z
}
“oscilador mı́nimo del ciclo celular”
Lo anterior sugiere que el sistema ciclina - quinasa cdc2 puede operar como
un sistema oscilador autónomo continuo.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
5 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Motivación
¿Cuál es el mecanismo molecular por medio del cual la activación de la
quinasa cdc2 ocurre de una manera periódica?
En huevos de anfibios:
acumulación de ciclina =⇒ activación quinasa cdc2 =⇒ degradación de quinasa
|
{z
}
“oscilador mı́nimo del ciclo celular”
Lo anterior sugiere que el sistema ciclina - quinasa cdc2 puede operar como
un sistema oscilador autónomo continuo.
El modelo aquı́ estudiado pretende mostar que:
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
5 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Motivación
¿Cuál es el mecanismo molecular por medio del cual la activación de la
quinasa cdc2 ocurre de una manera periódica?
En huevos de anfibios:
acumulación de ciclina =⇒ activación quinasa cdc2 =⇒ degradación de quinasa
|
{z
}
“oscilador mı́nimo del ciclo celular”
Lo anterior sugiere que el sistema ciclina - quinasa cdc2 puede operar como
un sistema oscilador autónomo continuo.
El modelo aquı́ estudiado pretende mostar que:
La activación de quinasa cdc2 y la degradación de ciclina pueden surgir de
manera natural como resultado de modificaciones quı́micas que ocurren
después de ser sintetizada la proteina.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
5 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Motivación
¿Cuál es el mecanismo molecular por medio del cual la activación de la
quinasa cdc2 ocurre de una manera periódica?
En huevos de anfibios:
acumulación de ciclina =⇒ activación quinasa cdc2 =⇒ degradación de quinasa
|
{z
}
“oscilador mı́nimo del ciclo celular”
Lo anterior sugiere que el sistema ciclina - quinasa cdc2 puede operar como
un sistema oscilador autónomo continuo.
El modelo aquı́ estudiado pretende mostar que:
La activación de quinasa cdc2 y la degradación de ciclina pueden surgir de
manera natural como resultado de modificaciones quı́micas que ocurren
después de ser sintetizada la proteina.
La “cascada mitótica” entre ciclina y quinasa cdc2 puede oscilar como
resultado de retrasos en el tiempo asociados a los umbrales que las ciclinas
deben alcanzar para activar el ciclo celular y a la rápida degradación de la
quinasa cdc2.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
5 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Motivación
¿Cuál es el mecanismo molecular por medio del cual la activación de la
quinasa cdc2 ocurre de una manera periódica?
En huevos de anfibios:
acumulación de ciclina =⇒ activación quinasa cdc2 =⇒ degradación de quinasa
|
{z
}
“oscilador mı́nimo del ciclo celular”
Lo anterior sugiere que el sistema ciclina - quinasa cdc2 puede operar como
un sistema oscilador autónomo continuo.
El modelo aquı́ estudiado pretende mostar que:
La activación de quinasa cdc2 y la degradación de ciclina pueden surgir de
manera natural como resultado de modificaciones quı́micas que ocurren
después de ser sintetizada la proteina.
La “cascada mitótica” entre ciclina y quinasa cdc2 puede oscilar como
resultado de retrasos en el tiempo asociados a los umbrales que las ciclinas
deben alcanzar para activar el ciclo celular y a la rápida degradación de la
quinasa cdc2.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
5 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Descripción
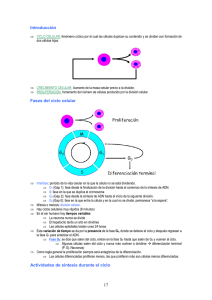
El modelo asume que la ciclina es sintetizada a una tasa constante y
desencadena la activación de quinasa cdc2.
vi : velocidad (constante) de
sı́ntetisis la ciclina
M + : fracción de quinasa cdc2
inactiva.
M : fracción de quinasa cdc2
activa.
X + : fracción de proteasa inactiva
que degrada la ciclina.
X: fracción de proteasa activa que
degrada la ciclina.
vd : velocidad máxima con que la
proteasa X degrada a la ciclina.
Vi (i = 1 − 4): velocidad de las
enzimas.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
6 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Descripción
El modelo asume que la ciclina es sintetizada a una tasa constante y
desencadena la activación de quinasa cdc2.
vi : velocidad (constante) de
sı́ntetisis la ciclina
M + : fracción de quinasa cdc2
inactiva.
M : fracción de quinasa cdc2
activa.
X + : fracción de proteasa inactiva
que degrada la ciclina.
X: fracción de proteasa activa que
degrada la ciclina.
vd : velocidad máxima con que la
proteasa X degrada a la ciclina.
Vi (i = 1 − 4): velocidad de las
enzimas.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
6 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Descripción
El modelo asume que la ciclina es sintetizada a una tasa constante y
desencadena la activación de quinasa cdc2.
vi : velocidad (constante) de
sı́ntetisis la ciclina
M + : fracción de quinasa cdc2
inactiva.
M : fracción de quinasa cdc2
activa.
X + : fracción de proteasa inactiva
que degrada la ciclina.
X: fracción de proteasa activa que
degrada la ciclina.
vd : velocidad máxima con que la
proteasa X degrada a la ciclina.
Vi (i = 1 − 4): velocidad de las
enzimas.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
6 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Descripción
Las tres variables del modelo son la ciclina, la quinasa cdc2 activa
(dephosphorylated) y la ciclina proteasa activa (phosphorylated):
C: concentración de ciclina
M : fracción de quinasa cdc2 activa
X: fracción de proteasa activa (ciclina)
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
7 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Descripción
Las tres variables del modelo son la ciclina, la quinasa cdc2 activa
(dephosphorylated) y la ciclina proteasa activa (phosphorylated):
C: concentración de ciclina
M : fracción de quinasa cdc2 activa
X: fracción de proteasa activa (ciclina)
La dinámica del sistema está dada por el sistema de ecuaciones diferenciales
ordinario
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
7 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Descripción
Las tres variables del modelo son la ciclina, la quinasa cdc2 activa
(dephosphorylated) y la ciclina proteasa activa (phosphorylated):
C: concentración de ciclina
M : fracción de quinasa cdc2 activa
X: fracción de proteasa activa (ciclina)
La dinámica del sistema está dada por el sistema de ecuaciones diferenciales
ordinario
dC
C
= vi − vd X
− kd C
(1)
dt
Kd + C
dM
(1 − M )
M
= V1
− V2
(2)
dt
K1 + (1 − M )
K2 + M
dX
(1 − X)
X
= V3
− V4
(3)
dt
K3 + (1 − X)
K4 + X
donde
V1 =
C
VM 1 ,
Kc + C
V3 = M VM 3
(4)
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
7 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Descripción
Las tres variables del modelo son la ciclina, la quinasa cdc2 activa
(dephosphorylated) y la ciclina proteasa activa (phosphorylated):
C: concentración de ciclina
M : fracción de quinasa cdc2 activa
X: fracción de proteasa activa (ciclina)
La dinámica del sistema está dada por el sistema de ecuaciones diferenciales
ordinario
dC
C
= vi − vd X
− kd C
(1)
dt
Kd + C
dM
(1 − M )
M
= V1
− V2
(2)
dt
K1 + (1 − M )
K2 + M
dX
(1 − X)
X
= V3
− V4
(3)
dt
K3 + (1 − X)
K4 + X
donde
V1 =
C
VM 1 ,
Kc + C
V3 = M VM 3
(4)
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
7 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Descripción
Parámetros del sistema:
vi : velocidad (constante) de sı́ntetisis la ciclina.
vd : velocidad máxima a la que es degradada la ciclina por la proteasa cuando
X = 1.
Kd : Constante de Michaelis para la degradación de la ciclina.
Kc : Constante de Michaelis para la activación de ciclina de la fosfotasa que
actúa sobre la forma fosforilizada de quinasa cdc2.
kd : Velocidad (constante) relacionada con la degradación no especı́fica de
ciclina .
Vi y Ki (i=1–4) caracterizan la cinética de las enzimas involucradas en los
dos ciclos: 1) La fosfotasa E1 y la quinasa E2 actúan sobre la molécula; 2) la
quinasa cdc2 (E3 ) y la fosfotasa (E4 ) actúan sobre la proteasa ciclina.
Los términos no lineales del modelo son de tipo Michaleano.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
8 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Descripción
Parámetros del sistema:
vi : velocidad (constante) de sı́ntetisis la ciclina.
vd : velocidad máxima a la que es degradada la ciclina por la proteasa cuando
X = 1.
Kd : Constante de Michaelis para la degradación de la ciclina.
Kc : Constante de Michaelis para la activación de ciclina de la fosfotasa que
actúa sobre la forma fosforilizada de quinasa cdc2.
kd : Velocidad (constante) relacionada con la degradación no especı́fica de
ciclina .
Vi y Ki (i=1–4) caracterizan la cinética de las enzimas involucradas en los
dos ciclos: 1) La fosfotasa E1 y la quinasa E2 actúan sobre la molécula; 2) la
quinasa cdc2 (E3 ) y la fosfotasa (E4 ) actúan sobre la proteasa ciclina.
Los términos no lineales del modelo son de tipo Michaleano.
No hay cooperativismo positivo en el modelo.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
8 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Descripción
Parámetros del sistema:
vi : velocidad (constante) de sı́ntetisis la ciclina.
vd : velocidad máxima a la que es degradada la ciclina por la proteasa cuando
X = 1.
Kd : Constante de Michaelis para la degradación de la ciclina.
Kc : Constante de Michaelis para la activación de ciclina de la fosfotasa que
actúa sobre la forma fosforilizada de quinasa cdc2.
kd : Velocidad (constante) relacionada con la degradación no especı́fica de
ciclina .
Vi y Ki (i=1–4) caracterizan la cinética de las enzimas involucradas en los
dos ciclos: 1) La fosfotasa E1 y la quinasa E2 actúan sobre la molécula; 2) la
quinasa cdc2 (E3 ) y la fosfotasa (E4 ) actúan sobre la proteasa ciclina.
Los términos no lineales del modelo son de tipo Michaleano.
No hay cooperativismo positivo en el modelo.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
8 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Oscilaciones del modelo
El sistema (1) − (4) se resolvió numéricamente utilizando la rutina ode45 de
Matlab.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
9 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Oscilaciones del modelo
El sistema (1) − (4) se resolvió numéricamente utilizando la rutina ode45 de
Matlab.
Condiciones iniciales: C(0) = M (0) = X(0) = 0,01.
Parámetros:
VM 1 = 3, V2 = 1,5, VM 3 = 1, V4 = 0,5.
K1 = 0,005, K2 = 0,005, K3 = 0,005, K4 = 0,005, Kc = 0,5, Kd = 0,02.
vi = 0,025, vd = 0,25, kd = 0,01.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
9 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Oscilaciones del modelo
El sistema (1) − (4) se resolvió numéricamente utilizando la rutina ode45 de
Matlab.
Condiciones iniciales: C(0) = M (0) = X(0) = 0,01.
Parámetros:
VM 1 = 3, V2 = 1,5, VM 3 = 1, V4 = 0,5.
K1 = 0,005, K2 = 0,005, K3 = 0,005, K4 = 0,005, Kc = 0,5, Kd = 0,02.
vi = 0,025, vd = 0,25, kd = 0,01.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
9 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Condiciones iniciales: C(0) = M (0) = X(0) = 0,01.
Parámetros:
VM 1 = 3, V2 = 1,5, VM 3 = 1, V4 = 0,5.
K1 = 0,005, K2 = 0,005, K3 = 0,005, K4 = 0,005, Kc = 0,5, Kd = 0,02.
vi = 0,1, vd = 0,25, kd = 0,01.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
10 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Condiciones iniciales: C(0) = M (0) = X(0) = 0,01.
Parámetros:
VM 1 = 3, V2 = 1,5, VM 3 = 1, V4 = 0,5.
K1 = 0,005, K2 = 0,005, K3 = 0,005, K4 = 0,005, Kc = 0,5, Kd = 0,02.
vi = 0,25, vd = 0,25, kd = 0,01.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
11 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Ciclo lı́mite
Condición inicial C1: C(0) = 0,1, M (0) = 0,4.
Condición inicial C2: C(0) = 0,2, M (0) = 0,04.
Parámetros:
VM 1 = 0,5, V2 = 0,167, VM 3 = 0,2, V4 = 0,1.
K1 = K2 = K3 = K4 = 0,1, Kc = 0,3, Kd = 0,02.
vi = 0,023, vd = 0,1, kd = 0,0033.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
12 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Parámetros iguales a los anteriores.
Condiciones iniciales:
C1:
C2:
C3:
C4:
C5:
C6:
C(0)
C(0)
C(0)
C(0)
C(0)
C(0)
=
=
=
=
=
=
0,1, M (0) = 0,4.
0,0, M (0) = 0,4.
0,05, M (0) = 0,8.
0,2, M (0) = 0,04.
0,2, M (0) = 0,85.
0,3, M (0) = 0,2.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
13 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Espacio de fases
Condición inicial: C(0) = M (0) = X(0) = 0,01.
Parámetros:
VM 1 = 0,5, V2 = 0,167, VM 3 = 0,2, V4 = 0,1.
K1 = K2 = K3 = K4 = 0,1, Kc = 0,3, Kd = 0,02.
vi = 0,023, vd = 0,1, kd = 0,0033.
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
14 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Parámetros como los anteriores
Condiciones iniciales:
C1:
C2:
C3:
C4:
C5:
C6:
C(0)
C(0)
C(0)
C(0)
C(0)
C(0)
=
=
=
=
=
=
0,2, M (0) = 0,2, X(0) = 0,01
0,1, M (0) = 0,2, X(0) = 0,1
0,1, M (0) = 0,8, X(0) = 0,1
0,1, M (0) = 0,2, X(0) = 0,1
0,3, M (0) = 0,2, X(0) = 0,1
0,01, M (0) = 0,2, X(0) = 0,1
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
15 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Deducción de la función de Goldbeter-Koshland
El modelo está dado por Michaelis-Menten
d[A]
Va [I]
Vi [A]
=
−
dt
Ja + [I]
Ji + [A]
(5)
donde [I] y [A] representan las concentraciones de las enzimas catalizadas.
Debido a que el mecanismo es cı́clico y no hay pérdida de masa, adicional a
(5) tendremos
[I] + [A] = C ,
constante
(6)
Si [A] es un estado estacionario del sistema (i.e., no depende del tiempo),
d[A]/dt = 0 y la ecuación diferencial (5) se convierte en la ecuación
algebraica
Va [I]
Vi [A]
−
=0
Ja + [I]
Ji + [A]
(7)
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
16 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Para simplificar los cálculos introducimos la siguiente notación
a := [A] ,
i := [I] ,
as :=
[A]
C
(8)
De (6) tenemos i = C − a y sustituyendo en (7)
Va [I]
Vi [A]
−
=0
Ja + [I]
Ji + [A]
Va [I]
Vi [A]
=
Ja + [I]
Ji + [A]
Va i
Vi a
=
Ja + i
Ji + a
Va (C − a)
Vi a
=
Ja + C − a
Ji + a
Va (C − a)(Ji + a) = Vi a(Ja + C − a)
Va CJi + Va (C − Ji )a − Va a2 = (Vi Ja + Vi C)a − Vi a2
Al pasar todo al lado izquierdo obtenemos . . .
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
17 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
(Vi − Va )a2 + (Va C − Va Ji − Vi Ja − Vi C)a + Va CJi = 0
„
«
Ja
Ji
(Vi − Va )a2 − C Vi − Va + Vi
a + Va CJi = 0
+ Va
C
C
|
{z
}
B
Una de las raices de la última ecuación está dada por
p
(CB)2 − 4Va Ji (Vi − Va )C
2(Vi − Va )
p
p
CB − (CB)2 − 4Va Ji (Vi − Va )C CB + (CB)2 − 4Va Ji (Vi − Va )C
p
=
·
2(Vi − Va )
CB + (CB)2 − 4Va Ji (Vi − Va )C
a=
CB −
=
(CB)2 − (CB)2 + 4Va Ji (Vi − Va )C
“
”
p
2(Vi − Va ) CB + (CB)2 − 4Va Ji (Vi − Va )C
=
2Va Ji C
p
2
CB + C B 2 − 4Va Ji (Vi − Va )C
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
18 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
De la última ecuación se deduce que
as :=
a
2Va Ji
p
=
2
2
C
CB + C B − 4Va Ji (Vi − Va )C
(9)
La solución obtenida en [Aguda, 2006] (fórmula A.3, pág. 22) está dada por
as =
B+
p
2Va Ji
B 2 − 4Va Ji (Vi − Va )
(10)
y difiere de la nuestra por las C’s que aparecen en el denominador (sólo
coinciden en el caso C = 1).
Finalmente observemos que nosotros en (8) definimos
[A]
C
mientrás que en [Aguda, 2006] se define
as :=
as :=
[A]s
C
y no se aclara lo que significa [A]s .
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
19 / 20
Introducción
El modelo
Resultados
Apéndice
Referencias
Referencias
B.D. Aguda.
Tutorials in Mathematical Biosciences III, Modeling the cell division cycle
Springer-Verlag, 2006.
A. Goldbeter, D.E.,Jr. Koshland.
An amplified sensitivity arising from covalent modification in biological
systems
Proc. Natl. Acad. Sci. USA 78, 6840-6844, 1981.
A. Goldbeter.
A minimal cascade model for the mitotic oscillator involving cyclin and
cdc2 kinase
Proc. Natl. Acad. Sci. USA 78, 9107-9111, 1991.
Wikipedia contributors
Cell cycle
Wikipedia, The Free Encyclopedia., 2008.
http://en.wikipedia.org/w/index.php?title=Cell cycle&oldid=234304750
Modelo de cascada mı́nimo propuesto por A. Goldbeter para el sistema ciclina - quinasa cdc2.
20 / 20
 0
0
Anuncio
Documentos relacionados
Descargar
Anuncio
Añadir este documento a la recogida (s)
Puede agregar este documento a su colección de estudio (s)
Iniciar sesión Disponible sólo para usuarios autorizadosAñadir a este documento guardado
Puede agregar este documento a su lista guardada
Iniciar sesión Disponible sólo para usuarios autorizados