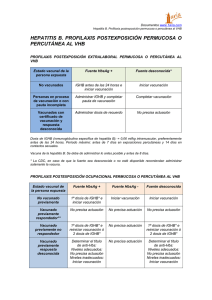
Profilaxis postexposición a la hepatitis B
Anuncio

EN ESTE NUMERO Redacción: CADIME Escuela Andaluzade Salud Publica. Aptdo. 2070. 18080 Granada. Espar'la. TIno. (958) 16 10 44. Fa. (958) 16 12 04 n ' 1 • Utilización de Medicamentos Profilaxis postexposición a la hepatitis B En la profilaxis postexposicián a la hepatitis B, la administración conjunta de la inmunoglobulina y la vacuna aporta una protección a corto y a largo plazo frente a la enfermedad. 2 • Tribuna terapéutica Hiperuricemia asociada a la utilización de pirazinamida El tratamiento de la tuberculosis con pirarinamida se asocia a incrementos en los niveles sanguíneos de ácido úrico, que en algunos pacientes provoca la aparición de sintomatología. m Util ización de Medicamentos Profilaxis postexposición a la hepatitis B La hepatitis B representa un problema de salud pública a nivel mundial. Inicialmente se inmunizaba sólo a los grupos de alto riesgo, pero con poco éxito, por lo que se ha adoptado una estrategia global que también incluye la inmunización de los niños. En Andalucía se ha introducido la vacunación antihepatitis B en el calendario vacuna!. Tras la exposición al virus de la hepatitis B está indicada la profilaxis en situaciones de exposición perinatal, exposición accidental a través de piel o mucosas, exposición sexual y exposición intrafamiliar. La pauta de inmunoprofilaxis combinada (pasiva-activa) con la inmunoglobulina y la vacuna de la hepatitis B, es la terapia de elección. IICUILA "ID.llUIA DI~lUD ,Q.LlC. La hepatitis B (HB) es una infección extendida por todo el mundo que es endémica en el Africa sub-sahariana y en el sureste de Asia. En las áreas de alta endemia, una gran parte de los niños contraen la infección en los primeros años de vida. Los niños nacidos de madres portadoras crónicas de la enfermedad presentan un alto riesgo de desarrollar la infección durante el período perinatal. La transmisión intraútero es rara, ya que el virus no atraviesa fácilmente la barrera placentaria intacta. En la primera infancia es frecuente la transmisión entre hermanos y con los contactos cercanos (1). La HB representa un problema de salud pública en todo el mundo, con 300 millones de personas portadoras del virus de la HB. Cada año mueren 250.000 personas por enfermedades hepáticas relacionadas con la HB (2-3), mientras que otros padecen la enfermedad durante décadas (2). Dos formas importantes de transmisión en adultos no infectados previamente son el contacto sexual y la transfusión sanguínea en algunos paises. Los drogadictos y los profesionales sanitarios tienen un alto riesgo de infección por inoculación con sangre infectada (1). En los niños y adolescentes jóvenes la HB se propaga frecuentemente por los contactos interpersonales de sus actividades cotidianas (4). En EE.UU. se introdujo por primera vez la vacuna de la HB en 1982 con una estrategia que sólo iba dirigida a grupos de alto riesgo (contactos familiares y sexuales de personas infectadas por PROTOCOLOS DE INMUNOPRORLAXISPOSTEXPOSIOON A LA HEPATITIS B el virus de la HB, homoSEGUN EL TIPO DE EXPOSICION sexuales, drogadictos por vía parenteral, EXPOSIClON INMUNOPROFILAXIS hemodializados, hemofílicos y personas con Perinatal VacHB + IGHB múltiples parejas sexuaSexual les). Esta estrategia tuvo Infección aguda IGHB ± Vac HB un escaso impacto VacHB Infección crónica sobre la incidencia de la HB y sobre la prevenContacto familiar ción de la infección VacHB Portador crónico durante la infancia, Contacto estrecho, caso agudo IGHB + Vac HB Contacto casual, caso agudo debido al difícil acceso a Ninguno las personas de alto Exposición accidental por piel o IGHB + Vac HB riesgo, entre otros proTabla 1 mucosas (no vacunado) blemas. Por ello, finalTomada de. (4) mente se ha adoptado una estrategia global (anti-HBs). Suelen aparecer cuando consecuencias. que también incluye la inmunización La HB suele cursar de forma se negativiza el AgHBs y la infección rutinaria de niños, en un intento de aguda se ha resuelto. Son los resanictérica en los niños, y con manieliminar tanto la transmisión como ponsables de la inmunidad a largo festaciones clínicas de daño hepátilas consecuencias de la HB (5). plazo (1). co, incluyendo ictericia, en los adulCon la estrategia de vacunación - Anticuerpos frente al antígeno infantil universal se puede eliminar la tos y niños mayores. Raramente evodel core de la HB (anti-HBc). transmisión perinatal de la HB y luciona de forma fulminante y fatal. La mayoría de los niños infectados Aparecen a los 2-3 meses de la infecdetener la transmisión infantil, pero se sabe que no tiene un impacto sig- llegan a hacerse portadores crónicos ción aguda y pueden detectarse durante largo tiempo (1). nificativo sobre los adolescentes y los del virus (1). - Antígeno HBe (AgHBe). Indica La infección se acompaña de la jóvenes (6-7), por lo que en este un alto nivel de replicación vírica e aparición de varios marcadores intervalo sería necesaria la vacunainfectividad (1). inmunológicos: ción de grupos adicionales para con- Anticuerpos frente al antígeno - Antígeno de superficie del seguir una reducción rápida del HBe (anti-HBe). Aparecen tras la virus de la HB (AgHBs). Se detecta grado de infección (6). muy precozmente en suero, aproxiinfección aguda y frecuentemente En este sentido, en Andalucía madamente a los 30-60 días tras la persisten en el suero de los portadorecientemente se ha puesto en marexposición y cuando la positividad res una vez que el AgHBe ha desapacha un programa de vacunación unirecido (1). se mantiene durante seis meses o versal contra la HB integrada en el De todos estos marcadores, el más, indica un estado de portador calendario vacunal rutinario en neocrónico (1). AgHBs y el anti-HBc se consideran natos y niños de 12 años, como marcadores serológicos prevacuna- Anticuerpos frente al antígeno estrategia para eliminar la transmisión del virus de la HB y sus graves de superficie del virus de la HB les; el anti-HBs es un marcador post- ------------------_......: RECOMENDAaONES PARA LA PROFILAXIS DE LA HEPATITIS BTRAS LA EXPOSIOON CUTANEA OMUCOSA TRATAMIENTO CUANDO LA FUENTE ES: PERSONAS EXPUESTAS FUENTE NO ANALIZADA O AgHBs-POSITIVO AgHBs-NEGATIVO DESCONOCIDA No vacunados IGHB (1 d)(a) + Iniciarvac HB Iniciar vac HB Iniciarvac HB Vacunados previamente con respuesta inmunológica positiva Analizar anti-HBs: 1- Si es adecuada (b): no tratar. 2- Sies inadecuada: 1 dosis de recuerdo de la vac HB. No tratar No tratar Vacunados previamente sin respuesta inmunológica positiva IGHB (2d) (c)o IGHB (1 d) + 1 dosisde recuerdo de vac HB No tratar Si la fuente es de alto riesgo, tratar como si fuera AgHBs-positiva. Vacunados previamentecon respuesta inmunológica desconocida Analizar anti-HBs: 1- Si es adecuada: no tratar. 2- Sies inadecuada, IGHB (1 d) + 1 dosis de recuerdo de vac HB. No tratar Analizar anti-HBs: 1- Si esadecuada: no tratar. 2- Sies inadecuada, 1 dosis de recuerdo de la vac HB. Tabla 2 (al 1 dOSIS: 0,06 mi / Kg 1M. Tomada de (10, 11) (b) La respuesta adecuada a anti-Hss es ~ a 10 mUI/ml. (e) La primera dosis de IGHB lo antes posible tras la exposición y la segunda dosis un mes después. 2 .!.":o! :Au' ANDA L 1995; 11 (1) vacunal que se determ inará pasados de 1 a 6 meses de la vacunación, o bien a los 3 - 9 meses, en los recién nacidos de madres portadoras (8). Internacionalmente se acepta como t ítulo protector de an t i- HBs aq uel que es superior a 10 UI/I (9). la seg u n da y te rc era do sis d e la IGHB. Además, a los niños no inf ectad os d urante el per iodo pe rinat al les conf iere inmunidad a largo plazo (8,12). EXPOS ICION A TRA VES DE PIEL Y M UCOSAS PROFILAX IS POSTEXPOSICION Tras la expo sición al virus de la HB se debe hacer pr o fil axi s, par a prevenir la infección, en las siguientes situacio nes: - expo sición peri natal de un niño nacido de una madre AgHBspositiva, - exposición accidental a través de piel o mucosas a sangre AgHBspositiva, - exposició n sexual con personas AgHBs-posit ivas, - expos ic ió n in t raf am ilia r d e niños menores de 12 meses de edad cua ndo la pe rsona que los cui da tiene una HB aguda (10). En estudios prospectivos realizados en niños con expo sición perinatal al AgHBs, hijo s de m adres AgHBe-positivas, se ha demostrado la efi cacia de la vacuna de la HB (Vac HB) y de la inmunogl obulina de la HB (IGHB). A consecuencia de estos bu en os resultados en niño s, y por ext en sión , se han m odifi cad o las reco menda ciones de la profil axis postexposición en adultos, en el sentido de incluir la vac HB con la pauta al t e rn at iva rápida ( O, 1, 2 , Y 12 meses)(4). La pauta de inmunoprofil axis co m b ina d a (pasiva-acti va) apo rta inm unidad a corto y largo plazo y además, resulta más econó mica que el rég imen de 2 do sis de IGHB ( 1, 10 -11) . Aunque co n anteriorid ad únicament e se ut ilizaba la inmunización com binada en exposicio nes de a lt o ri esg o , actu alm ente en lo s EE .UU. el Comité Asesor sobre Práct icas de Inmunización (ACIP) consider a la inmunización co m binad a, como terapia de elección en la profilax is po stexpos ición en t o dos los casos( l1). La Tabla 1 present a los protocolos de profilaxis postexpo sición a la HB en fun ción de lo s d istintos tipo s de exposición. EXPOS ICION PERINATAL El principal objetivo de la pro f ilaxi s postexposición per inatal es evit ar que los niños se co nviert an en po rtadores de la HB, aun qu e tam bién es importante prevenir la apar ición de una hep at it is clínica grave ( 12) . Con la inmunoprofilaxis pasivaactiva que combi na la IGHB con la vac HB (0,5 mi/1M), prefer ent ement e dentro de las 12 horas posterior es al nacimiento, la eficacia aumenta y se elimina la necesidad de adm inistrar Después de la exposició n acciden t al a sangre a tra vés de pi el o mucosas, y antes de instaurar la prof il axi s, h ay q u e co nsi d er ar lo s siguientes facto res: 1) respecto a la f uent e de infección (sangre): po sib ilidad de an alizarla, para dete rminar el AgHBs; 2) respe cto a la persona expuesta si está o no vacunada, y la respu e st a i n m u n ol ó g i ca en su caso ( 10) . En la tabl a 2 se señ alan las difer ent es paut as de profila xi s ten iendo en cu en t a la s d istint as situacio nes que se pueden presentar en f unc ión de los f act or es citados anteriormente (10). EXPOSIC ION SEXUAL E INT IM A Las parejas de personas AgHBsposit ivas, tien en un alt o riesgo de sufr ir un a HB y, en éstos casos la IGHB es ef ic az en el 75 % de lo s casos. La información disponible en este tip o de profil axis postexposición es escasa, pero si se extr apolan los result ados o bt enidos en estudios realizado s en otr os mecanismos de transm isión , parece que es preciso administrar la IGHB antes de que transcurran 14 días desde el último contacto sexual para que sea eficaz. El AC IP recom iend a que todos los ind ividuos suscepti bles de tener conta ct o sexua l o ín t imo co n qui en tiene una HB activa, contrae una HB, o es un por tad o r crónico , debe n recibir una profilaxis postexposición con una dosis única de IGHB e iniciar la vacunación de la HB (10-11). Ante s del trat amiento, y sin que se demore más de 14 días, es importante hacer un estudio serológico de la pareja y, en especial una determinación del nivel de anti-HB c ( 10- 11). Si se admi nist ran la IGHB y la vac HB conju nta mente, puede mejorar la efi cacia del t ratamient o postexposición y además, la vac HB confiere inmun idad a largo plazo (1011) EXPOSIC ION INTRAFAMILlAR Cuando la madre o la persona q ue est á al cuidado del niño menor de 12 meses, tiene una HB agud a, está indicado hacer una profil axis con la vac HB y con IGHB (0,5 mi) en el niño, ya que en éstos casos el contacto es muy estrecho y los niño s pequeños presenta n un alto riesgo de convert irse en portadores tra s una infe cción aguda por el virus de la HB (10- 11). En ot ros t i pos de con tac t o int rafamiliar no está ind icada la profilax is, a no ser que se conozca una exposición a la sangre del paciente, origin ada por ejempl o , por compartir cepillos de dientes, máqui nas de afeitar... etc. Estos casos se tr atan de igual form a que las exposiciones por contacto sexual (10). En el caso de que el pacie nte qu e ti ene la HB agu d a se convierta en portado r, t odos los co nta ct os f am ili ares deb er ían rec ibi r la vac HB (10). CONCLUSIONES La inmunoprofilaxis pasiva-activa (IGHB + vac HB) es eficaz en individuos expuestos accidentalmente a sang re inf ectada por el viru s de la HB, neonatos na cido s de m adres inf ecta das por HB y persona s q ue t ien en co nt act o sexual con ind ivid uo s co n HB, ya que apo rt a un a protección a corto y a largo plazo f rent e a la enfermedad. De forma general se considera la inm unización combin ada, com o tera pia de elección en la prof ilaxis post exposición a la HB en tod os los casos, aunq ue existen ciertas matizacion es y diferen cia s, relacionada s con el tipo de exposició n O BIBL/OGRAFiA 7- Virai hepati(¡s. WHO Orug Inf 7993; 7(3) ' 728-33. 2- Krahn M et al. universo! hepati(¡s B vaconation: the economics o f prevention. Can M ed Assoc J 1992; 746 :19 2 1. 3- Econom ic da ta sugg est hepa ti tis 8 vaccina rion is general/y ju srified in neona res and high-risk adult s. Orugs Ther Perspect 79 94; 3: 7-5. 4- Oindzans VI Viral hepa tis. Preexposure and postexposure prop hylexis. Postgrad M ed 1992, 92 (4):43 52. 5- Shapiro CN. Epidemiology of hepatius 8 Pediatr Infect 015 J 7993; 12 (5)' 433 -7 6- Goldberg NA et al. Hepat it is B in Cana da: the case for un iversal vaccination. Can Med Assoc J 1992; 146 '25· 8. 7- de Clavija I et al. Updat e on childho od imm unizations. Ann Pharmaco rher 7994; 28:6 33 -42. 8 - Normativa de vacunación contra la Hepatitis B en Andalucia. Circu lar 7/92 de 23 de Junio de la Consejeria de Salud de la Junta de Andalucia Pharmacother 7994; 28: 633 -42 . 9- Saenz MC Hepat itis virica. EN: Piédrola G y cols. M edicina Preventiva y Salud Pública, 9" ed. Barcelona ' Masson -Salvat, 7997 .'672 -94 . 10- Recommendation s of (he Immunization ñecuces Advisory Com mit tee (AClP). Hepatitis 8 viru s: A comprehensive stra tegy for eiJmina ting transmission in the United States rhrough universal childhoo d vaccina tion . MMWR 7997. 40 (RR73!:7 -25 77- McEvoy GK, edit or. AHFS 94: Orug In formation. Bethesda: American Society of Hospita l Pnetmecists. 7994.2148-54.21 9 5·203. 72- Hepati/is B immune globulin 7984 COC rccommen de notv: (Orug Consul ts) IN. Gelman CR. et a l (eds): Orugdex@ mtot metton System . M ieromedex . tnc., Oenver. Colorado u />"/7..'r ANDA L 1995 ; 11 (1) 3 - Hiperucemia asociada a la utilización de pirazinamida 25 El papel de la pirazinamida en el tratamiento de la tuberculosis se ha reforzado ~ ~ e como parte esencial de los regímenes cortos de tratamiento de esta enfermedad. Su uso se asocia a incrementos en los niveles de ácido úrico que, normalmente, no suelen causar sintomatologia. Cuando aparecen síntomas, y aunque se han descrito algunos casos de gota en pacientes con antecedentes , generalmente se trata de cuadros de polialtralgia no gotosa (de carácter autolimt tado¡ que no precisan interrumpir el tratamiento con este medicamento. ~ La pirazinamida es un medicamento que se ha venido utilizando desde hace años como agente de segunda línea en el tratamiento de la tuberculosis, aunque en los últimos tiempos, ha pasado a desempeñar un papel más importante como parte esencial de los regímenes cortos de quimioterapia antituberculosa junto a la isoniacida y la rifampicina (1). La pirazinamida, presenta una excelente penetración a través de las membranas biológicas y una mínima incidencia de efectos adversos cuando se utiliza durante períodos breves de tiempo (1). No obstante, por un mecanismo no totalmente aclarado, parece que el ácido piraziónico, principal metabolito de la pirazinamida, inhibe la secreción tubular de ácido úrico induciendo un incremento en las concentraciones séricas de éste (1,2,3,4,5) Este incremento en los niveles de ácido úrico, que suele aparecer en los primeros días del tratamiento con este fármaco (2,4,6), generalmente no suele producir sintomatología en los pacientes tratados, si bien se han descrito dos tipos de cuadros clínicos distintos: - En una minoría de los casos se asocia con la aparición de gota en pacientes con antecedentes de esta enfermedad (2,6,7,8); en estos casos, la administración concurrente de agentes uricosúricos con la pirazinamida, puede reducir la hiperuricemia (2). Si ésta es grave o se acompaña de sintomatología se aconseja interrumpir el Programa del Servicio Andaluz de Salud dirigido por la Escuela Andaluza de Salud Pública tratamiento con pirazinamida (2,6). - Se han descrito cuadros de poliartralgía no gotosa en más del 40% de los pacientes tratados con pirazinamida (1,2.4,5,6,7,9). Estos cuadros, a diferencia de la poliartralgia gotosa, afectan a las articulaciones grandes y pequeñas (las más frecuentes son hombros, rodillas y dedos), siendo con frecuencia autolimitados y respondiendo al tratamiento sintomático con ácido acetilsalicílico (4,5,6,7). Normalmente, la aparición de cuadros de este tipo no requiere la interrupción del tratamiento con pirazinamida (1,2,5,6,7,9). Los cuadros de poliartralgia no gotosa son más frecuentes durante la terapia diaria que durante la terapia intermitente con pirazinamida (4,5,7); al mismo tiempo, las concentraciones séricas de ácido úrico son significativamente mayores durante la terapia diaría que durante la terapia intermitente con pirazinamida (7). La incidencia es menor en aquellos enfermos a los que se administra rifampicina de forma conjunta con pirazinamida, lo que parece deberse a la inducción enzimática a nivel microsomal hepático originada por la rifampicina (1,5). En conclusión, la aparición de hiperuricemia asociada al tratamiento con pirazinamida es un efecto adverso bien conocido asociado a la terapia con este fármaco. La hiperuricemia aparece en más del 40 % de los pacientes tratados, sobre todo en los primeros días de tratamiento, y generalmente no suele producir sintomatología. 4 7- Girling O J. Adverse effects of antituberculosis drugs. Drugs 1982, 23:56-74. 8- Hart FD. Drug-induced arthritis and arthralgia. Drugs 1984; 28:347-54. 9- American Medical Association (eds.): Drug Evaluations. Annual 1993. Chicago 1993. p:1610. Ram ón CosCil lo F"erran do , Javier Galia na M arn nez. Pab lo Gar ete López, Raf ael Pe inado A lvarez, Julio Romero González, Antonio Matas Hoces, M aria Teresa Nieta Rodriguez, José Maria Recalde M an nqu e . 24:1115-6. Angel Gil a .vas. Maria Isabel Lucena SECRfT. Anto nio M atas Hoces 548-51. 4- Nariman S. Adverse reactions to drug used in the treatment of tuberculosis. Adverse Drug React Acute Poisoning Rev 1988,4:207-27. 5- Pyrazinamide (Drug Evaluation) in Gelman CRet al (eds): Drugdex® Information System. Micromedex, tnc., Denver, Colorado. 6- Amodio MI et al. Development of acute gout secondary to pyrazinamide in a patient without a prior history of gout (letter). Ann Pharmacother 1990; C a n e la , v icto r Bollv a r Gal iana, Juan Go nz ález, M ig uel M arq ués. de Torr es. REOACClON: 818L10GRAFíA 1- Steele MA et al. The role of pyrazinamide in tuberculosis chemotherapy Chest 1988; 94:845-50. 2- American Society of Hospital Pharmacists (eds): AHFS Drug Information 1994; 8ethesda, 1994. p.377. 3- Natural deterioration or drug induced? Adverse Drug React 8ul/ 1991, 146: CONSEJO DE REOACClON: Manano Aguayo CONSEJO DE REDACCION REOAaOR JEFE: José M' Recalde Manri que Redacción CADIME: VIC to ria n ménez Esprnola. Maria del Mar La ~ n e z Sánchez, No obstante se han descrito dos cuadros clínicos distintos asociados al aumento en los niveles séricos del ácido úrico: poliartralgía gotosa en una minoría de los pacientes, que en caso de ser grave precisa de la interrupción del tratamiento con pirazinamida; y poliartralgía no gotosa, mucho más frecuente y con frecuencia autolimitada, que responden bien al tratamiento sintomático con ácido acetilsalicílico y no requiere, por lo general, la interrupción del tratamiento con pirazinamida D Francisco Martfn ez Ho mero , Anto nio Ma nue l d e la Rosé! Fra ile, Jo sé Sa r-rb e z M orcillo DISEÑO GRAFI(O: Pablo Gallego Córdoba IMPR.ESION Copartgrat Granada. l ío; ;;'FAN DAL 1995; 11 (1) S~rvício A"~Ul d~ S4lud