FACULTAD DE INGENIERÍA Y CIENCIAS AGROPECUARIAS
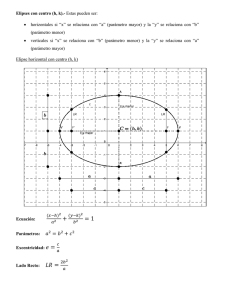
Anuncio

FACULTAD DE INGENIERÍA Y CIENCIAS AGROPECUARIAS VERMIFILTROS PARA EL TRATAMIENTO DE AGUAS RESIDUALES Trabajo de Titulación presentado en conformidad con los requisitos establecidos para optar por el título de Ingeniera Ambiental en Prevención y Remediación Profesor Guía Ing. Yasser Alejandro González Romero, MSc. Autora Verónica Gabriela Velasco Andrade Año 2015 ii DECLARACIÓN DEL PROFESOR GUÍA “Declaro haber dirigido este trabajo a través de reuniones periódicas con el estudiante, orientando sus conocimientos y competencias para un eficiente desarrollo del tema escogido y dando cumplimiento a todas las disposiciones vigentes que regulan los Trabajos de Titulación”. Yasser Alejandro González Romero Ingeniero MSc. CI: 070373762-7 iii DECLARACIÓN DE AUTORÍA DEL ESTUDIANTE “Declaro que este trabajo es original, de mi autoría, que se han citado las fuentes correspondientes y que en su ejecución se respetaron las disposiciones legales que protegen los derechos de autor vigentes.” Verónica Gabriela Velasco Andrade CI: 080252945-3 iv AGRADECIMIENTOS A Dios porque su presencia ha sido sentida en cada instante de mi vida. A mis padres que con su ejemplo, consejos y amor me han acompañado en este camino. A la Ing. Paola Posligua por su amable y constante ayuda. Al Ing. González por su motivación durante mi formación profesional. Al Ing. Wilson Tapia, al Ing. Javier Álava, al PhD Markus Gräfe por su tiempo y gentil colaboración. A mis amigos Pavi y Sebastián por su apoyo. v DEDICATORIA Dedicado con todo cariño a mi padre quien con su sacrificio y trabajo duro ha sacado adelante a mi familia. A mi madre por su total entrega. A mi hermano por su compañía incondicional. A mis dos ángeles en el cielo. A Gonzalo por darle esa chispa de emoción a mi vida. Los amo infinitamente. vi RESUMEN En Ecuador, se reporta que en promedio reciben tratamiento el 6,3% de las aguas residuales. A nivel rural reciben tratamiento el 5%, mientras que a nivel urbano un 7%. Generalmente las aguas residuales son vertidas directamente al sistema de alcantarillado o conducidas a cursos de agua. La concentración de contaminantes de las aguas residuales domésticas tiende a variar según los hábitos de la población, estilo de vida y los aspectos culturales y climáticos, pero en general suelen presentar tres rangos de concentración: fuerte, medio y bajo. El objetivo de este estudio fue tratar aguas residuales domésticas de fuerte y mediana concentración mediante tres vermifiltros, filtros biológicos que combinan los conocimientos del proceso de filtración convencional y las técnicas de vermicompostaje. Los vermifiltros se conformaron con grava, arena, suelo, fibra de coco, aserrín y lombrices de tierra de la especie Eisenia foetida. Mediante la incorporación de fibra de coco al sistema, se logró obtener una mayor remoción de contaminantes; para el agua residual de concentración fuerte la remoción obtenida fue: 97,7% de turbidez, 59,7% de conductividad eléctrica, 81,4% de sólidos totales, 94,5% de DBO5, 94,1% de DQO, 74,5% de nitrógeno total y 50,6% de fósforo total. Para el agua residual doméstica de concentración media, la remoción alcanzada fue: 98,3% de turbidez, 32,6% de conductividad eléctrica, 66,2% de sólidos totales, 97,6% de DBO 5, 96,6% de DQO, 74,2% de nitrógeno total y 85,2% de fósforo total. Los resultados obtenidos sugieren que la fibra de coco puede ser utilizada como variante en el sistema tradicional de vermifiltración. vii ABSTRACT In Ecuador, the wastewater treatment coverage is in average 6.3%. In rural areas the average is 5 % while in urban areas is the 7%. In general, wastewater is discharged directly in water bodies. The concentration of pollutants in domestic wastewater varies according with the habits of the population, lifestyle, cultural and climate aspects. But in general there are three concentration ranges: strong, medium and low. The goal of this study was to treat two of these three types of domestic wastewater. The technology used was Vermifilters which is a biological treatment that works as a filter with vermicomposting techniques. The three Vermifilters were built in layers of gravel, soil, sand, coconut fiber, sawdust and worms (Eisenia foetida). With the incorporation of coir in the system, it was possible to obtain a greater treatment of contaminants; for the highest wastewater concentration, the treatment was: 97.7% of turbidity, 59.7% of electrical conductivity, 81.4% of total solids, 94.5% of BOD5, 94.1% of COD, 74.5% of total nitrogen and 50.6% of total phosphorus. For domestic wastewater with medium concentration, removal achieved was: 98.3% of turbidity, 32.6% of electrical conductivity, 66.2% of total solids, 97.6% of BOD5, 96.6% of COD, 74.2% of total nitrogen and 85.2% of total phosphorus. The results suggest that coconut fiber can be used as an alternative support layer in the traditional vermifiltration system. ÍNDICE INTRODUCCIÓN ...................................................................................... 1 Antecedentes .............................................................................................. 1 Alcance ......................................................................................................... 2 Justificación ................................................................................................. 3 Objetivos....................................................................................................... 4 Objetivo General .......................................................................................... 4 Objetivos Específicos................................................................................... 4 I. DESARROLLO DEL TEMA.............................................................. 5 CAPÍTULO I: MARCO REFERENCIAL .......................................... 5 1.1 Agua ....................................................................................................... 6 1.1.1 Uso del agua en Ecuador ................................................................... 6 1.1.2 Aguas residuales ................................................................................ 7 1.1.3 Marco legal........................................................................................ 10 1.2 Vermifiltro ............................................................................................ 12 1.2.1 Tecnología ........................................................................................ 12 1.2.2 Componentes del Vermifiltro ............................................................. 13 CAPÍTULO II: METODOLOGÍA ....................................................... 18 2.1 Descripción del experimento........................................................ 19 2.1.1 Materiales de construcción ............................................................... 19 2.1.2 Estratificación de los vermifiltros ....................................................... 20 2.2 Condiciones de operación ............................................................ 25 2.2.1 Carga hidráulica ................................................................................ 25 2.2.2 Carga orgánica superficial ................................................................ 26 2.2.3 Tiempo de retención hidráulico ......................................................... 26 2.2.4 Porosidad .......................................................................................... 26 2.3 Caracterización físico-química del agua residual y tratada .. 27 2.3.1Turbidez ............................................................................................. 28 2.3.2 pH ..................................................................................................... 28 2.3.3 Conductividad Eléctrica .................................................................... 28 2.3.4 Sólidos Totales ................................................................................. 29 2.3.5 Demanda Química de Oxígeno......................................................... 29 2.3.6 Demanda Biológica de Oxígeno (DBO5) ........................................... 30 2.3.7 Nitrógeno Total ................................................................................. 31 2.3.8 Fósforo Total ..................................................................................... 32 2.4 Medición de las propiedades físicas de los sustratos ............ 33 2.4.1 Temperatura ..................................................................................... 33 2.4.2 pH ..................................................................................................... 33 2.4.3 Textura.............................................................................................. 34 2.5 Análisis estadístico......................................................................... 34 CAPÍTULO III: RESULTADOS Y ANÁLISIS .............................. 35 3.1 Caracterización del agua ................................................................. 36 3.1.1 Agua residual .................................................................................... 36 3.1.2 Efluente ............................................................................................. 38 3.2 Condiciones de funcionamiento ..................................................... 40 3.2.1 Funcionamiento ................................................................................ 40 3.3 Análisis estadístico............................................................................ 47 3.3.1 Parámetro Turbidez .......................................................................... 49 3.3.2 Parámetro pH ................................................................................... 59 3.3.3 Parámetro Conductividad Eléctrica ................................................... 65 3.3.4 Parámetro Sólidos Totales ................................................................ 70 3.3.5 Parámetro DBO5 (Demanda Biológica de Oxígeno) ......................... 76 3.3.6 Parámetro DQO (Demanda Química de Oxígeno) ........................... 79 3.3.7 Parámetro Nitrógeno Total ................................................................ 83 3.3.8 Parámetro Fósforo Total ................................................................... 86 CAPÍTULO IV:CONCLUSIONES Y RECOMENDACIONES ........................................................................ 89 4.1 Conclusiones ...................................................................................... 89 4.2 Recomendaciones ............................................................................ 91 REFERENCIAS ....................................................................................... 93 ANEXOS ................................................................................................... 105 ÍNDICE DE FIGURAS Figura 1. Resumen del Marco Referencial. ........................................................ 5 Figura 2. Caudal concesionado de uso y aprovechamiento de agua. ................ 6 Figura 3. Resumen de la metodología. ............................................................ 18 Figura 4. Esquema del experimento. ................................................................ 20 Figura 5. Conteo de las lombrices empleadas en la experimentación. ............ 22 Figura 6. Estratificación de los vermifiltros. ...................................................... 24 Figura 7. Materiales utilizados en la estratificación de los vermifiltros. ............ 24 Figura 8. Diagrama del proceso de medición de la demanda química de oxígeno mediante fotometría. ........................................................................... 30 Figura 9. Diagrama del proceso de medición de nitrógeno total mediante fotometría. ........................................................................................................ 32 Figura 10. Diagrama del proceso de medición de fósforo mediante fotometría ......................................................................................................... 33 Figura 11. Resumen de los resultados y análisis. ............................................ 35 Figura 12. Estado de la capa 1 en los vermifiltros. ........................................... 43 Figura 13. Incremento de la biomasa de lombrices en los vermifiltros. ............ 46 Figura 14. Resultados de turbidez en los efluentes en función del tiempo (Etapa 1)........................................................................................................... 53 Figura 15. Resultados de turbidez en los efluentes en función del tiempo (Etapa 2)........................................................................................................... 54 Figura 16. Porcentaje de remoción de turbidez en la etapa 1. ......................... 56 Figura 17. Apariencia del agua residual antes y después del tratamiento Etapa 1 ............................................................................................................. 57 Figura 18. Porcentaje de remoción de turbidez en la etapa 2. ......................... 57 Figura 19. Apariencia del agua residual antes y después del tratamiento Etapa 2 ............................................................................................................. 58 Figura 20. Resultados de pH en los efluentes en función del tiempo (Etapa 1) ............................................................................................... 62 Figura 21. Resultados de pH en los efluentes en función del tiempo (Etapa 2).......................................................................................................... 63 Figura 22. Tendencia del parámetro pH en los vermifiltros en función del tiempo. ............................................................................................................. 63 Figura 23. Resultados de conductividad eléctrica en los efluentes en función del tiempo (Etapa 1)............................................................................. 67 Figura 24. Resultados de conductividad eléctrica en los efluentes en función del tiempo (Etapa 2)............................................................................ 68 Figura 25. Tendencia del parámetro conductividad eléctrica en los vermifiltros en función del tiempo. .................................................................... 68 Figura 26. Resultados de sólidos totales en los efluentes en función del tiempo (Etapa 1). ........................................................................................ 72 Figura 27. Resultados de sólidos totales en los efluentes en función del tiempo (Etapa 2). ........................................................................................ 73 Figura 28. Tendencia del parámetro sólidos totales en los vermifiltros en función del tiempo. ........................................................................................... 73 Figura 29. Remoción de sólidos totales alcanzada en los tratamientos en la etapa 1. ............................................................................................................ 74 Figura 30. Remoción de sólidos totales alcanzada en los tratamientos en la etapa 2. ............................................................................................................ 75 Figura 31. Resultados en la etapa 1 de DBO5 en los tratamientos. ................. 76 Figura 32. Resultados en la etapa 2 de DBO5 en los tratamientos. ................. 77 Figura 33. Remoción alcanzada de DBO5 en los tratamientos en la etapa 1. .. 77 Figura 34. Remoción alcanzada de DBO5 en los tratamientos en la etapa 2. .. 78 Figura 35. Resultados en la etapa 1 de DQO en los tratamientos. .................. 79 Figura 36. Resultados en la etapa 2 de DQO en los tratamientos. .................. 80 Figura 37. Remoción alcanzada de DQO en los tratamientos en la etapa 1. ... 81 Figura 38. Remoción alcanzada de DQO en los tratamientos en la etapa 2. ... 81 Figura 39. Resultados de nitrógeno total en los tratamientos en la etapa 1. .... 83 Figura 40. Resultados de nitrógeno total en los tratamientos en la etapa 2. .... 84 Figura 41. Remoción alcanzada de nitrógeno total en los tratamientos en la etapa 1. ............................................................................................................ 84 Figura 42. Remoción alcanzada de nitrógeno total en los tratamientos en la etapa 2. ............................................................................................................ 85 Figura 43. Resultados de fósforo total en los tratamientos etapa 1.................. 86 Figura 44. Resultados de fósforo total en los tratamientos en la etapa 2. ........ 87 Figura 45. Remoción alcanzada de fósforo total en los tratamientos en la etapa 1. ............................................................................................................ 87 Figura 46. Remoción alcanzada de fósforo total en los tratamientos en la etapa 2. ............................................................................................................ 88 ÍNDICE DE TABLAS Tabla 1. Composición de las aguas residuales domésticas ............................... 8 Tabla 2. Volumen de agua consumido y tratado en Ecuador ............................. 9 Tabla 3. Vermifiltro comparado con sistemas de tratamiento convencionales . 13 Tabla 4. Características de la especie Eisenia Foetida .................................... 14 Tabla 5. Estratificación de los vermifiltros ........................................................ 23 Tabla 6. Factores de conversión en base al DBO5 esperado ........................... 31 Tabla 7. Caracterización del agua residual empleada en la experimentación .. 36 Tabla 8. Caracterización físico-química de los efluentes ................................. 39 Tabla 9. Condiciones de funcionamiento de los vermifiltros ............................. 40 Tabla 10. Propiedades de los materiales empleados en la capa uno .............. 41 Tabla 11. Resultados de las mediciones de temperatura realizadas ............... 44 Tabla 12. Incremento de la biomasa de lombrices ........................................... 45 Tabla 13. ANOVA para el parámetro turbidez Etapa 1 .................................... 49 Tabla 14. Comparaciones múltiples para el parámetro turbidez Etapa 1 ......... 50 Tabla 15. ANOVA para el parámetro turbidez Etapa 2..................................... 51 Tabla 16. Comparaciones múltiples para el parámetro turbidez Etapa 2 ......... 52 Tabla 17. ANOVA para el parámetro pH Etapa 1 ............................................. 59 Tabla 18. ANOVA para el parámetro pH Etapa 2 ............................................. 60 Tabla 19. Comparaciones múltiples para el parámetro pH Etapa 2 ................. 61 Tabla 20. ANOVA para el parámetro conductividad eléctrica Etapa 1 ............. 65 Tabla 21. ANOVA para el parámetro conductividad eléctrica Etapa 2 ............. 66 Tabla 22. ANOVA para el parámetro sólidos totales Etapa 1 ........................... 70 Tabla 23 Comparaciones múltiples para el parámetro sólidos totales Etapa 1 ............................................................................................................. 71 Tabla 24. ANOVA para el parámetro sólidos totales Etapa 2 ........................... 72 1 INTRODUCCIÓN Antecedentes El acelerado crecimiento poblacional, la presión ejercida sobre los recursos naturales, el desarrollo de zonas rurales y urbanas plantean en la actualidad grandes desafíos en cuanto a la gestión y manejo sustentable del medio ambiente. De acuerdo al informe de la CEPAL del año 2012, en el Ecuador la calidad de los recursos hídricos se ve alterada por la descarga de aguas residuales, los agroquímicos que por acción de la escorrentía superficial se desplazan hacia los cuerpos de agua y por la mala disposición de residuos sólidos. Tan solo un 7% de las aguas residuales de origen urbano e industrial reciben algún tipo de tratamiento, comúnmente son vertidas directamente al sistema de alcantarillado y conducidas a cursos de agua. (CEPAL, s.f.) Las aguas residuales domésticas (ARD) son el resultado de las descargas líquidas generadas en actividades de la vida diaria como preparación de alimentos, limpieza de baños, aseo personal, lavado de ropa, entre otros. (Palta y Morales, 2013, p. 59) La composición de este tipo de agua residual varía según los hábitos de la población y los aspectos socioeconómicos, culturales y climáticos, pero en general presentan un alto contenido de materia orgánica, nutrientes y microorganismos. Contiene alrededor de 0,1% de sólidos suspendidos, disueltos y coloidales, mientras que los nutrientes fluctúan entre 10 y 40 mg/l de K, 10 y 100 mg/l de N, y 25 mg/l de P. (Jiménez, 2009, p. 163; Torres, 2013, p. 117) Los principales problemas ambientales que se relacionan con la descarga sin tratamiento de aguas residuales domésticas son: el alto aporte de nutrientes, materia orgánica y sólidos suspendidos que contribuyen a daños en el cuerpo receptor ocasionando eutrofización, reducción de la biodiversidad, proliferación de algas, alteración en la estructura de comunidades, además de provocar 2 problemas de orden estético, recreacional y de elevar los costos de tratamiento de aguas de consumo. (Cárdenas et al., 2012, p. 112) Derivado de la importancia de brindar un tratamiento a las aguas residuales con alto contenido orgánico se han desarrollado una gran cantidad de tecnologías como humedales artificiales, biorreactores de membrana, reactores en secuencia y aireación prolongada. Sin embargo, algunos de estos tratamientos presentan limitaciones en cuanto a su operación y eficiencia. (Manosalva, Ruiz y Pérez, 2012, p. 91) Actualmente, las investigaciones están encaminadas a lograr una mayor eficiencia en los tratamientos, empleando instalaciones no sofisticadas y con bajo consumo de energía. (Sinha, Patel, Soni y Li, 2014, p. 11) Dentro de estos lineamientos se encuentra el vermifiltro, una tecnología que emplea diferentes estratos filtrantes, lombrices y microorganismos asociados. Entre las ventajas de este tratamiento tenemos que no produce lodos inestables, ocupa poco espacio y los costos operacionales son muy bajos. (Lakshmi, Ranjitha y Vijayalakshmi, 2014, p. 582; Piérart y Rojas, 2013, p. 44) Alcance El presente trabajo de titulación fue de aplicación tecnológica; se construyeron vermifiltros a escala laboratorio para evaluar la eficiencia de los estratos utilizados y la influencia de las lombrices en el tratamiento de aguas residuales, ésta fue de origen sintético y respondió a las características del agua residual doméstica. La instalación de los vermifiltros se realizó en la Universidad de Las Américas sede Queri. En el proyecto propuesto se planteó la evaluación de los vermifiltros en el tratamiento de aguas residuales. 3 Justificación La descarga de ARD genera un gran impacto tanto en aguas subterráneas como superficiales, este tipo de aguas residuales contamina recursos empleados para riego y uso doméstico, convirtiéndose en un medio potencial de transmisión de enfermedades. La contaminación de los cuerpos de agua a causa de la descarga de aguas residuales domésticas sin tratamiento se extiende en todo el Ecuador, se ha reportado que los ríos del país cercanos a zonas pobladas presentan altos contenidos de N, P y DBO 5. (Paredes, 2010) De acuerdo al informe presentado por la Organización Oxfam Internacional los recursos hídricos del Ecuador se encuentran en una situación crítica debido a que la mitad de sus principales ríos están gravemente contaminados, dentro de esta lista se destacan el río Esmeraldas, Guayas, Guayllabamba y Machángara. (Oré, Castillo, Orsel y Vos, 2009, p. 241) El Ministerio del Ambiente (MAE) ha establecido lineamientos estratégicos de investigación ambiental y entre una de sus líneas se encuentra la prevención, impacto y remediación de la calidad ambiental la cual considera prioritaria la gestión integral de efluentes. Conocidos los impactos ambientales que puede ocasionar la descarga de ARD directamente a cuerpos hídricos y los esfuerzos de las instituciones públicas por mejorar la calidad ambiental en el país, se ha identificado la necesidad de desarrollar procesos cada vez más eficientes que puedan ser empleados para el tratamiento de este tipo de aguas. El vermifiltro se presenta como una tecnología que puede ser económicamente viable, ambientalmente sustentable y socialmente aceptada, pues no requiere mucha energía, degrada casi la totalidad de sólidos orgánicos y no produce lodos inestables. Con el presente trabajo de titulación se evaluó la calidad del agua tratada con la tecnología de vermifiltros y se determinó la eficiencia del tratamiento. 4 Objetivos Objetivo General Evaluar la eficiencia de vermifiltros en el tratamiento de aguas residuales domésticas. Objetivos Específicos Caracterizar el agua residual antes y después del tratamiento con vermifiltros mediante análisis físico-químicos. Evaluar las condiciones de operación de los vermifiltros. Determinar las diferencias entre los tratamientos propuestos mediante el análisis de los porcentajes de remoción alcanzados en cada tratamiento. 5 I. DESARROLLO DEL TEMA CAPÍTULO I: MARCO REFERENCIAL La figura 1 presenta un breve resumen de los puntos a ser tratados en el presente capítulo. Uso del agua en Ecuador Aguas residuales MARCO REFERENCIAL Agua Características del agua residual doméstica Problemática ambiental Marco Legal Tecnología Componentes del vermifiltro Vermifiltro Lombrices Medio filtrante Figura 1. Resumen del Marco Referencial. 6 1.1 Agua 1.1.1 Uso del agua en Ecuador En Ecuador, el uso que se le da al agua se puede dividir en dos categorías: consuntivos y no consuntivos. Según los datos de concesiones de uso y aprovechamiento del agua de la SENAGUA publicados por la CEPAL (s.f.) los principales usos consuntivos son el agrícola que representa el 80% de las concesiones, seguido por el uso doméstico con un 13% y el industrial con un 7%; mientras que los usos no consuntivos se ven representados por la generación de energía hidroeléctrica 45,5%, la generación de energía térmica 43,11% y otros usos con el 11,38%. Para entender el escenario real de la demanda de agua y su utilización en el Ecuador es necesario conocer los caudales concesionados para cada tipo de uso. El caudal total concesionado según Vega (2009) es de 2`400.227 l/seg el cual como se refleja en la figura 2 se distribuye de la siguiente manera. 0,91% 0,05% 3,41% Consumo humano Uso en agricultura 20,95% 72,86% 0,91% Uso pecuario 1,79% Aprovechamiento Industrial Generación Energética Uso en psicultura Aprovechamiento recreativo Figura 2. Caudal concesionado de uso y aprovechamiento de agua. Adaptado de: Vega, 2009, p.310. a. Explicación: Descripción del caudal concesionado en porcentajes de acuerdo al uso en Ecuador. 7 1.1.2 Aguas residuales El término agua residual es definido por la FAO (s.f.) como aquella “que no tiene valor inmediato dada su calidad, cantidad o al momento en que se dispone de ella”. Proviene de la descarga de usos industriales, domésticos, municipales, agrícolas y pecuarios por lo que ya se encuentra contaminada con heces, orina, productos agrícolas e industriales. (Manivasakam, 2005, p. 14; Rao, Senthilkumar, Byrne y Feroz, 2012, p. 1; Tiwari, 2009, p. 4) De acuerdo al uso el agua termina con una carga contaminante distinta, las aguas residuales industriales por ejemplo contienen elevadas concentraciones de materia orgánica, altas temperaturas, compuestos inorgánicos, metales pesados, sólidos en suspensión y aceites, mientras que las domésticas se caracterizan por presentar en su composición materia orgánica, detergentes, gérmenes, sólidos, nitrógeno y fósforo y las agropecuarias elevadas concentraciones de materia orgánica, sólidos en suspensión, compuestos orgánicos, inorgánicos y pesticidas. (Antizar-Ladislao y Sheikholeslami, 2011, pp. 2–11; Robbins y Ligon, 2014, pp. 13–18; Stephens y Fuller, 2009, pp. 7–11) 1.1.2.1 Características del agua residual doméstica Las aguas residuales domésticas contienen agua en un 99,9 % y sólidos en un 0,1%. Constituyen una mezcla de contaminantes suspendidos o disueltos tanto orgánicos (70%) como inorgánicos (30%), que si bien es cierto no se encuentran en grandes concentraciones dado el volumen pueden convertirse en focos de infección, causar enfermedades al ser humano y daños al medio ambiente. Los compuestos orgánicos del ARD están constituidos por material fecal, urea, proteínas (40-60%), lípidos (10%) y carbohidratos (25-50%) entre los que se encuentran azúcares, almidón y celulosa; la fracción inorgánica está representada por nitrógeno, fósforo, arenas, gravas y arcillas. (Bitton, 2010, pp. 271–272; Knobelsdorf, 2005, p. 9; Rodríguez y Lozano, 2012, p. 14; Sekhar, Sruthi y Kumar, 2014, p. 415) 8 La composición de este tipo de agua residual tiende a variar según los hábitos de la población, estilo de vida y los aspectos culturales y climáticos, pero en general suelen presentar rangos de concentración que se muestran en la siguiente tabla. (Duncan, 2013, p. 2; Henze, 2008, p. 33) Tabla 1. Composición de las aguas residuales domésticas. Constituyente Unidad Fuerte Media Débil Sólidos totales : mg/L 1230 720 390 Disueltos totales mg/L 860 500 270 En suspensión totales mg/L 400 210 120 Sólidos sedimentables mL/L 20 10 5 DBO5 mg/L 350 190 110 DQO mg/L 800 430 250 COT mg/L 260 140 80 Nitrógeno total mg/L 70 40 20 Fósforo total mg/L 12 7 4 Aceites y grasas mg/L 100 90 50 Adaptado de: Metcalf y Eddy, 2004, p. 186.) 1.1.2.2 Problemática ambiental Bhise y Anaokar (2015, p. 44) afirman que cerca del 80% del agua usada por la sociedad se convierte en agua residual, de este porcentaje según el PNUMA (s.f.) en el mundo tan solo un 20% recibe tratamiento antes de ser descargadas en ríos y otros cuerpos de agua. En América Latina del total de agua recolectada por el alcantarillado un 15% recibe tratamiento, adicionalmente existen cuestionamientos acerca del modo de operación de las PTAR existentes. (Reynolds, 2012) En el caso de Ecuador, se reporta que en promedio reciben un tratamiento el 6,3% de las aguas residuales siendo a nivel rural un 5% y a nivel urbano un 7%. (Moncayo y Ayala, 2011) 9 Según las estadísticas ambientales presentadas por el INEC (2013, p. 16) en promedio un 49,8% de los municipios del Ecuador dieron algún tratamiento a sus aguas residuales. En la región Insular lo hizo un 66,7%, en la Costa un 51,2 %, en la Amazonía un 58,5 %, mientras que en la región Sierra disminuyó el tratamiento de un 51,1% en el año 2012 a un 44,1% en el 2013. En la tabla siguiente se expresan el volumen de agua consumido y tratado en Ecuador. Tabla 2 . Volumen de agua consumido y tratado en Ecuador. Volumen total de Volumen total de Volumen total de Región agua consumida agua residual agua residual (m3) tratada (m3) sin tratar (m3) Sierra 212.292.549,4 10.561.710,5 201.730.838,8 Costa 173.006.293,1 47.893.914,2 125.112.378,9 Amazonía 28.594.296,0 3.472.768,6 25.121.527,4 Insular 107.034,8 ND -------- Adaptado de: INEC, 2013, p. 26.) Como se muestra en la tabla anterior, en nuestro país existe un déficit en cuanto al tratamiento de las aguas residuales. La descarga directa de aguas industriales, domésticas, pecuarias y agrícolas causa problemas de diferente índole destacándose principalmente los relacionados a la salud pública y el medio ambiente. En cuanto a las ARD el mayor impacto que produce la materia orgánica biodegradable presente es la disminución de la concentración de oxígeno en los cuerpos hídricos, los microorganismos la descomponen y emplean oxígeno en el proceso. Cuando la población aumenta, se incrementa la demanda de oxígeno disuelto. Existen 3 fases de contaminación: cuando la carga orgánica es pequeña, se producirá un cambio menor en las especies de plantas, animales presentes en el agua y la contaminación se reducirá por efecto de procesos naturales de purificación. Si la carga aumenta el nivel de oxígeno disuelto decaerá y las especies se verán afectadas de acuerdo a su nivel de 10 tolerancia. Si ésta se incrementa aún más la eficacia del sistema natural para hacer frente a la contaminación disminuirá, así como el oxígeno disuelto, lo que afectará seriamente a la vida acuática. El nitrógeno y el fósforo, componentes del ARD promueven el crecimiento de las plantas acuáticas, motivo por el cual se relacionan directamente con la eutrofización. (Harrison, Chester y Slater, 2001, p. 88; Kazlauskiene, Svecevicius, Marciulioniene y Montvydiene, 2012, p. 2; Nesaratnam, 2014, p. 55; Sharma y Sanghi, 2012, p. 19) El contenido de agentes patógenos tiene serias implicaciones en la salud pública, la mala gestión del ARD puede provocar la propagación de enfermedades como hepatitis, tifoidea, cólera, disentería amebiana, enteritis, esquistosomiasis etc. (Bitton, 2010, p. 10; Tiwari, 2009, p. 28) 1.1.3 Marco legal Esta sección expone la normativa considerada para el análisis de los resultados obtenidos en el presente trabajo de investigación. Es importante iniciar mencionando que, la Constitución de la República del Ecuador es la norma suprema que rige en nuestro territorio; la misma integra al cuidado de la naturaleza como uno de los ejes fundamentales para potenciar un desarrollo sustentable en nuestro país, que se alinea con la ya conocida filosofía del Buen Vivir. Con el fin de fortalecer el cumplimiento de lo antes descrito, se han creado leyes y reglamentos que indican todas aquellas disposiciones que deben ser consideradas para la protección del medio ambiente. Uno de estos instrumentos, es la Ley de Gestión Ambiental (2004), misma que en su artículo 33 establece lo siguiente: “Art. 33.- Establécense como instrumentos de aplicación de las normas ambientales los siguientes: parámetros de calidad ambiental, normas de efluentes, régimen de permisos y licencias administrativas, evaluaciones 11 de impacto ambiental, listados de productos contaminantes y nocivos para la salud humana y el medio ambiente, certificaciones de calidad ambiental de servicios.” En referencia a la descarga de efluentes, se tiene a la Ley de Aguas (2004) que, en su artículo 22 señala: “Art. 22.- Prohíbase toda contaminación de las aguas que afecten a la salud humana o al desarrollo de la flora o de la fauna.” Asimismo, la Ley de Prevención y Control de la Contaminación Ambiental (2004), en su artículo 6 indica lo siguiente: “Art. 6.- Queda prohibido descargar, sin sujetarse a las correspondientes normas técnicas y regulaciones a los ríos, las aguas residuales que contengan contaminantes que sean nocivos a la salud humana, fauna y flora.” En función a lo previamente descrito, se ha empleado la Tabla 12 “Límites de Descarga a un Cuerpo de Agua Dulce” del Anexo 1 de la Reforma del Libro VI del Texto Unificado de Legislación Ambiental Secundaria (Norma de Calidad Ambiental y de Descarga de Efluentes: Recurso Agua), Acuerdo Ministerial 061 (2015) como la principal referencia legal que indica los límites máximos permisibles que se deben cumplir antes de realizar la descarga del efluente tratado. Dicha tabla se encuentra incluida en el Anexo 16. 12 1.2 Vermifiltro 1.2.1 Tecnología El vermifiltro es un filtro biológico que combina los conocimientos del proceso de filtración convencional y las técnicas de vermicompostaje, contiene lombrices y microorganismos asociados que degradan la materia orgánica presente en el agua residual y diferentes capas de empaque que actúan como un filtro percolador ofreciendo valores añadidos frente a tecnologías biológicas convencionales. (Mercy, Kadzungura y Boka, 2013, p. 83) Entre las ventajas que ofrece un vermifiltro en el tratamiento de aguas destacan que no existe producción de lodos (lo que involucra costos adicionales debido a la disposición final), no se producen malos olores, requiere poca energía para su funcionamiento, su operación es sencilla, la inversión económica es baja, el agua tratada puede ser empleada para usos no potables como el riego de jardines, parques y en la agricultura. Del tratamiento se obtiene vermicompost que puede ser empleado como biofertilizante. (RohitPathania y Suresh, 2012, p. 3; Sinha, Herat, Valani y Chauhan, 2010, p. 277; Sinha et al., 2014, p. 11) Investigaciones experimentales de vermifiltración llevadas a cabo por Cardoso, Ramírez y Garzón (2011, pp. 34–39) mostraron altas eficiencias en el tratamiento de ARD, reduciendo el DQO de 568 mg/l a 46 mg/l, el DBO5 de 186 mg/l a 2 mg/l y los sólidos suspendidos totales de 147 mg/l a 4 mg/l . 13 Tabla 3 . Vermifiltro comparado con sistemas de tratamiento convencionales. Parámetros de estudio área tiempo de retención Vermifiltros Lodos Activados Lagunas Aireadas 0,5 m2 / persona 0,7 m2 / persona 5 m2 / persona 30 minutos 6-8 horas 20 días equipo Muy simple requerido y (bombas y procesos desinfección) inversión Complejo (bombas, tanques de aireación, tratamiento de lodos aireadores y desinfección) US $ 35-60 / US $ 150-300 / US $ 60-100 / persona persona persona Muy baja Muy alta Alta Humus Ninguno Ninguno >90% de Remoción 80% de Remoción de DBO5 de DBO5 energía requerida recurso generado >90% de eficiencia y desinfección) Simple (bombas, Remoción de DBO5 Adaptado de: Sinha y otros, 2014, p. 21. 1.2.2 Componentes del Vermifiltro De acuerdo con Bhise y Anaokar (2015, p. 45), en un vermifiltro el agua residual es asperjada en un sustrato con lombrices y percola por el medio filtrante, la materia orgánica es consumida por las lombrices y transformada en humus, el medio filtrante contribuye a la filtración y tratamiento del agua residual debido a que adsorbe las impurezas orgánicas en su superficie. Está constituido por una capa de sustrato que alberga lombrices y diferentes capas de agregados de distinto tamaño que constituyen el medio filtrante de soporte. A continuación se menciona el rol de cada uno en el funcionamiento de esta tecnología. 14 Lombrices Son los principales organismos degradadores en el tratamiento, actúan como estimuladores biológicos y promueven el crecimiento de bacterias aerobias. Con su movimiento construyen túneles que aseguran una alta permeabilidad en el filtro; su cuerpo funciona como un biofiltro y a través de mecanismos de ingestión, biodegradación y absorción reducen patógenos, compuestos químicos y digieren materiales sólidos orgánicos presentes en aguas residuales y que comúnmente colmatan otro tipo de filtros. (Bajsa, Nair, Mathew y Ho, 2009, p. 128) Según Gheisari, Danesh y Mousavi (2010, p. 1268) y Sinha y otros (2014) Eisenia foetida, Eisenia andrei, Perionyx excavatus, Eudrilus euginae y Lumbricus rubellus han sido investigadas en el tratamiento de residuos sólidos y líquidos orgánicos, sin embargo se ha determinado que Eisenia foetida es una especie más versátil, esto debido a su alta tasa de crecimiento, alta eficiencia productiva, tolerancia a factores ambientales y a su fácil manejo. En la siguiente tabla se muestran sus principales características. Tabla 4. Características de la especie Eisenia Foetida. Diámetro Largo Peso Capacidad Condiciones reproductiva ambientales T:15,7- 28,2 oC Eisenia foetida 3-5 mm 4-10 cm 0,6-1 gr 1300 lombrices Humedad: 70- al año 80% pH: 5-8.4 Adaptado de: Campesinos, Conde, Fajardo, Delgado y Aguirre, 2005, pp. 114116; Velásquez, 2008, pp. 59-61.) Las lombrices de esta especie consumen una cantidad de alimento similar a su peso, incorporan una tercera parte del alimento consumido a su masa corporal y el resto lo transforman en humus un producto útil como fertilizante orgánico que contiene fósforo, potasio, nitrógeno, calcio, magnesio entre otros nutrientes 15 y que puede ser utilizado en jardines y huertos. (De la Cruz et al., 2010, p. 364; López, Sañudo, Armenta, Rey y Félix, 2013, p. 82) Poseen órganos sexuales tanto femeninos como masculinos, se reproducen por fertilización cruzada y ponen un cocón cada 10-30 días. Cada cocón contiene por lo general de 2 a 11 lombrices que a los 21 días emergen. Las lombrices miden de 12-15 mm a los 15 días y tienen un color rosa pálido, presentan un color rojo oscuro, clitelio y miden unos 3 cm a los 90 días y ya son capaces de reproducirse. A los 7 meses pesan 1 gramo y miden de 8 a 10 cm. (Durán y Henríquez, 2009, p. 279; Gonzalez, 2008) Organismos Asociados Las lombrices actúan como estimuladores biológicos y promueven el desarrollo de organismos aerobios descomponedores que contribuyen a la depuración de los contaminantes. Existe una relación entre la cantidad de lombrices y bacterias, pueden vivir sinérgicamente pseudomonas, haerotilus natans, nitrobacter, achromobacter, alcaligenes entre otros. (Cardoso et al., 2011, p. 40; Piérart y Rojas, 2013, p. 42) Cama para los organismos degradadores Los materiales que brindan un hábitat para las lombrices se denominan ropa de cama, éstos deben cumplir con características importantes como gran capacidad de absorción y retención de agua, bajo contenido de nitrógeno y proteínas. Tiene como función proteger a las lombrices de temperaturas extremas y regular los niveles de oxígeno y humedad. (Munroe, 2007, p. 5) En los últimos años las investigaciones se han dirigido a probar materiales de bajo costo y que puedan ser empleados como ropa de cama para las lombrices. 16 El aserrín es el principal residuo orgánico en los aserraderos, se considera un material de desecho, sin embargo presenta una alta capacidad de absorción que sumada a su bajo costo y a su abundancia hace que sea factible emplearlo en lechos filtrantes y como ropa de cama para lombrices brindándoles un hábitat relativamente estable. (Fakhrul, Mahbub y Islam, 2013, p. 136; Manaf et al., 2009, p. 82) La fibra de coco es una fibra orgánica natural que se obtiene de la cáscara del coco, posee una gran capacidad de retención de agua y si se incorpora al suelo mejora sus propiedades químicas y físicas al aumentar la capacidad de retención de humedad, la conductividad hidráulica y la porosidad total. Puede ser utilizada como cama para lombrices debido a que es un material completamente renovable, abundante y de bajo costo, además de presentar una estructura altamente estable que brinda un hábitat idóneo para estos organismos degradadores. (Abdullah, Jamaludin, Anwar, Noor y Hussin, 2011, p. 264; Hakeem, Jawaid y Alothman, 2015, pp. 491–493) Medio filtrante Azuar y Ibrahim (2012, p. 1415) y Manyuchi, Kadzungura y Boka (2013, p. 539) reportaron que los agregados de roca de distintos diámetros, el suelo y la arena contribuyen en la filtración del agua residual y proveen un lecho para microorganismos que favorece la disminución del DQO, DBO 5, sólidos disueltos y turbidez. A medida que el agua residual percola por el medio filtrante se forma una capa de biofilm, la cual es directamente proporcional al volumen tratado; ésta junto con los agregados constituye el sistema geológico y microbiológico de filtración. De acuerdo a Toole, Kaplan y Kolter (2010, p. 49) y Watnick y Kolter (2008, p. 2675) el biofilm es una interacción compleja entre microorganismos y una superficie, en el vermifiltro se desarrolla a medida de que el agua residual fluye por el medio filtrante, las moléculas orgánicas proporcionan nutrientes y carbono que aseguran el crecimiento microbiano. La biopelícula es una 17 compleja agrupación microbiana que puede estar formada por una o varias especies de hongos, protozoos, bacterias aerobias, anaerobias, nitrificantes y facultativas. (Almeida, Azevedo, Santos, Keevil y Vieira, 2011, p. 1; Yang et al., 2011, p. 74) 18 CAPÍTULO II: METODOLOGÍA La figura 3 presenta un breve resumen de los puntos a ser tratados en el capítulo. METODOLOGÍA Descripción del experimento Condiciones de operación Caracterización del agua residual y tratada Propiedades físicas de los sustratos Figura 3.Resumen de la metodología. 19 2.1 Descripción del experimento La fase experimental consistió en el montaje de tres vermifiltros a escala laboratorio en un espacio asignado en la parte posterior del bloque 7 de la Universidad de Las Américas sede Queri. Los mismos contenían diferentes estratos con el fin de determinar el mejor tratamiento para las aguas residuales domésticas. La experimentación tuvo dos etapas que se llevaron a cabo en un periodo de 12 semanas. La primera etapa fue de adaptación con una duración de 2 semanas, tiempo necesario para que las lombrices se adecúen a las nuevas condiciones del medio y el sistema se estabilice según lo indicado por Arora y otros (2014, p. 134). La segunda etapa duró 8 semanas y se monitorearon parámetros físicos y químicos de los efluentes tratados. Esta etapa se dividió en dos fases, en la primera se suministró una carga orgánica superficial de 288,47 (g/m2*día) correspondiente a una concentración fuerte de agua residual doméstica (formulación 1) y en la segunda fase se redujo la carga orgánica superficial a 167,5 (g/m2*día) que hace referencia a una concentración media (formulación 2). La formulación del agua residual se resume en el Anexo 1. 2.1.1 Materiales de construcción Los reactores fueron colocados en paralelo con el fin de evaluar cada tratamiento por separado. La alimentación con agua residual se realizó a través de un sistema de distribución conectado a un tanque homogenizador. Por medio de la gravedad el agua residual se condujo a los reactores y no existió recirculación del agua tratada. Los materiales empleados y las medidas del sistema se describen en los Anexos 2 y 3. 20 Figura 4. Esquema del experimento. 2.1.2 Estratificación de los vermifiltros Cada uno de los vermifiltros se conformó con distintos estratos que dieron lugar al medio filtrante y de soporte para las lombrices empleadas. Para la conformación de los estratos se tomó como referencia la distribución planteada por Bharambe, Bapat y Sinha (2009, p. 487), dando lugar a la siguiente composición: 4 estratos distribuidos de abajo hacia arriba de la siguiente manera 31,25% de agregados de 7,5 cm, 31,25% de agregados entre 3,5 a 4,5 cm, 25% de agregados de 10 a 12 mm mezclados con arena y 12,5 % de suelo (este estrato alberga las lombrices). 21 En los 3 vermifiltros se planteó la distribución del tamaño de los agregados siguiendo la composición descrita anteriormente e incorporando nuevas variaciones tanto del tamaño de los agregados como de los sustratos que contienen lombrices. Lombrices La especie empleada para el estudio fue Eisenia foetida, para determinar el número de lombrices que fueron colocadas en cada vermifiltro se siguió la relación de 10 Kg de lombrices por m3 de suelo descrito por Komarowski (2001). (Ecuación 1) ( ) ( ) Dónde: V: volumen (m3) r: radio del cilindro (m2) h: altura del sustrato (m2) ( ) ( ) ( ) (Ecuación 2) 22 Una vez determinado el peso requerido, se procedió a seleccionar lombrices de la especie Eisenia foetida sub-adultas y cliteliadas, se las enjuagó con agua para remover las partículas de tierra y se las pesó empleando una balanza la cual tiene un rango de 0,1 g a 600 g y una precisión de 0,01 g. (ADAM, s.f.) Se llevó a cabo el conteo de los 3 grupos pesados obteniéndose las siguientes cantidades 121, 109 y 111 lombrices. Figura 5. Conteo de las lombrices empleadas en la experimentación. Estratos Para la estratificación de los vermifiltros se utilizaron agregados de grava, arena, suelo, aserrín y fibra de coco. Los agregados de grava y la arena fueron adquiridos en un depósito de materiales de construcción en la ciudad de Quito, el aserrín se obtuvo de una carpintería y la fibra de coco en un comercio de la ciudad. La fibra de coco lavada y tratada se adquirió en bloques compactos de 7,5 Kg por lo que se realizó un proceso de descompactación para obtener el volumen requerido (Anexo 4). 23 Tabla 5. Estratificación de los vermifiltros. No. Vermifiltro Material A Contenido Suelo y 121 lombrices Volumen(l) Altura (cm) 25,132 8 50,264 16 62,83 20 62,83 20 25,132 8 50,264 16 62,83 20 62,83 20 25,132 8 50,264 16 62,83 20 62,83 20 Agregados de grava B 1 D A B C D A B 3 mezclados con arena C 2 de 10 - 12 mm C D Agregados de grava de 3,5 - 4,5 cm Agregados de grava de 7,5 cm Fibra de coco y 111 lombrices Arena Agregados de grava de 10 - 12 mm Agregados de grava de 3,5 - 4,5 cm Aserrín y 109 lombrices Arena Agregados de grava de 10 - 12 mm Agregados de grava de 3,5 - 4,5 cm 24 Figura 6. Estratificación de los vermifiltros. Figura 7. Materiales utilizados en la estratificación de los vermifiltros. 25 2.2 Condiciones de operación El experimento se diseñó de modo que los resultados de cada tratamiento sean comparables. Se prepararon las dos formulaciones de agua residual, ésta se almacenó en un tanque homogenizador y se condujo a los vermifiltros durante 12 semanas de ensayo. 2.2.1 Carga hidráulica Uno de los parámetros que se calculó para el funcionamiento óptimo de los tratamientos fue la carga hidráulica, según lo expresado por RohitPathania y Suresh (2012) la carga hidráulica es el volumen de agua residual aplicado diariamente que un sistema de vermifiltración puede tratar. Para calcular la carga hidráulica se midieron previamente los caudales de entrada en los vermifiltros mediante el método volumétrico que consiste en la medición directa del tiempo que se demora en llenar un recipiente de volumen conocido.(Villavicencio y Villablanca, 2010) Se emplearon probetas y con la ayuda de un cronómetro el caudal medido fue 540 ml/h. ( Dónde: Q: Caudal (m3/día) A: Área (m2) ) (Ecuación 3) 26 2.2.2 Carga orgánica superficial Autores como Singh y Dwivedi (2009, pp. 97–105) mencionan que la carga orgánica superficial es la cantidad de orgánicos que se aplican en el vermifiltro por unidad de área y por día. Este parámetro se consideró importante debido a que representó la fuente de alimento para los organismos degradadores. ( ) (Ecuación 4) Dónde: CH: Carga hidráulica (m3/m2*día) DQO: Demanda química de oxígeno (g/m3) 2.2.3 Tiempo de retención hidráulico Este parámetro es definido por Sinha, Bharambe y Chaudhari (2008, p. 413) como el tiempo en que el agua residual está en contacto con el sistema de vermifiltración, para calcularlo se empleó un trazador y se tomó el tiempo que se demoró en atravesar cada uno de los vermifiltros la primera gota de esta sustancia y de esta manera se estimó el tiempo de residencia del agua residual en el tratamiento. 2.2.4 Porosidad Para medir la porosidad del medio filtrante se aplicó un método gravimétrico referido por M. Gräfe (comunicación personal, 15 de mayo, 2015), se colocaron los agregados en la estufa WiseVen WOF105 a 105 oC durante 24 horas, cumplido este tiempo se retiraron las muestras y se dejaron en el desecador, una vez frías se pesaron en la balanza analítica y se registraron los valores. Las muestras se colocaron en probetas que contenían agua con un volumen 27 conocido, el volumen de agua que se incrementó en cada probeta fue registrado. Las muestras se dejaron allí por un periodo de 7 días para lograr su saturación, posteriormente se las retiró y fueron pesadas nuevamente. ( ) ( ) (Ecuación 5) Dónde: P.M.H: Peso de la muestra húmeda (g) P.M.S: Peso de la muestra seca (g) ( ) (Ecuación 6) Dónde: V1: volumen de agua inicial en probeta (cm3) V2: volumen de agua final en probeta después de colocar la muestra (cm3) ( ) ( ( ) ( ) ) (Ecuación 7) 2.3 Caracterización físico-química del agua residual y tratada Se realizaron análisis físico-químicos de los efluentes de los tres vermifiltros, así como del agua residual para el levantamiento de la línea base. Los parámetros analizados fueron turbidez, pH, conductividad eléctrica, sólidos totales, nitrógeno total, fósforo, DQO y DBO5, los mismos efectuados en el laboratorio de la universidad. que fueron 28 Durante 12 semanas de tratamiento se realizó la toma de muestras efectuándose una réplica diaria de cada reactor para los parámetros físicos y cada 15 días una réplica para los parámetros químicos. 2.3.1 Turbidez Se empleó el equipo Turbidimeter de Hanna Instruments, el cual tiene un rango de 0 a 4000 NTU (Nephelometric Turbidity Unit). Este equipo mide la turbidez mediante el cálculo de luz dispersada y transmitida para lo cual emplea un LED infrarrojo como fuente luminosa de 850 nm, un detector de luz dispersada de 90º y uno de luz transmitida de 180º lo que permite obtener estabilidad y precisión en las mediciones. (HANNA Instruments, s.f.) Para medir este parámetro se llenó una cubeta con 10 ml de muestra, se la colocó en el equipo y se pulsó la tecla “READ”. 2.3.2 pH Para la medición se empleó el equipo Hanna Instruments HI 2550 un multiparámetro de dos canales que utiliza un método de sonda potenciométrica y tiene un rango de medición de -2 a 16. (HANNA Instruments, s.f.) Se sumergieron los electrodos de pH y temperatura dentro de la muestra hasta una profundidad de 3 cm y se esperó que los electrodos se estabilicen y la lectura aparezca en la pantalla. 2.3.3 Conductividad Eléctrica Para medir la conductividad eléctrica se utilizó el equipo Hanna Instruments HI 2550 que tiene una precisión de ±0.05 μs/cm, se sumergió el electrodo en la muestra a analizar cubriendo completamente sus agujeros, posteriormente se esperó que se estabilice la lectura en la pantalla. (HANNA Instruments, s.f.) 29 2.3.4 Sólidos Totales Para la medición, se preparó una cápsula de porcelana lavándola con HNO3 a una concentración de 1 M y secándola en la estufa marca WiseVen WOF105 a 105 oC hasta que alcance un peso constante. Se retiró la cápsula y se la colocó en el desecador y posteriormente fue pesada en la balanza analítica Ohaus Adventurer AR 2140. Se vertió 100 ml de muestra en la cápsula pesada y se la dejó en la estufa a 105 oC hasta que el agua se evapore, se la colocó en el desecador y se registró su peso en la balanza. (Torres, 2006) El cálculo de los ST se lo realizó según la ecuación 8. ( ) ( ) ( ) (Ecuación 8) A: peso de la cápsula de evaporación vacía (g) B: peso de la cápsula de evaporación + residuo seco (g) 2.3.5 Demanda Química de Oxígeno La medición se la llevó a cabo utilizando el test Nanocolor referencia No.029 y el test No.027. Para determinar el DQO se adicionó 2 ml de muestra en el tubo de test, se lo agitó y se lo colocó en el digestor durante 30 minutos a una temperatura de 160 ºC, cumplido el tiempo se retiró el tubo, se lo dejó secar, se lo limpió y se procedió a medir en el fotómetro Macherey-Nagel Nanocolor D500 a una longitud de onda de 620 nm. El principio de análisis fue determinación fotométrica de la concentración de Cromo (III) tras oxidación con ácido sulfúrico, sulfato de plata y dicromato de potasio. (MACHEREY-NAGEL, 2011, p. 2) 30 Figura 8. Diagrama del proceso de medición de la demanda química de oxígeno mediante fotometría. Tomado de: MACHEREY-NAGEL, 2011, pp.33–35. 2.3.6 Demanda Biológica de Oxígeno (DBO5) Este parámetro se lo midió con el equipo Oxitop IS 6, mediante un principio de medición manométrico se determinó el decaimiento de presión en el sistema debido al consumo de oxígeno en la oxidación biológica de la materia orgánica. Los microorganismos consumieron parte del oxígeno contenido y produjeron CO2 el cual reaccionó con el Na (OH) generando diferencia de presiones, las cuales interpretó el equipo. (WTW, 2006, pp. 35–60) Para determinar la DBO5 se colocó dentro de las botellas un agitador, un volumen de muestra de acuerdo al valor de DBO5 esperado según la tabla 6 y cinco gotas de inhibidor de nitrificación. Se colocó el tapón de plástico al interior con dos perlas de hidróxido de sodio, el cabezal de la botella y se enceró. El registro se lo realizó a diario y se lo multiplicó por el factor correspondiente de conversión. 31 Tabla 6. Factores de conversión en base al DBO₅ esperado. Volumen de muestra(ml) Factor Rango esperado (mg O2/l) 22.7 100 0-4000 43.5 50 0-2000 97 20 0-800 164 10 0-400 250 5 0-200 365 2 0-80 432 1 0-40 Tomado de: WTW, 2006, p. 24. 2.3.7 Nitrógeno Total Este parámetro se lo analizó con el Test 0-88 Nanocolor. Para la medición se preparó un tubo A con 500 µl de muestra y una cucharada de reactivo de descomposición NANOx N y se colocó el tubo en el digestor a 120 ºC por 30 minutos. Cumplido el tiempo se retiró el tubo de test y se dejó enfriar a temperatura ambiente, posteriormente se colocó una cucharada de reactivo de compensación NanOx N, se cerró y se agitó. En la segunda parte del procedimiento se abrió un tubo de test de nitrógeno total y se añadió 0.5 ml de la muestra resultante del tubo A y 0.5 ml de R2, se mezcló, se limpió el tubo y se procedió a medir en el fotómetro NANOCOLOR ® 500D. 32 Figura 9. Diagrama del proceso de medición de nitrógeno total mediante fotometría. Tomado de: MACHEREY-NAGEL, 2011, p. 92. 2.3.8 Fósforo Total Para la medición del fósforo se utilizó el test 76. El procedimiento fue el siguiente: se vertió 4 ml de muestra en el tubo de reacción y se le agregó una pastilla de Nanofix R2, posteriormente se lo calentó en el digestor a una temperatura de 120 oC por 30 minutos. Cumplido el tiempo se retiró el tubo del digestor, se lo dejó enfriar y se añadió 1 ml de R3, se agitó el tubo, se lo limpió y se esperó diez minutos para medir en el fotómetro NANOCOLOR ® 500D. 33 Figura 10. Diagrama del proceso de medición de fósforo mediante fotometría. Tomado de: MACHEREY-NAGEL, 2011, pp. 78-79. 2.4 Medición de las propiedades físicas de los sustratos 2.4.1 Temperatura Durante las semanas de experimentación se monitoreó la temperatura en la ropa de cama de los 3 vermifiltros utilizando el termómetro trazable de Control Company el cual tiene un rango de medición de –50 a 300°C. (Control Company, s.f.) Para la medición se retiró el termómetro de la carcasa protectora, se lo encendió y se seleccionó la escala de temperatura (°C), se introdujo el termómetro dentro de cada uno de los reactores y se esperó a que se estabilice la lectura. 2.4.2 pH Se realizó la medición de pH en campo directamente empleando el pHmetro de HANNA INSTRUMENTS HI 99121. Se introdujo el electrodo en la capa uno empujándolo ligeramente para lograr un contacto adecuado, se esperó que el resultado se estabilice en la pantalla y se registró el valor. 34 2.4.3 Textura Para determinar la textura del suelo del vermifiltro 1 se empleó el método de Bouyoucos que consiste en determinar los % de limo, arcilla y arena que se encuentran presentes en la fracción mineral del suelo (González, Coronado y Acosta, 2007, p. 23), esta medición se realizó en el laboratorio de la Agencia Ecuatoriana de Aseguramiento de la Calidad del Agro (AGROCALIDAD). 2.5 Análisis estadístico El diseño empleado para la experimentación fue el completamente aleatorio (DCA) que de acuerdo a lo mencionado por Gutiérrez y De la Vara (2013, p. 52) se emplea para comparar 2 o más tratamientos, debido a que solo se considera 2 fuentes de variabilidad: el error aleatorio y los tratamientos. A través de este diseño se evaluó la variable de interés (remoción de contaminantes en cada tratamiento). Se emplearon figuras, tablas, diagramas, ecuaciones y por medio de programas estadísticos como Microsoft Excel y SPSS® 23 se establecieron comparaciones entre los tratamientos planteados. 35 CAPÍTULO III: RESULTADOS Y ANÁLISIS La figura 11 presenta un breve resumen de los puntos a ser tratados en el capítulo. Agua residual Caracterización del agua RESULTADOS Y ANÁLISIS Agua tratada Condiciones de funcionamiento Parámetro turbidez Parámetro pH Parámetro conductividad eléctrica Parámetro sólidos totales Análisis estadístico Parámetro DBO5 Parámetro DQO Parámetro nitrógeno total Parámetro fósforo total Figura 11. Resumen de los resultados y análisis. 36 3.1 Caracterización del agua 3.1.1 Agua residual El apartado de este capítulo explica los resultados obtenidos de la caracterización tanto del agua residual empleada para el estudio como de los efluentes tratados en los vermifiltros durante el período de experimentación. La caracterización físico-química se realizó en función de los siguientes parámetros: turbidez (NTU), conductividad eléctrica (µS/cm), pH, sólidos totales (mg/l), nitrógeno total (mg/l), fósforo total (mg/l), DQO (mg/l) y DBO5 (mg/l). La caracterización del agua residual utilizada se muestra en la tabla 7. Tabla 7. Caracterización del agua residual empleada en la experimentación. Parámetros Concentración 1 Concentración 2 Turbidez (NTU) 84,4 59,4 pH 7,3 7,1 Conductividad eléctrica 325,18 220,7 Sólidos totales (mg/l) 624 473 Nitrógeno total (mg/l) 47 31 Fósforo total (mg/l) 7,61 5,2 DQO (mg/l) 699 406 DBO5 (mg/l) 380 125 (µS/cm) Sandoval y Cisneros (2012) mencionan que la concentración del ARD obedece primordialmente al consumo de agua y a la cantidad de residuos producidos a diario por cada habitante. Al realizar una comparación entre la tabla 1 con los resultados obtenidos en la tabla 7 se observa que las concentraciones utilizadas en el estudio se asemejan a una concentración fuerte y media de agua residual doméstica. 37 Los valores de DQO de la tabla 1 señalan que, 800 mg/l corresponden a una concentración fuerte de ARD y 430 mg/l a una concentración media. El valor obtenido en la caracterización 1 fue de 699 mg/l de DQO, por tanto se encuentra entre la carga fuerte y media siendo más próximo a la primera; en cuanto al valor de 406 mg/l de DQO, este es muy cercano a la concentración media. Los resultados obtenidos de DBO5 fueron 380 mg/l y 125 mg/l, la tabla 1 indica que para una concentración fuerte el valor de DBO 5 se encuentra alrededor de 350 mg/l y para la media alrededor 190 mg/l, por lo cual los valores están próximos a los indicados en la bibliografía. Para los nutrientes nitrógeno y fósforo los valores resultantes de la caracterización inicial fueron: 47 mg/l, 31 mg/l de nitrógeno total y 7,61 mg/l, 5,2 mg/l de fósforo total. Los valores señalados en la tabla 1 para una concentración alta son: 70 mg/l de nitrógeno total y 12 mg/l de fósforo total y para la media: 40 mg/l y 7 mg/l de nitrógeno total y fósforo total respectivamente. Por ende el contenido de nitrógeno de la concentración uno (47 mg/l) pertenece a una concentración media-fuerte y el valor de 31 mg/l a una media-débil, en el caso del fósforo presente en el agua residual la concentración uno se acerca a la concentración media y el valor de 5,2 mg/l a una media-débil. En cuanto a los sólidos totales, los valores obtenidos según la tabla 7 fueron: 624 mg/l y 473 mg/l, los mismos de acuerdo a la tabla 1 son cercanos a una concentración media (720 mg/l) y a una concentración débil (390 mg/l) de agua residual doméstica. En lo que se refiere a los parámetros pH y turbidez no existe un rango definido para cada concentración, no obstante el agua residual doméstica tiene un pH que oscila entre 6-8 y una turbidez entre 34 y 372 NTU, por tal motivo los resultados obtenidos de pH: 7,3 y 7,1; y de turbidez 84,4 y 59,4 se enmarcan en los valores de un ARD típica. 38 Si se relacionan los resultados obtenidos y el consumo de agua diario necesario, se tiene que para una concentración fuerte este debe estar alrededor de 240 litros/persona*día, mientras que para una concentración media este valor se acerca a los 460 litros/persona* día. (Metcalf y Eddy, 2004, p.186) En países desarrollados donde el consumo de agua puede llegar a 400 litros al día el agua residual es diluida, mientras que en países en desarrollo en los cuales el consumo alcanza 135 litros ésta es más concentrada (Knobelsdorf, 2009), por ejemplo: en el área urbana de Quito se consume alrededor de 200 litros/persona*día, en tanto este volumen se reduce a 120 litros/persona*día en las zonas rurales. (Jácome, 2014) Las concentraciones 1 y 2 utilizadas durante la fase experimental se pueden relacionar directamente con factores inherentes a la población que se abastece del líquido vital, es así que el agua residual tendrá una carga media en poblaciones que tienen mayor acceso a este recurso y será más concentrada en comunidades que tienen un acceso más limitado. 3.1.2 Efluente A continuación se presenta un promedio de los parámetros físico – químicos medidos en los efluentes de los 3 vermifiltros; dichos resultados serán analizados a través de un análisis estadístico en el apartado 3.3. 39 Tabla 8.Caracterización físico-química de los efluentes. Reactor Parámetro Etapa 1 Etapa 2 Turbidez (NTU) 20,85 8,42 pH 7,13 7,05 204,22 224,81 Sólidos totales (mg/l) 342,16 217,72 Nitrógeno total (mg/l) 15,5 13 Fósforo total (mg/l) 4,27 3,3 DQO (mg/l) 82,5 33,5 DBO5 (mg/l) 38,5 19 Turbidez (NTU) 5,65 0,89 pH 7,21 6,72 189,15 193,26 Sólidos totales (mg/l) 202,34 201,85 Nitrógeno total (mg/l) 14,5 9 Fósforo total (mg/l) 4,09 1,61 DQO (mg/l) 52 20 DBO5 (mg/l) 24 4,00 Turbidez (NTU) 10,35 3,44 pH 7,17 7,20 211,82 221,25 Sólidos totales (mg/l) 271,95 225,35 Nitrógeno total (mg/l) 24 13,5 Fósforo total (mg/l) 4,27 2,95 DQO (mg/l) 69,5 39 DBO5 (mg/l) 35,5 25,5 Conductividad eléctrica (µS/cm) Vermifiltro 1 Conductividad eléctrica (µS/cm) Vermifiltro 2 Conductividad eléctrica (µS/cm) Vermifiltro 3 40 3.2 Condiciones de funcionamiento 3.2.1 Funcionamiento En la siguiente sección se presentan los resultados de las condiciones de trabajo de cada vermifiltro y se evalúa si las mismas fueron las adecuadas para el óptimo funcionamiento de los sistemas. Tabla 9. Condiciones de funcionamiento de los vermifiltros. Vermifiltro 1 Vermifiltro 2 Vermifiltro 3 Carga hidráulica (m3/m2*día) 0,4127 0,4127 0,4127 Carga orgánica superficial 288,47 288,47 288,47 (g/m2*día) 167,5 167,5 167,5 Tiempo de retención (h) 0,76 1,08 0,9 25 25 Porosidad (%) Capa 2 25 7,56 Capa3 8,41 7,56 7,56 Capa 4 8,12 8,41 8,41 Como se muestra en la tabla 9, los vermifiltros fueron sometidos a la misma carga hidráulica y orgánica superficial. La carga hidráulica se estipuló considerando el estudio experimental de Cardoso y otros (2011, p. 35) que señala que una carga hidráulica de 0,48 m3/m2*día es satisfactoria en este tipo de biofiltros. Se probaron varias cargas y se determinó que con una carga de 0,4127 m3/m2*día, los sustratos permanecían húmedos y se tenía un buen tiempo de retención para el tratamiento del agua residual, esto debido a que cargas hidráulicas altas reducen el tiempo de retención y por ende la eficiencia en el tratamiento. En tanto, las cargas orgánicas superficiales se obtuvieron 41 como resultado de los valores de DQO de las dos formulaciones de agua residual utilizada en la experimentación. El tiempo de retención fue de 0,76 h, 1,08 h y 0,9 h para el primero, segundo y tercer vermifiltro respectivamente; a pesar de que las diferencias no son tan representativas, éstas se pueden atribuir al tipo de material que se usó en la capa 1 y a la porosidad de los diferentes agregados que forman parte del filtro que pueden aumentar o disminuir la velocidad con la que fluye el agua residual modificando el tiempo de retención en cada biofiltro. Spalletti (2007) y Vera (2011) manifiestan que la porosidad en una roca condiciona su comportamiento frente a la circulación de agua, a menor porosidad menor permeabilidad, es decir se reduce la capacidad de transmitir un fluido. De acuerdo a la carga contaminante presente en el agua residual los tiempos de retención de los tres vermifiltros son aceptables, Baumgartner (2013, p. 15) refiere que para cargas de DBO5 comprendidas entre 200 mg/l y 400 mg/l se requiere de 30 a 40 minutos de tratamiento para alcanzar reducciones significativas y para lograr una mayor eficiencia en la reducción de patógenos del agua residual doméstica es aconsejable un tiempo de retención de 1 a 2 horas. Propiedades físicas Tabla 10. Propiedades de los materiales empleados en la capa uno. Capa 1 Vermifiltro 1 Vermifiltro 2 Vermifiltro 3 Material suelo fibra de coco aserrín pH 7,27 6,41 6,19 Textura Franco N/A N/A arenoso Las lombrices de tierra son sensibles al pH, este factor influye en su crecimiento. (Velásquez, 2008, p. 59) La tabla 10 indica que el pH de los 42 materiales fue el siguiente: 7,27 (suelo), 6,41(coco) y 6,19 (aserrín) estos valores se encuentran dentro del rango que la especie Eisenia foetida requiere para su normal desarrollo, que según Vincent (2012, pp. 114–116) varía entre 5 y 8,4. Por tanto los tres materiales usados ofrecen un pH adecuado para la especie empleada en el estudio. La ropa de cama debe proporcionar un ambiente cercano al contenido de humedad que requieren las lombrices de tierra, ésta debe estar húmeda pero no totalmente saturada pues provoca la asfixia de las lombrices. (Visvanathan, Traenklar, Kurian y Nagendran, 2009, p. 24) Durante las seis primeras semanas de experimentación (incluidas dos semanas de aclimatación) no se observó obstrucción en los vermifiltros, sin embargo a mediados de la séptima semana se hizo evidente la obstrucción del vermifiltro tres llegando a saturarse a inicios de la octava semana, las lombrices contenidas se asfixiaron pues el agua no pudo percolar a los estratos siguientes acumulándose en la parte superior del vermifiltro. Por tal motivo, se retiró el material saturado y se colocó nuevo aserrín y biomasa de lombrices para evaluar su factibilidad en el tratamiento de la segunda concentración de agua residual, la biomasa de lombrices colocada se sometió nuevamente a un periodo de aclimatación por lo que en este biofiltro la experimentación se extendió dos semanas más. Adugna, Andrianisa, Konate, Ndiaye y Maiga (2015, p. 7) reportan la saturación de vermifiltros con aserrín debido a la acumulación de sólidos y taponamiento de los poros, el motivo de la saturación en el vermifiltro 3 pudo deberse a que no soportó el caudal y la carga contaminante empleada en la etapa 1 de experimentación. 43 Suelo Fibra de coco con presencia de biofilm Obstrucción en el vermifiltro con aserrín Figura 12. Estado de la capa 1 en los vermifiltros. Saturación del aserrín 44 Temperatura en la capa uno Los resultados del monitoreo de temperatura realizados durante la fase experimental se muestran en la tabla siguiente. Tabla 11. Resultados de las mediciones de temperatura realizadas. Capa uno Temperatura Temperatura Temperatura promedio (oC) máxima (oC) mínima (oC) Suelo 20,44 27,3 13,7 Fibra de coco 22,54 31,4 14 Aserrín 21,60 30,4 13,6 Se midió la temperatura en la capa uno diariamente debido a sus efectos sobre la actividad metabólica, reproductiva y motora de las lombrices. En el vermifiltro 1 cuya primera capa estaba conformada por suelo la temperatura promedio registrada fue de 20,44 oC, mientras que la máxima fue de 27,3 oC y la mínima de 13,7 oC. En el segundo vermifiltro que contenía fibra de coco la temperatura máxima medida fue 31,4 oC, la mínima 14 oC y la media 22,54 oC. El aserrín perteneciente al vermifiltro tres registró una temperatura promedio de 21,6 oC, una máxima de 30,4 oC y una mínima de 13,6 oC. Campesinos y otros (2005, p. 42) manifiestan que la especie Eisenia foetida empleada en la experimentación tiene un límite inferior de temperatura letal de 0 oC y un límite superior letal de 34 oC, con una temperatura óptima de desarrollo de entre 15,7 y 28,2 oC. De acuerdo a lo antes señalado, en los tres materiales se registró una temperatura promedio que se encuentra dentro del rango óptimo por lo que las condiciones climáticas que se registran en el lugar de experimentación brindan un buen ambiente para el normal desarrollo de las lombrices de tierra. Las temperaturas mínimas registradas 13,7oC (suelo), 14oC (fibra de coco) y 13,6 oC (aserrín) a pesar de que se encuentran bajo el rango de condiciones ideales se alejan del límite inferior letal. Arora y Kazmi (2015, p. 97) señalan que temperaturas similares a las registradas en el sitio de 45 desarrollo del estudio permiten alcanzar mayores eficiencias de remoción de contaminantes con vermifiltros. Condiciones de las lombrices Lombrices de la especie Eisenia foetida fueron colocadas al inicio del experimento sobre la capa uno de cada vermifiltro para evaluar si éstas son capaces de reproducirse en este medio. La determinación de la biomasa de lombrices es importante para evaluar la viabilidad del sistema y su rendimiento a largo plazo, la medición de este parámetro se realizó registrando el peso inicial y final de las lombrices en los tres vermifiltros. En la tabla 12 se encuentran los resultados, cabe destacar que al inicio del experimento se colocó la misma cantidad de biomasa en los 3 vermifiltros (25,12 g), pero que debido a la saturación en el filtro 3 nuevas lombrices fueron colocadas a inicios de la octava semana de experimentación. Tabla 12. Incremento de la biomasa de lombrices. Biomasa de lombrices Peso inicial de Peso final de Incremento de lombrices (g) lombrices (g) la biomasa (%) Vermifiltro 1 25,12 36,9 46,89 Vermifiltro 2 25,12 70,4 180,25 25,12 N/A ----- 25,12 34,3 36,54 Filtro Vermifiltro 3 Incremento de la biomasa (%) 46 200 180 160 140 120 100 80 60 40 20 0 Vermifiltro 1 Vermifiltro 2 Vermifiltro 3 Figura 13. Incremento de la biomasa de lombrices en los vermifiltros. En cuanto se refiere a la tasa de incremento de la biomasa de lombrices (Figura 13), el tratamiento 1 muestra un incremento del 46,89% de biomasa en relación al peso inicial, mientras que el tratamiento 2 refleja un aumento del 180,25%, en el tratamiento 3 la biomasa final no pudo ser medida debido a la colmatación del filtro, sin embargo la biomasa de lombrices colocada a inicios de la octava semana de experimentación registró un incremento del 36,54%. Como se puede observar, el tratamiento 2 exhibe el mejor desempeño con una tasa de crecimiento mayor a la del tratamiento uno que tiene las mismas condiciones iniciales y periodo de duración lo que demuestra que la fibra de coco ofrece mejores condiciones para la reproducción de las lombrices de esta especie, esto puede deberse a que la humedad es la recomendada para su desarrollo óptimo. 47 3.3 Análisis estadístico El análisis estadístico se lo realizó mediante un ANOVA usando el software SPSS® 23, a través de este análisis de varianza fue posible comparar los resultados obtenidos en los tratamientos y contrastar la hipótesis nula con la hipótesis alternativa. La hipótesis nula señala que las medias de K poblaciones son iguales, mientras la hipótesis alternativa indica que al menos una de esas K poblaciones es diferente en cuanto al valor que se espera. Adicionalmente se realizaron comparaciones de rangos múltiples mediante los métodos de DMS y TUKEY que permitieron contrastar las medias de cada tratamiento bajo la hipótesis general que se presenta a continuación: Prueba general Pruebas entre tratamientos Ho: µ1 = µ2 / HA: µ1 ≠ µ2 Ho: µ1 = µ3 / HA: µ1 ≠ µ3 Ho: µ2 = µ3 / HA: µ2 ≠ µ3 El método de Tukey conocido como prueba honesta de significación realiza las comparaciones entre las medias empleando una distribución del rango estandarizado, el mismo se encuentra definido según la siguiente ecuación. ( )√ (Ecuación 9) 48 Dónde: = Modelo de prueba estadístico Tukey = punto porcentual de la distribución del rango de T-student con grados de libertad del error del análisis de varianza N-K = grados de libertad del error del análisis de varianza CME = cuadrado medio del error n = número de muestras de cada tratamiento El método DMS (Diferencia mínima significativa) realiza una prueba de hipótesis por parejas basándose en la distribución t de student, este método se encuentra definido por la ecuación siguiente: |̅ ̅| √ (Ecuación 10) Dónde: ̅ = media muestral del i-ésimo valor ̅ = media muestral del j-ésimo valor = valor de la prueba T de student con N-k grados de libertad N-K = grados de libertad del error del análisis de varianza CME = cuadrado medio del error n = número de muestras de cada tratamiento 49 3.3.1 Parámetro Turbidez Para el parámetro turbidez se realizó una prueba de análisis de varianza ANOVA para cada fase de tratamiento con la finalidad de determinar si la hipótesis nula es aceptada o rechazada y se aplicó los métodos de Tukey y DMS para identificar los tratamientos que generan la significancia. Ho = µ1 = µ2 = µ3 HA = µi ≠ 0 para algún i = 1, 2,3 Tabla 13. ANOVA para el parámetro turbidez Etapa 1. Fuente de Suma de variación cuadrados Entre grupos Dentro de grupos Total Grados de libertad Media cuadrática 2420,881 2 1210,440 7941,377 57 139,322 10362,258 59 Valor F Sig crítico para F 8,688 ,001 3,16 Para determinar la significación estadística se debe comparar el valor crítico de F frente al valor calculado de F, si este último es menor se concluye que no existen diferencias significativas entre los tratamientos, en tanto se debe tomar en cuenta el nivel de significación escogido (0,05) para decidir si la diferencia entre los tratamientos es muy grande, si el valor obtenido es menor a 0,05 se concluye que existen diferencias significativas y se rechaza la hipótesis nula. (Díaz, 2009, pp. 52-53; Gallego, 2003, p. 76; Tomás-Sábado, 2010) El análisis de varianza sobre este experimento ha permitido advertir diferencias significativas entre los tratamientos probados. En la tabla 13, se evidencia que el valor calculado de F (8,68) es mayor al valor crítico de F (3,16) y que el nivel de significación es menor a 0,05 lo cual indica que se debe aceptar la hipótesis 50 alternativa de que al menos uno de los tratamientos es diferente en referencia al parámetro turbidez. Tabla 14. Comparaciones múltiples para el parámetro turbidez Etapa 1. Prueba (I) (J) Tratamiento Tratamiento 1 Tukey 2 3 1 DMS 2 3 Diferencia de medias (I-J) Error estándar Sig. 2 15,1945* 3,73259 ,000 3 10,4975* 3,73259 ,018 1 -15,1945* 3,73259 ,000 3 -4,6970 3,73259 ,424 1 -10,4975* 3,73259 ,018 2 4,6970 3,73259 ,424 2 15,1945* 3,73259 ,000 3 10,4975* 3,73259 ,007 1 -15,1945* 3,73259 ,000 3 -4,6970 3,73259 ,213 1 -10,4975* 3,73259 ,007 2 4,6970 3,73259 ,213 Las pruebas de Tukey y DMS presentadas en la tabla 14 muestran que no existe diferencia entre el tratamiento 2 y 3 en cuanto al parámetro turbidez pues los niveles de significación obtenidos son mayores a 0.05, sin embargo las diferencias son observables entre el tratamiento 1 con respecto a los tratamientos 2 y 3, al comparar los datos del nivel de significación se advierte que la diferencia entre el tratamiento 1 y 2 es mayor que la del tratamiento 1 y 3. 51 Tabla 15 . ANOVA para el parámetro turbidez Etapa 2. Fuente de Suma de Grados de Media variación cuadrados libertad cuadrática 586,450 2 293,225 grupos 935,357 57 16,410 Total 1521,806 59 Entre grupos Valor F Sig crítico para F 17,869 0,000 3,16 Dentro de De acuerdo con los resultados del análisis de la varianza presentados en la tabla 15, se determinó que existen diferencias altamente significativas entre los tratamientos pues el valor calculado de F es mayor que el valor crítico de F y el nivel de significancia es de 0,000 motivo por el cual la hipótesis nula es rechazada y se acepta que al menos uno de los tratamientos difiere en cuanto al parámetro turbidez estudiado. 52 Tabla 16. Comparaciones múltiples para el parámetro turbidez Etapa 2. Prueba Diferencia Error de medias estánda (I-J) r 2 7,5300* 1,2810 ,000 3 4,9725* 1,2810 ,001 1 -7,5300* 1,2810 ,000 3 -2,5575 1,2810 ,122 1 -4,9725* 1,2810 ,001 2 2,5575 1,2810 ,122 2 7,5300* 1,2810 ,000 3 4,9725* 1,2810 ,000 1 -7,5300* 1,2810 ,000 3 -2,5575 1,2810 ,051 1 -4,9725* 1,2810 ,000 2 2,5575 1,2810 ,051 (I) (J) Tratamiento Tratamiento 1 Tukey 2 3 1 DMS 2 3 Sig. Las pruebas de comparaciones múltiples de Tukey y DMS expuestas en la tabla 16, indican que existe diferencias entre el tratamiento 1 con respecto a los tratamientos 2 y 3, en tanto no se advierte diferencias entre el tratamiento 2 y 3 con respecto al parámetro turbidez pues los niveles de significancia calculados son mayores a 0,05. En las figuras 14 y 15 se ilustra el comportamiento de la turbidez a lo largo del experimento. 53 Figura 14. Resultados de turbidez en los efluentes en función del tiempo (Etapa 1). 54 Figura 15. Resultados de turbidez en los efluentes en función del tiempo (Etapa 2). En las figuras 14 y 15, se evidencia que los 3 tratamientos son eficaces en la reducción de la turbidez pues este parámetro decrece a lo largo del tiempo. La figura 14, muestra que en el vermifiltro 1 la turbidez decrece hasta alcanzar un comportamiento constante llegando a 2,41 NTU; mientras que, el vermifiltro 2 presentó siempre un tratamiento efectivo de la turbidez pues los valores son bajos empezando en 24, 2 NTU y llegando a valores menores a 3 NTU desde la tercera semana de observación. En el vermifiltro 3 también se hace evidente la disminución progresiva de este parámetro. 55 En la figura 15, es apreciable que los valores de turbidez son bajos, al trabajarse en esta etapa con una turbidez inicial menor (59,4 NTU), la turbidez de los efluentes tratados también lo fue. En esta etapa los vermifiltros presentaron una tasa de remoción relativamente constante con pequeñas variaciones, valores inferiores a 15 NTU para el tratamiento 1, menores a 2,8 NTU para el tratamiento 2 y menores a 11 NTU para el tratamiento 3 fueron medidos. La reducción de la turbidez después del tratamiento en los vermifiltros puede atribuirse a la acción degradadora de las lombrices de tierra y de los microorganismos presentes en las diferentes capas, así como al sistema geológico que permitió la adsorción de las partículas suspendidas en el agua residual, corroborando lo mencionado por Li, Xiao, Qiu, Dai y Robin (2009, p. 3009 y Manyuchi y otros (2013, p. 549). El porcentaje de remoción de turbidez en cada vermifiltro se determinó aplicando la ecuación 11, en la cual se hace una relación entre las concentraciones iniciales y finales del agua residual. (Ecuación 11) Dónde: C afluente: concentración del afluente C efluente: concentración del efluente 56 % remoción de turbidez 110,00 100,00 90,00 80,00 70,00 Vermifiltro 1 60,00 Vermifiltro 2 50,00 Vermifiltro 3 40,00 30,00 20,00 1 3 5 7 9 11 13 15 17 19 Tiempo (días) Figura 16. Porcentaje de remoción de turbidez en la etapa 1. La turbidez es un parámetro que proporciona una idea del grado de contaminación del agua, pues hace referencia a la presencia tanto microscópica como macroscópica de solidos en suspensión, como se observa en la figura 16 el vermifiltro 2 presentó desde un principio porcentajes altos de remoción estabilizandose antes que los otros vermifiltros estudiados. Con una turbidez en el afluente de 84,4 NTU el vermifiltro 1 mostró al inicio la eficiencia más baja entre los tratamientos, pero se observó una tendencia creciente de remoción, mientras que el vermifiltro 3 mostró fluctuaciones en las mediciones estabilizandose a partir de la medición 16. Como lo afirman Kumar y otros (2015, p. 6) la turbidez puede verse afectada por el tipo de material que se utilice como ropa de cama, pues se puede presentar un arrastre de particulas que dan como resultado un aumento en la turbidez. La diferencia de turbidez en los efluentes tratados se puede visualizar en la figura 17 donde se nota claramente que el tratamiento 2 tiene mejores resultados en cuanto a la remoción de este parámetro. 57 Figura 17. Apariencia del agua residual antes y después del tratamiento Etapa 1. a.Explicación: de izquierda a derecha se presenta el agua residual antes del tratatamiento, el efluente del vermifiltro 1, el efluente del vermifiltro 2 y el efluente del vermifiltro 3. % de remoción de turbidez 110,0 100,0 90,0 80,0 Vermifiltro 1 70,0 Vermifiltro 2 60,0 Vermifiltro 3 50,0 40,0 1 3 5 7 9 11 13 15 17 19 Tiempo (días) Figura. 18 Porcentaje de remoción de turbidez en la etapa 2. 58 En la figura 18, que corresponde al porcentaje de remoción de turbidez en la etapa dos, se observa claramente que el tratamiento 2 presenta una tendencia lineal de remoción de turbidez y que ésta se mantiene constante por encima del 96% de remoción, en tanto en el tratamiento 1 la remoción alcanza 88% en un inicio descendiendo alrededor de 55 % para luego adoptar un comportamiento creciente de remoción, el tratamiento 3 muestra remociones por encima de 90% a lo largo de la etapa, sin embargo en la observación siete y ocho se evidencia un descenso de remoción que se debe al cambio de material en la capa uno de este biofiltro y al nuevo periodo de aclimatación al que fue sometido. Figura. 19 Apariencia del agua residual antes y después del tratamiento Etapa 2. a.Explicación: de izquierda a derecha se presenta el agua residual antes del tratatamiento, el efluente del vermifiltro 1, el efluente del vermifiltro 2 y el efluente del vermifiltro 3. 59 En la primera fase de experimentación la remoción de turbidez lograda fue 97,14%, 97,16% y 96,80% en los tratamientos 1, 2 y 3 respectivamente y, 93,27%, 98,32% y 91,58% en la segunda fase experimental. En base a estos resultados se puede discutir que la remoción alcanzada por los vermifiltros se encuentra dentro del rango establecido por estudios similares como los realizados por Keshav y Garkal (2014, p. 73); Lakshmi y otros (2014, p. 587) y Sinha y otros (2008, p. 415) que reportan eficiencias cercanas a 96%. 3.3.2 Parámetro pH Para comprobar si entre los efluentes tratados por los vermifiltros existe alguna diferencia estadística en cuanto al parámetro pH se aplicó una prueba del análisis de varianza ANOVA para determinar si la hipótesis nula debe ser rechazada o aceptada. Ho = µ1 = µ2 = µ3 HA = µi ≠ 0 para algún i = 1, 2,3 Tabla 17. ANOVA para el parámetro pH Etapa 1. Fuente de Suma de variación cuadrados Grados de libertad Media cuadrática Entre ,070 2 ,035 grupos 5,318 57 ,093 Total 5,388 59 grupos Valor F Sig crítico para F ,375 ,689 3,16 Dentro de Según el análisis de varianza exhibido en la tabla 17, se evidencia que no existen diferencias significativas entre los tratamientos en la etapa 1 pues, el 60 valor calculado de F es menor al valor crítico de F y el nivel de significancia es mayor a 0,05 razón por la cual se acepta la hipótesis nula de que los tratamientos son iguales en cuanto al parámetro pH. Tabla 18. ANOVA para el parámetro pH Etapa 2 Fuente de Suma de variación cuadrados Grados de libertad Media cuadrática Entre 2,435 2 1,218 grupos 4,292 57 ,075 Total 6,728 59 grupos Valor F Sig crítico para F 16,171 0,000 3,16 Dentro de Los resultados presentados del análisis de varianza en la tabla 18, muestran que existen diferencias significativas entre los tratamientos pues el nivel de significancia es menor a 0,05 y el valor calculado de F es mayor al valor crítico de F; por tal motivo la hipótesis nula se rechaza y se acepta que al menos uno de los tratamientos es diferente en cuanto al parámetro pH estudiado en la etapa 2. 61 Tabla 19. Comparaciones múltiples para el parámetro pH Etapa 2. Prueba (I) (J) Tratamiento Tratamiento 1 HSD Tukey 2 3 1 DMS 2 3 Diferencia de medias (I-J) Error estándar Sig. 2 ,33100* ,08678 ,001 3 -,15150 ,08678 ,197 1 -,33100* ,08678 ,001 3 -,48250* ,08678 ,000 1 ,15150 ,08678 ,197 2 ,48250* ,08678 ,000 2 ,33100* ,08678 ,000 3 -,15150 ,08678 ,086 1 -,33100* ,08678 ,000 3 -,48250* ,08678 ,000 1 ,15150 ,08678 ,086 2 ,48250* ,08678 ,000 La prueba de comparación múltiple que se muestra en la tabla 19, indica que entre el tratamiento 2 y los tratamientos 1 y 3 existen diferencias pues los valores del nivel de significación se encuentran por debajo de 0,05; además es observable que no existe diferencia significativa entre los tratamientos 1 y 3 con relación al parámetro evaluado. Los valores de pH medidos durante la fase experimental se presentan en las siguientes figuras. 62 Figura 20. Resultados de pH en los efluentes en función del tiempo (Etapa 1). 63 Figura 21. Resultados de pH en los efluentes en función del tiempo (Etapa 2). 8 pH 7,5 Vermifiltro 1 7 Vermifiltro 2 Vermifiltro 3 6,5 6 1 3 5 7 9 11 13 15 17 19 21 23 25 27 29 31 33 35 37 39 Tiempo (días) Figura 22. Tendencia del parámetro pH en los vermifiltros en función del tiempo. 64 Como se ilustra en las figuras 20, 21 y 22, el pH del efluente del vermifiltro 1 se incrementó inicialmente durante el tratamiento mostrando leves disminuciones en las mediciones, posteriormente el pH disminuyó ligeramente estabilizándose en un pH cercano a 7 al final de la experimentación. El pH en el vermifiltro 2, en un inicio mostró un comportamiento alcalino y subsiguientemente decreció exhibiendo los valores más bajos de pH en los tres tratamientos alcanzando valores de 6,1; durante los días finales del experimento se observó una tendencia de incremento gradual del pH hasta alcanzar un valor de 7,1. En el vermifiltro 3 una tendencia de ligero incremento de pH se observó durante los primeros días, posteriormente los valores decrecieron, sin embargo cuando eran observables valores bajos de pH en las mediciones el biofiltro se saturó y el material de cama fue renovado, a partir de entonces se observó un aumento en el pH del efluente tratado. Los valores obtenidos de potencial de hidrógeno en los efluentes de los tres vermifiltros experimentales se encuentran dentro de los límites de descarga a un cuerpo de agua dulce (5-9) y del rango establecido para aguas de uso agrícola (6-9) por lo que se cumple con la normativa vigente contenida en el Anexo 1 del libro VI del TULSMA. Arora y otros (2014, p. 123); Hughes, Nair, y Ho (2008, p. 1219); Tomar y Suthar (2011, p. 99) y Wang, Guo, Zheng, Luo, y Zhang (2011, p. 9467) notaron la misma tendencia observada en el experimento en relación al parámetro pH, es decir se observó que en los vermifiltros el pH en un inicio mostró una tendencia creciente durante los primeros días de experimentación, posteriormente éste decreció llegando a valores ligeramente ácidos, para luego ascender y estabilizarse cerca del pH neutro. El incremento de pH en los efluentes en la primera etapa del experimento se puede comprobar debido a que en el análisis de ANOVA no existen diferencias significativas entre los vermifiltros con respecto al pH. Arora y Kazmi (2015, p. 92) atribuyen el incremento de pH en un efluente tratado con vermifiltros a la degradación de materia orgánica y a la intensa actividad microbiana que se produce durante los primeros días de tratamiento, mientras que la disminución 65 en el pH se debe a que dentro del vermifiltro se producen procesos de nitrificación por lo que se puede asumir que en el vermifiltro 2 que presenta valores más bajos de pH el proceso de nitrificación fue más intenso que en los demás vermifiltros, lo cual puede deberse a que en este biofiltro existió una mayor reproducción de lombrices las mismas que estimularon un mayor desarrollo de bacterias. La tendencia a un pH neutro mostrado en los vermifiltros 1 y 2 puede atribuirse a la capacidad inherente de las lombrices de tierra para actuar como agentes tampón y neutralizantes de pH como lo mencionan Hughes, Nair, Mathew y Ho (2007, p. 211); Kumar, Bhargava, Prasad y Pruthi (2015, p. 376); Kumar, Rajpal, Bhargava y Prasad (2014, p. 77); Sinha, Bharambe y Chaudhari (2008, p. 415) y Li y otros (2009, p. 3002). 3.3.3 Parámetro Conductividad Eléctrica De acuerdo a las mediciones realizadas se llevó a cabo una prueba de análisis de varianza ANOVA con el fin de determinar si existen diferencias estadísticas entre los tratamientos con relación a este parámetro o si la hipótesis nula planteada debe ser aceptada. Ho = µ1 = µ2 = µ3 HA = µi ≠ 0 para algún i = 1, 2,3 Tabla 20. ANOVA para el parámetro conductividad eléctrica Etapa 1. Fuente de Suma de variación cuadrados Grados de libertad Media cuadrática Entre 5323,274 2 2661,637 grupos 187767,187 57 3294,161 Total 193090,462 59 grupos Dentro de Valor F Sig crítico para F ,808 ,451 3,16 66 En la tabla 20, se hace evidente que el valor calculado de F es menor al valor crítico de F y que el nivel de significancia es mayor a 0,05 lo que indica que la hipótesis nula se acepta y que no existe diferencia significativa entre los tratamientos por lo que éstos son iguales en cuanto al parámetro conductividad eléctrica en la primera etapa de experimentación. Tabla 21. ANOVA para el parámetro conductividad eléctrica Etapa 2. Fuente de variación Suma de cuadrados Grados de libertad Media cuadrática Valor F Sig para F Entre 11945,782 2 5972,891 grupos 130811,683 57 2294,942 Total 142757,466 59 grupos crítico 2,603 ,083 3,16 Dentro de Según el análisis de varianza mostrado en la tabla 21, se evidencia que no existen diferencias significativas entre los tratamientos en la etapa 2 pues, el valor calculado de F es menor al valor crítico de F y el nivel de significancia es mayor a 0,05 razón por la cual se acepta la hipótesis nula de que los tratamientos son iguales en cuanto al parámetro conductividad eléctrica. Los resultados de conductividad eléctrica obtenidos en la experimentación se muestran en las figuras siguientes. 67 Figura 23. Resultados de conductividad eléctrica en los efluentes en función del tiempo (Etapa 1). 68 Figura 24. Resultados de conductividad eléctrica en los efluentes en función del tiempo (Etapa 2). Conductividad (µS/cm) 400 350 300 250 Vermifiltro 1 Vermifiltro 2 200 Vermifiltro 3 150 100 1 3 5 7 9 11 13 15 17 19 21 23 25 27 29 31 33 35 37 39 41 Tiempo (días) Figura 25. Tendencia del parámetro conductividad eléctrica en los vermifiltros en función del tiempo. 69 La conductividad eléctrica del agua residual presentó cambios significativos después del tratamiento con vermifiltros, se observó diferentes patrones de fluctuación durante el proceso experimental. En el vermifiltro 1 los valores de conductividad eléctrica descendieron muy por debajo del valor del agua residual cruda (325,18 µS/cm), posteriormente exhibieron una tendencia creciente y bajaron nuevamente hasta el final de la experimentación; sin embargo, en los últimos días se notó un aumento de este parámetro. En un inicio el vermifiltro 2 mostró una tendencia decreciente de la conductividad eléctrica y se incrementó ligeramente entre la medición 16 y 22, no obstante los valores volvieron a descender y a ubicarse por debajo de los valores de conductividad eléctrica de los vermifiltros 1 y 3. Durante los primeros días los valores medidos de conductividad eléctrica del efluente del vermifiltro 3 mostraron una ligera tendencia decreciente, sin embargo estos valores aumentaron y fue observable una fluctuación llegando al final del experimento con un ligero decrecimiento de los valores. Singh y Kaur (2015, p. 15); Tomar y Suthar (2011, pp. 99–100); Yang, Zhang y Xing (2014, p. 94) reportaron similar comportamiento de este parámetro durante el tratamiento con vermifiltros es decir fluctuaciones de los valores de conductividad eléctrica y posteriormente una tendencia decreciente. Los autores mencionados indican que el decrecimiento de la conductividad eléctrica puede ser producto de la adsorción y absorción de constituyentes inorgánicos del agua residual en los componentes biológicos del biofiltro. La conductividad eléctrica permite medir el contenido iónico del agua, con respecto a este parámetro en el tratamiento 1 se obtuvo una disminución del 52,30% para la etapa 1 y 19,16% para la etapa 2; mientras que en el tratamiento 2 la disminución obtenida fue 59,7% y 32,6% y en el tratamiento 3 se alcanzó una remoción de 34,31 % y 10,10% para la primera y segunda etapa de experimentación respectivamente. Según los datos presentados, en el vermifiltro dos se logró una mayor disminución de la conductividad eléctrica en el agua tratada superando el valor de 37% reportado por Lou, Yang y Wang, (2010, p. 490). 70 3.3.4 Parámetro Sólidos Totales Para comprobar si entre los efluentes tratados por los vermifiltros existe alguna diferencia en cuanto a este parámetro se aplicó una prueba del análisis de varianza ANOVA para determinar si la hipótesis nula debe ser aceptada o rechazada. Ho = µ1 = µ2 = µ3 HA = µi ≠ 0 para algún i = 1, 2,3 Tabla 22. ANOVA para el parámetro sólidos totales Etapa 1. Fuente de variación Suma de cuadrados Grados de libertad Media cuadrática Entre 151376,778 2 75688,389 grupos 403073,562 44 9160,763 Total 554450,340 46 grupos Valor F Sig crítico para F 8,262 ,001 3,2 Dentro de El análisis de varianza sobre este experimento ha permitido advertir diferencias significativas entre los tratamientos evaluados. En la tabla 22, es notorio que el valor calculado de F (8,26) es mayor al valor crítico de F (3,2) y que el nivel de significación es igual a 0,01 lo cual indica que se debe aceptar la hipótesis alternativa de que al menos uno de los tratamientos es diferente en referencia a este parámetro. 71 Tabla 23. Comparaciones múltiples para el parámetro sólidos totales Etapa 1 Prueba (I) (J) Tratamiento Tratamiento 1 Tukey 2 3 1 DMS 2 3 Diferencia de medias (I-J) Error estándar Sig. 2 139,8128* 34,3986 ,001 3 70,2052 34,3986 ,114 1 -139,8128* 34,3986 ,001 3 -69,6076 33,8393 ,111 1 -70,2052 34,3986 ,114 2 69,6076 33,8393 ,111 2 139,8128* 34,3986 ,000 3 70,2052* 34,3986 ,047 1 -139,8128* 34,3986 ,000 3 -69,6076* 33,8393 ,046 1 -70,2052* 34,3986 ,047 2 69,6076* 33,8393 ,046 La prueba de Tukey presentada en la tabla 23, muestra que no existe diferencia entre el tratamiento 2 y 3, ni entre el tratamiento 1 y 3 en cuanto al parámetro mencionado pues los niveles de significación obtenidos son mayores a 0.05, sin embargo las diferencias son observables entre el tratamiento 1 con respecto al tratamiento 2. Por otro lado, la prueba de DMS indica que si existe diferencias entre todos los tratamientos. 72 Tabla 24. ANOVA para el parámetro sólidos totales Etapa 2 Fuente de Suma de variación cuadrados Grados de libertad Media cuadrática Entre 5283,969 2 2641,984 grupos 169049,989 53 3189,622 Total 174333,958 55 grupos Valor F Sig crítico para F ,828 ,442 3,17 Dentro de Según el análisis de varianza exhibido en la tabla 24, se evidencia que no existen diferencias significativas entre los tratamientos, debido a que el valor calculado de F es menor al valor crítico de F y el nivel de significancia es mayor a 0,05 razón por la cual se acepta la hipótesis nula de que los tratamientos son iguales en esta etapa de experimentación con relación a los sólidos totales. Figura 26. Resultados de sólidos totales en los efluentes en función del tiempo (Etapa 1). 73 Figura 27. Resultados de sólidos totales en los efluentes en función del tiempo (Etapa 2). Sólidos totales (mg/l) 700 600 500 400 Vermifiltro 1 300 Vermifiltro 2 200 Vermifiltro 3 100 0 1 3 5 7 9 11 13 15 17 19 21 23 25 27 29 31 33 35 Tiempo (días) Figura 28. Tendencia del parámetro sólidos totales en los vermifiltros en función del tiempo. 74 Como se ilustra en las figuras 26, 27 y 28, los vermifiltros exhibieron una tendencia decreciente de sólidos totales. En la primera etapa fue observable que el vermifiltro 2 logró una mayor reducción de este parámetro comenzando con valores cercanos a 300 mg/l hasta llegar a aproximadamente 116 mg/l, seguido por el vermifiltro 3 que presentó fluctuaciones en un inicio para luego descender hasta ubicarse en 170 mg/l de sólidos totales; en cuanto el vermifiltro 1 mostró los valores más altos entre los tres tratamientos pues se midieron valores desde 647 mg/l a 227 mg/l. En la etapa dos se observa que las mediciones se encuentran más cercanas, que le vermifiltro 1 comienza a estabilizarse y que el tratamiento 3 denota una ligera disminución en la reducción de este parámetro, en tanto el vermifiltro 2 nuevamente presenta una mayor disminución de los sólidos totales. Se compararon los resultados obtenidos en las dos etapas con los valores máximos permitidos por el TULSMA para descarga a un cuerpo de agua dulce y el resultado fue que estos 700 90,0 80,0 70,0 60,0 50,0 40,0 30,0 20,0 10,0 0,0 Sólidos Totales (mg/l) 600 500 400 300 200 100 0 Vermifiltro 1 Vermifiltro 2 Vermifiltro 3 A.R (mg/l) 227 116 170 624 % Remoción 63,6 81,4 72,8 % de Remoción se encuentran por debajo de los valores exigidos por la normativa. Figura 29. Remoción de sólidos totales alcanzada en los tratamientos en la etapa 1. 500 450 400 350 300 250 200 150 100 50 0 70,0 60,0 50,0 40,0 30,0 20,0 % de Remoción Sólidos Totales (mg/l) 75 10,0 0,0 Vermifiltro 1 Vermifiltro 2 Vermifiltro 3 A.R (mg/l) 218 160 205 473 % Remoción 53,9 66,2 56,7 Figura 30. Remoción de sólidos totales alcanzada en los tratamientos en la etapa 2. En la figura 29, se observa que en la primera etapa se logró una remoción del 63,6%, 81,4% y 72,8 % en el primero, segundo y tercer tratamiento respectivamente. En tanto en la etapa 2 la reducción conseguida según la figura 30 fue de 53,9 % en el tratamiento 1, 66,2% en el tratamiento 2 y 56,7 % en el tratamiento 3. Como es evidente el vermifiltro 2 presenta una tasa de remoción más alta a lo largo de la experimentación lo que denota que existe una mayor interacción entre las lombrices de tierra y los microorganismos presentes. Los sólidos totales disminuyeron después del tratamiento de vermifiltración debido a que durante el proceso los sólidos disueltos, suspendidos, orgánicos e inorgánicos fueron atrapados por adsorción y estabilizados para luego ser sometidos a un proceso ingestión y de biodegradación. . 76 3.3.5 Parámetro DBO5 (Demanda Biológica de Oxígeno) En cuanto se refiere a este parámetro contaminante la disminución es notoria, en la figura 31 se puede apreciar que en el vermifiltro 1 los valores de DBO 5 oscilan entre 40 y 37 mg/l con una media de 38,5 mg/l. Es evidente que el tratamiento con mayor remoción es el 2, pues los valores medidos fueron 27 y 21 mg/l de DBO5 con una media de 24 mg/l, en tanto en el vermifiltro 3 se obtuvo 35 y 36 mg/l con una media de 35,5 mg/l. Figura 31. Resultados en la etapa 1 de DBO5 en los tratamientos. En la etapa 2 se puede apreciar que los valores de DBO 5 se encuentran menos dispersos en los tratamientos 1 y 2 (figura 32), es notorio que el vermifiltro 2 tiene mejores resultados en cuanto a este parámetro pues los valores medidos (5 y 3 mg/l) son menores a los obtenidos en el tratamiento 1 (20 y 18 mg/l) y en el tratamiento 3 (28 y 23 mg/l). 77 Figura 32. Resultados en la etapa 2 de DBO5 en los tratamientos. Se calculó la remoción alcanzada en los tratamientos según la ecuación 11 y 400 95,0 350 94,0 300 93,0 250 92,0 200 91,0 150 90,0 100 89,0 50 0 DBO5 % Remoción % de Remoción DBO5 (mg/l) los resultados son presentados a continuación. 88,0 Tratamiento 1 Tratamiento 2 Tratamiento 3 A.R TULSMA 37 21 35 380 100 90,3 94,5 90,8 Figura 33. Remoción alcanzada de DBO5 en los tratamientos en la etapa 1. 140 100,0 120 95,0 DBO5 (mg/l) 100 90,0 80 85,0 60 80,0 40 75,0 20 0 DBO5 % Remoción % de Remoción 78 70,0 Tratamiento 1 Tratamiento 2 Tratamiento 3 A.R TULSMA 18 3 23 125 100 85,6 97,6 81,6 Figura 34. Remoción alcanzada de DBO5 en los tratamientos en la etapa 2. Según las figuras 33 y 34, se presentó una elevada remoción de DBO5 en los tratamientos; así por ejemplo, el tratamiento 1 exhibió una remoción del 90,26% y 85,6% para la primera y segunda etapa respectivamente. En tanto, el tratamiento 2 logró una mayor remoción de DBO5 con 94,47% para la primera concentración de agua residual y 97,6% para la segunda, esto puede atribuirse a que en este biofiltro se registró la mayor población de lombrices de tierra. En el tratamiento 3 las remociones observadas fueron del 90,7% y 81,6%. Las concentraciones finales de DBO5 alcanzadas en los tratamientos se encuentran dentro de los límites permisibles fijados en la ley para descargas a un cuerpo de agua dulce. Los resultados obtenidos son superiores a los publicados por Adugna y otros (2015, p. 5); Arora y otros (2014, p. 135); Li y otros (2009, pp. 3004–3006) quienes en sus estudios indican que el tratamiento con vermifiltros puede reducir la concentración de DBO5 en un rango del 81,4 % al 90,1%. 79 La reducción en la demanda bioquímica de oxígeno del agua residual puede imputarse a los efectos de la relación simbiótica que se produce entre las lombrices de tierra y los microorganismos asociados que consumen y aceleran la descomposición de la materia orgánica, adicionalmente ésta pudo quedarse adherida al medio filtrante y posteriormente oxidarse gracias a la biopelícula formada en estas capas, corroborando lo mencionado por Kumar y otros (2015, p. 373); Adugna y otros (2015, p. 5); Kharwade y Khedikar (2011, p. 588); Kumar y otros (2014, p. 78). 3.3.6 Parámetro DQO (Demanda Química de Oxígeno) En relación a la demanda química de oxígeno se distingue en la figura 35 que el tratamiento 2 presentó valores más bajos (63 mg/l y 41 mg/l) con una media de 52 mg/l, seguido por el tratamiento 3 (75 mg/l y 64 mg/l) con un valor promedio de 69,5 mg/l y el tratamiento 1(87 mg/l y 78 mg/l) con una media de 82,5 mg/l. Figura 35. Resultados en la etapa 1 de DQO en los tratamientos. 80 En la figura 36 se visualiza que en el tratamiento dos se obtiene nuevamente un mayor decrecimiento del parámetro contaminante DQO, es así que los valores medidos (26 mg/l y 14 mg/l) son menores a los de los vermifiltros 1 y 3 (36 mg/l y 31 mg/l) y (42 mg/l y 36 mg/l), respectivamente. La alta efectividad observada en el tratamiento 2, tanto en la remoción del DQO como la del DBO5, descrita anteriormente se puede atribuir a la mayor población de lombrices de tierra que estimularon un crecimiento bacteriano superior a los demás vermifiltros y a la fibra de coco que forma parte de la capa 1 pues como lo mencionan Dharmarathne, Sato, Kawamoto y Takana (2013, p. 629) este material presenta una gran área superficial y específica, a la vez que ofrece una alta capacidad de humectación que permite la adecuada adhesión de microorganismos que degradan materia orgánica. Figura 36. Resultados en la etapa 2 de DQO en los tratamientos. La remoción alcanzada en los tratamientos con respecto al parámetro DQO se calculó según la ecuación 11, los resultados obtenidos son presentados en las siguientes figuras. 81 800 95,0 700 94,0 93,0 92,0 500 % de Remoción DQO (mg/l) 600 91,0 400 90,0 300 89,0 200 88,0 100 0 DQO % Remoción 87,0 86,0 Tratamiento 1 Tratamiento 2 Tratamiento 3 A.R TULSMA 78 41 64 699 250 88,8 94,1 90,8 450 97,0 400 96,0 350 95,0 300 94,0 250 93,0 200 92,0 150 91,0 100 90,0 50 89,0 0 DQO % Remoción Tratamiento 1 Tratamiento 2 88,0 Tratamiento 3 A.R TULSMA 406 250 31 14 36 92,4 96,6 91,1 % de Remoción DQO (mg/l) Figura 37. Remoción alcanzada de DQO en los tratamientos en la etapa 1. Figura 38. Remoción alcanzada de DQO en los tratamientos en la etapa 2. 82 En las figuras 37 y 38, se observa que en los tres tratamientos se logró una reducción muy significativa de la demanda química de oxígeno. En el primer tratamiento, el DQO llegó a 78 mg/l en la primera etapa y 31 mg/l en la segunda, lo que representa una remoción del 88,8 % y 92,4% respectivamente. En el efluente del vermifiltro 2, los valores del DQO alcanzaron 41 mg/l y 14 mg/l para cada una de las etapas, lo que constituye una remoción del 94,1 % y 96,6%. En tanto el tratamiento 3 mostró una remoción del 90,8% y del 91,1% con valores de 64 mg/l y 36 mg/l de DQO para la primera y segunda etapa respectivamente. Comparando los valores obtenidos con la normativa legal para descargas a un cuerpo de agua dulce presentado en el TULSMA se advierte que se encuentran dentro de los límites permisibles. Los resultados son superiores a los reportados por Merly, Logeswari, Mano y Kannadasan (2013, p. 151) que lograron una remoción del DQO en un 80% y se acercan a los alcanzados por Cardoso y otros (2011); Keshav y Garkal (2014, p. 73) y Sinha y otros (2010, p. 9) quienes en sus estudios con vermifiltros indican eficiencias del 90% en la disminución de la demanda química de oxígeno. La elevada remoción de DQO que se consigue en este tipo de biofiltros según diversos autores se relaciona con la sedimentación, adsorción y biodegradación de materia orgánica que se queda adherida en la superficie de los materiales que forman parte del sistema geológico del vermifiltro y a las enzimas secretadas por las lombrices de tierra que contribuyen a la degradación de diversos componentes químicos que de otro modo no podrían ser degradados. (Lakshmi et al., 2014, p. 588; Manyuchi et al., 2013, p. 540; Sinha et al., 2010, p. 9) 83 3.3.7 Parámetro Nitrógeno Total Como se ilustra en la figura 39, el tratamiento 3 presenta los niveles más altos de nitrógeno con 26 mg/l y 22 mg/l dando un promedio de 24 mg/l, se puede apreciar que en el tratamiento 2 los valores de nitrógeno total medidos fueron 17 y 12 mg/l con una media de 14,5 mg/l, en tanto el tratamiento 1 se encuentra cercano con una media de 15,5 mg/l. Figura 39. Resultados de nitrógeno total en los tratamientos en la etapa 1. En la etapa 2, según la figura 40 se puede visualizar que el tratamiento 2 logró nuevamente una mayor remoción de este parámetro llegando a un valor de 8 mg/l con una media de 9 mg/l, seguido por el tratamiento 1 con una media de 13 mg/l y valores de 15 mg/l y 11 mg/l, es notorio que la disminución en el tratamiento 3 se mantiene casi constante pues los valores medidos fueron 13 y 14 mg/l de nitrógeno total. 84 Figura 40. Resultados de nitrógeno total en los tratamientos en la etapa 2. La remoción alcanzada en los tratamientos con respecto al parámetro nitrógeno total se calculó según la ecuación 11, los resultados obtenidos son presentados 50 80,0 45 70,0 40 60,0 35 30 50,0 25 40,0 20 30,0 15 20,0 10 10,0 5 0 (mg/l) % Remoción % de Remoción Nitrógeno Total (mg/l) en las figuras siguientes. 0,0 Tratamiento 1 Tratamiento 2 Tratamiento 3 A.R TULSMA 13 12 22 47 15 72,3 74,5 53,2 Figura. 41 Remoción alcanzada de nitrógeno total en los tratamientos en la etapa 1. 35 80,0 30 70,0 60,0 25 50,0 20 40,0 15 30,0 10 20,0 5 0 % de Remoción Nitrógeno Total (mg/l) 85 10,0 0,0 Tratamiento 1 Tratamiento 2 Tratamiento 3 A.R TULSMA 11 8 13 31 15 64,5 74,2 58,1 (mg/l) % Remoción Figura. 42 Remoción alcanzada de nitrógeno total en los tratamientos en la etapa 2. Según las figuras 41 y 42, se presentó una alta remoción de nitrógeno total en los tratamientos, es así que los valores obtenidos se encuentran por debajo del límite máximo permisible fijado en la ley para descargas a un cuerpo de agua dulce. Las remociones alcanzadas se describen a continuación: el tratamiento 1 logró una reducción de nitrógeno total en un 72,3% y 64,5%, el tratamiento 3 mostró una disminución del 53,2% y 58,1 %, mientras que el tratamiento 2 exhibió una mayor tasa de remoción con un 74,5% y 74,2%. La remoción de nitrógeno total registrada en el vermifiltro 2 supera los resultados publicados por Wang y otros (2014, p. 168) que reporta una remoción del 56,3% y los resultados de Nie y otros (2015, p. 8) que indican remociones de este parámetro entre un 30 a 70%, por lo que se puede discutir que la remoción alcanzada por este tratamiento se encuentra por encima del rango establecido por estudios similares lo que demuestra una buena remoción de nitrógeno total. 86 La disminución del nitrógeno se puede atribuir al proceso de adsorción en el medio filtrante y biomasa y a la posterior acción biológica, además según reporta Lou y otros (2010, p. 490) las lombrices de tierra segregan varios componentes que pudieron contribuir a la reducción del parámetro mencionado. 3.3.8 Parámetro Fósforo Total Como se ilustra en la figura 43, los tres tratamientos presentan similares tasas de remoción para el fósforo total así, en el tratamiento 1 los valores medidos fueron: 4,51 mg/l y 4,03 mg/l con una media de 4,27 mg/l, en tanto el tratamiento 2 mostró valores de 4,42 y 3,76 mg/l con una media de 4,09, muy cercano a este tratamiento está el vermifiltro 3 con una media de 4,27 mg/l. Figura 43. Resultados de fósforo total en los tratamientos etapa 1. En la etapa 2 se puede visualizar que el tratamiento 2 presenta valores más bajos de fósforo total (figura 44) llegando a 0,77 mg/l de fósforo, logrando una mayor disminución de este parámetro pues en los tratamientos 1 y 3 las concentraciones de fósforo total medidas fueron (3,79 mg/l y 2,82 mg/l) y (3,51 y 2,39 mg/l) respectivamente. 87 Figura 44. Resultados de fósforo total en los tratamientos en la etapa 2. La remoción alcanzada en los tratamientos con respecto al parámetro fósforo total se calculó según la ecuación 11, los resultados obtenidos son presentados 12 51,0 10 50,0 8 49,0 6 48,0 4 47,0 2 46,0 0 45,0 Tratamient o1 Tratamient o2 Tratamient o3 A.R TULSMA (mg/l) 4,03 3,76 3,89 7,61 10 % Remoción 47,0 50,6 48,9 Figura 45. Remoción alcanzada de fósforo total en los tratamientos en la etapa 1. % de Remoción Fósforo Total (mg/l) en las figuras siguientes. 88 12 90,0 80,0 Fósforo Total (mg/l) 10 8 60,0 50,0 6 40,0 4 30,0 % de Remoción 70,0 20,0 2 10,0 0 0,0 Tratamiento 1 Tratamiento 2 Tratamiento 3 A.R TULSMA (mg/l) 2,82 0,77 2,39 5,2 10 % Remoción 45,8 85,2 54,0 Figura 46. Remoción alcanzada de fósforo total en los tratamientos en la etapa 2. Según las figuras 45 y 46, el fósforo total es uno de los parámetros que presenta las menores tasas de remoción en el estudio, no obstante las concentraciones de fósforo medidas tanto en el afluente como en los efluentes se encuentran por debajo del límite máximo permisible fijado en la ley para descargas a un cuerpo de agua dulce. Las remociones alcanzadas se describen a continuación: el tratamiento 1 consiguió una reducción de fósforo total en un 47% y 45,8%, el tratamiento 3 mostró una disminución del 48,9% y 54 %, mientras que el tratamiento 2 exhibió una mayor tasa de remoción con un 50,6% y 85,2%. Las remociones descritas se encuentran dentro del rango señalado en el estudio de Li y otros (2009, p. 3006) que indica disminuciones de fósforo total entre un 19,8 y 59,3 %, sin embargo la remoción en el filtro 2 (85,2%) supera dicha referencia. 89 CAPÍTULO IV: CONCLUSIONES Y RECOMENDACIONES 4.1 Conclusiones La caracterización del agua residual se realizó mediante la determinación de pH, turbidez, conductividad eléctrica, sólidos totales, nitrógeno total, fósforo total, DBO5 y DQO, a través de métodos estándar que permitieron la comparación del agua residual y el agua tratada. Esta caracterización inicial, permitió determinar que las cargas empleadas en el estudio experimental se encontraron en un intervalo de concentración que clasificó al agua residual como fuerte y media respectivamente. El agua residual con carga fuerte presentó la siguiente concentración: turbidez (84,4 NTU), pH (7,3), conductividad eléctrica (325,18 µS/cm), sólidos totales (624 mg/l), nitrógeno total (47 mg/l), fósforo total (7,61 mg/l), DQO (699 mg/l) y DBO 5 (380 mg/l); mientras que en el agua residual con carga media la concentración fue: turbidez (59,4 NTU), pH (7,1), conductividad eléctrica (220,7 µS/cm), sólidos totales (473 mg/l), nitrógeno total (31 mg/l), fósforo total (5,2 mg/l), DQO (406 mg/l) y DBO5 (125 mg/l). De acuerdo a la caracterización del agua tratada en los vermifiltros se evidenció que en las dos etapas de experimentación los parámetros contaminantes medidos en los efluentes (DQO, DBO 5, sólidos totales, nitrógeno total y fósforo total) cumplen con la normativa legal contenida en el Libro VI del TULSMA Anexo 1 Norma de Calidad Ambiental y de Descarga de Efluentes: Recurso Agua. En cuanto al parámetro turbidez, éste tendió a decrecer con el paso de los días, las variaciones medidas pueden deberse a un arrastre de partículas en los efluentes tratados. El porcentaje de remoción de turbidez después del tratamiento con vermifiltros al final de cada etapa supera el 91%. 90 En referencia al comportamiento del pH, se puede indicar que los tres vermifiltros en un inicio presentaron una tendencia alcalina, posteriormente de acuerdo al grado de actividad bacteriana el pH decreció siendo más notoria esta predisposición en el vermifiltro 2, por lo que se puede concluir que en este biofiltro existió un mayor número de bacterias. Al final de la experimentación el pH pudo estabilizarse alrededor de pH neutro. El comportamiento de la conductividad eléctrica fue homogéneo en todos los tratamientos, el vermifiltro 1 presentó una remoción del 52,30% y 19,16% para la primera y segunda etapa de experimentación respectivamente. Mientras que en el vermifiltro 2, la disminución obtenida fue 59,7% y 32,6% y en el tratamiento 3 se alcanzó una remoción de 34,31% y 10,10%. Los sistemas de vermifiltración probados removieron el DBO 5 entre un 81% a 97%, el DQO entre un 88,8% y 96,6%, el nitrógeno total entre 53,2% y 74,5% y el fósforo total entre un 45,8% y 85,2%. En el vermifiltro 1, la temperatura promedio en la capa uno fue de 20,44 oC y el pH 7,27. En el vermifiltro 2, el pH de la capa uno fue 6,41 y la temperatura 22,54 oC y en el vermifiltro 3 se midió una temperatura promedio de 21,60 oC y un pH de 6,19. Las condiciones medidas tanto de temperatura como de pH en la capa uno de los tres vermifiltros se encontraron dentro del rango establecido para el normal desarrollo de la especie Eisenia foetida (pH: 5-8 y temperatura: 15,7 oC - 28,2 oC). Los vermifiltros 1 y 2 pudieron tratar con normalidad la carga orgánica superficial del agua residual en las dos etapas (288,47 g/m 2*día y 167,5 g/m2*día), sin embargo, el vermifiltro 3 se saturó después de haber trabajado con una carga hidráulica de 0,4127 m3/m2*día y una COS de 288,47 g/m2*día por lo que se puede concluir que el aserrín no funciona como medio de soporte bajo las condiciones propuestas para el tratamiento de ARD de concentración fuerte. 91 Comparando los tres tratamientos se pudo notar que el vermifiltro 2 se estabilizó más rápido y ofreció mayores remociones desde el principio de la experimentación, así las remociones alcanzadas en la primera y segunda etapa fueron: 97,7% y 98,3% de turbidez, 59,7% y 32,6% de conductividad eléctrica, 81,4% y 66,2% de sólidos totales, 94,5% y 97,6% de DBO5, 94,1% y 96,6% de DQO, 74,5% y 74,2% de nitrógeno total, 50,6% y 85,2% de fósforo total. Por tal motivo, se concluye que la acción combinada del medio filtrante, lombrices de tierra y fibra de coco permite mayores reducciones de parámetros contaminantes en el ARD. En el presente trabajo se demostró, que el vermifiltro 2 que incorpora fibra de coco como medio de soporte y filtración se presenta como una opción idónea para el tratamiento de ARD de fuerte y mediana concentración. 4.2 Recomendaciones El uso de vermifiltros para el tratamiento de aguas residuales domésticas es un tratamiento alternativo que por sus ventajas ecológicas y bajos costos de mantenimiento e instalación sin duda puede ser utilizado en pequeñas comunidades para la reducción de la carga contaminante del agua residual. Proyectos que involucren la implementación de este tratamiento pueden ser complementados con la inclusión de residuos orgánicos sólidos, lo que permitiría un tratamiento en conjunto del agua residual doméstica y los residuos orgánicos sólidos generados en una vivienda. Si se emplea un vermifiltro para el tratamiento de aguas residuales domésticas con aserrín como material de soporte, se debe incrementar la altura de la capa y trabajar con una COS inferior a 288,47 g/m2*día. Una vez instalado el vermifiltro se sugiere monitorear regularmente la temperatura de la capa de soporte debido a que temperaturas fuera del rango óptimo y tolerable para las lombrices de tierra pueden afectar su normal desarrollo y disminuir el tratamiento del agua residual; para mejorar 92 el rendimiento del sistema se puede incluir aireación dentro del medio filtrante para contribuir al desarrollo de microorganismos degradadores. 93 REFERENCIAS Abdullah, A., Jamaludin, S., Anwar, M., Noor, M. y Hussin, K. (2011). Assessment of Physical and Mechanical Properties of Cement Panel Influenced by Treated and Untreated Coconut Fiber Addition. Physics Procedia, 22, 263–269. doi.org/10.1016/j.phpro.2011.11.042 ADAM. (2015). Balanzas Compactas y Portátiles Serie Core. Recuperado el 20 de mayo de 2015 de http://www.adamequipment.com/am/ae_brochure/es/1/178 Adugna, A., Andrianisa, H., Konate, Y., Ndiaye, A. y Maiga, A. (2015). Performance comparison of sand and fine sawdust vermifilters in treating concentrated grey water for urban poor. Environmental Technology, 2, 1–7. doi.org/10.1080/09593330.2015.1046951 Almeida, C., Azevedo, N., Santos, S., Keevil, C. y Vieira, M. (2011). Discriminating Multi-Species Populations in Biofilms with Peptide Nucleic Acid Fluorescence In Situ Hybridization (PNA FISH). PLoS ONE, 6, 14680-14786. doi.org/10.1371/journal.pone.0014786 Antizar-Ladislao, B. y Sheikholeslami, R. (2011). Water Resource Planning, Development and Management : Water Production and Wastewater Treatment (1a ed.). New York, USA: Nova Science Publishers. Arora, S. y Kazmi, A. (2015). The effect of seasonal temperature on pathogen removal efficacy of vermifilter for wastewater treatment. Water Research, 74, 88–99. doi.org/10.1016/j.watres.2015.02.001 Arora, S., Rajpal, A., Bhargava, R., Pruthi, V., Bhatia, A. y Kazmi, A. (2014). Antibacterial and enzymatic activity of microbial community during wastewater treatment by pilot scale vermifiltration system. Bioresource Technology, 166, 132–141. doi.org/10.1016/j.biortech.2014.05.041 Azuar, S. y Ibrahim, M. (2012). Comparison of sand and oil palm fibrevermibeds in filtration of palm oil mill effluent (POME). International Annual Symposium on Sustainability Science and Management, 11, 1414– 1419. 94 Bajsa, O., Nair, J., Mathew, K. y Ho, G. (2009). Vermiculture as a tool for domestic wastewater management. Water Science & Technology, 48, 125–132. Baumgartner, R. (2013). Developing a testing protocol for Vermifiltration-based onsite Wastewater Treatment Systems (VOWTS). Recuperado el 30 de mayo de 2015 de http://researchrepository.murdoch.edu.au/16946/ Bharambe, G., Bapat, P. y Sinha, R. (2009). Removal of high BOD and COD loadings of primary liquid waste products from dairy industry by vermifiltration technology using earthworms. Indian Journal of Environmental Protection, 27(6), 486–501. Bhise, H. y Anaokar, G. (2015). Design and Suitability of Modular Vermifilter for Domestic Sewage Treatment. International Journal, 44, 44–51. Bitton, G. (2010). Wastewater Microbiology (4a ed.). NJ, USA: Wiley-Blackwell. Campesinos, J., Conde, M., Fajardo, V., Delgado, F. y Aguirre, S. (2005). Manual cría de la lombriz de tierra: una alternativa ecológica y rentable. (2a ed.). Bogotá, Colombia: Editorial San Pablo. Cárdenas, C., Yabroudi, S., Benítez, A., Páez, K., Perruolo, T., Angulo, N. y Herrera, L. (2012). Desempeño de un reactor biológico secuencial (RBS) en el tratamiento de aguas residuales domésticas. Revista Colombiana de Biotecnología, 14(2), 111–120. Cardoso, L., Ramírez, E., y Garzón, M. (2011). Evaluation of a pilot vermifilter for the treatment of wastewater. Recuperado el 2 de junio de 2015 de http://www.globalsciencebooks.info/JournalsSup/images/Sample/DSDP _4(SI1)83-88o.pdf CEPAL. (2012). Diagnóstico de las estadísticas de agua en Ecuador (No. 1).Recuperado el 18 de abril de 2015 de http://aplicaciones.senagua.gob.ec/servicios/descargas/archivos/downl oad/Diagnostico%20de%20las%20Estadisticas%20del%20Agua%20Pr oducto%20IIIc%202012-2.pdf Constitución de la República del Ecuador. (2008). Registro Oficial 449 de 20 de octubre de 2008. Reformas en Registro Oficial- Suplemento de 13 de julio de 2011. 95 Control Company. (2012). Traceable Lollipop Thermometer Instructions. Recuperado el 14 de junio de 2015 de https://traceable.com/media/import/Files/Inst/4371inst.pdf De la Cruz, E., Osorio, R., Martínez, E., Lozano, A., Gómez, A. y Sánchez, R. (2010). Uso de compostas y vermicompostas para la producción de tomate orgánico en invernadero. Interciencia, 35(5), 363–368. Dharmarathne, N., Sato, N., Kawamoto, K. y Takana, N. (2013). Evaluation of Wastewater Treatment Efficiency Using Coconut Fiber Biofilm Reactor System With Synthetic Leachate. Recuperado el 2 de junio de 2015 de http://www.researchgate.net/publication/275976424_Evaluation_of_Wa stewater_Treatment_Efficiency_Using_Coconut_Fiber_Biofilm_Reactor _System_With_Synthetic_Leachate Díaz, A. (2009). Diseño estadístico de experimentos (2.a ed.). Medellín, Colombia: Universidad de Antioquia. Duncan, M. (2013). Domestic Wastewater Treatment in Developing Countries (2.a ed.). London, United Kingdom: Routledge. Durán, L., y Henríquez, C. (2009). Crecimiento y reproducción de la lombriz roja (Eisenia foetida) en cinco sustratos orgánicos. Agronomía Costarricense, 33(2), 275–281. Fakhrul, T., Mahbub, R. y Islam, M. (2013). Properties of Wood Sawdust and Wheat Flour Reinforced Polypropylene. Composites, 1, 135–148. FAO. (2014). Aquastat. Recuperado el 30 de abril de 2015 de http://www.fao.org/nr/water/aquastat/data/glossary/search.html Gallego, R. (2003). Introducción al análisis de datos experimentales: tratamiento de datos en bioensayos. Recuperado el 9 de junio de 2015 de http://www.e-buc.com/portades/9788480217712_L33_23.pdf Gheisari, S., Danesh, S., y Mousavi, S. (2010). Growth and Reproduction of Eisenia fetida in Vermicomposting of Organic Fraction of Municipal Solid Wastes. Asian Journal of Chemistry, 22(2), 1266–1274. 96 Gonzalez, A. (2008). Lombricultura en Costa Rica. Recuperado el 20 de abril de 2015 de http://www.lombricultura.cl/lombricultura.cl/userfiles/file/biblioteca/sobre _lombricultura/Articulolombritica.pdf González, H., Coronado, J. y Acosta, D. (2007). El método del hidrómetro: base teórica para su empleo en la determinación de la distribución del tamaño de partículas de suelo. Revista Ciencias Técnicas Agropecuarias, 16(3), 19–24. Gutiérrez, H. y De la Vara, R. (2013). Análisis y Diseño de Experimentos (3a ed.). México DF, México: McGraw-Hill. Hakeem, K., Jawaid, M. y Alothman, O. (2015). Agricultural Biomass Based Potential Materials. Journal of Engineering Research and Studies, 2(4), 491–502. HANNA Instruments. (2009). HI 2550 Instruction Manual. Recuperado el 3 de junio de 2015 de www.hannainst.es/.../1042_HI_2550_Ingles.pdf HANNA Instruments. (2013). HI 88713 ISO Turbity Meter. Recuperado el 5 de junio de 2015 de http://www.hannainst.com/manuals/man88713_05_05_2008.pdf HANNA Instruments. (2015). Medidor de sobremesa para pH/ORP/ISE/EC/TDS/NaCl. Recuperado el 8 de junio de 2015 de http://www.hannachile.com/productos/index2.php?option=com_virtuem art&page=shop.pdf_output&showpage=shop.product_details&pop=1&o utput=pdf&product_id=305&category_id=2210&pop=1 Harrison, R., Chester, R. y Slater, D. (2001). Pollution : Causes, Effects and Control (4.a ed.). NJ, USA: Royal Society of Chemistry. Henze, M. (2008). Biological wastewater treatment: principles, modelling and design (1.a ed.). London, United Kingdom: IWA Pub. Hughes, R., Nair, J., Mathew, K. y Ho, G. (2007). Toxicity of domestic wastewater pH to key species within an innovative decentralised vermifiltration system. Water Science & Technology, 55(7), 211-224. doi.org/10.2166/wst.2007.147 97 Hughes, R., Nair, J. y Ho, G. (2008). The toxicity of ammonia/ammonium to the vermifiltration wastewater treatment process. Water Science & Technology, 58(6), 1215-1230. doi.org/10.2166/wst.2008.478 INEC. (2013). Censo de Información Ambiental Económica en Gobiernos Autónomos Descentralizados Municipales 2013. Recuperado el 24 de abril de 2015 de http://www.ecuadorencifras.gob.ec/documentos/webinec/Encuestas_Ambientales/Municipios_ConsProvinciales_2013/Munic ipios-2013/Presentacion_Principales_Resultados_Municipios.pdf Jácome, E. (2014). Consumo de agua y energía aumenta en verano. Recuperado el 5 de mayo de 2015 de http://www.elcomercio.com/actualidad/consumo-agua-energiaaumenta-verano-quito.html Jiménez, B. (2009). La Contaminación Ambiental en México (1.a ed.). México DF, México: Editorial Limusa. Kazlauskiene, N., Svecevicius, G., Marciulioniene, D. y Montvydiene, D. (2012). The effect of persistent pollutants on aquatic ecosystem: A complex study,8(2), 1–6. doi.org/10.1109/BALTIC.2012.6249198 Keshav, R. y Garkal, D. J. (2014). A pilot scale study of vermi-biofilter (VBF) for residential quarter wastewater. International Journal of Current Research in Chemestry and Pharmaceutical Sciences, 1(6), 71–76. Kharwade, A. y Khedikar, I. (2011). Laboratory scale studies on domestic grey water through vermifilter and non-vermifilter. Journal of Engineering Research and Studies, 2(4), 35–39. Knobelsdorf, J. (2005). Eliminación biológica de nutrientes en un ARU de baja carga orgánica mediante el proceso VIP. Recuperado el 28 de mayo de 2015 de http://upcommons.upc.edu/handle/10803/5909 Knobelsdorf, M. (2009). Depuración biológica de aguas residuales. Recuperado el 9 de junio de 2015 de http://www.tdx.cat/bitstream/handle/10803/5909/08Mjkm08de18.pdf?se quence=8 98 Komarowski, S. (2001). Vermiculture for sewage and water treatment sludges. Water, Publication of Australian Water and Wastewater Association, 12, 39–43. Kumar, T., Bhargava, R., Prasad, K. y Pruthi, V. (2015). Evaluation of vermifiltration process using natural ingredients for effective wastewater treatment. Ecological Engineering, 75, 370–377. doi.org/10.1016/j.ecoleng.2014.11.044 Kumar, T., Rajpal, A., Bhargava, R. y Prasad, K. (2014). Performance evaluation of vermifilter at different hydraulic loading rate using river bed material. Ecological Engineering, 62, 77–82. doi.org/10.1016/j.ecoleng.2013.10.028 Lakshmi, C., Ranjitha, J. y Vijayalakshmi, S. (2014). Waste water treatment using vermifilteration technique at institutional level. International Journal of Advanced Scientific and Technical Research, 1(3), 581–590. Ley de Aguas. (2004). Registro Oficial 339 de 20 de mayo de 2004. Ley de Gestión Ambiental. (2004). Registro Oficial 418 de 10 de septiembre de 2004. Ley de Prevención y Control de la Contaminación Ambiental. (2004). Registro Oficial 418 de 10 de septiembre de 2004. Li, Y., Xiao, Y., Qiu, J., Dai, Y. y Robin, P. (2009). Continuous village sewage treatment by vermifiltration and activated sludge process. Water Science & Technology, 60(11), 3001-3021 López, C., Sañudo, R., Armenta, C., Rey, D. y Félix, J. (2013). Influencia de diferentes sustratos orgánicos en la lombriz roja californiana (Eisenia foetida). Tecnociencia, 7(2), 81–87. Lou, S., Yang, J. y Wang, S. (2010). Wastewater treatment performance of a vermifilter enhancement by a converter slag–coal cinder filter. Ecological Engineering, 36(4), 489–494. doi.org/10.1016/j.ecoleng.2009.11.018 Manaf, L., Jusoh, M., Yusoff, M., Ismail, T., Harun, R., Juahir, H. y Jusoff, K. (2009). Influences of Bedding Material in Vermicomposting Process. International Journal of Biology, 1(1), 81-97. 99 Manivasakam, N. (2005). Physico-chemical examination of water sewage and industrial effluents.Physico-chemical examination of water sewage and industrial effluents (5.a ed.). Meerut, India: Pragati Prakashan. Manosalva, J., Ruiz, R. y Pérez, F. (2012). Diseño conceptual de una estación experimental de tratamiento de aguas residuales domésticas orientada a municipios con población menor a 30.000 habitantes. Revista Ingenierías Universidad de Medellín, 11(21), 87–99. Manyuchi, M., Kadzungura, L. y Boka, S. (2013). Vermifiltration of Sewage Wastewater for Potential Use in Irrigation Purposes Using Eisenia fetida Earthworms. World Academy of Science, Engineering and Technology,12, 538–542. Méndez, L., Miyashiro, V., Rojas, R., Cotrado, M. y Carrasco, N. (2004). Tratamiento de aguas residuales mediante lodos activados a escala de laboratorio. Rev. Inst. Investigación, 7(14), 74–83. Mercy, M., Kadzungura, L. y Boka, S. (2013). Pilot Scale Studies for Vermifiltration of 1000m3/day of Sewage Wastewater. Asian journal of engineering and technology, 1, 81–92. Merly, X., Logeswari, A., Mano, S. y Kannadasan, T. (2013). Vermiculture for the treatment of diary effluents. Journal of International Academic Research for Multidisciplinary, 1, 143–154. Metcalf, y Eddy. (2004). Wastewater engineering treatment and reuse (4.a ed.). Signapur: Mc Graw- Hill. Moncayo, I., y Ayala, D. (2011). Estudio de tratabilidad biológica de aguas residuales domésticas para optimizar resultados a escala real. Revista Digital VI CONGRESO Ciencia y Tecnología ESPE 2011. Recuperado el 21 de julio de 2015 de http://www.espe.edu.ec/portal/files/sitio_congreso_2011/papers/V3.pdf Munroe, G. (2007). Manual of On-Farm Vermicomposting and Vermiculture. Pub. of Organic Agriculture Centre of Canada. Recuperado el 16 de mayo de 2015 http://oacfo/docs/vermiculture_farmersmanual_gm.pdf Nesaratnam, S. (2014). Water Pollution Control (1.a ed.). NJ, USA: Wiley. de 100 Nie, E., Wang, D., Yang, M., Luo, X., Fang, C., Yang, X. y Zheng, Z. (2015). Tower bio-vermifilter system for rural wastewater treatment: benchscale, pilot-scale, and engineering applications. International Journal of Environmental Science and Technology, 12(3), 1053–1064. doi.org/10.1007/s13762-013-0479-6 Oré, M., Castillo, L., Orsel, S. y Vos, J. (2009). El agua, ante nuevos desafíos: actores e iniciativas en Ecuador, Perú y Bolivia. Recuperado el 4 de mayo de 2015 de http://library.fes.de/pdf-files/bueros/quito/07715.pdf Palta, G. y Morales, S. (2013). Fitodepuración de Aguas Residuales Domésticas con Poaceas: Brachiaria mutica, Pennisetum purpureum y Panicum maximun en el Municipio de Popayán, Cauca. Biotecnología En El Sector Agropecuario Y Agroindustrial, 11(2). Paredes, P. (2010). Calidad de las Aguas del Ecuador (No. 1). Ecuador: ECAPAG. Recuperado el 19 de abril de 2015 de http://www.pnuma.org/aguamiaac/CODIA%20CALIDAD%20DE%20LA S%20AGUAS/MATERIAL%20ADICIONAL/PONENCIAS/PARTICIPAN TES/Ecuador/CALIDAD%20AGUAS-ECUADOR.pdf Piérart, I. y Rojas, G. (2013). Modelo integrado de un sistema de biodepuración en origen de aguas residuales domiciliarias. Una propuesta para comunidades periurbanas del centro sur de Chile. Revista Gestión Y Ambiente, 16(3), 39–51. PNUMA. (2015). Implementación de mejoras para la calidad del agua y la protección de servicios ecosistémicos. Recuperado el 22 de marzo de 2015http://www.un.org/spanish/waterforlifedecade/waterandsustainable development2015/pdf/04%20risk_water_quality_esp_web.pdf Rao, D., Senthilkumar, R., Byrne, J. y Feroz, S. (2012). Wastewater Treatment : Advanced Processes and Technologies (1.a ed.). Hoboken, USA: Taylor and Francis. Reynolds, K. (2012). Tratamiento de Aguas Residuales en Latinoamérica. Identificación del Problema. Recuperado el 11 de abril de 2015 de http://www.agualatinoamerica.com/docs/pdf/DeLaLaveSepOct12.pdf 101 Robbins, D. y Ligon, G. (2014). How to Design Wastewater Systems According to Local Conditions (1.a ed.). London, United Kingdom: IWA Publishing. Rodríguez, I. y Lozano, W. (2012). Preparación, composición y uso de agua residual sintética para alimentación de reactores prototipo y de laboratorio. Revista de Didáctica Ambiental, 24, 10–16. RohitPathania, C. y Suresh, R. (2012). A review of vermifiltration and related low cost alternatives for waste water management. Recuperado el 13 de abril de 2015 de http://fosetonline.org/ENV/16-EVH_ROHIT.pdf Sandoval, D. y Cisneros, V. (2012). Tratamiento de aguas servidas en lagunas de oxidación para una población de 10000 habitantes. Recuperado el 11 de abril de 2015 de http://repositorio.ug.edu.ec/handle/redug/5039 Sekhar, R., Sruthi, L. y Kumar, S. (2014). Performance Evaluation of Sewage Treatment plant at a Point Source of Hussain sagar Lake Watershed. International Journal of Emerging Trends in Engineering and Development, 2(4), 415–420. Sharma, S. y Sanghi, R. (2012). Wastewater Reuse and Management (1.a ed.). Dordrecht, Holanda: Springer. Singh, D. y Dwivedi, S. K. (2009). Environmental Microbiology and Biotechnology. The Environmentalist, 27(4), 95–118 Singh, J. y Kaur, A. (2015). Vermicompost as a strong buffer and natural adsorbent for reducing transition metals, BOD, COD from industrial effluent. Ecological Engineering, 74, 13–19. doi.org/10.1016/j.ecoleng.2014.10.028 Sinha, R., Herat, S., Valani, D. y Chauhan, K. (2010). Earthworms–the environmental engineers: review of vermiculture technologies for environmental management and resource development. International Journal of Global Environmental doi.org/10.1504/IJGENVI.2010.037271 Issues, 10(3), 265–292. 102 Sinha, R., Bharambe, G. y Chaudhari, U. (2008). Sewage treatment by vermifiltration with synchronous treatment of sludge by earthworms: a low-cost sustainable technology over conventional systems with potential for decentralization. The Environmentalist, 28(4), 409–420. doi.org/10.1007/s10669-008-9162-8 Sinha, R., Patel, U., Soni, B. y Li, Z. (2014). Earthworms for safe and useful management of solid wastes and wastewaters, remediation of contaminated soils and restoration of soil fertility, promotion of organic farming and mitigation of global warming: A review. Journal of Environment and Waste Management, 1(1), 11–25. Spalletti, L. (2007). Textura de las rocas sedimentarias clásticas. Recuperado el 18 de julio de 2015 de http://www.fcnym.unlp.edu.ar/catedras/sedimentologia/pdf/textura.pdf Stephens, A. y Fuller, M. (2009). Waste and Waste Management : Sewage Treatment: Uses, Processes and Impact (2.a ed.).NY, USA: Nova Science Publishers Tiwari, B. (2009). Sewage Pollution and Microbiology (1.a ed.). New Delhi, India: Swastik Publishers & Distributors. Tomar, P. y Suthar, S. (2011). Urban wastewater treatment using vermibiofiltration system. Desalination, 282, 95–103. doi.org/10.1016/j.desal.2011.09.007 Tomás-Sábado, J. (2010). Fundamentos de bioestadística y análisis de datos para enfermería. Recuperado el 12 de junio de 2015 de http://publicacions.uab.es/pdf_llibres/TRII002.pdf Toole, G., Kaplan, H. y Kolter, R. (2010). Biofilm Formation as Microbial Development. Annual Review of Microbiology, 54, 49–79. doi.org/10.1146/annurev.micro.54.1.49 Torres, C. (2006). Procedimiento para la Medición de Sólidos Totales. Recuperado el 18 de mayo de 2015 de http://www.utp.ac.pa/sites/default/files/PCUTP-CIHH-LSA-211-2006.pdf 103 Torres, P. (2013). Perspectivas del Tratamiento Anaerobio de Aguas Residuales Domésticas en Países en Desarrollo. Revista EIA, 9(18), 115–129. TULSMA. (2003). Registro Oficial 51 de 31 de marzo de 2003. Vega, R. (2009). Diagnóstico de la temática de gestión integral del recurso hídrico. Recuperado el 24 de marzo de 2015 de http://app.sni.gob.ec/snilink/sni/RESPALDOS/R_PLANIF/consultoria%20agua%20raul%20vega /Exp_Diagn%C3%B3stico+Lineamientos_11feb10.ppt Velásquez, J. (2008). Guía para la cría, manejo y aprovechamiento sostenible de algunas especies animales promisorias y otras domésticas. Recuperado el 2 de abril de 2015 de https://www.google.com.ec/url?sa=t&rct=j&q=&esrc=s&source=web&cd =1&cad=rja&uact=8&ved=0CB0QFjAAahUKEwjvjoCivsjHAhXDpx4KHbt kD_U&url=https%3A%2F%2Fbooks.google.com Vera, D. (2011). Elementos de Geología-Rocas sedimentarias. Recuperado el 20 de julio de 2015 de http://www0.unsl.edu.ar/~geo/materias/Elementos_de_Geologia/docum entos/contenidos/apoyo_teorico/APU-2011-Rocas-Sedimentarias.pdf Villavicencio, A. y Villablanca, A. (2010). Métodos de aforos de caudal. Recuperado el 20 de mayo de 2015 de http://platina.inia.cl/ururi/informativos/Informativo_INIA_Ururi_50.pdf Vincent, W. (2012). The Complete Guide to Working with Worms: Using the Gardener’s Best Friend for Organic Gardening and Composting (2.a ed.). Florida, USA: Atlantic Publishing Company. Visvanathan, C., Traenklar, Vermicomposting management. as J., Kurian, J. an eco-tool Recuperado el 14 in y Nagendran, R. (2009). sustainable de julio de http://dste.puducherry.gov.in/envisnew/books&reports8.pdf solid waste 2015 de 104 Wang, L., Guo, Z., Che, Y., Yang, F., Chao, J., Gao, Y. y Zhang, Y. (2014). The effect of vermifiltration height and wet:dry time ratio on nutrient removal performance and biological features, and their influence on nutrient removal efficiencies. Ecological Engineering, 71, 165–172. doi.org/10.1016/j.ecoleng.2014.07.018 Watnick, P.y Kolter, R. (2008). Biofilm, City of Microbes. Journal of Bacteriology, 182(10), 2675–2679. WTW. (2006). WTW Operating Manual System Oxitop Control. Recuperado el 19 de mayo de 2015 de http://www.globalw.com/downloads/WQ/oxitop_oc_100.pdf Yang, J., Zhang, J. y Xing, M. (2014). Insight into the roles of earthworm in vermicomposting of sewage sludge by determining the water-extracts through chemical and spectroscopic methods. Bioresource Technology, 154, 94–100.doi.org/10.1016/j.biortech.2013.12.023 Yang, L., Liu, Y., Wu, H., Hoiby, N., Molin, S. y Song, Z. (2011). Current understanding of multi-species biofilms. International Journal of Oral Science, 3(2), 74–81.doi.org/10.4248/IJOS11027 105 ANEXOS ANEXO 1: Agua residual sintética. Para alimentar los vermifiltros se empleó agua residual sintética la cual contenía la concentración de contaminantes característicos del agua residual doméstica. Para formularla se tomó como referencia la composición del sustrato sintético planteado por el Departamento de Ingeniería Química de la Universidad de Valencia y se realizaron modificaciones de acuerdo a los rangos de parámetros físicos y químicos deseados. (Méndez, Miyashiro, Rojas, Cotrado, y Carrasco, 2004, p. 78; Rodríguez y Lozano, 2012, p. 12) Para efectos del experimento se emplearon dos variaciones de la formulación del sustrato sintético. Con el fin de obtener una concentración fuerte y otra media del agua residual doméstica descrita en la Tabla 1 se utilizaron las siguientes cantidades de compuestos. Tabla 25. Fórmula del agua residual sintética Formulación 1 (g/l) Formulación 2 (g/l) Almidón 0,1000 Almidón 0,05000 Azúcar 0,1710 Azúcar 0,08550 Bicarbonato 0,1504 Bicarbonato 0,07520 Gelatina 0,0342 Gelatina 0,01710 Jabón 0,0030 Jabón 0,00150 KH2O4 0,0440 KH2O4 0,02200 Leche en polvo 0,2000 Leche en polvo 0,10000 MgSO4 0,0033 MgSO4 0,00165 (NH4)2SO4 0,0744 (NH4)2SO4 0,03720 ANEXO 2: Materiales empleados en la construcción del sistema experimental. Módulo Característica Tanque homogenizador -Tanque de polietileno con una capacidad de 55 galones. -2 metros de tubería de pvc plastigama de Vermifiltros 20 cm de diámetro -6 agarraderas metálicas -1 metro de malla -6 m de tubería para agua caliente de ½ pulgada. Sistema de transporte del -Accesorios: codos de ½ pulgada, uniones agua residual de ½ pulgada, extensiones de de ½ pulgada, neplos - 4 válvulas bola. Cubierta -Vidrio de 4 mm de espesor cubierto con una lona de pvc blanca reciclada. -Termostato JAD de 75 W para mantener Equipo Adicional condiciones de temperatura en el tanque homogenizador. ANEXO 3: Medidas del sistema experimental. Vista Frontal (Unidad: mm) Vista Superior (Unidad: mm) Vista lateral (Unidad: mm) Anexo 4: Diagrama del proceso de descompactación de la fibra de coco. Fibra de coco 7,5 kg Descompactación Ropa de cama para el vermifiltro 2 Explicación: proceso de descompactación de la fibra de coco mediante hidratación Anexo 5: Sistema experimental. Anexo 6: Colocación de los estratos en los vermifiltros. Anexo 7: Ropa de cama de los vermifiltros. Suelo Aserrín Fibra de coco Anexo 8: Ubicación del tanque homogenizador. Anexo 9: Equipos empleados en las mediciones. Turbidimeter de Hanna Instruments Fotómetro Macherey-Nagel Nanocolor Termómetro de Control Company Oxitop IS 6 Turbidímetro de Hanna Instruments pHmetro HI 99121 Anexo 10: Medición de la turbidez en el turbidímetro. Anexo 11: Análisis de parámetros químicos. Anexo 12: Medición de parámetros químicos mediante fotometría. Anexo 13: Medición de la porosidad de los agregados. Anexo 14: Medición de la temperatura en la capa uno. Anexo 15: Resultado de textura del suelo. Anexo 16: Límites de descarga a un cuerpo de agua dulce. Parámetros Expresado como Aldehídos Unidad mg/l Límite máximo permisible 2,0 Aluminio Al mg/l 5,0 Arsénico total As mg/l 0,1 Bario Ba mg/l 2,0 Boro total B mg/l 2,0 Cadmio Cd mg/l 0,02 Cianuro total CN- mg/l 0,1 Cloro Activo Cl mg/l 0,5 Cloroformo Extracto carbón cloroformo ECC mg/l 0,1 Cloruros Cl- mg/l 1 000 Cobre Cu mg/l 1,0 Cobalto Co mg/l 0,5 Coliformes Fecales 1 Nmp/100 ml Remoción > al 99,9 % Compuestos fenólicos Fenol mg/l 0,2 Cromo hexavalente Cr+6 mg/l 0,5 Demanda Bioquímica de Oxígeno (5 días) D.B.O5. mg/l 100 Demanda Química de Oxígeno D.Q.O. mg/l 250 Dicloroetileno mg/l 1,0 Dicloroetileno Parámetros Expresado como Unidad Sn mg/l Límite máximo permisible 5,0 Fluoruros F mg/l 5,0 Fósforo Total P mg/l 10 Hierro total Fe mg/l 10,0 TPH mg/l 20,0 Manganeso total Mn mg/l 2,0 Materia flotante Visibles Estaño Hidrocarburos Totales de Petróleo Ausencia Mercurio total Hg mg/l 0,005 Níquel Ni mg/l 2,0 Expresado como Nitrógeno (N) mg/l 10,0 Nitrógeno Total N mg/l 15 Organoclorados totales Concentración de organoclorados mg/l 0,05 Organofosforados totales Concentración de organofosforados totales. mg/l 0,1 Plata Ag mg/l 0,1 Plomo Pb mg/l 0,2 Potencial de hidrógeno pH Selenio Se Nitratos + Nitritos Sólidos Sedimentables 5-9 mg/l 0,1 ml/l 1,0 Parámetros Expresado como Unidad Sólidos Suspendidos Totales mg/l Límite máximo permisible 100 Sólidos totales mg/l 1 600 Sulfatos SO4= mg/l 1000 Sulfitos SO3 mg/l 2,0 Sulfuros S mg/l 0,5 Temperatura Tensoactivos o C Sustancias activas al azul de metileno < 35 mg/l 0,5