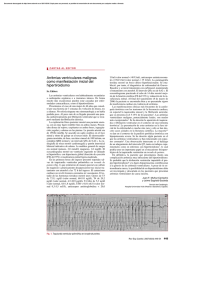
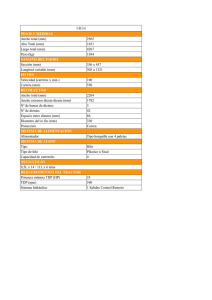
emergencias 2003;15:116-119 Nota clínica Torsade de pointes secundario al uso de tioridazina J.A. Martínez Vidal*, N. Martínez Velasco**, J. Mozota Duarte***, R. Cuartero Gutiérrez**, I. Gil Romea***, C. Pérez-Aradros Hernández*** *SERVICIO DE URGENCIAS DEL CENTRO COMARCAL DE EL VENDRELL (TARRAGONA). **MEDICINA FAMILIAR Y COMUNITARIA. ***SERVICIO DE URGENCIAS DEL HOSPITAL CLÍNICO UNIVERSITARIO "LOZANO BLESA" DE ZARAGOZA. RESUMEN ABSTRACT a Torsade de Pointes (TdP) es una taquiarritmia maligna que se caracteriza por un movimiento en forma helicoidal de sus complejos QRS alrededor de su eje isoeléctrico, que puede aparecer de manera adquirida o congénita, siendo fundamental el tratamiento de la causa desencadenante. La sobredosificación y/o la asociación de diversos fármacos de uso habitual son factores determinantes que pueden inducir esta taquiarritmia. Presentamos el caso de una paciente de 70 años que, tras la toma de tioridazina, sufrió una TdP. Torsade de pointes as a secondary effect to the use of thioridazine L Palabras clave: Torsade de Pointes. Tioridazina. Sulfato de Magnesio. orsade de Pointes (TdP) is a malign tachyarrhythmia characterised by an helicoidal movement of its QRS complexes around its isoelectric axis. It can appear in a congenital or acquired manner, and the treatment of the setting-out cause is fundamental. Overdosage and/or the association of several drugs normally used are determining factors capable of inducing this tachyarrythmia. We introduce a report about a seventy-year old patient that suffered a TdP after taking thioridazine. T Key Words: Torsade de Pointes. Thioridazine. Magnesium sulphate. INTRODUCCIÓN CASO CLÍNICO La Torsade de Pointes (TdP) es una variedad de taquicardia ventricular (TV) polimorfa que se caracteriza por un movimiento en forma helicoidal de sus complejos QRS alrededor del eje isoeléctrico y con una frecuencia que oscila entre 200250 latidos por minuto; suele iniciarse tras un R-R alargado (normalmente la pausa compensadora de un extrasístole ventricular) y suelen ser no sostenidas y recurrentes, en salvas, aunque a veces se prolongan y degeneran en una fibrilación ventricular. Por todo ello, son consideradas como arritmias malignas1. El principal mecanismo desencadenante es la prolongación del intervalo QT, que puede aparecer de una forma adquirida o congénita. Exponemos el caso clínico de una mujer de 70 años que presentó una TdP secundaria al tratamiento crónico con un psicofármaco (tioridazina). Paciente mujer de 70 años de edad sin alergias medicamentosas conocidas y con antecedentes personales de HTA leve, diabetes mellitus tipo 2 y esquizofrenia paranoide, en tratamiento actual con acarbosa 50 mg cada 8 horas y tioridazina: 75 mg en el desayuno y 165 mg en la cena. Acudió a su centro de salud con clínica de mareo de dos meses de evolución y en los últimos días fiebre de 38º C, temblor y dolor precordial leve. Se le monitorizó y a los pocos minutos sufrió perdida de conciencia, observándose en la tira de ritmo (nº 1) una arritmia diagnosticada en ese momento como taquicardia ventricular sin pulso (TV sin pulso) o una fibrilación ventricular (FV). Como tratamiento inicial recibió golpe precordial y masaje cardíaco externo con lo que revirtió la arritmia, tras lo cual, la paciente es trasladada en una UVI- Correspondencia: J.A. Martínez Vidal. C/Garraf 72, casa 30. 43700 El Vendrell, Tarragona. E-mail: [email protected] 116 Fecha de recepción: 21-6-2002 Fecha de aceptación: 26-3-2003 J.A. Martínez Vidal, et al TORSADE DE POINTES SECUNDARIO AL USO DE TIORIDAZINA móvil al hospital de referencia con una perfusión de lidocaína a un ritmo de 2 mg/minuto. A su llegada al Servicio de Urgencias de dicho hospital, la paciente se encontraba consciente, desorientada, normocoloreada, con flogosis (edema y eritema) en la extremidad inferior izquierda y fiebre de 39º C. Auscultación cardíaca: ruidos cardíacos rítmicos con soplo sistólico tricuspídeo 2/6 y sistólico pulmonar 3/6. Auscultación respiratoria: crepitantes inspiratorios en la base izquierda. Extremidad inferior izquierda: signos de celulitis a nivel de la pantorrilla. Mientras permanece en el Servicio de Urgencias, la paciente es monitorizada presentando frecuentes salvas de extrasístoles ventriculares, pasando posteriormente a una situación de TV sin pulso, precisando de una primera desfibrilación a 200 julios sin éxito, seguida de una segunda desfibrilación a 300 Julios (tira de ritmo nº 2), revirtiendo a ritmo sinusal con extrasístoles ventriculares frecuentes. Se suspende la perfusión de lidocaína y se le administran 3 gramos endovenosos de sulfato de magnesio. Finalmente, la paciente es trasladada a la Unidad de Cuidados Intensivos (UCI) de dicho hospital con un ritmo sinusal. Durante su estancia (6 días) en la UCI, la paciente es tratada con un marcapasos provisional, estimulando a una frecuencia cardíaca de 100 latidos por minuto (lpm) y manteniéndose la sobreestimulación durante unas 22 horas, sulfato de magnesio: 6 gs cada 24 horas durante 4 días, antibióticos, insulina, heparina de bajo peso molecular y se le sustituye la tioridazina por haloperidol: 4 mg por la noche, presentando buena evolución de su estado clínico. El ECG (nº 1) del primer día en la UCI mostraba una frecuencia cardíaca de 53 lpm, correspondiéndole un QT corregido (QTc) de 0,41 segundos, siendo su QT real de 0,64 segundos, bloqueo incompleto de la rama derecha del haz de Hiss (BIRDHH), hemibloqueo anterosuperior de la rama izquierda del haz de Hiss (HASRIHH) y signos de sobrecarga del ventrículo derecho. Al alta de la UCI, el electrocardiograma (ECG) tenía una frecuencia de 76 lpm que le corresponde un QTc de 0,36 segundos y con un QT real de 0,40 segundos. Tras ser trasladada al Servicio de Cardiología, se objetivan rachas aisladas de TV, por lo que se sospecha que pudieran estar relacionadas con la toma del haloperidol2. Se sustituye éste por risperidona: 1 mg/8 horas, tras lo cual pasa a ritmo sinusal con un QTc de 0,35 segundos a una frecuencia cardíaca de 78 lpm (su QT real es de 0,42 segundos) y estando la paciente asintomática. Durante su estancia en el Servicio de Cardiología, se le realiza un ecocardiograma que muestra una fracción de eyección de un 62%, ligero derrame pericárdico e HVI concéntrica. Hormonas tiroideas: hipertiroidismo subclínico con cifras de TSH: 0.196 µU/ml (0,35-4,94), T3 libre: 2,65 pg/ml (1,71-3,71) y T4 libre: 1,53 ng/ml (0,7-1,48). También se le realizó el estudio del dímero D cuyo resultado fue negativo. Tras la realización de las diversas pruebas complementarias, se descarta que la arritmia (Taquicardia Ventricular tipo Torsade de Pointes) sea provocada por patología orgánica, llegándose al diagnóstico de arritmia secundaria inducida por la toma de tioridazina. El ECG al alta del Servicio de Cardiología (12 días desde el ingreso) presentaba un ritmo sinusal a 100 lpm, QTc de 0,32 segundos y un QT real de 0,38 segundos, BIRDHH y un HASRIHH. DISCUSIÓN El síndrome del QT largo se caracteriza por la prolongación y/o anormalidades del segmento QT y la onda U, con frecuentes episodios de síncope y muerte súbita, asociados a una arritmia típica como la taquicardia ventricular polimórfica Torsade de Pointes3. La duración del intervalo QT depende en gran parte de la corriente de potasio que sale de la célula miocárdica a través de los canales de potasio y que se corresponde con la fase 3 del potencial de acción. Cuando se bloquea la salida de potasio se alarga el potencial de acción y se retrasa la repolarización dando un QT largo. La TdP síndrome clínico-electrocardiográfico3 cuya morfología típica es la de una taquicardia de complejos ventriculares polimórficos que varían de amplitud y polaridad de latido a latido y que parecen girar alrededor de la línea isoeléctrica, pero donde es necesario hacer el registro simultáneo de varias derivaciones para reconocerla, ya que esta morfología puede no objetivarse en todas las derivaciones. Para ello, debemos hacer el diagnostico diferencial3,4 con: 1. Otras taquicardias ventriculares polimórficas que aparecen en el curso de: isquemia aguda, infarto agudo de miocardio, angina variante, infarto crónico sin repolarización prolongada y la inducida por estimulación programada. 2. Con la FV de etiología distinta a la degeneración de una TdP real. 3. TV con enfermedad cardíaca estructural, que engloba a los pacientes con TV y enfermedad coronaria, miocardiopatía hipertrófica y/o dilatada y la displasia arritmogénica del ventrículo derecho. 4. TV del tracto de salida del VD, TV del tracto de salida del VI y las TV fasciculares o idiopáticas. 5. TV en el síndrome de Brugada. 6. Taquicardias supraventriculares (TSV) con conducción aberrante, dos o más TV simultáneas, extrasistolia multifocal y la taquicardia dual: TV+TSV con períodos de fusión. El Síndrome del QT largo se puede clasificar de dos formas: síndromes adquiridos o "pausa dependiente" y los síndromes congénitos o "adrenérgicos". 117 emergencias 2003;15:116-119 TABLA 1. Causas del síndrome QT largo "adquirido" 1. Drogas antiarrítmicas: a. Drogas clase Ia con propiedades clase III: quinidina, procainamida y disopiramida. b. Drogas clase III: amiodarona, sotalol, bretílio. 2. Bradiarritmias: bloqueo A-V completo y disfunción del seno sinusal. 3. Alteraciones electrolíticas: hipopotasemia, hipocalcemia, hipomagnesemia. 4. Psicofármacos: fenotiazinas, antidepresivos tricíclicos y tetracíclicos, haloperidol. 5. Agentes antihipertensivos: bepridilo, lidoflazine, prenilamina, ketanserina. 6. Antimicrobianos: eritromicina, claritromicina, troleandomicina, cloroquina, amantidina, pentamidina, trimetoprim-sulfametoxazol. 7. Antifúngicos: ketoconazol, itraconazol, metronidazol, fluconazol. 8. Antihistamínicos: terfenadina, astemizol, loratadina, acrivastina, ceteridina. 9. Otras: cocaína, insecticidas organofosforados, arsénico, vasopresina, diuréticos tiazídicos, cimetidina, cisaprida, flavonoides del zumo de pomelo, dieta líquida proteica, inanición. 10. Alteraciones cardiacas: miocarditis, tumor ventricular, cardiopatía isquémica, insuficiencia cardíaca. 11. Alteraciones endocrinas: acidosis, hiperparatiroidismo, hiperaldosteronismo, hipotiroidismo y feocromocitoma. 12. Alteraciones intracraneales: hemorragia subaracnoidea, accidente cerebro-vascular, encefalitis. Los síndromes congénitos se dividen en: Síndrome de Romano-Ward, que se transmite de manera autonómica dominante y cursa sin sordera y el Síndrome de Jerwell y LangeNielsen, de herencia recesiva asociado con sordera congénita y menos frecuente pero más grave que el anterior. En los síndromes adquiridos o "pausa dependiente" se produce una contracción ventricular prematura cercana al próximo complejo QRS normal y seguido por una pausa. El siguiente latido sinusal se inicia cerca de otra contracción ventricular prematura, lo cual desencadena la TdP 5 . Este mecanismo es el más frecuente asociado a drogas6, principalmente antiarrítmicos (Tabla 1). Con respecto al tratamiento del síndrome QT largo congénito, la terapia de elección es la antiadrenérgica7, donde usaremos principalmente los beta-bloqueantes (son particularmente efectivos en los pacientes que presentan mutaciones que involucran a los canales de potasio), tales como el propanolol y el nadolol a las dosis máximas tolerables. En el tratamiento de los síndromes adquiridos, suele bastar con la identificación y supresión del fármaco y/o tóxicos causantes de la prolongación del intervalo QT y la modificación de los factores de riesgo que contribuyan a agravar esta 118 anormalidad. Cuando los episodios son frecuentes y de difícil manejo, se debería recurrir a la colocación de un marcapasos definitivo. Con respecto al tratamiento para la taquicardia ventricular polimórfica tipo Torsades de Pointes, debemos considerar, en primer lugar, que a pesar de que en la mayoría de las ocasiones son episodios breves y autolimitados, pueden evolucionar hacia una fibrilación ventricular, lo que precisará de una desfibrilación para intentar revertir a ritmo sinusal, teniendo en cuenta que es una arritmia altamente recurrente, pudiendo repetirse sucesivamente los episodios hasta lograr controlar el episodio con otras medidas terapéuticas. En segundo lugar deberemos intentar suprimir la aparición de los extrasístoles ventriculares con la administración de sulfato de magnesio8, el cual disminuye la amplitud de la extrasistolia ventricular por bloqueo en la corriente del calcio. Simultáneamente con la administración del magnesio, se deberían administrar también suplementos de potasio9,10 para aumentar los niveles de potasio en sangre > 4.5 meq/l, con lo que se consigue un acortamiento en la repolarización ventricular (intervalo QT). La lidocaína9-13 también puede suprimir los extrasístoles ventriculares por bloqueo de la corriente de entrada tardía de sodio, acortando la repolarización ventricular (intervalo QT), pero solamente en el 50% de los casos de TdP responden, por lo que la lidocaína solamente debería ser administrada junto al sulfato de magnesio y el potasio cuando éstos no sean eficaces. En tercer lugar, deberemos aumentar la frecuencia cardíaca a un ritmo de 100-140 lpm con la colocación de un marcapasos9,10, con lo que se consigue un acortamiento del intervalo QT y de la pausa postextrasistólica. Si no disponemos de un marcapasos, podemos administrar isoproterenol10,14 hasta alcanzar una frecuencia cardíaca elevada de 100-140 lpm para evitar la aparición de extrasístoles ventriculares y acortando el intervalo QT. En nuestro caso, el uso de neurolépticos a altas dosis indujo una prolongación del intervalo QT que desencadenó una taquicardia ventricular tipo TdP15, precisando desfibrilación con 300 Julios y la administración de sulfato de magnesio intravenoso para conseguir un ritmo sinusal estable. Concluimos que la prevención pasa por un profundo conocimiento de los fármacos que utilizamos, ya que, aunque a dosis terapéuticas algunos fármacos pueden producir TdP, este riesgo se incrementa en la sobredosificación y la existencia de patologías previas (síndromes congénitos, bradiarritmias, hipopotasemia, etc.), así como por la asociación de diversos fármacos (incluyendo los inhibidores del citocromo P450) tales como la eritromicina, antidepresivos tricíclicos, antifúngicos, antihistamínicos, etc. que son de uso habitual por el médico para el tratamiento de las enfermedades más comunes. J.A. Martínez Vidal, et al TORSADE DE POINTES SECUNDARIO AL USO DE TIORIDAZINA BIBLIOGRAFÍA 1- López Gil M, Arribas Ynsaurriaga F. Arritmias. En: Medina Asensio J, editor. Manual de Urgencias Médicas. 2ª ed. Madrid: Díaz de Santos, S.A.; 1997;383-84. 2- Jackson T, Ditmanson L, Phibbs B. Torsade de Pointes and low-dose oral haloperidol. Arch Intern Med 1997;157:2013-5. 3- Torsade de pointes (fecha de acceso 03 de febrero de 2003). URL disponible en: http://orbita.starmedia.com/~ahpsm/tdp.htm 4- Montón Rodríguez AJ. Taquicardias ventriculares. Diagnóstico y tratamiento (fecha de acceso 03 de febrero de 2003). URL disponible en: http://www.uninet.edu/cimc2000/conferencia/conf45/monton.htm 5- Morganroth, J Relations of QT interval prolongation on the electrocardiogram to torsades de pointes: definicions and mechanism. Am J Cardiol 1993;72:10B-13B. 6- Drugs with Risk of Torsades de Pointes (fecha de acceso 03 de febrero de 2003). URL disponible en: http://www.torsades.org/medical-pros/druglists/list-01.cfm 7- Schwartz PJ, Locati E, Moss AJ. Left cardiac sympathetic denervation in the therapy of the congenital long Q-T síndrome. A worldwide report. Circulation 1991;804:503-11. 8- Tzivoni D, Banai S, Schuger C. Treatment of torsade de pointes with magnesium sulfate. Circulation 1988;77:392-97. 9- Syed Nacer, MD. Torsade de pointes (fecha de acceso 04 de febrero de 2003). URL disponible en: http://www.emedicine.com/med/topic2286.htm 10- Viskin S, Fish R, Roden D. Drug-Induced Torsades de Pointes (fecha de acceso 04 de febrero de 2003). URL disponible en: http://www.ehs.net/2235/handouts/DrugInduced%20Torsades%20de%20Pointes.pdf 11- Shimizu W, Kurita T, Matsuo K, et al. Improvement of repolarization abnormalities by a K+ channel opener in the LQT1 form congenital longQT syndrome. Circulation 1998;97:1581-8. 12- Richardson B. Recent changes in the Cardiac Life Support Guidelines (fecha de acceso 04 de febrero de 2003). URL disponible en: http://www.emedmag.com/html/pre/cov/covers/071501.asp 13- Guidelines 2000 for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. An International Consensus on Science. The American Heart Association in collaboration with the International Liaison Committee on Resuscitation. Circulation 2000;102:1-252. 14- Viskin S, Belhassen B. Polymorphic ventricular tachyarrhythmias in the absence of organic heart disease. Classification, differential diagnosis and implications for therapy. Prog Cardiovasc Dis 1998;41:17-34. 15- Hulisz DT, Dasa SL, Black LD, Heiselman DE. Complete heart block and torsade de pointes associated with thioridazine poisoning. Pharmacotherapy 1994;14:239-45. 119
 0
0
Anuncio
Documentos relacionados
Descargar
Anuncio
Añadir este documento a la recogida (s)
Puede agregar este documento a su colección de estudio (s)
Iniciar sesión Disponible sólo para usuarios autorizadosAñadir a este documento guardado
Puede agregar este documento a su lista guardada
Iniciar sesión Disponible sólo para usuarios autorizados