Resección endoscópica de cáncer colorrectal temprano como único
Anuncio

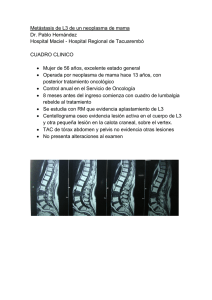
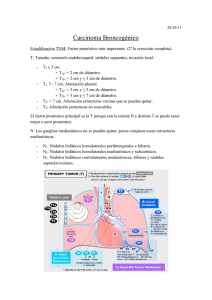
10. PDV 1750 - J. RUIZ TOVAR -:Maquetación 1 1130-0108/2010/102/7/435-441 REVISTA ESPAÑOLA DE ENFERMEDADES DIGESTIVAS Copyright © 2010 ARÁN EDICIONES, S. L. 5/7/10 08:37 Página 435 PUNTO DE VISTA REV ESP ENFERM DIG (Madrid) Vol. 102. N.° 7, pp. 435-441, 2010 Resección endoscópica de cáncer colorrectal temprano como único tratamiento J. Ruiz-Tovar1, J. Jiménez Miramón2, A. Valle2 y M. Limones2 Servicio de Cirugía General y del Aparato Digestivo. Hospital General Universitario de Elche. Alicante. 2Servicio de Cirugía General y del Aparato Digestivo. Hospital Universitario de Getafe. Madrid 1 RESUMEN ABSTRACT El screening mediante colonoscopia que se realiza en países occidentales ha permitido la detección y resección de un número elevado de tumores colorrectales en estadio temprano. Existe una gran controversia a la hora de decidir cuándo el tratamiento endoscópico es suficiente y cuándo debe realizarse la resección quirúrgica. A ello contribuye la gran diversidad en la nomenclatura para definir estas lesiones, la amplia variedad de clasificaciones de las mismas y los diferentes criterios que tiene cada autor. Mediante una revisión extensa de la literatura, pretendemos aclarar conceptos, enlazar los datos de las diferentes clasificaciones y unificar unos criterios que sirvan de guía para el tratamiento del cáncer colorrectal temprano. Tras ello, llegamos a la conclusión de que en el cáncer colorrectal temprano que aparece en pólipos pedunculados (0-Ip), estaría indicada la resección endoscópica como único tratamiento en los niveles 1, 2 y 3 de Haggitt, tumores menores de 2 cm de diámetro, en tumores bien o moderadamente diferenciados, sin afectación vascular ni linfática, con infiltración de la submucosa menor de 1 µm desde la muscularis mucosae y anchura máxima en la submucosa menor de 4 µm y resecados en bloque. En las lesiones polipoideas sésiles (0-Is) y no polipoideas elevadas (0-IIa) o planas (0-IIb) las recomendaciones serían las mismas descritas anteriormente, no siendo aplicables los niveles de Haggitt. Colonoscopic screening in developed countries allows detection and resection of a great number of early colorectal cancers. There is a strong controversy to decide when endoscopic treatment is enough or when surgical resection is necessary. To this contributes the diverse names to define the lesions, the wide number of classifications and the different criteria of each author. We perform an extense literature review, aiming to clarify concepts and unify criteria that can be used as a guide for the treatment of early colorectal cancer. We conclude that in early colorectal cancer arising in pedunculated polyps (0-Ip), mucosal endoscopic resection would be indicated as only treatment in Haggitt levels 1, 2 and 3, tumors smaller than 2 cm, well- or moderately differentiated, without vascular or lymphatic affection, with submucosal infiltration lower than 1 µm from the muscularis mucosae and maximal submucosal width lower than 4 µm, and undergoing en bloc resection. In sessile polyps (0-Is) or non-polypoideal elevated (0IIa) or plain (0-IIb) lesions, recommendations will be similar, without applicability of Haggitt levels. Palabras clave: Cáncer colorrectal temprano. Pólipo maligno. Resección endoscópica definitiva. Key words: Early colorectal cancer. Malignant polyp. Definitive endoscopic resection. Ruiz-Tovar J, Jiménez Miramón J, Valle A, Limones M. Resección endoscópica de cáncer colorrectal temprano como único tratamiento. Rev Esp Enferm Dig 2010; 102: 435-441. INTRODUCCIÓN Los adenomas del tracto gastrointestinal pueden presentar transformación maligna siguiendo la secuencia Recibido: 29-12-09. Aceptado: 04-03-10. Correspondencia: Jaime Ruiz-Tovar. Corazón de María, 64, 7º J. 28002 Madrid. e-mail:[email protected] histopatológica adenoma-carcinoma. La mayoría de adenomas colónicos son considerados como precursores de carcinomas colorrectales. En la literatura se describe que entre 2-10% de adenomas van a evolucionar hacia carcinomas infiltrantes, valores que se elevan hasta el 85% cuando se trata de adenomas vellosos (1-4). El screening mediante el test de sangre oculta en heces y, sobre todo, mediante colonoscopia, que se ha introducido recientemente en países occidentales, ha permitido la 10. PDV 1750 - J. RUIZ TOVAR -:Maquetación 1 436 5/7/10 08:37 J. RUIZ-TOVAR ET AL. detección y resección de un número elevado de pólipos adenomatosos en estadios iniciales de la transformación neoplásica, previniendo su progresión a carcinoma infiltrante (4-8). Clásicamente se consideraba que la mayoría de adenomas colorrectales eran estructuras polipoideas fácilmente resecables endoscópicamente. Sin embargo, el número de lesiones colorrectales planas o deprimidas está aumentando en las últimas décadas, llegando a representar hasta el 38% de los adenomas colónicos (9). Aquellos pólipos mayores de 3 cm, que afectan a más de un tercio de la circunferencia o a dos haustras colónicas, o con morfología plana o deprimida son más difíciles de extirpar con la técnica clásica de polipectomía endoscópica, si bien con nuevos abordajes endoscópicos como la resección mucosa endoscópica ha aumentado el número de pólipos difíciles resecados, evitando así la cirugía en muchos casos (10). Las indicaciones de resección endoscópica o quirúrgica continúa siendo controvertida, si bien con el avance de las técnicas endoscópicas, cada vez se van ampliando las indicaciones de resección endoscópica y son menos los casos que requieren tratamiento quirúrgico. CONCEPTOS El término “pólipo maligno” se refiere a un pólipo adenomatoso macroscópicamente benigno, en cuyo estudio histológico se descubre un carcinoma infiltrante. La infiltración tumoral submucosa posibilita la invasión vascular y linfática, por lo que los pólipos malignos tienen la posibilidad de desarrollar metástasis ganglionares, en cuyo caso, la resección endoscópica no sería curativa (1,3). El término “cáncer colorrectal temprano” se definió en Japón como la presencia de células neoplásicas en mucosa o submucosa, independientemente de la presencia o ausencia de metástasis ganglionares (11). Estos tumores superficiales corresponden al estadio T1 de la clasificación TNM, en los que la infiltración tumoral está limitada a mucosa y submucosa. Estas lesiones, polipoideas o sésiles no suelen ser obstructivas, siendo habitualmente asintomáticas y diagnosticadas de forma incidental o por el screening (12). CLASIFICACIÓN MACROSCÓPICA Página 436 Diversas clasificaciones se han propuesto para definir los distintos tipos de lesiones polipoideas o sésiles y en función de ellas se han descrito diferentes indicaciones para la resección endoscópica de lesiones colónicas. La Sociedad Japonesa para estudio del cáncer de colon y recto dividió las formas de aparición del cáncer colo- REV ESP ENFERM DIG (Madrid) Tabla I. Clasificación macroscópica para el cáncer colorrectal precoz de la Sociedad Japonesa para el estudio del cáncer de colon y recto (13,14) Características endoscópicas Tipo Descripción Lesiones protruyentes Ip Isp Is IIa IIb IIc IIa + IIc IIc + IIa Pólipos pedunculados Pólipos semipedunculados Pólipos sésiles Elevación plana de la mucosa Cambios mucosos planos Depresión mucosa Elevación plana con depresión central Depresión mucosa con borde elevado Lesiones planas Lesiones deprimidas rrectal precoz en 3 categorías: protruyentes o polipoideas, elevadas planas y deprimidas (13,14) (Tabla I). Existe otro tipo de lesiones denominadas pólipos de extensión lateral que se caracterizan por ser de forma extensa y circunferencial en la pared colónica. Estas lesiones se subdividen en granulares y no granulares. Kudo y cols. (14) consideran que los adenomas planos pequeños pueden crecer hacia la luz colónica (crecimiento exofítico) para convertirse en pólipos pediculados, u horizontalmente para convertirse en lesiones de extensión lateral. Las lesiones deprimidas crecen en profundidad (crecimiento endofítico) y habitualmente se asocian con tumores invasivos incluso cuando el tamaño de la lesión es muy pequeño. A efectos de la práctica clínica, se consideraron inicialmente los pólipos pediculados como lesiones de bajo riesgo que podían ser manejadas endoscópicamente, mientras que las lesiones sésiles, planas, ulceradas o de extensión lateral eran catalogadas como lesiones de alto riesgo y recomendaban la resección quirúrgica como tratamiento definitivo (14), si bien posteriormente esto fue matizado en función del tamaño de la lesión, limitándose la indicación quirúrgica absoluta a las lesiones deprimidas mayores de 1 cm de diámetro, mientras que las lesiones planas, las de extensión lateral y las deprimidas menores de 1 cm podrían ser susceptibles de resección mucosa endoscópica (10). Según la clasificación de París, el tipo polipoideo presenta morfología pedunculada/semipedunculada (Tipo 0Ip) o sésil (0-Is). El tipo no polipoideo se divide en ligeramente elevado (0-IIa), completamente plano (0-IIb) o ligeramente deprimido sin úlceras (0-IIc). Las lesiones ulceradas o excavadas (0-3) son prácticamente inexistentes para ellos (15) (Tabla II). Siguiendo esta clasificación, serían susceptibles de resección mucosa endoscópica lesiones tipo (0-IIa) y (0-IIb) menores de 2 cm y (0-IIc) menores de 1 cm, no siendo recomendable en aquellas deprimidas o ulceradas (0-3) (16,17). Estas clasificaciones se siguen utilizando como guías útiles para distinguir lesiones susceptibles de tratamiento endoscópico de las que no lo son. No obstante, no existe ninguna considerada como clasificación estándar, lo que conlleva a diferencias importantes en la definición e interpretación de las lesiones. REV ESP ENFERM DIG 2010; 102 (7): 435-441 10. PDV 1750 - J. RUIZ TOVAR -:Maquetación 1 Vol. 102. N.° 7, 2010 5/7/10 08:37 Página 437 RESECCIÓN ENDOCÓPICA DE CÁNCER COLORRECTAL TEMPRANO COMO ÚNICO TRATAMIENTO 437 Tabla II. Clasificación endoscópica de París de las lesiones neoplásicas gastrointestinales superficiales (15) Características endoscópicas Tipo Descripción Lesiones polipoideas 0-Ip 0-Is 0-IIa 0-IIb 0-IIc 0-3 Pólipos pedunculados Pólipos sésiles Superficial elevada Completamente plana Superficial, deprimida sin ulceración Excavadas y ulceradas Lesiones no polipoideas Lesiones no polipoideas excavadas CLASIFICACIÓN MICROSCÓPICA Haggitt y cols. clasificaron el cáncer colorrectal temprano en lesiones de tipo pediculado y sésil. Los pólipos pediculados tienen tallos con longitudes mayores que su diámetro, mientras que las sésiles no. El tallo está compuesto por mucosa normal, muscularis mucosae y un área central de tejido submucoso. La unión entre el tallo y la cabeza es un punto habitual de transición de epitelio normal a adenomatoso y se denomina cuello. Los linfáticos acompañan a la submucosa por el tallo hasta la cabeza. Haggitt estratificó los pólipos en función del grado de invasión (Tabla III), que es el factor pronóstico más importante de los carcinomas que aparecen sobre pólipos adenomatosos. Los niveles de invasión 1, 2 y 3 presentan bajo riesgo de metástasis ganglionares y pueden ser tratadas mediante resección endoscópica (18) (Fig. 1). Fig. 1. Clasificación de Haggitt (18). Tabla III. Grado de invasión en lesiones polipoideas según Haggitt (18) Grado 0 Grado 1 Grado 2 Grado 3 Grado 4 Invasión mucosa por encima de la muscularis mucosae (carcinoma in situ) Invasión de la submucosa, pero limitado a la cabeza del pólipo Invasión de la submucosa del cuello Invasión de la submucosa de cualquier parte del tallo Invasión de la submucosa por debajo del tallo sin alcanzar la muscular propia Haggitt definió la invasión submucosa en los pólipos sesiles como grado 4 en todos y por tanto de mal pronóstico, independientemente de la afectación o no de los bordes de resección (18). A pesar de que la clasificación de Haggitt ha sido ampliamente empleada para evaluar la calidad de la excisión en las polipectomías endoscópicas, esta pierde utilidad en las lesiones no pediculadas, planas o deprimidas. La clasificación más aceptada para estas lesiones es la de Kikuchi y cols., que cuantifica el grado de invasión vertical y horizontal de la submucosa; se divide la submucosa en tercio superior (Sm1), tercio medio (Sm2) y tercio inferior (Sm3) (Fig. 2). A su vez, el tercio REV ESP ENFERM DIG 2010; 102 (7): 435-441 Fig. 2. Clasificación de Kikuchi (19). superior (Sm1) se divide en 3 subtipos según el compromiso horizontal en relación con el tamaño del tumor (19) (Tabla IV). A nivel pronóstico, el Sm1 equivale a un grado 1 de Haggitt, Sm2 es similar a los grados 2 y 3 de Haggitt, mientras que Sm3 puede representar un grado 4 de Haggitt. Una lesión Sm1a o una Sm1b sin invasión vascular nunca da metástasis. Las lesiones con compromiso más profundo o más extenso sí tienen la capacidad de metastatizar, lo que va a determinar la necesidad de Tabla IV. Clasificación de la invasión submucosa en el cáncer colorrectal temprano según Kikuchi (19) Sm1 Sm1a Sm1b Sm1c Sm2 Sm3 Tercio superior de submucosa Invasión submucosa menor a ¼ del espesor del tumor Invasión submucosa entre ¼ y ½ del espesor tumoral Compromiso horizontal del tercio superior de la submucosa mayor a ½ del espesor tumoral Tercio medio de submucosa Tercio inferior de submucosa 10. PDV 1750 - J. RUIZ TOVAR -:Maquetación 1 438 5/7/10 08:37 Página 438 J. RUIZ-TOVAR ET AL. agregar tratamiento quirúrgico después de haber completado el tratamiento endoscópico de una lesión (1,2,10). DIAGNÓSTICO ENDOSCÓPICO Mediante visualización endoscopia se pueden observar algunas características de las lesiones colorrectales que pueden sugerir infiltración submucosa. En las lesiones elevadas son sospechosas aquellas que son de consistencia dura, cuando aparece un pólipo sobre otro pólipo, la ulceración en la punta, la presencia de pequeños puntos blancos satélites o el sangrado local. En las lesiones deprimidas es sospechosa la presencia de puntos sangrantes, la interrupción del patrón capilar de la mucosa y la deformación local de la pared. En caso de compromiso de la submucosa, se pierde el movimiento en bloque de la lesión y su mucosa vecina, evidenciándose una deformación local. Al instilar Índigo carmín 0,4% se observa la interrupción de los surcos innominados de la mucosa, otro signo sospechoso de afectación submucosa (20,21). El desarrollo de la endoscopia de amplificación ha permitido describir 6 patrones diferentes de organización de las glándulas en la mucosa colónicas, denominados pits (orificios en las criptas), que se describen en la tabla V. A medida que la submucosa es invadida, su estructura se destruye con desaparición del patrón glandular, que es lo que se define con pit tipo V. La presencia de asimetría y la falta de homogeneidad en el tamaño de las criptas determinan el grado amorfo de la lesión. Si el signo amorfo está presente, se clasifica la lesión como pit tipo Va, característico de un carcinoma invasor, mientras que cuando no hay amorfismo, con pérdida completa de la estructura, se clasifica como pit tipo Vn, característico de tumores con mayor invasión en profundidad de la submucosa (Sm2, Sm3). Actualmente el patrón pit observado en la colonoscopia de amplificación nos permite diferenciar el adenoma no invasor (pits I-IV) del carcinoma invasor Tabla V. Patrones de orificios en las criptas (pits) según la endoscopia de amplificación (21) Forma Localización Pit tipo I Circular Mucosa normal Leiomiomas Enfermedad inflamatoria intestinal Pit tipo II Pit tipo IIIL Pit tipo IIIs Pit tipo IV Estrellado Tubular grande Tubular pequeño Ramificado Pit tipo V Va Vn No estructurado Amorfo No amorfo Pólipos inflamatorios Áreas con cambios hiperplásicos Adenomas elevados Lesiones deprimidas Adenomas elevados Adenomas vellosos Pólipos de extensión lateral Adenocarcinoma submucoso Carcinoma invasor Carcinoma invasor de mayor grado (Sm2, Sm3) REV ESP ENFERM DIG (Madrid) (pit V) y predecir en cierto modo la profundidad del compromiso tumoral antes de instaurar un tratamiento, lo que mejora la exactitud del diagnóstico endoscópico del cáncer colorrectal temprano, sobre todo en las lesiones deprimidas (21,22). PARTICULARIDADES DEL CÁNCER RECTAL TEMPRANO El recto presenta ciertas características que hace que deban realizarse ciertas consideraciones acerca de su manejo diagnóstico y terapéutico. En primer lugar, la localización de un tumor rectal es importante en el proceso de decisión terapéutica, ya que los tumores localizados en los últimos 10 cm del recto pueden precisar un tratamiento neoadyuvante, lo que no ocurre en los situados cranealmente. Por otra parte, los tumores localizados en los últimos 5 cm del recto tienen más posibilidades de requerir una cirugía con resección esfinteriana (23). El tratamiento va a venir condicionado por varios factores con significación pronóstica: la penetración del tumor en el espesor de la pared del recto, la afectación del la fascia mesorrectal (denominado margen de resección circunferencial) y la presencia de metástasis ganglionares y a distancia. Estos factores son evaluados mediante pruebas de imagen. Las pruebas empleadas para determinar la extensión del tumor a nivel local, que es lo que interesa en el cáncer rectal temprano, son la ecografía endorrectal (EER) y la resonancia magnética (RM). La EER es la técnica más precisa para evaluar la penetración del tumor en la pared rectal, siendo muy precisa en la estadificación de tumores poco avanzados (T1-T2), como es el caso del cáncer rectal temprano con afectación hasta la submucosa (T1) (23). La EER permite establecer la presencia de extensión a la grasa mesorrectal en los tumores T3, pero no permite valorar la infiltración del margen de resección circunferencial. La RM permite un estudio adecuado de las capas de la pared rectal y es muy precisa para establecer la afectación de la fascia mesorrectal, pero pierde exactitud en la evaluación de tumores T1-T2. Ambas técnicas se han mostrado igual de eficaces en la evaluación de adenopatías regionales, evidenciándose sólo aquellas de tamaño patológico en la EER y mostrándose hipoecóicas y mayores de 1 cm en la RM. En teoría, en el cáncer rectal temprano, la posibilidad de afectación ganglionar es prácticamente nula, sin embargo, estudios recientes demuestran que en tumores que alcanzan el nivel de Kukuchi Sm1 el riesgo de existencia de metástasis ganglionares está entre 1-3% de los casos, pero en Sm2 aumenta hasta el 8%, mientras que en Sm3 alcanza hasta el 23% (22). Por ello, RM y EER deben realizarse tras la resección endoscópica, porque ofrecen una información complementaria y de gran importancia para predecir la validez del tratamiento endoscópico definitivo (24-27). REV ESP ENFERM DIG 2010; 102 (7): 435-441 10. PDV 1750 - J. RUIZ TOVAR -:Maquetación 1 Vol. 102. N.° 7, 2010 5/7/10 08:37 RESECCIÓN ENDOCÓPICA DE CÁNCER COLORRECTAL TEMPRANO COMO ÚNICO TRATAMIENTO INDICACIONES DE TRATAMIENTO ENDOSCÓPICO DEFINITIVO El papel de la resección endoscópica en el tratamiento del cáncer colorrectal temprano ha ido definiéndose en los últimos años. Inicialmente se consideraban sólo candidatos a este tratamiento los pólipos malignos de bajo riesgo, que debían cumplir los siguientes criterios: resección completa del pólipo, grado histológico bien o moderadamente diferenciado, examen histológico de la pieza completa (no se aceptaban resecciones en fragmentos “piecemeal”) y ausencia de invasión linfática o vascular (28,29). Haggitt describió que los pólipos con afectación de los niveles 1, 2 y 3 tienen un riesgo bajo de desarrollar metástasis ganglionares (< 3%) y, por tanto, son susceptibles de tratamiento endoscópico definitivo (sin necesidad de tratamiento quirúrgico posterior), mientras que la afectación del nivel 4 precisaría una resección quirúrgica (18). Para Kikuchi, sólo la afectación del tercio inferior de la submucosa Sm3 representa un riesgo elevado de metástasis linfáticas, por lo que Sm1 y Sm2 serían candidatos a excisión endoscópica como único tratamiento (19). Kafka y Coller recomiendan tratamiento endoscópico definitivo en los pólipos pedunculados que no alcanzan el nivel 4 de Haggitt, siempre que no presenten factores adversos como son tumores pobremente diferenciados (mayor frecuencia de metástasis ganglionares, aunque la afectación de la submucosa sea muy superficial), invasión linfática o vascular, o márgenes afectados o muy próximos al límite de resección, ya que en esas circunstancias el riesgo de recidiva local tras tratamiento endoscópico exclusivamente es elevado. Los pólipos sésiles son considerados como lesiones difíciles de resecar completamente y a menudo de forma inadecuada, por lo que recomiendan resección quirúrgica en todos los casos (30). Las recomendaciones de la Sociedad Japonesa de Endoscopia Digestiva incluyen como indicaciones para tratamiento endoscópico definitivo todos los adenomas colónicos y aquellos adenocarcinomas de pequeño tamaño, bien diferenciados, confinados a la mucosa o con invasión de la submucosa menor de 1 micra en profundidad y sin afectación linfática ni vascular (10,31). Estudios recientes cuantifican también la invasión de la submucosa, indicando que una afectación en profundidad mayor de 2 micras desde la muscularis mucosae o una anchura máxima en la submucosa mayor de 4 micras son factores de riesgo para metástasis ganglionares (32,33). Así mismo, no aconsejan un tratamiento endoscópico definitivo en aquellas lesiones de más de 2 cm de diámetro. Por otra parte especifican que las lesiones planas deprimidas (tipo 0-IIc) son lesiones de alto riesgo metastásico y aconsejan restringir la resección endoscópica definitiva a lesiones menores de 1 cm de diámetro (10,31). Para resecciones en bloque de tumores completamente resecados mediante endoscopia sin factores de mal pronóstico, la supervivencia a 5 años es equivalente a la que se obtiene tras resección quirúrgica. La resección en fragREV ESP ENFERM DIG 2010; 102 (7): 435-441 Página 439 439 mentos sólo se considera aceptable para adenomas (lesiones premalignas), ya que en carcinomas no es posible determinar el grado de afectación de la submucosa. Por lo tanto, tras resecciones en fragmentos (piecemeal) de carcinomas, debe completarse el tratamiento con resección quirúrgica. Hay dos técnicas diagnósticas que pueden ofrecer una información de gran importancia a la hora de decidir el tratamiento. Una de ellas es la colonoscopia de amplificación, que en función del patrón pit puede orientar a la invasividad de la lesión. Los patrones pit I-IV podrían considerarse como susceptibles de resección endoscópica, mientras que el patrón V, tanto en su forma amorfa como no amorfa, son muy sugestivos de invasividad y sería recomendable en esos casos optar por una resección quirúrgica (19,20). La otra técnica diagnóstica de gran utilidad antes de decidir la actitud sería la EER, que ha demostrado un elevado grado de correlación con la estadificación histológica en lo referente a la afectación local (T) (23). El seguimiento de los pacientes es un punto esencial para la realización de una resección endoscópica definitiva, siendo motivo suficiente para desestimarla si se piensa que el seguimiento no podrá llevarse a cabo de forma adecuada. Una vigilancia estricta va a permitir detectar recidivas precozmente. La estrategia de seguimiento es también un punto controvertido. Es obligatoria la realización de una nueva colonoscopia entre 1 y 3 meses después de la resección endoscópica definitiva de un carcinoma en estadios iniciales. Sin embargo hay autores que consideran suficiente una colonoscopia al año de la resección, cuando esta fue en bloque, al considerar el riesgo de recidiva bajo. Otros autores más prudentes reconocen que una colonoscopia cada 3-6 meses durante los 2 primeros años es aconsejable (10,34,35). El objetivo de este trabajo es recopilar factores pronósticos de los diferentes estudios e intentar unificarlos, para tratar de establecer indicaciones de tratamiento endoscópico definitivo y recomendaciones de seguimiento que aclaren un tema aún bastante controvertido en la práctica clínica. En primer lugar, es de gran importancia analizar los hallazgos de las pruebas preoperatorias: la endoscopia de amplificación y la EER. Un patrón pit V en endoscopia de amplificación y unos hallazgos en EER de infiltración tumoral más allá de la submucosa deben ser considerados criterios de contraindicación para resección endoscópica definitiva. En el estudio histológico, creemos que es esencial la cuantificación de la afectación de la submucosa, tanto en profundidad como en extensión lateral, hecho que muchos patólogos pasan por alto y que ha demostrado tener implicaciones pronósticas. En el cáncer colorrectal temprano que aparece en pólipos pedunculados (0-Ip) consideraríamos indicada la resección endoscópica como único tratamiento en los niveles 1, 2 y 3 de Haggitt, tumores menores de 2 cm de diámetro, en tumores bien o moderadamente diferenciados, sin afectación vascular ni linfática, con infiltración de la submucosa en menos de 1 micra desde la muscularis mucosae y 10. PDV 1750 - J. RUIZ TOVAR -:Maquetación 1 440 5/7/10 08:37 Página 440 J. RUIZ-TOVAR ET AL. anchura máxima en la submucosa menor de 4 micras y resecados en bloque. La afectación en profundidad de más de 2 micras parece indicación clara para resección quirúrgica, pero entre 1 y 2 micras la elección del tratamiento óptimo es controvertida, por lo que este deberá individualizarse según las circunstancias de cada paciente. En las lesiones polipoideas sésiles (0-Is) y no polipoideas elevadas (0-IIa) o planas (0-IIb) las recomendaciones serían las mismas descritas anteriormente, no siendo aplicables los niveles de Haggitt. Para las lesiones deprimidas sin ulceración (0-IIc), las recomendaciones son las mismas, exceptuando que la lesión no debe tener más de 1 cm de diámetro máximo; en este caso, por su naturaleza biológica más agresiva, sería razonable establecer 1 micra en profundidad como límite aceptable de afectación de la submucosa para resección endoscópica definitiva. Para las lesiones deprimidas y ulceradas, consideradas por algunos autores como inexistentes, no existe evidencia científica para establecer recomendaciones (Tabla VI). En las lesiones rectales consideramos recomendable realizar una RM o una EER tras la resección endoscópica para evaluar la validez de la resección realizada. El protocolo de seguimiento más adecuado tras resección endoscópica como tratamiento único sería la realización de una colonoscopia 1-3 meses tras la resección, seguida de nuevas colonoscopias cada 3-6 meses durante los primeros 2 años. Tabla VI. Indicaciones de resección endoscópica de cáncer colorrectal temprano 1. Lesiones polipoideas pedunculadas (0-Ip) Haggitt 1, 2 y 3 Lesiones < 2 cm Tumores bien o moderadamente diferenciados Ausencia de afectación vascular o linfática Infiltración de la submucosa en profundidad < 1-2 micras desde la muscularis mucosae Anchura máxima de afectación en la submucosa < 4 micras Resección en bloque 2. Lesiones polipoideas sésiles (0-Is) y no polipoideas elevadas (0IIa), planas (0-IIb) Lesiones < 2 cm Tumores bien o moderadamente diferenciados Ausencia de afectación vascular o linfática Infiltración de la submucosa en profundidad < 1-2 micras desde la muscularis mucosae Anchura máxima de afectación en la submucosa < 4 micras Resección en bloque 3. Lesiones no polipoideas deprimidas no ulceradas (0-IIc) Lesiones < 1 cm Tumores bien o moderadamente diferenciados Ausencia de afectación vascular o linfática Infiltración de la submucosa en profundidad < 1 micra desde la muscularis mucosae Anchura máxima de afectación en la submucosa < 4 micras Resección en bloque REV ESP ENFERM DIG (Madrid) BIBLIOGRAFÍA 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. Seitz U, Bohnacker S, Seewald S, Thonke F, Brand B, Bräiutigam T, et al. Is endoscopic polypectomy an adequate therapy for malignant colorectal adenomas? Presentation of 114 patients and review of the literature. Dis Colon Rectum 2004; 47: 1789-97. Nivatvongs S. Surgical management of malignant colorectal polyps. Surg Clin N Am 2002; 82: 959-66. Cooper HS, Deppisch LM, Gourley WK, Kahn EI, Lev R, Manley PN, et al. Endoscopically removed malignant colorectal polyps: clinicopathologic correlations. Gastroenterology 1995; 108: 1657-65. Cappell MS. From colonic polyps to colon cancer: pathophysiology, clinical presentation, screening and colonoscopic therapy. Minerva Gastroenterol Dietol 2007; 53: 351-73. Winawer SJ, Zauber AG, Ho MN, O’Brien MJ, Gottlieb LS, et al. Prevention of colorectal cancer by colonoscopic polypectomy. The National Polyp Study Workgroup. N Engl J Med 1993; 329: 1977-81. Nicholson FB, Barro JL, Atkin W, Lilford R, Patnick J, Williams CB, et al. Review article: population screening for colorectal cancer. Aliment Pharmacol Ther 2005; 22: 1069-77. Navarro M, Peris M, Binefa G, Nogueira JM, Miquel JM, Espinás JA, et al; Catalan Colorectal Cancer Screening Pilot Programme Group. Hallazgos colonoscópicos del estudio piloto de cribado de cáncer colorrectal realizado en Cataluña. Rev Esp Enferm Dig 2008; 100: 343-8. Diaz Tasende J, Marín Gabriel C. Cribado del cáncer colorrectal mediante test de sangre oculta en heces. Rev Esp Enferm Dig 2008; 100: 315-9. Hurlstone DP, Cross SS, Adam I, Shorthouse AJ, Brown S, Sanders DS, et al. A prospective clinic-pathologic and endoscopic evaluation of flat and depressed colorectal lesions in the United Kingdom. Am J Gastroenterol 2003; 98: 2543-9. Repici A, Pellicano R, Strangio G, Danese S, Fagoonee S, Malesci A. Endoscopic mucosal resection for early colorectal neoplasia: pathologic basis, procedures and outcome. Dis Colon Rectum 2009; 52: 1502-15. Japanese Society for cancer of colon and rectum. Japanese classification of colorectal carcinoma: Tokyo: Kanehara & Co., LTD; 1997. Hamilton SR, Vogelstein B, Kudo S, Riboli E, Nakamura S, Hainant P, et al. Tumors of the colon and rectum. En: Hamilton SR, Aaltonen LA, editors. WHO classification of tumors: Pathology and genetics of tumors of the digestive system. Lyon: International agency for research on cancer; 2000. p. 103-43. Koyama Y, Kotake K. Overview of colorectal cancer in Japan: report from the Registry of the Japanese Society for Cancer of the Colon and Rectum. Dis Colon Rectum 1997; 40(Supl. 10): S2-9. Kudo S, Kashida H, Nakajima T, Tamura S, Nakajo K. Endoscopic diagnosis and treatment of early colorectal cancer. World J Surg 1997; 21: 694-701. The Paris endoscopic classification of superficial neoplastic lesions: esophagus, stomach and colon: November 30 to December 1, 2002. Gastrointest Endosc 2003; 58 (Supl. 6): S3-43. Rembacken BJ, Fujii T, Cairns A, Dixon MF, Yoshida S, Chalmers DM, et al. Flat and depressed colonic neoplasms: a prospective study of 1000 colonoscopies in the UK. Lancet 2000; 355: 1211-4. Waye JD. Endoscopic mucosal resection of colon polyps. Gastrointest Clin N Am 2001; 3: 537-48. Haggitt RC, Glotzbch RE, Soffer EE, Wruble LD. Prognostic factors in colorectal carcinomas arising in adenomas: implications for lesions removed by endoscopic polypectomy. Gastroenterology 1985; 89: 328-36. Kikuchi R, Takano M, Takagi K, Fujimoto N, Nozaki R, Fujiyoshi T, et al. Management of early invasive colorectal cancer. Risk of recurrence and clinical guidelines. Dis Colon Rectum 1995; 38: 1286-95. Kashida H, Kudo SE. Early colorectal cancer: concept, diagnosis and management. Int J Clin Oncol 2006; 11: 1-8. Kudo S, Rubio CA, Teixeira CR, Kashida H, Kogure E. Pit pattern in colorectal neoplasia: endoscopic magnifying view. Endoscopy 2001; 33: 367-73. Hurlstone DP, Fujii T. Practical uses of chromoendoscopy and magnification at colonoscopy. Gastrointest Endosc Clin N Am 2005; 15(4): 687-702. REV ESP ENFERM DIG 2010; 102 (7): 435-441 10. PDV 1750 - J. RUIZ TOVAR -:Maquetación 1 Vol. 102. N.° 7, 2010 23. 24. 25. 26. 27. 28. 5/7/10 08:37 RESECCIÓN ENDOCÓPICA DE CÁNCER COLORRECTAL TEMPRANO COMO ÚNICO TRATAMIENTO Vila JJ, Jiménez FJ, Irisarri A, Martínez A, Amorena E, Borda F. Estadificación del cáncer de recto mediante ultrasonografía endoscópica: correlación con la estadificación histológica. Rev Esp Enferm Dig 2007; 99: 132-7. Ortiz Hurtado H, Armendariz Rubio P. Cáncer de recto. En: Parrilla Paricio P, Landa García JI. Cirugía AEC. Madrid: Panamericana; 2009. p. 519-30. Tytherleigh MG, Warren BF, Mortensen NJ. Management of early rectal cancer. Br J Surg 2008; 95: 409-23. Lahaye MJ, Engelen SM, Nelemans PJ, Beets GL, van de Velde CJ, van Engelshoven JM, et al. Imaging for predicting the risk factors – the circumferencial resection margin and nodal disease of local recurrence in rectal cancer: a meta-analysis. Semin Ultrasound CT MR 2005; 26: 259-68. Pahlman L, Bohe M, Cedemark B, Dahlberg M, Lindmark G, Sjödahl R, et al. The Swedish rectal cancer registry. Br J Surg 2007; 94: 1285-92. Morson BC, Whiteway JE, Jones EA, Macrae FA, Williams CB. Histopathology and prognosis of malignant colorectal polyps treated by endoscopic polypectomy. Gut 1984; 25: 437-44. REV ESP ENFERM DIG 2010; 102 (7): 435-441 Página 441 29. 30. 31. 32. 33. 34. 35. 441 Hermanek P, Gall FP. Early (microinvasive) colorectal carcinoma. Pathology, diagnosis, surgical treatment. Int J Colorectal Dis 1986; 1: 79-84. Kafka NJ, Coller JA. Endoscopic management of malignant colorectal polyps. Surg Oncol Clin N Am 1996; 5: 633-61. Kudo S, Kashida H, Tamura T, Kogure E, Imai Y, Yamano H, et al. Colonoscopic diagnosis and management of nonpolypoid early colorectal cancer. World J Surg 2000; 24: 1081-90. Yasuda K, Inomata M, Shiromizu A, Shiraishi N, Higashi H, Kitano S. Risk factor for occult lymph node metastases of colorectal cancer invading the submucosa and indications for endoscopic mucosal resection. Dis Colon Rectum 2007; 50: 1370-6. Ueno H, Mochizuki H, Hashiguchi Y, Shimazaki H, Aida S, Hase K, et al. Risk factors for an adverse outcome in early invasive colorectal carcinoma. Gastroenterology 2004; 127: 385-94. Noshirwani KC, van Stolk RU, Rybicki LA, Beck GJ. Adenoma size and number are predictive of adenoma recurrence: implications for surveillance colonoscopy. Gastrointest Endosc 2000; 51: 433-7. Repici A, Tricerri R. Endoscopic polypectomy: techniques, complications and follow-up. Tech Coloproctol 2004; 8: 283-90.