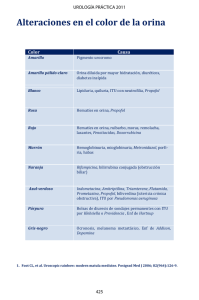
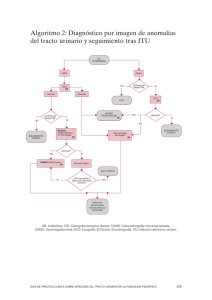
ITU ped Julio 2016
Anuncio

INFECCIONES DEL TRACTO URINARIO (ITU) EN PEDIATRÍA Etiología: Gram negativos: Eschericchia coli (70-90%), Klebsiella spp, Proteus mirabilis (más frecuente en niños con fimosis). Klebsiella spp, Pseudomonas aeruginosa, Enterobacter cloacae, Serratia ssp en niños con infecciones recurrentes, tratados previamente con antibióticos o con patología estructural del tracto urinario. Gram positivos: Stphylococcus aureus, Streptococcus del grupo B y Enterococcus faecalis (más frecuentes en neonatos). TRATAMIENTO ANTIBIÓTICO CIRCUNSTANCIA ELECCIÓN GR ALTERNATIVA GR MEDIDAS NO FARMACOLÓGICAS MODIFICADORA 2,8 Bacteriuria asintomática No indicado • No es necesario tratar ni repetir urocultivo. • No está indicado hacer urocultivo si el niño no presenta clínica. Infección del tracto urinario C Tratamiento en medio 2,8 hospitalario (ITU*) en niños menores de € 3 meses ¥ Alérgicos a betalactámicos o A • Se recomienda toma de muestras antes ITU* febril en niños mayores de Cefuroxima oral, § 1,6 sospecha de pielonefritis : de iniciar el tratamiento (GR A). 3 meses sin indicación de 30 mg/Kg/día en 2 tomas, 7-10 # 1,2, 6,8 Tobramicina o gentamicina im, D • No se recomienda la realización de ingreso hospitalario días 8 5 mg/Kg, 1 dosis diaria, 7 días urocultivos durante o al final del (buen estado general, buena 8 ¥ tratamiento si la evolución es favorable. tolerancia oral, sin Cefixima oral, 8 mg/Kg en 1 ó A • No se debe recoger una muestra de deshidratación, buen # 2,8 2 tomas, 7 días orina para cultivo mediante bolsa cumplimiento del tratamiento y adhesiva por la alta probabilidad de otras circunstancias descritas contaminación. Seguir recomendaciones. en “criterios de derivación”) & específicas para la toma de muestras 8 • Hidratación adecuada (GR C). • Investigar hábitos miccionales e 8 intestinales. 8 • Evitar estreñimiento (GR D). • Recomendación de medidas higiénicas 8 preventivas adecuadas. • Se recomienda informar a los familiares o cuidadores sobre la necesidad del tratamiento precoz y la importancia de 8 hacerlo completo. • En niños con fimosis e ITU recurrentes plantear tratamiento médico para 8 conseguir la retracción del prepucio. ¥ Alérgicos a betalactámicos: B • Se recomienda la toma de muestras de ITU* en niños mayores de Cefuroxima oral, 30 mg/Kg/día 1,6 8 Trimetoprim-sulfametoxazol oral, D iniciar el tratamiento (GR A). 2 años con clínica de cistitis en 2 tomas, 3-5 días 10-50 mg/Kg/día, en 2 tomas, • En caso de bajo riesgo, no ITU de (síntomas miccionales, sin 8 3-5 días repetición, no patología urlógica previa fiebre o con febrícula, sin afectación del estado general) Profilaxis antibiótica de ITU en niños sin alteraciones estructurales y/o funcionales Profilaxis antibiótica de ITU en £ niños con ITU recurrente En niños > 6 años: Fosfomicina-trometamol oral, 2,8 2 g, dosis única No indicada ε A A 1 Niños <2 meses: Amoxicilina oral, 12,5 mg/kg (1/3 o 1/4 de la dosis total de 50 mg/Kg) en 1 sola toma, por la 8 noche B Cefuroxima oral, 15 mg/Kg, en 8 1 sola toma, por la noche Λ Niños >2 meses : Trimetoprim-sulfametoxazol oral, 2 mg/10 mg/Kg al día, 8 1 dosis al día £ Duración individualizada Si imposibilidad de tratamiento de elección, fracaso de los anteriores o intolerancia: B B puede iniciarse tratamiento sin recogida 2 de urocultivo. • No se recomienda la realización de urocultivos durante o al final del 8 tratamiento si la evolución es favorable. • No se debe recoger una muestra de orina para cultivo mediante bolsa adhesiva por la alta probabilidad de contaminación. Seguir recomendaciones & específicas para la toma de muestras 8 • Hidratación adecuada (GR C). • Investigar hábitos miccionales e 8 intestinales. 8 • Evitar estreñimiento (GR D). • Recomendación de medidas higiénicas 8 preventivas adecuadas. • Se recomienda informar a los familiares o cuidadores sobre la necesidad del tratamiento precoz y la importancia de 8 hacerlo completo. • Se recomienda descartar oxiuriasis en 8 niñas con ITU recurrente. • Prevención no farmacológica: - Evitar estreñimiento, higiene genital adecuada, usar ropa interior holgada de algodón, hábito miccional correcto. - Evitar retención urinaria. - Descartar oxiuriasis. • No existe evidencia para apoyar el uso 8 de las siguientes medidas : - Vacunas con cepas uropatógenas - Ácido ascórbico - Zumo de arándanos - Probióticos. OBSERVACIONES: *Se sospechará infección urinaria si en la tira reactiva de orina son positivos la leucocitoesterasa y/o los nitritos o si en el análisis de orina por citometría de flujo o 1,2 microscopía se observa bacteriuria y/o piuria . La infección de orina se confirma cuando el cultivo de orina es positivo con más de 100.000 UFC/ml, si la muestra se recoge a chorro medio y más de 10.000 UFC/ml, si se recoge mediante sondaje vesical. Si no se dispone de microscopía y la tira reactiva es leucitoesterasa positiva y nitritos negativos se valorará inicio de antibioterapia empírica en función de los síntomas y la situación clínica del paciente. Ante sospecha fundada de infección urinaria febril, se recomienda iniciar el tratamiento antibiótico de forma precoz para prevenir la extensión de la infección y reducir 1,6,8 6 el riesgo de daño renal (GR D) . Si el tratamiento es eficaz, la orina se vuelve estéril después de 24 horas . Se recomienda evaluar al paciente en un plazo 8 aproximado de 48 horas tras el inicio del tratamiento . Estudios de imagen: Se recomienda la realizacion de: 8 - ECO de vías urinarias en las siguientes situaciones : Tras primera ITU si se cumple cualquiera de los siguientes criterios: – ITU febril, – paciente que no controla la micción y que no tiene una ecografía prenatal o posnatal normal, – signos de disfuncion del tracto urinario, – masa abdominal o vesical, – creatinina elevada, – ITU por un microorganismo distinto a E. coli. 8 ITU recurrentes . 8 - gammagrafía DMSA diferida (a partir de los 6 meses) tras una primera ITU febril si se cumple cualquiera de los siguientes criterios (GR D) : – Evolucion atípica (persistencia de la fiebre > 48 horas). – Signos de disfunción del tracto urinario inferior. – Masa abdominal o vesical. – Niveles de creatinina elevados. – Septicemia. – ITU por un microorganismo distinto a E. coli. – Hallazgos patológicos en estudios de imagen previos (ECO, cistografía). € La ITU en menores de 3 meses es una infección bacteriana potencialmente grave que habitualmente se presenta con fiebre sin foco y afectación del estado general, sin síntomas locales. El diagnóstico precoz es esencial para evitar la progresión de la enfermedad. ¥ En base a los datos de resistencias locales en población pediátrica, cefalosporinas de 2ª generación orales constituyen el tratamiento de elección en nuestro medio. Se debe priorizar la utilización de cefalosporinas de 2ª generación (cefuroxima) en lugar de cefalosporinas de 3ª generación (cefixima) dado el menor espectro de acción y menor impacto ecológico. 2,8 Amoxicilina-clavulánico oral (50 mg/Kg/día en 3 tomas, 3-5 días) (GR A) queda relegada a tratamiento alternativo en ITU no complicadas (niños con tracto urinario morfológica y funcionalmente normales y con un sistema inmune competente), dados los datos locales de sensibilidad antibiótica de E. coli. %Sensibilidad en <15 años: Cefalosporinas 2ª generación Cefalosporinas 3ª Amoxicilina/ Amoxicilina/ Trimetroprim/ Fosfomicina generación clavulánico clavulánico sulfametoxazol (ITU no complicada) (ITU complicada) E. coli (n=104) 95,4% 99% 90,3% 67,0% 76,9% 100% K. pneumoniae (n=30) 100% 100% 93,3% 90,7% 96,6% 76,6% P. mirabilis (n=45) 93,3% 100% 97,7% 84,4% 88% 86% Datos H. San Juan de Dios del Aljarafe. EUCAST: En ITU no complicada: cepas resistentes CMI>32; ITU complicada CMI>8. # & Nitrofurantoína . 100% 93,3% - . 6 No se recomiendan pautas cortas. Los resultados de 1-3 días de tratamiento son peores que los de 4-7 días . Recogida de la muestra de orina: No se debe recoger una muestra de orina para cultivo mediante bolsa adhesiva por la alta probabilidad de contaminación. - En niños no continentes: Según el nivel de adiestramiento, la muestra deberá extraerse mediante sondaje vesical. Si el medio no es adecuado, se 8 recomienda recoger la orina mediante bolsa perineal o al acecho (GR C) . Si el análisis de orina recogida mediante técnica no estéril resulta alterado, se 1 recomienda confirmación en nueva muestra obtenida en medio estéril: sondaje vesical (GR A) 8 - En niños continentes: recogida de orina limpia de la mitad del chorro medio previo lavado de genitales . § Sospecha de pielonefritis: fiebre elevada, afectación del estado general, dolor lumbar o abdominal, vómitos. ε No se recomienda en niños previamente sanos. Sin embargo no puede considerarse inapropiada hasta descartar reflujo de alto grado. Puede mantenerse hasta la 5 realización de estudios de imagen, siempre que no se demore más de un mes . £ 8 Valorar profilaxis antibiótica individualmente tras estudio de descarte de anomalías estructurales o funcionales del tracto urinario . Cuando esté indicada, se 8 seleccionarán antibióticos con el menor espectro posible para evitar la aparición de resistencias en patógenos de las vías respiratorias . No se recomienda en prevención de recurrencias en: 8 - niños con reflujo vésico-uretral (rVU) de bajo grado, ni en cicatrices renales previas sin reflujo, ni en infecciones recurrentes (GR C) . 8 - profilaxis antibiótica en los niños varones con rVU grados I-III, ni en niñas con rVU grados I-II (GR A) . Sí se recomienda en: 1 - niñas con rVU grados III-V durante un año o hasta que se evalúe nuevamente el grado de rVU mediante control cistográfico (GR B) . 2, 6,8 niños varones con rVU grados IV-V durante un año o hasta que se evalúe nuevamente el grado de rVU mediante control cistográfico (GR B ) . Λ 8 En niños >2 años se venía contemplando el tratamiento con nitrofurantoína▼ oral (1-2 mg/kg/día, en 1 dosis) (GR B). Dados los últimos datos de seguridad de nitrofurantoína y los riesgos asociados a su uso, especialmente a largo plazo, este medicamento ha sido restringido y no puede seguir siendo utilizado en profilaxis ni a largo plazo. ▼NOTAS DE SEGURIDAD Amoxicilina-clavulánico: La Agencia Española del Medicamento (AEMPS) (Nota informativa ref. 2006/1) ha alertado sobre el riesgo de hepatotoxicidad de amoxicilina/clavulánico. La hepatotoxicidad por amoxicilina/clavulánico es la primera causa de ingreso hospitalario por hepatotoxicidad medicamentosa en adultos. Restringir su uso a las infecciones causadas por bacterias resistentes a amoxicilina debido a la producción de betalactamasas. Nitrofurantoína: La AEMPS (Nota Informativa ref 16/2016) ha publicado una alerta sobre la asociación del uso de nitrofurantoína y reacciones adversas graves pulmonares (fibrosis, neumonitis intersticial) y hepáticas (hepatitis crónica, hepatitis colestásica, hepatitis crónica, cirrosis) en tratamientos profilácticos prolongados o intermitentes a largo plazo. Está contraindicada en insuficiencia renal, en tratamientos prolongados (>7 días) o intermitentes y en el embarazo a término. Su uso se ha restringido al tratamiento de la cistitis aguda en niñas >6 años, adolescentes y mujeres adultas (información de la Ficha Técnica) CRITERIOS DE DERIVACIÓN: Edad inferior a 3 meses, afectación del estado general (signos de deshidratación, decaimiento o signos de alteración de la perfusión tisular), intolerancia a la medicación oral, antecedentes de inmunodeficiencia o patología urológica o renal grave (reflujo de alto grado o alteración de la función renal), sospecha de mal control en el entorno familiar (riesgo social). La sospecha clínica de pielonefritis no debe considerarse como indicación de ingreso hospitalario. Las infecciones del tracto urinario (ITU) son, tras las infecciones respiratorias de las vías altas, el proceso infeccioso más frecuente en la infancia y adolescencia. Engloban un grupo de síndromes que se caracterizan por la presencia en la orina de gérmenes procedentes de algún punto del aparato urinario: uretra, vejiga, uréter, pelvis renal o parénquima. La pielonefritis, o infección del parénquima renal, es una de las enfermedades bacterianas serias (potencialmente graves) más comunes en la práctica pediátrica. Además de causar morbilidad aguda, pueden ocasionar cicatrices renales que podrían llevar a largo plazo a insuficiencia renal crónica e hipertensión arterial2. Es muy importante el diagnóstico y tratamiento precoz sobre todo en niños <3 años ante la sospecha de ITU para evitar el daño renal. Las ITU se deben diferenciar de alto o bajo riesgo en función de la presencia de fiebre y afectación del estado general2. Los lactantes y niños que tienen bacteriuria y fiebre de 38ºC o mayor o dolor lumbar deben ser considerados como pielonefritis aguda. Si presentan bacteriuria pero sin clínica sistémica se considerarán como cistitis/infección de vías bajas2. A pesar de la extraordinaria importancia de diagnosticar y tratar adecuadamente la pielonefritis aguda en el niño, el diagnóstico es difícil, sobre todo en lactantes pequeños donde habitualmente los síntomas son inespecíficos. También es compleja la recogida adecuada de la muestra y la interpretación de los datos, por lo que, con cierta frecuencia es imposible confirmar el diagnóstico3,4. Se sospechará infección urinaria si en la tira reactiva de orina son positivos la leucocitoesterasa y/o los nitritos. Si está disponible sobre todo en niños menores de tres años: análisis de orina por citometría de flujo o microscopía con bacteriuria y/o piuria1,2. La infección de orina se confirma cuando el cultivo de orina sea positivo con más de 100.000 UFC/ml, si la muestra se recoge a chorro medio o más de 10.000 UFC/ml, si se recoge mediante sondaje vesical. El tratamiento en las infecciones de orina será siempre empírico hasta la recepción del urocultivo que confirmará el diagnóstico. Cualquier niño mayor de 3 meses y sin criterios de ingreso hospitalario, con sospecha de ITU podrá ser tratado en medio ambulatorio. BIBLIOGRAFÍA CONSULTADA (POR ORDEN ALFABÉTICO) 1. American Academy of Pediatrics. Urinary Tract Infection: Clinical Practice Guideline for the Diagnosis and Management of the Initial UTI in Febrile Infants and Children 2 to 24 Months. Pediatrics. 2011; 128: 595-610. 2. National Institute for Health and Clinical Excellence. Urinary tract infection in children. Diagnosis, treatment and long-term management. Clinical Guideline, August 2007. Disponible en URL: www.nice.org.uk. 3. Ochoa Sangrador C et al. Métodos para la recogida de muestras de orina para urocultivo y perfil urinario. An Pediatr 2007; 67(5): 442-9. 4. Ochoa Sangrador C et al. Utilidad de los distintos parámetros del perfil urinario en el diagnóstico de infección urinaria. An Pediatr 2007; 67(5):450-60. 5. Ochoa Sangrador C et al. Panel de expertos de la Conferencia de Consenso y Grupo Investigador de la Conferencia de Consenso. Recomendaciones de la Conferencia de Consenso “Manejo Diagnóstico y Terapéutico de las Infecciones del Tracto urinario en la Infancia”. An Pediatr 2007; 67 (5):517-25. 6. Tekgül S, Dogan HS, Erdem E, Hoebeke P, Kocvara R, Nijman JM et al. European Society for Paediatric Urology/ European Association of Urology. Guidelines on Paediatric Urology. 2015 (consultado 11/03/2015). Disponible en: http://uroweb.org/wp-content/uploads/23- Paediatric-Urology_LR_full.pdf. 7. Urinary tract infection - children – Management. Clinical Knowledge Summaries [clinical topics]. Disponible en URL: http://www.cks.nhs.uk/urinary tract infection children/management/detailed answer s/age 3 years or older/follow up and aftercare#-3 14208. 8. Grupo de trabajo de la Guía de Práctica Clínica sobre Infección del Tracto Urinario en la Población Pediátrica. Guía de Práctica Clínica sobre Infección del Tracto Urinario en la Población Pediátrica. Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad, Política Social e Igualdad. Instituto Aragonés de Ciencias de la Salud; 2011. Guías de Práctica Clínica en el SNS: I+CS No 2009/01.