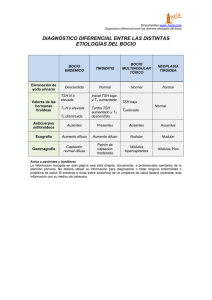
Bocio nodular
Anuncio

Actualización de diagnóstico y tratamiento del bocio nodular Autor Ana María Orlandi Jefa del Sector Tiroides de la Unidad de Endocrinología del Hospital Municipal Dr. Teodoro Alvarez, Ciudad Autónoma de Buenos Aires. Jefa de Trabajos Prácticos de la Carrera de Médico Especialista de Endocrinología de la Facultad de Medicina Universidad de Buenos Aires. Directora de Comisión Directiva de la Sociedad Latinoamericana de Tiroides. Miembro del Departamento de Tiroides de la Sociedad Argentina de Endocrinología y Metabolismo. Ex Vice-Presidenta de la Sociedad Argentina de Endocrinología y Metabolismo. -1- Actualización de diagnóstico y tratamiento del bocio nodular INDICE INTRODUCCIÓN . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3 PREVALENCIA . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3 ETIOLOGIA . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 4 EPIDEMIOLOGIA . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5 HISTORIA Y PRESENTACION CLINICA. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5 Exámen clínico: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 6 Evaluación del riesgo de malignidad:. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 7 Laboratorio:. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 8 Condiciones fisiológicas . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 8 Drogas . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 8 Patologías no tiroideas . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 8 Patologías tiroideas . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 8 Diagnóstico por imágenes:. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9 ¿Cuáles son las estrategias propuestas para minimizar los resultados falso negativos? . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 15 ¿Cuáles son las estrategias posibles según la interpretación de las muestras de PAAF? . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 20 MANEJO Y TRATAMIENTO DE BOCIO NODULAR . . . . . . . . . . . . . . . . . . . . . . . . . 21 Muestras de PAAF no diagnósticas por PAAF:. . . . . . . . . . . . . . . . . . . . . . . . . . . . . 21 Nódulos benignos por PAAF . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 22 Tratamiento del bocio nodular con radioiodo. . . . . . . . . . . . . . . . . . . . . . . . . . . . . 25 Nódulos sospechosos por PAAF. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 26 Nódulos malignos por PAAF . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 26 ALGORRITMO DE DIAGNÓSTICO Y TRATAMIENTO DE BOCIO NODULAR . . 27 CONCLUSIONES . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 28 BIBLIOGRAFIA . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 30 -2- Separata Montpellier 2011 - Vol. 19 N°10 ACTUALIZACIÓN DE DIAGNÓSTICO Y TRATAMIENTO DEL BOCIO NODULAR: INTRODUCCIÓN Los bocios nodulares son agrandamientos de la tiroides clínicamente reconocibles caracterizados por crecimiento excesivo, con transformación estructural y /o funcional de una o varias áreas dentro de una glándula normal. En ausencia de disfunción tiroidea, enfermedad autoinmune, tiroiditis y enfermedad maligna, constituyen una entidad generalmente descripta como bocio nodular simple. Los nódulos tiroideos son un hallazgo clínico frecuente, cuya prevalencia varía según se consideren diversos factores como iodosuficiencia del área en estudio, edad, sexo, método de detección, etc. Estudios epidemiológicos han mostrado que en áreas con suficiente aporte de iodo, la prevalencia de nódulos detectados por palpación es de aproximadamente el 5% en mujeres y 1% en hombres (1), la cual aumenta de 20 a 67% cuando se evalúa una población al azar mediante estudios ecográficos (2). La importancia clínica ante un paciente con nódulo tiroideo, radica en descartar cáncer tiroideo, el cual ocurre en el 5 al 10%, dependiendo de la presencia de determinados factores de riesgo (edad, sexo, historia familiar, exposición a radiaciones, etc.) (3) (4). El nódulo tiroideo puede presentarse como una lesión distinguible palpatoria y / o ecográficamente del tejido circundante, así como, algunas lesiones pueden no corresponder a formaciones diferenciables por estudios de imágenes (5). Otros nódulos no palpables, hallados incidentalmente, son fácilmente vistos por ecografía u otros métodos de imágenes, y son denominados “incidentalomas”. Los nódulos no palpables tienen el mismo riesgo de cáncer que los palpables de igual tamaño (6). PREVALENCIA Los estudios epidemiológicos sobre bocio nodular están condicionados por circunstancias tales como criterio de selección (edad, sexo), factores ambientales (ingesta de iodo, drogas, consumo de alcohol y tabaco), método de detección del nódulo (palpación, ecografía, centellografía), y la determinación de la función tiroidea (7). En el estudio Whickman sobre una muestra representativa de la población adulta, el 15,5% presentó un bocio palpable, con una relación mujer: varón de 4.5:1 (8); mientras que en el estudio Framingham, en un área con suficiente ingesta de iodo, el 1% de las personas entre los 30 y 59 años tenía bocio multinodular por palpación (9). Sin embargo, estos números varían marcadamente cuando el método con que se estudia a la población es la ecografía. Entonces, le prevalencia de nódulos, aún cuando se refiere a lesiones de alrededor de -3- Actualización de diagnóstico y tratamiento del bocio nodular los 10 mm de diámetro es usualmente de 20 - 30 % en poblaciones no seleccionadas (10) (11) (12) (13), siendo aún mayor, en población de añosos y en áreas de insuficiencia iodada (7). ETIOLOGIA Ha sido generalmente aceptado que la deficiencia de iodo es el factor ambiental de mayor importancia que contribuye a la aparición del bocio simple, tanto endémico como esporádico (14). Factores constitucionales como el sexo, se ven claramente implicados en su etiología, dado que la relación mujer/varón en regiones no endémicas puede exceder de 5:1 a 10:1. Otros factores que se ha sugerido aumentan el riesgo de nódulo tiroideo son el tabaquismo (15), bociógenos naturales, stress emocional (16), drogas (17), e infecciones (18). Se han reportado mayores tasas de concordancia para bocio simple en mellizas homozigotas mujeres, tanto en áreas endémicas como no endémicas, cuando se comparan con mellizas heterozigotas (19), lo que aportaría evidencias de un componente genético en la etiología del bocio simple. Aunque los datos de mellizos no pueden ser críticamente interpretados como de relativa importancia de herencia y ambiente, en cualquier población tanto el bocio simple endémico, como el esporádico, se desarrollarían sobre la base de susceptibilidad genética interactuando con factores ambientales, de los cuales, los más importantes serían el nivel de ingesta de iodo y el consumo de tabaco. Algunas investigaciones han evaluado el papel como posibles candidatos de determinados genes, incluyendo tiroglobulina, receptor de TSH y el NIS en la etiología del bocio simple con resultados conflictivos. Corral y col (20) encontraron una mutación puntual del gen de Tg en el cromosoma 8 asociado a bocio no endémico, hallazgo que no pudo ser confirmado por otros autores (21). Los resultados de estos estudios, todos en grupos familiares reducidos, no pueden al presente ser extrapolados a la población general. Es posible que ciertos genes únicos jueguen un rol en determinadas familias, sin embargo, son necesarios estudios en gran número de líneas o grupos familiares, teniendo en cuenta la interacción gen - medio ambiente. -4- Separata Montpellier 2011 - Vol. 19 N°10 EPIDEMIOLOGIA Los estudios epidemiológicos sobre bocio nodular son conflictivos por problemas tales como criterios de selección, influencia de factores ambientales, ingesta de iodo y drogas, hábitos tabáquicos y/ o consumo de alcohol, evaluación del tamaño y morfología nodular, determinación de la función tiroidea y criterio de inclusión o no de sujetos con disfunción tiroidea subclínica (7). La mayoría de los estudios se han focalizado en mujeres de mediana edad y en sujetos añosos, mientras que solo unos pocos han documentado la prevalencia de la enfermedad nodular tiroidea en una población variada y más representativa. Están faltando estudios poblacionales a gran escala, longitudinales, con estudios de imágenes que permitan la distinción entre bocio uni o multinodular, tanto desde el punto de vista morfológico como funcional. Por lo tanto, no están disponibles datos adecuados sobre prevalencia, incidencia, factores de riesgo e historia natural de la enfermedad. Tales limitaciones deben ser tenidas en cuenta, al momento de considerar los datos disponibles. A pesar de las mismas, es regla un patrón de aumento de volumen y nodularidad tiroidea en áreas deficientes de iodo (7) (22). De igual modo, no hay datos suficientes que permitan una estimación del nivel óptimo de iodo para minimizar la ocurrencia de bocio; y por otra parte, se ha enfatizado que el bocio y los nódulos tiroideos, pueden también ocurrir tanto en áreas de iodo suficiencia como de exceso del mismo (23). HISTORIA Y PRESENTACION CLINICA Los antecedentes pueden proveer un índice de sospecha de lesión maligna. Se deben considerar factores predisponentes a malignidad, entre otros, a la historia de irradiación en cabeza o cuello, irradiación corporal total por transplante de médula ósea, historia familiar de cáncer de tiroides en familiares de 1º grado, rápido crecimiento y ronquera. Ante el hallazgo de un nódulo, el examen físico debe considerar las características del mismo (tamaño, consistencia, movilidad, fijeza a planos superficiales y/o profundos), así como, el resto del examen del cuello buscando adenopatías. La mayoría de los pacientes con bocio uninodular tienen pocos o casi nulos síntomas clínicos. Cuando los mismos están presentes, los de mayor jerarquía, son los causados por compresión de estructuras vitales del cuello y del mediastino superior, característicos de la extensión intratorácica del bocio. El mismo se desarrolla en forma insidiosa, más a menudo en los ancianos portadores de bocios de larga data. -5- Actualización de diagnóstico y tratamiento del bocio nodular La evidencia de obstrucción de flujo venoso (por compresión o trombosis de las venas yugular, subclavia o cava superior), puede provocar el signo de Pemberton, caracterizado por la dificultad para respirar, estridor, distensión de venas de cuello o plétora facial al extender los brazos por encima de la cabeza, producido por compresión del bocio dentro de la caja torácica. Exámen clínico: La evaluación de un paciente con bocio nodular comprende inicialmente una historia clínica detallada y examen físico focalizados en la inspección del cuello (incluyendo la búsqueda de adenopatías cervicales) y tórax superior, y palpación del bocio para determinar su tamaño y características nodulares. El reconocimiento de la variabilidad inter e intra observador en relación al tamaño y morfología de la glándula, podría ser alguna de las explicaciones para el uso aumentado del diagnóstico por imágenes por parte de los tiroideologos (24) (25). En general, el bocio cuando es pequeño suele ser sobrestimado y contrariamente, cuando es de gran tamaño puede ser subestimado (26). La detección de un nódulo tiroideo depende de su tamaño, morfología, localización, así como de la anatomía del cuello del paciente y del entrenamiento del médico. El paciente habitualmente no se percata de la presencia de nódulos del orden de 1 - 2 cm, salvo que su ubicación, rápido crecimiento o la presencia de dolor, lo hagan más evidentes. Tabla 1: Síntomas, signos clínicos e investigaciones en el diagnóstico de bocio nodular Síntomas y Signos • • • • • • • • • • • • • -6- Historia familiar de enfermedad tiroidea benigna Crecimiento lento de masa en región anterior del cuello Nódulo único o múltiple por palpación Agrandamiento tiroideo durante embarazo Molestias cosméticas Asimetría, desviación y/o compresión traqueal Obstrucción de vía aérea superior, disnea, tos y disfagia Dolor transitorio con agrandamiento secundario a hemorragia nodular Desarrollo gradual de hipertiroidismo Síndrome de obstrucción de vena cava superior (raro) Parálisis de nervio recurrente (raro) Síndrome de Horner (raro) Ausencia de adenopatías Separata Montpellier 2011 - Vol. 19 N°10 Investigaciones • • • • • • • • • • TSH T4 y T3 totales y/o libres Tiroglobulina Calcitonina Anticuerpos antitiroideos (aTPO y aTg) Centellografía Ecografía TAC y RMN Pruebas de función pulmonar Punción aspiración con aguja fina y estudio citológico Evaluación del riesgo de malignidad: Ante la presencia de un nódulo tiroideo, si bien la incidencia de cáncer es baja, uno de los objetivos principales de la evaluación clínica es excluir la presencia de cáncer tiroideo. Tabla Nº 2 Factores que sugieren malignidad tiroidea de acuerdo al grado de sospecha Alta sospecha • • • • • • • Historia familiar de carcinoma medular o neoplasia endócrina múltiple Rápido crecimiento tumoral ( especialmente durante tratamiento inhibitorio con LT4) Nódulo de consistencia dura Fijación a estructuras vecinas Parálisis de cuerdas vocales Presencia de adenopatías regionales MTS a distancia (óseas o pulmonares) Moderada sospecha • • • • • • • Edad < 20 o > 60 años Sexo masculino Nódulo solitario Historia de irradiación en cabeza y/o cuello Consistencia firme y posible fijación Nódulo > 4 cm y parcialmente quístico Síntomas compresivos: disfagia, disnea, tos, disfonía Baja sospecha • Todos los otros -7- Actualización de diagnóstico y tratamiento del bocio nodular Laboratorio: Desde el advenimiento de ensayos ultrasensibles de TSH, esta determinación se ha transformado en la investigación de primera línea en el estudio de un paciente con bocio nodular. Los ensayos por quimioluminiscencia de tercera generación con límites de detección cercanos a 0,01 mU/ml, deberían ser de uso corriente en la práctica. Con ellos se pueden detectar niveles disminuidos de TSH aún en casos leves de hipertiroidismo, permitiendo un diagnóstico confiable de hiperfunción tiroidea subclínica (27). Aunque es un estudio preferido por más de la mitad de los especialistas, se discute si una determinación inicial de hormonas tiroideas podría dar información adicional, dado que en la mayoría de los casos la TSH se encuentra en rango normal. Respecto a la medición de anticuerpos antitiroperoxidasa (aTPO), son solicitados por más de la mitad de los clínicos (28) (29). Los mismos pueden ser encontrados en cerca del 10% de la población, y por lo tanto, no es infrecuente que la autoinmunidad pueda coexistir con un bocio. Con respecto a la medición de tiroglobulina sérica, aunque es conocido que la misma correlaciona con el status de iodo y / o el tamaño glandular, este marcador es ineficaz a nivel individual como diagnóstico de bocio (30). Otra determinación que provoca discusión y aún no hay acuerdo al respecto, es la medición de calcitonina. El carcinoma medular constituye aproximadamente menos del 10% de todos los cánceres tiroideos y menos de 0.5% de los nódulos tiroideos. La presencia de anticuerpos heterófilos puede ser causa de niveles falsamente elevados de calcitonina (31). Aunque también están descriptas elevaciones de este marcador no relacionadas con carcinoma medular que deben ser tomadas en consideración. Tabla Nº 3: Elevaciones de calcitonina no relacionadas con carcinoma medular (32) Condiciones fisiológicas Patologías no tiroideas • Sexo • Hipergastrinemias • Edad • Hipercalcemias (Hiperparatiroidismo) • Actividad física • Insuficiencia Renal Drogas • Tumores neuroendócrinos • Omeprazol o similares Patologías tiroideas • Corticoides • Carcinoma papilar • Beta bloqueantes • Carcinoma folicular • Glucagon • Tiroiditis autoinmune • Pancreozimina -8- Separata Montpellier 2011 - Vol. 19 N°10 Los resultados de diversos estudios sobre el uso rutinario de la medición de calcitonina en pacientes con enfermedad nodular tiroidea varían en cuanto a sus resultados, mostrando prevalencias de carcinoma medular entre 0.28 a 3.9% (33) (34). Debe entonces tenerse en cuenta, que no hay aún disponible una conclusión clara en base a los datos existentes, y el costo - beneficio debe considerarse por la alta tasa de falsos positivos que rondaría el 60 - 80 % (34). Diagnóstico por imágenes: Ecografía: De los distintos métodos de estudios por imágenes disponibles (ecografía, centellografía, tomografía computada, resonancia magnética y PET Scan), sin dudas, la ecografía es de uso prioritario entre los clínicos (35) (36). La introducción de la ecografía tiroidea ha tenido un gran impacto en la práctica clínica. Las principales razones para su uso tan difundido son la alta disponibilidad, el bajo costo, la falta de molestias para el paciente y la ausencia de radiaciones ionizantes. Cuándo está indicada la realización de una ecografía tiroidea? La ecografía con transductor de alta resolución, es el estudio más sensible para detectar lesiones tiroideas. Permite obtener una medida del volumen basal del nódulo y/o de la glándula, así como, describir los criterios ecográficos estandarizados que indican posición, tamaño, forma, márgenes, contenido, ecogenicidad y patrón vascular del nódulo. Si la palpación tiroidea es normal, la evaluación ecográfica estaría justificada cuando se sospecha un desorden tiroideo o cuando se reconocen factores de riesgo. Sin embargo, debe considerarse que su alta sensibilidad, lleva a detectar lesiones clínicamente insignificantes que no harían más que promover la ansiedad del paciente. Por algunas de estas ventajas, más del 80% de los especialistas consultados por la Asociación Europea de Tiroides (ETA) y 60% de los pertenecientes a la Asociación Americana de Tiroides (ATA), incluyen la ecografía como estudio rutinario inicial en el manejo de pacientes con bocio nodular (28) (29) (35) (36). Algunos estudios han evaluado la capacidad de predecir si un nódulo es benigno o maligno sobre la base de sus características ecográficas (37) (38) (39) (40). El tamaño nodular, por su parte, no es predictor de malignidad, dado que la probabilidad de cáncer en un nódulo tiroideo es la misma independientemente de su tamaño (37) (41). -9- Actualización de diagnóstico y tratamiento del bocio nodular Tabla Nº 4: Características ecográficas en enfermedad nodular Benignas Malignas • Ecogenicidad normal o hiperecogenicidad • Hipoecogenicidad • Calcificaciones groseras • Microcalcificaciones • Halo delgado, bien definido • Halo grueso, irregular • Márgenes regulares • Márgenes desflecados • Falta de crecimiento invasivo • Crecimiento invasivo • Ausencia de adenopatías regionales • Adenopatías regionales • Bajo flujo intranodular por Doppler • Alto flujo intranodular por Doppler Algunas de las características ecográficas descriptas, se han encontrado asociadas con riesgo aumentado de cáncer. Tabla Nº 5: Hallazgos ecograficos asociados con cáncer tiroideo Hallazgo ecográfico Sensibilidad (%) Microcalcificaciones 26.1 - 59.1 Hipoecogenicidad Valor Predictivo Positivo (%) Valor Predictivo Negativo (%) 85.8 - 95.0 24.3 - 70.7 41.8 - 94.2 26.5 - 87.1 43.4 - 94.3 11.4 - 68.4 73.5 - 93.8 Márgen irregular o ausencia de halo 17.4 - 77.5 38.9 - 85.0 9.3 - 60.0 38.9 - 97.8 Sólido 69.0 - 75.0 52.5 - 55.9 15.6 - 27.0 88.0 - 92.1 Vascularidad intranodular 54.3 - 74.2 78.6 - 80.8 24.0 - 41.9 85.7 - 97.4 32.7 92.5 66.7 74.8 Nódulo más alto que ancho Especificidad (%) Sin embrago, la sensibilidad, especificidad y valor predictivo positivo para estos criterios son extremadamente variables entre un estudio y otro y ninguna característica ecográfica tiene alto valor predictivo positivo para cáncer. La combinación de factores mejora el valor predictivo positivo de la ecografía. En particular, un nódulo predominantemente sólido con microcalcificaciones tiene un 31.6% de posibilidades de ser un carcinoma, cuando se lo compara con un nódulo predominantemente quístico (más del 95% quístico) sin calcificaciones, el cual tiene una probabilidad del 1% de ser maligno (42). - 10 - Separata Montpellier 2011 - Vol. 19 N°10 El Doppler color también ha sido evaluado como herramienta diagnóstica para predecir cáncer tiroideo, en la hipótesis que el flujo periférico es sugestivo de nódulo benigno, mientras que un flujo predominantemente central, es sugerente de malignidad. Los resultados son contradictorios, ya que algunos reportes informan la utilidad de este procedimiento (41), mientras otros no encuentran que esta metodología mejore la eficacia diagnóstica (39). Si bien algunos estudios muestran que el flujo central es más frecuente en nódulos malignos, el Doppler color no puede ser usado para excluir la malignidad con un alto grado de certeza. Recientemente, la elastosonografía ha sido aplicada en el diagnóstico del nódulo tiroideo, mostrando una alta sensibilidad y especificidad en pacientes seleccionados. El valor predictivo del método se ha visto independiente del tamaño nodular (43) (44), así como para lesiones caracterizadas como indeterminadas por PAAF (45). No obstante, esta metodología presenta algunas limitaciones, como por ejemplo, los nódulos quísticos y los bordes calcificados y se necesitarán más experiencias para poder considerarla como un elemento diagnóstico de jerarquía. En 2009, Horvath y col. publicaron su experiencia sobre el desarrollo de la caracterización ecográfica estandarizada y la creación de un sistema de reporte de lesiones tiroideas para el manejo clínico: el TIRADS (Thyroid Imaging Reporting and Data System). Se trató de un estudio prospectivo sobre la correlación entre una serie de 1959 lesiones nodulares biopsiadas bajo control ecográfico y estudiadas histológicamente durante un período de 8 años. Se generaron grupos de clasificación TIRADS 1 a 6 para patología tiroidea general y TIRADS 2 a 6 para los nódulos. La sensibilidad, especificidad, valor predictivo positivo, valor predictivo negativo y eficacia diagnóstica fueron del 88, 49, 49, 88 y 94% respectivamente, por lo que concluyeron que este sistema les permitió mejorar el manejo del paciente, la eficacia costo - beneficio, así como, evitar PAAF innecesarias (46). Centellografía: Si bien la centellografía tiroidea tiene hoy día escaso valor como estudio anatomo - topográfico, es de utilidad en la determinación de la funcionalidad del nódulo tiroideo. Las pruebas de supresión con T3 o T4 no son usadas rutinariamente. El cetellograma tiroideo no es un estudio recomendado en la evaluación inicial de pacientes con bocio nodular no tóxico; sin embargo, no se discute su indicación en el estudio de un bocio nodular con hipertiroidismo (clínico o subclínico), de modo de visualizar los nódulos hipercaptantes, pasibles de tratamiento con Iodo 131 (47). - 11 - Actualización de diagnóstico y tratamiento del bocio nodular Tomografía computada y Resonancia Magnética Nuclear: Ambos estudios proveen visualización de alta resolución de la glándula tiroides y estructuras vecinas. Ninguno de estos métodos tiene ventajas sobre la ecografía en cuanto a visualización de estructuras intratiroideas. La mayor utilidad de ambos métodos es en el estudio de bocios con prolongación subesternal, en forma mucho más precisa que otros estudios de imagen. Sin embargo, estas técnicas son usadas en esta situación por solo el 15 - 20 % de los clínicos (29). Seguramente influye en esto la disponibilidad y el costo de estas técnicas; así como su escaso valor en la diferenciación entre lesiones benignas y malignas. El PET - Scan, tiene en ese sentido un valor más promisorio, ya que algunos reportes informan que cerca del 50% de nódulos detectados por este tipo de imágenes son nódulos malignos (48) (49). Lamentablemente, el alto costo y escasa disponibilidad, hace que este método de estudio tenga limitada accesibilidad hasta el momento. Punción Aspiración con aguja fina (PAAF) La PAAF y el estudio citológico son los métodos universalmente aceptados para el estudio del nódulo tiroideo, y en manos de operadores experimentados tiene una alta eficiencia diagnóstica. Se trata de un procedimiento seguro, eficaz, de bajo costo y con complicaciones infrecuentes y de escasa magnitud. Las muestras citológicas han sido tradicionalmente clasificadas en cuatro categorías: benignas, indeterminadas o sospechosas de malignidad, malignas e insatisfactorias o no diagnósticas. La sensibilidad, especificidad, valor predictivo negativo y positivo, la tasa de falsos positivos y falsos negativos, así como la eficiencia diagnóstica, varían según se trate de nódulos sólidos, quísticos, mixtos, entre otros factores a considerar. Tabla Nº6: Sensibilidad. especificidad, valor predictivo y falsos positivos y/o negativos de PAAF (50) (51) HALLAZGO MEDIA (%) Sensibilidad 83 65 - 98 Especificidad 92 72 - 100 Valor Predictivo Positivo 75 50 - 96 Falsos (-) 5 1 - 11 Falsos (+) 5 0-7 - 12 - RANGO (%) Separata Montpellier 2011 - Vol. 19 N°10 Con este procedimiento diagnóstico, se obtienen muestras adecuadas en aproximadamente el 80% de los casos de PAAF (52). Las muestras insatisfactorias o no diagnósticas dependerán de la experiencia del operador y del citólogo, del número de aspirados, carácter del nódulo y de los criterios usados para considerar una muestra como adecuada. El número de estudios diagnósticos aumenta si el procedimiento es guiado por ecografía (53) (54) (55) y por otra parte, el número de muestras insuficientes disminuye con la repetición del procedimiento (52) Tabla Nº 7: Categorías diagnósticas de nódulos tiroideos, distribución relativa de resultados de PAAF Frecuencia (rango) Benigno 69 % (53 - 90) • Bocio coloide • Hiperplasia nodular • Hiperplasia adenomatosa • Tiroiditis (crónica, aguda, subaguda) • Quiste Sospechoso Neoplasia folicular 10 % (5 - 23) • Normofolicular (simple) • Macrofolicular • Microfolicular (fetal) • Trabecular y sólido (embrionario) de células de Hürthle Maligno 4 % (1 - 10) • Carcinoma folicular • Carcinoma papilar • Carcinoma medular • Carcinoma anaplásico • Linfoma • Metastásico No diagnóstico (insuficiente) 17 % (15 - 20) La probabilidad de malignidad según los resultados de PAAF indican que ante una muestra compatible con malignidad la misma es del 100%, en categoría sospechoso de malignidad es de 60%, neoplasia folicular de 14%, en muestras compatibles con benignidad del 1% y muestras no diagnósticas del orden del 10% (52). - 13 - Actualización de diagnóstico y tratamiento del bocio nodular Recientemente y con el objetivo de unificar criterios en cuanto a interpretación de las muestras citológicas y terminología de los informes, se ha dado a conocer el Sistema Bethesda para Reporte de Citopatología Tiroidea (56). La interpretación deberá proveer información clínicamente relevante. Los términos de los informes reportados deberían constar de riesgo implícito (o explícito) de malignidad y recomendaciones para el manejo del paciente (ej. seguimiento anual, repetición de PAAF, extensión recomendada de cirugía tiroidea, etc.). Table 1: The Bethesda System for Reporting Thyroid Cytopathology: Recommended Diagnostic Categories* I. Nondiagnostic or Unsatisfactory Cyst fluid only Virtually acellular specimen Other (obscuring blood, clotting artifact, etc) II. Benign Consistent with a benign follicular nodule (includes adenomatoid nodule, colloid nodule, etc) Consistent with lymphocytic (Hashimoto) thyroiditis in the proper clinical context Consistent with granulomatous (subacute) thyroiditis Other III. Atypia of Undetermined Significance or Follicular Lesion of Undetermined Significance IV. Follicular Neoplasm or Suspicious for a Follicular Neoplasm Specify if Hürthle cell (oncocytic) type V. Suspicious for Malignancy Suspicious for papillary carcinoma Suspicious for medullary carcinoma Suspicious for metastatic carcinoma Suspicious for lymphoma Other VI. Malignant Papillary thyroid carcinoma Poorly differentiated carcinoma Medullary thyroid carcinoma Undifferentiated (anaplastic) carcinoma Squamous cell carcinoma Carcinoma with mixed features (specify) Metastatic carcinoma Non - Hodgkin lymphoma Other - 14 - Separata Montpellier 2011 - Vol. 19 N°10 Table 2: The Bethesda System for Reporting Thyroid Cytopathology: Implied Risk of Malignancy and Recommended Clinical Management Diagnostic Category Risk of Malignancy (%) Usual Management† Nondiagnostic or Unsatisfactory Benign Atypia of Undetermined Significance or Follicular Lesion of Undetermined Significance Follicular Neoplasm or Suspicious for a Follicular Neoplasm Suspicious for Malignancy 1-4 0-3 ~5 - 15‡ Repeat FNA with ultrasound guidance Clinical follow-up Repeat FNA 15 - 30 Surgical lobectomy 60 - 75 Malignant 97 - 99 Near-total thyroidectomy or surgical lobectomy§ Near-total thyroidectomy§ En nuestro medio, la Sociedad Argentina de Endocrinología y Metabolismo, a través del Departamento de Tiroides y la Sociedad Argentina de Citología, están trabajando en el análisis e implementación de este sistema de informes citológicos. Si bien la tasa de falsos negativos es baja, no es despreciable y alcanza una proporción del 1 - 11% según distintas series (57) (58); por lo tanto, es aconsejable el seguimiento longitudinal en los nódulos diagnosticados como benignos. ¿Cuáles son las estrategias propuestas para minimizar los resultados falso negativos? • • • • • • • • Realizar PAAF bajo control ecográfico Realizar múltiples punciones de un nódulo para obtener muestras de diversas áreas Considerar PAAF bajo guía ecográfica repetida para el seguimiento de nódulos benignos Para nódulos múltiples, priorizar la PAAF de nódulos de acuerdo a sus características ecográficas Para nódulos quísticos, realizar punción bajo ecografía de las áreas sólidas y enviar líquido para su examen Obtener al menos seis preparados con muestra celular adecuada Realizar una inmediata fijación para tinción con técnica de Papanicolaou Citopatólogo experto en la revisión de preparados El crecimiento del nódulo, no es en sí mismo una indicación de malignidad, pero ante esta eventualidad está indicado repetir la PAAF. Para nódulos con citología inicial benigna, en nuestra experiencia sobre 799 PAAF realizadas en 306 pacientes y seguidos por una media de 42 meses, el cambio de benigno a - 15 - Actualización de diagnóstico y tratamiento del bocio nodular maligno se observó en 1.3% de los casos, de benigno a sospechoso en 0.98%; mientras que el 97.70% repitió diagnóstico citológico de benignidad a largo plazo, independientemente del crecimiento o no del nódulo estudiado (59). Este hallazgo coincide con otras series, cuando se considera PAAF guiada por palpación (60) (53), no solo en cuanto a porcentaje de cambio en diagnóstico citológico, sino en el número de procedimientos aconsejados para disminuir los falsos negativos. A este respecto y en coincidencia con nuestras conclusiones, Illouz y col. reportaron que la repetición de la PAAF diagnostica un número relevante de cánceres los cuales no son detectados en la primera PAAF, aconsejando un mínimo de tres punciones para disminuir el subdiagnóstico de cáncer en el seguimiento a largo plazo (61). Este porcentaje disminuye cuando se analizan los resultados en PAAF guiadas por ecografía que se describen en aproximadamente el 0.6% (53). Dada la variabilidad del examen palpatorio para definir los cambios en el tamaño nodular en orden de detectar cambios clínicos significativos, el cual es menor que el realizado por ecografía, es recomendable efectuar el seguimiento a largo plazo con esta metodología No hay consenso en cuanto a que se considera crecimiento nodular, o dicho en otras palabras, cuál sería el umbral del mismo que requeriría una nueva PAAF. Algunos autores sugieren un incremento del 15% en el volumen nodular, mientras otros recomiendan medir los cambios considerando el diámetro del nódulo (62) (60) (53) (63). Una razonable definición de crecimiento sería un aumento del 20% en el diámetro nodular con un incremento mínimo en dos o más dimensiones de al menos 2 mm. (64). Es motivo de discusión el decidir qué nódulos deben ser punzados, ya sea bajo guía palpatoria o ecográfica, y cuales nódulos no requieren este procedimiento. Considerando los datos disponibles y la bibliografía existente, hay diversos consensos que han tratado de fijar su posición al respecto. No obstante, las recomendaciones permiten a los médicos alguna flexibilidad en la selección de los pacientes a estudiar con PAAF, teniendo en cuenta características del paciente y del nódulo propiamente dicho. El objetivo primario de evaluar un nódulo con la PAAF es determinar si el mismo es benigno o maligno, de modo que pacientes con cáncer tengan un diagnóstico y tratamiento precoz con una reducción de la morbi-mortalidad, y por otra parte, evitar la cirugía innecesaria en pacientes portadores de nódulos benignos. En los últimos años y con el rol fundamental alcanzado por la ecografía en la evaluación de la enfermedad nodular tiroidea, diversos trabajos han buscado demostrar si las características ecográficas permitirían predecir el riesgo de malignidad. En 2002, Kim y col describieron una sensibilidad de 93,8%, especificidad de 66%, valor predictivo positivo de 56.1%, valor predictivo negativo de 95,9% y eficacia diagnóstica de 74.8%, basándose en la clasificación ecográfica de los nódulos, lo que haría recomendar la PAAF en aquellos nódulos clasificados como positivos, independientemente de la palpación (37). Sahin y col. por su parte, evaluaron la utilidad de la PAAF bajo guía palpatoria tanto en nódulos infracentimétricos como supracentimétricos; así como las características ecográficas para evaluar el riesgo - 16 - Separata Montpellier 2011 - Vol. 19 N°10 de malignidad. No encontraron diferencias significativas entre los nódulos infra y supracentimétricos en cuanto a sensibilidad, especificidad, valor predictivo positivo y negativo, así como en la eficacia diagnóstica. Asimismo, demostraron que el tamaño pequeño de los nódulos no garantiza un bajo riesgo de malignidad (65). Más recientemente, Bastin y col. revisaron la evidencia de las características ecográficas de los nódulos y su capacidad para predecir malignidad. Encontraron que nódulos predominantemente sólidos, la hipoecogenicidad, presencia de microcalcificaciones, macrocalcificaciones, márgenes mal definidos, vascularidad intranodular y una forma más alta que ancha, estaban asociadas con riesgo aumentado de malignidad. No obstante, una única característica no fue suficientemente sensible o específica para excluir o diagnosticar cáncer, sino que la malignidad fue mucho mayor en nódulos con al menos dos características sospechosas (66). En nuestra experiencia, sobre 1046 punciones realizadas en 683 pacientes, las características ecográficas en cuanto a decidir la PAAF y su relación con los diagnósticos citológicos y/ o histológicos hallados, mostraron los siguientes resultados: Relación entre las características ecográficas y citología Características Ecográficas Benignas Malignas Citología Benigna (n=650) 312 (48%) 338 (52%) Citología Maligna (n=127) 41 (32%) 86 (68%) Relación entre las características ecográficas e histología Características Ecográficas Benignas Malignas Histología Benigna (n=100) 50 (50%) 50 (50%) Histología Maligna ( n=53) 12 (23%) 41 (77%) La sensibilidad fue de 80%, especificidad de 47%, el valor predictivo positivo de 44% y el valor predictivo negativo de 81%. Concluimos que las características ecográficas mostraron alta sensibilidad y baja especificidad. El bajo valor predictivo positivo para malignidad podría estar relacionado con la alta tasa de falsos positivos encontrados. En nuestra experiencia, las características ecográficas de benignidad no descartan el hallazgo citológico de malignidad, reafirmando que la PAAF es el método más confiable para el estudio de los nódulos tiroideos (67). En el Consenso de la Sociedad de radiologistas en ultrasonido (SRU), se consideró nódulo a cualquier discreta lesión que es ecográficamente distinguible del parénquima vecino. Estas recomendaciones se - 17 - Actualización de diagnóstico y tratamiento del bocio nodular aplican a nódulos de un centímetro o mayores en virtud de la falta de evidencias acerca de si el hallazgo de un cáncer pequeño modifica o no la expectativa de vida, así como en lo que se refiere a incluir nódulos muy pequeños para punzar, lo que podría llevar a un número exagerado de biopsias. El criterio del tamaño para la selección del nódulo a punzar fue hecho sobre la base del riesgo de cáncer asociado con las características ecográficas. Para nódulos con características ecográficas asociadas a un mayor riesgo de carcinoma, el límite de corte puede ser menor que para nódulos con hallazgos ecográficos asociados con citologías benignas (68). Tabla Nº 8: Recomendaciones para Nódulos Tiroideos de 1 cm o mayores en diámetro máximo. Adaptado de Frates y col. (68) HALLAZGO ECOGRÁFICO RECOMENDACIÓN Nódulo Solitario Microcalcificaciones Considerar PAAF bajo ecografía en nódulo ≥ 1 cm. Sólido (o predominantemente sólido) y con calcificaciones groseras. Considerar PAAF bajo ecografía en nódulos ≥ 1.5 cm. Mixto o casi enteramente mixto con componente mural sólido. Considerar PAAF bajo ecografía en nódulo ≥ 2 cm. Ninguna de las anteriores, pero crecimiento sustancial desde ecografía previa. Considerar PAAF bajo ecografía. Nódulo casi exclusivamente quístico, o sin ninguna de las características mencionadas o sin crecimiento desde última ecografía. PAAF bajo guía ecográfica probablemente innecesaria. Nódulos Múltiples Considerar PAAF bajo ecografía en uno o más nódulos, sobre la base de criterios de selección para el nódulo solitario. Respecto a aspirados no diagnósticos en una PAAF inicial, recomiendan considerar un nuevo procedimiento en nódulos con los criterios mencionados para nódulo solitario. Con relación a la presencia de nódulos linfáticos anormales, independientemente de los criterios ecográficos, aconsejan efectuar rápidamente una biopsia. Más recientemente. la ATA publicó la revisión de las Guías para pacientes con nódulos tiroideos y cáncer de tiroides (69), donde consideran las características clínicas y ecográficas en la decisión de efectuar una PAAF. De acuerdo a ellas surgen las recomendaciones observadas en la siguiente tabla. - 18 - Separata Montpellier 2011 - Vol. 19 N°10 Tabla No 9: Recomendaciones de PAAF según características clínicas y ecográficas Adaptado de Cooper D y col (69) Hallazgos clínicos y ecográficos de nódulos Recomendación de PAAF según tamaño nodular Antecedentes de alto riesgo Nódulo CON hallazgos ecográficos sospechosos Nódulo SIN hallazgos ecográficos sospechosos Nódulos linfáticos cervicales anormales Microcalcificaciones > 5 mm - Recomendación A > 5 mm - Recomendación I Todos - Recomendación A ≥ 1 cm - Recomendación B Nódulo sólido e hipoecogenicidad Isoecogénico o hiperecogénico > 1 cm - Recomendación B ≥ 1 - 1.5 cm - Recomendación C Nódulo mixto (sólido - quístico) CON algún hallazgo ecográfico sospechoso SIN hallazgo ecográfico sospechoso ≥ 1.5 - 2 cm - Recomendación B ≥ 2 cm - Recomendación C Nódulo espongiforme ≥ 2 cm - Recomendación C Nódulo puramente quístico PAAF no indicada - Recomendación E Con respecto al tipo de procedimiento de PAAF a elegir (guiada por palpación o por ecografía), existen posiciones diversas. Mientras la Asociación Americana de Endocrinólogos Clínicos recomienda la PAAF guiada por ecografía para todos los nódulos ≥1 cm en sujetos eutiroideos (70), la ATA, por el contrario, recomienda la PAAF tanto guiada por palpación como por ecografía (47). Diversos trabajos han analizado la eficiencia en la obtención del material comparando ambas técnicas, coincidiendo en demostrar que la PAAF bajo guía ecográfica es superior a la guiada por palpación para la obtención de material adecuado, especialmente en nódulos pequeños o de difícil acceso (71) (72). En nuestra experiencia, la PAAF con guía ecográfica logró mejorar la suficiencia del material de punción en aproximadamente el 30% de los nódulos evaluados al comparar ambas metodologías. Por tal motivo, coincidimos en considerar que cuando está disponible, la PAAF bajo guía ecográfica sería de elección. Podría decirse entonces que la PAAF bajo guía ecográfica está especialmente indicada en las siguientes situaciones: • Pequeños nódulos de difícil palpación o no palpables - 19 - Actualización de diagnóstico y tratamiento del bocio nodular • Áreas sólidas de nódulos predominantemente quísticos • Incidentalomas asociados a factores de riesgo • Múltiples nódulos en bocios multinodulares • Nódulos palpables con punciones bajo palpación no diagnósticas • Nódulos no palpables con aumento de tamaño, factores de riesgo o signos ecográficos sugestivos de malignidad ¿Cuáles son las estrategias posibles según la interpretación de las muestras de PAAF? Muestras no diagnósticas La mayoría de los autores y guías de manejo de patología nodular, luego de un diagnóstico inicial de muestra no diagnóstica, aconsejan repetir la PAAF bajo guía ecográfica, lo que resultará en la obtención de material adecuado en 75% de nódulos sólidos y 59% de los quísticos (73). No obstante, cerca de un 7% de los nódulos continúan presentando muestras no diagnósticas en las PAAF subsecuentes y podrán ser malignas al momento de la cirugía (74). En el caso de nódulos parcialmente quísticos que repetidamente muestran resultados no diagnósticos, sería aconsejable estrecho seguimiento y/o cirugía; mientras que en el caso de nódulos sólidos, la conducta quirúrgica debería ser considerada más fuertemente ante muestras reiteradamente insatisfactorias. Muestras sospechosas de carcinoma Ante diagnóstico citológico compatible con sospecha de carcinoma, la cirugía es la conducta recomendada (75). Muestras compatibles con carcinoma Ante el diagnóstico compatible con carcinoma, se impone la conducta quirúrgica. Muestras indeterminadas (neoplasia folicular - proliferación folicular - neoplasia a células de Hürthle) Las mismas pueden ser encontradas en 15 - 30 % del total de muestras de PAAF (3) y el riesgo de carcinoma es de aproximadamente 20 - 30% (76). Las características clínicas del paciente y/o del nódulo propiamente dicho, tienen en sí mismas, una eficacia diagnóstica extremadamente bajas. Algunos marcadores moleculares como actividad de telomerasa (77), galectina - 3 (78), BRAF (79), entre otros, han sido evaluados para mejorar la eficacia diagnóstica en este tipo de diagnósticos citológicos. Si bien algunos trabajos prospectivos recientes han confirmado la eficacia diagnóstica preoperatoria del uso de algunos de estos marcadores en PAAF con diagnóstico de proliferación folicular, y encontrarse algunos de ellos disponibles para uso comercial, su alto costo y los resultados contradictorios encon- - 20 - Separata Montpellier 2011 - Vol. 19 N°10 trados en distintos reportes, hacen que su implementación en la práctica clínica como examen de rutina no esté recomendado. Muestras diagnósticas compatibles con benignidad Ante un resultado de PAAF compatible con patología benigna, no se recomiendan otros procedimientos diagnósticos inmediatos. Los nódulos benignos deberían ser controlados ecográficamente cada 6 - 18 meses. Si el nódulo se mantiene estable (no más del 50% de aumento en volumen, o < 20% incremento en al menos dos diámetros nodulares o crecimiento del componente sólido de un nódulo mixto), el intervalo entre controles podría ser mayor. Si por el contrario, hay evidencias de crecimiento o cambios, se impone la repetición de la PAAF, preferentemente bajo control ecográfico. En el caso de nódulos quísticos citológicamente benignos, los mismos pueden ser monitoreados para controlar la recurrencia de la acumulación de líquido intranodular, evento que ocurre en 60 - 90 % de los pacientes (80) (81). En los casos de quistes recurrentes y sintomáticos, los mismos serían pasibles de tratamiento quirúrgico o inyección percutánea de etanol, recomendada por numerosos investigadores (82) (83). MANEJO Y TRATAMIENTO DE BOCIO NODULAR El manejo clínico de los nódulos tiroideos se basa fundamentalmente en los resultados de la evaluación ecográfica y de la PAAF (84) (85). Muestras de PAAF no diagnósticas por PAAF: Las muestras de PAAF no diagnósticas son habitualmente provenientes de nódulos quísticos, lesiones esclerosadas benignas o malignas, nódulos con una gruesa cápsula calcificada, abscesos y lesiones necróticas o hipervasculares (86) (87); además de errores en la obtención de la muestra o en la técnica de PAAF. La repetición del procedimiento, logra obtención de material adecuado en 50 - 62% de los casos (88). No obstante, y a pesar de una correcta obtención de material y/o repetición del procedimiento, un 5 30% de los nódulos permanecen sin diagnóstico por factores relacionados con el tipo de lesión (89). En estos, se impone la PAAF bajo guía ecográfica (53). - 21 - Actualización de diagnóstico y tratamiento del bocio nodular Respecto a la tasa de malignidad en muestras no diagnósticas, la misma se reporta entre 2 - 12%. En el caso de nódulos completamente quísticos y con material puramente coloide, la conducta aconsejada sería el seguimiento clínico y ecográfico. Ante muestras de lesiones complejas con material hemático e histiocitos, se aconseja un cuidadoso control de antecedentes familiares y hallazgos clínico-ecográficos, y ante una nueva PAAF no diagnóstica, debería considerarse la resolución quirúrgica (89). En el caso de nódulos sólidos no diagnósticos, algunos autores están a favor de la conducta quirúrgica, mientras otros consideran que ante la ausencia de signos clínicos y/o ecográficos desfavorables, podría plantearse vigilancia a largo plazo (84) (85). Recientemente, Richards y col sobre un total de 241 pacientes que fueron punzados y luego enviados a cirugía, evaluaron los factores asociados con muestras no diagnósticas. Las mismas ocurrieron en 51 pacientes (21%) y la PAAF bajo guía ecográfica no disminuyó la posibilidad de muestras con igual resultado. Los pacientes con nódulos mayores a 3 cm fueron los que presentaron mayor frecuencia de muestras no diagnósticas. En esta serie se reportó un 14% de malignidad. Los factores analizados tales como edad, sexo, función tiroidea, tamaño glandular, nódulos múltiples y patología final no mostraron correlación con el hallazgo de muestras insatisfactorias (90). Nódulos benignos por PAAF Varios de los recientes consensos coinciden en que la mayoría de los nódulos con citología compatible con benignidad y sin características clínicas y/o ecográficas de riesgo, podrían ser seguidos longitudinalmente sin indicación de tratamiento (3) (91). El tiempo adecuado para la evaluación clínica y/o ecográfica, así como, la repetición rutinaria de la PAAF no están debidamente estipulados (59) (92). En la mayoría de los casos, parecería apropiado efectuar un examen clínico y ecográfico, con control de TSH en un lapso entre 6 a 18 meses. La repetición de la PAAF en forma rutinaria en estos pacientes, podría considerarse ante la baja pero no ausente posibilidad de falsos negativos (93); mientras que ante un agrandamiento significativo del nódulo, componente quístico o cambios sospechosos, se recomienda la PAAF bajo guía ecográfica (85). Respecto al tratamiento con levotiroxina, solo una minoría de pacientes muestra una disminución significativa (> 50%) en el volumen nodular (94). La respuesta es más efectiva en nódulos de pequeño tamaño y hallazgos coloides por PAAF (95), logrando la supresión de TSH a largo plazo, la prevención del incremento del tamaño de los nódulos y del volumen glandular (63) (96). - 22 - Separata Montpellier 2011 - Vol. 19 N°10 No obstante, se observa ante la suspensión del mismo, un nuevo crecimiento de los nódulos. El conocido efecto sobre la densidad mineral ósea en mujeres post menopáusicas (97) (98), así como el riesgo aumentado de fibrilación auricular en pacientes añosos con niveles suprimidos de TSH (99) (100), han hecho que el tratamiento supresivo con levotiroxina a largo plazo sea cuestionado. En 2005, Sdano y col en un meta-análisis sobre la eficacia del mismo, incluyeron nueve trabajos randomizados (609 sujetos). La terapia supresiva mostró que 88% de pacientes tuvo más de 50 % de disminución del volumen nodular comparados con placebo o no tratamiento (p = 0.008). Sin embargo, 8 sujetos debieron ser expuestos a riesgo de efectos cardiovasculares u óseos de la terapia supresiva, para uno lograr el beneficio de la misma (p = 0.0003). La revisión del único estudio con tratamiento a largo plazo (5 años) no evidenció diferencias significativas entre el tratamiento supresivo de TSH y el placebo. Los autores concluyen que este tipo de tratamiento parece más efectivo que el placebo o la falta de tratamiento para reducir significativamente el volumen de nódulos tiroideos benignos, pero que el tratamiento a largo plazo pareció ser menos eficiente y su suspensión coincidió con nuevo crecimiento nodular. Considerando los riesgos que acarrea, el uso rutinario de esta terapia no sería recomendada (101). Recientemente en un estudio en Dinamarca, se evaluó cuales pacientes portadores de bocio no tóxico no serían seleccionables para el tratamiento supresivo, considerando los criterios de exclusión sugeridos por las guías recientes de manejo del bocio nodular. Se analizaron 822 pacientes y se vio que el 84% presentaban alguna característica que hacía desaconsejable el tratamiento con hormona tiroidea (TSH baja, postmenopausia, grandes bocios o sospecha de malignidad), por lo que concluyeron que estos hallazgos, sumados a la conocida escasa eficacia y los potenciales efectos adversos, hacen no aconsejable este tipo de terapia (102). El tratamiento con levotiroxina podría ser considerado en pacientes jóvenes que habitan en áreas de iodo deficiencia, que presentan pequeños nódulos y sin evidencia de autonomía funcional. Una posibilidad es buscar una dosis de LT4 que no llegue a valores extremos de supresión de TSH, sino a valores de inhibición. En 2002, Koc y col comparando pacientes tratados con tiroxina en orden de alcanzar niveles de TSH entre 0.4 - 0.6 mUI/ml y TSH < a 0.01 mUI/ml, encontraron que la disminución del volumen nodular en ambos grupos fue igualmente efectiva y por lo tanto, aconsejan utilizar dosis de LT4 para mantener una menor inhibición de TSH, en orden de evitar las complicaciones que se producirían con las dosis necesarias para alcanzar una supresión más marcada de tirotrofina (103). Por su parte, en la actualidad la mayoría de los consensos desaconsejan el tratamiento supresivo en forma rutinaria en pacientes con bocios de larga data o de gran tamaño, en pacientes con TSH normal baja, en post menopausia, en pacientes de más de 60 años, especialmente en hombres y en general en pacientes con osteoporosis, enfermedad cardiovascular o enfermedades sistémicas (98) (99) (100). - 23 - Actualización de diagnóstico y tratamiento del bocio nodular Existen situaciones en las que la corrección quirúrgica de un nódulo benigno debe ser considerada: presión en cuello, disfagia, disnea, dolor. Es importante verificar que esos síntomas sean relacionados con el bocio y no una manifestación de trastornos asociados, tales como enfermedades cardíacas o pulmonares, desórdenes esofágicos u otros tumores de cabeza y cuello (84). Si el nódulo muestra un aumento sugestivo o cambios significativos en el control ecográfico, a pesar de una PAAF benigna, la resección quirúrgica es aconsejada por algunos autores (85). Recientemente, los procedimientos de cirugía mínimamente invasiva han sido recomendados y pueden ser realizados con un mínimo riesgo para el paciente, especialmente en el caso de pequeños nódulos (104) (105). La inyección percutánea de etanol puede ser curativa en nódulos quísticos; sin embargo, las recurrencias son muy frecuentes y la cirugía es a menudo la decisión terapéutica final en el caso de lesiones recidivantes (83). Algunos estudios prospectivos, randomizados, han mostrado que este tratamiento es superior a la simple aspiración del contenido de nódulo quístico o complejo con un gran componente líquido (106) (81) (107). La reducción del volumen es habitualmente seguida de mejoría de los síntomas compresivos locales (80). Con relación a este tratamiento en el caso de grandes lesiones quísticas, pueden ser necesarias varias sesiones (106) (81); mientras que, en el caso de nódulos hiperfuncionantes, si bien la reducción de volumen en el corto plazo ha sido demostrada (108) (109), la TSH puede continuar suprimida incluso hasta los 5 años posteriores a esta terapia (106) (81). Por estos motivos, el tratamiento con inyección con etanol no está especialmente indicado para bocios hiperfuncionantes, por la alta tasa de recurrencias, así como, por la amplia disponibilidad de otros tratamientos que han mostrado ser más efectivos. Con respecto a la implementación de este tratamiento en nódulos sólidos, hipofuncionantes desde el punto de vista centellográfico, se han reportado disminuciones clínicamente significativas (110) (111), aunque la respuesta es de menor tenor que en los nódulos quísticos, con necesidad de más intervenciones y el consecuente riesgo aumentado de efectos adversos más frecuentes (106) (81). Por su parte, la ablación con láser por guía ecográfica, evidenció ser un procedimiento mínimamente invasivo, que en dos o tres sesiones indujo disminución clínicamente evidente en el volumen nodular con la subsecuente mejoría de los síntomas locales (112). En 2007, Papini evaluó los cambios producidos en el volumen nodular en un grupo de 62 pacientes, comparando un grupo tratado con fotocoagulación por láser bajo ecografía, otro con tratamiento supresivo con LT4 y un grupo sin tratamiento. Encontró que los pacientes que fueron tratados con fotocoagulación mostraron una reducción del volumen nodular estadísticamente significativa comparada con el grupo bajo tratamiento con LT4, mientras que el grupo sin tratamiento evidenció crecimiento del tamaño nodular en el seguimiento longitudinal (113). - 24 - Separata Montpellier 2011 - Vol. 19 N°10 Dado que esta metodología de tratamiento es bastante reciente, el seguimiento a largo plazo de pacientes tratados con este procedimiento, no está aún disponible (114). Por tal motivo, la ablación por láser debería estar reservada para pacientes con síntomas locales o cosméticos que se niegan a la cirugía o en quienes el tratamiento quirúrgico implica riesgo aumentado. Tratamiento del bocio nodular con radioiodo El uso del radioiodo para el tratamiento del bocio nodular no tóxico, ha sido especialmente reportado en estudios provenientes de áreas con deficiencia relativa de iodo (115). No hay estudios disponibles que comparen el tratamiento con iodo radiactivo con y sin restricción del iodo dietario. En general, una disminución de hasta 50 - 60% puede observarse luego de 5 años de tratamiento (116), aunque cerca del 20 % de los nódulos no responde al mismo. En un estudio, Wesche y col, mostraron que, mientras el tratamiento con levotiroxina no tuvo efecto, el radioiodo logró disminuir el tamaño del bocio en alrededor del 50% luego de 1 - 2 años del tratamiento inicial (117). En grandes bocios (>100ml), la respuesta obtenida a un año del radioiodo suele ser de menor cuantía (30 - 40%) y se ha encontrado que la magnitud de la disminución correlaciona con el tamaño inicial del bocio (118) (119). Este tipo de tratamiento ha mostrado mejorar los síntomas locales y la función respiratoria (115), sin embargo, puede presentar algunos efectos adversos moderados y en general transitorios (116). Los mismos pueden ser tiroiditis por radiación, tirotoxicosis y ocasionalmente está descripto un aumento del tamaño del bocio de hasta un 25% en las primeras semanas. En cuanto a los efectos adversos tardíos, podría mencionarse el hipotiroidismo en 20 - 58% luego de 5 a 8 años del tratamiento. En algunas circunstancias, se utiliza la TSH humana recombinante (rhTSH), basado en el principio de aumentar la captación del radioiodo en el grupo de pacientes con captación baja y para disminuir la misma en el tejido extranodular (120). Datos recientes sugieren que la dosis adecuada de rhTSH para lograr un aumento significativo de la captación de iodo se encuentra en el orden de 0.03 - 0.1 mg, pudiendo administrar la dosis de iodo radiactivo 24 - 48 hs posteriores a la aplicación de rhTSH (121). Este tipo de tratamiento ha sido capaz de alcanzar una disminución del tamaño del bocio del orden del 35 a 56% comparado a la administración sin este estímulo (122), con la consiguiente mejoría de la función respiratoria. La inducción de hipertiroidismo transitorio de manera dosis - dependiente, es el efecto adverso más importante, el cual alcanza un pico 24 - 48 hs de administrado el fármaco, con normalización de la función tiroidea alrededor de las tres semanas (123). Del mismo modo, ha sido descripto un agrandamiento agudo del volumen tiroideo (24 - 48 hs). En ambos casos, los efectos adversos se han visto - 25 - Actualización de diagnóstico y tratamiento del bocio nodular aminorados cuanto menor es la dosis de rhTSH administrada (122). Por lo tanto, las distintas experiencias parecerían avalar el uso de dosis de 0.1 mg o menores como dosis óptimas de dicha sustancia (124) (125). En cuanto a las consecuencias a largo plazo, la principal es el hipotiroidismo, con un incremento entre 21 - 65% comparado con los grupos controles (122) (126). Proliferación folicular por PAAF Esta categoría diagnóstica característica es empleada para indicar una lesión con patrón folicular, en la cual el diagnóstico citológico de malignidad no es posible. Hasta la actualidad, no existen criterios morfológicos claros para distinguir las lesiones benignas y malignas (76). Una vez obtenido este resultado no se recomienda una nueva PAAF, dado que puede crear confusión en el manejo del paciente y no provee información adicional (84). En la cirugía, cerca del 20 % de tales muestras confirman el hallazgo de carcinoma (76) (127). La conducta quirúrgica y el posterior estudio histológico deben ser realizados en la mayoría de los casos. En tales circunstancias está recomendada la lobectomía más istmectomía o la tiroidectomía total, dependiendo de la situación clínica. En casos con hallazgos clínico - ecográficos favorables, un diagnóstico de proliferación folicular de bajo grado podría avalar un seguimiento sin requerir la resolución quirúrgica inmediata (128) (129) (130) (131) (132). Nódulos sospechosos por PAAF Esta categoría incluye muestras caracterizadas por hallazgos citológicos que sugieren carcinoma, pero que no cumplen con todos los criterios para definir un diagnóstico, así como muestras con celularidad inadecuada pero con características que hacen pensar fuertemente en malignidad celular (128) (129). La tasa de cáncer confirmada por histología en estos casos ronda el 60% (133) y la mayoría de ellos corresponden a carcinoma papilar en la histología definitiva (129) (134). En estos casos, se recomienda la evaluación histológica intraoperatoria, dado que puede servir en la decisión quirúrgica final (129). En algunas circunstancias podría estar recomendada la repetición de la PAAF, con el objetivo de mejorar la calidad de la muestra o facilitar estudios de inmunohistoquímica o citometría de flujo (76) (129). Nódulos malignos por PAAF Cuando es factible, el reporte citológico debería informar el tipo de carcinoma (76) (129). Si los resultados citológicos son compatibles con carcinoma diferenciado, se impone la conducta quirúrgica (47) (135). - 26 - Separata Montpellier 2011 - Vol. 19 N°10 ALGORRITMO DE DIAGNÓSTICO Y TRATAMIENTO DE BOCIO NODULAR (Adaptado de Cooper D. y col. (47) y Gharib H. y col. (136) Nódulo tiroideo detectado por palpación / ecografía Historia Clínica / Examen Físico / TSH TSH baja TSH normal o elevada Centellograma tiroideo Ecografía Nódulo hiperfuncionante Nódulo < 1 cm sin características clínicas / ecograficas sospechosas Nódulo ≥ 1 cm con características clínicas / ecograficas sospechosas Seguimiento y control PAAF bajo guía palpatoria o ecográfica según características nódulo / disponibilidad PAAF no diagnóstica PAAF maligna PAAF bajo ecografía Cirugía PAAF PAAF sospechosa profliferación de carcinoma folicular Cirugía Cirugía o control según alto o bajo grado PAAF benigna Control o tratamiento según indicaciones Persistencia de muestra no diagnóstica: control estricto o cirugía - 27 - Actualización de diagnóstico y tratamiento del bocio nodular CONCLUSIONES Aunque el bocio nodular afecta millones de individuos en el mundo, varios aspectos fundamentales relacionados con la etiología, historia natural, herramientas diagnósticas y manejo terapéutico, permanecen aún siendo discutidas. La evaluación de factores ambientales, las evidencias que sugieren algún rol de la herencia, los estudios que se refieren a susceptibilidad genética y los estudios sobre las bases moleculares del bocio, posiblemente permitan en un futuro focalizarse en acciones preventivas. Mientras tales conocimientos se perfeccionan, sigue siendo objeto de interés el debatir el manejo costo - efectivo de la enfermedad nodular tiroidea. Podría decirse a la luz de los conocimientos actuales, que la PAAF y la determinación de TSH juegan un papel central en la evaluación inicial de los pacientes con dicha patología; y más recientemente, se agrega el estudio ecográfico, tanto como método de soporte diagnóstico, así como para aumentar la eficacia de la PAAF bajo guía ecográfica. Respecto al tratamiento, este se focaliza principalmente en la terapia supresiva con LT4, el cual logra una disminución en el crecimiento del nódulo por un período limitado de tiempo en una minoría de los pacientes, sin dejar de considerar los efectos adversos hoy ya conocidos, relacionados con el hueso y sistema cardiovascular. Las evidencias disponibles sugieren que el tratamiento con LT4 podría ser evitado en sujetos eutiroideos. La cirugía, por su parte, podría ser considerada en sujetos jóvenes con grandes bocios (especialmente con prolongación subesternal) y en casos de cambios clínicos y/o muestras citológicas sospechosas de malignidad. Respecto al Yodo 131, si bien el mismo tiene en esta patología determinadas indicaciones, es una opción escasamente utilizada. Finalmente y teniendo en cuenta las investigaciones y experiencias realizadas, hay algunos interrogantes que tienen actualmente respuestas aceptadas. ¿Cuál es la definición correcta de crecimiento de un nódulo?. En un nódulo con diagnóstico inicial de benignidad, ¿cuál es el límite de crecimiento del mismo o el período de seguimiento en que estaría justificada la repetición de la PAAF?, ¿En qué casos debería realizarse la PAAF bajo guía palpatoria o ecográfica?, ¿Las características ecográficas pueden ser utilizadas para predecir el carácter de benigno o maligno de un nódulo?, ¿Pueden estas características ser utilizadas para condicionar el tipo de nódulo a punzar?, ¿Cuál es la costo - efectividad de diversas técnicas diagnósticas en el bocio nodular? - 28 - Separata Montpellier 2011 - Vol. 19 N°10 Si bien las evidencias de múltiples estudios controlados, randomizados y diversos meta-análisis sugieren que la hormona tiroidea en dosis para alcanzar niveles subnormales de TSH, puede resultar útil para disminuir el tamaño nodular y prevenir la aparición de nuevos nódulos, la indicación rutinaria de este tratamiento no está recomendada, especialmente cuando se consideran los efectos deletéreos del mismo sobre diversos tejidos. Teniendo en cuenta estas consideraciones, el mismo estaría potencialmente indicado en un grupo seleccionado de pacientes, buscando niveles óptimos de inhibición de TSH y por períodos no prolongados, como para evitar efectos adversos no buscados. Quizás debamos concluir que es en este campo en el que se esperan nuevas experiencias y nuevas herramientas terapéuticas. - 29 - Actualización de diagnóstico y tratamiento del bocio nodular BIBLIOGRAFIA (1) Mazzaferri EL 1993 Management of a solitary thyroid nodule. N Eng J Med 328: 553 - 559. (2) Tan GH, Gharib H 1997 Thyroid incidentalomas: Management approaches to nonpalpable nodules discovered incidentally on thyroid imaging. Ann Intern Med 126: 226 - 231. (3) Hegedüs L 2004 Clinical practice. The thyroid nodule. N Engl J Med 351:1764 - 1771. (4) Mandel SJ 2004 A 64-year-old woman with a thyroid nodule. JAMA 292:2632 - 2642. (5) Marqusee E, Benson CB, Frates MC, Doubilet PM, Larsen PR, Cibas ES, Mandel SJ 2000 Usefulness of ultrasonography in the management of nodular thyroid disease. Ann Intern Med 1339:696 - 700. (6) Hagag P, Strauss S, Weiss M 1998 Role of ultrasoundguided fine-needle aspiration biopsy in evaluation of nonpalpable thyroid nodules. Thyroid 8:989 - 995. (7) Wang C, Crapo LM 1997 The epidemiology of thyroid disease and implications for screening. Endocrinol Metab Clin North Am 26: 189 - 218. (8) Tunbridge WMG, Evered DC, Hall R, Appleton D, Brewis M, Clark F, Evans JG, Young E, Bird T, Smith PA 1977 The spectrum of thyroid disease in a community: The Whickham Survey. Clin Endocrinol (Oxf) 7:481 - 493. (9) Vander JB, Gaston EA, Dawber TR 1968 The significance of nontoxic thyroid nodules. Ann Intern Med 69:537 - 540. (10) Wang C, Crapo LM 1997 The epidemiology of thyroid disease and implications for screening. Endocrinol Metab Clin North Am 26: 189 - 218. - 30 - Separata Montpellier 2011 - Vol. 19 N°10 (11) Knudsen N, Perrild H, Christiansen E, Rasmussen S, Dige - Petersen H, Jørgensen T 2000 Unselected population with borderline iodine deficiency. Eur J Endocrinol 142:224 - 230. (12) Brander A, Viikinkoski P, Nickels J, Kivisaari L 1991 Thyroid gland: US screening in a random adult population. Radiology 181: 683 - 687. (13) Tan GH, Gharib H 1997 Thyroid incidentalomas: management approaches to nonpalpable nodules discovered incidentally on thyroid imaging. Ann Intern Med 126:226 - 231. (14) Medeiros - Neto G 2000 Iodine deficiency disorders. In: de Groot LJ, Jameson JL, eds. Endocrinology. Philadelphia: WBSaunders; 1529 - 1539. (15) Brix TH, Hansen PS, Kyvik KO, Hegedus L 2000 Cigarette smoking and risk of clinically overt thyroid disease: a population-based twin case-control study. Arch Intern Med 160:661 - 666. (16) Orenstein H, Peskind A, Raskind MA 1988 Thyroid disorders in female psychiatric patients with panic disorder or agoraphobia. Am J Psychiatry 145:1428 - 1430. (17) Surks MI, SievertR 1995 Drugs and thyroid function. NEngl J Med 333:1688 - 1694. (18) Farwell AP, Braverman LE 1996 Inflammatory thyroid disorders. Otolaryngol Clin North Am 29:541 - 556. (19) Greig WR, Boyle JA, Duncan A, Nicol J, Gray MJ, Buchanan WW, McGirr EM 1967 Genetic and non-genetic factors in simple goiter formation: evidence from a twin study. Q J Med 36:175 - 188. (20) Corral J, Martin C, Perez R, Sanchez I, Mories MT, San Millan JL, Miralles JM, Gonzalez-Sarmiento R 1993 Thyroglobulin gene point mutation associated with non-endemic simple goitre. Lancet 341:462 - 464). (21) Neumann S, Willgerodt H, Ackermann F, Reske A, Jung M, Reis A, Paschke R 1999 Linkage of familial euthyroid goiter to the multinodular goiter-1 locus and exclusion of the candidate genes thyroglobulin, thyroperoxidase, and Na/I symporter. J Clin Endocrinol Metab 84:3750 - 3756. - 31 - Actualización de diagnóstico y tratamiento del bocio nodular (22) Knudsen N, Perrild H, Christiansen E, Rasmussen S, Dige - Petersen H, Jørgensen T 2000 Thyroid structure and size and two-year follow-up of solitary cold thyroid nodules in an unselected population with borderline iodine deficiency. Eur J Endocrinol142:224 - 230. (23) Laurberg P, Pedersen IB, Knudsen N, Ovesen L, Andersen S 2001 Environmental iodine intake affects the type of non-malignant thyroid disease. Thyroid 11:457 - 469. (24) Morris LF, Ragavendra N, Yeh MW 2008 Evidence - based assessment of the role of ultrasonography in the management of benign thyroid nodules. World J. Surg 32: 1253 - 1263. (25) Blum M, Yee J 1997 Advances in thyroid imaging: Thyroid sonography when and how should it be used?. Thyroid Today Vol XX N°3. (26) Jarløv AE, Nygaard B, Hegedüs L, Hartling SG, Hansen JM 1998 Observer variation in the clinical and laboratory evaluation of patients with thyroid dysfunction and goiter. Thyroid 8:393 - 398. (27) Baloch Z, Carayon P, Conte - Devolx B, et al; 2003 Guidelines Committee, National Academy of Clinical Biochemistry. Laboratory medicine practice guidelines: Laboratory support for the diagnosis and monitoring of thyroid disease. Thyroid 13:3 - 126. (28) Bonnema SJ, Bennedbæk FN, Wiersinga WM, Hegedüs L 2000 Management of the nontoxic multinodular goitre: a European questionnaire study. Clin Endocrinol (Oxf) 53: 5 - 12. (29) Bonnema SJ, Bennedbæk FN, Ladenson PW, Hegedüs L 2002 Management of the nontoxic multinodular goiter: a North American survey. J Clin Endocrinol Metab 87: 112 - 117. (30) Date J, Feldt-Rasmussen U, Blichert-Toft M, Hegedüs L, Graversen HP 1996 Long-term observation of serum thyroglobulin after resection of nontoxic goiter and relation to ultrasonographically demonstrated relapse. World J Surg 20: 351 - 356. (31) Tommasi M, Brocchi A, Cappellini A, Raspanti S, Mannelli M 2001 False serum calcitonin high levels using a non-competitive two-site IRMA. J Endocrinol Invest 24: 356 - 360. - 32 - Separata Montpellier 2011 - Vol. 19 N°10 (32) Toledo S, Lourenço D, Santos M, Tavares M, Toledo R M, Menezes Correia, J 2009 Hypercalcitoninemia is not pathognomonic of medullary thyroid carcinoma Clinics 64(6):699 - 706. (33) Vierhapper H, Raber W, Bieglmayer C, Kaserer K, Weinhausl A, Niederle B 1997 Routine measurement of plasma calcitonin in nodular thyroid diseases. J Clin Endocrinol Metab 82:1589 - 1593. (34) Hahm JR, Lee MS, Min YK, Lee MK, Kim KW, Nam SJ, Yang JH, Chung JH 2001 Routine measurement of serum calcitonin is useful for early detection of medullary thyroid carcinoma in patients with nodular thyroid diseases. Thyroid 11:73 - 80. (35) Bennedbæk FN, Perrild H, Hegedüs L 1999 Diagnosis and treatment of the solitary thyroid nodule. Results of a European survey. Clin Endocrinol (Oxf) 50:357 - 363. (36) Bennedbæk FN, Hegedüs L 2000 Management of the solitary thyroid nodule: results of a North American survey. J Clin Endocrinol Metab 85:2493 - 2498. (37) Kim EK, Park CS, Chung WY, et al. 2002 New sonographic criteria for recommending fine-needle aspiration biopsy of nonpalpable solid nodules of the thyroid. AJR Am J Roentgenol. 178: 687 - 691. (38) Chan BK, Desser TS, McDougall IR, et al. 2003 Common and uncommon sonographic features of papillary thyroid carcinoma. J Ultrasound Med. 22:1083 - 1090. (39) Wienke JR, Chong WK, Fielding JR, et al. 2003 Sonographic features of benign thyroid nodules: interobserver reliability and overlap with malignancy. J Ultrasound Med. 22: 1027 Y 1031. (40) Alexander EK, Marqusee E, Orcutt J, et al. 2004 Thyroid nodule shape and prediction of malignancy. Thyroid. 14: 953 - 958. (41) Papini E, Guglielmi R, Bianchini A, et al. 2002 Risk of malignancy in nonpalpable thyroid nodules: predictive value of ultrasound and color Doppler features. J Clin Endocrinol Metab. 87: 1941 - 1946. - 33 - Actualización de diagnóstico y tratamiento del bocio nodular (42) Frates MC, Benson CB, Doubilet PM, et al. 2004 Likelihood of thyroid cancer based on sonographic assessment of nodule size and composition [Abstract]. In: Radiological Society of North America, Assembly and Annual Meeting Program. Oak Brook, IL: Radiological Society of North America 395. (43) Asteria C, Giovanardi A, Pizzocaro A, et al. 2008 US elastography in the differential diagnosis of benign and malignant thyroid nodules. Thyroid. 18: 523 - 531. (44) Tranquart F, Bleuzen A, Pierre-Renoult P, Chabrolle C, Sam Giao M, Lecomte P. 2008 Elastosonography of thyroid lesions [article in French]. J Radiol. 89: 35 - 39. (45) Rago T, Santini F, Scutari M, Pinchera A, Vitti P. 2007 Elastography: New developments in ultrasound for predicting malignancy in thyroid nodules. J Clin Endocrinol Metab. 92:2917 - 2922. (46) Horvath, E; Majlis, S; Rossi, R; Franco, C; Niedmann, J; Castro, A and Dominguez, M 2009 An ultrasonogram reporting system for thyroid nodules stratifying cancer risk for clinical management JClin Endocrinol Metab 90 (5): 1748 - 1751. (47) Cooper, D, Doherty G, Haugen B, Kloos R, Lee S, Mandel S, Mazzaferri E, McIver E, Sherman S, and Tuttle M 2006 Management Guidelines for Patients with Thyroid Nodules and Differentiated Thyroid Cancer The American Thyroid Association Guidelines Taskforce Thyroid 16(2): 1 - 33. (48) Uematsu H, Sadato N, Ohtsubo T, Tsuchida T, Nakamura S, Sugimoto K, Waki A, Takahashi N, Yonekura Y, Tsuda G, Saito H, Hayashi N, Yamamoto K, Ishii Y 1998 Fluorine-18-fluorodeoxyglucose PET vs. thallium-201 scintigraphy evaluation of thyroid tumors. J Nucl Med 39:453 - 459. (49) Cohen MS, Arslan N, Dehdashti F, Doherty GM, Lairmore TC, Brunt LM, Moley JF 2001 Risk of malignancy in thyroid incidentalomas identified by fluorodeoxyglucose-positron emission tomography. Surgery 130:941 - 946. (50) Goellner JR, Gharib H, Grant CS, Johnson DA. 1987 Fine needle aspiration cytology of the thyroid, 1980 to 1986. Acta Cytol.; 31: 587 - 590. (51) Daniels GH. 1996 Thyroid nodules and nodular thyroids: a clinical overview Comp Therapy 22:239 - 250. - 34 - Separata Montpellier 2011 - Vol. 19 N°10 (52) Gharib H, Goellner JR 1995 Fine-needle aspiration biopsy of the thyroid: an appraisal. Ann Intern Med 1993, 118:282 - 289. (53) Danese D, Sciacchitano S, Farsetti A, Andreoli M, Pontecorvi A 1998 Diagnostic accuracy of conventional vs. sonography-guided fine-needle aspiration biopsy of thyroid nodules. Thyroid, 8:15 - 21. (54) Deandrea M, Mormile A, Veglio M, et al. 2002 Fine-needle aspiration biopsy of the thyroid: comparison between thyroid palpation and ultrasonography. Endocr Pract. 8: 282 - 286. (55) Can AS, Peker K. 2008 Comparison of palpation-versus ultrasound - guided fine-needle aspiration biopsies in the evaluation of thyroid nodules. BMC Res Notes 1:12. (56) Cibas E, Alí, S 2009 The Bethesda System for Reporting Thyroid Cytopathology Am J Clin Pathol 132: 658 - 665. (57) Carmeci C, Jeffrey RB, McDougall IR, Nowels KW, WeigelRJ 1998 Ultrasound-guided fine-needle aspiration biopsy of thyroid masses. Thyroid, 8:283 - 289. (58) Ylagan LR, Farkas T, Dehner LP 2004 Fine needle aspiration of the thyroid: A cytohistologic correlation and study of discrepant cases. Thyroid, 14:35 - 41. (59) Orlandi A, Puscar A, Capriata E, Fideleff H 2005 Repeated fine-needle aspiration of the thyroid in benign nodular thyroid disease: Critical evaluation of long-term follow-up. Thyroid, 15:274 - 278. (60) Erdogan MF, Kamel N, Aras D, Akdogan A, Baskal N, Erdogan G 1998 Value of re-aspirations in benign nodular thyroid disease. Thyroid, 8:1087 - 1090. (61) Illouz, F; Rodien, P; Saint-Andre, JP; Triau, S; Laboureau-Soares, S; Dubois, S; Vielle, B; Antoine, H; and Rohmer, V 2007 Usefulness of repeated fine-needle cytology in the follow-up of non-operated thyroid nodules European Journal of Endocrinology 156 303 - 308. - 35 - Actualización de diagnóstico y tratamiento del bocio nodular (62) Alexander EK, Hurwitz S, Heering JP, Benson CB, Frates MC, Doubilet PM, Cibas ES, Larsen PR, Margusee E 2003 Natural history of benign solid and cystic thyroid nodules. Ann Intern Med. 138:315 - 318. (63) Papini E, Petrucci L, Guglielmi R, Panunzi C, Rinaldo R, Bacci V, Crescenzi A, Nardi F, Fabrinni R, Pacella CM 1998 Long-term changes in nodular goiter: A 5-year prospective randomized trial of levothyroxine suppressive therapy for benign cold thyroid nodules. J Clin Endocrinol Metab, 83: 780 - 783. (64) Brander AE, Viikinkoski VP, Nickels JI, Kivisaari LM 2000 Importance of thyroid abnormalities detected at US screening: A 5-year follow-up. Radiology, 215:801 - 806. (65) Sahin, M; Sengul, A; Berki, Z; Tutuncu, N and Guvener, N 2006 Ultrasound- guided fine needle aspiration biopsy and ultrasonographic features of infracentimetric nodules in patients with nodular goiter: correlation with pathological findings Endocrine Pathology 17(1): 67 - 74. (66) Bastin, S; Bolland, M and Croxson, M 2009 Role of ultrasound in the assessment of nodular thyroid disease Journal of Medical Imaging and Radiation Oncology 53:177 - 187. (67) Puscar, A; Orlandi, A; Frascaroli,G; Urrutia, A; Sobrado, P y Fideleff, H 2009 Ventajas y limitaciones de la inclusión de las características ecográficas en la evaluación y seguimiento de los nódulos tiroideos RAEM 46 (Supl) :124. (68) Frates, M, Benson C; Charboneau J W; Cibas, S; Clark, O; Coleman, B; Cronan,J; Doubilet, P; Evans, D; R. Goellner, J; Hay,I.; Hertzberg, B; Intenzo, C; Brooke Jeffrey, R; Langer,J 2006 Management of Thyroid Nodules Detected at US Society of Radiologists in Ultrasound Consensus Conference Statement Ultrasound Quarterly; 22:231 - 240. (69) Cooper, D; Doherty, G; Haugen, B; Kloos R; Lee, S; Mandel, S; Mazzaferri, E; McIver, B; Pacini, F; Schlumberger, M; Sherman, S; Steward D; Tuttle, M 2009 Revised American Thyroid Association Management Guidelines for patients with thyroid nodules and differentiated thyroid cancer Thyroid 19 (11):1167 - 1214. (70) American Association of Clinical Endocrinologist and American Medici Endocrinologi 2006 Medical guidelines for clinical practice for the diagnosis and management of thyroid nodules Endocr Pract, 12: 63 - 102. - 36 - Separata Montpellier 2011 - Vol. 19 N°10 (71) Cesur, M; Corapcioglu, D; Bulut, S; Gursoy, A; Ender Yilmaz, A; Erdogan, N and Kamel, N 2006 Comparison of palpation - guided fine needle aspiration biopsy to ultrasound - guided fine needle aspiration biopsy in the evaluation of thyroid nodules Thyroid 16(6): 555 - 560. (72) Izquierdo R, Arekat MR, Knudson PE, Kartun KF, Khurana K, Kort K, Numann PJ 2006 Comparison of palpation - guided versus ultrasound - guided fine needle aspiration biopsies of thyroid nodules in an outpatient endocrinology pratice Endrocr Pract 12: 609 - 614. (73) Alexander EK, Heering JP, Benson CB, Frates MC, Doubilet PM, Cibas ES, Marqusee E 2002 Assessment of nondiagnostic ultrasound-guided fine needle aspiration of thyroid nodules. J Clin Endocrinol Metab 87: 4924 - 4927. (74) Yeh MW, Demircan O, Ituarte P, Clark OH 2004 False negative fine-needle aspiration cytology results delay treatment and adversely affect outcome in patients with thyroid carcinoma. Thyroid 14: 207 - 215. (75) Gharib H, Goellner JR, Johnson DA 1993 Fine-needle aspiration cytology of the thyroid. A 12-year experience with 11,000 biopsies. Clin Lab Med 13: 699 - 709. (76) Baloch ZW, LiVolsi VA, Asa SL, Rosai J, Merino MJ, Randolph G, Vielh P, DeMay RM, Sidawy MK, Frable WJ 2008 Diagnostic terminology and morphologic criteria for cytologic diagnosis of thyroid lesions: a synopsis of the National Cancer Institute Thyroid Fine-Needle Aspiration State of the Science Conference. Diagn Cytopathol 36:425 - 437. (77) Guerra, L; Miler, E; Moiguer,S; Karner, M; Orlandi, AM; Fideleff, H, and Burdman, J 2006 Telomerase activity in fine needle aspiration biopsy samples: Application to diagnosis of human thyroid carcinoma Clinica Chimica Acta 370: 180 - 184. (78) Bartolazzi A, Orlandi F, Saggiorato E, Volante M, Arecco F, Rossetto R, Palestini N, Ghigo E, Papotti M, Bussolati G, Martegani MP, Pantellini F, Carpi A, Giovagnoli MR, Monti S, Toscano V, Sciacchitano S, Pennelli GM, Mian C, Pelizzo MR, Rugge M, Troncone G, Palombini L, Chiappetta G, Botti G, Vecchione A, Bellocco R; Italian Thyroid Cancer Study Group (ITCSG) 2008 Galectin-3-expression analysis in the surgical selection of follicular thyroid nodules with indeterminate fine-needle aspiration cytology: a prospective multicentre study. Lancet Oncol 9:543 - 549. - 37 - Actualización de diagnóstico y tratamiento del bocio nodular (79) Sapio MR, Posca D, Raggioli A, Guerra A, Marotta V, Deandrea M, Motta M, Limone PP, Troncone G, Caleo A, Rossi G, Fenzi G, Vitale M 2007 Detection of RET=PTC, TRK and BRAF mutations in preoperative diagnosis of thyroid nodules with indeterminate cytological findings Clin Endocrinol (Oxf ) 66:678 - 683. (80) Bennedbaek FN, Hegedüs L 2003 Treatment of recurrent thyroid cysts with ethanol: a randomized double-blind controlled trial. J Clin Endocrinol Metab 88:5773 - 5777. (81) Valcavi R, Frasoldati A 2004 Ultrasound-guided percutaneous ethanol injection therapy in thyroid cystic nodules. Endocr Pract 10:269 - 275. (82) Antonelli A, Campatelli A, Di Vito A, Alberti B, Baldi V, Salvioni G, Fallahi P, Baschieri L 1994 Comparison between ethanol sclerotherapy and emptying with injection of saline in treatment of thyroid cysts. Clin Investig 72:971 - 974. (83) Verde G, Papini E, Pacella CM, Gallotti C, Delpiano S, Strada S, Fabbrini R, Bizzarri G, Rinaldi R, Panunzi C, Geili D 1994 Ultrasound guided percutaneous ethanol injection in the treatment of cystic thyroid nodules. Clin Endocrinol (Oxf ) 41:719 - 724. (84) Gharib H, Papini E. 2007 Thyroid nodules: Clinical importance, assessment, and treatment. Endocrinol Metab Clin North Am.36: 707 - 735. (85) Kwak JY, Kim EK, Kim HJ, Kim MJ, Son EJ, Moon HJ. 2009 How to combine ultrasound and cytological information in decision making about thyroid nodules. Eur Radiol. 19: 1923 - 1931. (86) McHenry CR, Walfish PG, Rosen IB. 1993 Non-diagnostic fine needle aspiration biopsy: a dilemma in management of nodular thyroid disease. Am Surg. 59: 415 - 419. (87) Schmidt T, Riggs MW, Speights VO Jr. 1997 Significance of nondiagnostic fine-needle aspiration of the thyroid. South Med J. 90: 1183 - 1186. (88) Gharib H, Goellner JR. 1995 Fine-needle aspiration biopsy of thyroid nodules. Endocr Pract. 1: 410 - 417. - 38 - Separata Montpellier 2011 - Vol. 19 N°10 (89) Kini SR. 2008 Specimen adequacy and assessment, reporting system. In: Thyroid Cytopathology: An Atlas and Text. Philadelphia, PA: Lippincott Williams & Wilkins, 17 - 26. (90) Richards, M; Bohnenblust E; Sirinek, K and Bingener, J 2008 Nondiagnostic thyroid fine-needle aspiration biopsies are no longer a dilema Am J Surg 196: 398 - 402. (91) Ross DS. 2008 Diagnostic approach to and treatment of thyroid nodules. I. In: Rose BD, ed. UpToDate. Wellesley, MA: UpToDate. Last accessed December. (92) Gallo M, Pesenti M, Valcavi R. 2003 Ultrasound thyroid nodule measurements: the “gold standard” and its limitations in clinical decision making. Endocr Pract. 9: 194 - 199. (93) Menendez Torre E, Pineda Arribas J, Martinez de Esteban JP, et al. 2007 Value of repeated fine needle aspiration cytology in patients with nodular goiter. Acta Cytol; 51: 850 - 852. (94) Gharib H, James EM, Charboneau JW, Naessens JM, Offord KP, Gorman CA. 1987 Suppressive therapy with levothyroxine for solitary thyroid nodules: A double-blind controlled clinical study. N Engl J Med. 317: 70 - 75. (95) La Rosa GL, Ippolito AM, Lupo L, et al. 1996 Cold thyroid nodule reduction with L-thyroxine can be predicted by initial nodule volume and cytological characteristics. J Clin Endocrinol Metab. 81: 4385 - 4387. (96) Wemeau JL, Caron P, Schvartz C, et al. 2002 Effects of thyroid-stimulating hormone suppression with levothyroxine in reducing the volume of solitary thyroid nodules and improving extranodular nonpalpable changes: a randomized, double-blind, placebo-controlled trial by the French Thyroid Research Group. J Clin Endocrinol Metab. 87: 4928 - 4934. (97) Faber J, Galloe AM. 1994 Changes in bone mass during prolonged subclinical hyperthyroidism due to L-thyroxine treatment: a meta-analysis. Eur J Endocrinol. 130: 350 - 356. - 39 - Actualización de diagnóstico y tratamiento del bocio nodular (98) Uzzan B, Campos J, Cucherat M, Nony P, Boissel JP, Perret GY. 1996 Effects on bone mass of long term treatment with thyroid hormones: A meta-analysis. J Clin Endocrinol Metab. 81:4278 - 4289. (99) Sawin CT, Geller A, Wolf PA, et al. 1994 Low serum thyrotropin concentrations as a risk factor for atrial fibrillation in older persons. N Engl J Med. 331:1249 - 1252. (100) Parle JV, Maisonneuve P, Sheppard MC, Boyle P, Franklyn JA. 2001 Prediction of all-cause and cardiovascular mortality in elderly people from one low serum thyrotropin result: A 10-year cohort study. Lancet. 358:861 - 865. (101) Sdano, M; Falciglia,M; Welge, J and Steward, D 2005 Efficacy of Thyroid Hormone Suppression for Benign Thyroid Nodules: Meta-analysis of Randomized Trials Otolaryngology Head and Neck Surgery 133, 391 - 396. (102) Fast, S; Bonnema, S and Hegedüs, L 2008 The majority of Danish nontoxic goitre patients are ineligible for Levothyroxine suppressive therapy Clinical Endocrinology 69, 653 - 658. (103) Koc, M; Ersoz, O; Akpinar, I; Gogaz - Yavuz, D; Deyneli, O and Akalin, S 2002 Effect of low - and high-dose levothyroxine on thyroid nodule volume: a crossover placebocontrolled trial Clinical Endocrinology 57, 621 - 628. (104) Miccoli P, Minuto MN, Ugolini C, Pisano R, Fosso A, Berti P. 2008 Minimally invasive video-assisted thyroidectomy for benign thyroid disease: An evidence-based review. World J Surg. 32: 1333 - 1340. (105) Alvarado R, McMullen T, Sidhu SB, Delbridge LW, Sywak MS. 2008 Minimally invasive thyroid surgery for single nodules: an evidence-based review of the lateral miniincision technique. World J Surg. 32:1341 - 1348. (106) Guglielmi R, Pacella CM, Bianchini A, et al. 2004 Percutaneous ethanol injection treatment in benign thyroid lesions: role and efficacy. Thyroid 14: 125 - 131137. (107) Kim JH, Lee HK, Lee JH, Ahn IM, Choi CG. 2003 Efficacy of sonographically guided percutaneous ethanol injection for treatment of thyroid cysts versus solid thyroid nodules. AJR Am J Roentgenol 180: 1723 - 1726. - 40 - Separata Montpellier 2011 - Vol. 19 N°10 (108) Lippi F, Ferrari C, Manetti L, et al; the Multicenter Study Group. 1996 Treatment of solitary autonomous thyroid nodules by percutaneous ethanol injection: Results of an Italian multicenter study. J Clin Endocrinol Metab; 81: 3261 - 3264. (109) Livraghi T, Paracchi A, Ferrari C, Reschini E, Macchi RM, Bonifacino A. 1994 Treatment of autonomous thyroid nodules with percutaneous ethanol injection: 4-year experience. Radiology; 190: 529 - 533. (110) Zingrillo M, Collura D, Ghiggi MR, Nirchio V, Trischitta V. 1998 Treatment of large cold benign thyroid nodules not eligible for surgery with percutaneous ethanol injection. J Clin Endocrinol Metab; 83:3905 - 3907. (111) Bennedbaek FN, Nielsen LK, Hegedus L. 1998 Effect of percutaneous ethanol injection therapy versus suppressive doses of L-thyroxine on benign solitary solid cold thyroid nodules: A randomized trial. J Clin Endocrinol Metab; 83:830 - 835. (112) Dossing H, Bennedbaek FN, Hegedus L. 2006 Effect of ultrasound-guided interstitial laser photocoagulation on benign solitary solid cold thyroid nodules: One versus three treatments. Thyroid; 16: 763 - 768. (113) Papini, E; Guglielmi, R; Bizzarri, G; Graziano, F; Bianchini, A; Brufani, C; Pacella, S; Valle,D and Pacella, M 2007 Treatment of Benign Cold Thyroid Nodules: A Randomized Clinical Trial of Percutaneous Laser Ablation Versus Levothyroxine Therapy or Follow-up Thyroid 17: 3, 229 - 235. (114) Cakir B, Ugras NS, Gul K, Ersoy R, Korukluoglu B. 2009 Initial report of the results of percutaneous laser ablation of benign cold thyroid nodules: Evaluation of histopathological changes after 2 years. Endocr Pathol; 20:170 - 176. (115) Hegedus L, Bonnema SJ, Bennedbaek FN. 2003 Management of simple nodular goiter: Current status and future perspectives. Endocr Rev; 24:102 - 132. (116) Weetman AP. 2007 Radioiodine treatment for benign thyroid diseases. Clin Endocrinol (Oxf); 66:757 - 764. - 41 - Actualización de diagnóstico y tratamiento del bocio nodular (117) Wesche MF, Tiel-V Buul MM, Lips P, Smits NJ, Wiersinga WM. 2001 A randomized trial comparing levothyroxine with radioactive iodine in the treatment of sporadic nontoxic goiter. J Clin Endocrinol Metab; 86:998 - 1005. (118) Bonnema SJ, Bertelsen H, Mortensen J, et al. 1999 The feasibility of high dose iodine 131 treatment as an alternative to surgery in patients with a very large goiter: Effect on thyroid function and size and pulmonary function. J Clin Endocrinol Metab; 84:3636 - 3641. (119) Huysmans DA, Hermus AR, Corstens FH, Barentsz JO, Kloppenborg PW. 1994 Large, compressive goiters treated with radioiodine. Ann Intern Med.; 121:757 - 762. (120) Nielsen VE, Bonnema SJ, Hegedüs L. 2004 The effects of recombinant human thyrotropin, in normal subjects and patients with goitre. Clin Endocrinol (Oxf).; 61:655 - 663. (121) Fast S, Nielsen VE, Bonnema SJ, Hegedüs L. 2009 Time to reconsider nonsurgical therapy of benign non-toxic multinodular goitre: focus on recombinant human TSH augmented radioiodine therapy. Eur J Endocrinol.; 160:517 - 528. (122) Nielsen VE, Bonnema SJ, Boel-Jorgensen H, Grupe P, Hegedüs L. 2006 Stimulation with 0.3-mg recombinant human thyrotropin prior to iodine 131 therapy to improve the size reduction of benign nontoxic nodular goiter: a prospective randomized double-blind trial. Arch Intern Med.; 166:1476 - 1482. (123) Barca MF, Gruppi C, Oliveira MT, et al. 2007 Cardiovascular assessment of hyperthyroid patients with multinodular goiter before and after radioiodine treatment preceded by stimulation with recombinant human TSH. Endocrine.; 32:175 - 181. (124) Nielsen VE, Bonnema SJ, Hegedüs L. 2006 Transient goiter enlargement after administration of 0.3 mg of recombinant human thyrotropin in patients with benign nontoxic nodular goiter: a randomized, double-blind, crossover trial. J Clin Endocrinol Metab.; 91:1317 - 1322. (125) Pena S, Arum S, Cross M, et al. 2006 123I thyroid uptake and thyroid size at 24, 48, and 72 hours after the administration of recombinant human thyroid-stimulating hormone to normal volunteers. J Clin Endocrinol Metab.; 91:506 - 510. - 42 - Separata Montpellier 2011 - Vol. 19 N°10 (126) Silva MN, Rubio IG, Romao R, et al. 2004 Administration of a single dose of recombinant human thyrotrophin enhances the efficacy of radioiodine treatment of large compressive multinodular goitres. Clin Endocrinol (Oxf).; 60:300 - 308. (127) Castro MR, Gharib H. 2005 Continuing controversies in the management of thyroid nodules. Ann Intern Med.; 142:926 - 931. (128) British Thyroid Association. 2002 Guidelines for the management of thyroid cancer in adults. London: Royal College of Physicians of London and the British Thyroid Association, Available at: http://www. british-thyroid-association.org/complete%20guidelines.pdf. (129) European Federation of Cytology Societies Fadda G. SIAPEC consensus review [written February 27, 2009; cited June 2009]. Available at: www.efes.eu. (130) Yassa L, Cibas ES, Benson CB, et al. 2007 Long-term assessment of a multidisciplinary approach to thyroid nodule diagnostic evaluation. Cancer.; 111: 508 - 516. (131) Puscar, A; Orlandi, A; Capriata, E; Frascaroli, G; Sobrado, P and Fideleff, H 2005 Usefulness of subcategorization of follicular neoplasm (FN) diagnosis in the management of thyroid nodule disease Thyroid, 15 (Suppl): 152. (132) Reyes, A; Gagneten, C; Laudi, R; De Rosa, R; Olstein, G y Lowenstein, A 2003 Citologías tiroideas de alto riesgo: Resultados del uso de nuestra clasificación RAEM, 40 (2): 106. (133) Yang J, Schnadig V, Logrono R, Wasserman PG. 2007 Fine needle aspiration of thyroid nodules: A study of 4703 patients with histologic and clinical correlations. Cancer; 111:306 - 315. (134) Cersosimo E, Gharib H, Suman VJ, Goellner JR. 1993 “Suspicious” thyroid cytologic findings: outcome in patients without immediate surgical treatment. Mayo Clin Proc.; 68: 343 - 348. (135) Pacini F, Schlumberger M, Dralle H, Elisei R, Smit JW, Wiersinga W; European Thyroid Cancer Taskforce. 2006 European consensus for the management of patients with differentiated thyroid carcinoma of the follicular epithelium Eur J Endocrinol; 154:787 - 803. - 43 - Actualización de diagnóstico y tratamiento del bocio nodular (136) Gharib, H; Papini, E; Paschke, R; Duick, D; Valcavi, R; Hegedüs, L; Vitti, P for the AACE/AME/ETA Task Force on Thyroid Nodule 2010 American Association of Clinical Endocrinologists, Associazione Medici Endocrinologi, and European Thyroid Association Medical Guidelines for Clinical Practice for the Diagnosis and Management of Thyroid Nodules. J. Endocrinol Invest 33 (5 Suppl): 51 - 56. - 44 -