INTRODUCCION A LA DETERMINACION DE
Anuncio

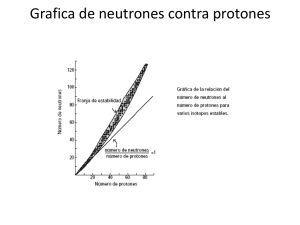
Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom INTRODUCCION A LA DETERMINACION DE RADIOCARBONO POR EL METODO DE ESPECTOMETRIA DE ACELERADOR DE MASA. Conteo por AMS Hay tres principales isótopos de carbono que se producen naturalmente - 12C, 13C (ambos estables) y 14C (inestable o radioactivo). Estos isótopos están presentes en la siguientes cantidades: 12C en un 98,89%, 13C en un 1,11% y 14C en un 0,00000000010%. Por lo tanto, un átomo de carbono 14 existe en la naturaleza por cada 1.000.000.000.000 de átomos de carbono 12 de la materia viva o (1 en un billón). El método del radiocarbono se basa en la velocidad de desintegración del carbono radiactivo o isótopo inestable 14 (14C), que está formado en la atmósfera superior a través del efecto de los neutrones de rayos cósmicos a nitrógeno-14. La reacción es: 14 N + n => 14C + p (Donde n es un neutrón y p es un protón) El carbono 14 formado se oxida rápidamente a 14CO2 y entra a los modos de vida de las plantas y animales del planeta a través de la fotosíntesis y la cadena alimenticia. La rapidez de la dispersión del 14C en la atmosfera se ha demostrado mediante mediciones de carbono radiactivo producido a partir de las pruebas de bombas termonucleares. El carbono 14 también entra a los océanos de la tierra en un intercambio atmosférico y como carbonato disuelto [el inventario completo de 14C se denomina el intercambio de depósito de carbono (Aitken, 1990)]. Las plantas y animales que utilizan carbono en las cadenas alimenticias biológicas toman C durante sus vidas. Ellos existen en equilibrio con la concentración de 14C de la atmósfera; es decir, el número de átomos de 14C y átomos de carbono no radioactivo se mantiene aproximadamente igual a través del tiempo. Tan pronto una planta o animal muere, cesa en ellos la función metabólica de absorción de carbono; no hay reposición de carbono radioactivo, sólo desintegración. 14 Libby, Anderson y Arnorld (1949) fueron los primeros en medir la velocidad de esta decadencia. Encontraron que después de 5,568 años, la mitad del material restante se ha deteriorado, y así sucesivamente (ver figura 1). La vida media (t ½) es el nombre dado a este valor el cual Libby midió en 5568±30 años. Esto se conoció como la vida media de Libby. Después de 10 vidas medias, hay una muy pequeña cantidad de carbono presente en una muestra radiactiva. A unos 50,000 – 60,000 años, y luego, el límite de la técnica es alcanzado (más allá de este tiempo, otras técnicas radiométricas deben ser utilizadas para fechados). Mediante la medición de la concentración de 14C o radioactividad residual de una muestra cuya edad no se conoce, es posible obtener el conteo o el número de eventos de desintegración por gramo de carbono. Al comparar esta con los niveles actuales de actividad (madera en 1890 corregido para la descomposición a 1950 dC) y Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom utilizando la medida de vida media, se hace posible calcular una fecha de la muerte de la muestra. A medida que el carbono 14 se desintegra emite una partícula beta débil (b), o electrón, que posee una energía media de 160keV. La decadencia se puede mostrar: 14 C => 14N + b Por lo tanto, el 14C decae nuevamente a 14N. Existe una relación cuantitativa entre la desintegración del 14C y la producción de una partícula beta. La decadencia es constante pero espontánea. Es decir, la probabilidad de desintegración de un átomo de 14C en una muestra discreta es constante, lo que requiere la aplicación de métodos estadísticos para el análisis de conteo de datos. De ello se deduce que cualquier material que se compone de carbono puede ser fechado. Aquí radica la verdadera ventaja del método de radiocarbono - es capaz de ser aplicado uniformemente en todo el mundo en cualquier material residual que contenga carbono. Debido a esto, los laboratorios de todo el mundo están produciendo ensayos de radiocarbono para la comunidad científica. La técnica de 14C ha sido y continua siendo aplicada y utilizada en muchos campos diferentes, incluyendo la hidrología, la ciencia atmosférica, la oceanografía, la geología, paleoclimatología, la arqueología, la biomedicina y ciencias de los materiales. El método de Espectrometría por Acelerador de Masa por conteo directo de isotopos de C fue realizado por primera vez en 1977 por los equipos de investigación científica en Rochester y Toronto, de General Ionex Corporation, y poco después medidas adicionales fueron llevadas a cabo en las Universidades de Simon Fraser y McMaster (Gove, 1994). 14 La datación por radiocarbono utilizando la Espectrometría por Acelerador de Masas (AMS) difiere de los métodos de conteo por desintegración en que la cantidad de 14C en la muestra es medida directamente, en lugar de esperar que ocurran eventos individuales de desintegración radioactiva. Esto hace que la técnica sea de 1.000 a 10.000 veces más sensible que la de conteo por desintegración. La sensibilidad mejorada se logra mediante la aceleración de los átomos de la muestra como iones a altas energías utilizando un acelerador de partículas, además de técnicas de detección de partículas nucleares. Además, debido a la mayor sensibilidad, los tiempos de conteo son reducidos considerablemente (de minutos a horas, no de días) y muestras con tamaños mucho más pequeños puede ser medidas de forma rutinaria. Debido a esto, un rango mucho mayor de tipos y tamaños de muestra pueden ser ahora medidos, algo que previamente las técnicas de conteo proporcional de gases o LSC no podía. En la técnica AMS 14C, el elemento de interés (muestra de carbono) es químicamente separado de la muestra original, convertido en grafito, es presionado a un Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom cátodo (soporte de la muestra objetivo) donde se forma un tapón de grafito sólido o capa, y se coloca entonces en una fuente de iones por pulverización catódica de un acelerador. Esta metodología describe la preparación general de muestras de grafito (química) y los procedimientos de conteo por AMS en Beta Analytic Inc. Para muestras orgánicas y de carbonato. A través de este proceso, el CO2 producido a partir de materiales carbonaceos en bruto es criogénicamente purificado (separado de gases no combustibles) y reducido a grafito sólido para la medición en un AMS. Conversion de Muestra de Carbono a Grafito Pre tratamiento de la Muestra Cada muestra debe ser primero pre tratada o el material de interés aislado para asegurar que sólo el carbono primario de interés será analizado. Como muchos tipos de carbono que contienen los compuestos están presentes, diferentes regímenes de tratamientos previos han sido desarrollados para concentrar y aislar la fracción de carbono particular de interés antes al fechado (véase el Glosario de Pre tratamiento – Protocolos de Pre tratamiento estándar de Beta Analytic). Generación de CO2 El carbono de la muestra pre tratada se oxida primero a CO2 ya sea por la combustión en una corriente de oxigeno o por reacción directa con Óxido Cúprico reducido (alambre de metal/ en polvo) para orgánicos o por medio de hidrólisis ácida para carbonatos. Combustión o Hidrólisis Ácida Orgánico + O2 + ∆H => Carbonato CO2 +HCl => CO2 (Muestra) (900°C) (Muestra) Orgánico + CuO + ∆H => CO2 (Muestra) (900°C) El CO2 generado es entonces criogénicamente purificado mediante la eliminación de vapor de agua y cualquier gas no combustible/condensable pasando a través de una serie de trampas de hielo seco / agua-metanol (~ -78°C) y, dependiendo del tipo de muestra una serie de trampas de nitrógeno líquido / Pentano granizado (~ -129°C). Conversión de CO2 a Grafito (reacción de grafitización ) Para producir las pequeñas cantidades de carbono elemental desde CO2 para la medición en un AMS, se utiliza la reacción Bosch (Manning y Reid, 1977) que es la Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom reacción química entre el dióxido de carbono y de hidrógeno que produce el carbono elemental (grafito), agua y calor. La reacción se lleva a cabo como dos reducciones sucesivas; primero a monóxido de carbono y luego a carbono, que penetra y se adhiere a la superficie del polvo de Cobalto (catalizador). Más detalles sobre las técnicas de grafitización y catalizadores puede ser encontrado en Vogel et al, 1984. La reacción completa es la siguiente: (550 a 650 °C) CO2 (q) + 2 H2 (g) → C(s) + 2 H2O (l) (Co catalizador) Sin embargo, la reacción anterior es en realidad el resultado de dos reacciones separadas. La primera reacción - la reacción de desplazamiento de agua-gas es una rápida: CO2 + H2 → CO + H2O La segunda reacción controla la velocidad de la reacción completa: CO + H2 → C + H2O Durante el procedimiento de grafitización, limpiado criogénicamente, CO2 seco producido a partir de la combustión o hidrólisis ácida es transferido criogénicamente (con Nitrógeno Líquido a 196 ° C) * a una célula de grafitización especialmente diseñada bajo vacío que se compone de vidrio Vycor, vidrio Pyrex y acero inoxidable (diseño modificado después de Lloyd et al, 1991). * NOTA: Antes de la introducción del CO2 sobre el catalizador de cobalto en la celda de grafitización, el cobalto es pre-acondicionado para eliminar cualquier contaminante de carbono siendo evacuados y luego purgados varias veces con hidrógeno y finalmente reducido sobre ¾ atmósferas de hidrógeno durante 1-2 horas a 550 ° C a 650 ° C. La célula de grafitización pre-acondicionada contiene tanto 4,5 mg o 3,5 mg alícuota de polvo de metal de cobalto (una mezcla de 85% Alfa Aesar -400 mesh, y 15% Alfa Aesar Puratronic -22 mesh) que es específico para el tamaño de la muestra a ser grafitizada. Sobre la base de la cantidad de CO2 generado durante la combustión, el CO2 es criogénicamente transferido a una célula de grafitizacion conteniendo una cantidad de cobalto que es tres veces mayor en peso que la cantidad de carbono (en proporción de 3:1), entonces Hidrogeno de Investigación de grado Ultra-Puro se añade de tal manera que la cantidad de hidrógeno es tres veces mayor en volumen que la muestra de CO2 (en proporción de 3:1). La celula de grafitización se coloca entonces en un horno a una temperatura de 550 ° C a 650 ° C durante un período de 10-12 horas mientras que el Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom agua producida durante la grafitización es continuamente removida, a través de un dedo frío que es parte de la célula de grafitización, por hielo seco Metanol slush (-78 º C). Después de pasado 10-12 horas, la presión en la celda de grafitización es inspeccionada para asegurar que la reacción se ha completado (que el CO2 se ha convertido en grafito con un rendimiento mínimo que cae en el intervalo de 80-100%). Si la reacción no se ha completado, la célula de grafitización es devuelta al horno, y se hace reaccionar de nuevo durante un periodo de 4-10 horas. Si la reacción alcanza a una conclusión en un 80100% tras el segundo intento de grafitización, la muestra se analiza de nuevo a partir de la combustión. Si la grafitización se ha completado, la célula de grafitización se coloca bajo un vacío y se deja calentar a temperatura ambiente causando que todo el vapor de agua formado durante la reacción de grafitización sea bombeada, dejando el grafito seco. El grafito es purgado una vez con Argón ultra-puro (99,999) el cual ha pasado través de un tamiz molecular de ascarite para eliminar cualquier CO2 y un agente secado de silicona para eliminar cualquier vapor de agua. Esto seguido por el bombeo a un vacío luego purgando otra vez con Argón ultra-puro (99,999) para igualar con la presión atmosférica. El tubo de grafitización es retirado entonces de la célula de grafitización y tapado con una cubierta de hoja delgada de aluminio y se coloca en una gradilla de tubos de prueba listos para ser cargados en un cátodo para el recuento de AMS. Cargando el cátodo AMS (Destino) La muestra de grafito preparado se coloca en un cátodo de AMS (de destino) vertiendo el grafito directamente desde el tubo de grafitización en el cátodo. El polvo de grafito se comprime a continuación a un mínimo de 150 psi (lectura manométrica) en una prensa Arbor o por golpes con una prensa de perno. La superficie del grafito (frente del objetivo) es ópticamente inspeccionado para garantizar que el grafito parezca ser liso y homogéneo (es decir, el grafito no debe verse irregular o manchado en la coloración). El cátodo (de destino) se coloca entonces en una rueda de cátodo y se coloca en el AMS junto con las suficientes muestras ciegas de aseguramiento de calidad (muestras previamente medidas por LSC y/o AMS) con las normas modernas necesarias (OXI y / o OXII, orgánica y carbonato de espacios en blanco, normas de edad TIRI conocida, orgánica y/o carbonato) para la detección C14/13 y C14/12. Contando AMS Como es común con otros tipos de espectrometría de masas, el conteo de AMS se realiza mediante la conversión de los átomos de la muestra (grafito) en un haz de iones que se mueven rápidamente (átomos cargados). La masa de estos iones se separa entonces por la aplicación de los campos magnético y eléctrico y medido por la técnica de detección de partículas nucleares. La medición de radiocarbono por espectrometría de masas es muy Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom difícil debido a que su concentración es de menos de un átomo en un 1.000.000.000.000 (un billón) de átomos. Así, el acelerador se utiliza para ayudar a eliminar los iones que podrían confundirse con radiocarbono antes de la detección final. La muestra se coloca en la fuente de iones (como grafito) y es ionizado por bombardeo con iones de cesio y luego centrado en un haz de rápido movimiento. Los iones producidos son negativos que impiden la confusión de 14C con 14N puesto que el nitrógeno no forma un ion negativo. El imán de curvatura primero se utiliza en la misma manera que el imán en un espectrómetro de masa ordinaria para seleccionar iones de masa 14 (esto incluye gran número de iones de 12CH2- y 13CH- y algunos pocos de 14C-). Los iones entonces entran al acelerador. A medida que viajan al detector terminal son acelerados lo suficiente que cuando colisionan con las moléculas de gas en el separador, todos los iones moleculares (tales como 12CH2 y 13CH) son divididos permitiendo que la mayoría de los iones de carbono pasen a través de un segundo imán curvo que separa mucho más los iones con la masa y momento esperados de 14C, 13C, y 12C. Finalmente, los iones filtrados de 14C Iones entran al detector donde su velocidad y energía son revisadas por lo que el número de iones de 14C en la muestra pueden ser contados. No todos los átomos de radiocarbono son puestos en la fuente de iones en el extremo del detector, es por esto que isotopos estables, tales como 12C y 13C son medidos también con el fin de supervisar la eficiencia de la detección. Para cada muestra, una relación de 14C / 13C se calcula y se compara con las mediciones realizadas bajo las normas con proporciones conocidas. Las incertidumbres en AMS Poco después de que los primeros espectrómetros AMS fueron desarrollados, la calidad de las mediciones AMS se demostró mediante comparaciones del error en la media de una serie de n mediciones AMS para una muestra (error externo) para la estadística de recuento de los conteos totales medidos, N, en la serie de mediciones (error interno). Si μ es la media de un grupo de mediciones individuales, cada uno con varianza σ2 (aquí se supone equivalente para todas las mediciones), las precisiones fraccionadas mostraron ser equivalentes: σ2 ext = σ2 / n (n -1) µ2 = σ2 int = 1/N total En efecto, la equivalencia del error estándar de la media de las mediciones de AMS a la precisión esperada de las estadísticas de recuento demostró el grado en que el espectrómetro y su funcionamiento están libres de error sistemático. (Wölfli, et al., 1983; Donahue, Jull, & Zabel, 1984; Farwell, et al, 1984;. Suter, et al, 1984). El desarrollo de un material de muestra uniforme para AMS de 14C, un grafito fulereno o filamentoso (Vogel et al, 1984), a condición de haces intensos de iones para todas las muestras y normas, con lo que las incertidumbres internas y externas a la equivalencia rutinaria para una cuantificación AMS exacta (σ ≤ 1%). (Bonani, et al, 1987;. Vogel, Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom at al., 1987). Fraccionamiento isotópico de Muestra (Relación de Isótopos Estables 13/12C) Con el fin de proporcionar determinaciones de radiocarbono que son a la vez exactas y precisas, es necesario medir los isótopos estables de 13C y 12C y sus relaciones. Esto se realiza mediante la extracción de una pequeña cantidad de CO2 generado durante la combustión o hidrólisis ácida y la medición de la relación relativa de 13/12C a la norma de espectrometría de masa PDB. Esta relación se usa más tarde en el cálculo de la edad y error radiocarbónicos para corregir fraccionamiento isotópico en la naturaleza. El fraccionamiento durante la transferencia geoquímica de carbono en la naturaleza produce variación en la distribución de equilibrio de los isótopos de carbono (12C, 13C y 14 C). Craig (1953) identificó por primera vez que ciertos procesos bioquímicos alteran el equilibrio entre los isótopos de carbono. Algunos procesos, como la fotosíntesis, por ejemplo, favorece un isótopo sobre otro, así que después de la fotosíntesis, el isótopo 13C se agota en un 1,8% con respecto a su proporción natural en la atmósfera (Harkness, 1979). A la inversa el carbono inorgánico disuelto en los océanos está generalmente enriquecido en un 0,7% en 13C respecto al dióxido de carbono atmosférico. La medida de fraccionamiento isotópico en la relación 14C/12C, el cual debe medirse con precisión, es aproximadamente el doble que para la relación medida de 13C/12C medido. Si el fraccionamiento isotópico se produce en los procesos naturales, una corrección puede realizarse por medio a la medición de la relación del isótopo 13C al isótopo 12C en la muestra a ser datada. La relación se mide utilizando un espectrómetro de masa común. La composición isotópica de la muestra que se está midiendo se expresa como que delta13C la cual representa la diferencia en partes por mil (por mil) entre la muestra carbono-13 y el contenido de la norma internacional de carbonato PDB (Keith et al, 1964;. Aitken, 1990). Un valor d13C, entonces, representa la desviación por mil (partes por mil) de la norma PDB. PDB se refiere a la Formación de la belemnita en el Cretácico en Peedee, Carolina del Sur, EE.UU. Esta nomenclatura ha cambiado recientemente a VPDB (Coplen, 1994). En resumen, el fraccionamiento isotópico se refiere a la fluctuación en las proporciones del isótopo de carbono como un resultado de procesos bioquímicos naturales como una función de su masa atómica (Taylor, 1987). Estas variaciones no están relacionadas con el tiempo y la desintegración natural radiactiva. Es una práctica común en los laboratorios de radiocarbono el corregir actividades de radiocarbono para el fraccionamiento de la muestra. Las edades resultantes se denominan "normalizadas", es decir, la actividad medida es modificada con respecto a -25 por mil VPBD. El factor de corrección se debe añadir o restar a la edad radiocarbónica convencional. El valor deltaC13 para una muestra puede proporcionar información importante sobre el Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom medio del cual procede la muestra o las mezclas de los materiales utilizados para producirla porque el valor de isótopos de la muestra refleja la composición isotópica del medio ambiente inmediato. En el caso de los moluscos, por ejemplo, las conchas marinas suelen poseer un valor dC13 de entre -1 y +4 por mil, mientras que los depósitos fluviales poseen un valor de entre -8 y -12 por mil. Por lo tanto, en el caso en que el entorno preciso de la cáscara no es conocido, es posible determinar el más probable por el análisis del resultado dC13. El fraccionamiento también describe variaciones en las relaciones isotópicas de carbono traídas por causas no naturales. Por ejemplo, las muestras pueden ser fraccionadas en el laboratorio a través de una variedad de medios. Por lo general, esto se debe a la falta de atención de detallar y una conversión incompleta de la muestra de una etapa a otra o de una parte del laboratorio a otro. En el recuento de centelleo líquido, por ejemplo, la síntesis incompleta de acetileno durante la preparación de carburo de litio puede resultar en un bajo rendimiento y el fraccionamiento simultáneo. De manera similar, la transferencia de gases en un sistema de vacío puede implicar un error en el fraccionamiento si el gas de muestra no se le permite equilibrar a través del volumen total. Los átomos de mayor o menor masa pueden ser favorecidos en tal situación. Sí, no obstante, toda la muestra es convertida completamente a partir de una forma a otra (por ejemplo, sólido a gas, acetileno a benceno), entonces no se producirá fraccionamiento. Edad Radiocarbonica y Error de Cálculo Gran parte de la información presentada en esta sección se basa en el artículo Stuiver, M. y Polach, H. A. 1977. Discusión: Presentación de datos 14C. Radiocarbono 19, 355-63. La edad radiocarbónica de una muestra se obtiene por medición de la radiactividad residual. Esto se calcula a través de la medición cuidadosa de la actividad residual (por gramo de C) que permanece en una muestra cuya edad es desconocida, comparada con la actividad presente en las muestras modernas y Antecedentes. Norma Moderna La principal norma moderna de radiocarbono es NIST (Instituto Nacional de Normas y Tecnología, Gaithersburg, Maryland, EE.UU.) Ácido Oxálico I (C2H2O4). El ácido oxálico I es la designación NIST de SRM 4990 B y se denomina HOx1. Este es el estándar internacional de datación de radiocarbono. El noventa y cinco por ciento de la actividad de ácido oxálico a partir del año 1950 es igual a la actividad medida del estándar de radiocarbono absoluto el cual es madera en 1890. La madera en 1890 fue elegido como el estándar de radiocarbono porque crecía anterior a los efectos de combustibles fósiles de la revolución industrial. Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom La actividad de la madera de 1890 es corregida por la desintegración radiactiva hasta 1950. Así que 1950, es el año 0 BP por convención en la datación por radiocarbono y se considera que es el 'presente'. El año 1950 fue elegido por ninguna razón en particular que no sea para honrar a la primera publicación del primer cálculo de fechas de radiocarbono en diciembre de 1949 (Taylor, 1987; 97). El estándar de ácido oxálico se hizo a partir de un cultivo de la remolacha azucarera en 1955. Habían producidas unas 1000 libras. La relación isotópica de HOx I es -19,3 por mil con respecto a (WRT) el estándar de belemnita PBD (Mann, 1983). El estándar de ácido oxálico, que era desarrollado ya no está disponible en el mercado. Otro estándar, oxálico Ácido II se preparó cuando las acciones de HOx 1 comenzaron a disminuir. El ácido oxálico II estándar (HOx 2; NIST SRM designación C 4990) se hizo a partir de un cultivo de melaza de remolacha francesa en 1977. A principios de 1980, un grupo de 12 laboratorios midieron las relaciones de los dos estándares. La relación de la actividad de ácido oxálico II a 1 es 1,2933 ± 0,001 (la media ponderada) (Mann, 1983). La relación isotópica de HOx II es -17,8 por mil. Según Stuiver y Polach (1977), todos los laboratorios deben informar sus resultados ya sea directamente relacionado con el ácido oxálico NBS o indirectamente a través de una subnorma que está relacionada con ella. Antecedentes de Detección Es vital para un laboratorio de radiocarbono el conocer la contribución a la actividad de muestra de rutina la no radiactividad de la muestra. Obviamente, esta actividad es adicional y debe ser eliminada de los cálculos. Con el fin de hacer concesiones para conteos a fondo y evaluar los límites de detección, los materiales que especialistas de radiocarbono pueden estar bastante seguros no contienen actividad se miden en idénticas condiciones de conteo como las muestras normales. Muestras de fondo por lo general consisten en muestras geológicas de edad infinita, tales como carbón, lignito, piedra caliza, carbonato antiguo, antracita, mármol o madera de pantano. Por la medición de la actividad de una muestra de fondo, la radioactividad normal presente en una muestra de edad desconocida que se está midiendo puede ser explicada y deducida. Edades de radiocarbono convencionales (BP) Una medición de radiocarbono denomina una edad radiocarbónica convencional (o CRA) es obtenida utilizando un conjunto de parámetros esbozados por Stuiver y Polach (1977), en la revista Radiocarbono. Un nivel de tiempo independiente de actividad de 14C para el pasado es asumido en la medición de un CRA. La actividad de este nivel hipotético de actividad 14C es igual a la actividad de la norma internacional radiocarbono absoluta. El Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom radiocarbono convencional Edad BP se calcula utilizando la ecuación radiocarbono de descomposición: t = -8033 ln (Asn/Aon) Cuando -8033 representa el tiempo de vida media de 14C (Stuiver y Polach, 1977). Aon es la actividad en recuentos por minuto de la norma moderna. Asn es el equivalente cpm de la muestra. 'ln' representa el logaritmo natural. Un CRA abarca las siguientes convenciones recomendadas: • una vida media de 5568 años; • el uso de ácido oxálico I o II como el estándar moderno de radiocarbono; • Corrección para el fraccionamiento isotópico de muestras (deltaC13) a un normalizado o valor base de -25,0 por mil con respecto a la relación de 12C/13C en el estándar de carbonato VPDB (más sobre el fraccionamiento y deltaC13); • el uso de 1950 dC como 0 BP, es decir, todas las edades del 14C regresan hacia atrás en el tiempo a partir de 1950; • la suposición de que todos los depósitos de 14C se han mantenido constantes en el tiempo. Los términos adicionales algunas veces exigen ser o informados con, o en lugar de la Edad radiocarbónica convencional estándar BP resultado de la cual todas las demás son derivadas matemáticamente. Se trata de la "Edad de medición de radiocarbono BP", Porcentaje Carbono Moderno (PMC), Resultado base biológica promedio (expresado en %), porcentaje de la media del contenido de carbono biogénico, CO2 por ciento de biomasa, Fracción carbón Moderno (fmdn o FMC), así como d14C, D14C, 14C delta, ∆14C y delta 13/12C (todos los cuales se expresan en notación per mil (%) en lugar de la notación por ciento.) d14C representa el agotamiento por mil en 14 muestras de carbono antes de la corrección de fraccionamiento isotópico y se mide por; d14C=((Asn/Aon) – 1) 1000 por mil D14C representa el valor "normalizado" de d14C. "Normalizado" significa que la actividad es escalada en relación con el fraccionamiento de la muestra, o su valor deltaC13. Todos los valores D14C están normalizados al valor base de - 25,0 por mil con respecto al carbonato estándar (VPDB). D14C se calcula utilizando: D14C = d14C – 2(dC13 + 25) (1 + d14C/1000) por mil Este valor puede entonces ser usado para calcular el CRA usando la ecuación dada más abajo: Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom Figura 1 – Curva de desintegración para 12C mostrando la actividad de una media vida (t/2). Los términos “%Moderno” o “pMC” y D14C se muestran relacionando en este diagrama junto con la edad Radiocarbonica en años BP (Antes de 1950 dC). Reporte de Edad Si el depósito corregido de edad radiocarbónica convencional calculada está dentro de la últimos 200 años, se debe, por convención, ser denominado 'moderno' (Stuiver y Polach, 1977; 362). Si la edad de la muestra es posterior a 1950, se denomina superior a Moderno, o > Moderno. Por ciento absoluto moderno (% M o PMC - 'por ciento de carbono moderno ») es calculado utilizando: %M = 100 x Asn/Aabs ó Asn/Aon (1/8267(y-1950)) x 100 porciento Donde Aabs es la actividad estándar internacional absoluta, 1/8267 es la vida útil basada en la vida media nueva (5730 años), Y = el año de la medición de la norma pertinente. Esta es una expresión de la relación de la actividad moderna neta frente a la actividad residual normalizada de la muestra, expresada como un porcentaje y representa la proporción de átomos de radiocarbono en la muestra en comparación con el presente en el año 1950 dC. Así, Modern% se convierte en un útil término en la descripción de las mediciones de radiocarbono en los últimos 45 años en los que, debido a la influencia del radiocarbono artificial a la atmósfera como resultado de pruebas de la bomba nuclear, la "edad" de cálculo se convierte en un "futuro" de cálculo. Si la muestra se aproxima a D14C = -1000 por mil dentro de 2 desviaciones estándar, se considera que es indistinguible de los antecedentes del laboratorio, es decir, no puede ser capaz de ser separado con confianza de las tasas de recuento del laboratorio las cuales resultan a partir de una muestra que no contiene radionúclido. En este ejemplo, una edad mayor-que es calculada. n ejemplo de una edad mayor que es > 55, 000 años o > 50, 000 años (Gupta y Polach, 1985). Las muestras cuya edad se sitúa entre moderno y antecedentes y son dadas edades finitas. Los errores estándar publicados con cada análisis de radiocarbono son generalmente redondeados por convención (Stuiver y Polach, 1977). Una vez más, no todos los laboratorios se suscriben a estas convenios, algunos no redondean las edades. Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom Error Estándar y Fuentes de Error El análisis estadístico es necesario en la datación por radiocarbono, porque la desintegración del 14C aunque constante, es espontánea. No es posible medir la totalidad radiactividad en una muestra dada, de ahí la necesidad de algún tipo de análisis estadístico de los datos contados. La distribución de los acontecimientos contados desintegración del 14C, en un cierto tiempo, produce un patrón. El patrón se denomina una "curva de distribución normal". Una distribución normal o “Gaussiana” describe la distribución en forma de campana simétrica el grupo de acontecimientos en torno a la media o promedio de los datos. En una distribución normal, 2 fuera de 3, o sea el 68% de los valores o recuentos observados estarán incluidas en una desviación estándar de la media de los datos. En dos desviaciones estándar, el 95% de los recuentos observados se encuentran dentro del rango y de tres desviaciones estándar, 99% de los recuentos que comprenden la distribución normal caerán dentro de esta región. Cada fecha de radiocarbono es publicada como una edad radiocarbónica convencional con "error estándar". Este es el valor '±' y por convención es de ± 1 sigma. El error estándar se basa principalmente en estadísticas de conteo, sin embargo otras fuentes de error son posibles y sus efectos se enumeran a continuación: Resumen; La exactitud de las fechas de radiocarbono (modificado de Polach, HA 1976). fuentes de error 1. Precisión de la determinación de la edad 2. Inherente a. vida media de 14C b. fraccionamiento de 12C/13C c. Estándar moderno de 14C d. Variación de las últimas Efecto de la edad determinación Medidas para reducir al mínimo el error incurrido Estadística; típicamente Moderno ± 1% o menos Muestras grandes, tiempos de conteo más largos, repetir ensayos de muestras Libby vida media del 3% Multiplicar CRA por 1,03 demasiado bajo si es necesario Variable, hasta 450 años Los análisis de isótopos para concha, estables usando Espectrometría de masa Variable > 80 años Verificación cruzada Internacional de las normas secundarias. 0-800 años, más allá Calibración anillo de CA12 ka no árbol; Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom tasas de producción 14C e. Distribución de 14C en la naturaleza f. Cambios de concentración de 14C en la atmosfera 3. Contaminación 4. Edad biológica del material 5. Asociación de muestra y evento 6. Humano 7. Interpretación de resultados determinado de lo contrario interpretar resultados en escala de tiempo radiométrica. dependencia latitudinal Interpretación de resultados de superficie del océano400 a 750 años. Océano profundo 1800 años. Efecto industrial ca - Interpretación de 2.5% y efecto de la resultados bomba atómica +160% en la atmosfera. Interpretación de Nil a 300 años hasta resultados, análisis y a 15 ka,> 20 ka datación de fracciones posible más allá de pretratadas extraídas. 25 ka. <10 años a >1000 años Identificación de especies de material en el caso de madera y carbón vegetal a muestras de vida corta solamente. Intermedio Interpretación de resultados Intermedio Intermedio Cuidado en campo y laboratorio Cuidado en interpretación, enfoque y colaboración interdisciplinario Exactitud y Precisión en Datación por Radiocarbono Es importante tener en cuenta el significado de "exactitud" y "precisión" de datación de radiocarbono. La exactitud se refiere a la fecha de ser una estimación "verdadera" de la edad de una muestra dentro del intervalo de los límites estadísticos o el valor ± de la fecha. Por lo tanto, en aras del argumento, si tuviéramos una muestra de datación por radiocarbono de los huesos humanos de un individuo que sabíamos que murió en 1066 dC y obtuvo una fecha de 1040 ± 40 dC, habríamos fechado el evento de su muerte de forma exacta. Sin embargo, si la fecha obtenida fuera 1000 ± 15 dC, seriamos inexactos. En términos de precisión, sin embargo, la primera es imprecisa en comparación con el último por el valor de error tan grande indicado. Como tal, puede verse que la fecha de Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom 1000 ± 15 AD mientras que puede ser muy precisa es, en este caso, inexacta. Efectos Reservorio Una edad radiocarbónica convencional o CRA no tiene en cuenta diferencias específicas entre la actividad de los diferentes reservorios de carbono. La CRA se deriva mediante un cálculo de edad basado en la actividad corregida de desintegración del estándar de radiocarbono absoluto (1890 madera dC) que está en equilibrio con los niveles de radicarbono atmosférico (como se ha mencionado anteriormente, 1890 madera ya no se utiliza como el estándar de radiocarbono primario, en su lugar normas de Ácido Oxálico I y II fueron correlacionadas con la actividad de la norma original). A fin de determinar las edades de las muestras que fueron formadas en equilibrio con diferentes depósitos a estos materiales, es necesario proporcionar una corrección de edad. Implícita en la Edad radiocarbónica convencional BP es el hecho de que no se ajusta para esta corrección. Muestras de radiocarbono que obtienen su carbono a partir de una fuente de carbono diferente (o depósito) a la atmósfera puede producir lo que se llaman las edades aparentes. Los mariscos vivos hoy en día en un lago dentro de una cuenca de piedra caliza, por ejemplo, producirán una fecha de radiocarbono demasiado vieja. La razón de esta anomalía es que la piedra caliza, que es resistida y disuelta en bicarbonato, no tiene carbono radiactivo. Así, esta diluye la actividad del lago significando esto que la radiactividad se agota en comparación con la actividad de 14C en otro lugar. El lago, en este caso, tiene un depósito de radiocarbono diferente que la de la mayoría del radiocarbono en la biosfera y por lo tanto una edad radiocarbónica exacta requiere que una corrección se haga para dar cuenta de ello. Uno de los efectos reservorio más comúnmente referenciado se refiere al océano. La diferencia media entre una fecha de radiocarbono de una muestra terrestre como un árbol, y una concha en el medio marino es de unos 400 años de radiocarbono (ver Stuiver y Braziunas, 1993). Esta edad aparente del agua oceánica es causada tanto por el retraso de las tasas de cambio entre el CO2 atmosférico y el bicarbonato del océano, y el efecto de dilución provocado por la mezcla de las aguas de superficie con aguas profundas que ascienden y que son muy viejas (Mangerud 1972). Una corrección de depósito por lo tanto se debe ser hecha a cualquier fechado convencional de conchas para dar cuenta de esta diferencia. El hueso humano puede ser un medio problemático para fechar en algunos casos debido a consumo humano de pescado, cuya etiqueta de 14C reflejará el depósito del océano. En tal caso, es muy difícil determinar la exacta diferencia del depósito y por lo tanto aplicar una corrección a la medida edad radiocarbónica. Fechas radiocarbónicas falsas causadas por las emanaciones volcánicas de radiocarbono de CO2 disminuido probablemente pertenecen también a la categoría de correcciones de reservorios. Las plantas que crecen en las proximidades de fumarolas volcánicas activas dan lugar a una edad radiocarbónica muy vieja. Bruns et al. (1980) midió la radiactividad Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom de plantas modernas que crecen cerca de aguas termales calentadas por rocas volcánicas en Alemania Occidental y demuestra una deficiencia en radiocarbono de hasta 1500 años través de la comparación con los niveles modernos de radiocarbono atmosférico. Del mismo modo, este efecto se ha observado en plantas en la bahía de Palaea Kameni cerca del sitio prehistorico de Akrotiri, que fue sepultado por la erupción del volcán Thera hace más de 3500 años (ver Weninger, 1989). El efecto ha sido sugerido como proporcionar fechas en error por la erupción de Thera, que se ha relacionado con la desaparición de la civilización minoica en el Egeo. Una moderna planta que crece cerca de la emanaciones tenía una edad aparente de 1390 años. El efecto volcánico no obstante, tiene una distancia limitada. Bruns et al. (1980) encontró que a 200 m de distancia de la fuente, plantas arrojaron una edad de acuerdo con lo esperado. Se sugirió que la influencia de CO2 empobrecido disminuyó rápidamente al aumentar la distancia desde la fuente. Discrepancias radiocarbónicas debido a las emisiones volcánicas de CO2 son una popular fuente de munición de puntos de vista de los fundamentalistas deseosos de presentar pruebas que muestren que el método del radiocarbono es de alguna manera fundamentalmente erróneo. Efecto de Suess o Industrial Desde alrededor de 1890, el uso de combustibles fósiles y la industria han generado grandes cantidades de CO2 que se emiten a la atmósfera. Debido a que la fuente de los combustibles industriales han sido predominantemente materiales de edad geológica infinita (por ejemplo, carbón, petróleo), cuyo contenido de radiocarbono es nula, la actividad de radiocarbono en la atmosfera se ha reducido en la primera parte del siglo 20 hasta la década de 1950. La señal de radiocarbono atmosférico ha sido, en efecto, diluido sobre un 2%. Hans Suess (1955) descubrió el efecto industrial (nombrado después de él) en la década de 1950. Un número de investigadores encontraron que la actividad que se espera de material en crecimiento desde 1890 dC fue menor. La conclusión lógica de esto era que con el fin de obtener un estándar de referencia de radiocarbono moderno, que representa el actividad radiocarbono de la 'actualidad', no se puede utilizar muy bien la madera que creció en la década de 1900, ya que se vio afectada por este efecto industrial. Así fue que la madera de 1890 fue utilizada como el estándar moderno radiocarbono, extrapolado por la desintegración hasta 1950 dC. Efecto de la Bomba Atómica Desde aproximadamente 1955, las pruebas termonucleares han incrementado considerablemente el reservorio atmosférico de 14C. El 14C es "artificial" o 14C 'bomba', producido por bombas nucleares que produjeron un enorme flujo de neutrones térmicos. El efecto de esto ha sido a casi el doble de la cantidad de actividad de 14C en el carbono que lleva los materiales terrestres (Taylor, 1987). Beta Analytic Inc. (Headquarters) Beta Analytic Limited 4985 SW 74 Court London Bioscience Innovation Centre Miami, Florida 33155 2 Royal College Street USA London NW10NH United Kingdom De Vries (1958) fue el primero en identificar este efecto "bomba atómica". En el hemisferio norte la cantidad de carbono artificial en la atmósfera ha alcanzado un pico en 1963 (en el hemisferio sur en torno a 1965) en aproximadamente un 100% por encima de los niveles normales. Desde entonces, la cantidad ha disminuido debido al intercambio y la dispersión de 14C en el ciclo del carbono del sistema terrestre. La presencia del carbono bomba en la biosfera de la Tierra ha permitido que sea utilizado como trazador para investigar la mecánica de carbono mezclado y procesos de intercambio.