trabajo datación carbono 14 - Departamento de Sistemas Informáticos
Anuncio

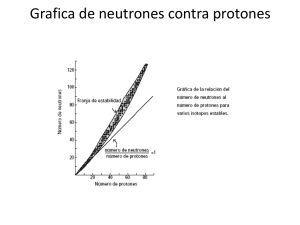
TRABAJO DATACIÓN CARBONO 14 AUTORES Antonio Jesús Caro Alonso-Rodríguez Francisco Alfonso Cano González INDICE 1 INTRODUCCION CARBONO 14 2 DATACION POR RADIOCARBONO -INTRODUCCION -QUIMICA BASICA -MEDIDAS Y ESCALAS 3 APLICACIONES INFORMATICAS -CALIB 14C CALIBRATION PROGRAM INTRODUCCION FUNCIONAMIENTO CALIB EJEMPLO -CALPAL INTRODUCCION FUNCIONAMIENTO CALPAL EJEMPLO 4 BIBILIOGRAFIA 1 INTRODUCCION En la tierra se conocen actualmente 112 elementos, de los cuales 90 comprendidos entre el hidrógeno y el uranio son elementos naturales, pero existen el promecio y el tecnecio que no son naturales, y los demás se obtienen por reacciones nucleares. La clasificación de los elementos de la tierra podía ser en 4 grandes grupos: 1. Siderófilos: se refiere a aquellos elementos amantes del Fe ó parecidos a él, y normalmente se encuentran e el núcleo metálico ó cerca de este, pero también se encuentran en la corteza terrestre pero su aparición es debida a reacciones que los originan. 2. Litófilos: son aquellos elementos amantes de las rocas, forman parte de ellas, estos se combinan fácilmente con él O y X y son los más abundantes de la corteza terrestre. 3. Calcófilos: Son aquellos que se combinan fácilmente con S, Ar, Se... También forman parte mayoritariamente de la corteza terrestre. 4. Atmósfilos: Son aquellos elementos gaseosos que forman parte de la atmósfera terrestre. El carbono se conoce desde la antigüedad. El término Carbono procede del latín carbo que significa carbón de leña. Los primeros compuestos de carbono se identificaron en la materia viva a principios del siglo XIX, y por ello el estudio de los compuestos de carbono se llamó química orgánica. El carbono es un elemento ampliamente difundido en la naturaleza, aunque sólo constituya aproximadamente el 0,025% de la corteza terrestre, en la que se encuentra principalmente en forma de carbonatos. Podemos encontrar el carbono en tres variedades alotrópicas: diamante, grafito y carbono amorfo que son sólidos con puntos de fusión sumamente altos y son insolubles en todos los disolventes a temperaturas ordinarias. Las propiedades físicas de las tres formas difieren ampliamente a causa de las diferencias en la estructura cristalina. En el diamante, una de las sustancias más duras conocidas, cada átomo se vincula a otros cuatro átomos en una estructura tridimensional. Es incoloro y no conduce la electricidad. A temperaturas ordinarias el carbono se caracteriza por su baja reactividad. A altas temperaturas reacciona directamente con la mayoría de los metales para formar carburos, y con el oxígeno para formar monóxido de carbono (CO) y dióxido de carbono (CO2 ). El carbono en forma de coque se usa para quitar oxígeno a minerales de óxidos metálicos a fin de obtener el metal puro. El carbono también forma compuestos con la mayoría de los elementos no metálicos, aunque algunos de estos, como el tetracloruro de carbono (CCl4 ) deben ser obtenidos indirectamente. La estructura del carbono es la siguiente: Las principales características de una molecular de carbono son las siguientes: El carbono es un elemento químico de número atómico 6 y símbolo C. Es sólido a temperatura ambiente. Sus formas alotrópicas incluyen, sorprendentemente, una de las sustancias más blandas (el grafito) y la más dura (el diamante) y, desde el punto de vista económico, uno de los materiales más baratos (carbón) y uno de los más caros (diamante). Más aún, presenta una gran afinidad para enlazarse químicamente con otros átomos pequeños, incluyendo otros átomos de carbono con los que puede formar largas cadenas, y su pequeño radio atómico le permite formar enlaces múltiples. Así, con el oxígeno forma el dióxido de carbono, vital para el crecimiento de las plantas (ver ciclo del carbono); con el hidrógeno forma numerosos compuestos denominados genéricamente hidrocarburos, esenciales para la industria y el transporte en la forma de combustibles fósiles; y combinado con oxígeno e hidrógeno forma gran variedad de compuestos como, por ejemplo, los ácidos grasos, esenciales para la vida, y los ésteres que dan sabor a las frutas; además es vector, a través del ciclo carbononitrógeno, de parte de la energía producida por el Sol. El principal uso industrial del carbono es como componente de hidrocarburos, especialmente los combustibles fósiles (petróleo y gas natural). El segundo se está imponiendo como fuente de energía por su combustión más limpia. Otros usos son: • El isótopo carbono-14, descubierto el 27 de febrero de 1940, se usa en la datación radiométrica. • El diamante Es transparente y muy duro. • Como elemento de aleación principal de los aceros. • En varillas de protección de reactores nucleares. • Las pastillas de carbón se emplean en medicina para absorber las toxinas del sistema digestivo y como remedio de la flatulencia. • El carbón activado se emplea en sistemas de filtrado y purificación de agua. • El carbón amorfo ("hollín") se añade a la goma para mejorar sus propiedades mecánicas. Los compuestos de carbono tienen un amplio rango de toxicidad. Los gases orgánicos eteno, etino y metano son explosivos e inflamables en presencia de aire. Por el contrario, muchos otros compuestos no son tóxicos sino esenciales para la vida. Los seres vivos estamos formados por moléculas orgánicas, proteínas, ácidos nucleicos, azúcares y grasas. Todos ellos son compuestos cuya base principal es el carbono. La química orgánica es la química del carbono y de sus compuestos. La parte más importante de la química orgánica es la síntesis de moléculas. Los compuestos que contienen carbono se denominaron originalmente orgánicos porque se creía que existían únicamente en los seres vivos. Sin embargo, pronto se vio que podían prepararse compuestos orgánicos en el laboratorio a partir de sustancias que contuvieran carbono procedentes de compuestos inorgánicos. Los alcanos, son los compuestos más simples de la química orgánica, formados sólo por carbono e hidrógeno. Un ejemplo de esa molécula es el conocido como el “cubano”: Los isótopos de un elemento químico son las variedades en las que se suelen presentar sus átomos. Existen en la naturaleza tres isótopos del carbono: el 12C, el 13C y el 14C. Son tres variedades de un mismo elemento químico, el carbono, cuyos núcleos contienen el mismo número de protones (seis), pero un número diferente de neutrones (seis, siete y ocho), lo que les hace, a pesar de tener propiedades químicas semejantes, tener una masa atómica diferente: doce, trece y catorce.. Casi el 99 % del CO2 atmosférico es del tipo que contiene el carbono ligero 12C. Una pequeña parte, el 1,1 % del CO2 , es algo más pesado, ya que contiene 13C. Y finalmente existe también en la atmósfera, en muy pequeña proporción, un tipo de CO2 que contiene 14C , que es radiactivo e inestable, y cuyas aplicaciones han solido ser fundamentalmente paleocronológicas. El 14C (que posee 6 protones y 8 neutrones) tiene la particularidad de que es un isótopo inestable, que poco a poco va transmutándose en nitrógeno, 14N (que posee 7 protones y 7 neutrones), y desaparece según la reacción : C = N + ß + neutrino En compensación de esta pérdida, nuevos átomos de 14C se forman continuamente en la atmósfera como producto del choque de neutrones cósmicos sobre otros átomos atmosféricos de nitrógeno : neutrón + N = C + H Estos neutrones son parte de la radiación cósmica galáctica que tras atravesar el Sistema Solar llega a la atmósfera terrestre. Los choques de los rayos cósmicos con los átomos de 14N y, por lo tanto, la producción de 14C, es máxima a unos 15 km de altura. Rápidamente los átomos de 14C así formados se oxidan a CO2 y se difunden y se mezclan por toda la atmósfera con el resto del CO2. Los procesos de desintegración y de formación de 14C se compensan de tal forma que la concentración de 14C en la atmósfera es "más o menos" constante. El carbono-14 (14C, masa atómica=14.003241) es un radioisótopo del carbono y fue descubierto el 27 de febrero de 1940 por Martin Kamen y Sam Ruben. Su núcleo contiene 6 protones y 8 neutrones. Willard Libby determinó un valor para el periodo de semidesintegración o semivida de este isótopo: 5568 años. Debido a su presencia en todos los materiales orgánicos, el carbono-14 se emplea en la datación de especímenes orgánicos. El método de datación por radiocarbono es la técnica más fiable para conocer la edad de muestras orgánicas de menos de 60.000 años.El proceso de fotosíntesis incorpora el átomo radiactivo en las plantas, de manera que la proporción 14C/12C en éstas es similar a la atmosférica. Los animales incorporan, por ingestión, el carbono de las plantas. Ahora bien, tras la muerte de un organismo vivo no se incorporan nuevos átomos de 14C a los tejidos, y la concentración del isótopo va decreciendo conforme va transformándose en 14N por decaimiento radiactivo. Así pues, al medir la cantidad de radiactividad en una muestra de origen orgánico, se calcula la cantidad de 14C que aún queda en el material. Así puede ser datado el momento de la muerte del organismo correspondiente. Es lo que se conoce como "edad radiocarbónica" o de 14C, y se expresa en años BP (Before Present). Unos datos de interés serían: 2 Datación por radiocarbono -Introducción La datación por radiocarbono es un método de datación radiométrica que utiliza el isótopo carbono-14 (14C) para determinar la edad de materiales que contienen carbono hasta unos 60.000 años, puede emplearse en madera, carbón, hueso, sedimentos, y cualquier cosa orgánica que forme parte de la Biosfera, con un error promedio de unos 80 años. Dentro de la arqueología es considerada una técnica de datación absoluta. La velocidad con la que un elemento se desintegra disminuye exponencialmente con el tiempo.La desintegración de un núcleo cualquiera se produce al azar, y el número de núcleos que se desintegran en un intervalo de tiempo es directamente proporcional al tiempo y al número de núcleos existentes. N: Número de núcleos radiactivos en un instante t No: Número de núcleos radiactivos iniciales λ: Constante de desintegración radiactiva t: Tiempo transcurrido N = No x e-λt Despejando el tiempo (t) e incorporando el valor de λ obtenemos la ecuacion del calculo de la fecha radiocarbonica N = No x e-λt->Tiempo (t) = -8033 x Ln(N / No) A partir de la ecuación de la ley de la desintegración radiactiva puede obtenerse el tiempo que ha transcurrido desde que una muestra tenía la misma actividad en C-14 que una muestra moderna hasta el momento de la medida.Existen diferentes factores que alteran el contenido de C-14 en la muestra y la forma de detectarlo, por lo que al valor de la actividad medido en los contadores hay que realizar distintas correcciones (fondo, fraccionamiento isotópico, dilución) La fecha radiocarbónicaes un intervalo de edad, puesto que al valor calculado hay que incluirle su desviación estándar. Existen varios metodos para la datacion del Carbono 14, estos son: • Medida de la actividad (emisión beta): – Contador de centelleo líquido – Contadores proporcionales de gas (GPC) • Medida del número de átomos C14: – Acelerador acoplado a espectrometría de masa (AMS) – Contador de centelleo líquido Se mide la actividad específica (número de desintegraciones por unidad de tiempo) de una muestra y se compara con la curva de desintegración A = Ao*e -λt Las moléculas orgánicas se excitan al paso de la radiación y se desexcitan por fluorescencia.La luz producida es detectada por los fotomultiplicadoresy convertida en un pulso Líquido Contador de centelleo liquido Tiene una serie de ventajas y desventajas respecto a los otros metodos de datacion del carbono 14 Las ventajas que presenta es que hace medidas mas rapidas y en serie y tiene una gran precision en la medida. Por el contrario tiene una serie de desventajas como pueden ser es una tecnica destructiva, entre 5 y 200 gramos, y no es la tecnica mas rapida puesto que la tecnica de Acelerador acoplado a espectrometria de masa (AMS) es mejor. -Contadores proporcionales de gas Se basan en la recolección directa de la ionización producida por la partícula β emitida en la desintegración del 14C, al atravesar un gas sometido a una diferencia de potencial. Se llena con el gas que contiene la muestra, normalmente CO2, CH4 o C2H2, se aplica una diferencia de potencial que permite acelerar los electrones lo suficiente para que se produzcan ionizaciones secundarias. Los electrones secundarios producidos se aceleran igualmente dando nuevas ionizaciones que, finalmente, produce una avalancha electrónica sobre el ánodo. Aunque hay un gran número de ionizaciones secundarias, el contador trabaja de modo que éstas son proporcionales al número de sucesos primarios. Contador proporcional de gas -Acelerador de acoplado a espectrometría de masa (AMS) La espectrometría de masas es una técnica experimental que permite la medición de iones derivados de moléculas. El espectrómetro de masas es un instrumento que permite analizar con gran precisión la composición de diferentes elementos químicos e isótopos atómicos, separando los núcleos atómicos en función de su relación masa-carga (m/z). Puede utilizarse para identificar los diferentes elementos químicos que forman un compuesto, o para determinar el contenido isotópico de diferentes elementos en un mismo compuesto. Con frecuencia se encuentra como detector de un cromatógrafo de gases, en una técnica híbrida conocida por sus iniciales en inglés, GC-MS. En términos generales, moléculas diversas tienen masas diversas, hecho utilizado por un espectrómetro de masas para determinar qué moléculas están presentes en una muestra. Espectrometro de masa Los iones se envían a un compartimiento de aceleración y se pasan a través de una lámina metálica. Se aplica un campo magnético a un lado del compartimiento que atrae a cada uno de los iones con la misma fuerza (suponiendo carga idéntica) y se los desvía sobre un detector. Naturalmente, los iones más ligeros se desviarán más que los iones pesados porque la fuerza aplicada a cada ion es igual pero los iones ligeros tienen menos masa. El detector mide exactamente cuán lejos se ha desviado cada ion y, a partir de ese dato se calcula el "cociente masa por unidad de carga". Con esta información es posible determinar con un alto nivel de certeza cuál es la composición química de la muestra original. -Química Básica El Carbono tiene dos isótopos estables no radiactivos, carbono-12 (12C), y carbono-13 (13C). Además hay minúsculas cantidades de isotopos inestables de carbono-14 (14C) en la Tierra. El carbono-14 tiene un periodo de semidesintegración de 5730 años y podría haber desaparecido de la tierra hace mucho tiempo si no fuera por los incesantes impactos de rayos cósmicos sobre el nitrógeno en la Atmósfera de la Tierra, donde se forma más isótopos. Cuando los rayos cósmicos entran en la atmósfera, experimentan varias transformaciones, incluyendo la producción de neutrones. Los neutrones resultantes participan en la siguiente reacción en la que uno de N átomos son lanzados fuera de la molécula de nitrógeno(N2) en la atmósfera: La tasa más alta de producción de carbono-14 tiene lugar en altitudes entre 9 y 15 km (30,000 y 50,000 ft), y en altas latitudes geomagnéticas, pero el carbono-14 se esparce uniformemente sobre la atmosfera y reacciona con el oxígeno para formar dióxido de carbono. Este dióxido de carbono también penetra en los océanos, disolviéndose en el agua. El proceso de fotosíntesis incorpora el átomo radiactivo en las plantas de manera que la proporción 14C/12C en éstas es similar a la atmosférica. Los animales incorporan, por ingestión, el carbono de las plantas. Ahora bien, tras la muerte de un organismo vivo no se incorporan nuevos átomos de 14C a los tejidos y la concentración del isótopo va decreciendo conforme va transformándose en 14N por decaimiento radiactivo: Así pues, al medir la cantidad de radiactividad en una muestra de origen orgánico se calcula la cantidad de 14C que aún queda en el material. Así puede ser datado el momento de la muerte del organismo correspondiente. -Medidas y Escalas Las medidas se hacen tradicionalmente contando la desintegración radiactiva de átomos individuales de carbono por recuento proporcional gaseoso o por recuento de centelleo líquido, pero estas dos técnicas son relativamente insensibles y están sujetas a relativamente grandes incertidumbres estadísticas cuando las muestras son pequeñas (menores de 1g de carbono). Si hay poco carbono al comenzar, una semivida que dura mucho significa que solo unos pocos átomos se desintegran mientras se intenta su detección (4 atoms/s) /mol tan solo después de la muerte, de este modo, p ej: 1 (atom/s)/mol después de 10,000 años). La sensibilidad ha sido incrementada usando técnicas basadas en espectrometría de masas (AMS), donde todos los átomos de 14C pueden ser contados directamente, no solamente aquellos que se desintegran durante el intervalo de recuento asignado para cada análisis. La técnica de AMS permite datar muestras que contienen tan solo unos pocos miligramos de carbono. Las edades de radiocarbono brutas (es decir, aquellas no calibradas), lo que se conoce por edad radiocarbónica o de 14C, se expresan en años BP (Before Present- Hasta hoy día). Esta escala equivale a los años transcurridos desde la muerte del ejemplar hasta el año 1950 de nuestro calendario, siendo este el número de años de radiocarbono antes de 1950, basadas en un nominal (y asumiendo como constante) el nivel de carbono-14 en la atmósfera igual al nivel de 1950. Se elige esta fecha por convenio y porque en la segunda mitad del siglo XX, los ensayos nucleares provocaron severas anomalías en las curvas de concentración relativa de los isótopos radiactivos en la atmósfera. 3 APLICACIONES INFORMATICAS CALIB 14C CALIBRATION PROGRAM Introducción CALIB hace la conversión de la edad radicarbonica a los años del calendario habitual mediante calibración. Calculando la probabilidad de la distribución de la edad verdadera. Visión general de la aplicación Lo primero que haremos será explicar el funcionamiento del programa y seguidamente expondremos algunos ejemplos para su total comprensión Funcionamiento de Calib En nuestro programa disponemos de unos ficheros de datos que son con los que compararemos los datos de entrada que nosotros queramos calibrar. Estos datos han sido científicamente probados y estudiados. Para elementos marinos comparamos con el fichero Marine04 y para elementos no marinos tenemos dos ficheros. Los del hemisferio norte (IntCal04) y el hemisferio sur (SHCal04) El programa calcula la edad de los restos por el método de cálculo de la distribución de la probabilidad calibrada, este método consiste en la siguiente formula: P(R) = exp -[(g(T)-U)²/2s²]/s/(2p)½. Siendo U = edad radiocarbonica g(Y) = Curva de Calibración Sigma = Representa el estándar de la edad del carbono 14 Veremos las opciones que nos proporciona el programa para calcular la edad de los elementos, definiendo la entrada de los datos como los tipos de graficas y los resultados que CALIB nos proporciona. Datos de Entrada Los datos de entrada podemos introducírselos al programa mediante una hoja de cálculo, donde el fichero tendría que llamarse C14INP En esta hoja de Cálculo se introducen todos los datos necesarios para la calibración que explicaremos mas adelante Al presionar en FileNew Obtenemos una tabla de dialogo para acceder a la fila de la hoja de calculo que queremos evaluar Esta tabla contiene los siguientes variables a rellenar: Los datos que tendremos que rellenar serian: -Sample Number: Selecciona la fila de la Hoja de calculo que queremos evaluar y nos rellena automáticamente el resto de campos que tiene esta tabla. -Radiocarbon age: Aqui se establece la edad radiocarbonica que vamos a calibrar -Age Uncertainty: Aquí indicamos la edad de incertidumbre en años -Percent Marine: Aquí indicamos el porcentaje de restos marinos que el elemento posee en el caso que posea dichas caracteristicas -Delta R: Valor para los elementos con un componente marino en años -Delta R Uncertainty: Valor para los elementos con un componente marino en años de incertidumbre -Sample Age Span: Aquí indicamos la edad abarcada en años -Laboratory Error: Aquí indicamos el error que consideramos que puede tener el estudio a realizar, normalmente lo establecemos a uno. Tipos de Graficas Los tipos de graficas que podemos contemplar con Calib son los siguientes: Múltiple -Bar Plot -Block Plot -Probability plot Simple -Single Probability Normalized to Unit area -Single Probability Normalized to Unit height -Single sample cumulative Probability -Single sample with calibration curve Estas graficas nos ayudan a representar la edad de los datos calibrado y una comparative con la edad radiocarbonica introducida a calibrar Resultados Para generar los resultado debemos dar a Calibratego para que se calcule la edad en años del elemento a tratar. Los resultados que nos ofrece Calib los podemos ver en la hoja de calculo calout que son generados al pulsar go, y en la misma aplicación indicándonos un rango entre el comienzo y el final de su edad Aquí podemos ver un pequeño ejempl de salida: XY1235 Southern Hemisphere terrestrial sample Radiocarbon Age 812±16 Calibration data set: shcal04.14c # McCormac et al. 2004 One Sigma Ranges: [start:end] relative area [1230 AD:1249 AD] 0,541252 [1262 AD:1275 AD] 0,458748 Two Sigma Ranges: [start:end] relative area [1226 AD:1278 AD] 1, Ejemplo de Calib Veremos un ejemplo para comprender mejor el comportamiento de Calib y como calcula la edad en años de los elementos Introduciremos los datos en la hoja de calculo C14INP Abrimos el programa CALIB y abrimos la hoja creada Como podemos observar vamos a tratar 7 elementos que son los siguientes: 1 Elemento Terrestre del hemisfero Norte 2 Elemento Terrestre del hemisferio Sur 3 Elemento Marino de islandia usando Delta R = 3 4 Elemento con 50% de materia Marina usando Delta R = 4 5 Elemento con 70% de materia Marina de chile usando Delta R = 6 6 Elemento Terrestre del hemisferio Norte con una corta Vida 7 Elemento Terrestre del hemisferio Norte con una larga Vida Una vez introducidos todos los elementos con el boton enter, podemos calibrar las edades y ver las graficas comparativas: Para no poner todas las graficas disponibles ni los 7 elementos veremos algunas graficas para el primer elemento, entres ellas: Single sample with calibration curve Single Probability Normalized to Unit area Single sample cumulative Probability Para ver los resultados podemos verlos en el propio programa como veremos a continuación: Aquí vemos los resultados para los primeros 4 elementos y nos muestra las edades en años por ejemplo para el primer elemento podemos observar que: EL primer elemento es de 1226 AD al1278 AD Por ultimo los datos de salida son exportados a un fichero de excel con datos mas sofisticados sobre la datación de los elementos, ahora veremos un ejemplo de ese fichero. CALPAL Introducción CalPal es un programa de radiocarbono calibrado que proporciona un paquete de medidas destinado a apoyar la investigación sobre el comportamiento homínido en respuesta a los cambios climáticos. Los resultados se presentaran en forma de gráficos en el contexto de datos climáticos. CalPal se desarrolla para apoyar estudios cronológicos en el periodo glacial mediante el método de radiocarbono. CalPal es un programa escrito en Fortran 95 (Lahey LF95 v5.7 compilador) con interfaz gráfica y de rutinas basadas en Winteracter 7.1. La base de datos de radiocarbono hace uso de F90SQL. CalPal permite calibrar datos por diferentes rutinas, lo que permite producir alta calidad de vectores gráficos. Los gráficos se pueden ver en la pantalla, y pueden ser convertidos y exportados como HP-GL, PS, EPS, BMP, PCX, PNG, CGM, WMF, DXF, y SVG, así como a través de portapapeles. La iteración con las diferentes bases de datos se realiza de forma fácil utilizando SQL-dialog. La introducción de datos de radiocarbono es en formato ASCII, utilizando una hoja de cálculo. CalPal está diseñado, en parte, para la exploración de investigación. Hay que tener en cuenta que los procedimientos aplicados en CalPal no puede en todos los casos, ser idénticos a los procedimientos oficialmente recomendados por la comunidad-14 quater. Un diálogo adicional integrado en CalPal producirá un vector de ruta de los lugares, seleccionados a partir de la base de datos de radiocarbono, con el scienceware PanMap. Funcionamiento La pantalla inicial de la aplicación es la siguiente: • En el menú File podemos abrir, crear, modificar nuevos datos 14C para incorporarlos dentro de la base de datos. • En el menú Run elegimos la forma de calibración deseada. Recordemos que hay varias formas de calibración según las operación que queremos realizar: Operación deseada 1 Datación simple 2 Establecer datos 3 Datación multiple 4 Evaluar datos Archaeological & Dendrochronological 5 Evaluar datos con alta resolución y análisis de error 6 Establecer datos simples Paleoclimaticos mediante gráficos 7 Establecer datos multiples Paleoclimaticos mediante gráficos Ejecutar Gráfico CALCLIMATE/ CALKN 2-D CALCLIMATE / CALKN 2-D GROUP Multiple CALCLIMATE / CALKN WM GAUSSWM 2-D CALCLIMATE 2-D GROUP 2-D • En el menú Plots podemos elegir las opciones de los gráficos: Los datos que se obtienen en un calibrado, no siempre siguen comportamientos lineales, sino que, a veces, tienen la forma de una curva compleja, lo cual es frecuente en campos como la Biología, la Ecología,..etc, donde los sistemas a analizar engloban procesos complejos. Una técnica empírica muy utilizada para ajustar curvas es el procedimiento denominado de “tramos de cúbicas empalmados por nudos” (cubic splines). Esta técnica consiste en dividir el intervalo [a,b], que contiene los datos en varios subintervalos [a1,a2],[a2,a3],........,[an-1,an] (con a=a1 y b=an) y en cada subintervalo construir una cúbica (f(t) = A + Bx + Cx2 + Dx3) que sea continua hasta su segunda derivada de modo que en las uniones de los intervalos (que llamaremos nudos), las cúbicas y sus derivadas primera y segunda coincidan. • El programa CALCURVE realiza estos ajustes automáticamente, proporcionando una serie de tablas y tests estadísticos que permiten analizar la bondad del ajuste. Una vez que el usuario está satisfecho con la curva ajustada, el programa permite hacer “evaluación” y “predicción inversa” • El programa CLIMATE nos permite ver, comparar, y realizar cambios entre datos obtenidos y de la base de datos que seleccionemos. • En el menú CARTOGRAPHY podemos seleccionar la base de datos (PAN MAP o GLOBALIMAPPER) de la que queremos obtener datos de una manera sencilla y usando filtros. • Tenemos varios menús mas acerca de opciones sobre gráficas, tablas e incluso nos da la opción de Exportar nuestros datos a la base de datos seleccionada para incluirlos. • También observamos que tiene el menú MAPS que nos permite obtener imágenes captadas del satélite. Ejemplo CALPAL Veamos un ejemplo en el cálculo de una edad. Lo primero que hay que hacer es introducir nuevos datos obtenidos del laboratorio. La manera de introducir los datos se siguiendo el siguiente esquema: 01-12 15-20 22 23-26 28-29 31-34 Laboratorio Fecha de C 14 ± STD (x - niveau) BP AWM-distáncias Distancias de la edad de Calendric para emparejar del meneo (La edad Topmost debe tener distancia = 0.) 37-42 44 48 50-52 54-59 60 Absoluto de la edad de Calendric (sabido) # (línea para otros comentarios) 0 (línea para otros comentarios) [a] cal200 C (RGB- colores: R=red, G=green, B=blue, other=black) Así pues simulamos que hemos obtenidos los siguientes datos: Una vez introducidos los datos los ejecutamos en Run CalTable. Al darle a la opción CALCULATE nos sale la edad aproximada. NOTA: ¡¡Ojo sale en la escala BP!! Ejemplo de visualización calcurve: Es una visión general de las curvas de calibración incluidas en CALPAL. Dentro de esta aplicación podemos, visualizar, comparar y componer distintas tipos de curvas. Un ejemplo seria el que mostramos a continuación: El mismo ejemplo que hemos puesto en el caso anterior, podríamos haberlo echo dentro de la aplicación CLIMATE pero en este caso nos muestrearía como evoluciona en relación al cambio de clima. Ejemplo de base de datos: 1º seleccionamos un filtro a buscar o buscamos todo. 2ª buscamos las bases de datos deseadas. 3ª generamos el mapa. 4 BIBILIOGRAFIA http://depts.washington.edu/qil/: http://units.ox.ac.uk/departments/rlaha/orau/06_frm.htm www.ipen.gob.pe/site/capacitacion/2007/present_2007/08_02_07a.pdf www2.unia.es/nuevo_inf_academica/visualizar_file_Adjunto.asp?ID=1327 www2.unia.es/nuevo_inf_academica/visualizar_file_Adjunto.asp?ID=1325 http://www.textoscientificos.com/quimica/inorganica/origen-elementos http://www.educaplus.org/sp2002/1historia/c.html http://es.wikipedia.org/wiki/Carbono http://www.quimicaorganica.net/ http://homepage.mac.com/uriarte/carbono14.html http://es.wikipedia.org/wiki/Carbono-14 www.calpal.de www.calpal.de/calpal/manual/index.htm Manual CalPal.