F.Q UNAM. EBC
Anuncio

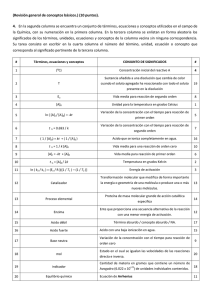
F.Q UNAM. EBC A. BAEZA Disoluciones amortiguadoras a) 25 mLCH3COONa y CH3COOOH concentrado (12 M), CBS0.05 mol/L y pH = 5.1; pKa = 4.8. Ecuación de Hendersson-Hasselbach : pH = pKa + log ([base]/[acido]) 5.1 = 4.8 + log ([base]/[acido]) Co = [acido]+[base] = 0.05 mol/L Acetato de sodio R.A. ácido acético concentrado 12M ¿gramos a pesar? [base] = ? ¿volumen a tomar? [ácido] =? Paso 1) 5.1 – 4.8 = log ([base]/[acido]) 0.3 = log ([base]/[acido]) 100.3 = ([base]/[acido]) = 2; [base] = 2[acido] Paso 2) Co = [acido]+[base] = 0.05 mol/L, 0.05 = [acido]+2[acido]= 3[acido] F.Q UNAM. EBC A. BAEZA [acido] = 0.05M/3 ; [base] = (2/3)0.05M Paso 3) [acido] = 0.016 mol/L; [base] = 0.032 mol/L Checando : pH = 4.8 + log(0.032/0.016)= 5.1; La cantidad de sal: [base]x Volumen = (0.035 mmol/mL)x(25 mL) = 0.87 mmol En gramos: (0.087 mmol)x(peso molecular de acetato de sodio) = (0.087mmol)x(82mg/mmol) Gramos de acetato de sodio a pesar: 71.3 mg = 0.0713g. La cantidad de ácido: [acido]x volumen = (0.016 mmol/mL)x(25 mL) = 0.4 mmol 12 mmol --------- 1 mL 0.4 mmol ----------- x x = (0.4/12) = 0.033 mL = 33 L. ______LA FUERZA IÓNICA SE DEFINE COMO : I = (1/2) z2[i] [acetato] = 0.035 M; [sodio] = 0.035 M: I = (1/2) [(-1)2(0.035M) + (1)2(0.035M)] = 0.035M “para sales 1:1 la fuerza iónica es igual a la concentración de la sal” ____________________________________________________________________________ INTERLUDIO El acido fosforico tiene 3 valores de pKa = 2, 7 y 12 como lo muestra el siguiente DIAGRAMA UNIDIMENSIONAL DE ZONAS DE PREDOMINIO, DUZP: H2PO4- H3PO4 2 HPO427 PO4312 pH ¿Cuánto KH2PO4 y Na2HPO4.2H2PO4 tengo que pesar para preparar 50 mL de un amortiguador de fosfatos de pH = 7 1 mM de buffer? pH =7 = pKa2 + log ([base]/[acido]) = 7 + log ([HPO4-]/[H2PO42-]) Co = [acido]+[base] = 0.001 mol/L; F.Q UNAM. EBC A. BAEZA “ pesar 3.4 mg de KH2PO4 y de 4.45 mg Na2HPO4.2H20 y mezclar con H2O c.b.p. 50 mL” CALCULO DE LA FUERZA IONICA DEL BUFFER DE FOSFATOS: Co = 0.001 mmol/mL [K+] = 0.5Co; [Na+] = Co ; [H2PO4-] = 0.5Co; [HPO42-] =0.5Co I = (1/2)[ 0.5Co + Co + 0.5Co + 2Co ] = (1/2)(4Co) = 2Co = 2(0.001M) = 2mM _____________________________________________________________________________ Cambiando de canal: Ley de Beer Problema 1) Si sigue sigue la Ley de Beer si le quitamos el estándar mas concentrado: 0.5 y = 0.037x - 0.000 R² = 1 0.4 0.3 Series1 0.2 Lineal (Series1) 0.1 0 0 5 10 15 -0.1 A = 0.037 mg-1cm-1L (C) + 0 con r2 = 1 El valor de la absortividad molar : = 0.037 mg-1cm-1L (243.22 mg/mmol)(1 mmol/0.001 mol) = 8999.14 mol-1cm-1L. _____________________________________________________________________________ ___ F.Q UNAM. EBC A. BAEZA ¨Problema 3: A 340 nm Amix = 0.311 = ANAD + ANADH = NADCNAD + NADHCNADH = 0 + 6220CNADH 0.311 = 6220CNADH A 260 nm Amix = 1.2 = ANAD + ANADH = NADCNAD 1.2 = 18000CNAD + 15000CNADH CNAD = 50 M CNADH = 25 M Interludio: 1) Alan López 2) Nadia Vera 3) Alfredo Flores 4) Tania Cuevas 5) Fernando Miguel 6) Beatriz Olivares 7) Veronica Garza 8) Ely Figueroa 9) Esther Correa 10) Carlos Montes 11) Rocío Castellanos 12) Elizabeth López 13) Javier Hernández + NADHCNADH = 18000CNAD + 15000CNADH