Universidad central de ecuador Facultad de - q
Anuncio

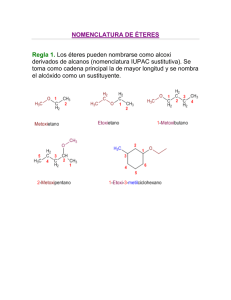
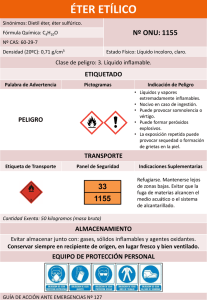
Universidad central de ecuador Facultad de ciencias químicas QUÍMICA ORGÁNICA II Integrantes: Johana Meneses Alejandra Gìa CAPITULO 16 Éteres y Epóxidos 16.22 Muchos éteres, incluyendo el éter etílico, son anestésicos generales eficaces. Como los éteres simples son muy inflamables, los éteres altamente halogenados, no inflamables, han ocupado su lugar en la práctica médica. Dos de estos anestésicos generales son el isoflurano y el enflurano. Esos compuestos son isómeros: el isoflurano es éter 1-cloro-2,2,3- trifluoroetil difluorometílico; el anflurano es éter 2-cloro1,1,2-trifluoetil de difluometilico. Escriba las fórmulas estructurales del isoflurano y el enflurano. 16.23 Aunque siempre se considera que los epóxidos tienen el átomo de oxígeno como parte de un anillo de tres miembros, se puede usar el prefijo epoxi en el sistema de nomenclatura de la IUPAC para indicar un éter de otros tamaños. Así, el Se puede llamar 1,3-epoxi-2-metilhexano. Utilizando el prefijo del epoxi, escriba el nombre de cada uno de los siguientes componentes: a) b) c) d) 16.24 Desarrolle los pasos de la preparación de cada uno de los éteres isoméricos, cuya fórmula molecular sea C4H10O, a partir de los alcoholes adecuados. Como la reacción clave aplique la síntesis de Williamson de éteres. Los ésteres isoméricos que pueden ser preparados son Metil-propil-èter Estos reactivos se pueden preparar a partir de: Isopropil metil éter Dietiléter Estos reactivos se pueden preparar a partir de: 16.25 Pronostique cuál es el producto orgánico principal en cada una de las reacciones siguientes. Especifique la estereoquímica cuando proceda. a. Este haluro secundario reacciona vía eliminación E2, debido a que el 2-butanolato de sodio es una bese fuerte. b. Este alcohóxido actúa como nucleófilo para atacar al yodoetano, dando lugar a la formación del c. La halohidrina vecinal es convertida en un éter al ser tratado con una base. d e. El ión azida es un buen nucleófilo, la sustitución ocurre en un carbono con inversión de configuración f. El amoniaco es un nucleófilo capaz de reaccionar con los epóxidos, g. El metóxido ataca al carbono menos sustituido, con una inversión de configuración. h I j. La sustitución nucleofílica provoca la inversión de configuración. 16.26 Cuando se deja reposar el (R)-(+)-2-fenil-2-butanol en metanol que contiene unas gotas de ácido sulfúrico, se forma el 2-fenil-2-metoxibutano racémico. Sugiera un mecanismo razonable para esta reacción. 16.27 Seleccione las condiciones de reacción que le puedan permitir efectuar cada una de las siguientes transformaciones esteroespecificas: a) b) 16.28 El último paso en el sistema del éter divinílico(que se usa como anestésico bajo el nombre de vineteno) es calentar ClCH2 CH2O CH2 CH2Cl con hidróxido de potasio. Indique como se podría preparar la materia prima necesaria, ClCH2 CH2O CH2 CH2Cl, a partir de etileno. 16.29 Sugiera secuencia cortas y eficiencias, adecuadas para preparar cada uno de los siguientes compuestos a partir de los materiales y de cualquier otro reactivo orgánico o inorgánico necesarios: a) b) c) d) e) f) 16.30 Entre las maneras como se puede preparar el 1,4-dioxano están los métodos representados por las siguientes ecuaciones: a) b) 16.31 Deduzca la identidad del compuestos faltante de las siguientes secuencias de reacciones. Muestre las esteroquímica en las partes b) y d) a) b) c) d) 16.34 El cienol o eucaliptol es el componente principal del aceite de eucalipto; su fórmula molecular es C10H18O, y no contiene enlaces dobles ni triples. Reacciona con el ácido clorhídrico formando el dicloruro siguiente: 16.36 El p-toluensulfonato de abajo sufre una reacción de Williamson intramolecular, al tratarlo con una base, y formar un éter espirocíclíco. Demuestre que se comprende la terminología usada en la frase anterior, escrubiendo la estructura y la esteoquímica del producto. 16.37 Todas las siguientes preguntas de refieren a espectros de RMN de ’H de éteres isoméricos cuya fórmula molecular es C5H12O. a. ¿Cuál muestra sólo los singuletes en su espectro de RMN de ‘H? b. Junto con otras señales, este éter muestra un patrón de acoplamiento de septeto de dobletes. Ninguno de los protones responsables de este patrón está acoplado con protones en lugar de alguno de la molécula. Identifique este éter. c. Además de otras señales en el espectro de RMN de ‘H, este éter muestra dos señales a campo relativamente bajo. Una es un singulete y la otra es un doblete. ¿Cuál es la estructura de este éter. d. Además de otras señales en su espectro de RMN de ‘H, este éter muestra dos señales a campo relativamente bajo. Una es un triplete y la otra es un cuarteto. ¿Cuál éter es? 16.38 El espectro de RMN de ‘H del compuesto A(C8H8O) consiste en dos singuletes de áreas iguales en 5.1ppm(agudo) y 7.2ppm(ancho). Al tratarlo con bromuro de hidrógeno en exceso, el compuesto A se convierte en un solo dibromuro (C8H8Br2). El espectro de RMN de ‘H del dibromuro es parecido al de A porque tiene dos singules en áreas iguales en 4.7ppm(agudo) y 7.3ppm(ancho). Sugiera estructuras razonables para el compuesto A y el dibromuro derivado del mismo. 16.39 En la figura 16.5 se muestra el espectro de RMN de ‘H de un compuesto (C10H13BrO). Cuando el compuesto se calienta con HBr forma bromuro de bencilo y el segundo compuesto C3H6Br2. ¿Cuál es el primer compuesto. 16.40 Un compuesto es un éter cíclico de fórmula molecular C9H10O. Su espectro de RMN de 13C se muestra en la figura 16.6. Por oxidación del compuesto con Dicromato de sodio y ácido sulfúrico se obtuvo ácido 1,2.bencenodicarboxilico. ¿Cuál es el compuesto?