Procesos de Separación: Destilación Simple de un Vino para la
Anuncio

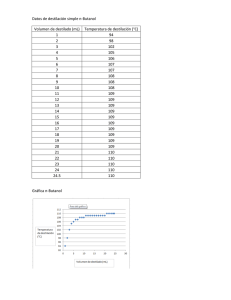
Destilación y Grado Alcohólico de un Vino EXPERIMENTACIÓN EN QUÍMICA EUITIG INGENIERO TÉCNICO EN QUÍMICA INDUSTRIAL PRÁCTICA Nº 14 Apellidos y Nombre: Grupo: . Apellidos y Nombre: Pareja: . Procesos de Separación: Destilación Simple de un Vino para la Determinación de su Grado Alcohólico OBJETIVOS: Reconocer la importancia de la destilación como proceso físico de separación. Manejar la técnica de destilación simple. Apreciar la utilidad de la densidad para determinar concentraciones. MATERIAL REACTIVOS 1 probeta de 100 mL 2 matraces erlenmeyer de 250 mL 1 vaso de precipitados de 100 mL 1 densímetro o alcohómetro 1 equipo de destilación simple: 1 matraz bombilla de 250 mL 1 pieza en T (pieza acodada) 1 refrigerante 1 pieza de recogida 1 Termómetro Soportes, pinzas y clips para esmerilados Cuentagotas y varilla Vino o sidra de mesa Tipos de Destilación La destilación es el método más común e importante para la purificación y separación de líquidos. Por ejemplo, cuando se destila un líquido se separan sus impurezas no volátiles. De hecho, la obtención de agua destilada o la purificación de disolventes orgánicos mediante destilación simple son procesos cotidianos en el laboratorio y en la industria. En algunas ocasiones se pueden separar dos o más líquidos mediante destilación simple siempre que sus temperaturas de ebullición difieran notablemente (más de 60 oC). Separar un líquido de sus impurezas no volátiles Objetivos de la destilacion Tipos de destilacion Destilación Destilación simple fraccionada a vacío Separar dos o más líquidos 130 Experimentación en Química Hay tres tipos de destilación: la simple, la fraccionada y a vacío. En una destilación simple el líquido a la presión atmosférica, se calienta en un recipiente cerrado que contiene una salida hacia un tubo refrigerado donde se condensan los vapores. Con esta sencilla operación podemos purificar un disolvente, pero no podemos separar completamente dos o más líquidos volátiles. La destilación fraccionada incorpora una columna de fraccionamiento (o de rectificación) entre la disolución y el refrigerante, lo que equivale a realizar etapas consecutivas de destilación simple. Suele utilizarse para la separación de líquidos. En el caso de la destilación a vacío, se trata de una destilación sencilla o fraccionada realizada a presión reducida. La presión reducida hace que las temperaturas de ebullición sean más bajas, lo que permite separar sustancias con puntos de ebullición elevados y/o que puedan descomponerse a temperaturas elevadas. EN ESTA PRÁCTICA VAS A REALIZAR UNA DESTILACIÓN SIMPLE • Al estudiar las propiedades termodinámicas de las mezclas, la composición y la temperatura de ebullición en una mezcla binaria de dos líquidos volátiles se relacionan en los diagramas Teb-composición a presión constante. Con la ayuda de los profesores, interpreta sobre el diagrama el proceso 1→2→3→4→5. p cte. V 5● Fracción molar del vapor TB0 4 L+V ● ● 3○ Teb(YA) ● 2● L 1● Teb(XA) TA0 Fracción molar del líquido 0.0 ZA 1.0 Fracción molar de la mezcla • Explica ahora por qué una etapa de destilación simple no es suficiente para separar completamente dos líquidos volátiles. Para aprender a montar y utilizar un equipo de destilación simple en el laboratorio, realizarás la destilación de un vino que es una etapa necesaria para determinar el grado alcohólico de un vino. Alcanzarás así dos objetivos: aprender a usar los equipos de destilación y conocer una importante técnica analítica de separación. Grado Alcohólico de un Vino 131 Destilación y Grado Alcohólico de un Vino El grado alcohólico de una bebida (o) se define como el tanto por ciento en volumen de alcohol etílico (etanol) contenido en la misma. Así, el grado alcohólico de una mezcla agua-etanol será: V Grado Alcohólico = %V etanol = e tan ol •100 Vdisolución Para determinar el grado alcohólico es necesario relacionarlo con otras formas de expresar concentración, en particular, con el tanto por ciento en peso. • Calcula el tanto por ciento en peso de etanol de una mezcla etanol-agua de 13o. (DATOS: ρdisolución=0.9828 g/mL, ρetanol=0.7907 g/mL). Para determinar experimentalmente un % en peso o un % en volumen, la magnitud clave es la densidad de la disolución. De hecho, en el cálculo anterior debe figurar necesariamente la densidad de la disolución (ρdisolución). En general, la relación entre el % vol. o el % en peso con ρdisolución no es simple, es decir, no obedece a una fórmula sencilla o a una relación de proporcionalidad simple. No obstante, es posible construir tablas empíricas que relacionan la concentración de disoluciones estándar con su densidad. Por ejemplo, en un Handbook de datos podemos encontrar la siguiente tabla para una mezcla entre etanol y agua Etanol-agua % en peso ρ 20 oC de etanol (g/mL) 0.50 0.9991 1.00 0.9981 1.50 0.9972 2.00 0.9962 2.50 0.9953 3.00 0.9945 3.50 0.9936 4.00 0.9927 4.50 0.9919 5.00 0.9911 % en peso de etanol 5.50 6.00 6.50 7.00 7.50 8.00 8.50 9.00 9.50 10.00 ρ 20 oC (g/mL) 0.9903 0.9895 0.9887 0.9880 0.9872 0.9865 0.9857 0.9850 0.9843 0.9836 % en peso de etanol 11.00 12.00 13.00 14.00 15.00 16.00 17.00 18.00 19.00 20.00 100.00 • A mayor grado alcohólico, ¿mayor o menor densidad de la mezcla? 132 ρ 20 oC (g/mL) 0.9822 0.9809 0.9796 0.9782 0.9769 0.9756 0.9743 0.9730 0.9717 0.9704 0.7907 Experimentación en Química • Utiliza ahora los datos de la tabla para averiguar el % en peso de la disolución con densidad 0.9828 g/mL. Interpola entre dos datos si es necesario. Observa, pues, que con la ayuda de las tablas empíricas, un método muy sencillo para conocer la concentración de una disolución es medir su densidad. Destilación del Vino En un vino el alcohol procede del proceso natural de fermentación del azúcar de la uva, que es metabolizado por bacterias que producen etanol como subproducto. Como hemos visto, las mezclas de etanol y agua tienen una densidad relacionada con su grado alcohólico. Ahora bien, el vino no es sólo etanol y agua, sino que tiene otros componentes que también influyen sobre la densidad, y, por lo tanto, una medida simple de la densidad del vino no nos proporciona su grado alcohólico. Destilado: Para superar esta dificultad, añadiremos Densidad Agua+Alcohol agua al vino y destilaremos la mezcla (100 mL) Vino hasta separar todo el etanol. Cuando el (100mL) Destilación + volumen de destilado sea al mismo que el Grado Simple Agua Alcohólico volumen de partida tendremos un líquido (50mL) Residuo: con el mismo grado alcohólico, pero sin Agua Ácidos otras sustancias que interfieran. Al medir la Azúcares densidad del destilado, averiguaremos el Glicerina Color grado alcohólico del vino de partida. • El esquema de separación de los componentes del vino por destilación nos indica qué componentes del vino permanecen en el residuo. Las fórmulas de algunos de estos componentes son: OH O H3C OH OH O HO HO ácido láctico OH OH O ácido tartárico HO HO OH R HO H HO H H OH O OH H D-glucosa ¿Por qué estos componentes no se separan? 133 HO OH OH Flavanoles (taninos) Destilación y Grado Alcohólico de un Vino La destilación de un vino puede aproximarse a la destilación de una mezcla etanol-agua. El diagrama Teb-composición representado esquemáticamente corresponde a una mezcla etanol-agua. p cte. 5 Teb(YA) TA0 agua • Representa de modo aproximado sobre el diagrama un proceso de destilación simple del vino. V TB0 etanol Teb(XA) ● Azeótropo L 0.0 ZA 1.0 Procedimiento 1) Reconoce primero las distintas piezas de un equipo de destilación simple: Termómetro Pinza - matraz bombilla - pieza acodada con termómetro - refrigerante de bolas - pieza de salida Si es necesario, lubrica las juntas esmeriladas con un pequeña porción de grasa de silicona. Pieza acodada Pinza Refrigerante Matraz esférico Pieza de recogida agua Manta Calefactora 2) Mide 100 mL de una muestra vino empleando la probeta y añádelos al matraz bombilla de 250 mL. 3) Con la misma probeta, mide 25 mL de agua destilada y añádelos al matraz con el propósito de recuperar el vino remanente en la probeta. Repite la operación con otros 25 mL de agua destilada. 4) Añade alrededor de 12 anillos de vidrio al matraz (anillos Rasching). 5) Monta el aparato de destilación. (Observa bien el esquema) - Ajusta primero el matraz y la pieza acodada con termómetro. - Monta después el refrigerante y la pieza de salida. Comprueba las gomas del refrigerante desde el grifo y hacia el desagüe de la pileta. - Conecta finalmente la pieza acodada y el refrigerante. - Comprueba que el bulbo del termómetro esté a la altura de la salida del matraz. - Asegura con clips las uniones entre piezas de material esmerilado. - Asegura la pieza acodada con una pinza. - Coloca un matraz erlenmeyer para recoger el destilado. 134 Experimentación en Química 6) Abre suavemente el grifo para que circule agua fría por el refrigerante de abajo a arriba. En todo momento debe evitarse la sobrepresión de agua. Comienza entonces la calefacción (posición II de la manta calefactora). La calefacción debe ser lenta pero sin interrupciones. A partir de la primera gota de destilado anota la temperatura cada dos minutos durante la destilación. tiempo (min.) 0 temperatura (oC) tiempo (min.) temperatura (oC) Durante la destilación, recoge el destilado en un matraz erlenmenyer. Periódicamente, trasvasa su contenido a una probeta. Cuando hayas alrededor de 80 mL de destilado, puedes dar por terminada la destilación. En cualquier caso, debes enrasar la probeta que contenga el destilado con agua hasta alcanzar un volumen de 100 mL. COMPLETADA LA DESTILACIÓN, DESCONECTA LA MANTA CALEFACTORA DEJA ENFRIAR ANTES DE DESMONTAR Y LAVAR EL EQUIPO DE DESTILACIÓN Responde a las siguientes cuestiones relacionadas con el procedimiento: • ¿Cuál es la misión del refrigerante? • Un matraz bombilla no debe llenarse nunca más allá de 2/3 de su contenido. ¿Por qué? • ¿Para qué se añaden los anillos Rasching al matraz de destilación? 135 Destilación y Grado Alcohólico de un Vino • ¿Cómo varió la Teb durante la destilación? ¿A qué es debida la variación de Teb? • ¿Cómo podemos estar seguros de que todo el etanol presente inicialmente en la mezcla se recuperó efectivamente en el destilado? • Si la Teb del vino depende de su contenido en alcohol, ¿sería útil un método ebullométrico para medir el grado alcohólico? Medida de la Densidad del Destilado Una vez que dispones de los 100 mL de destilado medidos en una probeta, vas a emplear un sencillo instrumento que recibe distintos nombres: densímetro, aerómetro o flotador de masa. El diseño y empleo de estos instrumentos pone en práctica el conocido principio de Arquímedes de modo que, para que un aerómetro flote sobre la superficie de un líquido, su peso debe ser igual al empuje, es decir maerómetro= ρlíquido Vdesalojado Conocida la masa del aerómetro y el volumen de la parte sumergida podemos conocer la densidad del líquido. En la práctica, el aerómetro dispone de un vástago o cilindro estrecho graduado que nos proporciona la densidad de líquido mediante la lectura directa del nivel alcanzado por la superficie del líquido. aerómetro 1) Toma un aerómetro graduado para medir densidades entre 1.000 g/mL y 0.900 g/mL. Límpialo y sécalo cuidadosamente. 2) Sumerge el aerómetro en la probeta que contiene el destilado etanol-agua. Hazlo con cuidado de no derramar líquido (Si es necesario, desaloja una porción del destilado antes de sumergir el aerómetro en la probeta). 3) Lee la densidad de la mezcla según la escala del aerómetro. Toma también la temperatura del destilado. ρdestilado= T= 136 Experimentación en Química 4) El aerómetro es un instrumento sencillo y preciso. Los aerómetros se calibran a 15 oC. Para mantener la exactitud en las mediciones a otras temperaturas, se dispone de tablas con factores de corrección ∆ρ que deben sumarse a las densidades medidas directamente con el aerómetro. Comprueba en la siguiente tabla si la medida de densidad que has efectuado debe corregirse por efecto de la temperatura. Si es necesario, corrige la densidad. T (oC) 10 11 12 13 14 15 16 17 18 19 Densidad corregida: T( oC) 20 21 22 23 24 25 26 27 28 29 ∆ρ (g/mL) -0.0006 -0.0005 -0.0004 -0.0003 -0.0001 0.0000 0.0002 0.0003 0.0005 0.0007 ∆ρ (g/mL) 0.0009 0.0011 0.0013 0.0016 0.0016 0.0021 0.0023 0.0026 0.0029 0.0032 ρdestilado= 5) Por ultimo, determina el grado alcohólico del vino. Transforma el dato de densidad de la mezcla etanol agua en su % en peso. Combinando el % en peso con los datos sobre la densidad del etanol puro, obtén finalmente el % en volumen o grado alcohólico. Grado Alcohólico = . 6) Dependiendo de la aplicación concreta, los aerómetros reciben nombres específicos como alcohómetros, sacarímetros, etc. En un alcohómetro el vástago está graduado directamente en grados alcohólicos. Utiliza un alcohómetro para medir el grado alcohólico del destilado etanol-agua. ¿Coincide con el resultado anterior? 137