cits neurológicos. Los síntomas suelen aparecer antes de 24 horas
Anuncio

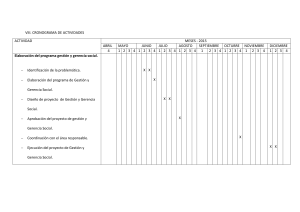
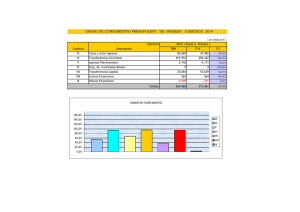
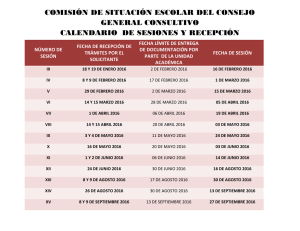
Documento descargado de http://www.elsevier.es el 19/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. CARTAS AL DIRECTOR cits neurológicos. Los síntomas suelen aparecer antes de 24 horas tras la PL, aunque pueden comenzar en sólo unos minutos o retrasarse varias semanas1,2. En nuestro caso la evolución fue subaguda, apareciendo el dolor lumbar a los seis días de la PL, y los síntomas neurológicos dos días después. La RM es el método diagnóstico de elección. Suelen ser posteriores a la médula espinal y en cortes axiales tienen forma de media luna2. A menudo son lesiones extensas, que ocupan varios segmentos espinales. Nuestro caso es típico en cuanto a su extensión (cuatro cuerpos vertebrales) y morfología del coágulo (forma de semiluna en cortes axiales), pero no en la localización (anterolateral a la médula espinal). El tratamiento conservador sólo está indicado en pacientes sin déficits neurológicos o cuando el estado general contraindica la cirugía2. En el resto, el tratamiento de elección es la evacuación quirúrgica antes de que aparezcan déficits completos e irreversibles. El pronóstico de los HSE depende del estado neurológico preoperatorio y del tiempo transcurrido desde el inicio de los síntomas2. Si aparece una hemorragia intracraneal o la hemorragia subdural se extiende al espacio subaracnoideo, como sucedió en nuestro caso, el pronóstico es peor. En conclusión, los HSE son una complicación muy poco frecuente de la PL. La existencia simultánea de una hemorragia intraventricular es un hecho excepcional, de mecanismos no conocidos y que ensombrece aún más el pronóstico. P. Varela Rois*, J. González García*, M.ª T. Pérez Rodríguez***, M. J. Paseiro García*, I. D. Carcacía Hermilla** *Servicio de Neurocirugía.**Servicio de Radiología. ***Medicina Interna. Complejo Hospitalario Universitario de Vigo (CHUVI). BIBLIOGRAFÍA 1. Peiró CM, Caballer N, Errando CL, Moliner S. Hematoma espinal y cerebral postpunción lumbar diagnóstica con evolución letal. Rev Esp Anestesiol Reanim. 2003;50(9):481-5. 2. Kreppel D, Antoniadis G, Seeling W. Spinal hematoma: a literature survey with meta-analysis of 613 patients. Neurosurg Rev. 2003;26(1): 1-49. 3. Reina MA, López A, De Andrés JA. Origen de los hematomas subdurales espinales. Estudio anatómico en cadáveres. Rev Esp Anestesiol Reanim. 2004;51(5):240-6. 4. Reina MA, De Leon Casasola O, López A, De Andrés JA, Mora M, Fernández A. The origin of spinal subdural space: Ultrastructural findings. Anesth Analg. 2002;94(4):991-5. 5. Stübgen JP. Intraventricular blood after “atraumatic” lumbar puncture: a report of two cases. Child´s Nerv Syst. 1995;11(8):492-3. IMPLICACIONES ANESTÉSICAS EN EL MANEJO DE UN PACIENTE CON HEMOFILIA A SOMETIDO A CIRUGÍA DE RESECCIÓN DE METÁSTASIS HEPÁTICAS Sr. Director: La hemofilia A o hemofilia clásica, es un trastorno de la coagulación hereditario recesivo ligado al 190 cromosoma X (afectación casi exclusiva de los varones), caracterizado por la ausencia o deficiencia severa del factor VIII en el plasma sanguíneo. Las primeras manifestaciones clínicas de hemorragia suelen acontecer en la infancia temprana, con deficiencia de factor VIII menor del 1%, o, en la hemofilia leve con 5-25% del valor normal de factor VIII, esta condición puede resultar inadvertida, incluso con ligero alargamiento de TTPA, resultando en hemorragias únicamente durante traumatismos o intervenciones quirúrgicas1. Son frecuentes las hemorragias articulares espontáneas en estos pacientes, a diferencia de las formas adquiridas, donde pueden observarse extravasaciones masivas subcutáneas o mucosas. Presentamos el caso de un varón con hemofilia A leve sometido a cirugía de resección hepática bajo anestesia general. Paciente varón de 72 años de edad y 68 kg de peso diagnosticado de metástasis hepáticas de un carcinoma colorrectal que se iba a someter a cirugía laparoscópica de resección hepática. Entre sus antecedentes destacaban hipertensión arterial y diabetes mellitus no insulinodependiente, así como leucemia linfática crónica tipo B en tratamiento con rituximab y quimioterapia CVP (ciclofosfamida, vincristina y prednisolona). También tenía hemofilia clásica A leve diagnosticada en su juventud por aparición de hemorragias dentales y subcutáneas incoercibles ante traumatismos. Había sido intervenido previamente de colectomía subtotal con anastomosis iliosigmoidea término-lateral por neoplasia de sigma en obstrucción. En el postoperatorio inmediato de aquella intervención precisó plasma fresco congelado, crioprecipitados y 2.500 UI de factor VIII recombinante cada 12 horas durante 5 días hasta conseguir una actividad superior al 80%. Recibió posteriormente quimioterapia. Para la resección de las metástasis presentaba Rx tórax y ECG normales, mientras que el estudio preoperatorio reveló un hematocrito de 40%, 164.000 plaquetas.microL, TTPA de 41 seg, TTPA-ratio de 1,59 y actividad de protrombina del 100% con una concentración de factor VIII de 0,23 UI ml-1. Tras consultar con el servicio de hematología se decidió pautar factor VIII recombinante 2.500 UI cada 12 horas iv durante 3 días iniciándose una hora antes de la cirugía, así como desmopresina 0,3 μmKg-1 y ácido tranexámico 25 mgKg-1 cada 8 horas como antifibrinolítico coadyuvante, tras la intervención durante 7 días. La actividad del factor VIII (estudio farmacocinético) fue del 112,1% previamente a la cirugía. El paciente fue premedicado con ranitidina iv. y midazolam oral. En quirófano se monitorizó ECG, presión arterial invasiva, saturación arterial de oxígeno, profundidad anestésica (BIS), presión venosa central mediante vía central de alto flujo, gasto e índice cardiaco mínimamente invasivos. La anestesia consistió en 0,01 mg Kg-1 de atropina y 2 mg Kg-1 de propofol y mantenimiento con oxígeno y aire (FiO2 0,4), sevofluorano 1-2%, atracurio y remifentanilo 0,15 µg Kg-1 min-1 para mantener el BIS 40-60. La temperatura corporal fue mantenida entre 36-37ºC utilizando manta térmica. La intervención duró 100 minutos y transcurrió sin incidencias. Las pérdidas sanguíneas estimadas fueron de 700 ml y se repusieron 1.000 ml de gelatinas y 2.000 ml de cristaloides. El paciente fue extubado en quirófano y trasladado a la unidad de reanimación. En el postoperatorio no se evi62 Documento descargado de http://www.elsevier.es el 19/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. CARTAS AL DIRECTOR denciaron signos de tendencia hemorrágica, objetivándose una actividad del factor VIII del 85% en las primeras 24 horas y del 53% a los 4 días. En la bibliografía científica ha sido descrito en varias ocasiones el uso con éxito de factores de la coagulación recombinantes en cirugías potencialmente sangrantes para el manejo terapéutico de la hemofilia A. Así, Cohen et al2 describen el empleo de factor VIII recombinante en 16 pacientes sometidos a cirugía de artroplastia total de rodilla con buen resultado. Para el tratamiento perioperatorio sustitutivo de la hemofilia, la cirugía de resección de metástasis hepáticas debe considerarse de alto riesgo hemorrágico. Por tanto, el objetivo debe ser mantener una actividad de factor VIII superior al 100% del valor considerado como normal, inmediatamente antes del acto quirúrgico, y entre el 70-100% en el postoperatorio inmediato hasta 2 a 7 días 3,4. En este supuesto, el tratamiento del paciente hemofílico sometido a cirugía no deberá diferir del paciente exento de coagulopatía5,6. En nuestro caso se alcanzaron valores dentro del rango previsto y el tratamiento mostró su eficacia para una adecuada hemostasia durante la intervención y el postoperatorio. Recomendamos por tanto en cirugía de alto riesgo hemorrágico la administración de factor VIII recombinante. El número de unidades necesario será el resultado de multiplicar la mitad del peso en Kg del paciente por el aumento deseado de concentración del factor VIII en tanto por cien. Considerando que 1 ml de plasma equivale a la actividad de 1 UI de factor VIII y que el volumen intravascular del plasma, similar al volumen de distribución del factor VIII es de 50 ml Kg-1, la dosis a administrar para lograr un aumento de 0 a 100% de actividad sería de 3.500 UI en un paciente promedio de 70 kg3. La desmopresina, análogo sintético de la vasopresina, es una alternativa a considerar en casos leves porque incrementa el factor VIII y el factor de Von Willebrand. Por otro lado cabe destacar las medidas para mantener baja la presión arterial, en un intento de disminuir la incidencia de hemorragia con niveles de presión venosa central inferiores a 5. La perfusión de remifentanilo mantuvo asimismo una excelente analgesia intraoperatoria. Debe considerarse reducir en lo posible el número de inyecciones y canalizaciones para venoclisis. Se ha descrito además la aparición de inhibidores que neutralizan el factor VIII recombinante tras dosis repetidas de tratamiento. Este hecho se da con mayor frecuencia en las formas graves, oscilando entre el 10-33%8. En nuestro caso la buena respuesta al tratamiento pudo favorecerse con la terapia inmunosupresora de base de su leucemia, pues se ha descrito el uso del rituximab y la ciclofosfamida contra estos inhibidores7,8. En conclusión, se ha presentado el caso de un paciente con hemofilia leve programado para resección hepática, con alto riesgo de hemorragia perioperatoria, con un resultado satisfactorio, siendo fundamental una valoración preoperatoria multidisciplinaria para afrontar su adecuado tratamiento perioperatorio. D. Fuentes García, G. Ramírez Muñoz Servicio de Anestesiología y Reanimación. Hospital Universitario “Virgen de la Arrixaca”. Murcia. 63 BIBLIOGRAFÍA 1. Cáceres W, McCurdy S. Recognition of hemophilia A in an elderly patient. Bol Asoc Med P R. 1998;90(4-6):85-7. 2. Cohen I, Heim M, Martinowitz U, Chechick A. Orthopaedic outcome of total knee replacement in haemophilia A. Haemophilia. 2000;6(2): 104-9. 3. Furie B, Limentani SA, Rosenfield CG. A practical guide to the evaluation and treatment of haemophilia. Blood. 1994;84(1):3-9. 4. Delumeau JC, Ikegawa C, Yokoyama C, Haupt V. An observational study of sucrose-formulated recombinant factor VIII for Japanese patients with haemophilia A. Thromb Haemost. 2008;100(1):32-7. 5. Barrio J, Añó C, Vicente R, Ramos F. Lorenzo JI, Argente J, et al. Trasplante pulmonar y hemofilia. Consideraciones perioperatorias. Rev Esp Anestesiol Reanim. 2000;47(9):412-6. 6. Barrio J, Peris V, Asensio I, Molina I, López F, García V. Tiempo de tromboplastina parcial activado prolongado no sospechado en cirugía de urgencia. Orientación diagnóstica y terapéutica. Rev Esp Anestesiol Reanim. 2002;49(8):424-7. 7. Barnett B, Kruse-Jarres R, Leissinger C. Current management of acquired factor VIII inhibitors. Curr Opin Hematol. 2008;15(5):451-5. 8. Haya S, Moret A, Cid AR, Cortina V, Casaña P, Cabrera N, et al. Inhibitors in haemophilia A: current management and open issues. Haemophilia. 2007;13(Suppl 5):52-60. ANESTESIA EN PACIENTE CON HOMOCISTINURIA Y EMBOLISMO PULMONAR SEVERO Sr. Director: La homocistinuria (HC) es el segundo error más frecuente en el metabolismo de los aminoácidos con una prevalencia de un caso por cada 300.000 habitantes1,2. Existen tres subtipos en los que diferentes defectos enzimáticos provocan acúmulo de homocisteína y metionina en sangre, orina y tejidos orgánicos, interfiriendo en la formación de los enlaces de colágeno1,2. Son pacientes altos, delgados y pueden presentar pectum excavatum, cifoescoliosis, osteoporosis, miopía por luxación del cristalino, retraso psicomotor, manifestaciones extrapiramidales, convulsiones, trastornos psiquiátricos, complicaciones tromboembólicas y crisis de hipoglucemia. El diagnóstico se basa en la clínica, la detección de aumento de homocisteína, metionina y cistationina en el organismo y cuantificación de la actividad cistationina sintetasa en los hepatocitos o fibroblastos2. Es fundamental la detección precoz, ya que algunos pacientes se benefician de dietas restrictivas en metionina y ricas en cisteína, piridoxina, ácido fólico y betaína3. Destacar complicaciones como hipoglucemia, tromboembolismo pulmonar (TEP) y la contraindicación de utilizar óxido nitroso (N2O)2. Presentamos el caso de un paciente afecto de HC que precisó anestesia general para colocación de filtro de cava por TEP severo. Varón de 21 años, 80 kg, 182 cm, diagnosticado de HC. Padecía retraso psicomotor, delirio y mal control de impulsos, crisis convulsivas controladas, asma bronquial, raquitismo, déficit de vitamina B12 y luxación bilateral de cristalino. Estaba en tratamiento con acenocumarol (trombosis venosa femoral y de seno longitudinal superior), olanzapina y oxcarbacepina hasta el día previo al ingreso. Presentaba disnea, taquipnea, agresividad, saturación periférica de oxígeno (SpO2) de 89% y taquicardia supraventricular a 120 lpm con bloqueo de rama derecha. 191