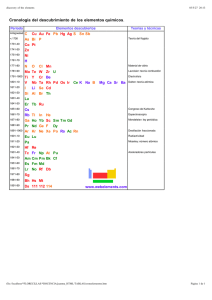
HNO SAg SH AgNO OH COLi CO LiOH H CaCl Ca HCl + → + + → +
Anuncio

GUÍA DE QUÍMICA ESTEQUIOMETRÍA Curso: AÑO 2015 2ºmedio Fecha: 1. 2. Defina: A) B) C) D) E) F) G) Cambio físico Cambio químico Ecuación química Coeficiente estequiométrico Ley de Dalton Ley de Lavoisier Ley de Proust Balancee las siguientes ecuaciones: HCl ( ac ) + Ca ( S ) → CaCl 2( ac ) + H 2 ( g ) LiOH ( S ) + CO2 ( g ) → Li 2 CO3( S ) + H 2 O AgNO3( ac ) + H 2 S ( ac ) → Ag 2 S ( ac ) + HNO3( ac ) N 2 + O2 → NO2 Al + HCl ↔ AlCl 3 + H 2 Cu + H 2 SO4 ↔ CuSO4 + SO2 + H 2 O 3. Un grupo de estudiantes realizó el siguiente experimento, buscando explicar la ley de Lavoisier. Colocaron una tableta efervescente en un recipiente cerrado con agua, como se representa en la figura: Masa recipiente de agua = 20g Masa tableta efervescente = 5g Masa total después de la reacción = 25g Este experimento explica la ley de Lavoisier, porque la reacción química: A) Libera energía B) Se forman sustancias nuevas C) La materia siempre se conserva D) Las sustancias se combinan de manera proporcional E) No ocurre reacción 3. Lea el siguiente enunciado: “En la formación de un compuesto, las masas de las sustancias involucradas se combinan siempre en la misma proporción”. La ley que se menciona es: A) Proporciones definidas B) Proporciones recíprocas C) Volúmenes de combinación D) Conservación de la materia E) De Lavoisier