Ciclo de Krebs - Bioquimica Kinesiologia UNLaM
Anuncio

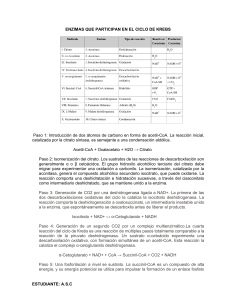
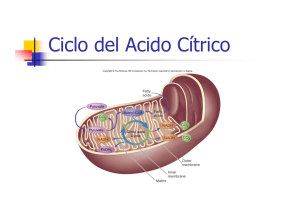
UNLaM-Kinesiología-Bioquímica-Ciclo de Krebs Ciclo de Krebs Ciclo del ácido cítrico (o ciclo de Krebs) El ciclo del acido cítrico es el modo habitual de degradación oxidativa en organismos eucariontes y procariontes. También conocido como ciclo de los ácidos tricarboxílicos y ciclo de Krebs, es el punto central del metabolismo. A través de su estudio se explican los procesos más importantes de la oxidación de carbohidratos, ácidos grasos y aminoácidos y se generan numerosos precursores biosintéticos. Por lo tanto se trata de una ruta metabólica anfibólica. Formación de Acetil-CoA El Acetil-CoA es el intermediario común formado por la mayoría de los combustibles metabólicos. A partir de este compuesto se producirá el ingreso al ciclo de Krebs del grupo acetilo, que se oxidara para dar dos moléculas de CO2. La coenzima A (ver anexo I) funciona como un transportador del grupo acetilo, mediante la formación de un enlace tioester de alta energía. La formación de una unión tioester en un compuesto metabólico intermediario, conserva una porción de la energía libre de su oxidación. Desde la glucolisis la síntesis del Acetil-CoA se produce mediante la descarboxilación oxidativa del piruvato. Primero el Piruvato debe atravesar la membrana mitocondrial externa (la cual es permeable) y la interna, a través de un transportador simporte con H+, piruvato translocasa. En la matriz mitocondrial se produce la descaboxilación del piruvato, con formación de una molécula de NADH, por acción del complejo enzimático piruvato deshidrogenasa. Este complejo multienzimatico se halla constituido por 3 enzimas que catalizan 5 reacciones, y cuyas coenzimas y grupos prostéticos son: Tiamina pirofosfato (TPP), Flavina Adenina Dinucleotido (FAD), Nicotinamida Adenina Dinucleotido (NAD+) y lipoamida. La piruvato deshidrogenada regula el ingreso de las unidades de acetilo derivadas de los carbohidratos, por lo que su regulación es muy importante. La regulación es bastante simple, se halla regulada negativamente por sus productos, NADH y Acetil-CoA que compiten con NAD+ y CoA por los sitios de unión. También la piruvato deshidrogenasa se halla regulada mediante modificación covalente (fosforilación/desfosforilación) que es inducida por un segundo mensajero, Ca2+. ∆Gr0=-33.4kJ/mol Figura 1: Producción de Acetil-CoA a partir de Piruvato. Ciclo de Krebs 1 El ciclo consiste en una serie de 8 reacciones, donde se oxidan el grupo acetilo, de Acetil-CoA a dos moléculas de CO2. De las 8 reacciones, 4 son oxidaciones, en las cuales la energía es eficientemente conservada, en forma de coenzimas reducidas, NADH Y FADH2, para usarla a posteriori en la producción de ATP. Durante el ciclo hay 8 enzimas involucradas y al final por cada molécula de Acetil-CoA se generan 3 moléculas de NADH, una de FADH2 y una de GTP. En la Figura 2 se observa un esquema del ciclo de Krebs. Figura 2: Ciclo del Acido Cítrico (también conocido como ciclo de Krebs) A continuación detallaremos las reacciones del ciclo de Krebs partiendo de la condensación del Acetil-CoA con el Oxalacetato: Reacción 1: Formación de citrato. 2 La primera reacción del ciclo es la condensación del Acetil-CoA con Oxalacetato (4 Carbonos) por acción de la citrato sintasa para producir Citrato (6 Carbonos). En esta etapa el grupo metilo del Acetil-CoA se une al carbonilo del Oxalacetado (C2), formando el intermediario Citril-CoA, que inmediatamente se hidroliza para dar Citrato y CoA libre (que puede formar más Acetil-CoA). La hidrólisis del enlace tioester de alta energía, es fuertemente exergónica, por lo tanto esta reacción es irreversible. Que esta reacción posea un ∆G muy negativo (o sea, que sea altamente favorable e irreversible) es de suma importancia para el funcionamiento del ciclo, como veremos más adelante, ya que mantiene bajos los niveles de Oxalacetato. Reacción 2: Isomerización del citrato. Los siguientes dos pasos del ciclo implican reestructurar el citrato a un isómero que se oxide con mayor facilidad. La aconitasa convierte el alcohol terciario en uno secundario (oxidable), para ello, primero se deshidrata generando un doble enlace cis y luego de hidrata con un grupo alcohol en el carbono 2. Reacción 3: Primera descarboxilación oxidativa del isocitrato. En esta primera oxidación del isocitrato (recordar que posee 6 Carbonos) se genera la primera molécula CO2 y α-cetoglutarato (que posee 5 Carbonos) por acción de la isocitrato deshidrogenasa. Esta enzima tiene como cofactor a NAD+ que actúa como aceptor de los electrones de alta energía generados en esta etapa para dar NADH. Esta es la Segunda reacción irreversible del ciclo y la principal reguladora del mismo. 3 Reacción 4: Segunda descarboxilación oxidativa del α-cetoglutarato. A través del complejo enzimático α-cetoglutarato deshidrogenasa (formada por 3 enzimas análogas a las del complejo enzimático piruvato deshidrogenasa, y que requieren los mismos cofactores TTP, NAD+, FAD, ácido lipoico y Co-A), se produce la segunda descarboxilación del α-cetoglutarato para dar succinil-CoA (el succinato posee 4 Carbonos) con la formación de una nueva molécula de NADH a partir de NAD+. Al igual que en el Acetil-CoA, en el succinil-CoA el enlace tioester formado es de alta energía. Reacción 5: Formación de GTP a partir de Succinil-CoA En esta etapa la energía del enlace tioester del Succinil-CoA se aprovecha para llevar a cabo la fosforilación a nivel de sustrato de GDP y generar GTP, Succinato y regenerar la Coenzima A. La enzima que actúa en esta etapa es la Succinil-CoA Sintetasa. De aquí en mas no se producirán mas descarboxilación, solo resta oxidar el succinato hasta oxalacetato y reiniciar el ciclo. Obtener GTP es equivalente a obtener ATP: Reacción 6: Oxidación del Succinato a Fumarato 4 La Succinato deshidrogenasa es la única enzima que no se encuentra en la matriz mitocondrial, sino que es una enzima integral de la membrana interna de la mitocondria. Esta forma parte de la cadena de transporte de electrones. Esta oxidación implica la formación de un doble enlace, proceso que genera electrones de alta energía, pero de energía menor que los que se requieren para reducir al NAD+, por ello esta enzima emplea como cofactor al FAD para obtener FADH2. Ya que la enzima se halla asociada a la membrana interna mitocondrial, los electrones obtenidos pasan directamente a la cadena respiratoria, proceso metabólico que veremos más adelante, para la obtención de ATP. Como la mayoría de la enzimas, la succinato deshidrogenasa en una enzima estereoespecífica que solo cataliza la formación del isómero trans (fumarato) y no el cis (maleato). Reacción 7: Hidratación del Fumarato La Fumarasa cataliza la hidratación del doble enlace del fumarato para obtener malato. La Fumarasa, igual que la succinato deshidrogenasa también estereoespecífica, solo cataliza la hidrólisis del fumarato (no maleato) para formar el isómero L-Malato. Reacción 8: Oxidación de malato a oxalacetato 5 Es la última reacción del ciclo de Krebs e implica la última oxidación para obtener el oxalacetato a partir de Malato con la reducción de una molécula más de NAD+ por acción de la enzima Malato deshidrogenasa. Aunque la reacción es poco favorable, solo exergonica a muy bajas concentraciones de Oxalacetato, recordar que la siguiente reacción (reacción 1 del ciclo) es una reacción irreversible, y muy exergonica, por lo que el poco oxalacetato que se produce es inmediatamente captado por la citrato sintasa para producir la condensación con el Acetil-CoA. De esta forma se mantiene bajas las concentraciones de oxalacetato (alrededor de 10-6M), la reacción de deshidrogenacion del malato se hace termodinámicamente posible y el ciclo avanza. (Ver Anexo II) A lo largo de una vuelta del ciclo de Krebs vemos como el grupo acetilo de dos carbonos ingresa el ciclo, combinándose con oxalacetato, y como resultado se liberan a lo largo del ciclo 2 carbonos en forma de CO2. Si embargo, tener en cuenta que estos 2 carbonos que se liberan no corresponden al acetilo, si no que son los pertenecientes al oxalacetato. Así los dos carbonos del acetilo formaran parte de la nueva molécula del oxalacetato generada, que serán oxidados y liberados en las subsiguientes vueltas del ciclo. Como balance general del ciclo, tenemos que por cada molécula de Acetil-CoA que ingresa al ciclo se generan una molécula de GTP, y tres de NADH y una FADH2 que luego en la cadena respiratoria cederán sus electrones para la formación de mas moléculas de ATP. Acetil-CoA + 3NAD+ + FAD + GDP + Pi + 2H2O → CoA-SH + 3(NADH + H+) + FADH2 + GTP + 2CO2 Regulación del ciclo de Krebs El ciclo del ácido cítrico presenta 3 puntos de regulación, en las enzimas que catalizan las reacciones irreversibles(Figura 3): • Citrato sintasa: se encuentra inhibida por su producto, citrato, por otro metabolito intermediario del ciclo, succinyl-CoA y por los productos del ciclo NADH y ATP. • Isocitrato deshidrogenasa: esta enzima se encuentra regulada por el estado energético de la célula, así cuando la célula presenta un estado de alta energía, o sea que las relaciones ATP/ADP y NADH/NAD+ son altas la actividad de la enzima disminuye, mientras que cuando el estado energético de la célula es bajo, o sea que estas relaciones son bajas, la enzima se encuentra activada. • α-cetoglutarato deshidrogenasa: Esta enzima se halla inhibida por su producto, succinil-CoA. También se regula por el estado energético de la célula, por la relación ATP/ADP y NADH/NAD+, como la Isocitrato deshidrogenasa. 6 Figura 3: Regulación del ciclo del acido cítrico. Carácter anfibólico del ciclo de Krebs Como ya se menciono, el ciclo del acido cítrico, a demás de ser una ruta catabólica, aporta muchos de los intermediarios de diversas rutas biosintéticas, es decir que también es una via anabólica (Figura 4). Las reacciones catapleroticas son aquellas que emplean intermediarios del ciclo de Krebs como precursores biosintéticos. Por ejemplo el α-cetoglutarato y el y el oxalacetato son precursores de los aminoácidos aspartato y glutamato por simple transaminación. A partir de estos dos aminoácidos se generan otros aminoácidos así como nucleótidos puricos y pirimidicos. El oxalacetato puede convertirse en glucosa en la gluconeogénesis y el succinil-CoA es un intermediario en la síntesis del anillo porfirinico del grupo hemo. Así como los intermediarios del ciclo son consumidos como precursores biosintenticos de muchas rutas metabolicas, se requiere su biosíntesis para evitar el vaciamiento del ciclo y mantener el equilibrio. Las reacciones que producen los intermediarios del ciclo de Krebs se denominan reacciones anapleroticas. A continuación de muestran las reacciones anapleroticas más comunes. Piruvato + HCO3- + ATP Fosfoenolpiruvato + CO2 + GDP Fosfoenolpiruvato + HCO3- Oxalacetato + ADP + Pi Oxalacetato + GTP Oxalacetato + Pi 7 Piruvato + HCO3- + NAD(P)H Malato 9 NAD(P)+ Figura 4: Reacciones Anapleroticas y Catapleroticas del ciclo de krebs 8 Apéndice Coenzima A La coenzima A es un grupo β-mercaptoetilamino unio mediante una unio amida a la vitamina ácido pantótenico, que a su vez se une a un resto 3´-fofoadenosina mediante puente pirofosfato. Químicamente un tiol que puede reaccionar con los ácidos carboxílicos para formar tioésteres, de modo que actúa como un transportador del grupo acilo Adenosina-3´-fosfato Residuo de β-mercaptoetilamino Residuo de ácido pantoténico Figura I: Coenzima A Dependencia del ΔG con la concentración Para dar una idea general de la espontaneidad de una reacción se presentan los valore de ∆G0r, que corresponde a la energía libre de una dada reacción en condiciones estándares, esto es a presión 1 atm y temperatura de 0°C (273K) y concentraciones de reactivos y productos de 1M. En general las condiciones que encontramos en los sistemas biológicos difieren ampliamente de las condiciones estándares, para encontrar el ∆G en las condiciones de interés se debe aplicar la siguiente formula: ∆G = ∆G0r – RT ln ([reactivos]n/[Productos]m) Donde R es una constante, T la temperatura en kelvin. Si aumentamos la temperatura, vemos que el ∆G se hace más negativo, mas espontanea es la reacción. También vemos que si la concentración de productos es baja respecto a la de reactivos (o sea [Reactivos]/[Productos]<<1) la reacción también es más espontanea. A medida que aumenta la concentración de productos, es decir que disminuye la relación [Reactivos]/[Productos], la reacción se vuelve menos espontanea. Incluso puede revertirse y ser favorable energéticamente la reacción inversa. (Ver figura II) 9 y x y=ln(x) Figura II: Grafico del logaritmo neperiano 10