- Ninguna Categoria
activacion de una sepiolita con disoluciones diluidas de no3h
Anuncio
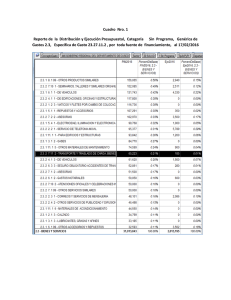
Clay Minerals (1981) 16, 103 113. A C T I V A C I O N DE U N A S E P I O L I T A CON D I S O L U C I O N E S D I L U I D A S DE NO3H Y P O S T E R I O R E S T R A T A M I E N T O S TERMICOS: I. E S T U D I O DE LA S U P E R F I C I E E S P E C I F I C A J. DE D . L 6 P E Z G O N Z A L E Z , R E I N O S O , C. V A L E N Z U E L A A. RAMIREZ CALAHORRO* S.&ENZ, F. RODRIGUEZ Y L. Z U R I T A H E R R E R A Departamento de Quimica Inorgdniea, Facultad de Ciencias, y *Facultad de Farmaeia. Universidad de Granada, Spain (Received30 April 1980) R E S U M E N Una sepiolita procedente de Toledo (Espafia) se ha activado por tratamiento con disoluciones 0.25, 0-50 y 0.75 N de NO3H, seguido de calentamiento durante 10 h a 110, 200, 300, 400 y 500~ Para cualquier concentraci6n/tcida, un calentamiento de 110, 200 y, a veces, 300~ produce un aumento del nfimero de poros mientras que las temperaturas superiores significan un cierre de los mismos tanto mayor cuanto mils elevada es la temperatura de tratamiento. El mfiximo desarrollo de la superficie accesible al N2 tiene lugar con una disoluci6n 0.50 y de NO3H y 200~ (449 m2/g, m&odo de BET); la superficie especifica de la sepiolita natural es de 321 mZ/g. INTRODUCCI6N El e s t u d i o del c o m p o r t a m i e n t o f i s i c o - q u l m i c o de la superficie de a l g u n o s de los minerales de la arcilla o c u p a desde hace afios la a t e n c i 6 n de m u c h o s investigadores. La r a z 6 n de ello es que estos minerales suelen p r e s e n t a r p r o p i e d a d e s que les p e r m i t e n c o m p o r t a r s e c o m o a d s o r b e n t e s y/o c o m o catalizadores. Se a d m i t e que dicho c o m p o r t a m i e n t o viene c o n d i c i o n a d o p o r la n a t u r a l e z a y m a g n i t u d de la superficie e x t e r n a (Ries, 1952), de m a n e r a que las modificaciones que afecten a la m a g n i t u d o a la n a t u r a l e z a de d i c h a superficie p u e d e n afectar a l a s p r o p i e d a d e s a d s o r b e n t e s y / o cataliticas del c o r r e s p o n diente m i n e r a l de la arcilla. M e d i a n t e t r a t a m i e n t o s i c i d o s y t6rmicos a d e c u a d o s ( K a i s e r & Block, 1952) se p u e d e m o d i f i c a r la m a g n i t u d de la superficie y el nfimero de centros i c i d o s superficiales de los minerales de arcilla. En el caso en que dichos t r a t a m i e n t o s a u m e n t e n la superficie especifica y el nfimero de centros i c i d o s superficiales, el p r o c e s o se suele d e s i g n a r c o n el n o m b r e gen6rico de activaci6n. L a a c t i v i d a d ( a d s o r b e n t e o catalitica) suele ir a u m e n t a n d o a m e d i d a que lo hacen las i n t e n s i d a d e s de los t r a t a m i e n t o s , h a s t a a l c a n z a r una a c t i v i d a d m i x i m a , a p a r t i r de la cual, t r a t a m i e n t o s mils severos p r o d u c e n u n a d i s m i n u c i 6 n de la a c t i v i d a d ( G r i m , 1962; Fernfindez Alvarez, 1970; Jim6nez L 6 p e z e t al., 1978). L a sepiolita es un silicato de e s t r u c t u r a fibrosa que en la a c t u a l i d a d e n c u e n t r a n u m e r o s a s aplicaciones c o m o a d s o r b e n t e , d e c o l o r a n t e , s o p o r t e p a r a c a t a l i z a d o r e s , etc. Estas aplicaciones prficticas son consecuencia de l a existencia de u n a alta a c t i v i d a d f i s i c o - q u i m i c a en la superficie de dicho silicato. 0009-8558/81/0300-0103502.00 9 1981 The Mineralogical Society 104 J. de D. L6pez Gonzdlez et al. Los estudios estructurales realizados en la sepiolita (Nagy & Bradley, 1955; Brauner & Preisinger, 1956; Rautureau & Mifsud, 1977) han mostrado la existencia de unos canales intracristalinos de dimensiones (3.8 x 10.6 A), que se extienden a lo largo de las fibras. Tratamientos t6rmicos y ficidos adecuados pueden modificar considerablemente tales canales, produciendo cambios notables en la porosidad y estructura de la sepiolita y, por tanto, sensibles modificaciones en la actividad superficial de la misma (Fernfindez Alvarez, 1970, 1972, 1978; Rautureau & Mifsud, 1977; Jim~nez L6pez et al., 1978). Teniendo en cuenta las anteriores consideraciones, en un trabajo anterior (Jim+nez L6pez et al., 1978) se procedi6 a estudiar la variaci6n de la superficie especifica de una sepiolita natural de Toledo (Espafia), al ser tratada con disoluciones acuosas de NO3H de concentraciones 1 a 5 y y, posteriormente, calentada a temperaturas comprendidas entre 110~ y 900~ Los resultados obtenidos en estos estudios pusieron de manifiesto que el grado de activaci6n de la sepiolita era (dentro del intervalo de concentraciones de NO3H alli utilizado: /> 1N) tanto menor cuando m a y o r era la concentraci6n de la disoluci6n de NO3H utilizada en el proceso. En estas condiciones, lo que realmente ocurre es una excesiva destrucci6n de la red del silicato, con el consiguiente colapsamiento de canales estructurales. C o m o consecuencia de dichos resultados se pens6 en la posibilidad de utilizar una activaci6n con disoluciones mils diluidas de NO3H (0.25, 0.50 y 0-75 y), seguida de los tratamientos t6rmicos que habian resultado ser m/is favorables. A fin de obtener informaci6n acerca del grado de activaci6n conseguido, se ha determinado en todas las muestras, la superficie especifica mediante la adsorci6n de N2 a 77 K, dfindose cuenta en el presente trabajo de los resultados obtenidos, en funci6n de los tratamientos ~cidos y t6rmicos efectuados. PARTE EXPERIMENTAL Se ha utilizado, como muestra de partida, una sepiolita natural (Toledo, Espafia), que nos fue suministrada por TOLSA. Para efectuar el anfilisis quimico de la misma, 6sta se calcin6 a 1000~ hasta pesada constante, y se disgreg6 despu6s, siguiendo el m6todo propuesto por Langmyhr & Paus (1968). En la disoluci6n resultante se d e t e r m i n a r o n - - p o r espectrofotometria de absorci6n at6mica, en la forma habitual los elementos constituyentes de la misma, a excepci6n del oxigeno. La determinaci6n de la capacidad de cambio de la sepiolita natural se efectu6 en una muestra homoi6nica am6nica, preparada previamente, siguiendo una t6cnica semimicro ya descrita (Valenzuela Calahorro, 1966). La sepiolita natural, una vez molturada y tamizada hasta conseguir un tamafio de particula comprendido entre 2.38 y 4.76 mm, fue sometida a tratamiento ficido con disoluciones acuosas 0.25, 0,50 y 0.75 y de NO3H, operando en la forma ya descrita con anterioridad (Jim6nez L6pez et al., 1978). De las muestras de sepiolita resultantes de la activaci6n ficida, una vez secadas al aire, se tomaron varias porciones, las cuales fueron sometidas a tratamiento t6rmico, consistente en mantenerlas a l a s temperaturas de 110, 200, 300, 400 y 500~ durante 10 h. Las propiedades adsorbentes en todas las muestras asi obtenidas se estudiaron mediante la adsorci6n de nitr6geno a 77 y 90 K. Para la obtenci6n de las isotermas de adsorci6n se ha utilizado un sistema gravim6trico convencional (Martinez Vilchez, 1978) en el que el aumento de peso experimentado pot la muestra, en funci6n de la presi6n de Acid and heat activation of sepiolite 105 equilibrio del gas adsorbato, se seguia mediante la utilizaci6n de dos espirales de cuarzo (sensibilidades: 38.65 y 32.35 cm/g, respectivamente) de las que colgaban unos dep6sitos de papel de aluminio conteniendo las muestras. El sistema gravim6trico va incluido dentro de unas c&maras de adsorci6n que, a su vez, est~n conectadas a un sistema de alto vacio apropiado. Para la medida de las elongaciones de las espirales, asi como de la presi6n de equilibrio para cada punto experimental de la isoterma, se utiliz6 un catet6metro que permite medir _ 0.01 mm. Todas las muestras fueron convenientemente desgasificadas antes de determinar las isotermas de adsorci6n. Para ello se utilizaron temperaturas de desgasificaci6n de 150~ para todas las muestras que habian sido tratadas t6rmicamente a temperaturas superiores a 200~ las muestras tratadas a 110~ fueron desgasificadas a 90~ y las muestras secadas a temperatura ambiente fueron desgasificadas a esta misma temperatura. En todos los casos, el tiempo de desgasificaci6n fue de cuatro horas, al cabo del cual la presi6n era siempre inferior a 10 -5 torr. U n a vez desgasificadas las muestras se procedi6 a realizar la adsorci6n isoterma de nitr6geno a 77 y 90 K; aun cuando en los primeros puntos experimentales, a presiones relativas bajas, se requeria aproximadamente una hora para que se alcanzara el equilibrio, dicho equilibrio era alcanzado mucho m/~s r&pidamente a presiones superiores; de todas formas, se estableci6 un tiempo minimo de 30 minutos para asegurar el equilibrio. En todas las isotermas de adsorci6n de N2 a 77 K se procur6 que el flltimo punto de la isoterma coincidiese con la presi6n de saturaci6n del nitr6geno a la temperatura de adsorci6n. RESULTADOS Y DISCUSION El an~lisis quimico de la sepiolita natural utilizada en el presente trabajo, ha suministrado los resultados que se expresan en la Tabla 1. La capacidad de cambio de la sepiolita natural result6 ser de 8 mEq/100 g, valor que est/l de acuerdo con lo que cabria esperar (Serna Pereda, 1973). A la vista de los resultados del an/disis quimico, se ha determinado la f6rmula mineral6gica de la sepiolita natural estudiada, desecada a 1000~ y libre de carbonatos. La f6rmula se ha referido a dieciseis "htomos de oxigeno (1/4 de malla), resultando ser la siguiente: (Si4.8+0A1~.2+0)(Al~.;sMg]~3Fe03.~3) O16" Na0.04" K0.07 A la vista de esta f6rmula mineral6gica, se puede deducir que la sepiolita natural de Toledo presenta sustituciones isom6rficas, tanto tetra6dricas como octa6dricas. En los huecos tetra6dricos, el 3"33~o de los Si 4+ han sido sustituidos por AI 3+. En cuanto a la capa octa6drica, se observa en primer lugar la existencia de defectos reticulares, de manera que aproximadamente el 2~o de las posiciones octa6dricas se hallan vacias. Asimismo, se observa una sustituci6n de una muy pequefia parte de los Mg2+ octa6dricos por Fe 3+ y A13+. Tambi6n hay una pequefia cantidad de Mn 2+ (Tabla 1) en las posiciones octa6dricas, que no se han incluido en la f6rmula mineral6gica. T a m p o c o ha sido incluido el Ti 4+ en la citada f6rmula. U n a vez sometida la sepiolita natural a los distintos tratamientos ~cidos y t6rmicos, se procedi6 a estudiar el proceso de adsorci6n de nitr6geno, a 77 y 90 K, por cada una de las muestras activadas. 106 J. de D. L6pez Gonztilez et al. TABLA 1. Composici6n quimica de la sepiolita desecada a 100ff'C Componentes SiO2 A1203 TiO2 MgO Fe203 MnO CaO* Na20 K20 Total 66-03 2.42 0.12 29.24 0-50 0.03 0-85 0.23 0.59 100.01 * Se puede suponer como constituyente de CO3Ca en la sepiolita natural, cuyo contenido en carbonatos en la sepiolita desecada a 110'~C seria del 1.31~ en peso (Serna Pereda, 1973). Las isotermas de adsorci6n de nitr6geno a 77 K correspondientes a todas las muestras se han representado en la Fig. 1, mientras queen la Fig. 2 se han incluido las isotermas de adsorci6n del mismo gas a 90 K. Las isotermas de adsorci6n de N 2 a 77 K son todas intermedias entre los tipos I y II, mientras que las de adsorci6n de N2 a 90 K parecen pertenecer al tipo I (Sing, 1976). No obstante, hay que tener en cuenta que esa aparente diferencia no es sino una consecuencia directa del distinto intervalo de presiones relativas cubierto alas dos temperaturas. Lo que si parece evidente, a la vista de las Figs 1 y 2, es que en todos los casos hay una considerable contribuci6n de microporos a la porosidad total de las muestras, siendo posible establecer comparaciones de tipo cualitativo acerca de la porosidad de las mismas, asi como de la superficie accesible al nitr6geno, a la vista de las formas de las isotermas. E1 primer hecho destacable es q u e e n cualquiera de las familias de isotermas de las Figs 1 y 2 (para un tratamiento ficido dado), las isotermas son pricticamente paralelas entre si. Esto quiere decir que todas las muestras sometidas a un mismo tratamiento icido tienen aproximadamente la misma distribuci6n relativa de tamafios de poros, variando tan solo el nflmero de poros segfln el tratamiento t6rmico a que se someten las muestras. En el caso de la adsorci6n a 77 K, cuando se comparan las tres series (0.25 N, 0-50 N y 0"75 N) se observa que varia la cantidad adsorbida de una a otra pero, sobre todo, que la pendiente se va intensificando a medida que aumenta la concentraci6n de la disoluci6n icida. Esto quiere decir que, ademis del efecto en el aumento de superficie especifica (que se comentari mils adelante), el aumento de la concentraci6n de NO3H en la disoluci6n produce un aumento de la mesoporosidad de las muestras. Este efecto no se aprecia en la adsorci6n a 90 K puesto que el intervalo de presiones relativas en este caso es muy inferior. Asi pues, el queen una serie dada de muestras se produzca el hecho de que las isotermas A cid and heat activation of sepiolite 107 200 - I00 ~ T ~ r ~ > j Ambiente ~ __~I~- 9 o.2sN-.Ooc 025N-200~ | 025N- 300~ 9 0.25N- 400'C 025 N- 500oC | Naturat-110~C ~..___.....4~----~ ' 020 'p d40 ~ ' 0160 L 0180 I I 200 T Ambiente ~oo ~ > ~ ,~ o 5 N - 200~ | 0 5 N- 300 C 05 N- 400oC 0.5 N- 500~ 020 P 0 40 080 (]60 20( ~ P ~ Ambiente t:m -. I00 E 9 075N- 110oc 075N- 200~ | 0.?SN- 300~ @ 075N- 400~ 075N- 500~ 9 o12o ' o!4o ' o!6o ~ o!8o ' I!o FIG. 1. Isotermas de adsorci6n de N2 a 77 K. son prficticamente paralelas se puede interpretar en el sentido de que un tratamiento ficido dado produce aumento del nfimero total de poros, sin que cambie la distribuci6n de tamafio de los mismos. Por otra parte, las isotermas de la Fig. I vienen a indicar que para cualquier concentraci6n ficida de las estudiadas, el tratamiento t6rmico tiene una influencia decisiva en la capacidad adsorbente de las muestras, 1o que estfi relacionado con la apertura o cierre de los poros de ias mismas. Asi, puede comprobarse que un tratamiento de I10, 200 y, a veces, 300~ produce tin aumento del nfimero de poros, J. de D. L6pez Gonzdlez et al. 108 O 0.25N-T.Ambiente| 0.25 N - 3 0 0 * C 9 0 . 2 5 N -llOOC 9 0 2 5 N-400*C @ 025N @ 0.25 N - 5 0 0 ' C -200'C 100- 01.05 0!I %~ 012 0!15 O 05 N-T. Ambiente | 9 05N- ~ 05 N - 4 0 0 ~ C Ol 05 II0~ N - 200~ 0.5N-300" 0125 013 0'.25 0!3 o~s 0'.3 C @ 0.5 N - 500 ~ C I00 0 0!05 0'I 0',5 O 0.75 N-T Ambiente 0'2 | 0.75 N - 3 0 0 " C 9 0.75 N - 1 1 0 ' C 9 0.75 N - d 0 0 * C 01075 N - 2 0 0 * C @ 075 N - 5 0 0 " C 100 > 0 0 ob5 o~.i o.'15 o!2 FIG. 2. Isotermas de adsorci6n de N2 a 90 K. mientras que las temperaturas superiores a estas significan un cierre mils o menos importante de los mismos, tanto mayor cuando mayor es la temperatura del tratamiento t6rmico (Jim6nez L6pez et al., 1978). Para ver mils claramente estos efectos, en la Fig. 1 se ha incluido tambi6n la isoterma de adsorci6n de N 2 a 77 K sobre la muestra natural de sepiolita desecada a 110~ A partir de las isotermas de adsorci6n de nitr6geno tanto a 77 K como 90 K se ha calculado el valor te6rico de la capacidad de monocapa, Vm, a partir del cual, si se conoce la superficie cubierta por cada mol6cula de adsorbato Am, puede calcularse la superficie especifica de las muestras. C o m o valores de Am se han utilizado 16.2 A 2 para la temperatura de 77 K y de 17.0 A 2 para la de 90 K (L6pez Gonz~lez et al., 1976). Los 109 Acid and heat activation of sepiolite TABLA 2 Superficie especifica (m2/g) 77K 90K Muestra BET L D-R t BET Natural-ll0~ 0-25N-T. amb. 0-25N-110~ 0.25N-200~ 0.25N-300~ 0.25N-400~ 0.25N-500~ 321 348 378 366 375 262 198 425 426 452 436 447 288 230 426 442 467 483 472 340 251 374 365 391 406 400 267 208 -354 319 304 297 199 188 0-50N-T. amb. 0.50N-II0~ 0.50N-200~ 0.50N-300~ 0-50N-400~ 0.50N-500~ 384 389 449 385 301 282 482 509 585 545 399 356 500 512 588 506 398 373 417 420 470 409 308 280 391 346 368 331 293 255 0-75N-T. amb. 0.75N-110~ 0.75N-200~ 0.75N-300~ 0-75N-400~ 0.75N-500~ 377 395 438 434 373 360 460 506 503 502 399 385 512 523 551 549 470 441 395 417 454 463 385 374 306 381 369 381 308 309 valores de superficie especifica calculados mediante la aplicaci6n de las ecuaciones de BET (Sing, 1976), Langmuir (Sing, 1976) y Dubinin-Radushkevich (Sing, 1976) se han incluido en la Tabla 2 (en el caso de la adsorci6n de N2 a 90 K se ha utilizado tan solo la ecuaci6n BET). Con el objeto de facilitar la discusi6n de los valores de la superficie especifica, los datos correspondientes obtenidos de la ecuaci6n de BET se han representado grfificamente en funci6n de la concentraci6n de la disoluci6n de NO3H (Fig. 3) y de la temperatura del tratamiento t6rmico (Fig. 4). E1 primer hecho destacable de los valores de superficie especifica accesible al N2, es el elevado valor correspondiente a la muestra de sepiolita natural, desecada a 110~ (321 m2/g). Este valor es muy superior al de otros minerales de la arcilla como la vermiculita, con superficie especifica de alrededor de 10 m2/g (Van Olphen, 1976). Este hecho hay que basarlo en la naturaleza cristalina de la sepiolita, con un gran nfimero de canales intracristalinos, accesibles a una mol6cula de dimensiones reducidas, como es la de nitr6geno. Por otra parte, de la Fig. 3, en la que se han incluido a efectos comparativos los resultados de superficie especifica de las muestras tratadas con disoluci6n 1 N de NO3H (Jim6nez L6pez et al., 1978), se puede deducir que, para las distintas temperaturas de tratamiento t6rmico, los miximos valores de superficie especifica se dan para disoluciones 0-50 N 6 0"75 N de NO3H. Es de destacar que para las muestras tratadas alas temperaturas mils elevadas (300, 400 y 500~ el m i x i m o aparece a 0.75 N, mientras que para las temperaturas de 200~ y ambiente el m i x i m o aparece para 0.50 N. La serie tratada a 110~ presenta el m i x i m o a 0-75 N, pero dicho valor es muy pr6ximo al correspondiente a J. de D. L6pez Gonzcilez et al. 110 500 - 4OO Noturo[ 110 300 t~ 2OO 9 110 ~ 200~ | 3GO~ 400'C 500 ~ C )00 i 0.25N i 0.50 N 01?5 N I 1.00 N FIG. 3. V a r i a c i 6 n de la superficie especifica (BET) con la c o n c e n t r a c i 6 n de la disoluci6n de NO3H. 0.50 N. Todo parece indicar que, a efectos de aumento de la superficie especifica, las temperaturas de tratamiento mils bajas de las utilizadas son las mils adecuadas para las muestras tratadas con HO3H 0-50 N y que las mils elevadas lo son para la concentraci6n 0.75 N. El efecto de la temperatura de tratamiento t6rmico puede verse f~,cilmente en la Fig. 4, de la que se deduce que, en general, para cualquier concentraci6n ~cida se produce el m~ximo de superficie especifica a 200~ (excepto para la concentraci6n 0.25 N, cuyo mhximo se da a 110~ para despu6s descender a medida que aumenta la temperatura. Tambi6n es de destacar que el aumento de superficie especifica producido por los tratamientos t6rmicos m/is bajos (ambiente y 110~ es poco marcado, mientras que temperaturas superiores a 200~ dan lugar a un descenso pronunciado de la superficie especifica, descenso que es tanto m~s marcado cuanto menor es la concentraci6n de la disoluci6n de NO3H utilizada en la activaci6n; en algunos de estos casos la superficie especifica se hace incluso inferior a la correspondiente a la de la sepiolita natural desecada a 110~ Por otra parte, de los valores de superficie especifica dados en la Tabla 2 se deduce que en todos los casos, aquellos valores calculados por aplicaci6n de la ecuaci6n de BET (SBET) son inferiores a los calculados mediante las ecuaciones de Langmuir (SO y Dubinin-Radushkevich (SD-R), siendo estos dos filtimos, a su vez bastante pr6ximos entre Acid and heat activation of sepiolite | 500- ill 0.25N O O. 50 N 9 0.75N @ 1. OON .dOG N * 300. co 20O 100 0 ~ 2~o 3;o ~b0 5~o T(*C) FIG. 4. Variaci6n de la superficieespecifica(BET) con la temperatura del tratamiento t~rmico. si. U n comportamiento paralelo ha sido encontrado en otros trabajos sobre sepiolitas activadas (Fernhndez Alvarez, 1972; Jim6nez L6pez et al., 1978). Con el objeto de poder conocer la causa de este comportamiento, se ha calculado el valor del par~tmetro c de la ecuaci6n de BET que, como es bien conocido, est~ relacionado exponencialmente con el calor de adsorci6n de la primera capa de gas adsorbido. En todos los casos, el valor de c es relativamente elevado (entre 100 y 600, en general) y ello viene a indicar que los valores de superficie especifica calculados por el m6todo de BET se han de t o m a r con cierta reserva (Sing, 1976). Los valores elevados del par~imetro c est~in asociados, bien a la formaci6n de una m o n o c a p a localizada (como ocurre en la adsorci6n de N2 a 77 K sobre carbones grafitizados) o bien al llenado de los microporos. Si la isoterma de adsorci6n de N2 es del tipo I, entonces el mecanismo de adsorci6n consiste en el llenado de los microporos en vez de adsorci6n en m o n o c a p a y siesta interpretaci6n es correcta, implica que el valor de la cantidad de gas adsorbido a presi6n relativa unidad est~i condicionado por el volumen de microporos en lugar de por la superficie especifica del adsorbente. En nuestro caso, las isotermas son intermedias entre los tipos I y I I ~ e ahi los valores encontrados para el parhmetro c - - y los valores de superficie especifica deducidos por el m6todo BET son inferiores a los calculados, por ejemplo, segfln el m6todo de Dubinin-Radushkevich, ya 112 J. de D. L6pez Gonzdlez et al. que el intervalo de aplicabilidad de la ecuaci6n de BET en nuestro caso estfi, en general, comprendido entre presiones relativas de 0.005 a 0.15; este intervalo es bastante inferior al usual del m&odo (0-05 a 0.35). Ahora bien, como se puede observar en la Tabla 2, se ha calculado tambi6n la superficie especifica segfin el m&odo t (Lippens & De Boer, 1965) y los valores resultantes, aunque algo superiores a los deducidos del m & o d o BET, son mucho m~ts pr6ximos a estos que a los deducidos por los m6todos de Dubinin-Radush kevich y Langmuir. A su vez, el mbtodo t ha permitido c o m p r o b a r de manera clara el caricter microporoso de las muestras. Esta es la raz6n por la que se han tomado los valores de superficie especifica deducidos pot la ecuaci6n de BET, como referencia para la discusi6n de los efectos de los tratamientos ficidos y t6rmicos sobre la sepiolita original. En lo que respecta a los valores de superficie especifica deducidos de las isotermas de adsorci6n de N2 a 90 K, 6stos son, aunque bastante similares, algo inferiores en general, a los deducidos de la adsorci6n del mismo gas a 77 K. Esto viene a indicar que no hay restricciones en los poros de las muestras de sepiolita que impliquen una adsorci6n activada, es decir, que los poros son igualmente accesibles a l a s mol6culas de nitr6geno a las dos temperaturas. En conclusi6n, la sepiolita natural de Toledo, cuando se somete a tratamientos con disoluciones diluidas de NO3H seguidos de calentamiento desde la temperatura ambiente hasta 200~ (en algunos casos hasta 300~ experimenta un incremento de su superficie accesible al N2 a 77 K 6 90 K, que llega a ser hasta de un 40~o en el caso mils favorable (disoluci6n 0.50 N y tratamiento a 200~ durante 10 h); este incremento de la superficie accesible al N2 parece ir acompafiado de un aumento del nfimero total de poros, sin que se altere apreciablemente la distribuci6n del tamafio de los mismos. Por otra parte, a temperaturas superiores a l a s mencionadas, se produce un colapsamiento de poros, tanto m i s intenso cuanto m a y o r es la temperatura del tratamiento t6rmico. BIBLIOGRAFIA BRAUNER K. & PREISINGERA. (1956) Struktur und Entstchen des Sepioliths Mineral. Petrog. Mitt. 6, 120~140. FERNANDEZ ALVAREZT. (1970) Superficie especifica y estructura de poro de la sepiolita calentada a diferentes temperaturas Proc. Reuni6n Hispano-Belga de Minerales de la Arcilla, Madrid, 202-209. FERNANDEZ ALVAREZT. (1972) Etude de la structure de pore de divers solides par adsorption de l'azote. I. Sepiolite naturelle el activ6e par HC1. Proc. Int. Clay Conf. Madrid, 571-582. FERNANDEZALVAREZT. (1978) Efecto de la deshidratacion sobre las propiedades adsorbentes de la palygorskita y sepiolita. I. Adsorci6n de nitr6geno. Clay Miner. 13, 325-335. GRIM R.E. (1962). Applied Clay Mineralogy. Pp. 307-318. McGraw-Hill Book Co. Inc. London. JIMENEZ LOPEZ A., LOPEZ GONZALEZ J. DE D., RAM1REZ SAENZ A., RODR1GUEZ REINOSO F., VALENZUELA CALAHORRO,C. & ZURITA HERRERAL. (1978) Evolution of surface area in a sepiolite as a function of acid and heat treatments. Clay Miner. 13, 375-385. KAYSER F. & BLOCH I.M. (1952) Some catalytic properties of montmorillonite. Compt. rend. 234, 1885-1887. LANGMYHR F.J. & PAUS P.E. (1968) The analysis of inorganic siliceaus materials by atomic absorption spectrophotometry and the hydrofluoric acid decomposition technique. Part I. The analysis of silicate rocks. Anal. Chim. Acta 43, 397-408. LIPPENS B.C. & DE BOER J.H. (1965) Studies on pore systems in catalysts. V. The t method. J. Catalysis 4, 319-323. LOPEZ GONZALEZ J. DE D., RODRIGUEZ REINOSO F., BAr'ARES MU~OZ, M.A. & LINARES SOLANO A. (1976). Isotermas de adsorci6n de nitr6geno y argon en un grafito de origen mineral. An. Quire. 72, 441-449. MARTINEZ VILCrlEZ F. (1978) Procesos de carbonizaci6n y activaci6n de hueso y orujo de aceituna y sus efectos en la textura y capacidad adsorbente de los carbones activos resultantes. Tesis Doctoral, Universidad de Granada. NAGY B. & BRADLEYW.F. (1955) The structural scheme of sepiolite. Am. Miner. 40, 885-892. A c i d and heat activation o f sepiolite 113 RAUTUREAUM. & MIFSUD A. (1977) Etude par microscope blectronique des diff6rents &ats d'hydratation de la s~piolite. Clay Miner. 12, 309-318. RIES H.E. JR. (1952) Structure and sinteringproperties of cracking catalysts and related materials. Pp. 87-147 in: Advances in Catalysis, 4, Academic Press, New York. SERNA PEREDAJ.C. ( 1973) Naturaleza y propiedades de la superficie de ta sepiolita. Tesis Doctoral, Universidad de Madrid. SING K.S.W. (1976) Surface Characterization: Physical. Pp. 1-56 in: Characterization of Powder Surfaces (G.D. Parfitt & K.S.W. Sing, editors). Academic Press, London. VALENZUELA CALAHORROC. (1966) Estudio de la difusidn de las mol~culas de p-p'-DDT a travds de algunos rninerales de la arcilla. Tesis Doctoral, Universidad de Granada. VAN OLPHEN H. (1976) Clays. Pp 427~,55 in: Characterization of Powder Surfaces ( G . D Parfitt & K.S.W. Sing, editors). Academic Press, London. A B S T R A C T : A sepiolite from Toledo, Spain, with a BET surface area of 321 m2/g, has been activated with dilute solutions of HNO3 (0.25, 0.50 and 0-75 N) followed by heat treatment at 110, 200, 300, 400 and 500"C for 10 h. For any of the acid solutions, heating at 110, 200 and, in some cases, 300'-C produced an increase in porosity, whereas higher temperatures (400, 500~ produced some pore closing. The maximum development of surface area available to N2 (449 m2/g) occurred following treatment with a 0-50 N acid solution and subsequent heating at 200~ R E S U M E : Une s6piolite de TolMe (Espagne) dont la surface BET= 321 m2/g a +t+ activ6e avec des solutions de HNO3 (0.25, 0.50 et 0.75 N), puis trait6e thermiquement fi 110, 200, 300, 400 et 500~ pendant 10 heures. Pour chacune de ces solutions acides, le chauffage fi 110, 200 et dans certains cas 300~ produit un accroissement de la porosit6 alors que des temperatures plus 61ev+es (400, 50if'C) entrainent la fermeture de quelques pores. Le d~,eloppement maximum de la surface utilisable vis ~i vis de l'azote (449 mZ/g) s'obtient en utilisant un traitement avec une solution 5. 0.50 N en acide et un chauffage ult6rieur fi 200~ K U R Z R E F E R A T : Ein Sepiolit aus Toledo, Spanien, mit einer BET-Oberfl/iche yon 321 mZ/g, wurde mit verdiinnten L6sungen yon HNO3 (0-25, 0-50 und 0.75 N) aktiviert und einer nachfolgenden Hitzebehandlung bei ll0, 200, 300, 400 und 500~ ffir jeweils 10 Stunden unterzogen. Bei jeder S/iurekonzentration bewirkte die Erhitzung auf 110, 200 und in einigen F~illen auf 300~ einen Zuwachs an Porosit/it, wogegen h6here Temperaturen (400, 500~ einige Poren verschlossen. Eine ffir N2 zug/ingliche, maximale Oberfl/iche (449 m2/g) stellte sich bei Behandlung mit 0.50 N S/iure und nachfolgender Erhitzung auf 200~ ein.
Anuncio
Documentos relacionados
Descargar
Anuncio
Añadir este documento a la recogida (s)
Puede agregar este documento a su colección de estudio (s)
Iniciar sesión Disponible sólo para usuarios autorizadosAñadir a este documento guardado
Puede agregar este documento a su lista guardada
Iniciar sesión Disponible sólo para usuarios autorizados