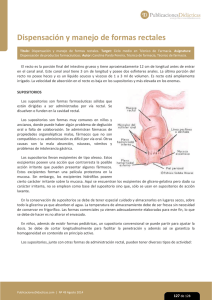
SUPOSITORIOS
Anuncio

SUPOSITORIOS García Martínez Miriam Negrete Tiburcio Mónica DEFINICIONES Son preparaciones que contienen uno o más fármacos disueltos o dispersos en una masa, la cual puede ser soluble o dispersable en agua. Normalmente son administrados en dosis única para acción local o absorción sistémica del medicamento. (FEUM 9ª) Son cuerpos sólidos de diversos pesos y formas, adaptados para introducirse en el recto, vagina o la uretra. En general se funden, ablandan o disuelven al entrar en contacto con la temperatura corporal. (USP 24) Formas farmacéuticas de dosificación única, semisólidas, de aplicación rectal, vaginal o uretral. VENTAJAS: Dosis única Biodisponibilidad Evita metabolismo “primer paso” de Efecto local y sistémico. El número de excipientes requeridos es reducido Protege al fármaco del pH del estómago o secreciones enzimáticas intestinales Se pueden administrar a pacientes inconscientes, bebes y ancianos. Adecuado para pacientes que no pueden recibir terapia oral. Protege al paciente de fármacos que causan nauseas y vómito o irritación en el estómago. El sabor, olor y color del fármaco no influyen en su administración DESVENTAJAS La absorción de los fármacos depende de la adecuada aplicación, lo mismo que el efecto de primer paso. Requiere condiciones especiales de transporte y almacenamiento. Hipersensibilidad vehículo. al No son aceptados socialmente. Lesiones o irritación de mucosas. Puede generar defecación y por tanto expulsión. Su administración requiere de privacidad. CLASIFICACIÓN DE SUPOSITORIOS Por la vía de administración Por el modo de acción Por la estructura interna CLASIFICACIÓN DE ACUERDO A LA VÍA DE ADMINISTRACIÓN Rectales Vaginales Uretrales RECTO Es la parte terminal del intestino grueso (aprox. 15 a 19 cm.). pH = 6.8. Tiene una reducida área superficial comparándola con el intestino delgado. La mucosa rectal posee propiedades de absorción que se pueden aprovechar para la administración de fármacos. RECTALES Generalmente cilíndricos o cónicos, con un extremo plano Pesan 2g y miden entre 2.54 y 3.81 cm de largo Los supositorios infantiles son 50 % mas pequeños (peso y tamaño). VAGINA Conducto aplanado que une el cuello del útero a la vulva (pH 3.5 – 4.2) Tubo fibromuscular de 7.5 cm. de longitud aprox. Circulación sanguínea vaginal: Suministro sanguíneo por la arteria vaginal (ramificación de la iliaca). La sangre retorna evitando el sistema porta hepático. VAGINALES En la formulación de los óvulos se emplean bases hidrosolubles como polietilenglicol (PEG) o gelatina para minimizar el goteo. También llamados óvulos Comúnmente de forma globular u ovoide. Su peso y tamaño van de 3 a 5 gramos. En la actualidad contamos con tabletas vaginales, conocidas como insertos. Uretra Conducto excretor por el que se expulsa al exterior la orina contenida en la vejiga En los hombres termina en la extremidad del pene y su tamaño es de 20 cm En las mujeres termina en la vulva y mide 4 cm Es pobremente perfundido por sangre URETRALES Son delgados y tienen forma de lápiz También llamados “ramitas” Para mujeres miden 5 mm de diámetro y 50 mm de longitudm con dos gramos de peso. Para hombres miden 5 mm de diámetro y 125 mm de longitud, con cuatro gramos de peso CLASIFICACIÓN DE ACUERDO A MECANISMO DE ACCIÓN Mecánica La finalidad es activar la motilidad el intestino por vía refleja, antiguamente se utilizaban supositorios a base de jabón. En el caso de los supositorios de glicerina se añade el fenómeno de ósmosis debido a la atracción de la glicerina por el agua, lo que incrementa los movimientos peristálticos. CLASIFICACIÓN DE ACUERDO A MECANISMO DE ACCIÓN Local La actividad del fármaco está destinada a tratar la mucosa rectal en el lugar de aplicación. Por ejemplo los supositorios para el tratamiento de hemorroides, en este caso se desea que el fármaco se libere lentamente y permanezca el mayor tiempo posible en contacto con el tejido dañado. CLASIFICACIÓN DE ACUERDO A MECANISMO DE ACCIÓN Sistémica El objetivo es que el fármaco sea absorbido por las membranas mucosas del recto con la finalidad de llegar a regiones del organismo lejanas al recto. El modo de acción se da a partir de la absorción de los fármacos a través del sistema hemorroidal, pasa a la circulación general y actúa sobre el órgano afectado. CLASIFICACIÓN DE ACUERDO A SU ESTRUCTURA INTERNA Supositorios en solución Cuando el fármaco es soluble en la base del supositorio aparece como una solución solidificada Se debe cuidar que el PA sea completamente soluble en los excipientes en fusión y que al enfriar no cristalice. La presencia de cristales en el supositorio puede causar severas lesiones al paciente CLASIFICACIÓN DE ACUERDO A SU ESTRUCTURA INTERNA Supositorio en emulsión Están formados de una emulsión solidificada, contienen una base lipofílica, emulsificantes y el fármaco liquido que no es soluble en grasas. La fabricación se realiza al incorporar un PA líquido a la base lipofílica, en la cual no es soluble y solidifica CLASIFICACIÓN DE ACUERDO A SU ESTRUCTURA INTERNA Supositorios en suspensión Son empleados cuando el fármaco no es soluble en la base lipofílica Este tipo de supositorios presenta algunas dificultades como: Lograr el contenido homogéneo del fármaco en todo el lote En ocasiones los primeros supositorios suelen tener mayor contenido de PA que los últimos La punta suele presenta mayor concentración del fármaco, lo cual se debe a la sedimentación de las partículas de PA en la masa en fusión SUPOSITORIOS EN SUSPENSIÓN La velocidad de sedimentación depende: El tamaño de partícula del PA La densidad del PA y de la base del supositorio La viscosidad de la masa fundida. La exactitud de la dosificación se alcanza cuando la sedimentación es baja en la masa fundida La sedimentación se determina por la ley de Stokes SUPOSITORIOS EN SUSPENSIÓN Por lo que: El radio de la partícula debe ser lo más pequeño posible, es conveniente utilizar PA pulverizados La densidad del PA y la densidad de la base deben ser lo más cercanas posibles La masa fundida debe tener alta viscosidad en el momento del vaciado en los moldes, ya que la sedimentación termina hasta el momento de la solidificación Es conveniente que la temperatura de fusión de la masa fundida y el punto de solidificación sean muy cercanos LIBERACIÓN DEL PRINCIPIO ACTIVO El PA debe ser liberado de la FF La absorción se realiza posterior a su liberación, disolución y difusión en el líquido rectal La etapa de disposición incluye a fusión, disolución y transferencia del PA al líquido rectal La etapa de absorción desde la difusión del PA, absorción y paso al torrente sanguíneo SOLUBILIDAD DEL PA Los PA`s deben poseer una buena solubilidad en agua y cierta solubilidad en lípidos. Solubilidad en agua: para disolverse en el fluído rectal y líquido tisular que rodea las células Solubilidad en lípidos: para que puedan difundirse a través de las membranas y las capas de tejidos que tiene carácter lipídico COEFICIENTE DE REPARTO La absorción rectal del PA se influye por la relación de reparto entre la base y el líquido rectal El coeficiente de reparto es dependiente de la solubilidad del PA en las fases hidrofílicas y lipofílicas El PA que es muy solubles en la base grasa se difunden lentamente al líquido rectal y la aparición del efecto se demora, aunque su duración es larga El PA que tiene poco solubilidad lipídica, pero muy solubles en agua se absorben fácilmente INTERVALO DE LIBERACIÓN DEL FÁRMACO Característica PA Característica Base Intervalo aprox de liberación del PA Soluble en aceite Base oleosa Liberación lenta, pobre tendencia a liberarse PA soluble en agua Base oleosa Liberación rápida PA soluble en aceite Base miscible en agua Liberación moderada PA miscible en agua Base miscible en agua Liberación moderada, basada en la difusión LIBERACIÓN DEL FÁRMACO Si la constante de partición (K) es muy grande, el PA tiene afinidad por la fase oleosa y permanecerá en ella. C K= C oleosa acuosa Valor de K Concentración fase oleosa 1000 99.9 100 99.00 10 90.90 1 50.00 0.1 9.09 0.1 0.99 Formulación y Excipientes ASPECTOS FISICOQUÍMICOS: CARACTERÍSTICAS DEL FÁRMACO Y ELECCIÓN DEL EXCIPIENTE. TAMAÑO DE PARTÍCULA Cuanto menor sea el tamaño de partículas del PA en suspensión, mayor será el grado de dispersión del PA en la base, y más rápidamente se liberará. Si el fármaco se incorpora en forma de suspensión, el tamaño de partícula condicionará la velocidad de disolución. o SOLUBILIDAD Cuanto mayor sea más fácil y rápida es la cesión (Considerar el pequeño volumen en el que debe disolverse). Si el fármaco se halla disuelto su velocidad de absorción dependerá en gran medida de su lipofilia. ASPECTOS FISICOQUÍMICOS: CARACTERÍSTICAS DEL FÁRMACO Y ELECCIÓN DEL EXCIPIENTE. Concentración de fármaco. Dado que la absorción rectal suele ser incompleta, estas formas se sobre dosifican respecto a las orales. Este incremento de la concentración no modifica la velocidad de disolución pero provee mayores cantidades disueltas por unidad de tiempo y que por tanto están disponibles para la absorción. Influencia del pH. Se pueden utilizar tampones para modificar el pH y favorecer la disolución. Puesto que fundamentalmente se absorbe la fracción no ionizada, debe encontrarse un equilibrio entre estos dos factores. Se intenta conseguir pH= pKa ionizado sea del 50%. para que el porcentaje de fármaco Tipo de excipiente. Las bases de supositorios deben tener en la medida de lo posible escasa afinidad por el fármaco para favorecer la cesión del principio activo. EXCIPIENTES Los excipientes utilizados para la preparación de supositorios deben ser adecuados para que la forma farmacéutica funda en el recto a 37 ºC o se disuelva en el líquido que baña la zona de administración. Deben ser inocuos, no irritantes e inertes frente al principio activo así como garantizar la estabilidad del mismo. Debe tener la consistencia adecuada y favorecer la liberación del principio activo en aquellos supositorios destinados a tener acción sistémica. LA BASE DE UN SUPOSITORIO DEBE CONSIDERAR LA SIGUIENTES CARACTERÍSTICAS Estables Q y F durante la fabricación y el almacenamiento Deben fundir, disolverse o dispersarse a 37ºC Compatible con los fármacos Fácil de manejar e inerte Fácil de adquirir Dureza y consistencia adecuada No sensibilizante No irritante Con apariencia estética Sin olor No tóxica Buenas propiedades de expansión-contracción No unirse o interferir con el PA Intervalo de fusión y solidificación pequeño CLASIFICACIÓN DE LAS BASES: Lipofílicas Hidrofílicas ELECCIÓN DE LA BASE Los factores a considerar al elegir una base: Vía de administración (rectal, vaginal o uretral) Tipo de efecto (interno o local) Compatibilidad y estabilidad Comodidad del paciente BASES LIPOFÍLICAS ACEITES HIDROGENADOS Se obtienen a partir de aceites vegetales por hidrogenación de los ácidos grasos que integran los triglicéridos. Mezcla de ésteres, triglicéridos de ácidos grasos saturados de C-12 a C-18 y menores cantidades de mono y diglicéridos. Puede también contener cera de abeja, lecitina, polisorbatos, alcoholes etoxilados. Estas bases son estables, poco irritables; no requieren de condiciones especiales de almacenamiento, es uniforme su composición. Presentan buenas características para el moldeo, por lo que no requieren de lubricación. BASES LIPOFÍLICAS Ventajas Se obtienen bases de diferentes puntos de fusión y dureza La presencia de glicéridos parciales (algunos de ellos emulsificantes A/O) les da capacidad de incorpora agua (mayor hidrofilia). Funden entre 33-37ºC. No se oxidan y el p.fusión no se modifica por sobrecalentamiento. La distancia entre el punto de fusión y el de solidificación es pequeña. Presentan buen poder de retracción al enfriar. (Evita que se peguen a los moldes y se rompan al desmoldar.) o Inconvenientes Fundidos son poco viscosos facilitando la sedimentación de los principios incorporados en forma de suspensión. Dificulta n la reparación. Para evitarlo se pueden añadir viscosizantes. BASES OLEOSAS HIDROGENADAS Son una mezcla de ésteres, triglicéridos de ácidos grasos saturados de C-12 a C-18 y menores cantidades de mono y diglicéridos. Puede también contener cera de abeja, lecitina, polisorbatos, alcoholes etoxilados. Estas bases son estables, poco irritables; no requieren de condiciones especiales de almacenamiento, es uniforme su composición. Presentan buenas características para el moldeo, por lo que no requieren de lubricación. BASES OLEOSAS HIDROGENADAS Tienen un punto de fusión entre 35ºC a 37ºC, una densidad especifica de 0.89 a 37ºC. Base Witepsol.-Estas bases solidifican rápidamente en el molde, no requieren de lubricación, son blancas. Base Fattibase. Es mezcla de triglicéridos de palma, centro de palma y aceites de coco, monoestearato de glicerilo y estearato de polioxilo Bases Wecobee.-Son derivadas de aceite de palma y de coco. Están adicionados con monoestearato de glicerilo y glicolmonoestearato propileno. Otras bases:, Akosol, Novata, Suppocire, Massuprol BASES LIPOFÍLICAS ACEITES HIDROGENADOS DISPERSABLES EN AGUA. Se obtienen añadiendo a los aceites hidrogenados monoésteres y diésteres de Polietilenglicoles (tensoactivos no iónicos de HLB alto) que aumentan su hidrofilia. Base Densidad a Cont. de 20ºC (g/cm3) Humedad Calor específico Massa estarium Novata 0.955- 0.975 ≤ 0.2 % w/w ≈2.6 J/g/ºC 0.955- 0.975 ≤ 0.1 % w/w 1.9-2.1 J/g/ºC Suppocir 0.950- 0.960 < 0.5 % w/w 1.7-2.5 J/g/ºC e Witepsol 0.950- 0.980 ≤ 0.2 % w/w ≈ 2.6 J/g/ºC BASES HIDROFÍLICAS Cuando una base soluble es empleada, el fármaco se disuelve y mezcla con los fluidos corporales. Las bases solubles pueden causar irritación Sin embargo son ampliamente empleados en la actualidad. Las bases para supositorios de PEG y gelatinas, son las más empleadas. Debido a la variación en el peso molecular brindan flexibilidad en el punto de fusión. BASES DE POLIETILENGLICOL Son masas solubles de agua de PF relativamente alto. Constituido por productos de polimerización del oxido de etileno con diferentes masas moleculares La consistencia y PF varia con respecto al PM, el de 600 es líquido, el de 1500 es semisólido y el 5000 es sólido Son incompatibles con sales de plata, aminopiridina, quinina, aspirina, benzocaína, sulfonamidas, fenobarbital sódico, ácido salicílico. Por otro lado las bases de polietilenglicol nteractúan con el poliestireno, por lo que deben acondicionarse en contenedores de vidrio o aluminio GELATINA GLICERINADA Esta base de está compuesta de un 70% de glicerina, 20% gelatina y 10% de agua. Es de consistencia suave (favorece su uso vía vaginal pero no rectal) Debido a su carácter higroscópico deben ser acondicionados en envases herméticos No son recomendados para aplicación rectal pueden favorecer la defecación. Una base de glicerina esta compuesta de glicerina 87%, estearato de magnesio 8% y agua purificada 5%. CONSIDERAR AL FORMULAR: ¿Que tipo de efecto se espera sistémico o local? ¿Que vía de administración rectal, vaginal o uretral? ¿Qué tipo de liberación del fármaco requerimos lenta, rápida o prolongada? Métodos de fabricación Moldeo manual Fusión Compresión MOLDEO MANUAL Esta metodología requiere que el formulador cuente con experiencia ya que sin emplear calor se logre fabricar supositorios que en su mayoría emplean como base manteca de cacao. El moldeo involucra tamizado de la manteca de cacao, la adición del fármaco, mezclado (mortero y pistilo), vaciado de la mezcla en cilindros, cortado y acondicionado. MÉTODO DE MOLDEO Ventajas Desventajas No requiere equipo especial La manteca de cacao se encuentra disponible (en barras, tubos ralladura) comprimibles, Su preparación no requiere cálculos especiales Requiere experiencia y buena técnica Aun bien preparado no se tiene la apariencia de los elaborados por fusión FUSIÓN En esta metodología se calentará la base del supositorio hasta fundirla Se mezcla con el fármaco y los excipientes complementarios La mezcla se vaciara en los moldes, dejándose enfriar hasta solidificar. Una vez que la mezcla ha solidificado, se procede al acondicionado secundario FUSIÓN Ventajas. Apariencia elegante No necesita operaciones manuales Mayor uniformidad de dosis Menor riesgo de contaminación Desventajas. Se requieren moldes especiales Cuidado con fármacos termosensibles Cálculos de densidad y calibración de molde Mayor consumo de energía Se requiere de equipo de especializado Proceso de enfriamiento limitante en la calidad del producto obtenido COMPRESIÓN En esta metodología es adecuada para las bases que pueden formar supositorios por presión. Es especialmente adecuada para componentes termosensibles. En la compresión pueden emplearse bases como la mezcla de 6% de1,2,6-hexanotriol con PEG 1450 y 12% de Oxido de PE 4000. Las etapas claves para la fabricación de supositorios: 1.-Preparación de los moldes (verificar limpieza y estado general) 2.-Preparación de la base 3.-Preparación del fármaco 4.-Mezclado 5.-Dosificado 6.-Enfriamiento 7.-Acondicionado final Preparación del fármaco El tamaño de partícula del fármaco debe ser uniforme, para asegurar las distribución homogénea del mismo. Mezclado Los fármacos pueden ser mezclas parcialmente con parte de la base antes de su incorporación final. El tiempo de mezclado debe ser establecido para asegurar uniformidad de dosis. Una vez que la mezcla esta lista, esta se vaciara en los contenedores correspondientes. Los moldes o envases no deben emplearse fríos ya que provocaran fisuras en el supositorio. EVALUACIÓN DEL SUPOSITORIO Apariencia Peso promedio Dimensiones Hermeticidad (ME) Dureza Tiempo de desintegración Tiempo de fusión % Disolución Contenido del fármaco Uniformidad de contenido Limites microbianos Dureza Tiempo de desintegración Fusión Material de empaque primario PVC / PE 1.25 mL PVC / PE 3.3 mL Peel-off Aluminio Enfriamiento y acondicionamiento Equipo y maquinaria FACTORES A CONSIDERAR EN EL PROCESO DE FABRICACIÓN DE SUPOSITORIOS: o Presencia de agua o Higroscopicidad o Viscosidad o Contracción de volumen o Fragilidad FACTOR DE DESPLAZAMIENTO Dado que la dosificación se hace en volumen y que las densidades del principio activo y excipiente difieren, es necesario para calcular la cantidad de excipiente necesario conocer el denominado factor de desplazamiento. Factor de desplazamiento: Gramos de excipiente que son desplazados por un gramo de principio activo. Depende de la densidad: si el fármaco tiene la misma densidad de la base, desplazará un peso equivalente. Si la densidad es mayor que la de la base, desplazará un peso proporcionalmente menor de la base. Donde: f = factor de desplazamiento del P.A. en la base utilizada. p = Gramos de P.A. necesarios para n supositorios y = Peso en gramos n supositorios con P.A. (promedio). X = Peso en gramos n supositorios de solo base. (promedio) EJEMPLO DE CÁLCULO Ibuprofeno 250 mg C.b.p. 1 supositorio. Suponiendo que preparáramos 6 supositorios El factor de desplazamiento es especifico para la base con que se realizó Una vez que se conoce el factor de desplazamiento del principio activo en la base a utilizar se puede establecer la cantidad de base necesaria en el lote a fabricar a utilizar aplicando la siguiente formula: Donde: M = Masa en gramos de la base a utilizar por supositorio. F = Capacidad en gramos del molde. f = factor de desplazamiento. S= Cantidad de P.A. en gramos. ENSAYOS DE LOS SUPOSITORIOS TERMINADOS Aspecto La superficie debe ser regular y homogénea, lisa y sin fisuras. No debe presentar cristalización del fármaco en superficies. Las anomalías de superficie y fisura se advierten horas después del enfriamiento. Homogeneidad Seleccionados en distintas direcciones deben presentar una superficie regular, sin grietas, burbujas de aire ni grumos. Fundamentalmente no deben mostrar depósito de fármacos. ENSAYOS DE LOS SUPOSITORIOS TERMINADOS Peso Aunque los moldes liberan siempre el mismo volumen con cada supositorio, el peso de éstos puede variar por sedimentación o incluso por aire. Se acepta que haya diferencias de hasta cuatro a cinco %. Sin embargo, se establece que la desviación en el peso medio de veinte supositorios deberá estar comprendida en los siguientes valores: Supositorios de hasta 1.5g del peso +/- 10 %. Supositorios de 1.5g a 2.5g de peso +/- 7.5 % Supositorios de mas de 2.5 g de peso +/- 5% Temperatura de fusión. Para supositorios con excipiente liposoluble, la temperatura de fusión no deberá ser mayor de 37° C con un intervalo de fusión bien definido Tiempo de fusión Aquí lo que varía es el tiempo y la temperatura permanece constante: 37° centígrados +/- 0,50. Una vez estabilizada dicha temperatura se coloca el supositorio, previa exposición de 24 horas a temperatura ambiente, en el tubo de prueba y a partir de ese momento se mide el tiempo hasta que se produce la fusión completa. Dados los diferentes tipos de formulaciones considera aceptable un tiempo de fusión entre treinta y 40 minutos. Tiempo de disolución o disgregación. Para supositorios con excipiente hidrosoluble, la solución o disgregación debe producirse a una temperatura de 37 °C en no mas de 40 minutos. Para la determinación se puede emplear la misma técnica y el mismo aparato de escrito para determinar fusión, aunque puede usarse así mismo el método y aparato de la U. S. P para la desintegración de comprimidos. ENSAYOS DE LOS SUPOSITORIOS TERMINADOS Control de dureza Se coloca el supositorio entre dos discos (dentro de una cámara a 37ºC). Sobre el superior se va añadiendo peso (200 g cada minuto) hasta que el supositorio se colapsa. Uniformidad de contenido (Ensayo B). Cuando p.a. < 2 mg o si p.a. < 2% masa total n = 10 unidades: determinar contenido ENSAYOS DE LOS SUPOSITORIOS TERMINADOS Resistencia a la ruptura Es útil para determinar la igualdad de consistencia en diferentes partidas o en distintas etapas de una partida. Se aconseja tener en cuenta los siguientes valores: Para supositorios con excipiente liposoluble, a temperatura constante de 25 ±1°C igual a 1 a 4 Kg. Óptimo, 2 a 2,5 Kg., a temperatura cte de 30± 1°C no más de 2 Kg. (óptimo 1 Kg.) Para supositorios con excipiente hidrosolubles, a temperatura constante de 25 +/-1°C no menos de 2 Kg. Uniformidad de masa. (n = 20 unidades) BIBLIOGRAFÍA The theory and Practice of Industrial Pharmacy Theory and Practice of Contemporary Pharmaceutics Ghosh, Tapash & Jasti Bhaskara, CRC Press. Práctica Contemporánea en Farmacia Thompson, Judith, Mc Graw Hill, 2da Ed. The Art, Science and Technology of Pharmaceutical Compounding. Allen, Loyd, APhA