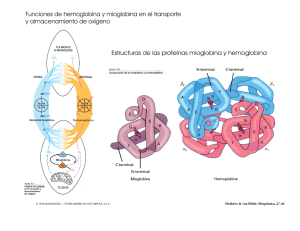
portadores de oxigeno artificiales de hemoglobina humana o
Anuncio

19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS A61K 35/14 (2006.01) C07K 14/805 (2006.01) C08G 65/32 (2006.01) ESPAÑA 12 11 Número de publicación: 2 275 712 51 Int. Cl.: TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 01962733 .0 86 Fecha de presentación : 12.06.2001 87 Número de publicación de la solicitud: 1294386 87 Fecha de publicación de la solicitud: 26.03.2003 54 Título: Portadores de oxígeno artificiales de hemoglobina humana o porcina reticulada modificada, procedi mientos para su preparación a partir de material modificado y su uso. 30 Prioridad: 29.06.2000 DE 100 31 740 73 Titular/es: SanguiBioTech GmbH Alfred-Herrhausen-Strasse 44 58455 Witten an der Ruhr, DE 45 Fecha de publicación de la mención BOPI: 16.06.2007 72 Inventor/es: Barnikol, Wolfgang; Burkhard, Oswald; Pötzschke, Harald; Domack, Ulrike; Dinkelmann, Stephanie; Fiedler, Bernd y Manz, Birgit 45 Fecha de la publicación del folleto de la patente: 74 Agente: Carpintero López, Francisco ES 2 275 712 T3 16.06.2007 Aviso: En el plazo de nueve meses a contar desde la fecha de publicación en el Boletín europeo de patentes, de la mención de concesión de la patente europea, cualquier persona podrá oponerse ante la Oficina Europea de Patentes a la patente concedida. La oposición deberá formularse por escrito y estar motivada; sólo se considerará como formulada una vez que se haya realizado el pago de la tasa de oposición (art. 99.1 del Convenio sobre concesión de Patentes Europeas). Venta de fascículos: Oficina Española de Patentes y Marcas. Pº de la Castellana, 75 – 28071 Madrid ES 2 275 712 T3 DESCRIPCIÓN Portadores de oxígeno artificiales de hemoglobina humana o porcina reticulada modificada, procedimientos para su preparación a partir de material modificado y su uso. 5 La presente invención comprende según las reivindicaciones la preparación de hemoglobinas químicamente modificadas reticuladas con propiedades funcionales mejoradas, las hemoglobinas reticuladas preparadas según este procedimiento así como su uso como portadores de oxígeno artificiales. El procedimiento de preparación se caracteriza tanto por simplicidad técnica como también por altos rendimientos. 10 15 20 25 30 35 40 45 50 55 60 65 Se conjuga hemoglobina altamente pura desoxigenada bajo la protección de un agente antioxidante con un efector de la unión de oxígeno, en especial pirixodal-5-fosfato, después se lleva a cabo la polimerización de la hemoglobina con glutardialdehído con un gran aumento del volumen de la mezcla de reacción y con ello una gran dilución de los reactantes durante la adición del reticulante. A continuación, tras la dilución con agua, se acopla químicamente un derivado de poli(óxido de etileno) a la hemoglobina reticulada. Se obtienen polímeros compatibles con plasma sanguíneo con características de unión a oxígeno optimizadas, que se pueden usar como portadores de oxígeno artificiales, en especial divididos en una proporción de bajo peso molecular y una de alto peso molecular como sustitutos sanguíneos o como aditivos sanguíneos, por ejemplo en el tratamiento de estados de falta de oxígeno. En la medicina resulta deseable por diferentes indicaciones médicas disponer de un sistema artificial de apoyo para el transporte de oxígeno. En caso de una grave pérdida de sangre parece no sólo razonable sustituir el volumen de forma isotónica e isooncótica, sino también restituir una función adicional de la sangre, concretamente, el transporte de oxígeno. Con la cada vez menor disposición a la donación de sangre, en casos catastróficos graves (entre otros en caso de guerra) hay cada vez menos sangre conservada adecuada disponible, en especial para poder cubrir una necesidad imprevisible. La disponibilidad momentánea de sangre conservada apropiada conlleva además considerables problemas logísticos. Además, la sangre conservada sólo se puede almacenar normalmente aproximadamente 35 días y por ello tiene que renovarse continuamente - lo que ocasiona costes considerables - mientras que soluciones artificiales se pueden conservar durante un tiempo esencialmente más prolongado, ya que dado el caso se pueden congelar. En función del tiempo de almacenamiento, la sangre conservada se adicifica intracelularmente, y por ello sus características de unión a oxígeno no son de ninguna manera óptimas, sino que más bien se deben regenerar en primer lugar en el organismo. Por el contrario, un portador de oxígeno artificial funciona de forma óptima desde el primer momento. La cada vez menor disposición a la donación de sangre se enfrenta por otro lado al creciente envejecimiento de la población que aumenta la demanda. De forma simultánea, a causa del envejecimiento también se reduce el número de los donantes de sangre potenciales. De la misma forma, a causa de los riesgos de infección ineludibles (debilidades inmunes, hepatitis), la población de los suburbios (“slums”) queda excluida como donante de sangre. Un sustituto sanguíneo artificial transportador de oxígeno también sería universal, independientemente del grupo sanguíneo. Es posible además que con un sustituto sanguíneo de este tipo se pueda atravesar un choque por hipovolemia antes que con una sangre conservada, ya que los eritrocitos de la conserva están rígidos y por ello presentan una transitabilidad capilar reducida. En cualquier caso, los experimentos con animales han demostrado que se puede combatir el choque por hipovolemia con un sustituto sanguíneo transportador de oxígeno de forma más eficaz que con expansores plasmáticos simples (Pabst, R. (1977): “Sauerstofftransport mit stromafreien Hämoglobinlösungen und Fluorocarbonen”, Med. Klin. 72: 1555-1562, Keipert P.E., Chang T. M.S. (1985) “Pyridoxylated Polyhemoglobin as a Red Cell Substitute for Resucitation of Letal Hemorrhagic Shock in Conscious Rats2”, Biomater., Med. Dev. Artif. Organs 13: 1-15). A esto se añaden otras aplicaciones de un portador de oxígeno artificial: cada vez se pueden realizar menos intervenciones quirúrgicas complicadas que cursan obligatoriamente con graves pérdidas de sangre porque faltan las reservas de sangre necesarias. En cambio se desarrollan intervenciones quirúrgicas cada vez mayores y más invasivas - entre las que se cuentan especialmente también transplantes - cuya realización en cada caso concreto depende decisivamente de la disponibilidad de muchas reservas de sangre apropiadas. Adicionalmente, se pueden conservar mucho mejor órganos previstos para un transplante si se prefunden con portadores de oxígeno (artificiales). Sólo un transplante de hígado requiere hasta 100 unidades de transfusión de 450 ml cada una. En casos de daños por politraumatismo (por ejemplo a causa de un accidente de automóvil) se requieren grandes cantidades similares. Pero no sólo en caso de una grave pérdida de sangre, sino también en caso de trastornos circulatorios crónicos (en especial cerebrales, coronarios, renales y periféricos - por ejemplo en caso de sordera sensitiva súbita - o de una crisis anémica por ejemplo en caso de osteomielitis crónica o después de quimioterapia tumoral) existe una necesidad de una sustancia sanguínea transportadora de oxígeno artificial. También en caso de una falta de oxígeno fetal a causa de una insuficiencia placentaria para evitar una amenaza de aborto o para evitar los daños por la falta de oxígeno en el parto se ofrece la aplicación del aditivo o para la deshabituación de la respiración asistida. Una necesidad de este tipo es incluso considerablemente superior a la del caso mencionado anteriormente de una grave pérdida de sangre: tales trastornos circulatorios crónicos son la causa de la muerte de aproximadamente 750.000 personas al año en Alemania. A esto se añaden los casos de enfermedad por esta causa. Sólo aproximadamente la mitad de personas mueren de cáncer anualmente. La falta crónica de oxígeno en los tejidos se intenta tratar de forma conocida mediante suministro de oxígeno hiperbárico. Independientemente de que esta terapia sólo surte efecto mientras impera la sobrepresión de oxígeno e independientemente de que el procedimiento no está exento de peligro, A este respecto existe el peligro de daños tisulares oxidativos por reacciones radicálicas de oxígeno que se pueden comprobar mediante los correspondientes productos de reacción. Un portador de oxígeno artificial actúa mientras está presente y ofrece a los tejidos el llamado oxígeno de baja presión, de forma que no aparecen los daños mencionados. La aplicación de un aditivo sanguíneo transportador de oxígeno como apoyo provisional del sistema de transporte de oxígeno endógeno 2 ES 2 275 712 T3 representa otra posibilidad y alternativa para la lucha contra la falta de oxígeno tisular crónica que hasta ahora se ha intentado tratar con agentes potenciadores de la circulación (por ejemplo, vasodilatadores). 5 10 15 20 Para el tipo de aplicación, resulta muy adecuado el concepto de que se trate de una terapia de oxígeno funcional: no se aplica el sustrato (el oxígeno), sino que se mejora la función del sistema portador que lleva el oxígeno a los tejidos. Esto hace multiplicativo el efecto de la terapia, así como muy efectivo, y le proporciona simultáneamente un carácter catalítico. A esto se añaden también indicios claros de que un portador de oxígeno disuelto en plasma es mucho más eficaz que uno “empaquetado” en eritrocitos. Adicionalmente, un sustituto sanguíneo artificial de este tipo puede prepararse exento de los patógenos conocidos; de esta forma se pueden evitar problemas infecciosos como hepatitis y el síndrome de inmunodeficiencia adquirida (SIDA). Un grupo receptor potencial adicional para soluciones transportadoras de oxígeno artificiales son pacientes para los que se prevé una reacción alérgica por ejemplo frente a los antígenos HLA. Hasta ahora se ha intentado eliminar los leucocitos de la sangre conservada mediante una filtración sobre algodón. Las soluciones de sustitutos sanguíneos artificiales estarían por el contrario completamente exentas de leucocitos. Muy recientemente se ha observado en cerdos que tras la mejora del suministro de oxígeno (disminución de la afinidad de la hemoglobina por el oxígeno), se reduce el volumen de latido del corazón y la frecuencia cardiaca permanece inalterada (Villereal M.C. y col. (1987): “Engineered Red Blood Cells with Modified Oxygen Transport Properties: A New Oxygen Carrier”, Biomater., Med. Dev., Artif. Organs 15: 397). En otro trabajo (Bosman R.J. y col., (1992): “Free Polymerized Hemoglobin Versus Hydroxyetyl Starch in Resucitation of hypopovolemic dogs”, Anesth. Analg. 75: 811-817) se mostró que la administración de soluciones transportadoras de oxígeno tras un choque de hipovolemia en perros evita el aumento de volumen del corazón y por lo tanto protege al corazón. Aquí se abre la posibilidad de alcanzar una protección miocárdica funcional mediante la mejora del suministro de oxígeno, lo que resulta de ayuda por ejemplo en el caso de un infarto. Esto sería un aspecto completamente nuevo para aplicación de soluciones transportadoras de oxígeno. 25 30 Otra aplicación de tales portadores de oxígeno artificiales sería el aumento de la sensibilidad a la irradiación de tumores, ya que cada vez se insinúa más que portadores de oxígeno moleculares disueltos en el plasma ceden oxígeno a los tejidos de forma mucho más efectiva que sangre completa: tales portadores artificiales ocasionan una sinergia con los portadores nativos (intraeritrocitarios). Es decir, el portador artificial molecularmente disperso en el plasma sanguíneo no sólo cede oxígeno a los capilares de la mejor manera de por sí, sino que además refuerza la cesión de oxígeno del sistema nativo existente, y concretamente mediante el mecanismos de la difusión facilitada. Esto significa que para este propósito sólo se requiere una pequeña concentración del portador artificial en el plasma. A pesar de ello, esta terapia funcional se mantiene excepcionalmente efectiva (véase anteriormente). 35 Todo lo dicho pone de manifiesto la necesidad de un transportador de oxígeno artificial. Resulta imprescindible para la utilización de un portador de oxígeno artificial que su material de partida esté disponible en cantidad suficiente. Las reservas de sangre caducadas no resuelven por tanto el problema. Por ello es necesario utilizar hemoglobinas animales, preferentemente de los animales de matadero más importantes; vacas y/o cerdos. 40 A partir de la representación de la necesidad de portadores de oxígeno artificiales resultan a grandes rasgos dos tipos de aplicación: por una parte en caso de una gran pérdida de sangre y por otra parte en caso de una falta de oxígeno crónica. En el primer caso, para la compensación se necesita un sustituto volumétrico isooncótico transportador de oxígeno (portadores de oxígeno artificiales de primera generación), en el segundo caso por el contrario, un aditivo sanguíneo transportador de oxígeno (portadores de oxígeno artificiales de segunda y nueva generación). Como se ha mencionado, el segundo caso es con mucho el más común. Por lo habitual, un aditivo sanguíneo correspondiente permite, en combinación con un llamado expansor de plasma, también la terapia de una perdida de sangre grave con la gran ventaja de que el médico tiene la posibilidad de adaptar tanto el aporte de portadores de oxígeno como también del volumen de líquido a las necesidades del paciente concreto. 45 50 También el organismo puede modificar ambos (cantidad del portador de oxígeno y volumen sanguíneo) independientemente entre sí, concretamente la formación de eritrocitos a través de eritropoyetina y el volumen plasmático mediante un sistema de regulación propio. Ambas magnitudes se desacoplan por el hecho de que el portador tiene en la sangre una presión osmótica coloidal mucho menor que el plasma. 55 Hasta ahora otros han seguido fundamentalmente tres estrategias para el desarrollo de un portador de oxígeno para la sangre (estado de la técnica; Rudolph A.S. y col. (eds.): Red Blood Cell Substitutes: Basic principles and Clinical Applications, Marcel Dekker, Nueva York, u.a. 1998; Tsuchida E. (ed.): Blood Substitutes: Present and Future Perspectives, Elsevier Sciences, Ámsterdam 1998; Chang, T.M.S. (autor o ed.): Blood Substitutes: Principles, Methods, Products and Clinical Trials, Volumen 1 y Volumen 2, Karger Landes, Basilea u.a. 1997 y 1998). 60 65 Uso de emulsiones con hidrocarburos fluorados - últimamente también se utilizan otros halógenos como bromo - en las que el oxígeno puede disolverse especialmente bien (Hirlingen W.K. y col. (1982): “Auswirkunden eines teilweisen Blutaustausches mit Fluosol DA 20% auf den intakten Organismus des Schweines”, Annästhesist 31 660-666). Dado que los fluorocarburos son lipófilos, es de esperar sin embargo que se produzcan interacciones y trastornos en las capas lipídicas de las membranas celulares. Estas últimas son componentes funcionales integrantes de las células. Además los fluorocarburos se deben dispersar con emulgentes tales como fosfolípidos, los cuales pueden interferir adicionalmente con las membranas de las células (los llamados portadores de oxígeno artificiales sobre la base de fluorocarburos de primera generación). 3 ES 2 275 712 T3 5 10 15 20 25 30 35 40 45 50 La microencapsulación de soluciones altamente concentradas de hemoglobina natural y también químicamente modificada en vesículas fosfolipídicas con la adición de efectores apropiados de la unión de hemoglobina (“eritrocitos artificiales o hemosomas”) representa una estrategia adicional (Ogata Y. (1994): “Characteristics of Neo Red Cells, Their Function and Safety: In-Vivo Studies”, Artificial Cells, Blood Substiutes, and Immobilization Biotechnologies 22 875-881). En este campo se han realizado también los primeros experimentos animales (Hunt, A.C, y col., (1995): “Synthesis and Evaluation of a Protypal Artificial Red Cell”, Science 230: 1165-1168). Las vesículas tenían un diámetro de menos de 0,05 µm y eran por lo tanto en cuestión de volumen dos potencias decimales menores que los glóbulos rojos naturales. La tercera estrategia consiste en la preparación de soluciones de hemoglobina que se pueden infundir. El portador de oxígeno artificial está presente por lo tanto de forma extracelular en la sangre. Mientras que las dos primeras soluciones del problema se pueden ver como la preparación de una sangre artificial, de forma que no puede aparecer la dificultad de una interferencia osmótica coloidal, en el caso de esta solución del problema se encontraba inicialmente un expansor plasmático cuyas macromoléculas también podían transportar oxígeno (los llamados portadores de oxígeno artificiales sobre la base de hemoglobina de primera generación). La hemoglobina nativa no se puede usar para esto, ya que por ejemplo es excretada muy rápidamente por los riñones. Es ineludible por lo tanto una modificación química. En el marco de esta estrategia por ejemplo se ha unido la hemoglobina por sus grupos amino de forma covalente a dextranos o se ha polimerizado entre sí hasta un peso molecular de aproximadamente 700.000 g/mol. Lo primero fue perseguido por ejemplo por la empresa Fresenius (Fresenius E. (1976): “Blood and Plasma Substitute Comprising a Colloidal Solution of Hydroxyethyl Starch Coupled To Haemoglobin Free Stroma”, publicación de patente DE-P 2616-086)I y lo último por la empresa Biotest (Bonhard K. y col. (1983): “Verfahren zur Gewinnung von hepatitissicheren, sterilen, pyrogenfreien und stromafreien Hämoglobinlösungen”, documento de patente DE-O-3130770) y la empresa Alza (Bonsen P. (1976): “Water-soluble Polymerized Hemoglobin”, documento de patente DE-O-2607706). Otra estrategia referente a soluciones extracelulares es estabilizar la hemoglobina, reticulándola en tetrámeros o enganchando grupos laterales (oligoetilenglicol), sin aumentar esencialmente el peso molecular (tetramérico) (estabilisierte Hämoglobine (Matsushita M., y col. (1987): “In vivo Evaluation of Pyridoxylated Hemoglobin-Polyoxyethylene Conjugate”, Biomat. Artif. Cells., artif. Org. 15: 377). Como se ha mencionado anteriormente, las soluciones de sustitutos sanguíneos extracelulares han demostrado en experimentos animales resultados prometedores en lo referente a un tratamiento de choque. Es una ventaja del uso de hemoglobinas como portadores de oxígeno artificiales - frente a los fluorocarburos - que se puedan aprovechar las adecuadas propiedades de la unión natural a oxígeno. A ellas pertenecen la afinidad por el oxígeno media óptimamente adaptada, la cooperatividad homotrópica, es decir, la forma de S de la curva de unión a oxígeno, así como el efecto de Bohr (alcalino), que forma la base de un mecanismo de autorregulación natural para la cesión dirigida de oxígeno a tejidos con carencia de suministro. De la bibliografía relacionada se desprende claramente que un acoplamiento covalente intratetramérico de las unidades de hemoglobina (Keipert P.E. y col. (1989): “Metabolism, Distribution and Excretion of HbXL: A Nondissociation Interdimerically Crosslinked Hemoglobin with excepcional Oxygen Offloading Capability”, - en Chang T.M.S., Geyer R.P. (Eds.): Blood Substitutes, Marcel Dekker, Nueva York 1989) y/o una polimerización de la hemoglobina conducen a un fuerte aumento del tiempo de permanencia en sangre (Chang T.M.S. (1987): “Modified Hemoglobin as Red Cell Blood Substitutes”, Biomater., Med. Devices Artif. Organs 14: 323-328; Friedman H.J. y col. (1984): “In vivo Evaluation of Pyridoxylated-Polymerized Hemoglobin Solution”, Surg., Gynecol., Obstet. 159: 429-435). Esto es una condición esencial para la utilidad clínica de tales soluciones. En el caso de los portadores de oxígeno artificiales extracelulares molecularmente dispersos, se han desarrollado hasta ahora sin embargo ignorando un gran campo de demanda - la falta de oxígeno crónica -, intentando soluciones isooncóticas. Las consecuencias de trastornos circulatorios crónicos que aparecen considerablemente más a menudo, como se ha mencionado anteriormente, sólo se pueden mejorar mediante soluciones transportadoras de oxígeno cuya presión osmótica coloidal se despreciable frente a la normal (3,5 kPa), es decir, sólo con ayuda de un aditivo sanguíneo transportador de oxígeno, en cierto modo un concentrado eritrocítico molecular”. Estos son portadores de oxígeno artificiales basados en hemoglobina de segunda generación. 55 En los distintos intentos de desarrollar un transportador de oxígeno artificial surgieron los problemas que se mencionan a continuación: 60 65 • Aumento de la afinidad oxígeno-hemoglobina: la presión de semisaturación (P50) se reduce a causa de la modificación química en la molécula de hemoglobina. Por ello se dificulta la cesión del oxígeno al tejido. Esto aparece marcadamente en el caso de la unión de hemoglobina a dextrano. Para evitar el aumento de la afinidad de oxígeno, se han unido efectores apropiados (por ejemplo, piridoxalfosfato) a los grupos prostéticos de la hemoglobina. • A menudo disminuyen simultáneamente el llamado valor n50 (índice de HILL) como una expresión de la cooperatividad homotrópica disminuida (forma de S atenuada de la curva de unión oxígeno-hemoglobina), lo que de igual modo dificulta el suministro de oxígeno al tejido. Esta forma de S de la curva de unión oxígeno-hemoglobina facilita asimismo la captación de oxígeno en los pulmones y su cesión a las células. 4 ES 2 275 712 T3 Los fluorocarburos poseen por el contrario una “curva de unión a oxígeno” lineal y no tienen por lo tanto la misma ventaja funcional. 10 • El portador de oxígeno artificial tiene a menudo un tiempo de permanencia en el organismo demasiado escaso, la excreción de las hemoglobinas disueltas se lleva a cabo a través de los riñones. En caso de soluciones de hemoglobina extracelulares como portadores de oxígeno artificiales se ha intentado impedir la excreción mediante reticulación intermolecular, no obstante el tiempo de permanencia de las hemoglobinas extracelulares sigue siendo inferior al deseado. Por el contrario, los hemosomas son retirados del plasma por el sistema retículoendotelial del organismo. Por ejemplo, el tiempo medio de los eritrocitos artificiales ascendió a sólo 5,8 horas (véase anteriormente). 15 • Respecto a la alta presión osmótica coloidal: A causa de ello se puede producir una pérdida de volumen (choque hipovolémico). Este efecto aparece cuando el peso molecular del portador de oxígeno artificial es comparable con el de las proteínas plasmáticas. Tampoco se tiene libertad a este respecto con la dosificación del portador de oxígeno artificial, sino que se tienen que tomar en consideración las proporciones oncóticas. 5 • El ambiente oncótico del plasma se determina además de forma decisiva por el llamado segundo coeficiente del virial (valor A2 ): éste caracteriza la interacción del portador de oxígeno (siempre macromolecular) con el disolvente (agua). La síntesis ha de ajustarse de tal manera que este valor se aproxime a cero. 20 • Respecto a la alta viscosidad de la solución de portador: esta va acompañada normalmente por un valor A2 demasiado elevado, y aparece preferiblemente cuando un portador está compuesto de moléculas en cadena. Una viscosidad demasiado elevada no aparece según la ley de la viscosidad de Einstein cuando las moléculas portadoras poliméricas son redondeadas y compactas. 25 • Estabilidad in vitro de las moléculas portadoras: esta se refiere por un lado a la desintegración de las moléculas y por otro a la unión oxidativa de metahemoglobina, la cual ya no puede unir oxígeno y finalmente a la viscosidad a través de interacciones que se modifican lentamente entre el portador y la albúmina del plasma. 30 • Reacción desproporcionada del sistema reticuloendotelial (SRE): Un factor de influencia principal es el tamaño molecular del portador artificial. Existe para ello un límite crítico en aproximadamente 0,3 µm: partículas mayores activan el SRE. 35 • Daño renal y hepático: Un choque renal apareció sobre todo cuando se usó solución de hemoglobina con contenido en estroma. Desde que se ultrafiltran las soluciones, ya no se ha observado ningún daño renal. Los daños hepáticos se indicaron con ayuda del perfil de transaminasas plasmáticas, estas se basan presumiblemente en interacciones de la membrana celular: el hígado posee una circulación abierta (capilares fenestrados). 40 • También debe comprobarse la hemostasia; son posibles trastornos en el sentido de una potenciación o de un impedimento, se debe prestar especial atención a la agregación de los trombocitos. 45 50 55 • Efecto antigénico: respecto a esto se ha demostrado recientemente en estudios homólogos con ratas que la hemoglobina nativa no tiene un efecto antigénico y que la polimerización con glutardialdehído no aumenta la antigenicidad (Hertzman C.M. y col. (1986): “FERUM Antibody Titers in Rats Receiving Repeated Small Subcutaneous Injection of Hemoglobin or Polyhemoglobin. A Preliminary Report”. Int. J. Artif. Organs 9: 179-192). En el mismo trabajo se muestra que la hemoglobina humana nativa y polimerizada actúa de forma poco antigénica en ratas y que el efecto mediante la polimerización se refuerza como mucho en un grado mínimo. • Los efectos tóxicos se pueden diferenciar en pirogénicos, vasoconstrictores - por ejemplo en los vasos coronarios - y endotóxicos. El efecto vasoconstrictor se basa presumiblemente en la captura de los radicales de monóxido de nitrógeno, los cuales son sustancias de control vasodilatadoras endógenas conocidas; el efecto vasoconstrictor se puede aclarar no obstante también mediante la alta eficacia de los portadores artificiales, ya que se suministra “demasiado bien” oxígeno a la musculatura lisa. • Estabilidad in vivo: Se puede pensar en una catálisis enzimática endógena, por ejemplo mediante proteasas. 60 65 • Sobrecarga del organismo con lipoides (emulgentes): esta complicación aparece con la aplicación de soluciones de hemoglobina y fluorocarburos microencapsuladas, a este respecto se determinaron en ratas una activación del complemento a través de la ruta alternativa así como una formación de anticuerpos. • La tolerabilidad de los portadores artificiales con plasma sanguíneo humano reciente, en función del valor de pH puede producir precipitaciones. Presumiblemente a causa de los problemas mencionados hasta ahora no está disponible un portador de oxígeno artificial para la aplicación clínica rutinaria. 5 ES 2 275 712 T3 A partir de la mención de los diversos problemas se deduce que aún sigue habiendo un gran catálogo de requerimientos para un portador de oxígeno artificial útil. 5 10 En la naturaleza el oxígeno siempre se transporta en enormes agregados microscópicos. Aquí se han desarrollado básicamente dos “soluciones al problema” diferentes. En animales superiores (y también en los seres humanos), el portador de oxígeno molecular está empaquetado en células (en los eritrocitos). En segundo lugar se desarrollaron enormes moléculas de unión a oxígeno que no se encuentran intracelularmente, sino extracelularmente disueltas en la hemolinfa, esta variante se encuentra predominantemente en animales inferiores con diferentes características. Los anélidos poseen por ejemplo hemoglobinas de alto peso molecular con un peso molecular medio alrededor de 3000000 g/mol como portadores de oxígeno. Además existen las llamadas hemoeritrinas, en las que el hierro como agente de unión a oxígeno está directamente acoplado molecularmente a la proteína. Finalmente se encuentran las hemocianinas con un peso molecular alrededor de 8000000 g/mol, en las que el ión de metal pesado de unión a oxígeno es cobre, véase también Barnikol W.K.R., y col. (1996): “Hyperpolymere Hämoglobine als küstliche Sauerstoffträger. Ein innovativer Ansatz der medizinischen Entwicklung”, Therapiewoche 46: 811-815. 15 La transición en la historia del desarrollo desde los portadores de oxígeno extracelulares hasta los eritrocitos ha llevado a que el contenido en oxígeno del fluido sanguíneo se incremente tres veces: mientras que 1 ml de “sangre” de la lombriz de tierra sólo puede unir como máximo 3,6 µmoles de oxígeno, en el mismo volumen de sangre humana se unen hasta 9,0 µmoles de oxígeno. 20 25 30 35 40 45 50 55 60 65 La lombriz de tierra posee en su sangre enormes moléculas (eritrocruorina) como portadores de oxígeno con un peso molecular de aproximadamente 3400000 g/mol con alrededor de 200 sitios de unión para oxígeno. Además la molécula es muy compacta y su estructura cuaternaria es altamente ordenada. La molécula es tan grande que se puede ver directamente con ayuda del microscopio electrónico. Su concentración en la hemolinfa asciende a al menos 6 g/dl. La medición de la curva de unión a oxígeno en condiciones in vivo simuladas da como resultado una presión de semisaturación (P50) de 9,1 Torr (1,2 kPa) (Barnikol W.K.R., Burkhard O. (1987): “Highly Polymeryzed Human Hemoglobin as an Oxygen Carrying Blood Substitute”, Advances in Experimental Medicine and Biology Volumen 215: 129-134; Barnikol W.K.R. (1986): “The Influence of Glutardialdehyde on the Oxygen Cooperativity of Human Hemoglobin”, Pflügers Archiv 406: R61). Este sistema suministra por lo tanto suficiente oxígeno a las células de la lombriz de tierra. Por el peso molecular extremadamente alto, la hemoglobina de la lombriz de tierra prácticamente ya no tiene ningún efecto osmótico coloidal (sólo aproximadamente 4 kPa). Con ello, como en la sangre de los mamíferos - la presión oncótica de los eritrocitos asciende sólo a 1,3 10−6 Pa - tanto la función de coloidoosmolaridad y de unión a oxígeno están desacopladas, y ambas pueden variarse libremente por el organismo como variable de control. Si se quiere transmitir el principio del sistema de la lombriz de tierra a portadores de oxígeno artificiales que se basen en hemoglobina humana o animal, se debe modificar la molécula de hemoglobina de tal forma que pueda apoyar como enorme molécula extracelular con presión oncótica despreciable al transporte de oxígeno normal de los eritrocitos al menos temporalmente. Tales portadores de oxígeno artificiales son por lo tanto hemoglobina altamente polimerizada que debe tener en cuenta toda la problemática anteriormente mencionada. La “hemoglobina” de lombriz de tierra, que cumple con los requisitos de presión oncótica, no se puede usar para este propósito en humanos porque presumiblemente posee una alta antigenicidad, además la presión de semisaturación es con 1,2 kPa demasiado baja (Barnikol W.K.R., Burkhard O. (1987): “Highly Polymeryzed Human Hemoglobin as an Oxygen Carrying Blood Substitute”, Advances in Experimental Medicine and Biology Volumen 215: 129-134; Barnikol W.K.R. (1986): “The Influence of Glutardialdehyde on the Oxygen Cooperativity of Human Hemoglobin”, Pflügers Archiv 406: R61). Además, presumiblemente no se puede obtener en las cantidades necesarias. Hasta ahora, en el desarrollo de portadores de oxígeno artificiales se ha intentado ajustar su presión de semisaturación exactamente al valor normal para el ser humano de aproximadamente 3,47 kPa. Experimentos con animales muestran en realidad que un portador de oxígeno artificial molecularmente disperso con una presión de semisaturación de aproximadamente 2 kPa oxigena los órganos de la mejor forma (Conover y col. (1999), Art. Cells, Blood Subst., and Immobil. Biotech. 27 93-107). Por otra parte, experimentos con animales muestran también no obstante que para un suministro suficiente de oxígeno resulta igualmente importante una capacidad de oxígeno de la sangre suficientemente grande (Moss G.S., y col. (1984): “Hemoglobin Solution - From Tetramer to Polymer”, en: The Red Cells; Sixth Aven Arbor Conference, Alan Riss, Nueva York, 1984: 191-210). Esta depende a su vez de la concentración posible del portador de oxígeno en el plasma. Además se demuestra a este respecto que una presión de semisaturación de 3,47 kPa no se debe mantener indispensablemente. Esencialmente consiste más bien en que no se puede quedar por debajo de un valor crítico determinado. A los requerimientos en el desarrollo de un portador de oxígeno artificial se suman el hecho de que un procedimiento de preparación debe ser lo más simple posible y con ello rentable, sobre todo ya que se debe trabajar de forma estéril desde el principio. El producto se debe poder obtener con el mayor rendimiento posible. Durante la reacción de reticulación se debe producir simultáneamente material para su uso como aditivo sanguíneo así como aquel para su uso como sustituto del volumen sanguíneo transportador de oxígeno. En especial, en la preparación de los polímeros artificiales de hemoglobina mediante la reticulación de las moléculas de hemoglobina a través de sus grupos amino por medio de reticulantes difuncionales se debe prestar atención además a que no se formen redes moleculares que son insolubles y por lo tanto disminuyen el rendimiento del producto. Por ello debe evitarse la aparición de la llamada distribución de percolación de los pesos moleculares: 6 ES 2 275 712 T3 La presente invención tenía como objetivo poder preparar en un procedimiento técnicamente sencillo con grandes rendimientos portadores de oxígeno artificiales hipooncóticos de hemoglobina reticulada que poseyesen buenas características funcionales optimizadas, en especial la característica de la unión a oxígeno y que fuesen adecuados para aplicarse como productos farmacéuticos a seres humanos. 5 10 15 El objetivo se consigue según la invención como se describe a continuación. El problema fundamental de la aparición de una distribución de percolación de los grados de multimerización y de los pesos moleculares a través de la reticulación de las hemoglobinas polifuncionales con el reticulante difuncional glutardialdehído se pudo resolver sorprendentemente gracias al hecho de que durante la reticulación el volumen de la mezcla de reacción se aumenta en gran medida (en total de 2 a 10 veces), y concretamente, añadiendo en primer lugar simultáneamente el reticulante en solución diluida y a continuación diluyéndolo adicionalmente con agua. Con ello se producen hemoglobinas reticuladas con alto grado de reticulación con altos rendimientos, sin que se produzca una distribución de percolación de los pesos moleculares con formación de redes moleculares insolubles. El producto en bruto de la reticulación destaca más bien por un límite superior deseado (aproximado) determinado del intervalo de pesos moleculares. Se obtiene en el cromatograma en gel una llamada distribución en cuadrilátero del peso molecular (véanse la figura 1, figura 2 y figura 3). La preparación según la invención comprende por lo tanto las siguientes etapas: 20 En una reacción en un recipiente, la hemoglobina i) en primer lugar se desoxigena, en especial mediante flujo de nitrógeno; ii) a continuación se hace reaccionar covalentemente con un efector químicamente reactivo de la unión a oxígeno: 25 iii) luego se mezcla la solución con un efector no reactivo químicamente y entonces 30 iv) la hemoglobina se reticula entre sí covalentemente de modo estable con glutardialdehído, bajo una gran dilución (de 2 a 5 veces) del volumen de la mezcla de reacción, con adición simultánea del reticulante (en solución), y a continuación el volumen de reacción se aumenta adicionalmente (dilución total del volumen de la solución hasta 210, en especial 2-7, especialmente 5-6 veces el volumen) y después v) se acopla covalentemente un óxido de polietileno. 35 El producto obtenido se puede procesar de forma conocida. Preferiblemente, la hemoglobina de partida es de origen porcino o proviene de seres humanos, con muy especial preferencia, de origen porcino, en especial del cerdo doméstico. 40 45 En especial, según la invención, en la etapa iii) se añade glutardialdehído en una solución altamente diluida de forma cronometrada. Preferiblemente, se lleva a cabo a continuación una dilución adicional y un aumento del volumen de reacción con agua, de forma que se alcance la dilución total anteriormente mencionada. A este respecto se prefiere que en la etapa iv) se añada glutardialdehído en una cantidad en moles de 6-10, preferiblemente 7-9 mol/mol en relación con la hemoglobina monomérica, disuelto en 1-4, preferiblemente 1-2, en especial 1,5-2, con muy especial preferencia 1,7-1,9 litros de agua por litro de solución de reacción original. Esta adición se lleva a cabo de forma cronometrada entre aproximadamente 3 y 15, preferiblemente 3-10, en especial 4-6 minutos. A continuación la solución reacciona entre 1 y 6 horas. 50 Adicionalmente se prefiere que a la solución que contiene hemoglobina antes de la reacción según la etapa ii) se le añadan 2-8, en especial 3-6, con muy especial preferencia 3-4 moles de ascorbato de sodio por mol de hemoglobina no reticulada. Esta reacción se lleva a cabo a lo largo de 0,5-6 horas, en especial 70-120 minutos. 55 60 Además se une covalentemente, en la etapa ii) preferentemente, como efector piridoxal-5’-fosfato en una proporción molar, en relación con la hemoglobina monomérica de 0,5 a 3, preferiblemente de 1 a 2,5 mol/mol a lo largo de un periodo de 0,5-20, en especial de 1-7 horas. Según la invención resulta además ventajoso y se prefiere que en la etapa iii) así como en la etapa iv) tras la unión covalente de piridoxal-5’-fosfato así como glutardialdehído se añada respectivamente borohidruro sódico reductor. Este se añade en especial en la etapa ii) en una cantidad de 1-9, preferiblemente de 1-5, en especial de 1-2,5 mol/mol, por ejemplo de 30 a 90 minutos, y en la etapa iv) en una cantidad de 5-20, en especial de 6-12 mol/mol, respectivamente en relación con la hemoglobina monomérica durante 15 a 100 minutos. 65 Con especial preferencia, en la etapa iii) se añade como efector químicamente no reactivo 2,3-difosfoglicerato en una cantidad de 0,5-6, en especial de 1-4 mol/mol, en relación con la hemoglobina monomérica y aproximadamente 5-50 minutos, en especial 10-20 y con muy especial 15 minutos después se añade glutardialdehído. 7 ES 2 275 712 T3 5 Como poli(óxido de etileno) se acopla preferiblemente un éter polieteilenglicólico por ejemplo con un resto alquilo C1-C5 como metilo, etilo, butilo con un peso molecular de 500 a 3000 g/mol, en especial un derivado de metoxipolietilenglicol con un peso molecular de 1500-2500 g/mol, en especial de 2000 g/mol, como especialmente succinimidil-propionato de metoxi-polietilenglicol, en cantidades de 2-12, en especial de 3-8 mol/mol de hemoglobina. Otros productos de derivatización son metoxi-polietilenglicol-succinimidill-succinamida y succinimidil-oxiacetato de metoxipolietilenglicol. El acoplamiento de poli(óxido de alquileno) a hemoglobinas no reticuladas se describe en los documentos US-A 4179337, US 5478805, US 5386014, EP-A 0206448, EP-A 0067029, DE-OS 3026398. 10 La reacción se lleva a cabo preferiblemente a lo largo de 1-4, en especial 2-3 horas. 15 20 25 Adicionalmente resulta ventajoso que todas las reacciones de preparación se lleven a cabo especialmente en soluciones que se han liberado de oxígeno mediante tonometría con gases libres de oxígeno. El procedimiento usado se describe en: Pötzschke H.: Hyperpolymere des menschliches Hämoglobins: Entwicklung präparativer Verfahren zu ihrer Synthese, Validierung analitischer Methoden und Geräte zu ihrer Charakterisierung, Tesis doctoral, Facultad de Medicina, Universidad de Viena, 1997. El producto obtenido puede procesarse de forma conocida, como se indica a continuación. Presenta especialmente una distribución de pesos moleculares de 50000 hasta 5000000, dado el caso hasta 10000000 g/mol o más. El producto obtenido se puede separar en una fracción de peso molecular medio superior y una fracción de peso molecular medio inferior, estando el límite de separación preferiblemente en torno a los 700000 g/mol, mediante un procedimiento de separación de sustancias preparativo, como por ejemplo una cromatografía de exclusión volumétrica, una ultrafiltración, una precipitación fraccionada, por ejemplo con poli(óxido de alquileno) o sales como sulfato amónico como agente de precipitación o un procedimiento de fraccionamiento de campo-flujo (véase Curling J.M. (ed) Methods of Plasma Protein Fractionation, Academic Press, Londres entre otros 1980, así como los documentos de patente EP-A 0854151 y EP-A 95107280). 30 A partir del producto de masa molecular superior y a partir del producto de masa molecular inferior se puede preparar respectivamente una preparación farmacéutica, obteniéndose a partir de la porción de bajo peso molecular de los polímeros un sustituto sanguíneo parenteral y a partir de la porción de alto peso molecular de los polímeros un aditivo sanguíneo parenteral. 35 El ajuste del valor de pH antes (y después) de las etapas de reacción individuales se lleva a cabo preferiblemente con ácido láctico o sosa cáustica hasta valores entre 6 y 10, dependiendo de la etapa de reacción, por ejemplo 6,5-7,5 antes de la etapa ii), a continuación a 7,5-8,5 y después de nuevo a 6,5-7,5 antes de la etapa iii), después a 7,5 a 9 así como antes de la etapa v) a 7,5-10. 40 La concentración de hemoglobina asciende preferiblemente a 200-380 g/l, en especial 240-360 g/l, la solución contiene adicionalmente 10 a 150 mmol/l de NaHCO3 así como 10 a 150 mmol/l de NaCl. La temperatura durante la “reacción de un recipiente” asciende a 2-42ºC, en especial a 3-25ºC, preferiblemente a 4-22ºC. 45 El portador de oxígeno artificial preparado según la invención presenta preferiblemente un valor n50 (cooperatividad) de 1,6 a 2,5 y un valor de p50 (presión de semisaturación) de 2,1 a 3,2 kPa. 50 El producto obtenido según la invención con las características mencionadas se puede usar para la preparación de un agente para la aplicación intravascular o biomédica como portador de oxígeno artificial o en forma de una preparación farmacéutica como reemplazo sanguíneo (sustituto sanguíneo) o como un añadido a la sangre para aumentar la capacidad de transporte de oxígeno (aditivo sanguíneo) o a una solución alimenticia en el organismo humano o animal, en órganos individuales o en aplicaciones biotecnológicas, en especial para el tratamiento de una falta de oxígeno crónica en el ser humano. 55 Para la preparación de los productos que se van a administrar, los derivados de hemoglobina según la invención se disuelven en medios apropiados, como soluciones para infusión, por ejemplo en solución acuosa salina o de glucosa, preferiblemente a concentraciones isotónicas con el plasma sanguíneo. 60 65 El procedimiento según la invención se basa por lo tanto en etapas de reacción individuales coordinadas entre sí, cuyo significado y repercusión se explican a continuación. Como material de partida sirve hemoglobina altamente pura. Esta se puede obtener según procedimientos conocidos a partir de sangre fresca de animales de matadero o por ejemplo a partir de sangre conservada caducada. Se describen procedimientos para la obtención de hemoglobina purificada en: Antonini E. y col. (eds.): Hämoglobins (Colowick S.P., Kaplan N.O. (eds.): Methods in Enzymology, Volume 76), Academic Press, Nueva York, entre otros 1981. 8 ES 2 275 712 T3 5 Como se ha mencionado, según la invención la hemoglobina está desoxigenada (es decir, libre de su ligando fisiológico) durante la reticulación con glutardialdehído, la cual es conocida en sí misma, véanse los documentos DE 2499885, US 4857636, US-A 4001200, US-A 4001401, DE 449885, US 5439882, EP-A 0201618, ya que sólo los polímeros preparados a partir de hemoglobina desoxigenada durante la reticulación poseen propiedades de unión de oxígeno que posibilitan un empleo como portador de oxígeno artificial en las indicaciones deseadas. Preferiblemente, para una segunda protección contra la oxidación de la hemoglobina por trazas de oxígeno restante, éste se puede eliminar mediante reacción química con iones ascorbato. 10 Como efector de la unión de oxígeno se une en especial piridoxal-5’-fosfato, en una cantidad optimizada según las propiedades del producto final, de forma covalente a la hemoglobina porcina o humana. Esta unión de piridoxal5’-fosfato a hemoglobina es en principio conocida, por ejemplo, el documento de patente EP-P0528841 describe un procedimiento para la preparación de hemoglobina piridoxilada. La piridoxilación conduce a los valores de presión de semisaturación deseados, cuando se procede como se describe según la invención. 15 20 Los lugares de acoplamiento (aldiminas = bases de Schiff) del acoplamiento covalente no estable de piridoxal5’-fosfato se pueden estabilizar de forma conocida (v.a.) mediante reducción con borohidruro de sodio (se producen aminas), manteniéndose según la invención las condiciones especiales mencionadas. Para proteger la capacidad de las moléculas de hemoglobina de una cooperatividad homotrópica de los sitios de unión de oxígeno entre sí, que en la mayoría de los casos se pierde claramente con la reticulación de la hemoglobina con el reticulante glutardialdehído, según la invención se añade antes de la reticulación 2,3-difosfoglicerato, un efector químico (heterotrópico) no reactivo de la unión de oxígeno de la hemoglobina. Este puede estar almacenado con ello durante la reticulación de forma reversible en su sitio de unión en la molécula de hemoglobina. Tras la síntesis, se eliminan completamente 2,3-difosfoglicerato junto con los reactantes no consumidos así como productos de reacción sobrantes (véase más adelante). 25 Como reticulante bifuncional se emplea glutardialdehído en las condiciones según la invención especificadas anteriormente. 30 Los sitios de acoplamiento (aldiminas = bases de Schiff) de los puentes de glutardialdehído moleculares de reticulación se estabilizan como se ha descrito mediante la reacción con borohidruro de sodio (se producen aminas), debiéndose mantener las condiciones según la invención. Mediante la reticulación se producen hemoglobinas reticuladas con una distribución de los pesos moleculares entre aproximadamente 50000 y 5000000 g/mol (y mayores, por ejemplo 10-15000000 g/mol). 35 40 45 Para mejorar la compatibilidad con las proteínas del plasma, se acopla a la hemoglobina reticulada un derivado(MVV) de poli(óxido de etileno), en especial el recientemente mencionado (metoxi)polietilenglicol monofuncionalmente activado con un peso molecular de 1500-2500 g/mol. El acoplamiento de polietilenglicol (PEG), la llamada pegelación así como también la reticulación de hemoglobina son en sí conocidas (véase también E. Tsucheda (ed.): Blood Substituts: Present and Future Perspectives, Elsevier Science, Ámsterdam 1998). No obstante son nuevas tanto la pegelación como también la reticulación de hemoglobina conjuntamente, así como la aplicación del efector químicamente ineficaz antes de la reticulación, lo que contribuye en especial al mantenimiento de la cooperatividad, como también en especial las condiciones de reticulación detalladas. Mediante la pegelación que se propone en este documento, se impide ahora la en cualquier caso débil reacción del SER y también la degradación enzimática mediante proteasas. El ajuste del valor de pH se lleva a cabo como se ha detallado anteriormente. 50 Mediante el desarrollo y las condiciones de reacción conseguidos para ello se puede por una parte impedir la aparición de una distribución de percolación (mediante la dilución según la invención), por otra parte se pueden evitar las alteraciones indeseables de la afinidad por el oxígeno y la cooperatividad condicionadas por la reticulación y las uniones covalentes a la hemoglobina por ejemplo de glutardialdehído, piridoxalfosfato y poli(óxido de etileno), y en especial también se puede conseguir una alta compatibilidad plasmática. 55 Todas las etapas de reacción contribuyen a estas propiedades especiales del producto preparado según la invención. 60 65 El procesamiento posterior se encentra en el marco del conocimiento del experto en la materia: los componentes insolubles se pueden separar por centrifugación (por ejemplo durante 20 minutos con una aceleración centrifuga relativa de 20000 g). Las hemoglobinas reticuladas se separan mediante una etapa de procedimiento (conocida) preparativa, por ejemplo mediante una cromatografía de exclusión volumétrica o una ultrafiltración, una precipitación fraccionada o un fraccionamiento de campo-flujo, en una porción de bajo peso molecular y otra de alto peso molecular. Eligiendo procedimientos adecuados (son especialmente importantes el límite de separación nominal de peso molecular de la membrana de ultrafiltración o la zona de separación de peso molecular del gel empleado), se eliminan a este respecto al mismo tiempo todos los reactantes no consumidos así como los productos de reacción no deseados. 9 ES 2 275 712 T3 Una configuración especialmente preferida de la invención se aclara con más detalle por medio del siguiente ejemplo de preparación: 5 Se disuelve hemoglobina porcina o humana purificada con una concentración entre 200 y 380 g/l, preferiblemente entre 240 y 360 g/l en una solución acuosa electrolítica. Esta contiene hidrogenocarbonato de sodio con una concentración entre 10 y 150 mmol/l, preferiblemente entre 40 y 60 mmol/l, así como cloruro de sodio con una concentración entre 10 y 150 mmol/l, preferiblemente entre 50 y 100 mmol/l. La temperatura asciende a 2 a 42ºC, preferiblemente entre 3 y 25ºC. 10 Esta solución de hemoglobina se agita, se lleva a cabo una desoxigenación de la hemoglobina mediante flujo de nitrógeno puro. 15 A esta solución se añaden de 2 a 8, preferiblemente de 3 a 4 mol de ascorbato de sodio (como solución 1 molar en agua) por mol de hemoglobina y se deja reaccionar entre 0,5 y 6 horas, preferiblemente entre 70 y 120 minutos. El valor de pH de la solución se titula ahora con ácido láctico o sosa cáustica (de una concentración entre 0,1 y 1, preferiblemente entre 0,4 y 0,6 mol/l) hasta un valor entre 6,5 y 7,5, preferiblemente entre 6,9 y 7,3. 20 En este momento se añaden 0,5 a 3,0, preferiblemente de 1,0 a 2,5 moles de piridoxal-5’-fosfato por mol de hemoglobina y se dejan reaccionar entre 0,5 y 20, preferiblemente entre 1 y 7 horas. El valor de pH se ajusta con sosa cáustica o ácido láctico (de una concentración entre 0,1 y 1, preferiblemente entre 0,4 y 0,6 mol/l) a un valor entre 7,5 y 8,5, preferiblemente entre 7,7 y 8,2. 25 30 35 Ahora se añaden de 1,0 a 9,0, preferiblemente aproximadamente de 1,0 a 2,5 moles de borohidruro de sodio (como solución 1 molar en sosa cáustica 0,01 molar) y se dejan reaccionar entre 30 y 90, preferiblemente entre 50 y 70 minutos. El valor de pH de la solución se titula con ácido láctico o sosa cáustica (de una concentración entre 0,1 y 1, preferiblemente entre 0,4 y 0,6 mol/l) a un valor entre 6,5 y 7,5, preferiblemente entre 6,9 y 7,5. En este momento se añaden de 0,5 a 6,0, preferiblemente de 1,0 a 4,0 moles de 2,3-difosofoglicerato por mol de hemoglobina y se dejan reaccionar entre 5 y 50, preferiblemente entre 10 y 20 minutos. A continuación se lleva a cabo la adición controlada cronometrada del reticulante bifuncional, se añaden entre 6 y 10, preferiblemente entre 7 y 9 moles de glutardialdehído por mol de hemoglobina, disuelto en 1-4, preferiblemente en 1,5 a 2 litros de agua por litro de solución de hemoglobina, durante 3 a 10, preferiblemente durante 4 a 6 minutos y se dejan reaccionar entre 1 y 6, preferiblemente entre 2 y 3 horas. El valor de pH se ajusta con sosa cáustica o ácido láctico (de una concentración entre 0,1 y 1, preferiblemente entre 0,4 y 0,6 mol/l) a un valor entre 7,5 y 9,0, preferiblemente entre 7,6 y 8,8. 40 Se añaden de 5 a 20, preferiblemente de 6 a 12 moles de borohidruro de sodio (como solución 1 molar en sosa cáustica 0,01 molar) por mol de hemoglobina y se dejan reaccionar entre 15 y 100, preferiblemente entre 30 y 80 minutos. 45 Entonces se lleva a cabo una adición de 0 a 4, preferiblemente entre 0,5 y 3 litros de agua por litro de la solución de hemoglobina origina. El valor de pH se ajusta, en caso de que fuese necesario, con sosa cáustica o ácido láctico (de una concentración entre 0,1 y 1, preferiblemente entre 0,4 y 0,6 mol/l) a un valor entre 7,5 y 10, preferiblemente entre 8 y 9. 50 En este momento se añaden por mol de hemoglobina monomérica entre 2 y 12, preferiblemente entre 3 y 8 moles de un derivado de poli(óxido de alquileno) activado, preferiblemente succinimidil-propionato de metoxi-polietilenglicol, con un peso molecular entre 500 y 3000, preferiblemente 1000 y 2500 g/mol, en especial 2000 g/mol. 55 A continuación se sustituye con agitación constante de la solución de hemoglobina la atmósfera de nitrógeno durante 1 a 3 horas por oxígeno puro y se oxigena completamente la hemoglobina. El procesamiento se lleva a cabo como se ha detallado anteriormente. Las ventajas del procedimiento según la invención se pueden resumir como sigue: 60 65 Mediante el desarrollo de la reacción según la invención, en especial mediante el aumento de volumen de reacción en la etapa iv) del procedimiento, se obtiene un producto que se puede utilizar íntegramente para la preparación de portadores de oxígeno artificiales y concretamente, aproximadamente por igual respectivamente como aditivo sanguíneo (la fracción con la hemoglobina reticulada de mayor grado de polimerización: fracción I) y como sustituto de volumen sanguíneo (fracción II, con las porciones de bajo peso molecular). La separación se puede llevar a cabo fácilmente con procedimientos conocidos, algunos procedimientos posibles se especifican por ejemplo en los documentos de patente EP-A95107280 y EP-A 97100790. Los polímeros de la fracción I, preferiblemente hasta un peso molecular mayor de 700000 g/mol son tan suficientemente uniformes molecularmente, que en la concentración plasmática terapéutica 10 ES 2 275 712 T3 5 10 15 deseable poseen una presión osmótica coloidal suficientemente baja. Gracias a esta uniformidad molecular se alcaza simultáneamente una coeficiente virial bajo, así como una escasa viscosidad. La compatibilidad con las proteínas del plasma sanguíneo, una compatibilidad inmune y tiempo de permanencia intravasal suficientes así como unos efectos secundarios vasoconstrictores suficientemente escasos, es decir, una escasa extravasación de los polímeros de la fracción molecular I se consigue mediante un acoplamiento covalente de poli(óxidos de alquileno). Adicionalmente, el requisito de simplicidad y rentabilidad se tiene en cuenta de forma decisiva en este nuevo procedimiento ya que toda la preparación tiene lugar en un único recipiente (la llamada preparación en un recipiente) y se consiguen altos rendimientos de más del 70%, ascendiendo los rendimientos de polímeros con un peso molecular mayor de 700000 g/mol a más del 15%. El procedimiento de preparación posibilita la preparación de hemoglobinas modificadas y reticuladas en pocas etapas de procedimiento. Los parámetros de procedimiento elegidos conducen a este respecto a una distribución definida de los polímeros de hemoglobina modificados, que son adecuados como portadores de oxígeno artificiales y tienen en cuenta las circunstancias fisiológicas en el suero sanguíneo. Además, la cooperatividad de la hemoglobina no reticulada se mantiene considerablemente en el producto reticulado y la presión de semisaturación se puede ajustar de forma adecuada. Los portadores de oxígeno artificiales preparados según la invención de hemoglobina reticulada son compatibles con el plasma en administración parenteral y se pueden aplicar clínicamente como se ha detallado. 20 La invención se explicará más detalladamente por medio de los siguientes ejemplos. A este respecto, las figuras 1-3 muestras lo siguiente: 25 Figura 1: una distribución ponderada en masa de los tamaños moleculares y de los pesos moleculares (M) del polímero de hemoglobina porcina del ejemplo 1, representada como cromatograma de exclusión volumétrica (obtenido con gel Sephacryl S-400 HR, Pharmacia, Friburgo, Alemania). E425nm es la extinción en el eluido de cromatografía a 425 nm. Se incluyen los valores de abscisas de 700000 y 5000000 g/mol. Figura 2: cromatograma para el ejemplo de aplicación 2, para las aclaraciones véase la figura 1. 30 Figura 2: cromatograma para el ejemplo de aplicación 3, para las aclaraciones véase la figura 1. Además se aplicaron los siguientes procedimientos de determinación: 35 1. Contenidos en hemoglobina: se midieron fotométricamente con el procedimiento de cianohemiglobina modificado según Drabkin (“Hämoglobin-Farbtest MRP 3”, Boehrimger Manheim, Alemania). 2. Valores de pH: se midieron potenciométricamente (electrodo de vidrio de pH) con un analizador de gases sanguíneos (“ABL 5”, Radiómetro, Willich, Alemania). 40 45 3. Se llevaron a cabo determinaciones de la distribución de pesos moleculares de las hemoglobinas reticuladas mediante cromatografía de exclusión volumétrica (según: Pötzschke H. y col. (1996): “Vernetzte globuläre Proteine eine neue Klasse halbsynthetischer polymerer Moleküle: Characterisierung ihrer Struktur in Lösung am Beispiel hyperpolymeren Hämoglobins und Myoglobins mittels Volumenausschluss-Chromatografie, Viskometrie, Osmometrie und Lichtstreuung”, Macromolecular Chemistry and Physics 197, 1419 - 1437, así como Pötzschke H. y col. (1996): “Ein neuartiges Verfahren zur bestimmung Molarer Massen breit verteilter Polymerer mit Hilfe der Gel-Chromatographie und der Viskometrie am Beispiel Hämoglobin-Hyperpolymerer”, Macromolecular Chemistry and Physics 197, 3229 - 3250) en el gel “Sephacryl S-400HR” (Pharmacia Bioitech, Friburgo, Alemania). 50 4. Se llevaron a cabo determinaciones de las características de unión a oxígeno de las hemoglobinas por medio de un procedimiento y aparato propio (como se describe en: Barnikol W.K.R. y col. (1978); “Eine verbesserte Modifikation der Mikromethode nach Niesel und Thews zur Messung von O2 -Hb-Bindungskurven in Vollblut und konzentrierten Hb-Lösungen”, Respiration 36, 86 - 95. 55 5. La investigación de la compatibilidad plasmática de hemoglobinas reticuladas se llevó a cabo por medio de una prueba de precipitación estandarizada in vitro. (Domack U. (1997), “Entwicklung und in vivo Evaluation eines künstliches Sauerstoffsträgers auf Basis von Rinderhämoglobin”, Tesis doctoral, Departamento de Química, Universidad Johannes Gutenberg, Maguncia, 1997): se mezclaron soluciones de hemoglobina (contenidos en hemoglobina aproximadamente 30 g/l, en una solución acuosa electrolítica (StLg) de la composición NaCl 125 mM, KCl 4,5 mM y NaN3 3 mM) con las mismas cantidades de plasma humano esterilizado por filtración recién obtenido y a continuación se añadieron respectivamente a 500 µl de la mezcla hasta 20 µl de ácido láctico 0,5 molar y se mezcló, de forma que para cada derivado de hemoglobina que se iba a investigar se dieron respectivamente valores de pH de un intervalo entre aproximadamente 7,4 hasta 6,8. Tras una incubación de 30 minutos a temperatura ambiente y centrifugación de las muestras, se llevó a cabo la determinación del contenido en hemoglobina como medida de la hemoglobina no precipitada, así como el pH correspondiente en el sobrenadante, así como el control óptico subjetivo de precipitaciones no coloreadas de proteínas plasmáticas. 60 65 11 ES 2 275 712 T3 Ejemplo de realización 1 Preparación de una hemoglobina porcina según la invención reticulada y molecularmente modificada a 4ºC según el procedimiento general de preparación 5 10 15 20 25 Hemoglobina porcina altamente pura, en una concentración de 330 g/l disuelta en una solución electrolítica acuosa de la composición NaHCO3 50 mM y NaCl 100 mM se desoxigenó a 4ºC con agitación de la solución bajo nitrógeno puro continuamente renovado sobre la solución. A continuación se añadieron 4 moles de ascorbato de sodio (como solución 1 molar en agua) por mol de hemoglobina (monomérica) y se dejó reaccionar 6 horas. La solución se tituló con ácido láctico 0,5 molar hasta un valor de pH de 7,1, se añadieron 1,1 moles de piridoxal-5’-fosfato por mol de hemoglobina y se dejó reaccionar durante 16 horas. En este momento se ajustó un valor de pH de 7,8 con sosa cáustica 0,5 molar, se añadieron 1,1 moles de borohidruro de sodio (como solución 1 molar en sosa cáustica 0,01 molar) y se dejó reaccionar durante una hora. Ahora se ajustó un valor de pH de 7,3 con ácido láctico 0,5 molar, a continuación se añadieron 1,1 moles de 2,3-difosfoglicerato por mol de hemoglobina y tras 15 minutos de reacción, 8 moles de glutardialdehído por mol de hemoglobina, disueltos en 1,8 litros de agua pura por litro de solución de hemoglobina para la reticulación de la hemoglobina durante 5 minutos y se dejó reaccionar 2,5 horas. Tras la titulación con sosa cáustica 0,5 molar hasta un valor de pH de 7,8 siguió una adición de 15 moles de borohidruro de sodio (como solución 1 molar en sosa cáustica 0,01 molar) por mol de hemoglobina durante 1 hora. Siguió una adición de 2 litros de agua por litro de solución de hemoglobina original. El valor de pH ascendió entonces a 9,3, y siguió directamente una adición de 4 moles de succinimidil-propionato de metoxi-polietilenglicol de 2000 g/mol de peso molecular durante 2 horas. La atmósfera de nitrógeno sobre la solución se sustituyó por una atmósfera de oxígeno puro. Después de 1 hora se separaron componentes insolubles mediante centrifugación (20000 g durante 15 minutos). A continuación se llevó a cabo una cambio de la solución electrolítica mediante una cromatografía de exclusión volumétrica (gel Sephadex G-25, Pharmacia, Alemania) a una solución electrolítica acuosa de la composición NaCl 125 mM, KCl 4,5 mM y NaCOH3 20 mM. El rendimiento ascendió a 77%; el rendimiento para peso molecular mayor de 700000 g/mol es de 28%. 30 35 La figura 1 muestra una representación de la distribución de las masas moleculares de los polímeros de hemoglobina obtenidos en forma de un cromatograma de exclusión volumétrica. Las mediciones de las características de unión a oxígeno en condiciones fisiológicas (una temperatura de 37ºC, una presión parcial de dióxido de carbono de 5,3 kPa y un valor de pH de 7,4) dieron para el producto un valor de p50 de 2,9 kPa y un valor de n50 de 1,95. En la “prueba de precipitación”, la hemoglobina porcina reticulada no mostró en el intervalo de pH de 7,4 a 6,8 ninguna interacción con el plasma humano, en especial ninguna precipitación perceptible, ni de la hemoglobina ni de las proteínas plasmáticas. 40 Ejemplo de realización 2 Preparación de una hemoglobina porcina según la invención reticulada y molecularmente modificada a temperatura ambiente según el procedimiento general de preparación 45 50 55 60 65 Hemoglobina porcina altamente pura, en una concentración de 330 g/l disuelta en una solución electrolítica acuosa de la composición NaHCO3 50 mM y NaCl 100 mM se desoxigenó a 22ºC con agitación de la solución bajo nitrógeno puro continuamente renovado sobre la solución. A continuación se añadieron 4 moles de ascorbato de sodio (como solución 1 molar en agua) por mol de hemoglobina (monomérica) y se dejó reaccionar 90 minutos. La solución se tituló con ácido láctico 0,5 molar hasta un valor de pH de 7,1, se añadió 1,1 moles de piridoxal-5’-fosfato por mol de hemoglobina y se dejó reaccionar durante 2 horas. En este momento se ajustó un valor de pH de 7,8 con sosa cáustica 0,5 molar, se añadieron1,5 moles de borohidruro de sodio (como solución 1 molar en sosa cáustica 0,01 molar) y se dejó reaccionar durante una hora. Ahora se ajustó un valor de pH de 7,3 con ácido láctico 0,5 molar, a continuación se añadieron 1,1 moles de 2,3-difosfoglicerato por mol de hemoglobina y tras 15 minutos de reacción, 9 moles de glutardialdehído por mol de hemoglobina, disueltos en 1,8 litros de agua pura por litro de solución de hemoglobina para la reticulación de la hemoglobina durante 5 minutos y se dejó reaccionar 1 hora. Tras la titulación con sosa cáustica 0,5 molar hasta un valor de pH de 7,8 siguió una adición de 10 moles de borohidruro de sodio (como solución 1 molar en sosa cáustica 0,01 molar) por mol de hemoglobina durante 0,5 horas. El valor de pH ascendió entonces a 8,7, y siguió directamente una adición de 8 moles de succinimidil-propionato de metoxi-polietilenglicol de 1000 g/mol de peso molecular durante 1 hora. La atmósfera de nitrógeno sobre la solución se sustituyó por una atmósfera de oxígeno puro. Después de 1 hora se separaron componentes insolubles mediante centrifugación (10 minutos a 20000 g). A continuación se llevó a cabo una cambio de la solución electrolítica mediante una cromatografía de exclusión volumétrica (gel Sephadex G-25, Pharmacia, Alemania) a una solución electrolítica acuosa de la composición NaCl 125 mM, KCl 4,5 mM y NaCOH3 20 mM. El rendimiento ascendió a 79%; el rendimiento para peso molecular mayor de 700000 g/mol ascendió a 28%. 12 ES 2 275 712 T3 La figura 2 muestra una representación de la distribución de las masas moleculares de los polímeros de hemoglobina obtenidos en forma de un cromatograma de exclusión volumétrica. 5 10 Las mediciones de las características de unión a oxígeno en condiciones fisiológicas (una temperatura de 37ºC, una presión parcial de dióxido de carbono de 5,3 kPa y un valor de pH de 7,4) dieron para el producto un valor de p50 de 2,9 kPa y un valor de n50 de 1,96. En la “prueba de precipitación”, la hemoglobina porcina reticulada no mostró en el intervalo de pH de 7,4 a 6,8 ninguna interacción con el plasma humano, en especial ninguna precipitación perceptible, ni de la hemoglobina ni de las proteínas plasmáticas. Ejemplo de realización 3 15 20 25 30 35 Preparación de una hemoglobina humana según la invención reticulada y molecularmente modificada (a 4ºC) según el procedimiento general de preparación Hemoglobina humana altamente pura, en una concentración de 330 g/l disuelta en una solución electrolítica acuosa de la composición NaHCO3 50 mM y NaCl 100 mM se desoxigenó a 4ºC con agitación de la solución bajo nitrógeno puro continuamente renovado sobre la solución. A continuación se añadieron 4 moles de ascorbato de sodio (como solución 1 molar en agua) por mol de hemoglobina (monomérica) y se dejó reaccionar 3 horas. La solución se tituló con ácido láctico 0,5 molar hasta un valor de pH de 7,1, se añadió 1,1 moles de piridoxal-5’-fosfato por mol de hemoglobina y se dejó reaccionar durante 16 horas. En este momento se ajustó un valor de pH de 7,8 con sosa cáustica 0,5 molar, se añadieron 1,5 moles de borohidruro de sodio (como solución 1 molar en sosa cáustica 0,01 molar) y se dejó reaccionar durante una hora. Ahora se ajustó un valor de pH de 7,3 con ácido láctico 0,5 molar, a continuación se añadieron 1,5 moles de 2,3-difosfoglicerato por mol de hemoglobina y tras 15 minutos de reacción, 9 moles de glutardialdehído por mol de hemoglobina, disueltos en 1,8 litros de agua pura por litro de solución de hemoglobina para la reticulación de la hemoglobina durante 5 minutos y se dejó reaccionar 2,5 horas. Tras la titulación con sosa cáustica 0,5 molar hasta un valor de pH de 8,0 siguió una adición de 10 moles de borohidruro de sodio (como solución 1 molar en sosa cáustica 0,01 molar) por mol de hemoglobina durante 1 hora. Siguió una adición de 2 litros de agua por litro de solución de hemoglobina original. El valor de pH ascendió entonces a 8,6, y siguió directamente una adición de 4 moles de succinimidil-propionato de metoxi-polietilenglicol de 2000 g/mol de peso molecular durante 2 horas. La atmósfera de nitrógeno sobre la solución se sustituyó por una atmósfera de oxígeno puro. Después de 1 hora se separaron componentes insolubles mediante centrifugación (10 minutos a 20000 g). A continuación se llevó a cabo una cambio de la solución electrolítica mediante una cromatografía de exclusión volumétrica (gel Sephadex G-25, Pharmacia, Alemania) a una solución electrolítica acuosa de la composición NaCl 125 mM, KCl 4,5 mM y NaCOH3 20 mM. 40 La figura 3 muestra una representación de la distribución de las masas moleculares de los polímeros de hemoglobina obtenidos en forma de un cromatograma de exclusión volumétrica. El rendimiento total ascendió a 75%; el rendimiento para peso molecular mayor de 700000 g/mol ascendió a 17%. 45 Las mediciones de las características de unión a oxígeno en condiciones fisiológicas (una temperatura de 37ºC, una presión parcial de dióxido de carbono de 5,3 kPa y un valor de pH de 7,4) dieron para el producto un valor de p50 (como medida de una afinidad media por el oxígeno) de 2,8 kPa y un valor de n50 (una cooperatividad media aparente de los sitios de unión de oxígeno) de 1,74. En la “prueba de precipitación”, la hemoglobina porcina reticulada no mostró en el intervalo de pH fisiológica y fisiopatológicamente interesante de 7,4 a 6,8 ninguna interacción con el plasma humano, en especial ninguna precipitación perceptible, ni de la hemoglobina ni de las proteínas plasmáticas. 50 55 60 65 13 ES 2 275 712 T3 REIVINDICACIONES 5 1. Procedimiento para la preparación de portadores de oxígeno artificiales de hemoglobina reticulada con propiedades funcionales mejoradas, caracterizado porque la hemoglobina i) en primer lugar se desoxigena ii) a continuación se hace reaccionar covalentemente con un efector de la unión de oxígeno químicamente reactivo; 10 15 iii) después la solución se mezcla con un efector no reactivo químicamente; y después iv) la hemoglobina se reticula entre sí covalentemente de forma estable con glutardialdehído, bajo muy intensa dilución de la mezcla de reacción con adición simultánea del reticulante, a continuación la solución se diluye de nuevo con agua, incrementándose el volumen total de la mezcla de reacción en un factor de 2 a 10 y después de ello, v) se acopla covalentemente un poli(óxido de etileno), vi) el producto obtenido se procesa de forma conocida. 20 2. Procedimiento según la reivindicación 1, caracterizado porque la hemoglobina es de origen porcino o humano. 3. Procedimiento según la reivindicación 2, caracterizado porque como material de partida sirve hemoglobina porcina. 25 30 35 40 45 4. Procedimiento según una de las reivindicaciones 1 a 3, caracterizado porque en la etapa iv) se añade glutardialdehído en una solución muy intensamente diluida cronometradamente y de esa forma el volumen de la mezcla de reacción y la concentración de hemoglobina durante la reacción de polimerización varían simultáneamente de forma inversa y a continuación se diluye la solución. 5. Procedimiento según la reivindicación 4, caracterizado porque en la etapa iv) se añade glutardialdehído en una cantidad de 6 a 10 moles, en relación con la hemoglobina monomérica, disuelto en 1 a 2 litros de agua por litro de solución de reacción original durante 3 a 15 minutos y reacciona 1 a 6 horas adicionales. 6. Procedimiento según una de las reivindicaciones 1 a 5, caracterizado porque a la solución que contiene hemoglobina antes de la reacción según la etapa ii) se le añaden 2 a 8 moles de ascorbato de sodio por mol de hemoglobina no reticulada durante 0,5 a 6 horas. 7. Procedimiento según una de las reivindicaciones 1 a 6, caracterizado porque en la etapa ii) se une covalentemente como efector piridoxal-5’-fosfato en una proporción molar, en relación con la hemoglobina monomérica de 0,5 a 3, preferiblemente de 1 a 2,5 mol/mol durante 0,5 a 20 horas. 8. Procedimiento según la reivindicación 7, caracterizado porque en la etapa ii), así como en la etapa iv) tras la unión covalente de piridoxal-5’-fosfato a la hemoglobina así como tras el acoplamiento covalente de la hemoglobina con glutardialdehído se añade respectivamente borohidruro de sodio reductor. 9. Procedimiento según una de las reivindicaciones 1 a 8, caracterizado porque en la etapa iii) se añade 2,3difosfoglicerato en una cantidad relativa de 0,5 a 6 moles en relación con la hemoglobina monomérica, y se comienza de 5 a 50 minutos después la etapa iv). 50 55 60 10. Procedimiento según una de las reivindicaciones 1 a 9, caracterizado porque en la etapa v) se acopla un éster de polietilenglicol con un peso molecular de 500 a 3000 g/mol. 11. Procedimiento según una de las reivindicaciones 1 a 10, caracterizado porque el producto obtenido se separa mediante un procedimiento de separación en una fracción de mayor peso molecular medio y un fracción de menor peso molecular medio. 12. Procedimiento según la reivindicación 11, caracterizado porque a partir de la porción de bajo peso molecular de los polímeros se prepara un sustituto sanguíneo parenteral y a partir de la porción de mayor peso molecular de los polímeros se prepara un aditivo sanguíneo parenteral. 13. Portador de oxígeno artificial, caracterizado porque se trata de una hemoglobina conjugada covalentemente con un efector de la unión a oxígeno así como polimerizada con glutardialdehído y acoplada químicamente con un derivado de poli(óxido de alquileno). 65 14. Portador de oxígeno artificial según la reivindicación 13, caracterizado porque el portador presenta un valor de n50 de 1,6 a 2,5 y un valor de p50 de 2,1 a 3,2 kPa. 14 ES 2 275 712 T3 15. Uso de hemoglobina reticulada según la reivindicación 13 ó 14 para la preparación de un agente para la aplicación por vía intravascular o biomédica como portador de oxígeno artificial en el organismo humano o animal para el tratamiento de estados de falta de oxígeno. 5 16. Uso según la reivindicación 15 para el tratamiento de una falta de oxígeno crónica en el ser humano. 17. Uso según la reivindicación 16, caracterizado porque el agente se usa en forma de una preparación farmacéutica como un reemplazo de la sangre (sustituto sanguíneo) o como un añadido a la sangre para aumentar la capacidad de transporte de oxígeno (aditivo sanguíneo) o en órganos individuales. 10 18. Uso ex vivo de hemoglobina reticulada según la reivindicación 13 ó 14 como añadido a una solución de alimentación o en aplicaciones biotecnológicas. 15 20 25 30 35 40 45 50 55 60 65 15 ES 2 275 712 T3 16 ES 2 275 712 T3 17 ES 2 275 712 T3 18