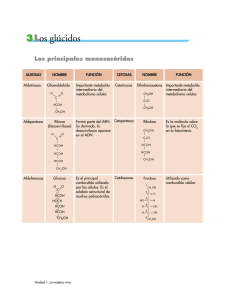
c A p i T u L o 2 CARBOHIDRATOS `
Anuncio

c A
p
u
i T
L
o
2
CARBOHIDRATOS '
siguientes capftulos de esta obra se estudiarin las unide la biosfera (azdcares simples, ~cidos gra~tidos) que se unen para formac los biopolfmeros
proteinas y ~idos nucleicos). En el presente
simples, los carbohidratos de reserva y los poel tema de la estereoqufmica y se presentaa los carbohidratos por medio de diferentes
las propiedades ffsicas y qufmicas de los
de algunos de los poli~dos de recarbohidratos complejos no 8610 tienen
tambi6n funcionan como dep6sitos
segt1n las necesidades del organisson la eelulosa, el principal comy los ~lltidoglicanos de la
reserva in"luyen al almid6n
iSWlnen segl1n las necesidades
'lnft'Ant,p•.::
ialdlehidos 0 polihidroxice;nplJlesbos al hidrolizarse.
'''''''"C.'' de los carhidr6geAdemas, el
37
38
Carbohidratos
2.1
CLASIFICACION DE LOS CARBOHIDRATOS
Los carbohidratos pueden clasificarse en tres grupos con base en el numero de un idades de azucar que contienen: monosacaridos, oligosacaridos y polisacaridos. Los
monosacaridos son azucares simples que no pueden hidrolizarse en unidades mas
pequenas en condiciones razonablemente moderadas. Los monosacaridos mas simples que se ajustan a la definicion y formula empfricas dadas anteriormente son gliceraldehfdo (una aldosa) y su isomero, la dihidroxicetona (una cetosa). Ambos
azucares son triosas debido a que poseen tres Momos de carbono. Ademas de los
grupos funcionales (aldehfdo y cetona) que se utilizan para describir estos dos azucares, notese que contienen hidroxilos alcoholicos y, en el casu del gliceraldehfdo,
un atomo de carbono asimetrico.
CHzOH-C- CH 20H
~
Gliceraldehido
Dihidroxiacetona
Los oligosacaridos son polfmeros hidrolizables de monosacaridos que contienen de
dos a seis moleculas de azucares simples. Los disacaridos, que tienen dos unidades
de monosacarido, son los mas abundantes; los trisacaridos existen tambien libres en
la naturaleza. Los oligosacaridos con mas de tres subunidades se encuentran por
10 general unidos como cadenas laterales a las glicoprotefnas.
Los polisacaridos son polfmeros, con frecuencia insolubles, que constan de cientos 0 miles de unidades de monosacaridos; su estructura puede ser lineal 0 rami ficada. Si el polfmero se compone de monosacaridos de una sola clase, el polisacarido
se denomina homopolisacarido. Si dos 0 mas monosacaridos distintos se encuentran
en el polfmero, se denomina heteropolisacarido. Algunos de los monosacaridos que
se unen entre sf mediante enlaces glicosfdicos para formar polisacaridos son la glucosa, la xilosa y la arabinosa.
2.2
ESTEREOISOMERISMO
El estudio de los carbohidratos requiere entender el isomerismo 0 isomerfa, especialmente el estereoisomerismo. El tema del isomerismo puede dividirse en isomerismo estructural y estereoisomerismo. Los isomeros estructurales tienen la rnisma
formula molecular pero difieren entre sf por tener diferentes estructuras; es decir,
difieren en el orden en el que sus atomos se unen. Los estereoisomeros tienen la
rnisma formula molecular' y la misma estructura, pero difieren en configuracion,
es decir, en la disposici6n de sus atomos en el espacio. Los is6meros estructurales,
a su vez, son de tres tipos. Uno es el de los isomeros de cadena, en los que los
isomeros presentan diferentes disposiciones de los atomos de carbono. Como ejemplo, el n-butano es un isomero de cadena del isobutano.
H H H H
I I I I
H-C-C-C-C-H
I I I I
H H H H
n·Butano
H
I
H-CI
H
H H
I
I
C-C-H
I
I
CH] H
Isobutano
Estereoisomerismo
39
Otros ejemplos de isomeros estructurales son los isomeros de posicion, doruro de
n-propilo y doruro de isopropilo, en los quc los dos compuestos implicados tienen
la misma cadena de carbono pero difieren en la posicion de un grupo sustituyente.
H
H
H
I I I
H-C-C- CI I I
H
H
H
CI
H-
H
H
H
Cloruro de n-propilo
H
I I I
C- C- CI I I
H
CI H
Cloruro de isopropilo
El tercer tipo de isomeros estructurales es el de los isomeros de grupo funcional,
en los que los compuestos tienen distintos grupos funcionales. Ejemplos son el npropanol y el eter metiletflico.
H]C-CH2- CH 20H
H]C- CH2-0-CH 3
n-Propanol
Eter metiletOico
El tema del estereoisomerismo puede dividirse en las areas mas pequefias de isomerismo optico e isomerismo geometrico (0 isomerismo cis-trans). Este ultimo tipo de isomerismo 10 ilustra el par cis-trans de los acidos fumarico y maleico.
H"
C/
COOH
/ C"
~
H/
H
Acido tumarico
'GOOH
Acido maleico
(cis)
(trans)
2.2.1
/ COOH
"C
II
HOOC
H
ISOMERISMO OPTICO
Este es el tipo de isomerismo que se encuentra comunrnente en los carbohidratos;
se observa por 10 general cuando una molecula contiene uno 0 mas atomos de carbono quirales (del griego cheir = mano) 0 asimetricos. El tema del estereoisomerismo se desarrollo ampliamente despues de que van t Hoff y LeBel introdujeron
el concepto del atomo de carbono tetraedrico. Esta estructura atomica tiene cuatro enlaces covalentes 0 ejes de enlace que van del nudeo de carbono central a las
esquinas de un tetraedro (estructura 2. 1).
Cuando cuatro grupos distintos esmn unidos a esos enlaces, se dice que el alomo
de carbono del centro de la molecula es un centro quiral (0 un atomo de carbono
quiral). Esto se indica en la estructura 2.2, en la que el compuesto C (ABDE),
I
H
H
ESTRUCTURA 2.1
40
Carbohidratos
ESTRUCTURA 2.2
que contiene un solo atomo de carbono quiral, se representa con los cuatro grupos
A, B, DyE unidos. Estos grupos pueden disponerse en el espacio de dos maneras
distintas, de modo que se forman dos compuestos distintos. Estos compuestos son
obviamente distintos; es decir, no pueden superponerse. Mas bien, cada compuesto
se relaciona con el otro como la mana derecha se relaciona con la mana izquierda. Se dice que dichas moleculas quirales poseen "sentido de las manos" y son por
10 tanto imagenes especulares; si una molecula se coloca ante un espejo, la imagen
en este corresponde a la otra molecula (estructura 2.3).
Estos is6meros especulares constituyen un par enantiomerico; se dice que un
miembro del par es el enanti6mero del otro.
En el caso de moleculas que poseen mas de un atomo de carbono quiral, existen
mas de dos estereois6meros. Cualquier par de compuestos que sean is6meros especulares, y en consecuencia constituyan un par enantiomerico, estaran relacionados
con los estereois6meros restantes como diastere6meros. Estos son estereois6meros, pero no is6meros especulares, de los compuestos restantes.
2.2.2
ACTIVIDAD OPTICA
Casi todas las propiedades de los dos miembros de un par enantiomerico son identicas:
tienen el mismo punto de ebullici6n, el mismo punto de fusi6n, la misma solubilidad en varios solventes. Asimismo, presentan actividad 6ptica; en esta propiedad,
difieren en forma importante. Un miembro del par enantiomerico hace rotar un plano
de luz polarizada en direcci6n de las manecillas del reloj y se dice por 10 tanto que
es dextrorrotatorio 0 dextr6giro. Su is6mero de imagen de espejo 0 enanti6mero
rotara el plano de luz polarizada al mismo grado, pero en direcci6n opuesta al mo-
Espejo
ESTRUCTURA 2.3
Estereoisomerismo
8
8
I
I
I
I
A-C-D
A-C-D
I
I
I
I
E
E
F6rmula
de perspectiva
F6rmula
de proyecci6n
Modelo de barras y esferas
41
ESTRUCTURA 2.4
vimiento de las manecillas del reloj. Se dice entonces que este is6mero es levorrotatorio . 0 lev6giro. Sin embargo, debe observarse que no todos los compuestos que
poseen un centro quiral son quirales ni muestran actividad 6ptica. Por otra parte,
una molecula puede poseer quiralidad, mostrar actividad 6ptica y carecer de un centro
quiral.
2.2.3
FORMULAS DE PROYECCION Y DE PERSPECTIVA
Al estudiar los carbohidratos, se encuentran muchos ejemplos de isomerismo 6ptico, por 10 que es necesario contar con una forma de representar los diferentes isomeros posibles. Una forma de representarlos es utilizar la formula de proyeccion
introducida en el siglo pasado por el ilustre qufmico organico aleman Emil Fischer.
La formula de proyeccion representa los cuatro grupos unidos al atomo de carbona
proyectados en un plano. Esta proyeccion puede representarse por la molecula asimetrica esquematizada anteriormente como se muestra en la estructura 2.4. En la
formula de proyeccion de Fischer, se considera que los enlaces horizontales estan
situados enfrente del plano del papel, mientras que los enlaces verticales esmn por
detras. Esta relaci6n se observa mas claramente en la formula de perspectiva. Aquf,
las lfneas discontinuas indican enlaces que se yxtienden por detras del plano de
la pagina, mientras que los segmentos triangulares representan enlaces que se proyectan por delante del plano de la pagina. Las formulas de proyeccion y de
perspectiva pueden utilizarse para distinguir entre el compuesto mostrado en la
estructura 2.4 y su isomero especular que enseguida se muestra. Estos dos pares
de formulas junto con una version simplificada del modelo de barras y esferas
constituyen tres formas distintas de escribir formulas para representar los pares enantiomericos.
I
D- C -A
I
E
Modelo simplificado
de barras y esferas
F6rmula de proyecci6n
8,
,
,,
D-¢-A
!
E
F6rmula de perspectiva
42
Carbohidratos
De manera imaginaria, la formula de perspectiva puede rotarse en todos los pIanos sin que se corra e1 riesgo de confundir los dos enantiomeros . Debe tenerse cuidado al utilizar las formulas de Fischer; aunque estas pueden rotarse hasta 180 0 en
e1 plano del papel, resulta una rotacion de solo 90 0 en el enantiomero debido a la
convencion de que los enlaces horizontales se representan como si estuvieran enfrente del plano del papel. La formula de Fischer no puede, con la imaginacion,
trasladarse fuera del plano del papel.
2.2.4
EL D-GLICERALDEHfDO COMO COMPUESTO DE REFERENCIA
Dado que existen un gran mlmero de isomeros opticos en los carbohidratos, es necesario contar con un compuesto de referencia. Como compuesto de referencia se
ha elegido el monosacarido mas simple que posee un atomo de carbona asimetrico;
este compuesto es la triosa glicerosa 0 gliceraldehido. Puesto que este compuesto
tiene un centro quiral, existe como dos estereoisomeros. Estos pueden representarse mediante sus formulas de proyeccion de Fischer, asf como por modelos simplificados de barras y esferas y formulas de perspectiva.
CHO
I
HO-C- H
I
CH 2 0H
CHO
I
H-C-O H
I
CH 2 0H
F6rmulas de Fischer
A~H
CHO
Mod,'o, d, b,,,,, y
'"":~OH
HO
~
CH 2 0H
~HO
:
F6rmulas de perspectiva
H - 9 -OH
:
CHPH
CH 20H
CHO
!
HO-?-H
,
CH 20H
Estos tres pares de estructuras se relacionan entre sf como isomeros especulares.
Aunque tienen los mismos punto de fusion, punto de ebullicion y solubilidad en
H20, difieren en la direccion en la que desvfan el plano de luz polarizada. El isomero que desvfa dicha luz en la direccion de las manecillas del reloj se identifica
con el simbolo (+) para indicar que es el enantiomero dextrorrotatorio. A principios de este siglo, a tal isomero se Ie asigno tambien la formula de Fischer en la
que el grupo hidroxilo aparece a la derecha cuando el grupo aldehido se encuentra
en la parte superior. Asimismo se convino que esta forma debfa designarse como
D( + )-gliceraldehfdo. Para entenderlo mejor, se dan la formula de proyeccion y las
representaciones de barras y esferas que a menudo se emplean.
~HO
O( + )-Gliceraldehfdo
CHO
I
H-C-O H
I
CH 2 0H
:
H - 9 -0H
:
CH 2 0H
Proyecci6n de Fischer Modelo de barras y esferas F6rmula de perspectiva
Estereoisomerismo
43
Esta asignacion de las estructuras anteriores al isomero del gliceraldehfdo que
desvfa la luz polarizada en direcci6n de las manecillas del Teloj tenfa s610 una probabilidad del 50% de seT correcta. Cincuenta arros despues, los estudios de difraccion de rayos X con el acido tartarico demostraron que la proyeccion de Fischer
era la correcta.
EI D( + )-gliceraldehfdo cumple una importante funcion como compuesto de referencia no solo para carbohidratos, sino tambien para hidroxi y aminoacidos encontrados en bioqufmica. La notaci6n D y L ha sido particularmente util para
relacionar grupos de carbohidratos (los D-azucares que existen naturalmente) y aminoacidos (los L-aminoacidos que tambien se encuentran de manera natural). Sin embargo, el sistema D y L no puede utilizarse para todos los compuestos que contienen
centros quirales, puesto que, en teorfa, esto requerirfa convertir el compuesto de
interes en D- 0 L-gliceraldehfdo 0 un compuesto que se sabe esta relacionado mediante estereoqufrnica a estos patrones de referencia. Por 10 tanto, se ha desarrollado un nuevo sistema denominado la "regIa de secuencia" de Cahn-Ingold-Prelog
para describir, de una manera absoluta, la configuracion de los centros quirales individuales. Descrito brevemente, dicho metodo se basa en orientar la molecula de
modo que el grupo de menor importancia unido al centro quiral quede proyectado hacia atras y luego observar que direccion sigue la vista, ya sea en el sentido
de las manecillas del reloj (R para recta) 0 en direccion opuesta (S para siniestra),
conforme se pasa esta en un orden de importancia asignado desde el numero atomico mas alto de los atomos sustituyentes al numero atomico mas bajo. De acuerdo
con dicha regIa, el D( + )-gliceraldehfdo se designarfa como (R)-gliceraldehfdo. Aunque la regIa de secuencia se emplea en muchas areas de la qufmica organica, no
es conveniente utilizarla con carbohidratos 0 aminoacidos para los que se conservan
los "sistemas locales" basados en el D( + )-gliceraldehfdo y la Ls-serina (veanse las
secciones 2.2.5 y 4.2).
2.2.5 SrNTESIS DE CIANOHIDRINA
Como ejemplo del uso del D-gliceraldehfdo como compuesto de referencia, considerese la formaci6n de azucares tetrosas a partir de una triosa mediante la sfntesis
de Kiliani-Fischer. Esta sfntesis es un proceso por el cualla longitud de la cadena de
una aldosa aumenta en un atomo de carbono, y se forman dos nuevas aldosas (figura 2.1). En esta sfntesis, la quiralidad del carbono asimetrico del D-gliceraldehfdo
no se altera, pero el carbono del aldehfdo se convierte en un nuevo centro quiral.
En consecuencia, se forman dos compuestos de cuatro carbonos con configuracion opuesta en ese centro. Estos nuevos compuestos son la D-eritrosa y la D-treosa;
el prefijo D denota especificamente su relacion con el D-gliceraldehfdo. Si la sfntesis
de cianohidrina se aplicara al L-gliceraldehfdo, se formarfan los compuestos L-eritrosa
y L-treosa.
Cuando la sfntesis de Kiliani-Fischer se aplica a las dos D-aldotetrosas mostradas en la figura 2.1, se forman cuatro aldopentosas. El alargarniento de estas cuatro
pentosas resulta en un total de ocho aldohexosas que incluyen la bien conocida
D-glucosa, la D-manosa y la D-galactosa.
En este punto, resulta instructivo considerar las relaciones estereoqufmicas entre
las ocho aldohexosas y el compuesto de referencia, D-gliceraldehfdo. Primero, las
ocho hexosas tienen la misma formula estructural, CH 20H- CHOH- CHOHCHOH- CHOH- CHO y, por 10 tanto, son estereoisomeros en vez de isomeros
estructurales. Segundo, con respecto a su estereoisomerismo, son isomeros opticos
44
Carbohidratos
CHO
H60H
I
CH 20H
o-Gliceraldehido
~
CHO
~
I
CHO
I
HCOH
HOCH
H60H
H60H
I
I
CH 20H
CH 20H
o-Eritrosa
~ CHO
/
CHO
H60H
I
I
HCOH
I
I
I
HCOH
I
I \
CH 20H
o-Alosa
H60H
I
CHpH
o-Arabinosa
CHO
I
HOCH
I
HCOH
I
HCOH
I
HCOH
I
CH 20H
o-Altrosa
I \
CHO
I
HCOH
I
HOCH
I
HCOH
I
HCOH
I
CH 20H
o-Glucosa
FIGURA 2_1
CHO
I
HOCH
I
HOCH
I
HCOH
I
HCOH
I
CH 20H
D-Manosa
I
I
HOCH
I
HCOH
I
HOCH
HOCH
CH 20H
o-Ribosa
I
HCOH
I
HCOH
I
HCOH
I
HCOH
I
I
I
HCOH
HCOH
CH 20H
~ CHO
/
CHO
Ho6H
HCOH
CHO
o-Treosa
CH 20H
o-Xilosa
I \
CHO
I
HCOH
I
HCOH
I
HOCH
I
HCOH
6H 2OH
o-Gulosa
o-Li xosa
CHO
I
HOCH
I
HCOH
I
HOCH
I
HCOH
I
CH 20H
o-Idosa
I \
CHO
I
HCOH
I
HOCH
I
HOCH
I
HCOH
I
CHpH
o-Galactosa
CHO
I
I
HOCH
I
HOCH
I
HOCH
HCOH
6H 2OH
o-Talosa
Estructura de las D-aldosas.
y no isomeros geometricos_ Tercero, estas D-aldohexosas esmn relacionadas estructuralmente con el D-gliceraldehfdo debido a que, en teorfa, es po sible producirlas
por aplicacion de la sfntesis de cianohidrina a dicha triosa. Esta relacion se muestra
tarnbien en las formulas de proyecci6n para las ocho hexosas en las que el grupo
hidroxilo (-OR) del atomo de carbono de referenda, el carbona quiral con el
numero mas alto, esm a la derecha, como en el D-gliceraldehfdo (los carbonos de
las aldosas se numeran a partir del carbona del aldehfdo) . Cuarto, estas aldohexosas
se relacionan como diastereois6meros; no pueden ser enanti6meros debido a que
sus is6meros especulares, por ejemplo, la L-glucosa, el isomero especular de la
D-glucosa, no se han encontrado . Quinto, existen cuatro pares de epimeros (diastere6meros que difieren en cuanto a configuracion en un solo atomo de carbono) entre
las aldohexosas (por ejemplo, D-alosa y D-altrosa). Por ultimo, el hecho de que
estos azucares sean "D-azucares" derivados del D-gliceraldehido nada tiene que ver
con que el azucar sea dextrorrotatorio 0 levorrotatorio.
Estructura de 10 glucoso
45
A medida que aumenta el mimero de atomos de carbona asimetricos en una molecula de carbohidrato, el mlmero de is6meros 6pticos tambien aumenta. Van' t Hoff
estableci6 que 2 n representa el mimero de is6meros 6pticos posibles, donde n es
el mlmero de ::itomos de carbona asimetricos. De este modo, en las triosas donde
n es 1, existen dos is6meros 6pticos; en las tetrosas donde n es 2, se encuentran
cuatro is6meros 6pticos, conocidos como D-eritrosa, L-eritrosa, D-treosa y L-treosa.
En las aldohexosas, donde hay cuatro ::itomos de carbono asimetricos, existen 16
is6meros 6pticos, ocho de los cuales son los D-azticares mostrados en la figura 2.1.
En las cetohexosas, cuando n es 3, existen ocho is6meros posibles.
Aunque en la figura 2.1 se muestran ocho aldohexosas, s6lo tres de ellas se encuentran con frecuencia en la naturaleza. Sus f6rmulas de proyecci6n se repiten aquf
junto con la estructura de la D-fructosa, una cetohexosa importante. Asimismo, pueden
hacerse las siguientes afirmaciones acerca de su isomerismo: los cuatro azticares
son D-azticares debido a que tienen la misma configuraci6n que el D-gliceraldehfdo en
el atomo quiral con el ntimero mas alto; el uso del termino D nada tiene que ver con
que estos azticares sean dextrorrotatorios 0 levorrotatorios.
CHO
I
HCOH
I
HOCH
I
HCOH
I
HCOH
I
CH 2 0H
0-( + )-Glucosa
CHO
CHO
I
HOCH
I
HOCH
I
HCOH
I
HCOH
I
I
HCOH
I
HOCH
I
HOCH
I
HCOH
I
CH 2 0H
CH 2 0H
o( + )-Manosa
o( + )-Galactosa
CH 2 0H
I
I
HOCH
I
HCOH
I
HCOH
I
c=o
CH 2 0H
o(-)-Fructosa
Las tres aldohexosas son estereois6meros, mas especificamente, is6meros 6pticos. Dado que ninguna de las tres es enanti6mero de las otras dos, estan relacionadas como diastere6meros. Como tales, tienen diferentes puntos de fusi6n, diferentes
puntos de ebullici6n, diferentes solubilidades, diferentes rotaciones especificas y,
en general, diferentes propiedades qufmicas.
Puede decirse que la D( + )-glucosa es un epimero de la D( + )-manosa dado que
estos compuestos difieren entre sf por su configuraci6n en un solo atomo de carbona
asimetrico. De manera similar, la D( + )-glucosa es un epfmero de la D( + )-galactosa.
Por otro lado, no existe relaci6n epimerica alguna entre la D( + )-manosa y la D( + )galactosa.
La D-fructosa es un is6mero estructural de las otras tres hexosas. Aunque tiene
la misma f6rmula molecular (C 6H 120 6), tiene un grupo funcional distinto; es una
cetosa en lugar de una aldosa.
2.3
ESTRUCTURA DE LA GLUCOSA
Emil Fischer recibi6 el Premio Nobel de qufmica por sus estudios sobre la estructura de la glucosa, mas especfficamente por establecer la configuraci6n de los cuatro
atomos de carbono asimetricos de esta aldohexosa relacionada con el D( + )-gliceraldehfdo. A partir de los trabajos de Fischer, los qufmicos pudieron representar
las f6rmulas de proyecci6n y de barras y esferas de la D- y la L- glucosa (estructura
2.5).
46
Carbohidratos
CHO
H
HO
CHO
CHO
H
H
H
OH
HO
H
H
H
H
OH
CH 2 0H
HO
H
HO
H
CH 2 0H
CH 2 0H
L( + )-Glucosa
CH 2 0H
o( + )Glucosa
ESTRUCTURA 2_5
Si el modelo de barras y esferas antes representado se construye de modo material y los grupos -CHO y -CH2 0H se fijan de modo que se alejan del punto de
soporte (hacia atnis del plano del papel), el resto de los atomos de carbona tendera
a formar un anillo que se extienda hacia el punto de soporte, y los grupos H y OH
se proyectaran hacia fuera en direcci6n del punto de soporte.
Aunque las aldohexosas se han considerado hasta aquf como polihidroxialdehfdos 0 polihidroxicetonas, hay un gran numero de pruebas que indican que otras
formas (por ejemplo, de glucosa) existen y, realmente, predominan tanto en la fase
s61ida como en solucion. Por ejemplo, las aldohexosas experimentan la sfntesis de
Kiliani-Fischer con dificultad, aunque la formaci6n de cianohidrina con aldehfdos
simples es por 10 general nipida_ La glucosa y otras aldosas no responden a la prueba de Schiff para aldehfdos. La glucosa s6lida es bastante inerte al oxfgcno, pero
los aldehfdos son notoriamente autooxidables. Por ultimo, es posible preparar dos
formas cristalinas de D-glucosa. Cuando la D-glucosa se disuelve en agua y se deja
que cristalice por evaporaci6n del agua, se obtiene una forma conocida como cx-Dglucosa. Si la glucosa se cristaliza a partir de acido acetico 0 piridina, se obtiene
otra forma, la {:l-D-glucosa. Estas dos formas de D-glucosa presentan el fenomeno
de mutarrotaci6n. Una solucion de cx-D-glucosa recien preparada muestra una rotacion especffica [cx]~? de + 113°; cuando la soluci6n se deja en reposo, cambia a
+ 52 .5°. Por otra parte, una solucion de i3-D-glucosa recien preparada tiene una
rotacion especffica [cx]6° de + 19°; cuando se deja en reposo, cambia tambien al
mismo valor, es decir, + 52.5 ° .
La existencia de ambas form as de la glucosa, asf como tambien las otras propiedades anormales descritas anteriormente, fueron explicadas por el qufmico ingles
W. N. Haworth, quien demostro que las aldohexosas y otros azucares reaccionan
internamente para formar hemiacetales cfclicos. La formaci6n de hemiacetales es
una reaccion caracterfstica entre aldehfdos y alcoholes.
H
/H
+ R'OH
R- C
o
1
--->
R- C- OR '
1
OH
47
Estructuro de 10 glucoso
,P
H"
1 C:7'
21
H- C- OH
31
HO- C- H
4
1
H- C- OH
51
H- C- OH
61
CH 2 0H
D-Glucosa
(F6rmula de proyecci6n de Fi scher)
Cuando se hace un modelo
de este tipo, rotarc:t como
sigue:
1
/H
/ I
~-,
',6
l 5,C- - C H2 0H
4
H~I
l'
1/
OH -/
OH
H
1
Y
Ho~1C
I-
3
H
CH = O
21 /
C
I
OH
EI grupo unido al
C-4 gira como
indica la flecha
1
CH 20H
I
H/
O
"
5I
YH
I H
"'I
Y~ OH
H
HO '\. 1
1/ OH
C-C
I
H
CHpH
6
/Y ( ,
I
OH
a-D( + )-Glucosa
y-
H/
/
EI ataque nucle6filo sobre el
carbona del grupo carbonilo
deficiente en electrones form a un
anillo de seis atomos y constituye
los hemiacetales ciciicos
H
I
H
I
O
"",
4 I
H
\, ~
C
OH
H 1 CH = O ,
H6,,\ 1
21 /
C-C
3
CH 20H
I
OH
Forma abierta
de la glucosa
H/
I
'
C
YH
OH
O
"
OH
"' I
H
C
H6~1c - cI /~
I
I
H
OH
{3-D( + )-Gl ucosa
FIGURA 2.2 Esquema que muestra 10 formaci6n de las formas hemiacet61icas de
10 D-glucosa. Observese que existe un equilibrio entre las formas ex y {3 y 10 estructura
de cadena abierta.
La formacion de la estructura cfclica de hemiacetal para la D-glucosa se muestra
en la figura 2.2.
La rotacion del enlace entre los atomos de carbo no 4 y 5 mueve el grupo hidroxi10 del carbono 5 a una posicion donde puede reaccionar con el grupo aldehfdo del
carbono 1. Esto coloca al grupo -CH2 0 H del carbono 5 arriba del anillo. Con forme se forma el anilJo de hemiacetal , notese que el carbono I se convierte en un centro quiral.
48
Carbohidratos
En consecuencia, son posibles dos moleculas diastereomericas. Estos is6meros son
las formas a y {3 de la glucosa; sin embargo, son diastere6meros en vez de enantiomeros, ya que la forma a difiere de la {3 solo en la configuracion de un solo carbono. Puesto que las formas cfc1icas de las aldohexosas tienen cinco ,Homos de carbono
asimetricos, existen 32 isomeros opticos de las aldohexosas cfc1icas, consistentes en
16 pares de enantiomeros.
Como se hi~ notar anteriormente, los angulos del atomo de carbono tetraedrico
doblan la molecula de glucosa para formar un anillo. Cuando reacciona el grupo
hidroxilo del carbona 5, como se muestra en la figura 2.2, se forma un anillo de
seis miembros. Si el grupo hidroxilo del carbona 4 reacciona, se forma un anillo
de cinco miembros; un anillo de siete miembros tiene demasiada tension como para
permitir que el grupo hidroxilo del carbona 6 de una aldohexosa forme un hemiacetal. Los azucares cfclicos de seis miembros pueden considerarse como derivados
del pirano, mientras que los de cinco miembros se consideran derivados del furano.
o
CH -0
HC/
" CH
'~
-f"
C-C
2
H
H
a-Pirano
HC/
'------CH
~-e
H H
Furano
De aquf que sea habitual referirse a la forma piranosa 0 furanosa del monosacarido, En solucion, la forma furanosa de las hexosas es menos estable que la forma
piranosa; no obstante, en la naturaleza existen formas combinadas de azucares de
forma furanosa (como en la unidad de fructosa de la sacarosa).
Haworth propuso que estas formas de hemiacetal cfclico de la glucosa y otros
azucares se representaran como un anillo hexagonal en un plano perpendicular al
plano del pape\. Ellado del hexagono que esta mas proximo al lector se indica entonces mediante una linea gruesa. Cuando esto se hace, los sustituyentes del atomo
de carbona se prolongan entonces hacia arriba 0 hacia abajo del plano del anillo de
seis componentes. El atomo de carbono 6, un sustituyente del carbona 5, estara
en consecuencia por arriba del plano del anillo, Las formulas de Haworth para la
a-DC + )-glucosa y la /3-D( + )-glucosa pueden compararse entonces con las formulas de proyeccion de Fischer para estos diastereomeros (estructura 2.6).
Con respecto a la asignacion de estructuras a los anomeros a y {3, Fischer sugirio
originalmente que, en la serie D, el compuesto mas dextrorrotatorio se denominara
anomero a, mientras que, en la serie L, el anomero {3 serfa la substancia mas levorrotatoria. Mas tarde, Freudenberg propuso que los anomeros a y {3 se c1asificaran
con respecto a su configuracion en vez de su signo 0 magnitud de rotacion. La relacion que existe entre el hidroxilo anomerico y el atomo de carbono de referencia
se aprecia c1aramente cuando se utili zan las formulas de proyeccion de Fischer para
las estructuras en anillo. En estas proyecciones, el anomero a es el isomero en el
que el hidroxilo anomerico esta del mismo lado (cis) de la cadena de carbono que
el grupo hidroxilo en el atomo de carbona de referencia. Si ocurre que el grupo
hidroxilo de referencia (como sucede en la a-D-glucopiranosa) interviene en la formacion del anillo, entonces el hidroxilo anomerico del isomero a esta del mismo
lado que la estructura en anillo formada por el puente de oxfgeno. En el anomero
{3, el grupo hidroxilo del hemiacetal esta en posicion trans con respecto al hidroxilo
del atomo de carbo no de referencia.
La asignacion de configuracion al atomo de carbono anomerico se aprecia con
menos c1aridad cuando se utilizan las formulas de Haworth. En el caso de las
Estructuro de 10 glucosa
49
F6rmulas de proyecci6n de Fischer
H-9 OH
HO-Fi
I
J
H-C-OH
I
HO-y- H
H-C- OH
I
H-C I
H- 9 - 0H
I
0
I
0
HO-y~
H-C- OH
I
I
-
H-C
CH 2 0H
CH 2 0H
F6rmulas de Haworth
6
CH 2 0H
5
0
""H
OH
H
a-D-Glucosa
H
OH
{j-D-Glucosa
ESTRUCTURA 2_6
D-hexosas y las D-pentosas, el anomero a tiene el hidroxilo anomerico representado debajo del plano del anillo. EI anomero (3 tiene entonces el hidroxilo anomerico
por arriba del plano del anillo. Algunos ejemplos se dan en la figura 2.3.
Existe todavfa un aspecto final de la estructura de la glucosa que debe mencionarse , el de su conformaci6n. Puesto :jue el angulo de enlace c-o-c del anillo
hemiacetalico (111°) es similar a los angulos C-C-C del anillo (109°) del ciclohexano, el anillo de piranosa de la glucosa, en vez de formar un plano verdadero,
se pliega en forma muy similar al ciclohexano. Al igual que este, la glucopiranosa
puede existir en dos conformaciones: las estructuras de silla y de bote. La conformacion de silla de la glucosa reduce al mfnimo la fuerza de torsion y, ademas de
10 anterior, se prefiere la estructura conformacional en la que un numero maximo
de grupos voluminosos (-OH y -CH20H) son ecuatoriales, en lugar de axiales,
con respecto a un eje que pasa a traves del aniBo. En la siguiente estructura se muestra
que la {3-D( + )-glucopiranosa puede adquirir una conformacion en la que todos los
grupos voluminosos son ecuatoriales (perpendiculares) a un eje que pasa a traves
del plano del anillo. Esta conformacion es termodincimicamente mas estable que aqueBa en la que los hidroxilos y los grupos -CH20H son axiales (paralelos al eje mostrado) . La a-D-glucopiranosa tiene una conformacion en la que todos los grupos
enlaces axiales
enlaces ecuatoriales
OH
,,
H
a-D( + )-Glucopiranosa
50
Carbohidratos
OH
I
H- {
OH
I
H- C- OH
0
H- C- OH
0
H- {
HO-{~
I
I
HO-9~
H- C- OH
H- C
H-
H-
I
C
I
CH 20H
a-o-Glucopiranosa
I
CI
i=9- i=9-
0H
0H
0
I
H- C- OH
HO
0
HO-
C- H
OH
H-
H
CH 2
OH
CH 20H
CH 20H
{1-L-Arabinopiranosa
I
I
CI
HO - C- H
{ - H
I
CI
H- C- OH
a-D-Glucofuranosa
a-D-Galactofuranosa
Proyecciones de Fischer
H
H- C- OH
I
CHpH
a-o-Glucopi- .
ranosa
a-D-Glucofuranosa
a-D-Galactofuranosa
{1-L-Arabi nopiranosa
Proyecciones de Haworth
FIGU RA 2 _3
Formulas de Fischer y de Haworth de a lgunos monosacaridos comunes.
voluminosos excepto el hidroxilo anomerico son ecuatoriales; la estructura preferida para dicha ·forma puede representarse asi:
f;l
enlaces axiales
enlaces ecuatoriales
HO~'
4
CH 2 0H ....._____ 0
,5
H
2:H ~
HO :
~H 1 . H
i
H
OH
{3-0( + )-Glucopiranosa
Por 10 tanto, uno de los dos an6meros, el an6mero {3 que presenta todos los grupos voluminosos ecuatoriales, debe predominar en soluci6n sobre el an6mero ex que
presenta un grupo axial, el hidroxilo anomerico. De este modo, en soluci6n acuosa,
la {3-o( + )-glucopiranosa existe en una proporci6n cercana al 63 % despues de la
mutarrotaci6n, mientras que la ex-o( + )-glucopiranosa comprende alrededor del 36 %La forma lineal de polihidroxialdehido explica menos del 1 % del carbono total presente como glucosa (vease la figura 2_2)_
Estructura de otros monosacaridos
H
OH
51
H
H
H
/3-D-Fructopiranosa
a-D-Fructopi ranosa
ESTRUCTURA 21
2.4
ESTRUCTURA DE OTROS MONOSACARIDOS
Las formas piranosas de las de mas aldohexosas mencionadas en la pagina 45 pueden
escribirse mediante la disposicion adecuada de los grupos hidroxilo en los carbonos
2, 3 Y 4 _ De manera similar, las formulas de Haworth para la a-D-fructopiranosa
y (3-D-fructopiranosa se pueden escribir como se muestra en la estructura 2_7 _ Sin
embargo, notese que la estructura furanosa de cinco miembros es la unica encontrada para la fructosa cuando el grupo hemicetal (del grupo cetona de las cetohexosas)
es sustituido como en la sacarosa (v ease la seccion 2.6.1) y las fructosanas.
La pentosa D-ribosa, un componente del acido ribonuc1eico, existe como una furanosa; la 2-desoxi-D-ribosa, un componente del acido 2-desoxirribonuc1eico, es
tambien un azucar furanosido. Los isomeros y (3 pueden existir en solucion, pero
el isomero (3 es el unico que se encuentra en los acidos nuc1eicos.
a
H" ~O
~O
H
" C7'"
C7'"
1
1
HCOH
1
HCOH
1
HCOH
1
CH2 0H
D-Ribosa
HCH
1
HCOH
1
HCOH
1
OH
CH 2 0H
2-Desoxi-D-ribosa
/3-D-Ribofuranosa
ESTRUCTURA 2.8
Otros cuatro monosacaridos que son de gran importancia en el metabolismo de
los carbohidratos durante la fotosfntesis son la aldotetrosa, D-eritrosa; las cetopentosas , D-xilulosa y D-ribulosa; y la cetoheptosa, D-sedoheptulosa.
CH 2 0H
1
c=o
H,
0
" ,f'
C
1
HCOH
,I
HCOH
1
CH 2 0H
D-Eritrosa
CH 20H
1
c=o
1
HOCH
1
HCOH
1
CH 2 OH ·
D-Xiiuiosa
CH 2 0H
1
c= o
1
HCOH
1
HCOH
1
CH 2 0H
D-Ribuiosa
1
HOCH
1
HCOH
1
HCOH
1
HCOH
1
CH 2 0H
D-Sedoheptuiosa
52
Corbohidrotos
Aunque las estructuras hemiacetalicas de cinco miembros (eritrosa) 0 hemicetalicas (xilulosa, ribulosa) de estos monosacaridos pueden representarse, las formas
metab6licamente activas son los esteres de fosfato en los que el grupo alcohol primario (-CH20H) se ha esterificado con H3P04 , 10 que evita su participaci6n en una
estructura anular.
Otros dos desoxiazucares se encuentran en la naturaleza como componentes de
las paredes celulares: la L-ramnosa (6-desoxi-L-manosa) y la L-fucosa (6-desoxi-L-galactosa) .
H" ~O
C~
I
HCOH
HtOH
I
I
HOCH
I
HOCH
CH 1
L-Ramnosa
H
~O
"C ~
I
I
HCOH
I
HCOH
I
HOCH
I
HOCH
CH1
L-Fucosa
Asimismo, existen dos aminoazucares, D-glucosamina Y D-galactosamina, en
los que el grupo hidroxilo del carbona 2 es sustituido por un grupo amino_ La primera es un componente importante de la quitina, un polisacarido estructural presente en insectos y crustaceos. La D-galactosamina es un componente importante del
polisacarido del cartilago. Sus formas hemiacetalicas se muestran enseguida _ Las
formas derivadas de los aminoazucares se describiran despues.
2-Desoxi-2-amino-(3-D-glucopiranosa
((3-D-glucosamina)
2.5
2.5.1
2-Desoxi-2-amino-(3-D-galactopiranosa
((3-D-galactosami na)
PROPIEDADES DE LOS MONOSACARIDOS
M UTARROTACION
Ya se ha hecho referencia a1 fen6meno de mutarrotaci6n que presentan las formas
anomericas de la D-glucopiranosa. La mutarrotaci6n es una propiedad presentada
por las formas hemiacetalicas y cetalicas de los azucares libres para formar el azucar de cadena abierta. Como se seiial6 en la figura 2.2, el polihidroxialdehfdo 0
polihidroxicetona de cadena abierta es un intermediario en el proceso de interconversi6n de las formas a y {j durante la mutarrotaci6n.
Propiedades de los monosac6ridos
2.5.2
53
ENOLIZACION
Cuando la glucosa se expone a alcalis diluidos por varias horas, la mezcla resultante contiene tanto fructosa como manosa. Si cualquiera de estos azucares se trata
con alcali diluido, la mezcla de equilibrio contendra el otro azucar asf como tambien glucosa. Esta reacci6n, conocida como la transformaci6n de Lobry de Bruyn-von
Ekenstein, se debe a la enolizaci6n de estos azucares en presencia de alcali. Los
intermediarios enediol comunes a los tres azlicares mencionados determinan el establecimiento del equilibrio. A mayores concentraciones de alcali, los monosacaridos son
por 10 general inestables y experimentan oxidaci6n, degradaci6n y polimerizaci6n.
HC=O
I
HCOH
I
HOCH
I
HCOH
I
HCOH
6H 2 OH
D-Glucosa
HOCH
II
COH
I
~HOCH
I
HCOH
I
HCOH
6H 2 OH
HOCH
I
HOC
I
~HOCH
~HOCH
I
HCOH
H60H
I
I
HCOH
HCOH
6H 2OH
6H 2 OH
trans-Enediol
HOCH 2
I
C=O
I
D-Fructosa
cis-Enediol
~
~
O=CH
I
HOCH
I
HOCH
I
HCOH
I
HCOH
6H 2 OH
D-Manosa
Isomerizaci6n en alcali diluido
La enolizaci6n alcalina mostrada tiene sus contrapartes enzimaticas en las que
isomerasas y epimerasas catalizan la interconversi6n de las formas fosforiladas de
estas tres hexosas (secciones 10.3 y 10.6).
2.5.3 OXIDACION-REDUCCION
Los carbohidratos pueden clasificarse ya sea como azucares reductores 0 no reductores. Los azucares reductores, que son los mas comunes, tienen la capacidad de
funcionar como agentes reductores debido a que estlin presentes en la molecula grupos aldehfdos libres 0 potencialmente. libres como en las formas herniacetaIicas cfclicas. Este grupo aldehfdo es oxidado facilmente a acido carboxflico en pH neutro
por enzimas y agentes oxidantes moderados. Esta propiedad se utiliza para detectar
y cuantificar monosacaridos, especialmente glucosa, en fluidos biol6gicos como la
sangre y la orina. El acido monocarboxflico que se forma se conoce como un acido
ald6nico (por ejemplo, acido gluc6nico de la glucosa). Enseguida, se muestran las
estructuras de varios de estos acidos.
COOH
I
HCOH
Ho6H
H60H
I
HCOH
I
CH 20H
Acido
D-gluc6nico
COOH
I
HCOH
Ho6H
Ho6H
H60H
I
CHpH
Acido
D-galact6nico
COOH
I
HOCH
Ho6H
H60H
I
HCOH
I
CHpH
Acido
D-man6nico
En presencia de un agente oxidante energico como el HN0 3 , tanto el aldehfdo
como la funci6n alcohol primaria se oxidaran para dar el correspondiente acido dicarboxflico 0 aldarico (por ejemplo, acido galactarico).
54
Carbohidratos
Uno de los productos de oxidacion mas importantes de los monosacaridos es el
acido monocarboxilico obtenido por la oxidacion de unicamente el grupo alcohol
primario, por 10 comun mediante enzimas especificas, para producir el acido uronico correspondiente (por ejemplo, acido galacturonico) . Dichos acidos son componentes de heteropolisacaridos importantes encontrados en la naturaleza.
H
OH
Acido 0'-D-Galactur6nico
Los grupos aldehfdo y cetona de los monosacaridos pueden reducirse por medios
no enzimaticos (con hidrogeno 0 NaBH4) 0 con enzimas para producir los alcoholes
de azucar correspondientes. De esta manera, cuando se reduce, la D-glucosa, produce D-sorbitol, y la D-manosa, D~manitol. El sorbitol se encuentra en las bayas
de muchas plantas superiores, especialmente las Rosaceas; es un solido cristalino a
temperatura ambiente, pero tiene un punto de fusion bajo. EI D-manitol se encuentra
en algas y hongos. Ambos compuestos son solubles en H20 y tienen un sabor dulce.
2.5.4
FORMACION DE GLiCOSIDOS ·
Una de las propiedades mas importantes de los monosacaridos es su capacidad para
formar glicosidos. Considerese como ejemplo la formacion del metil glicosido de
. la glucosa. Cuando la D-glucosa en solucion se trata con metanol y HCl, se forman
dos compuestos. La determinacion de su estructura ha mostrado que estos dos compuestos son los diastereomeros metil -a-D~glucosido y metil-{3-D-glucosido. Estos
gluc6sidos, y 10sglic6sidos en general, son labiles en medioacido pero relativamente estables a un pH neutro y alcalino : Puesto que la formacion del metil glicosido convierte al hemiacetal en un grupo acetal, el glic6sido no es azucar reductor
y no presenta el fen6meno de mutarrotaci6n.
CHO
I
I
HOCH
I
HCOH
I
HCOH
H
+ CH 30H ~
OH
Metil-(3-D-gluGopiranosido
+
HOCH 2
HCOH
I
CH 2 0H
Metil-0'-D-gluGopiran6sido
Propiedades de los monosacaridos
55
Cuando un grupo hidroxilo alcoh61ico de una segunda moltkula de azucar reacciona con el hidroxilo del hemiacetal (0 hemicetal) , el glic6sido resultante es un
disacarido. El enlace entre los dos azucares se conoce como enlace glicosidico. Los
polisacaridos se forman por la uni6n de un gran numero de unidades de monosacaridos mediante enlaces glicosidicos .
Aunque el grupo hidroxilo anomerico de los azucares puede metilarse con facilidad, como en 'la formaci6n de metil glic6sidos que se acaba de describir, la metilaci6n
de las funciones hidroxilo restantes requiere agentes metilantes mucho mas fuertes.
No obstante, los cuatro grupos hidroxilo restantes del metil-a-o-glucopiran6sido
pueden hacerse reaccionar con yoduro de metilo 0 sulfato de dimetilo para producir
el derivado pentametilado. Dichos compuestos, a su vez, son utiles para determinar la
. estructura anular del azucar original como en el siguiente ejemplo:
CHO
I
HCOCH )
I
H 3COCH
I
HCOCH )
H+
~
H 20
I
I
HCOH
CH 20CH 3
H
Penta·O·metil·a·o-glucosa
2,3,4,6· T etra-O-metil·o·glucosa
El grupo metilo del carbona hemiacetalico, por ser un metilo glicosidico, es facilmente hidrolizado por los acidos. Por el contrario, esto no ocurre con los grupos
metilo restantes, ya que son eteres de metilo. Por 10 tanto, el tratamiento del derivado pentametilglucosa representado aqui con acido diluido a 100°C producira el
2,3,4,6-tetra-O-metil-o-glucosa. En cambio, el tratamiento del derivado pentametilado en el que el azucar esta en un anillo furan6sico produce el 2,3,5,6-tetra-Ometil-o-glucosa.
2.5.5
FORMACION DE ESTERES
Los grupos alcoh61icos de los carbohidratos pueden esterificarse en reacciones tal.
to enzimaticas como no enzimaticas. De este modo, cuando la a-o-glucopiranosa
se trata con anhidrido acetico, todas las funciones hidroxilo son acetiladas para dar
la penta-O-acetil-glucosa representada aqui. Estos grupos acetilo, por ser esteres,
pueden hidrolizarse en presencia ya sea de acido 0 de alcali.
H
Penta·O-acetil·a·o·glucosa
(Ac = CH3-C-)
8
Un tipo irnportante de ester de carbohidrato encontrado en el metabolismo intermediario es el ester de fosfato. Dichos compuestos se forman por la reacci6n del
56
Carbohidratos
carbohidrato con reactivos biol6gicos fosforilantes como el trifosfato del adenosina
(ATP) en presencia de una enzima apropiada. Un ejemplo es la fructosa-l ,6-bifosfato.
OH
,.
Acido a-D-fructosa-1 ,6-bifosforico
EI nombre correcto de la forma no ionizada de este compuesto es acido a-Dfructofuranosa-l,6-bifosf6rico. Dichos esteres de fosfato son acidos relativamente
fuertes con valores de pKa I Y pKa2 de aproximadamente 2.1 Y 7.2, respectivamenteo De esta manera, a un pH neutro, los fosfatos de azucar son aniones y se les asigna normalmente el nombre del ani6n, es decir, fructosa-l,6-bifosfato.
2.5.6 CONDENSACION ALDOLICA
Otra reacci6n importante que es tipica de los carbohidratos y ocurre con frecuencia
en bioquimica es la condensaci6n ald61ica (0 su inverso, la ruptura ald6lica). Esta
reacci6n depende de la acidez de los hidr6genos (a-hidr6genos) del atomo de carbono adyacente a un grupo carbonilo y de la capacidad del ion formado para estabilizarse por resonancia.
CH 2 0H
CH2 0H
I
C=O
I
~
~
CH 2 0R
I
C=
I
O
CH 2 0H
I
II
C=OG
+----+
HC - R
G
H-C-R
Is6mero de
resonancia
+
H+
El ion enolato es entonces capaz de actuar como nuc1e6filo y puede atacar al
grupo aldehido de una segunda moIecula de azucar.
CH2 0 H
CH 2 0 H
I
c=o +
I
H-C - OR
G
e
H-C-OG
I
I
HC - OH
CH2 0 H
I
I
I
c=o
w
->
H- C-O R
I
H- C-O H
I
H- y - OH
CH2 0 H
Como se muestra en la reacci6n anterior, dos triosas pueden condensarse en una
condensaci6n ald6lica para producir una hexosa. En el proceso, se forma un nuevo centro quiral. En teoria, se produciran dos hexosas con una configuraci6n R 0
Oisoc6ridos
57
Sen el carbono 4 . En el metabolismo, interviene una enzima en el proceso de formaci6n del ion enolato, y s610 se formani uno de los dos diastere6meros posibles .
2.6 DISACARIDOS
Los oligosacaridos (vease su definici6n en la pagina 38) que se encuentran con
mayor frecuencia en la naturaleza son disacaridos que al hidrolizarse producen dos
moleculas de monosacaridos. Entre los disacaridos encontrados esta el azucar maltosa; este azucar se obtiene como intermediario en la hidr6lisis del almid6n por las
enzimas conocidas como amilasas. En la maltosa, una molecula de glucosa se une
a traves del grupo hidroxilo del atomo de carbono C-l en un enlace glicosfdico al
grupo hidroxilo del carbono 4 de una segunda molecula de glucosa.
Maltosa
El enlace glicosfdico que se forma entre los dos residuos de glucosa se designa
como a(1-4) para especificar que el carbono anomerico que interviene en el enlace glicosfdico tiene la configuraci6n a y que esta unido a la posici6n 4 de la segunda
molecula de glucosa. Esta segunda fracci6n de glucosa posee un hidroxilo anomerico libre que puede existir ya sea en la configuraci6n a 0 (3 (se muestra el is6mero
(3); este hidroxilo anomerico libre Ie confiere asf la caracterfstica de mutarrotaci6n
ala maltosa, y este disacarido es un azucar reductor. Que la maltosa tiene la estructura mostrada se determin6 analizando los dos productos obtenidos por hidr61isis
acida de su derivado octametilado. La maltosa totalmente metilada produce mediante hidr61isis los compuestos 2,3,4,6-tetra-O-metil-D-glucosa y 2,3,6-tri-O-metil-D-
Octametil-D-maltosa
CHO
CHO
I
HCOCH 3
I
CHPCH
I
HCOCH 3
I
HCOH
I
CH 20CH 3
2,3,4,6-Tetra-Q-metil-D-glucosa
I
I
CHPCH
I
HCOH
I
HCOH
I
HCOCH 3
+
CH 2 0CH j
2,3,6-Tri-Q-metil-D-glucosci
58
Corbohidratos
.glucosa. Mientras que el carbono anomerico de la maltosa se metila luego de tratar
el disacarido con sulfato de dimetilo, esteenlace O-metil-glicosfdico asf como el
enlace glicosfdico que se forma entre las dos unidades de glucosa del disacarido son
labiles en presencia de acido y ambos se rompen por la hidrolisis con acido.
El disacarido celobiosa es identico a la maltosa excepto en que el primer compuesto tiene un enlace (J(1-4) glicosfdico. La celobiosa es un disacarido que se
forma durante la hidrolisis acida de la celulosa.
HOH
H
OH
Celobiosa
Es un azucar reductor y experimenta mutarrotacion. El tratamiento de este azucar con sulfato de dimetilo produce tambien un azucar octametilado y la hidrolisis
acida produce los mismos productos que se obtienen de la octametil maltosa.
La isomaltosa, otro disacarido obtenido durante la hidrolisis de ciertos polisacaridos, es similar a la maltosa excepto en que tiene un enlace a( 1 - 6). La metilacion
exhaustiva y la hidrolisis acida de la octametil isomaltosa produciran los compuestos 2,3,4,6-tetra-O-metil-o-glucosa y 2,3,4-tri-O-metil-o-glucosa.
H
H
OH
Isomaltosa
La lactosa es un disacarido que se encuentra en la leche; por hidrolisis, produce
un mol de D-galactosa y uno de o-glucosa. Posee un enlace (J(1-4), es un azucar
reductor y puede experimentar mutarrotacion. La a-lactosa tiene la siguiente formula en la que la configuracion en el extremo reductor del disacarido se muestra como a.
Lactosa
Disocaridos
59
Por ser el principal carbohidrato de la leche, la lactosa es de suma importancia
en la nutrici6n de los mamiferos j6venes. La mayor parte de la poblaci6n humana
del orbe depende de este azucar como una forma importante de energia durante el
primer ano de vida. La lactosa como tal no puede ser absorbida por la sangre, por
10 que primero debe ser hidrolizada hasta sus monosacaridos componentes por la
lactasa intestinal. Esta enzima es abundante en los lactantes, pero tiende a desaparecer con la edad. S610 los europeos del norte y algunos habitantes de Africa retienen
esta enzima en la edad adulta. La mayoria de los demas grupos humanos tienen poca lactasa intestinal en la edad adulta y algunos, en especial orientales y habitantes
. del Mediterraneo, pueden presentar cierta intolerancia al azucar. En estos individuos, el alto consumo de lactosa en la dieta produce malestar intestinal en forma
de diarrea y dolor.
La sacarosa, el azucar comercial, es producida por las plantas superiores; la remolacha azucarera y la cana de azucar son las principales fuentes comerciales. Por
hidr61isis, la sacarosa produce una moh!cula de glucosa y una de fructosa pero, en
contraste con todos los demas monosacaridos y disacaridos descritos anteriormente, la sacarosa no es un azucar reductor. Esto significa que los grupos reductores
de ambos monosacaridos deben intervenir en la formaci6n del enlace glicosidico
entre ambos azucares. Es decir, los atomos de carbona 1 y 2, respectivamente, de
las fracciones de glucosa y fructosa deben estar unidos covalentemente en un enlace glicosidico. Los estudios de permetilaci6n en la sacarosa han mostrado que debe
tener la siguiente estructura con una configuraci6n ex en la subunidad de glucosa
y una configuraci6n (3 en la subunidad de fructosa.
H
OH 0
Sacarosa
La sacarosa es un producto importante de la fotosintesis de las plantas (secci6n
11.2.2 y capitulo 15). Asimismo, constituye la forma en la que los carbohidratos, producidos en las hojas por la fotosintesis, son transportados hacia los 6rganos de almacenamiento como semillas, tuberculos o· rafces en desarrollo. Se ha sugerido que la
sacarosa tiene una ventaja, tanto como producto de reserva como una forma de transporte de carbohidratos, sobre la glucosa y los otros azucares comunes dado que sus
dos atomos de carbono anomericos estan protegidos del ataque oxidativo.
La sacarosa, y en menor grado la maltosa, son carbohidratos importantes de la dieta
humana. Sin embargo, no pueden ser absorbidos directamente por la sangre y, al igual
que la lactosa, primero deben ser hidrolizados por enzimas especificas, invertasa 0
sacarosa y maltasa, presentes en la mucosa intestinal. La sacarosa se uti liz a ampliamente como agente edulcorante en la industria alimentaria. Se obtiene facilmente y
es mas dulce que los otros azucares comunes, maltosa, lactosa y glucosa. S6lo la fruc-
60
Carbohidratos
tosa es mas dulce, y hoy en dfa mezclas de glucosa y fructosa producidas enzimaticamente a partir del almid6n del mafz y otras plantas estan sustituyendo a la sacarosa
como edulcorante comercial. Dichas mezclas equivalen desde el punto de vista nutricional a la sacarosa con respecto al peso y son considerablemente mas dulces.
2.7
POLISACARIDOS
Los polisacaridos existentes en la naturaleza tienen una funci6n estructural 0 tienen
una funci6n importante como una forma de energfa almacenada. Todos los polisacaridos pueden ser hidrolizados con acidos 0 enzimas para producir monosacaridos, derivados de estos, 0 ambos. Los polisacaridos que por hidr61isis producen
s610 un tipo de monosacarido se conocen como homopolisac3ridos. Los heteropolisacaridos por hidr6lisis producen una mezcla de los monosacaridos que los constituyen y productos derivados.
2.7.1
POLISACARIDOS DE RESERVA
El almid6n es un homopolisacarido de reserva producido por las plantas (vease la
secci6n 10.6.5). Mientras que todas las plantas verdes producen almid6n como producto final de la fotosfntesis, los cereales (trigo, arroz, mafz y sorgo) destacan por
el alto contenido de almid6n en sus semillas. De hecho, estos cereales junto con
otros cultivos como la papa y la mandioca 0 yuca, en los que el almid6n se almacena
en un tubercula subterraneo, proporcionan la mayor parte de las calorfas que casi
toda la humanidad consume. El almid6n consta de dos componentes, amilosa y amilopectina, que se presentan en cantidades variables. El componente amilosa consta
de unidades de D-glucosa unidas en forma lineal por enlaces ex(l - 4); tiene un extremo no reductor y uno reductor (estructura 2.9). Su peso molecular varfa de algunos miles hasta 150,000. La amilosa da un color azul caracterfstico en presencia
de yodo debido a la capacidad del haluro para ocupar una posici6n en el interior de
una espiral de unidades de glucosa que se forma cuando la amilosa se suspende en
agua (estructura 2.10).
La amilopectina es un polisacarido ramificado; en esta molecula, cadenas mas
cortas (de aproximadamente 30 unidades) de unidades de glucosa unidas por enlaces ex( 1 - 4) se unen tambien entre sf por enlaces ex( 1 - 6) (de las que puede obtenerse isomaltosa) (vease la estructura 2.11). El peso molecular de la amilopectina de
la papa varfa ampliamente y puede ser de 500,000 0 mas. La amilopectina da un
color de purpura a rojo en presencia de yodo.
Mucho se ha aprendido sobre la estructura del alrnid6n rio s610 a partir de estudios con agentes oxidantes y metilantes exhaustivos, sino tarnbien mediante la acci6n de enzimas sobre el polisacarido. Una enzima, la ex-amilasa, presente en el
tracto digestivo de los animales (en la saliva y el juga pancreatico), hidroliza la ca-
Amilosa
ESTRUCTURA 2.9
Polisac6ridos
61
ESTRUCTURA 2.10
dena lineal de la amilosa atacando los enlaces a(1-4) al azar a 10 largo de la cadena
para producir una mezcla de maltosa y glucosa. La ,B-amilasa, una enzima encontrada en las plantas, ataca al extremo no reductor de la amilosa para producir unidades sucesivas de maltosa. (Los prefijos a y ,B utilizados con las amilasas no se refieren
al enlace glicosfdico, simplemente designan estas dos enzimas.)
o
I
0-0404 00 040.
Amilopectina
ESTRUCTURA 2.11
62
Carbohidratos
La amilopectina tambien es atacada por las enzimas anteriores pero los enlaces
glicosfdicos a(1-4) proximos a1 punto de ramificacion de la amilopectina y e1 mismo
enlace a(1-6) no son hidrolizados por ellas. Una enzima "desramificante" individual, la a(1- 6) glucosidasa, hidroliza el enlace en el punto de ramificacion. En
consecuencia, la acci6n combinada de la a-amilasa y la a(1- 6) glucosidasa hidro··
lizanl finalmente a la amilopectina hasta una mezc1a de glucosa y maltosa.
El polisacarido de reserva de los tejidos animales es el gluc6geno; es similar en
estructura a la amilopectina en cuanto a que es un homopolisacarido ramificado compuesto de unidades de glucosa. No obstante, es mucho mas ramificado que la amilopectina ya que posee puntos de ramificaci6n cada 8 a 10 unidades de glucosa. Al
igual que la amilopectina, el gluc6geno es hidrolizado por las a- y {J-amilasas para
formar glucosa, maltosa y dextrina lfmite.
Bastara un ejemplo final de un polisacarido con valor nutricional. Se trata de la
inulina, un carbohidrato de reserva encontrado en los bulbos de muchas plantas [por
ejemplo, dalia y topinambor (Helianthus tuberosus)]. La inulina consta principalmente de unidades de fructofuranosa unidas por enlaces glicosfdicos 13(2-1). 1).
2.7.2
POLISACARIDOS ESTRUCTURALES
El compuesto de carbono mas abundante en el planeta es el polisacarido estructural
celulosa. La celulosa se encuentra en la pared celular de las plantas donde contribuye
en forma importante a la estructura ffsica del organismo (v ease la secci6n 8.12).
Por carecer de un esqueleto 6seo en el que los 6rganos y tejidos especializados puedan organizarse, las plantas superiores dependen de su pared celular para soportar
su propio peso, ya sea que se trate de un girasol 0 una secoya. La madera de los
arboles es una estructura insoluble y organizada compuesta de celulosa y otro polfmero denominado lignina derivado del aminoacido fenilalanina.
La celulosa es un homopolfmero lineal de unidades de o-glucosa unidas por enlaces glicosfdicos (J(l-4)(estructura 2.12). No obstante, la diferencia aparentemente pequeiia en cuanto a estructura que existe entre este polisacarido y la amilosa
Ie confiere a la celulosa propiedadesmuy distintas e iniportantes. En lugar de formar una helice enrollada, la celulosa forma una estructura de cadenas paralelas unidas transversalmente por puentes de hidr6geno.
En contraste con el almidon, los enlaces 13(1-4) de la cehilosa son aItamente
resistentes a la hidr6lisis acida; se requiere un acido mineral fuerte para producir
o-glucosa; la hidr6lisis parcial origina el disacarido reductor celobiosa. Los enlaces 13(1-4) de la celulosa no son hidrolizados por las amilasas que se encuentran
en el tracto digestivo de los humanos 0 la mayorfa de los demas anirriales superiores. Como consecuencia, el hombre y la mayor parte de los ani males no pueden
utilizar la energfa presente en este polfmero de glucosa. No obstante, los rumiantes
son una excepci6n importante, ya que las bacterias que residen en el rumen secretan
celulasa, una {J-glucosidasa, que cataliza la hidr6lisis de dicho polisacarido. Estas
Celulosa
ESTRUCTURA 2.12
Polisac6ridos de paredes celulares
63
bacterias y otros organismos residentes en el rumen metabolizan luego la glucosa
producida en una fermentaci6n no comun que beneficia al animal hospedante. Asimismo los caracoles y los hongos que producen la putrefacci6n de la madera secretan celulasa capaz de degradar la celulosa. Las termitas tambien son capaces de
degradar este polisacarido estructural, ya que su tracto digestivo contiene un parasito que secreta celulasa.
Asimismo, se conocen otros ejemplos de polisacaridos estructurales en las plantas. Estas contienen pectinas y hemicelulosas. Las ultimas no son derivados de la
celulosa, sino mas bien polisacaridos ricos en o-xilosa (xilanos), O-manosa (mananos) y galactosa (galactan os) y unidas por enlaces glicosfdicos (3(1-4) 0 (3(1- 3).
Las pectinas contienen arabinosa, galactosa y acido galactur6nico. El acido pectico
es un homopolfmero del ester metflico de acido o-galactur6nico.
/ l
...
o
OH
Acida peplica
n
La qUltma, un homopolfmero de N-acetil-o-glucosamina, unida por enlaces
(3(l-4) es el polisacarido estructural que constituye el caparaz6n de los crustaceos
y el exoesqueleto de los insectos .
H
NH
I
c= o
I
CH 3
Quilina
2.8
,i
J"
POLISACARIDOS DE PAREDES CELULARES
Las celulas animales carecen de una pared celular bien definida pero tienen una cubierta celular visible al microscopio electr6nico que tiene una funci6n importante
en la interacci6n con las celulas adyacentes. Esta cubierta celular contiene glicoprotefnas, glicolfpidos y mucopolisacaridos. La naturaleza qufmica de los dos primeros
componentes se describira mas adelante (secciones 2.9 y 7.7) . Los mucopolisacaridos son sustancias gelatinosas de alto peso molecular (hasta 5 x 10 6 ) que tienen
una funci6n tanto lubricante como cementante. Un mucopolisacarido comun es el
acido hialur6nico, un heteropolisacarido formado por unidades alternadas de acido
o-glucur6nico y N-acetil-o-glucosamina. Estos dos diferentes monosacaridos se unen
por un enlace (3(1-3) para formar un disacarido que se une por enlaces (3(l-4)
64
Carbohidrotos
ala siguiente unidad repetitiva. EI acido hialur6nico, presente en el humor vitreo
del ojo y el cord6n umbilical, es hidrosoluble pero forma soluciones viscosas.
H
OH
H
NH
I
I
c=o
Unidad de acido hialur6nico CH 3
La condroitina, similar en estructura al acido hialur6nico excepto en que el aminoazucar es N-acetil-D-galactosamina, es tambien un componente de las cubiertas
N-Acetilglucosamina
Acido N-acetilmuramico
L-Alanina
D-Isoglutamina
L-Lisina
1
D-Alanina
Unidad repetitiva del peptidoglicano
de Staphylococcus aureus
G/icoproteinos
65
celulares. Los esteres de sulfato (en las posiciones C-4 0 C-6 del aminoazucar) de
la condroitina son componentes estructurales importantes del cartflago, tendones y
huesos.
La pared celular bacteriana, que determina muchas de las caracterfsticas fisiologicas del organismo que encierra, contiene un heteropolisacarido unido a una cadena corta de aminoacidos. Puesto que las cadenas individuales de aminoacidos no
son tan largas como en las protefnas, dichos polfmeros se han denominado peptidoglicanos en vez de glicoprotefnas. El heteropolisacarido es una cadena alternante
de N-acetil-D-glucosamina (GlcNAc) y acido N-acetilmuramico (MurNAc) unidos
por un enlace glicosfdico (3(1-4). El acido N-acetilmunimico consta de una unidad
de N-acetil glucosamina que tiene su grupo hidroxilo C-3 unido al grupo a-hidroxilo
del acido lactico por un enlace eter. En el peptidoglicano, el grupo carboxilo de
cada unidad de acido lactico se une, a su vez, a un tetrapeptido que contiene por
10 general tanto D-alanina como L-alanina. Otros aminoacidos encontrados en el
tetrapeptido pueden incluir D-glutamina, D-iso-glutamina, L-lisina 0 acido diaminopimelico.
La cadena lineal de polisacarido del peptidoglicano tiene una ramificacion tetrapeptfdica en cada segunda unidad de hexosamina que esta unida transversalmente
a las cadenas adyacentes y paralelas de polisacaridos. En dicha union transversal
(figura 2.4), el grupo carboxilo de la porcion terminal de D-alanina se une a un
residuo de pentaglicina que, a su vez, se une al grupo 8-amino de la lisina en la
unidad adyacente de glicano.
La actividad antibiotica de la penicilina se debe a su capacidad para inhibir el
ultimo paso de la biosfntesis de peptidoglicanos bacterianos. Al ser inhibida la sfntesis de este componente esencial de la pared celular, las bacterias son incapaces
de desarrollarse 0 duplicarse.
2.9
GLiCOPROTEiNAS
La mayorfa de los oligosacaridos y polisacaridos de las celulas vegetales y animales
estan unidos covalentemente a moleculas de protefnas 0 lfpidos para formar glico-
FIGURA 2.4 Las cadenas lineales del peptido glicano estan unidas transversalmente por pentapeptidos de glicina.
66
Carbohidratos
protefnas 0 glicolipidos. En muchas glicoproteinas, el grupo amida de la asparagina
se une a traves de un enlace N-glicosilo a un trisacarido central que consta de una
molecula de manosa (Man) y dos moh!culas de N-acetil glucosamina (GlcNAc) .
H
N
o
0
"-
-C~
"C-CH
II
o
AcNH
2
c=o
"-
/ NH
AcNH
Manpl,4GlcNAcpl,4GlcNacp-Asn
El residuo de manosa del polisacarido central constituye un punto de rami ficaci6n donde otras dos moleculas de manosa se unen a traves de enlaces 0'(1- 3) y
0'(1-6). Cualquiera de estas dos moleculas de manosa, 0 ambas, pueden funcionar
despues como puntos de ramificaci6n adicionales para que aumente posteriormente
la longitud del polisacarido componente. En un ejemplo bastante ramificado, la galactosa, el acido siaIico y la N-acetil glucosa son otros componentes del polisacarido
ramificado.
Maned ,2ManO' 1, 2ManO' 1,3""
ManO'l ,2ManO'l,3
Manpl,4GlcNAcPl,4GlcNAcp-Asn
""ManO'l,6 /
.
Sla0'2,3Galpl ,4GlcNAcpl,6
/
Un acido siaIico es una cetosa que posee nueve atomos de carbono (cetononosa)
que pueden estar acilados con acido acetico 0 glic6lico. El acido N-acetil-Dneuraminico es un ejemplo especifico de un acido sialico.
HO C-C-OH
2
I
CH2
o
II
I
I
H-C-OH
CH3-C- -HN-C-H
I
I
O---C-H
H-C-OH
I
I
H-C-OH
CH2 0 H
Acido N-acetil-o-neuraminico
El polisacarido central puede estar unido tambien al componente proteinico a traves
de un enlace O-glicosilo al grupo hidroxilo de la serina en lugar del grupo amida
de la asparagina. La serina sustituye a la hidroxilisina serina y la GIcNAc a otros
azucares como la xilosa y la galactosa. Estos ultimos se encuentran en glicoproteinas como la colagena y el proteoglicano. Es evidente que las glicoproteinas, que
Problemas de repaso
67
esrnn ampliamente distribuidas en toda la materia viva, pueden mostrar una gran
diversidad.
Queda mucho por aprender sobre la estructura de las paredes celulares antes de
que puedan comprenderse del todo fen6menos tan importantes como la respuesta
inmune y el crecimiento y la diferenciaci6n celulares.
BIBLIOGRAFiA
1. R. T. Morrison and R. N. Boyd, Organic Chemistry, 4th ed. Boston: Allyn and Bacon. 1983.
2. W. Pigman and D. Horton, eds., The Carbohydrates, 2nd ed. New York: Academic Press,
1970, 1972, 1980 (4 volumenes) ..
3. R. Barker, Organic Chemistry of Biological Compounds. Englewood Cliffs, N.J .: PrenticeHall, 1971.
4. R.L. Whistler and M. L. Wolfrom, eds., Methods in Carbohydrate Chemistry. New York:
Academic Press, 1962-1980 (8 volumenes).
5. M.L. Wolfrom and R.S. Tipson, eds., Advances in Carbohydrate Chemistry and Biochemistry. New York: Academic Press, 1945-1984 (42 volumenes).
PROBLEMAS DE REPASO
1. Si se sintetizan heptosas (azucares de 7 carbonos) mediante la sfntesis de Kiliani a partir
de un determinado azucar de 4 carbonos, l,cmlntos isomeros se obtendnin?
2. Una mezcla en equilibrio de a - y !J-D-galactosa tiene una [alii" de +80.2°. La rotacion
especffica de la a-D-galactosa pura es de + 150.7°. La rotacion especffica de la !J-Dgalactosa pura es de 52.8°. Ca1cular las proporciones de ambos carbohidratos en la mezcia en equilibrio.
3. Dibujar la estructura de cualquier !J-D-aldoheptosa en la forma piranosa utilizando la proyeccion de Fischer 0 la estructura anular de Haworth y responder las siguientes preguntas:
a) l,Cmintos atomos de carbono asimetricos tiene el azucar seleccionado?
b) l,Cuantos estereoisomeros del mismo azucar son teoricamente posibles?
c) Dibujar la estructura del anomero de la !J-D-aldoheptosa de que se trata.
d) Dibujar la estructura del enantiomero de la !J-D-aldoheptosa de que se trata.
e) Dibujar la estructura de un epimero (distinto al anomero) del azucar de que se trata.
f) Dibujar la estructura de un diastereoisomero de la !J-D-aldoheptosa de que se trata.
g) Dibujar la estructura de un isomero estructural de la !J-D-aldoheptosa de que se trata.
h) Dibujar las estructuras de los dos azucares que se obtendrfan si se utilizara la aldohep-
tosa representada inicialmente como el punto de partida para una sfntesis de Kiliani
(incluyendo adicion de HCN, etc.).
i) l,Por que la sfntesis de Kiliani produce dos azucares distintos a partir de un solo precursor?
J) Dibujar las estructuras de dos azucares distintos que producirfan la misma osazona
que la !J-D-aldoheptosa inicialmente.
k) Dibujar la estructura de la misma !J-D-aldoheptosa representada inicialmente en forma de anillo furan6sico.
4. A partir de bacterias se purifico un disacarido desconocido. Se obtuvieron cantidades iguales
de D-glucosa y D-galactosa por la hidrolisis acida del disacarido y se encontro que ambos
azucares estaban unidos por un enlace a -glicosfdico. La metilacion exhaustiva del disacarido produjo cantidades iguales de 2,3,4,6-tetrametilgalactosa y 2,4,6-trimetilglucosa.
Utilizando la formula de Haworth, dibujar la estructura del disacarido de que se trata
basandose en la informacion anterior e indicar claramente el enlace entre los azucares .