CENTROS DE COLOR
Anuncio

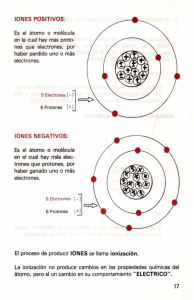
CENTROS DE COLOR Un centro de color es un defecto puntual en una estructura cristalina que produce color. Antonio Lara Rafael Rubio DEFECTOS EN CRISTALES IÓNICOS Frenkel: 1 vacante y 1 ión intersticial Schottky: 2 vacantes El cristal sigue siendo neutro Estos defectos están en todos los cristales en un 0.01% aproximadamente CENTROS DE COLOR La radiación EM puede desplazar iones (defectos Frenkel y Schottky) o arrancar electrones de los iones (lo más común). Estos electrones vuelven a sus iones, pero pueden quedar atrapados en una vacante que ya existiera. CENTROS F Eb: energía de bleaching (“blanqueo”): aumentando T se pierde el color. Ea: energía del pico de absorción En haluros alcalinos (F,Cl,Br,I,...+ Li,Na,K,Cs,...) se ha observado Ea=17.4/d1.83 [eV] ≈1 centro F por cada 10000 iones para cristales altamente coloreados CENTROS F APLICACIÓN 1 PIEDRAS PRECIOSAS CaF2 Fluorita púrpura que adquiere su color debido a centros F Al2O3 sin dopar Al2O3 dopado con Cr3+ (rubí) APLICACIÓN 2 LENTES FOTOCROMÁTICAS Las lentes se oscurecen (se ahúman) bajo la acción de los rayos ultravioleta presentes en la luz solar, cuando estamos en la calle, pero en lugares de interior las lentes ganan claridad gracias a que la red se ordena a temperatura ambiente y no están sometidas a los rayos ultravioleta. APLICACIÓN 3 DIODOS LED Desde los 60´s se usan LED a nivel industrial, tenían poca intensidad y trabajaban en rojo, verde y amarillo. Los diodos azules fueron creados a finales de los 90´s. Se ha necesitado la capacidad de trabajar con dopantes específicos y en concentraciones muy concretas. Los laboratorios que trabajan en UHV están ahora en condiciones de fabricar estructuras complejas con propiedades de semiconductores variado a la micra e incluso a nivel nanométrico. APLICACIÓN 4 LASER DE ESTADO SOLIDO Modificando el gap de semiconductores mediante dopantes por defecto o por exceso de electrones podemos modificar la frecuencia de emisión del laser. Los láseres de estado solido son muy útiles debido a que son extremadamente pequeños y requieren muy poca potencia de entrada Estructura de bandas del primer laser: Laser de rubí (1960 Maiman) Absorbe las frecuencias azul y verde y emite en la frecuencia del rojo 694,3 nm Problema Considerar al electrón confinado en un centro F en NaCl como una partícula encerrada en un pozo infinito de potencial, de anchura a (a es el parámetro de red, 564.02 pm). Suponer un salto de energía entre los niveles permitidos debido a la absorción de un fotón. Estudiar la validez de este modelo, sabiendo que el pico de absorción (la energía de un fotón) de luz debido a los centros F tiene un valor de 2.7 eV.