Transporte Gaseoso
Anuncio

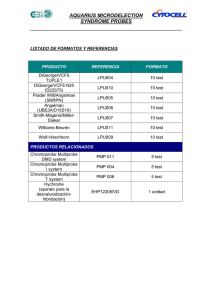
TEMA 2. TRANSPORTE GASEOSO Transporte de gases. Transporte de O2 en sangre. Factores que modifican las propiedades disociativas de la Hb. Transporte de CO2 en la sangre. Intercambio de gases entre los tejidos y la sangre. 1. OBJETIVOS • Analizar los procesos de transporte gaseoso y los factores que lo condicionan. • Estudiar el intercambio de gases entre la sangre y los tejidos. 2. CONTENIDOS 2.1. Transporte de gases Una vez que se ha producido el intercambio gaseoso a nivel pulmonar, los gases deben ser transportados hasta los tejidos para intercambiarlos con los mismos. Analizaremos los mecanismos de transporte que se ponen en marcha y los factores que lo condicionan. 2.2. Transporte de O2 en sangre El sistema de transporte de O2 se realiza fundamentalmente mediante dos sistemas: • Disuelto en el plasma en forma libre (3%). Supone una pequeña parte del transporte total. La cantidad de O2 transportado de esta forma está relacionado de forma lineal con la PO2 del aire alveolar, en una proporción de 0’003 ml O2 disuelto/100 ml sangre por cada 1 mm Hg de PO2. Así, cuando se inspira aire normal, la PO2 en el alveolo es de 100 mm Hg, y en consecuencia se transportan 0’3 ml de O2 disuelto/100 ml sangre, si a ese animal le aplicamos O2 puro podemos conseguir que la PO2 alveolar alcance los 600 mm Hg y en consecuencia la cantidad de O2 transportada es de 1’8 ml O2 disuelto/100 ml sangre. • Unido a la hemoglobina (97%). Una molécula de hemoglobina (Hb) (saturada 100%) es capaz de fijar 4 de O2, de manera que un gramo de Hb saturada puede movilizar 1’39 ml O2. Sabiendo que la sangre normal, presenta unos 15 mg/dl de Hb, podemos deducir que se movilizan ±20 ml O2/dl sangre por este sistema. La relación entre la PO2 y el O2 transportado no es lineal, ya que la saturación de la Hb presenta una curva muy característica, denominada curva de disociación de la hemoglobina (Fig. 1-1). Así, en la sangre arterial, donde la PO2 es de 90–100 mm Hg, la Hb se encuentra saturada al 97% de O2. Mientras que en los tejidos donde la PO2 es de 40 mm Hg, la Hb está saturada en un 72% de saturación, y si la PO2 decae hasta 25 mm Hg la Hb se mantiene con un 50% de saturación. La curva de disociación de la Hb permite amortiguar los cambios en la presión parcial de O2, mediante este sistema los cambios en presión parcial van a modificar en menor medida la capacidad de transporte de O2 en sangre que si tuvieran una relación lineal. Figura 1-1. Curva de disociación de la hemoglobina. 62v08n74-13030700tab01.gif Así, cuando la PO2 a nivel decrece (de 100 mm Hg a 70 por ejemplo, una reducción del 30%), la saturación de la Hb sólo pasa de 97 al 90% (un 7’2% de reducción). En el caso contrario, cuando aplicamos aire enriquecido con O2 puro, el incremento de PO2 alveolar (de 100 a 600 mm Hg) solo se traduce en el paso del 97 al 100% de saturación de Hb. 2.3. Factores que modifican las propiedades disociativas de la Hb Por presión parcial cincuenta (P50) se conoce la PO2 que supone el 50% de la saturación de la Hb. Cuando la curva de disociación se desplaza hacia la derecha, aumenta la P50, y esto supone que la Hb necesita mayor PO2 para mantener el mismo porcentaje de saturación, o lo que es lo mismo la Hb ante un descenso de la PO2 permite una mayor liberación de O2 al medio. Los factores que modifican estas propiedades disociativas de la Hb son: • Especie. Especies de menor tamaño corporal presentan una P50 mayor. De esta manera se compensa el mayor consumo proporcional de O2 que tienen las especies pequeñas, con altos niveles de metabolismo basal. • Temperatura. A mayor temperatura corporal mayor P50 (Fig. 1-2). • PCO2 (Efecto Bohr) La presencia de altas concentraciones de CO2 desplaza a la derecha la curva de disociación, con lo que aumenta la P50. De esta manera se facilita la oxigenación sanguínea en los pulmones donde la PCO2 es menor, y se intensifica la liberación de O2 en los tejidos donde la Figura 1-2. Factores que modifican la curva de PCO2 es mayor. disociación de la hemoglobina. • H+ (pH). A mayor concentración de H+ (pH (www.med.unne.edu.ar/catedras/ fisiologia1). menor) se produce un desvío a la derecha de la curva de disociación (mayor P50). • 2-3 Difosfoglicerato (DPG). El aumento de la concentración de esta sustancia desvía la curva de disociación hacia la derecha. En casos de hipoxia se produce un aumento de la concentración de DPG. • Ejercicio. El ejercicio desvía la curva a la derecha por diversas causas: el aumento de PCO2, la reducción del pH y el aumento de la temperatura. • Hb fetal. La presencia de Hb fetal desvía la curva de disociación hacia la izquierda, favoreciendo la liberación de O2 hacia los tejidos fetales. Otras situaciones se producen cuando el O2 es desplazado de la oxihemoglobina: • Monóxido de carbono (CO). Presenta una afinidad 100-200 veces mayor que el O2. Una pequeña cantidad de este gas puede desplazar al O2 de su unión a la Hb (acción directa) y por otra parte la curva de disociación se desplaza a la izquierda (acción indirecta). La sangre presenta una coloración rojo intenso (rojo cereza). • Nitritos. Se forma metahemoglobina (de color marrón) por la oxidación del hierro de la Hb de forma ferrosa a férrica. Esta metahemoglobina no permite la unión del O2. 2.4. Transporte de CO2 en la sangre El CO2 puede ser transportado de las siguientes maneras: En el plasma: • En solución (5%). El CO2 es mucho más soluble en soluciones acuosas que el O2. • En forma de bicarbonato (5%) CO2 + H2O → H2CO3 → HCO3- + H+ • Formando grupos carbaminos, al combinarse con radicales amino de las proteínas plasmáticas (1%). Dentro del GR: • En forma de bicarbonato (63%). Este proceso esta mediado por la acción de la enzima anhidrasa carbónica. CO2 + H2O → H2CO3 → HCO3- + H+ Los protones resultantes son fijados por la Hb. • Grupos carbaminos (21%). Combinado con radicales amino de las proteínas del GR, incluida la Hb formando la carbaminohemoglobina. Factores que modifican el transporte de CO2: El transporte de CO2 en sangre mantiene una relación prácticamente lineal con la PCO2. Esta relación esta condicionada por la presencia de O2, y se denomina efecto Haldane. La presencia de altas presiones de O2 (PO2) reduce la cantidad de CO2 que puede ser transportado en sangre, ya que se modifica la acidez de la Hb y su capacidad para fijar H+. Este sistema permite transportar más CO2 desde tejido (donde hay PO2 reducida) en la sangre venosa hasta los pulmones donde al aumentar la PO2 se aumenta la liberación del CO2. 2.5. Intercambio de gases entre los tejidos y la sangre La sangre arterial que llega a nivel tisular tiene una PO2 de 80-100 mm Hg, mientras que los tejidos presentan diferentes presiones dependiendo del grado de suministro de O2 y el consumo que el tejido haga del mismo, pero tiene unos valores medios de 40 mm de Hg. En cuanto al CO2, éste presenta unos niveles en sangre arterial de unos 40 mm Hg y en los tejidos se encuentra próximo a 50 mm de Hg. De manera que se produce el intercambio por un sistema de difusión igual al que se produce en el pulmón. Un factor muy determinante para el intercambio gaseoso de los tejidos es el grado de vascularización. En tejidos muy vascularizados, la distancia desde cualquier punto a un vaso sanguíneo es menor que en tejidos mal irrigados.