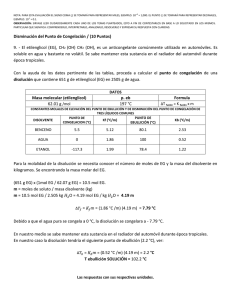
Cristalización
Anuncio

LABORATORIO DE QUÍMICA FACULTAD DE FARMACIA CRISTALIZACIÓN. Un compuesto orgánico cristalino está constituido por un empaquetamiento tridimensional de moléculas unidas principalmente por fuerzas de Van der Waals, que originan atracciones intermoleculares débiles. La cristalización es un proceso de purificación bastante selectivo, ya que en el crecimiento del cristal, el empaquetamiento regular de moléculas de un mismo tipo, forma y tamaño, tiende a excluir la presencia de impurezas. La cristalización es el método más adecuado para purificar compuestos sólidos, siempre que contengan una cantidad moderada de impurezas. Se basa en el hecho de que los sólidos orgánicos son más solubles en un disolvente caliente que en frío. Impureza Cristalización Cristal en crecimiento Sólido a cristalizar SÓLIDO IMPURO Figura 1 El primer paso en una cristalización implica disolver el sólido a purificar en la mínima cantidad del disolvente apropiado en caliente, con lo que se obtiene una disolución saturada. Al enfriar, la disolución se sobresatura con respecto al sólido, que empieza a formar pequeños núcleos de cristalización en las paredes del recipiente o en la superficie del líquido. Una vez que estos núcleos se han formado, otras moléculas llegan a la superficie y se unen dando lugar al retículo cristalino. Sin embargo, las impurezas solubles permanecen en disolución ya que no están lo suficientemente concentradas como para saturar la disolución y cristalizar. Los cristales obtenidos se recogen por filtración, separándose así de las aguas madres, se lavan varias veces con el mismo disolvente frío para eliminar las impurezas adheridas a la superficie, y 1 LABORATORIO DE QUÍMICA FACULTAD DE FARMACIA finalmente se secan. Si después de cristalizar no se obtiene el sólido con la pureza deseada, el proceso puede repetirse empleando el mismo u otro disolvente. La cristalización idónea es aquella que tiene lugar lentamente, ya que conduce a cristales muy puros. Si el enfriamiento de la disolución se realiza muy rápidamente se puede producir la formación de un sólido amorfo, en lugar de un sólido cristalino, que puede incluir impurezas. Impureza soluble Impureza insoluble AÑADIR DISOLVENTE (temperatura ambiente) disolvente CALENTAR (punto de ebullición del disolvente) Disolución transparente Compuesto a cristalizar e impurezas solubles FILTRAR EN CALIENTE ENFRIAR Y CRISTALIZAR (Tª ambiente) Impureza insoluble + FILTRAR En disolución: Impurezas solubles y sólido que aún no ha cristalizado En disolución: Compuesto a cristalizar e Impurezas solubles Impureza insoluble AGUAS MADRES En disolución: impurezas solubles y una pequeña cantidad de sólido que permanece disuelto Sólido cristalino SÓLIDO CRISTALIZADO LAVAR Y SECAR LOS CRISTALES Figura 2 1. Elección del disolvente. En los procedimientos descritos para la preparación de un producto, generalmente se especifica qué disolvente es el adecuado para cristalizar. Si no se dispone de ese dato, la elección del disolvente es el primer problema que se plantea. El éxito de la cristalización está condicionado a la elección del disolvente apropiado. 2 LABORATORIO DE QUÍMICA FACULTAD DE FARMACIA Disolventes de uso más frecuente para cristalización Disolvente p.e. (ºC) Agua 100 Metanol 65 Etanol 78 Acetato de etilo 56 Tolueno 111 Hexano 69 El disolvente ideal para cristalizar es aquel que cumple los siguientes requisitos: 1. Disolver el sólido a purificar en caliente (a la temperatura del punto de ebullición del disolvente). Un disolvente que disuelva el sólido en frío no es válido para cristalizar. 2. Disolver muy mal o muy bien a las impurezas para que puedan eliminarse al filtrar en caliente o quedar disueltas en las aguas madres, respectivamente. 3. No reaccionar con el compuesto a cristalizar. 4. Ser relativamente volátil con el fin de que los cristales obtenidos puedan secarse con facilidad. 5. No ser tóxico. A la hora de decidir en qué disolvente probar, la primera regla a considerar es que semejante disuelve a semejante, es decir, un disolvente disolverá mejor aquellos compuestos que presentes una estructura química similar a la suya. 2. Procedimiento experimental A) Adición de disolvente. Cuando el disolvente que se va a emplear es agua o etanol, colocar el compuesto a cristalizar en un erlenmeyer. Éste es el recipiente idóneo ya que tiene el fondo plano y una boca de tamaño pequeño. No utilizar un vaso de precipitados, ya que al calentar se favorecería la evaporación rápida del disolvente. Si se va a utilizar otro disolvente distinto a la agua o al etanol, se debe utilizar como recipiente de cristalización un matraz al que se le adapta un refrigerante de reflujo. Añadir la cantidad de disolvente necesaria para cubrir el sólido e introducir un par de trozos de porcelana porosa. Ésta no debe añadirse mientras se está calentando en las 3 LABORATORIO DE QUÍMICA FACULTAD DE FARMACIA proximidades del punto de ebullición del disolvente, ya que éste podría proyectarse al exterior. B) Disolución en caliente del sólido a cristalizar. Calentar la mezcla anterior hasta ebullición del disolvente, utilizando para ello una placa eléctrica. Agitar continuamente el erlenmeyer para favorecer la disolución del sólido. Mientras se calienta a ebullición con agitación constante, añadir gradualmente más disolvente hasta que el sólido se disuelva completamente. Si después de añadir una cantidad adicional de disolvente y calentar a ebullición sigue sin disolverse una parte, hay que tener en cuenta que podría tratarse de impurezas insolubles. Si se adiciona exceso de disolvente, la disolución no estará saturada, y puede ocurrir que, después de enfriar, no se produzca la separación de cristales. C) Filtración en caliente de las impurezas insolubles. El método para eliminar las impurezas insolubles consiste en filtrar la disolución caliente por gravedad utilizando un embudo cónico y un filtro de pliegues. Figura 3. D) Enfriamiento y cristalización. Dejar que la disolución se enfríe lentamente sin mover el erlenmeyer. Si una vez alcanzada la temperatura ambiente el sólido no ha cristalizado, a veces resultan útiles los siguientes consejos: - Enfriar la disolución en un baño de hielo. 4 LABORATORIO DE QUÍMICA FACULTAD DE FARMACIA - Rascar las paredes o el fondo del erlenmeyer con una espátula o una varilla de vidrio. - Añadir un cristal del compuesto que actúe como núcleo de cristalización (sembrado). E) Filtración de los cristales. Una vez que el sólido ha cristalizado, los cristales se separan de la disolución (aguas madres) filtrando a presión reducida con una trompa de agua, utilizando un kitasato y un embudo Büchner provisto de un filtro de papel. Grifo de agua Embudo Büchner Agua a presión Kitasato Frasco de seguridad Trompa de vacío desagüe Figura 4. F) Lavado y secado de los cristales. Lavar varias veces los cristales contenidos en el Büchner con el mismo disolvente, en el que se ha llevado a cabo la cristalización, previamente enfriado. Finalmente los cristales recogidos se pasan a un cristalizador y se dejan secar al aire o a vacío. 5 LABORATORIO DE QUÍMICA FACULTAD DE FARMACIA PUNTO DE FUSIÓN. El punto de fusión de un sólido cristalino es la temperatura del cambio de estado de sólido a líquido, a la presión atmosférica. Su determinación se realiza con los siguientes fines: a) Caracterización de sólidos. El punto de fusión, igual que el punto de ebullición, es función de la presión externa. Sin embargo, al contrario de lo que ocurre con el punto de ebullición, las fluctuaciones moderadas en torno a la presión atmosférica tienen un efecto muy poco pronunciado sobre el punto de fusión, por lo que no se consideran desde el punto de vista práctico. Por ello el punto de fusión constituye una constante física característica de los sólidos cristalinos puros que puede permitir su caracterización. b) Determinación cualitativa del grado de pureza de un sólido. El punto de fusión de un compuesto desciende notablemente con la presencia de impurezas, por lo que una disminución en el valor determinado experimentalmente con respecto al valor teórico, es indicativo de que el sólido no está puro. Además, un compuesto puro funde en un intervalo de 1-2 ºC, mientras que este intervalo aumente al existir impurezas. Procedimiento experimental. Se introduce una pequeña cantidad del sólido al cual se le va a medir su punto de fusión en un capilar de vidrio que tiene un extremo cerrado (hasta una altura de aproximadamente 50 mm). Los aparatos para medir el punto de fusión están provistos de un visor con luz y una lupa, además de un termómetro. El capilar de vidrio se dispone en vertical, con su extremo cerrado a la altura adecuada respecto al termómetro. El punto de fusión debe expresarse sin decimales, considerando todo el intervalo, e indicando entre paréntesis el disolvente empleado en la cristalización del sólido, por ejemplo, p.f. 150-152 ºC (etanol). La determinación rigurosa del punto de fusión requiere que el termómetro que se emplee esté debidamente calibrado. Este aspecto suele ignorarse en la práctica habitual. 6 LABORATORIO DE QUÍMICA FACULTAD DE FARMACIA CUESTIONES: 1) En el proceso de recristalización se efectúan dos filtraciones ¿En qué se diferencian? ¿Qué tipo de impurezas se eliminan en cada una de ellas? 2) ¿Por qué es conveniente lavar el sólido cristalizado con disolvente puro después de la segunda filtración? ¿Con qué disolvente se lava? ¿Es necesario que este disolvente para lavar se encuentre a ebullición? 3) Cuando se filtra un sólido con succión ¿Por qué se debe interrumpir siempre la succión antes de cerrar la trompa de agua? 7