Guia semanal unidad Q.2 - IntraEdu
Anuncio

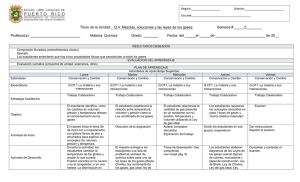
Región: __________________ Distrito: ________________________ Escuela: ____________________________________ Título de la Unidad: Q.2.El concepto del átomo y la tabla periódica Profesor(a): Materia: Química Grado: ______ Semana #: 1 de 6 Fecha: del _____ al _____ de _____________________ de 20__ RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a reformular el modelo moderno sobre la estructura del átomo. CD2 El trabajo de muchos científicos ha llevado al descubrimiento de las partículas subatómicas. CD3 La estructura de un átomo está organizada de una manera característica. EVALUACION DEL APRENDIZAJE Evaluación sumativa: PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: Lunes Martes Miércoles Estándares Estructura y niveles de Estructura y niveles de Estructura y niveles de organización de la materia organización de la materia organización de la materia Jueves Estructura y niveles de organización de la materia Viernes Estructura y niveles de organización de la materia Expectativas Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.1 ES.Q.CF1.EM.2 Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.1 ES.Q.CF1.EM.2 Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.1 ES.Q.CF1.EM.2 Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.1 ES.Q.CF1.EM.2 Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.1 ES.Q.CF1.EM.2 Estrategia Académica Aprendizaje Cooperativo Aprendizaje Cooperativo Ciclos de Aprendizaje Aprendizaje cooperativo Aprendizaje Cooperativo Mediante la construcción de un péndulo electrostático, el estudiante investigará satisfactoriamente sobre la relación entre el comportamiento del péndulo y la naturaleza eléctrica de la materia (existencia de los electrones). Al construir un afiche de un modelo de un átomo, el estudiante contrastará correctamente las diferencias de los modelos atómicos a través de los años. Mediante un diagrama conceptual, el estudiante describirá correctamente la estructura del átomo, incluida la ubicación de las partículas subatómicas. Con la creación de un afiche, el estudiante explicará correctamente otras partículas elementales del átomo. Luego de analizar el artículo “Encuentro de la partícula de Dios”, el estudiante argumentará a favor o en contra de los planteamientos que hacen los científicos a base de evidencia confiable. El maestro, con la ayuda de los estudiantes, hará un torbellino de ideas sobre el concepto: péndulo electrostático. El maestro dará una breve introducción sobre las primeras teorías acerca de la materia. Utilice el proyector para presentar la transparencia 14. Pida a los estudiantes que respondan las preguntas incluidas en ella. Repaso de la clase anterior sobre las partículas subatómicas. Entregar a cada estudiante una fotocopia del diagrama CDA donde contestarán lo que Conocen (C) y Desean (D) Objetivo Actividad de Inicio RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a reformular el modelo moderno sobre la estructura del átomo. CD2 El trabajo de muchos científicos ha llevado al descubrimiento de las partículas subatómicas. CD3 La estructura de un átomo está organizada de una manera característica. EVALUACION DEL APRENDIZAJE Evaluación sumativa: PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: Actividad de Desarrollo Actividad de Cierre Avalúos Formativos - Otras Formar grupos de 3 a 4 estudiantes y cada grupo construye y prueba un péndulo electrostático utilizando papel de aluminio, hilo, un globo, un soporte para colgar el péndulo y un paño de lana o un material apropiado para frotar el globo. Frotan el globo con el paño de lana y lo acercan al péndulo. Harán observaciones del funcionamiento del péndulo construido. Nota: Para más información del péndulo electrostático ir a la sección de recursos adicionales en el mapa curricular, página 21. Divida la clase en grupos y asigne uno de los siguientes científicos a cada grupo: John Dalton, Ernst Rutherford, JJ. Thomsom, Niels Bohr, o Erwin Schrӧdinger. Cada grupo diseñará un afiche del modelo de un átomo creado por su científico, el año en que el modelo fue introducido, el o los experimentos que condujeron a su formulación, etc. Nota: Los estudiantes usarán el libro de texto en el capítulo 4. Discusión socializada el comportamiento del péndulo y la naturaleza eléctrica de la materia (existencia de los electrones). Pegar los afiches en la pizarra y realizar una discusión para contrastar las diferencias de los modelos atómicos a través de los años. Crear rúbrica Crear rúbrica Discusión de la sección 4.2 de la página 92 del libro de texto. Los estudiantes trabajarán en grupos para crear un afiche sobre otras partículas elementales en el átomo como el bosón, positrón, fermión, neutrino, hadrón, leptón, quark y el mesón. Nota: El maestro puede tener la información para cada grupo o asignarla en la clase 3. aprender sobre la partícula de Dios. Luego, algunos estudiantes voluntariamente informarán lo escrito. Los estudiantes leen, comprenden y analizan el artículo “Encuentro de la partícula de Dios”. Formulan argumentos a favor o en contra de los planteamientos que hacen los científicos a base de evidencia confiable y debaten su postura con los demás compañeros de la clase (ver anejo Q.2 “Actividad de aprendizaje: Encuentro de la partícula de Dios”) Cada estudiante completará el diagrama conceptual del libro de texto (ejercicio 28, página 112). Diagrama conceptual Dos representantes de cada grupo presentarán el afiche y se genera una discusión socializada. Para demostrar el conocimiento adquirido en la clase, el estudiante completará la parte final del diagrama CDA. Discusión del mismo y entregar al maestro. Diagrama CDA RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a reformular el modelo moderno sobre la estructura del átomo. CD2 El trabajo de muchos científicos ha llevado al descubrimiento de las partículas subatómicas. CD3 La estructura de un átomo está organizada de una manera característica. EVALUACION DEL APRENDIZAJE Evaluación sumativa: PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: evidencias Materiales papel de aluminio, hilo, un globo, un soporte para colgar el péndulo y un paño de lana o un material apropiado para frotar el globo Traer marcadores de colores y/o crayolas para la clase 2. Asignación Estrategias de instrucción diferenciada ___ Educación Especial ___ LSP’ ___ Sección 504 ___ Dotados Reflexión de la Praxis Guía del maestro y Libro de texto: Química: Materia y Cambio Cartulinas, marcadores de colores, regla métrica y cinta adhesiva Guía del maestro y Libro de texto: Química: Materia y Cambio Proyector vertical Transparencia 13 Cada grupo buscará información sobre otras partículas elementales en el átomo como el bosón, positrón, fermión, neutrino, hadrón, leptón, quark y el mesón. Nota: Asignar uno específico a cada grupo. Guía del maestro y Libro de texto: Química: Materia y Cambio Cartulinas, marcadores de colores, regla métrica y cinta adhesiva Fotocopias del anejo Q.2 “Actividad de aprendizaje : Encuentro de la partícula de Dios” Copias en blanco del diagrama CDA Región: __________________ Distrito: ________________________ Escuela: ____________________________________ Título de la Unidad: Q.2.El concepto del átomo y la tabla periódica Profesor(a): Materia: Química Grado: ______ Semana #: 2 de 6 Fecha: del _____ al _____ de _____________________ de 20__ RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a reformular el modelo moderno sobre la estructura del átomo. CD2 El trabajo de muchos científicos ha llevado al descubrimiento de las partículas subatómicas. CD3 La estructura de un átomo está organizada de una manera característica. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Tarea de desempeño y prueba corta PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: Lunes Martes Miércoles Estándares Estructura y niveles de Estructura y niveles de Estructura y niveles de organización de la materia organización de la materia organización de la materia Expectativas Estrategia Académica Objetivo Jueves Estructura y niveles de organización de la materia Viernes Estructura y niveles de organización de la materia Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.1 ES.Q.CF1.EM.2 Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.1 ES.Q.CF1.EM.2 Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.3 ES.Q.CF1.EM.3 ES.Q.CF1.EM.3 Aprendizaje Cooperativo Ciclos de Aprendizaje Ciclos de Aprendizaje Aprendizaje Cooperativo Aprendizaje Cooperativo Al finalizar la actividad de la caja negra atómica, el estudiante comparará y contrastará correctamente los hallazgos sobre la estructura del átomo que explica la existencia de los diferentes elementos. Mediante la redacción de informe escrito, el estudiante explicará correctamente la utilidad de un modelo atómico en el tiempo que se introdujo, si fue descartado por nuevos modelos y las limitaciones que tiene ese modelo. Al terminar la lección, el estudiante: explicará correctamente el papel del número atómico para determinar la identidad de un átomo. Explicará correctamente el significado del concepto isótopo y sus aplicaciones. calculará correctamente Mediante una presentación oral, el estudiante explicará la formación de los isótopos de un elemento en particular y su aplicación en la medicina, la industria, entre otros. A través de la actividad “Laboratorio del centavo isotópico”, el estudiante investigará y calculará satisfactoriamente la abundancia relativa de los isótopos (centavos). RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a reformular el modelo moderno sobre la estructura del átomo. CD2 El trabajo de muchos científicos ha llevado al descubrimiento de las partículas subatómicas. CD3 La estructura de un átomo está organizada de una manera característica. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Tarea de desempeño y prueba corta PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: el número de electrones, protones y neutrones de un átomo a partir de su número atómico y su masa. Repaso de la estructura del El maestro repasará las partes Utilice el proyector para átomo. que debe tener el informe escrito. presentar la transparencia 15. Actividad de Inicio Pida a los estudiantes que respondan las preguntas incluidas en ella. Los estudiantes trabajarán en Los estudiantes escribirán un Discusión de la sección 4.3: grupos pequeños. Cada grupo informe de dos páginas sobre el Cómo se diferencian los recibirá una caja negra. Cada modelo asignado. El informe átomos (libro de texto, páginas caja negra contiene un objeto que debe incluir: 98 – 104) representa un átomo de un Lo útil que fue su modelo elemento distinto. El maestro en el tiempo que se prepara estos objetos utilizando introdujo. los mismos materiales para cada Si su uso fue descartado uno, por ejemplo las canicas en el según surgieron modelos Actividad de Desarrollo centro representan el núcleo nuevos. denso, envueltas con una bola Las limitaciones que tiene suelta de hilo. El tamaño de la el modelo. bola de hilo puede variar dependiendo del tamaño del átomo del elemento. Objetos pequeños (como habichuelas secas o cuentas para hacer collares) pueden intercalarse en la bola de hilo para representar a Repaso de la clase anterior, enfatizando el concepto de isótopo. Repasar el concepto de masa de átomos individuales (libro d texto, página 102). Los estudiantes trabajan en grupo para investigar sobre los isótopos de un elemento en particular que se les asignará, y sus aplicaciones en la medicina, la industria, la agricultura, el fechado de materiales, entre otros. Los estudiantes (formar grupos de 3 a 4 estudiantes) recibirán una mezcla de centavos que representarán la mezcla natural de dos isótopos del elemento imaginario “centavium”. Con los centavos, los estudiantes simularán una de las maneras en que los científicos pueden determinar las cantidades relativas de los isótopos presentes en una muestra de un elemento (ver anejo: “Q.2 Tarea de desempeño – Laboratorio del centavo isotópico”). Prepararán un informe oral de 2 minutos para presentar sus hallazgos a la clase. cálculos y las respuestas a las preguntas al final del RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a reformular el modelo moderno sobre la estructura del átomo. CD2 El trabajo de muchos científicos ha llevado al descubrimiento de las partículas subatómicas. CD3 La estructura de un átomo está organizada de una manera característica. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Tarea de desempeño y prueba corta PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: los electrones. (Alternativamente, el maestro puede preparar los átomos al intercalar canicas, habichuelas, etc., en gelatina, lo cual puede ser más fácil para que los estudiantes “experimenten”). Los estudiantes describirán átomo de ese elemento sin mirarlo, dibujarán un modelo de sus hallazgos y participarán en una discusión con la clase. Nota: El maestro evaluará a los estudiantes a base de las observaciones que anotaron, los dibujos de los modelos y sus discusiones sobre cómo esto se relaciona a la existencia de diferentes elementos. Discusión en clase de cada grupo El maestro dirige una discusión Discusión, oralmente, de los para comparar y contrastar los breve sobre los hallazgos de ejercicios (problemas hallazgos de los distintos grupos, cada modelo atómico. complementarios) 11 al 14 del Actividad de Cierre para desarrollar una teoría sobre libro de texto. la estructura del átomo que explica la existencia de los diferentes elementos. Avalúos Formativos - Otras evidencias Crear rúbrica Crear rúbrica Prueba corta laboratorio. Presentación de cada grupo a la clase sobre los hallazgos. Crear rúbrica Discusión, oralmente, de las preguntas del anejo. Crear rúbrica RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a reformular el modelo moderno sobre la estructura del átomo. CD2 El trabajo de muchos científicos ha llevado al descubrimiento de las partículas subatómicas. CD3 La estructura de un átomo está organizada de una manera característica. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Tarea de desempeño y prueba corta PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: Caja negra, hilo y objetos Guía del maestro y Libro de texto: Guía del maestro y Libro de Química: Materia y Cambio texto: Química: Materia y pequeños (canicas o Cambio habichuelas) Cartulinas, marcadores de Nota: La cantidad de materiales colores, regla métrica y cinta Proyector vertical Materiales dependerá de los grupos adhesiva Transparencia 15 (Teaching formados. Transparency 15 and Master) Calculadora científica Asignar a cada estudiante un Estudiar para prueba corta de la Cada estudiante buscará modelo atómico para buscar estructura atómica. información sobre un isótopo información sobre ese modelo. en particular. Ejemplos: H, C, K, Co, Au, I, P, Asignación Cl y Mg. Nota: Asignar el mismo isótopo a 2 o 3 estudiantes. Estos serán los grupos formados para la clase 4. Estrategias de instrucción diferenciada ___ Educación Especial ___ LSP’ ___ Sección 504 ___ Dotados Reflexión de la Praxis Libro de texto: Química: Materia y Cambio Traer tres (3) centavos de antes de 1982 y tres (3) centavos con fecha posterior a 1982. Nota: Los centavos en el sobre sellado le corresponde al maestro. Copias del anejo: “Q.2 Tarea de desempeño – Laboratorio del centavo isotópico”. Centavos de antes y después de 1982 Calculadora científica balanza Región: __________________ Distrito: ________________________ Escuela: ____________________________________ Título de la Unidad: Q.2.El concepto del átomo y la tabla periódica Profesor(a): Materia: Química Grado: ______ Semana #: 3 de 6 Fecha: del _____ al _____ de _____________________ de 20__ RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a CD5 Los átomos de los elementos tienen una estructura y propiedades que les permiten reformular el modelo moderno sobre la estructura del átomo. interactuar para formar diferentes tipos de compuestos químicos. CD3 La estructura de un átomo está organizada de una manera característica. CD4 La identificación sistemática y la caracterización de los elementos químicos y sus interacciones comenzaron con el trabajo de Antoine Lavoisier. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Examen PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: Lunes Martes Miércoles Jueves Viernes Estándares Estructura y niveles de Estructura y niveles de Estructura y niveles de Estructura y niveles de Estructura y niveles de organización de la materia organización de la materia organización de la materia organización de la materia organización de la materia Expectativas Estrategia Académica Objetivo Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.4 ES.Q.CF1.EM.4 ES.Q.CF1.EM.1, ES.Q.CF1.EM.2 ES.Q.CF1.EM.3, ES.Q.CF1.EM.4 ES.Q.CF1.EM.3 ES.Q.CF1.EM.3 ECA ECA ECA Ciclos de Aprendizaje Ciclos de Aprendizaje Después de estudiar los núcleos inestables y desintegración radiactiva, el estudiante analizará satisfactoriamente por qué los núcleos de los átomos de varios elementos son radiactivos. A través de un diagrama de Venn, el estudiante comparará y contrastará correctamente lo que ocurre en una reacción de fusión y en una reacción de fisión. Durante el examen, el estudiante demostrará satisfactoriamente los conocimientos adquiridos sobre la estructura atómica. Mediante el diseño de una línea cronológica, el estudiante comprenderá la organización periódica de los elementos y la estructura de la tabla periódica. Luego de la discusión del tema, el estudiante: Reconocerá correctamente que la Tabla Periódica es adaptada por un acuerdo internacional para clasificar los elementos y que es idéntica en todos los idiomas. Identificará RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a CD5 Los átomos de los elementos tienen una estructura y propiedades que les permiten reformular el modelo moderno sobre la estructura del átomo. interactuar para formar diferentes tipos de compuestos químicos. CD3 La estructura de un átomo está organizada de una manera característica. CD4 La identificación sistemática y la caracterización de los elementos químicos y sus interacciones comenzaron con el trabajo de Antoine Lavoisier. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Examen PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: correctamente el origen fundamental de los nombres de los elementos y las reglas de la Unión Internacional de la Química Pura y Aplicada (IUPAC, por sus siglas en inglés) para asignar nombres y símbolos. Utilice el proyector para presentar Utilice el proyector para presentar Ofrecer las instrucciones del Utilice el proyector para Repaso de la clase anterior. examen. la transparencia 16. Pida a los la transparencia 99. Pida a los presentar la transparencia 20. Utilizar la actividad de estudiantes que respondan las estudiantes que respondan las Pida a los estudiantes que diversidad cultural (Guía del Actividad de Inicio preguntas incluidas en ella. preguntas incluidas en ella. respondan las preguntas maestro, página 154) incluidas en ella. Discusión de la sección 4.4: Discusión de la sección 25.4: Los estudiantes contestarán el Discusión de la sección 6.1: Discusión socializada sobre la núcleos inestables y fisión y fusión de núcleos examen. Desarrollo de la tabla periódica organización IUPAC y cómo la desintegración radiactiva del libro atómicos (libro de texto, páginas moderna (libro de texto, organización establece reglas de texto en las páginas 105 -107. 821 – 826). páginas 151 – 158). para determinar los nombres de Actividad de Desarrollo los elementos en la tabla Nota: La discusión se puede periódica y para los nuevos ampliar con las secciones 25.1 y elementos que aún no han sido 25.2 del libro de texto en las descubiertos. páginas 805 – 813. Discusión de los ejercicios 23 y Utilizando un diagrama de Venn Recoger el examen. Los estudiantes crearán una Discusión del ejercicio 6 de la Actividad de Cierre 24 de la página 107 del libro de se establecen las semejanzas y línea cronológica sobre el página 158 del libro de texto. texto. diferencias entre las reacciones desarrollo de la tabla periódica RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a CD5 Los átomos de los elementos tienen una estructura y propiedades que les permiten reformular el modelo moderno sobre la estructura del átomo. interactuar para formar diferentes tipos de compuestos químicos. CD3 La estructura de un átomo está organizada de una manera característica. CD4 La identificación sistemática y la caracterización de los elementos químicos y sus interacciones comenzaron con el trabajo de Antoine Lavoisier. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Examen PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: de fusión nuclear y fusión con la contribución de los Nota: Dar instrucciones para la nuclear, respecto de las científicos como: Dobereiner, presentación de la clase 1, partículas involucradas y los Newlands, Moseley y semana 4 (ver punto número 4 cambios que experimentan. Mendeleev. del mapa curricular, página 14. Avalúos Formativos - Otras evidencias Materiales Diagrama de Venn Guía del maestro y Libro de texto: Química: Materia y Cambio Proyector vertical Transparencia 16 (Teaching Transparency 16 and Master) Guía del maestro y Libro de texto: Química: Materia y Cambio Proyector vertical Transparencia 99 (Teaching Transparency 99 and Master) Hacer un diagrama o modelo de las reacciones de fusión en el Sol y las reacciones de fisión para producir energía eléctrica en las centrales nucleares. Asignación Copias del examen Opcional: tabla periódicas y calculadora científica Guía del maestro y Libro de texto: Química: Materia y Cambio Proyector vertical Transparencia 20 (Teaching Transparency 20 and Master) Guía del maestro y Libro de texto: Química: Materia y Cambio Los estudiantes investigarán la organización IUPAC y cómo la organización establece reglas para determinar los nombres de los elementos en la tabla periódica y para los nuevos elementos que aún no han sido descubiertos. A grupos de tres estudiantes se le asignará un elemento para que construya un móvil para representarlo. El móvil (mobile) debe incluir usos y aplicaciones prácticas del elemento, una muestra u objeto hecho del elemento o una imagen que lo represente. Los móviles se exhibirán en el salón y cada estudiante debe explicarlo y proveer información sobre su elemento (ver ejemplos en el RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD1 Muchos hallazgos científicos respaldados por los avances tecnológicos han llevado a CD5 Los átomos de los elementos tienen una estructura y propiedades que les permiten reformular el modelo moderno sobre la estructura del átomo. interactuar para formar diferentes tipos de compuestos químicos. CD3 La estructura de un átomo está organizada de una manera característica. CD4 La identificación sistemática y la caracterización de los elementos químicos y sus interacciones comenzaron con el trabajo de Antoine Lavoisier. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Examen PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: enlace en la sección “Recursos adicionales”). Estrategias de instrucción diferenciada ___ Educación Especial ___ LSP’ ___ Sección 504 ___ Dotados Reflexión de la Praxis Región: __________________ Distrito: ________________________ Escuela: ____________________________________ Título de la Unidad: Q.2.El concepto del átomo y la tabla periódica Profesor(a): Materia: Química Grado: ______ Semana #: 4 de 6 Fecha: del _____ al _____ de _____________________ de 20__ RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD4 La identificación sistemática y la caracterización de los elementos químicos y sus CD5 Los átomos de los elementos tienen una estructura y propiedades que les permiten interacciones comenzaron con el trabajo de Antoine Lavoisier. interactuar para formar diferentes tipos de compuestos químicos. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Examen PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: Lunes Martes Miércoles Jueves Viernes Estándares Estructura y niveles de Estructura y niveles de Estructura y niveles de Estructura y niveles de Estructura y niveles de organización de la materia organización de la materia organización de la materia organización de la materia organización de la materia Expectativas Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.7 ES.Q.CF1.EM.8 ES.Q.CF1.EM.9 Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.7 ES.Q.CF1.EM.8 ES.Q.CF1.EM.9 Q.CF1: La materia y sus interacciones Aprendizaje cooperativo Aprendizaje cooperativo ECA ECA Al finalizar la presentación oral, el estudiante explicará correctamente la construcción de un móvil y sus aplicaciones prácticas. Al terminar la clase, el estudiante describirá correctamente los usos prácticos y las aplicaciones tecnológicas de varios elementos (metales, no metales, metaloides, gases inertes). Haciendo uso de la tabla periódica, el estudiante comparará satisfactoriamente las tendencias de periodo y grupo de varias propiedades. Mediante la creación de un plegable, el estudiante explicará correctamente las tendencias periódicas (radio atómico, electronegatividad, energía de ionización y reactividad). El maestro dará una breve introducción sobre las presentaciones. Utilice la fotografía de la página 178 de la guía del maestro. Utilice el proyector para presentar la transparencia 22. Pida a los estudiantes que respondan las preguntas incluidas en ella. Repaso de la clase anterior sobre las tendencias periódicas. ES.Q.CF1.EM.6 Estrategia Académica Objetivo Actividad de Inicio ES.Q.CF1.EM.10 Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.1, ES.Q.CF1.EM.3, ES.Q.CF1.EM.6, ES.Q.CF1.EM.8, ES.Q.CF1.EM.2 ES.Q.CF1.EM.4 ES.Q.CF1.EM.7 ES.Q.CF1.EM.9 ECA Durante el examen, el estudiante demostrará satisfactoriamente los conocimientos adquiridos sobre el desarrollo de la tabla periódica, clasificación de los elementos y tendencias periódicas. Ofrecer las instrucciones del examen. RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD4 La identificación sistemática y la caracterización de los elementos químicos y sus CD5 Los átomos de los elementos tienen una estructura y propiedades que les permiten interacciones comenzaron con el trabajo de Antoine Lavoisier. interactuar para formar diferentes tipos de compuestos químicos. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Examen PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: Cada grupo presentará, Divida la clase en pequeños Discusión de la sección 6.3: Los estudiantes crearán un Los estudiantes contestarán el oralmente, el móvil (mobile) que grupos y asígneles un grupo o tendencias periódicas (libro de plegable de cuatro lados que examen. debe incluir usos y aplicaciones familia de la tabla periódica para texto, páginas 163 – 169) muestre las tendencias prácticas del elemento, una determinar los usos prácticos y periódicas. Este plegable muestra u objeto hecho del las aplicaciones tecnológicas de consiste en una hoja de papel elemento o una imagen que lo varios elementos de ese grupo. doblado en cuatro partes, de represente. Los móviles se Nota: Utilizar el capítulo 7 del manera que haya cuatro exhibirán en el salón y cada libro de texto. pestañas que se puedan abrir y Actividad de Desarrollo estudiante debe explicarlo y cerrar. Seguir las instrucciones proveer información sobre su del mapa curricular en las elemento (ver ejemplos en el páginas 17 – 18. enlace en la sección “Recursos adicionales”). Nota: Ver la sección de Nota: La presentación por grupo recursos adicionales para debe ser de aproximadamente información de los plegables y dos minutos. tendencias periódicas. Discusión socializada sobre las Un representante de cada grupo Discusión del ejercicio 19 del Voluntariamente, algunos Recoger el examen. Actividad de Cierre aplicaciones de los móviles en el presentará los hallazgos. libro de texto en la página 169. estudiantes, presentarán su diario vivir. plegable a la clase. Avalúos Formativos - Otras evidencias Crear rúbrica Copias de la rúbrica Materiales Crear rúbrica Guía del maestro y Libro de texto: Química: Materia y Cambio Crear rúbrica Guía del maestro y Libro de texto: Química: Materia y Cambio Tabla periódica Proyector vertical Transparencia 22 (Teaching Transparency 22 and Master) Guía del maestro y Libro de texto: Química: Materia y Cambio Papeles de colores Marcadores de colores Copias del examen tabla periódica RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD4 La identificación sistemática y la caracterización de los elementos químicos y sus CD5 Los átomos de los elementos tienen una estructura y propiedades que les permiten interacciones comenzaron con el trabajo de Antoine Lavoisier. interactuar para formar diferentes tipos de compuestos químicos. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Examen PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: Estudiar para examen en la Estudiar para examen en la Asignación clase 5. clase 5. Estrategias de instrucción diferenciada ___ Educación Especial ___ LSP’ ___ Sección 504 ___ Dotados Reflexión de la Praxis Región: __________________ Distrito: ________________________ Escuela: ____________________________________ Título de la Unidad: Q.2.El concepto del átomo y la tabla periódica Profesor(a): Materia: Química Grado: ______ Semana #: 5 de 6 Fecha: del _____ al _____ de _____________________ de 20__ RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD3 La estructura de un átomo está organizada de una manera característica. CD4 La identificación sistemática y la caracterización de los elementos químicos y sus interacciones comenzaron con el trabajo de Antoine Lavoisier. EVALUACION DEL APRENDIZAJE Evaluación sumativa: Estándares Expectativas Estrategia Académica Objetivo Actividad de Inicio Actividad de Desarrollo Lunes Estructura y niveles de organización de la materia PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: Martes Miércoles Estructura y niveles de Estructura y niveles de organización de la materia organización de la materia Jueves Estructura y niveles de organización de la materia Viernes Estructura y niveles de organización de la materia Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.5 ES.Q.CF1.EM.5 ES.Q.CF1.EM.5 ES.Q.CF1.EM.5 ES.Q.CF1.EM.5 Ciclos de aprendizaje Ciclos de aprendizaje Ciclos de aprendizaje Ciclos de aprendizaje Ciclos de aprendizaje Al terminar la lección, el estudiante comparará correctamente el modelo atómico de Bohr y el modelo mecánico cuántico del átomo. Mediante un organizador gráfico, el estudiante describirá correctamente el principio de Aufbau, el principio de exclusión de Pauli y la regla de Hund para representar configuraciones electrónicas usando diagramas de orbital. Utilice el proyector para presentar la transparencia 18. Pida a los estudiantes que respondan las preguntas incluidas en ella. Discusión de la sección 5.2: La teoría cuántica y el átomo (libro de texto, páginas 127 – 134). Utilice el proyector para presentar la transparencia 19. Pida a los estudiantes que respondan las preguntas incluidas en ella. Discusión de la sección 5.3: Configuraciones electrónicas (libro de texto, páginas 135 – Utilizando la regla diagonal, el estudiante aplicará correctamente el principio de Aufbau, el principio de exclusión de Pauli y la regla de Hund para representar configuraciones electrónicas usando la notación de la configuración electrónica. Repaso de la clase anterior enfatizando las reglas para representar las configuraciones electrónicas. Discusión de la sección 5.3: Configuraciones electrónicas (libro de texto, páginas 138 – Utilizando una hoja de trabajo (anejo), el estudiante identificará satisfactoriamente patrones para determinar el orden en que los electrones llenan los orbitales de un átomo. Utilizando como base el modelo mecánico cuántico del átomo, el estudiante escribirá e interpretará las estructuras de símbolos electrónicos que representan los electrones de valencia de un átomo. Repaso de la clase anterior enfatizando las reglas para representar las configuraciones electrónicas. Los estudiantes completarán una hoja de trabajo para cubrir patrones en la configuración de Repasar la notación de la configuración electrónica con la regla diagonal. Discusión del tema de estructuras de símbolos electrónicos (libro de texto, RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD3 La estructura de un átomo está organizada de una manera característica. CD4 La identificación sistemática y la caracterización de los elementos químicos y sus interacciones comenzaron con el trabajo de Antoine Lavoisier. EVALUACION DEL APRENDIZAJE Evaluación sumativa: 137). Actividad de Cierre Discusión de los ejercicios 16 y 17 de la página 134 del libro de texto. Avalúos Formativos - Otras evidencias Materiales PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: 139). Nota: En la discusión puede utilizar la actividad de Analogía del Aufbau (mapa curricular, páginas 23 – 24). Los estudiantes crearán un organizador gráfico para describir las reglas del Aufbau, incluyendo el principio de exclusión de Pauli y la regla de Hund. Discusión de los ejercicios 18 – 22 de la página 139 del libro de texto. Organizador gráfico Guía del maestro y Libro de texto: Química: Materia y Cambio Proyector vertical Transparencia 18 (Teaching Transparency 18 and Master) Guía del maestro y Libro de texto: Química: Materia y Cambio Proyector vertical Transparencia 19 (Teaching Transparency 19 and Master) Tablas periódicas Guía del maestro y Libro de texto: Química: Materia y Cambio Tablas periódicas electrones (ver anejo “Q.2 Otra Evidencia – Patrones en la configuración electrónica”). páginas 140 – 141). Discusión de la hoja de trabajo. Discusión del ejercicio 28 (interpretación de ilustraciones científicas) del libro de texto en la página 141. Q.2 Otra Evidencia Prueba corta Guía del maestro y Libro de texto: Química: Materia y Cambio Copias del anejo “Q.2 Otra Evidencia – Patrones en la configuración electrónica” Tablas periódicas Asignación Estrategias de instrucción diferenciada ___ Educación Especial ___ LSP’ ___ Sección 504 ___ Dotados Reflexión de la Praxis Estudiar para prueba corta en la clase 5. Estudiar para prueba corta en la clase 5. Guía del maestro y Libro de texto: Química: Materia y Cambio Tablas periódicas Región: __________________ Distrito: ________________________ Escuela: ____________________________________ Título de la Unidad: Q.2.El concepto del átomo y la tabla periódica Profesor(a): Materia: Química Grado: ______ Semana #: 6 de 6 Fecha: del _____ al _____ de _____________________ de 20__ RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD3 La estructura de un átomo está organizada de una manera característica. CD6 Los átomos de los elementos tienen una estructura y propiedades que les permiten interactuar para formar diferentes tipos de compuestos químicos. EVALUACION DEL APRENDIZAJE Evaluación sumativa: tarea de desempeño y examen Estándares Expectativas Estrategia Académica Objetivo Lunes Estructura y niveles de organización de la materia PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: Martes Miércoles Estructura y niveles de Estructura y niveles de organización de la materia organización de la materia Jueves Estructura y niveles de organización de la materia Viernes Estructura y niveles de organización de la materia Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.5 ES.Q.CF1.EM.10 ES.Q.CF1.EM.10 ES.Q.CF1.EM.10 Q.CF1: La materia y sus interacciones ES.Q.CF1.EM.5 ES.Q.CF1.EM.10 Aprendizaje cooperativo Ciclos de aprendizaje Aprendizaje cooperativo Aprendizaje cooperativo Ciclos de aprendizaje Mediante la creación de un conjunto de tarjetas, el estudiante describirá correctamente el nombre del elemento, su número atómico y su ubicación en la tabla periódica (periodo, familia), el diagrama de Lewis y la configuración electrónica de una lista de elementos asignados. Al terminar la lección, el estudiante: definirá correctamente enlace químico. describirá correctamente los tipos de enlaces químico y covalente. Al finalizar la actividad de aprendizaje – enlaces químicos, el estudiante identificará correctamente el número de electrones de valencia en un átomo dado. describirá y demostrará satisfactoriamente cómo se forma un enlace iónico y covalente. Predecirán Al terminar la actividad “Rompecabezas, sal y pimienta”, el estudiante representará satisfactoriamente la existencia de distintas fuerzas de atracción y disociación en los distintos tipos de enlaces químicos. Durante el examen, el estudiante demostrará satisfactoriamente los conocimientos adquiridos sobre RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD3 La estructura de un átomo está organizada de una manera característica. CD6 Los átomos de los elementos tienen una estructura y propiedades que les permiten interactuar para formar diferentes tipos de compuestos químicos. EVALUACION DEL APRENDIZAJE Evaluación sumativa: tarea de desempeño y examen Actividad de Inicio Actividad de Desarrollo Actividad de Cierre Repaso de la ubicación de un elemento en la tabla periódica, configuración electrónica y diagrama de Lewis. Luego, dar las instrucciones para la tarea de desempeño (mapa curricular, página 11). Los estudiantes trabajarán en grupo y se les asignará una lista de elementos, representativa de los periodos y grupos o familias en la tabla periódica. Cada grupo creará un conjunto de tarjetas. Un lado de la tarjeta tendrá el nombre del elemento, su número atómico y su ubicación en la tabla Periódica (periodo, familia). El lado opuesto tendrá el diagrama de Lewis y la configuración electrónica. Los estudiantes harán preguntas a sus compañeros sobre la identidad de los elementos asignados a base de la configuración electrónica y el PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: correctamente el tipo de enlace que se produce entre dos elementos. Demostración breve: Frote un Repaso de la clase anterior enfatizando la formación de globo con un pedazo de cuero. enlaces químicas y covalentes. Ponga el globo sobre la cabeza de un estudiante que tenga el cabello largo. El globo debe atraer el cabello. Pregunte a los estudiantes porqué ocurre esto. Discusión de la sección 8.1: Los estudiantes realizarán la formación de enlaces químicos actividad “Conceptos básicos: (libro de tetxo, páginas 211 – enlaces químicos” para 214). representar diferentes enlaces Enlace iónico – páginas 215 – y contrastar entre los mismos 220 (ver anejo "Q.2 Actividad de Enlace covalente – páginas 241 - aprendizaje –Enlaces 243 químicos”). Clasifica los siguientes compuestos como iónicos o covalentes. Para cada compuesto, indica cuáles elementos son metales y cuáles Discusión de la actividad enfatizando las preguntas del paso 9. Repaso de los conceptos de fuerzas de atracción y disociación en los distintos tipos de enlaces químicos Se les proveerá a los estudiantes dos rompecabezas, uno de piezas entrelazadas y otro con piezas de bordes planos. (Idealmente, los rompecabezas pueden estar hechos de materiales a prueba de agua). También se les proveerá a los estudiantes ejemplos de sal de mesa y pimienta negra, que también transferirán al contenedor de agua para luego mezclarlos (ver más detalles al final del mapa). El maestro evaluará a los estudiantes a base de las observaciones de que las piezas de bordes planos del rompecabezas se disocian, lo Ofrecer las instrucciones del examen. Recoger el examen. RESULTADOS DESEADOS Compresión Duradera (entendimientos claves) El estudiante comprenderá: CD3 La estructura de un átomo está organizada de una manera característica. CD6 Los átomos de los elementos tienen una estructura y propiedades que les permiten interactuar para formar diferentes tipos de compuestos químicos. EVALUACION DEL APRENDIZAJE Evaluación sumativa: tarea de desempeño y examen diagrama de Lewis. PLAN DE APRENDIZAJE Actividades de Aprendizaje Sugeridas: son no metales. KCl Glucosa (C6H12O6) H2 CO ICl Avalúos Formativos - Otras evidencias Materiales Asignación Estrategias de instrucción diferenciada ___ Educación Especial ___ LSP’ ___ Sección 504 ___ Dotados Reflexión de la Praxis Guía del maestro y Libro de texto: Química: Materia y Cambio Tablas periódicas Index card Marcadores de colores (opcional) Guía del maestro y Libro de texto: Química: Materia y Cambio Proyector vertical Globo Pedazo de cuero Asignar diferentes tipos de dulces a los estudiantes para la clase 3. Los dulces dependerán de las modificaciones de la actividad. cual es análogo a los enlaces débiles que mantienen juntos los compuestos iónicos, como la sal de mesa, que se disocian fácilmente en una solución acuosa. Crear rúbrica Crear rúbrica Guía del maestro y Libro de texto: Química: Materia y Cambio Tablas periódicas Copias del anejo "Q.2 Actividad de aprendizaje –Enlaces químicos” Para materiales de la actividad, leer las instrucciones del mapa curricular en las páginas 17 y 22 – 23. Copias del examen Tablas periódicas