neuralgia_del_trigemino
Anuncio
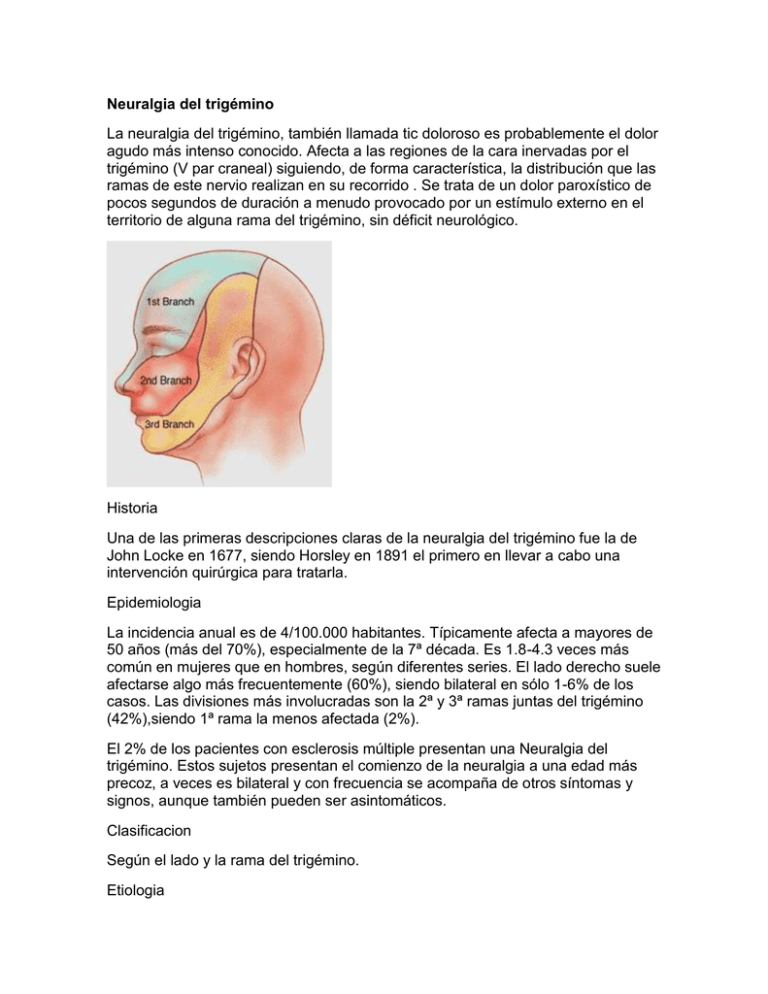
Neuralgia del trigémino La neuralgia del trigémino, también llamada tic doloroso es probablemente el dolor agudo más intenso conocido. Afecta a las regiones de la cara inervadas por el trigémino (V par craneal) siguiendo, de forma característica, la distribución que las ramas de este nervio realizan en su recorrido . Se trata de un dolor paroxístico de pocos segundos de duración a menudo provocado por un estímulo externo en el territorio de alguna rama del trigémino, sin déficit neurológico. Historia Una de las primeras descripciones claras de la neuralgia del trigémino fue la de John Locke en 1677, siendo Horsley en 1891 el primero en llevar a cabo una intervención quirúrgica para tratarla. Epidemiologia La incidencia anual es de 4/100.000 habitantes. Típicamente afecta a mayores de 50 años (más del 70%), especialmente de la 7ª década. Es 1.8-4.3 veces más común en mujeres que en hombres, según diferentes series. El lado derecho suele afectarse algo más frecuentemente (60%), siendo bilateral en sólo 1-6% de los casos. Las divisiones más involucradas son la 2ª y 3ª ramas juntas del trigémino (42%),siendo 1ª rama la menos afectada (2%). El 2% de los pacientes con esclerosis múltiple presentan una Neuralgia del trigémino. Estos sujetos presentan el comienzo de la neuralgia a una edad más precoz, a veces es bilateral y con frecuencia se acompaña de otros síntomas y signos, aunque también pueden ser asintomáticos. Clasificacion Según el lado y la rama del trigémino. Etiologia Probablemente se deba a una transmisión de las fibras A hacia las pobremente mielinizadas A delta y C. El origen de este cuadro clínico es desconocido. Pueden diferenciarse causas periféricas y centrales. Se ha relacionado con una irritación de la parte periférica del nervio trigémino por un vaso (arteria o vena, generalmente la arteria cerebelosa superior, arteria trigémina persistente o un tumor (menos del 0.8% del total de casos). Actualmente, la teoría de compresión vascular es la más aceptada y está ganando más adeptos. Se debería a una irritación pulsátil de dicho nervio a nivel de la unión de las partes periférica y central (zona de entrada de la raíz). Etiologías de la neuropatía trigeminal según la localización 1. Lesiones periféricas - Traumatismos: craneofaciales, fracturas de la base del cráneo, extracciones dentales - Patología infecciosa por proximidad: sinusitis, periodontitis - Tumores malignos primarios o metastásicos - Síndrome de la hendidura esfenoidal - Trombosis del seno cavernoso 2. Lesiones en el ganglio de Gasser - Herpes simple, zoster - Neurinoma del ganglio de Gasser 3. Lesiones a nivel de la raíz sensitiva - Vasculares: ramas aberrantes de la cerebelosa superior, loops, angiomas, aneurismas. - Tumorales: colesteatomas, meningiomas, neurinomas del acústico. 4. Lesiones a nivel de los núcleos centrales - Síndrome de Wallenberg - Tumor protuberancial o bulbar - Siringobulbia y siringomielia cervical - Esclerosis múltiple Clinica Dolor paroxístico de pocos segundos de duración a menudo provocado por un estímulo externo en el territorio de alguna rama del trigémino , sin déficit neurológico. Zonas de gatillo. Es característico de la NT que el enfermo localice zonas de gatillo en el territorio del trigémino donde ante determinados estímulos o movimientos se desencadene el dolor. En las NT que afectan a la región oral-auricular los estímulos habitualmente son motores como masticar, hablar, sonreír y con menos frecuencia los ataques se originan por estimulación sensitiva cutánea o sobre dientes y mucosa labial (ej. líquidos fríos o calientes). Cuando se trata del área nasal-periorbitaria las zonas gatillo se sitúan en las alas de la nariz, tercio externo del labio superior, canto interno del ojo, etc. y se desencadena la neuralgia por estímulos sensitivos cutáneos, cepillado de dientes, afeitado, sonarse... La severidad de los episodios viene determinada por su rapidez en reproducirse y ésta depende de la facilidad con que son desencadenados. Por este motivo, durante las crisis el paciente puede evitar cualquier gesticulación o contacto, incluso negarse a la anamnesis y exploración, lo cual constituye por sí sólo, un dato de interés. Será útil en estos casos la presencia de un acompañante para completar la historia clínica. Diagnostico El diagnóstico se basa fundamentalmente en la anamnesis (localización del dolor, momento del comienzo, desencadenantes, intervalos libres de dolor, medicación) y en la exploración física (evaluación sensitiva facial, reflejo corneal, evaluación de músculos masticadores). Siempre se debe explorar al enfermo buscando asimetrías y teniendo presente la distribución de las tres divisiones (oftálmica, maxilar y mandibular). Sensibilidad. Por lo expuesto, podemos deducir que el V par es un nervio de predominio sensitivo y la patología derivada del mismo se manifestará principalmente mediante alteraciones en dicha función. Hay que examinar todas las modalidades de sensibilidad ya que al ser distintos los núcleos propios de la térmica y dolorosa que los de la táctil, no es raro que lesiones centrales produzcan anestesias disociadas. Siempre se explorarán las mucosas, incluida la lingual. Es importante delimitar la región afectada: la anestesia del ángulo de la mandíbula corresponde al plexo cervical y no al trigémino; el signo de Roger es la hipoestesia o anestesia del mentón por neuropatía del n. mentoniano (rama terminal del n. mandibular); otras ramas sensitivas en cuyos puntos de emergencia se debe averiguar si existe dolor o un déficit sensitivo son el n. supraorbitario (rama del n. oftálmico) y el n. infraorbitario (rama del n. maxilar superior). Si existe una anestesia concéntrica como en bulbos de cebolla se descartará una patología central ya que la representación facial en los núcleos sigue esa distribución. El reflejo corneal se altera precozmente en las lesiones del trigémino de forma que en una afectación sensitiva de toda la cara con reflejo corneal íntegro, dudaremos la existencia de una lesión orgánica. Se explora tocando levemente la periferia de la córnea con un algodón mientras el sujeto mira hacia el otro lado. Se encuentra alterado si esto no provoca un cierre de los párpados o el paciente percibe menos estímulo que en el otro ojo. Hay que descartar que se trate de una lesión del nervio facial (VII par), encargado de la contracción palpebral. Movilidad. La función motora del V par se examina mediante los movimientos masticatorios de la mandíbula. En el cierre de la boca participan músculos muy potentes (maseteros y temporales) por lo que una afectación unilateral puede pasar inadvertida. Se explora pidiendo al enfermo que muerda con fuerza un depresor y se intentará sacarlo, realizando la maniobra en ambos lados. La apertura de la boca depende de músculos más pequeños y su alteración se evidencia con facilidad si al decirle al paciente que abra la boca al máximo o contra una resistencia que hagamos en el mentón, la mandíbula se desvía hacia el lado enfermo. Hay que distinguirlo de la parálisis facial donde únicamente se desvían partes blandas. Todos los pacientes con dolor facial atípico deberían ser estudiados mediante resonancia magnética (RM) para excluir lesiones que estén comprimiendo el nervio trigémino Características diferenciales de la neuralgia esencial y sintomática del trigémino NEURALGIA NEURALGIA ESENCIAL SINTOMÁTICA Etiología Desconocida Lesión estructural Edad de presentación < 50 años > 50 años Afectación Unilateral Uni o bilateral Calidad dolor Paroxismos latigazo Continuo Puntos gatillo Frecuente Infrecuente Déficit neurológico Ausente Frecuente. Refl. corneal Diagnóstico Historia clínica Resonancia Tratamiento Cirugía Médico o cirugía Historia de la cirugía de la neuralgia del trigémino: Los primeros intentos de tratamiento quirúrgico de la neuralgia del 5º par craneal iban orientados a realizar neurectomías (secciones o ablaciones) de las ramas nerviosas periféricas de este par craneal. Este tipo de procedimientos ya fueron probablemente propuestos por Albinus y Galeno. A comienzos del siglo XVIII cirujanos como Schilichting y Maréchal (médico y cirujano personal de Luis XIV). Pero fue Nicholas André en 1756 quien describe la enfermedad en un grupo de pacientes en su libro “Observations pratiques sur les maladies de l´urethre et sur plusieurs faits”. Tras 318 páginas dedicada a enfermedades de la uretra, la mayoría de origen venéreo, inicia bajo el título de “Remarques sur certains mouvements convulsivs” una detallada descripción de cinco pacientes con dolor facial paroxístico. El primero de ellos lo vio en 1732. Se trataba de una mujer a la que habían realizado la extracción de tres dientes en la arcada dentaria superior en un intento de curar la formación continua de un absceso a este nivel. Las extracciones fueron efectivas en la mejora de la infección pero dejaron a la paciente con unos dolores paroxísticos, muy intensos, de corta duración y que se podían provocar. Además iban acompañados de marcadas y características muecas de dolor. En 1730 Maréchal había fracasado en su intento de seccionar el nervio infraorbitario (rama de la segunda división del trigémino). André propuso dos años después aplicar piedras cáusticas y líquido cáustico durante 10 o 12 días hasta que el nervio infraorbitatio fuese destruido. La paciente mejoró completamente de su dolor y ante una nueva recaída 18 meses después fue de nuevo tratada y definitivamente curada. A esta enfermedad que cursaba con “estos movimientos violentos” André la denominó “tic douloureux”. Reconoció que se trataba de una entidad diferente a las otras y, a pesar del carácter explosivo de los episodios, “no se podía denominar propiamente convulsión... dado que los movimientos no son involuntarios”. En 1787, Pujol y otros cirujanos franceses y europeos de la época reconocieron la enfermedad con la denominación otorgada previamente por André, y sugirieron que más de un nervio de la cara debía ser seccionado (en ocasiones no bastaba con el n. infraorbitario), y con frecuencia se seccionaba el nervio facial también (nervio motor de la cara). Pujol ya predijo que las extracciones dentarias eran inefectivas en el tratamiento de este dolor. A comienzos del siglo XIX, Sir Charles Bell realizó la distinción entre el papel motor del nervio facial y el papel sensitivo del nervio trigémino. Aún así cirujanos de la época, incluido su propio hermano, John Bell, continuaron seccionando el nervio facial para el tratamiento del “tic douloureux”. En 1843, Malgaigne, cortó la segunda división del nervio 2 cm. posterior al borde inferior de la órbita, rompiendo el suelo de la órbita, y después tirando del nervio através del foramen infraorbitario. El objetivo era retrasar la regeneración del nervio seccionándolo a un nivel más posterior. Todas estas técnicas de neurectomía no eran realmente efectivas, y a mediados y finales del siglo XIX aparecen artículos reflejando el bajo número de curaciones (18 de 100, Rose 1892) y la alta incidencia de trastornos sensitivos en forma de hipoestesias (disminución de la sensibilidad) y alodinias (dolor al tacto). Por todo esto, aparecen técnicas de gangliectomía (sección del ganglio de Gasser, situado en el cavum de Meckel sobre la fosita de Rossenmüller, que es una depresión en la porción medial y posterior de la fosa media) (ver fig). El primero en llevarla a cabo fue el cirujano inglés William Rose en 1890. Su técnica suponía el acceso y sección del ganglio através de la base del cráneo realizando un trépano (agujero en el hueso del cráneo) al lado del foramen ovale (por donde sale la tercera división del nervio trigémino). En 1891 Hartley modificó el acceso y detalló la facilidad que suponía ir directamente lateral al ganglio, através de la escama del hueso temporal, levantando la dura madre (capa que cubre al cerebro). El abordaje de HartleyKrause fue perfeccionado por Tyffany en 1896 quien propone seccionar aquella parte del ganglio encargada de la segunda y tercera división, dado observó que la sección de la primera rama iba asociada a anestesia corneal con los problemas (queratitis y úlcera corneal) que ello comportaba. Estas cirugías iban asociadas a una alta mortalidad que podía llegar al 24% según las series (Tyffany). Fue Cushing en 1900 quien consigue reducir de manera notable la mortalidad (2 casos de 332). Esto se consiguió gracias a los estudios en 30 cadáveres, y a las “precauciones” anestésicas que seguía Cushing en sus cirugías. La alta mortalidad de las gangliectomías llevó a diseñar las rizotomías (sección de la raíz del nervio). Horsley en 1891 describió la sección a nivel de la protuberancia de las raíces que conformaban el ganglio de Gasser. En esta primera rizotomía el paciente falleció debido a un “shock”, a pesar según Horsley, de lo bien que transcurría la cirugía. El abordaje fue intradural con elevación del lóbulo temporal. Posteriormente, Spiller y Frazier popularizaron en 1901 la rizotomía siguiendo un abordaje extradural. La cirugía se extendió hasta mediados del siglo pasado, pero seguían apareciendo complicaciones como son: la parálisis facial por edema causado por la tracción que ejerce el nervio petroso superficial mayor sobre el ganglio geniculado del facial, al elevar extraduralmente el lóbulo temporal. También se siguieron viendo casos de anestesia dolorosa, disestesias y anestesia corneal. A partir de 1925 el neurocirujano norteamericano Walter Dandy comenzó a preconizar el abordaje a la raíz del nervio por la fosa posterior . Observó que en numerosas ocasiones el nervio presentaba indentaciones por vasos sanguíneos. Recomendaba para esos casos la separación de los vasos, pero sobretodo una rizotomía parcial, con la que conseguía preservar la sensibilidad de la hemicara y curar el dolor. El problema de este tipo de cirugía era el considerable número de recurrencias, y la mortalidad asociada al abordaje por vía posterior (hasta 8 veces mayor que por la fosa media en la serie de Olivecrona), por lo que no se popularizó este abordaje hasta comienzos de la segunda mitad del siglo pasado. En 1950 Garner y Milkos describieron el beneficio que suponía la descompresión vascular del nervio para el tratamiento de la neuralgia del 5º par craneal. En los años 70, Jannetta perfeccionó la técnica y confirmó que el dolor se podía solucionar con la liberación del nervio de los vasos que lo comprimían, sin necesidad de seccionar el nervio. Tratamiento Se ha demostrado que los anticonvulsivantes carbamazepina y fenitoína reducen o controlan el dolor. Hay otras medicaciones, como baclofén, pimozide o clonazepán, que tienen algún valor en el tratamiento, aunque no son muy efectivos. 1. Carbamazepina Provoca una mejoría completa o aceptable en 70% de los casos. Suele darse cada 8 horas hasta una dosis máxima de 1200-1800 mg/día. Puede causar somnolencia, afectación medular y hepática, por lo que es necesario hacer estudios periódicos. Si no consigue un alivio adecuado del dolor o presenta efectos secundarios significativos hay que intentar otro fármaco. 2. Fenitoína Es un fármaco de 2ª elección. Es más barato y tiene menos efectos secundarios que la carbamazepina, pero es menos efectivo. La dosis típica es 300-400 mg/día. Si la carbamazepina y la fenitoína no logran individualmente calmar el dolor pueden usarse asociadas. 3. Baclofen Fármaco de 2ª elección que puede ser útil en casos tratados con carbamazepina y fenitoína que han dejado de proveer alivio adecuado del dolor, pudiéndose asociar a bajas dosis de carbamazepina. Se comienza con 5 mg/8 horas y se van incrementando, no debiendo exceder 80 mg/día. Puede ser teratógeno y hay que evitar la retirada brusca, ya que causa alucinaciones y convulsiones. Tratamiento quirúrgico Indicada cuando el tratamiento médico es insuficiente o produce efectos adversos. Rizotomía percutánea (termocoagulación, glicerol, balón, ...) Se lleva a cabo bajo anestesia local con sedación, ya que es fundamental la colaboración del paciente. Se inserta una aguja en un punto 2.5-3 cm lateral a la comisura bucal. Palpando la mucosa bucal con un dedo dentro de la boca, para evitar penetrar la mucosa, se dirige la aguja, bajo control radiológico, hacia el agujero oval de la base del cráneo. Una vez que se penetra dicho agujero, se retira el estilete, con lo que suele salir líquido cefalorraquídeo. A continuación se introduce el electrodo por la aguja. Entonces el paciente es despertado de la sedación y se procede a la estimulación hasta conseguir reproducir la distribución del dolor en la cara. Entonces se seda de nuevo al paciente para realizar varias veces una coagulación parcial del ganglio trigeminal con temperatura a 65-75 ºC. En las otras dos variantes de esta técnica se introduce por la aguja ya colocada glicerol (0.1-0.5 ml)o bien un catéter-balón de Fogarty (4 F) que es inflado con 0.71 ml de contraste hidrosoluble durante 1 minuto. Decompresión microvascular A través de una pequeña apertura craneal (craniotomía) retromastoidea de 2 a 4 cm de diámetro se transpone el vaso que comprime e irrita el nervio trigémino y se interpone un material autólogo (músculo) o artificial (teflón, dacrón, esponja de polivinilo). La causa más frecuente de la compresión es la arteria cerebelosa superior. Radiocirugía estereotáctica. Cualquiera de estas 3 técnicas es válida aunque: la radiocirugía estereotáctica esta cobrando cada día más importancia. Su ventaja es que el paciente no se expone a riesgos directos de la cirugía (Infecciones ,lesiones vasculares...) pero el efecto analgésico no es inmediato y es una técnica cara. La rizotomía prepontina selectiva por vía suboccipital lateral Fué descrita por primera vez por Dandy en 1925, y popularizada nuevamente por Gadner en 1959 . Ellos mencionaron que se podía terminar con el dolor facial conservando o respetando la sensibilidad o el tacto fino del paciente al seccionar la porción mayor de la raíz del trigémino antes de que entre en la protuberancia La base anatómica de esta cirugía radica en la existencia de una somatotopía de las fibras del ganglio de Gasser y de la porción retrogasseriana de la raíz, siendo posible obtener un efecto topográfico selectivo sobre la zona dolorosa mediante la sección parcial de la raíz a la entrada del puente. A nivel yuxtaprotuberancial, las fibras se reacomodan conforme a su destino funcional: las fibras nocioceptivas se agrupan ventral y lateralmente para formar la pars mayor para luego proyectarse sobre el núcleo espinal del trigémino; las fibras del tacto epicrítico o tacto fino forman la pars intermediaris para terminar en el núcleo sensitivo principal protuberancial, y por último, las fibras motoras forman la pars menor que lleva fibras que salen del núcleo motor del trigémino, como fibras de la sensibilidad propioceptiva de los músculos masticatorios y mandíbula que terminan en el núcleo mesencefálico del trigémino . Entre las ventajas de la rizotomía parcial prepontina destacan: la baja incidencia reportada de dolor recurrente; esto se debe a que la raíz sensitiva no se regenera proximalmente al ganglio dorsal (ganglio de Gasser) la sección selectiva de la raíz posterior con la preservación del tacto fino evita una complicación común de la sección de un nervio periférico: la anestesia dolorosa, la cual puede ser tan molesta o más que la causa primaria del problema y la preservación de la raíz motora. Por lo tanto, consideramos que la rizotomía prepontina es un método efectivo para tratar la neuralgia trigeminal secundaria a infarto pontino; debe ser considerada como tratamiento de este problema clínico que, aunque infrecuente, es clínicamente significativo. BIBLIOGRAFIA: Barker FG, Jannetta PJ, Bisonette DJ, Larkins MV, Jho HD: The long term outcome of microvascular decompression for trigeminal neuralgia. N Engl J Med. 334:10771083, 1996. Brown JA, McDaniel MD, Weaver MT: Percutaneous trigeminal nerve compression for treatment of trigeminal neuralgia:. Neurosurgery. 32:570573, 1993 .Emmons WF., Rhoton AL.: Subdivision of the trigeminal sensory root. Experimental study in the monkey. J Neurosurg 35: 5811-591, 1971 Foroohar M., Herman M., Heller S., Levy R.: Radiofrecuency trigeminal rhizolysis for the treatment neuralgia secondary to brainstern infarction. Report of two cases. Neurosurgical focus: Jan 97/2: 1-6. Fromm GH; H., Terrence CF., Maroon JC.: Trigeminal Neuralgia. Current concepts regarding etiology and pathogenesis. Arch Neurol 41: 1204-1207, 1984 Golby JA, Norbash A., Silverberg S.: Trigeminal neuralgia resulting from infarction of the root Entry zone of the Trigeminal nerve: Case Report. Neurosurg 43: 620623, 1998 Gudmundsson K; Rhoton AL; Rushton J: Detailed anatomy of the intracranial portion of the trigeminal nerve. J Neurosurg. Vol 35: 592-600; 1971 Haines SJ., Janetta PJ., Zorub DS.: Microvascular relations of the trigeminal nerve. An anatomical study with clinical correlation. J Neurosurg 52: 381-386, 1980 Hitsselberger WE., Pulec JL.: Trigeminal nerve (posterior root) retrolabyrintine Selective Section. Arch Otolaryng 96: 412-415, 1972 Lunsford LD, Bennett MH, Martinez AJ: Experimental trigeminal glycerol injection:. Arch Neurol. 42:146149, 1985. Provost J., Hardy J.: Microchirurgie du trijumeau: anatomie functionelle. Neurochirurgie 16: 459-469, 1970 Rand R.:Gadner Neurovascular decompression of the trigeminal and facial nerves for Tic Douloureux and hemifacial spasm. Surg Neurol: 16:329-332,1981 Rappaport ZH., Devor M.: Trigeminal neuralgia: The role of self-sustaining discharge in the trigeminal ganglion. Pain 60: 229-231, 1995 Reutens DC.: Burning oral and mid-facial pain in ventral pontine infarction. Aust NZ J Med 20 (3): 249-250 Saunders RL., Sachs E.: Relation of the accessory rootlets of the trigeminal nerve to its motor root. A Microsurgical autopsy study. J Neurosurg 33: 317-324, 1970 Seltzer Z., Devor M.: Ephatic transmission in cronically damaged peripheral nerves. Neurol 29 (7): 1061-1064, 1979 Sindou M., Keravel Y., Abdennebi B., Szapiro J.: Traitment neuro-chirurgical de la neuralgie trigeminale. Abord direct ou méthode percutanee?. Neurochirurgie 33: 89-111, 1987 Stechison MT., Moller A., Lovely TJ.: Intraoperative Mapping of the Trigeminal Nerve Root : Technique and application in the surgical management of facial pain. Neurosurg 38: 89-111, 1987 Swanson SE., Farhat SJ.: Neurovascular descompression with selective partial rhizotomy of the trigeminal nerve for tic douloureux. Sur Neurol 18: 3-6, 1982 Szapiro J., Sindou M., Traitment microqhirurgical de la neuralgie du trijumeau. Resultats et facteurs pronostiques de la descompression vasculaire microquirurgical. Neurichirurgie 32: 103-121, 1986 Taha JM, Tew JM: A prospective 15-year follow-up of 154 consecutive patients with trigeminal neuralgia treated by percutaneous stereotactic radiofrequency rhizotomy. J Neurosurg. 83:989993, 1995.

