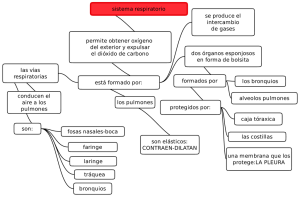
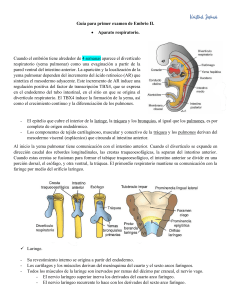
Guía para primer examen de Embrio II. Aparato respiratorio. Cuando el embrión tiene alrededor de 4 semanas aparece el divertículo respiratorio (yema pulmonar) como una evaginación a partir de la pared ventral del intestino anterior. La aparición y la localización de la yema pulmonar dependen del incremento del ácido retinoico (AR) que sintetiza el mesodermo adyacente. Este incremento de AR induce una regulación positiva del factor de transcripción TBX4, que se expresa en el endodermo del tubo intestinal, en el sitio en que se origina el divertículo respiratorio. El TBX4 induce la formación de la yema, así como el crecimiento continuo y la diferenciación de los pulmones. - El epitelio que cubre el interior de la laringe, la tráquea y los bronquios, al igual que los pulmones, es por completo de origen endodérmico. Los componentes de tejido cartilaginoso, muscular y conectivo de la tráquea y los pulmones derivan del mesodermo visceral (esplácnico) que circunda al intestino anterior. Al inicio la yema pulmonar tiene comunicación con el intestino anterior. Cuando el divertículo se expande en dirección caudal dos rebordes longitudinales, las crestas traqueoesofágicas, la separan del intestino anterior. Cuando estas crestas se fusionan para formar el tabique traqueoesofágico, el intestino anterior se divide en una porción dorsal, el esófago, y otra ventral, la tráquea. El primordio respiratorio mantiene su comunicación con la faringe por medio del orificio laríngeo. Laringe. - Su revestimiento interno se origina a partir del endodermo. Los cartílagos y los músculos derivan del mesénquima del cuarto y el sexto arcos faríngeos. Todos los músculos de la laringe son inervados por ramas del décimo par craneal, el nervio vago. - El nervio laríngeo superior inerva los derivados del cuarto arco faríngeo. - El nervio laríngeo recurrente lo hace con los derivados del sexto arco faríngeo. Como consecuencia de la proliferación rápida de este mesénquima, el orificio laríngeo cambia su aspecto, de ser una hendidura sagital a constituir una abertura en forma de T. De manera subsecuente, cuando el mesénquima de los dos arcos se transforma en los cartílagos tiroides, cricoides y aritenoides, puede reconocerse la configuración característica del orificio laríngeo en el adulto. Aproximadamente en el momento en que los cartílagos se forman, el epitelio laríngeo también prolifera con rapidez, lo que origina la oclusión temporal de su luz. Más tarde la vacuolización y la recanalización dan origen a un par de huecos laterales, los ventrículos laríngeos. Estos huecos están limitados por pliegues tisulares que se convierten en las cuerdas vocales falsas y verdaderas. Tráquea, bronquios y pulmones. Al tiempo que se separa del intestino anterior, la yema pulmonar forma la tráquea y dos sáculos laterales: las yemas bronquiales primarias. Al inicio de la quinta semana cada una de estas yemas se ensancha para constituir los bronquios primarios derecho e izquierdo. El derecho genera entonces tres bronquios secundarios, y el izquierdo dos, lo que anuncia la formación de tres lóbulos en el pulmón del lado derecho y dos en el izquierdo. Cavidades. Con el crecimiento subsecuente en dirección caudal y lateral, los pulmones se expanden hacia el interior de la cavidad corporal. Los espacios disponibles para los pulmones, los canales pericardioperitoneales, son estrechos. Estos se ubican uno a cada lado del intestino anterior y de manera gradual quedan ocupados por los pulmones en crecimiento. En última instancia, los pliegues pleuroperitoneales y los pleuropericárdicos separan los canales pericardioperitoneales de las cavidades peritoneal y pericárdica, respectivamente, y los espacios remanentes constituyen las cavidades pleurales primitivas. - El mesodermo que cubre el exterior del pulmón se convierte en la pleura visceral, que se extiende entre los lóbulos pulmonares. La capa de mesodermo somático, que cubre el interior de la pared corporal, se transforma en la pleura parietal. El espacio remanente entre la pleura parietal y la visceral corresponde a la cavidad pleural. Maduración de los pulmones. Al continuar el desarrollo, los bronquios secundarios se dividen una y otra vez con un patrón dicotómico para dar origen a 10 bronquios terciarios (segmentarios) en el pulmón derecho y a ocho en el izquierdo, lo que crea los segmentos broncopulmonares del pulmón adulto. Al final del sexto mes existen alrededor de 17 generaciones de subdivisiones. A pesar de esto, para que el árbol bronquial adquiera su configuración definitiva deben ocurrir seis divisiones adicionales durante la vida posnatal. La ramificación está regulada por interacciones epitelio-mesénquima entre el endodermo de las yemas pulmonares y el mesodermo visceral que las circunda. Las señales para la ramificación, que emite el mesodermo, implican a miembros de la familia del factor de crecimiento de fibroblastos. Al tiempo que se generan todas estas subdivisiones nuevas y el árbol bronquial se desarrolla, los pulmones asumen una posición más caudal, de tal modo que al momento del nacimiento la bifurcación de la tráquea coincide con el nivel de la T4. Hasta el séptimo mes de la gestación los bronquiolos experimentan división continua para dar origen a conductos cada vez más pequeños (fase canalicular) y la irrigación vascular se incrementa en forma constante. Los bronquiolos terminales se dividen para constituir bronquiolos respiratorios, y cada uno de estos se divide en tres a seis conductos alveolares. Los conductos terminan en los sacos terminales (alveolos primitivos), que están rodeados por células alveolares planas en contacto estrecho con los capilares vecinos. Al final del séptimo mes el número de sacos alveolares y capilares maduros es suficiente para garantizar un intercambio gaseoso adecuado, lo que permitiría la sobrevivencia en el neonato prematuro.Durante los últimos 2 meses de la vida intrauterina y varios años tras el nacimiento, el número de sacos terminales muestra incremento constante. Por otra parte, las células que recubren los sacos, conocidas como células epiteliales alveolares (neumocitos) tipo I, se adelgazan cada vez más, de modo que los capilares circundantes protruyen hacia la luz de los sacos alveolares. Este contacto íntimo entre las células epiteliales y las endoteliales constituye la barrera alveolocapilar. No existen alveolos maduros antes del nacimiento. Además de las células endoteliales y las células epiteliales alveolares planas, se desarrolla otro tipo de células al final del sexto mes. Éstas, las células epiteliales alveolares (neumocitos) tipo II, sintetizan surfactante, Surfactante: Líquido con alto contenido en fosfolípidos capaz de disminuir la tensión superficial en la interfase alveolocapilar. Sin la capa de surfactante los alveolos colapsarían durante la espiración (atelectasia). Antes del nacimiento los pulmones están llenos de un líquido con alto contenido en cloruro, proteínas escasas y cierta cantidad de moco proveniente de las glándulas bronquiales, así como el surfactante derivado de las células del epitelio alveolar (tipo II). La cantidad de surfactante en el fluido se incrementa, en particular durante las últimas 2 semanas previas al nacimiento. Al tiempo que las concentraciones de surfactante aumentan durante la semana 34 de la gestación, cierta cantidad de este fosfolípido llega al líquido amniótico y actúa sobre los macrófagos de la cavidad amniótica. Se dice que una vez “activados” estos macrófagos migran por el corion hacia el útero, donde comienzan a sintetizar proteínas del sistema inmunitario, entre ellas interleucina 1 beta (IL-1β). La regulación positiva de estas proteínas da origen al incremento de la síntesis de prostaglandinas que desencadenan las contracciones uterinas. Así, pudieran existir señales provenientes del feto que participen en el inicio del trabajo de parto y del parto. Los movimientos respiratorios fetales inician antes del nacimiento y generan la aspiración del líquido amniótico. Estos movimientos son importantes para estimular el desarrollo pulmonar y acondicionar a los músculos respiratorios. Cuando la respiración inicia al momento del nacimiento la mayor parte de líquido pulmonar se absorbe con rapidez por medio de los capilares sanguíneos y linfáticos, y un volumen escaso quizá sea expulsado por la tráquea y los bronquios durante el parto. Una vez que el líquido se absorbe de los sacos alveolares, el surfactante se deposita y forma una capa delgada de fosfolípidos sobre las membranas celulares alveolares. Cuando el aire ingresa a los alveolos en la primera respiración, la capa de surfactante evita el desarrollo de una interfase aire-agua (sangre) con una tensión superficial alta. Los movimientos respiratorios tras el nacimiento conducen el aire hacia los pulmones, que se expanden y llenan la cavidad pleural. Si bien el tamaño de los alveolos se incrementa en cierto grado, el crecimiento de los pulmones tras el nacimiento depende ante todo del aumento del número de bronquiolos respiratorios y alveolos. Se calcula que una sexta parte del número de alveolos del adulto ya existe al nacer. El resto de los alveolos se forma durante los primeros 10 años de la vida posnatal mediante la generación continua de alveolos primarios nuevos. Correlaciones clínicas. 1. Atresia esofágica (AE). Es una malformación congénita en la cual se ve interrumpida la luz esofágica de forma parcial o total, asociándose en el 94% de los casos con una fístula traqueoesofágica. La estadística es diversa y oscila entre 1 por cada 1300 y 1 por cada 4500. Sexo masculino 62 %. La causa primaria es una migración anómala de las células de la cresta neural, por lo tanto, es una neurocrestopatía; también se asocian a la etiología insuficiencia vascular y ulceración. talidomida, Vit. A, riboflavina. El embrión de cinco semanas (9mm) puede ya mostrar la malformación completa. Factores de riesgo: o Sexo masculino. o Factores ambientales. o Factores infecciosos. o Factores genéticos - Gemelos. - Recurrencia familiar. - Anomalías cromosómicas (se asocia con las trisomías 21, 18 y 13). o Edad materna. Clasificación. 1. AE con segmento proximal que termina en saco ciego + FTE distal (90%) 2. AE aislada (sin FTE) (4%). 3. FTE tipo H (sin atresia) (4%). 4. AE con segmento distal que inicia en saco ciego + FTE proximal (1%). 5. FTE doble (1%). 1 2 4 3 5 Cuadro clínico. o Sialorrea (salivación excesiva). o Cianosis (coloración azulada). o Broncoaspiración (aspiración accidental de líquidos o alimentos por las vías respiratorias). o Regurgitaciones (regreso sin esfuerzo del contenido alimentario a través del esófago [reflujo gastroesofágico], hasta la orofaringe). o Tos. o Dificultad para respirar durante la alimentación. Cuando existe una AE sin FTE, el abdomen está excavado, pues al no tener comunicación el cabo distal esofágico, no hay paso de gas al estómago y asas intestinales; puede haber broncoaspiración, pues cuando el cabo proximal se rebosa de alimento, este comprime la tráquea y parte de este líquido ingerido pasa al árbol traqueobronquial. En la AE con FTE proximal, la secreción aireada abundante por la boca es un signo característico. En estos niños, la broncoaspiración es inmediatamente después de ingerir alimentos, provocando cianosis y tos por oclusión de las vías aéreas, pudiendo morir en las primeras horas por neumonía espirativa masiva. En la AE con FTE distal, el aire pasa al estómago y asas delgadas a través de la fístula, por lo que el abdomen se muestra distendido, lo que provoca la elevación del diafragma y dificulta la respiración, además, el contenido que pasa al estómago por la tráquea llega a los pulmones, provocando neumonía química que después se convierte en bacteriana. A TODO RECIÉN NACIDO CON AE + FTE SE LE ADMINISTRAN ANTIBIÓTICOS PORQUE EL ALIMENTO PASARÁ A LA REGIÓN PULMONAR, OCASIONANDO UN SOBRECRECIMIENTO BACTERIANO QUE DARÁ LUGAR A UNA NEUMONÍA. Dx. o Colocación de sonda para aspiración, la cual se detiene por en su trayecto por la atresia. o Rayos X. 2. Síndrome de dificultad respiratoria (SDR), antes llamado enfermedad por membrana hialina. El SDR se debe a un déficit o disfunción de surfactante alveolar asociado a la arquitectura de un pulmón inmaduro. Es visto exclusivamente en neonatos pretérmino (antes de las 37 sem. --> Nacimiento prematuro). El riesgo de SDR disminuye con la edad gestacional: 60% de los RN <28 sem. 30% de los RN entre 28 y 34 sem. Menos del 5% de los RN >34 sem. Factores de riesgo. o Prematuridad. o Sexo masculino. o Diabetes gestacional con mal control metabólico. o Nacimiento por cesárea. o Factores genéticos. o Raza blanca. o Gestaciones múltiples. o Hipotermia. o Asfixia perinatal. Esteroides prenatales y rotura prolongada de membrana disminuyen riesgo de SDR. Etiopatogenia. Al no haber suficiente surfactante o ser disfuncional, al momento de la espiración en la primer ventilación, va a haber atelectasia (colapso alveolar). El aire no va a poder seguir llegando a los alvéolos, el O2 no va a atravesar la barrera alveolocapilar y se va a desarrollar hipoxemia (disminución de O2 en sangre) y, si el cuadro continúa, se puede producir hipercapnia (aumento de CO2 en sangre). Cuando el niño nace, el líquido pulmonar se absorbe mediante las células endoteliales y una pequeña parte se expulsa hacia el exterior a través del árbol bronquial y la tráquea, en un prematuro, el líquido no puede absorberse y empieza a acumularse en el tejido pulmonar, produciéndose edema, que, a su vez, produce lesión celular. Cuadro clínico. - Taquipnea (aumento de fr) Polipnea (aumento de fr + uso de musculatura accesoria) - Hipoxemia. - Hipercapnia. o Evolución clínica o Evaluación de Silverman-Andersen. < 3 No hay SDR 3 SDR leve 4 – 6 SDR moderado > 6 SDR grave (criterio de intubación y asistencia respiratoria) o Criterios radiológicos: Grado 1: Infiltrado retículo granular difuso. Grado 3: Infiltrado retículo granular difuso + broncogramas aéreos que sobrepasan la silueta cardíaca + borramiento de la silueta cardíaca. Grado 2: Infiltrado retículo granular difuso + broncogramas aéreos que no sobrepasan la silueta cardíaca. Grado 4: Opacificación total (vidrio esmerilado) + borramiento de la silueta cardíaca. Clasificación. o Según evolución. 1. Período inicial. 2. Período de deterioro. 3. Período de estado o meseta. 4. Período de recuperación. o Según evaluación de Silverman-Andersen. 1. Leve. 2. Moderado. 3. Grave. o Según criterio radiológico. - Grado 1. - Grado 2. - Grado 3. - Grado 4. Dx. o Exámenes de laboratorio. - Gasometría arterial. - Electrolitos séricos. - Glicemia. o Radiología.