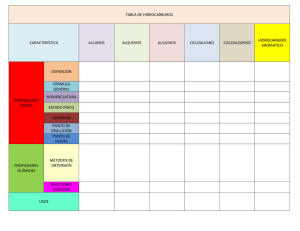
UNIVERSIDAD NACIONAL AGRARIA LA MOLINA Facultad de ciencias Departamento de Química Curso: Laboratorio de Química Orgánica Título de la práctica: Reacciones de hidrocarburos Grupo de práctica: Grupo N.º 5 Integrantes Códigos 1. Ramos Huamán, James Gonzalo 20220589 2. Reyna Medina, Bertha 20220680 3. Soto Zelada, Brenda Nicole 20220682 4. Rodriguez Navarro, Alexandra Rocio 20220681 Profesora de práctica: Arias Durand, Amelia Devorah Horario de la práctica: 11:00 am – 13:00 pm Fecha de la práctica: 10/11/2022 Fecha de informe: 17/11/2022 1. INTRODUCCIÓN La reactividad depende de la ESTRUCTURA de los reaccionantes y del MEDIO en el que se está efectuando la reacción. Bajo condiciones apropiadas una sustancia puede transformarse en otra que constituye una especie química diferente. Los ALCANOS, por carecer de grupos funcionales, son prácticamente inertes y generalmente insolubles no sólo en disolventes polares corrientes (agua) sino también en ácido sulfúrico concentrado en frío. En condiciones específicas ellos sufren algunas reacciones, la mayoría de las cuales no son de carácter preparatorio en el laboratorio. A diferencia de los alcanos, los enlaces dobles y triples de ALQUENOS Y ALQUINOS, respectivamente, hacen que sus moléculas sean mucho más reactivas y capaces de dar reacciones de ADICIÓN antes que de SUSTITUCIÓN. La gran estabilidad del sistema aromático hace que sus moléculas presentan menor actividad de los quenos. Los hidrocarburos AROMATICOS, se diferencian de los alquenos y alquinos porque generalmente no sufren de ADICCIÓN sino de SUSTITUCIÓN. 2. OBJETIVOS ● Identificar si un compuesto orgánico es un alcano, alqueno o aromático. ● Diferenciar un alcano de un aromático. ● Reconocer las reacciones de alcanos, alquenos y aromáticos. 3. MARCO TEÓRICO 3.1. HIDROCARBUROS: Los hidrocarburos son compuestos orgánicos abundantes en la naturaleza como gases, líquido, grasas y a veces sólidos; formados totalmente por carbono e hidrógeno. Las clases principales de hidrocarburos son alcanos, alquenos, alquinos e hidrocarburos aromáticos. 3.2. ALCANOS: Los alcanos, también conocidos como parafinas o hidrocarburos saturados, son hidrocarburos lineales o ramificados que poseen sólo enlaces covalentes simples entre sus átomos de carbono. Los alcanos son los componentes principales de los gases para la calefacción (gas natural y gas licuado de petróleo), de la gasolina, de los combustibles para aviones, gasóleo, aceite de motor, aceite combustible y “cera” de parafina. Además de la combustión, los alcanos experimentan pocas reacciones. Los alcanos experimentan pocas reacciones debido a que no tienen un grupo funcional, que es la parte de la molécula en donde por lo regular ocurren las reacciones. 3.3. ALQUENOS: Los alquenos son hidrocarburos acíclicos insaturados que se caracterizan por la presencia de un doble enlace en su molécula y tienen una fórmula general Cn H2n, en donde n es el número de átomos de carbono presentes. Los alquenos son hidrocarburos que contienen enlaces dobles carbono-carbono. Un enlace doble carbono-carbono es la parte más reactiva de un alqueno, por lo que decimos que el enlace doble es el grupo funcional del alqueno. 3.4. PRUEBA DE BROMO EN TETRACLORURO DE CARBONO: Una prueba muy cómoda para distinguir nítidamente los alcanos de los hidrocarburos alifáticos insaturados cosiste en tratarlos con bromo disuelto en tetracloruro de carbono; si el hidrocarburo desconocido es un alcano, apenas habrá reacción en la oscuridad. En cambio, frente a la luz, solar o artificial, el color del Bromo irá desapareciendo gradualmente a medida que avance la bromación. 3.5. PRUEBA DE BAEYER: Reacción útil para la distinción de alquenos de alcanos. Los alcanos no reaccionan con permanganato de potasio. Una prueba positiva es fácil de detectar visualmente porque las soluciones de permanganato de potasio son de color purpura intenso. Cuando esta solución se agrega a un alqueno, el color purpura desaparece rápidamente, dejando un precipitado pardo turbio de óxido de manganeso (Bailey, PS., Bailey CA. 1998). 3.6. REACCIÓN CON ÁCIDO SULFÚRICO: Es otro ensayo para diferenciar hidrocarburos insaturados de alcanos y aromáticos ya que estos últimos no reaccionan frente al reactivo a temperatura ambiente, mientras que el enlace doble sufre la rápida adición del H2SO4. 3.7. HIDROCARBUROS AROMÁTICOS Al benceno y a las demás sustancias que tienen estructuras y propiedades químicas semejantes a él, son clasificados como compuestos aromáticos. En realidad, el benceno es un híbrido de resonancia de las dos estructuras de Kekulé. Esta representación implica que los electrones pi están deslocalizados, con un orden de enlace de 11/2 entre los átomos de carbono adyacentes. Podemos definir a un compuesto aromático como un compuesto cíclico que contiene cierta cantidad de enlaces dobles conjugados y que tiene una energía de resonancia demasiado grande. 4. METODOLOGÍA 4.1. Tabla N°1. Materiales y equipos: Figura. Materiales Fuente: Elaboración propia 4.2. Tabla N°2. Reactivos: Figura. Reactivos Fuente: Elaboración propia 4.3. Procedimiento experimental: Figura . Proceso experimental Fuente: Elaboración propia 5. RESULTADOS Tabla N°3: Resultados de las reacciones positivas Fuente: Elaboración propia 6. DISCUSIÓN En la tabla 3 se presenta cómo actúan cada tipo de hidrocarburos dependiendo de la reacción. Cuando se llevó a cabo el ensayo con solución de bromo en tetracloruro de carbono, teniendo en cuenta que los átomos de bromo rompen un enlace doble generando una reacción de adición en los hidrocarburos insaturados y causando incorporación, (Aguilar Garduño, 2012), se apreció que la muestra problema sufrió dicho fenómeno, por lo cual este primer experimento nos estaría indicando que es un alqueno. Para el ensayo de Baeyer, se utilizó al permanganato de potasio, el cual también reacciona con los hidrocarburos insaturados formando un precipitado color marrón, esto permite reconocer la presencia de enlaces dobles (U.A.N.L), lo cual dicho fenómeno sucedió en el tubo de ensayo que contenía al alqueno y en la muestra problema, por lo cual estaríamos rectificando que se trata de un alqueno. En el ensayo con ac. Sulfúrico, la reacción positiva se da en los hidrocarburos insaturados, lo cual provoca la formación de una sola fase, y esto se pudo observar en el tubo que contenía a la muestra problema. Por último, el experimento realizado para saber la identidad de nuestra muestra problema, fue el ensayo con ácido nítrico, la reacción positiva nos indica que la sustancia es un aromático que reacciona por sustitución sólo en presencia de un catalizador ácido sulfúrico, (Primo Yúfera , 1995). Realizando dicho procedimiento, esta reacción positiva genera además la formación de un líquido aceitoso amarillento de olor aromático, lo que indica la nitración del benceno, hecho que no ocurrió con la muestra problema, por lo cual se comprueba de que la muestra no es un aromático 7. CONCLUSIÓN En el ensayo de la prueba con Br2/CCl4 sobre un hidrocarburo consistió en la comprobación de la presencia de fenoles o alquenos. Con los alquenos se produce una reacción electrofilia, rompiendo el enlace doble. En cambio, con un aromático ni existe la reacción. En el ensayo de baeyer nos permitió conocer la presencia de enlaces dobles. Al agregar el reactivo al alqueno se forma rápidamente un precipitado de color marrón. Co el n-hexano, benceno y la Muestra de prueba no existió reacción alguna y el color se mantuvo. En la reacción del H2SO4 se diferenció hidrocarburos insaturados de los alcanos y aromáticos. Teniendo una reacción a temperatura ambiente, mientras que los alquenos sufren rápida adición. Concluimos que la muestra problema es un alqueno debido a la reacción con la mayoría de las soluciones menos el ácido nítrico. 8. REFERENCIAS ● Garduño, A. (12 de 06 de 2012). Obtenido de Universidad Nacional Autónoma de México: https://www.scielo.org.mx/pdf/eq/v23n3/v23n3a2.pdf ● UNIVERSIDAD AUTONOMA DE NUEVO LEON. (s.f.). Obtenido de http://cdigital.dgb.uanl.mx/la/1020124207/1020124207_024.pdf ● Primo Yúfera, E. Química Orgánica Básica y Aplicada. De la molécula a la Industria. Editorial Reverté (1995). ● 9. Bailey, PS., Bailey CA. 1998. Química orgánica: conceptos y aplicaciones. Pearson Educación. 115p. ● Keese R., Muller RK., Toube TP. 1990. Métodos de laboratorio para química orgánica. 1° edición. Editorial Limusa. Mexico DF. ● Wade, L. (2012). QUÍMICA ORGÁNICA . Naucalpan de Juárez: Pearson CUESTIONARIO ● ¿Qué aplicación en los compuestos biológicos tienen las reacciones afectadas? ● ¿Si al isobutano se le añade bromo disuelto en tetracloruro de carbono en presencia de luz, que productos se formarán y cual en mayor porcentaje? ● Completar las siguientes reacciones(si es que producen): ● Si 0,25 moles de grasa o aceite consume 40 g de bromo: ¿cuantos enlaces dobles se puede estimar que tiene este lípido? ● Proponga dos métodos para determinar la presencia de insaturaciones en una muestra de grasa. ● ¿Cuál es el índice de octano u octanaje de la gasolina? Para determinar la medida de octanaje de los combustibles, se usa una escala arbitraria de número de octano. En la escala, se da a los hidrocarburos iso-octano (que son poco detonantes) un índice RON de 100 octanos y al n-heptano (que es muy detonante) un índice RON de 0 octanos. Con menor octanaje, el combustible tiene más facilidad de hacer ignición a temperaturas más bajas. Si esta explosión se realiza en un momento que no es óptimo, podría dañar seriamente algunos componentes del motor, como son el pistón, la biela, la camisa, la culata y el cigüeñal; mientras que con un número mayor de octanaje la combustión que se genere en el cilindro del motor será más uniforme y por ende, más controlada y efectiva. Una medida de octanaje mayor aumenta el desempeño del motor de tu vehículo y asegurando que se aproveche mejor el combustible. En el manual del fabricante, puedes ver la medida de octanaje ideal para el motor de tu vehículo. ● ¿Que son antidetonantes y porque se añaden a la gasolina? Un agente antidetonante es un aditivo de gasolina que se utiliza para reducir el golpeteo del motor y aumentar el octanaje del combustible al elevar la temperatura y la presión a las que se produce la autoignición. La mezcla conocida como gasolina o gasolina, cuando se usa en motores de combustión interna de alta compresión , tiene tendencia a golpear (también llamado "ping" o "pinking") y / o encenderse antes de que ocurra la chispa en el momento correcto ( pre-ignición , consulte el golpeteo del motor ). ● De los solventes utilizados en esta experiencia, ¿cuáles de ellos emplea para limpiar una tela manchada con grasa?. Explique Se utilizará el ensayo de Br2/CCl4 para limpiar la tela manchada de grasa, ya que se volvería incoloro al entrar en contacto con el Br2 pues una grasa es una cadena larga de alcanos o alquenos.