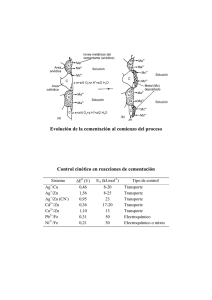
4.1. Evaluación de la Cementación de Cobre con Chatarra de Fierro
Anuncio
IV. RESULTADOS Y DISCUSIÓN 4.1. Evaluación de la Cementación de Cobre con Chatarra de Fierro 4.1.1. Evaluación a Nivel Laboratorio A continuación se presentan los resultados de la cementación de cobre con chatarra de fierro, realizada en el laboratorio, con el fin de determinar la efectividad de este proceso, para la recuperación de cobre de los licores de lixiviación de la PACC. En esta etapa se llevaron a cabo dos experimentos: “Experimento 1”, realizado en reposo, (Figura 13) y “Experimento 2” realizada con agitación constante y vigorosa (Figuras 14 y 15), obteniéndose los siguientes resultados: Tabla III. Resultados del Experimento 1 en Laboratorio. Licores Relación Acidez Cu Fe Cu Relación Fe : Cu (g/L) (g/L) (g/L) Cementado Real (Fe/Cu) (%) 490 4.84 4.22 Licor Madre 532.85 4.59 4.45 5.17 0.92 2.5 Corrida 1 522.22 4.09 4.86 15.50 0.85 5 Corrida 2 547.5 3.58 5.27 26.03 0.83 10 Corrida 3 *Debido a la relación Fe:Cu del licor madre, se les depositó a las corridas 1, 2 y 3, 2.42 g, 4.84g y 9.68 g de Fe, respectivamente, para la cementación con 200 mL de licor. Figura 13. Licor de la PACC Filtrado después de la Cementación (Experimento 1). Tabla IV. Resultados del Experimento 2 en Laboratorio. Licores Relación Acidez Cu Fe Cu Relación Fe : Cu (g/L) (g/L) (g/L) Cementado Real (%) (Fe/Cu) Licor Madre 480.58 4.14 2.63 Corrida 1 2.5 480.58 1.34 5.47 67.63 0.94 Corrida 2 5 480.20 0.037 6.73 99.11 1.00 Corrida 3 10 482.77 0.037 7.2 99.11 1.11 *Debido a la relación Fe:Cu del licor madre, se les depositó a las corridas 1, 2 y 3, 2.07 g, 4.14 g y 8.28 g de Fe, respectivamente, para la cementación con 200 mL de licor. Figura 14. Licor de la PACC Filtrado después de la Cementación (Experimento 2). Figura 15. Cobre Cemento, Corrida 1; Experimento 2. La diferencia entre los dos experimentos, es indiscutiblemente muy notoria, alcanzándose valores mucho más altos de eficiencia en el Experimento 2, logrando casi el 100% de la extracción de Cu en el caso de las Corridas 2 y 3, y un porcentaje de extracción de cobre de 67.63% en la Corrida 1. Cabe aclarar que en el Experimento 2, se consumió bastante chatarra de Fe, en relación con el Experimento 1. Se analizó completamente, los resultados satisfactorios de la prueba, teniendo como resumen los siguientes puntos de discusión: • A los dos experimentos se les dispuso de las mismas cantidades de chatarra de fierro, por lo que debieron de haber tenido las dos el mismo rendimiento, sin embargo, se puede ver que el hecho de haber agitado uno de los experimentos, hizo más eficaz el proceso. • El hecho de agregar una razón de Fe:Cu bastante pronunciada, es para contemplar todas las reacciones secundarias que se dan durante la cementación, por lo que si al agregar mucha chatarra de fierro, no se cementa el Cu, quiere decir que la reacción no se está llevando a cabo correctamente, una de las razones principales seria que el área de contacto entre la chatarra y la solución de cobre, no se está logrando eficientemente debido al cobre cemento que se sitúa en las paredes de la chatarra; y si en dado caso (como en las Corridas 2 y 3 del Experimento 2) hay área de contacto y todavía queda chatarra de Fe, quiere decir que ya se cementó toda la cantidad de Cu que se encontraba en solución. Otra justificación también puede ser que el tiempo de residencia que se le esté dando a la cementación es insuficiente (como en el caso de la Corrida 1 del Experimento 2, que tenía chatarra suficiente para reaccionar pero el área de contacto fue insuficiente para el tiempo de residencia dado). 4.1.2 Evaluación a Nivel Planta Piloto Para esta evaluación se realizaron dos corridas en la planta piloto con la metodología antes descrita, variando solo la cantidad de fierro añadida a cada garrafón. Corrida 1 Se añadió 3.5 kg de chatarra de fierro, cantidad que ocupó gran parte del volumen del garrafón. Sin embargo, a los pocos minutos que empezó la corrida, el sistema se salió de control, debido a que el licor entro demasiado caliente (50°C), aunado a esto, el excesivo contenido de fierro hizo que la reacción se diera de una manera violenta. Los motivos antes mencionados, hicieron imposible tener resultados concisos y determinantes, por lo que se tuvo que abandonar. Corrida 2 En esta corrida se le agregaron cantidades de chatarras de fierro, mismas que ocuparon el 5%, 10%, 15% y 20% del volumen total del garrafón, desde del tanque más alto al más bajo, respectivamente a 50°C. Realizándolo de esta manera, el sistema operó adecuadamente, (Figuras 16, 17 y 18) arrojando los siguientes resultados: Tabla V. Resultados de la Corrida 2. Licores Licor Madre Licor 1-2 Licor 2-3 Licor 3-4 Licor Final Licor M-F Acidez (g/L) Cu (g/L) Fe (g/L) 3.443 % Extracc Cu - % Fe Consumido - 374.04 3.84 361.623 301.53 320.26 312.101 312.101 3.26 3.115 2.318 2.053 2.053 4.245 5.943 6.981 8.82 8.82 15.10 4.45 25.59 11.43 46.54 23.29 49.32 53.44 102.73 156.17 Figura 16. Reacción del Licor de Lixiviación de la PACC con el Fierro. Figura 17. Cemento de Cobre Sacado de cada Garrafón. Figura 18. Filtración del Cemento de Cobre. Con la realización de esta prueba piloto nos pudimos percatar de varios aspectos importantes, mediante los cuales se generaron los siguientes puntos de discusión: • Al realizar la Corrida 1, se demostró que el exceso en el área de contacto generada por un exceso en la cantidad de fierro y una alta temperatura, aceleran la reacción y por ende, la formación de hidrogeno es muy agresiva (genera un burbujeo), hace que se produzca rápidamente una nata, provocando con ello el desbordamiento del material. • En la Corrida 2, la idea de poner poca cantidad de chatarra de fierro al inicio, e ir aumentando gradualmente la cantidad en cada garrafón, se hizo para que el licor fuera dejando poco a poco el cobre, siendo menos agresiva la reacción de un nivel a otro del proceso. • La extracción de cobre en el tren de cementación, fue casi del 50%, la cual se puede mejorar, regulando el sistema con flujos más lentos, así como también disminuyendo la temperatura. 4.1.3 Aproximación de la Cinética de la Reacción de Cementación Para hacer una aproximación de la cinética de reacción y con ello determinar los mejores parámetros en el proceso de cementación de cobre con chatarra de fierro, fue necesario calcular la constante de Velocidad (k) para calcular el porcentaje del metal que depositará por el método de cementación a una temperatura dada, para diferentes intervalos de tiempo; para lo cual se desarrolló la siguiente estrategia de análisis: Los resultados de este análisis, se presentan a continuación. Al desarrollar la reacción de cementación de cobre con chatarra de fierro, esta última con un área de 3801.336 cm2, en un recipiente con un volumen de operación de 12 L, y un volumen por alícuota de 20 mL, se obtuvieron los datos que se presentan en la Tabla VI. Para definir el modelo cinético para la reacción de cementación, se considera la ecuación siguiente: = (9) dónde: M = Concentración molar del ion metálico t= Tiempo (s) k = Constante de velocidad (cm/seg) A = Área del metal cementante (cm2) V = Volumen de la solución (cm3) Tabla VI. Variación de la Concentración de Cobre en el Licor con el Tiempo, a dos Temperaturas Diferentes. Tiempo (min) 0 10 20 30 40 Concentración (M) a 55° C 0.062343 0.059352178 0.053009318 0.048681063 0.04501385 Concentración (M) Volumen de a 28° C Sol (cm3) 0.062343 0.059683 0.058675 0.056015 0.053009 12000 11980 11960 11940 11920 Integrando la ecuación diferencial (9) y evaluando los límites de concentración del metal disuelto en el licor, a t = 0 y t = t, resulta la siguiente ecuación: = . (10) La ecuación (10) representa una línea recta, que pasa por el origen, con un valor de pendiente: = 2.303 . Esta ecuación corresponde al modelo cinético de una reacción de primer orden, la cual se desarrolla a temperatura constante. Los datos de la Tabla VI se sustituyeron en la ecuación del modelo cinético para la reacción de cementación, que aparece en la ecuación (10), dando lugar a los resultados presentados en la Tabla VII. Tabla VII. Valores del Término Vlog = . , Evaluado a Varios Intervalos de Tiempo y a dos Temperatura Diferentes. Tiempo (min) Muestra a 55° C Muestra a 28° C Área (cm2) Vlog(M0/Mt) Vlog(M0/Mt) 0 10 20 30 0 256 844 1285 0 227 315 556 3801.336 3801.336 3801.336 3801.336 40 1689 841 3801.336 Para conocer las constantes de velocidad de cada una de las corridas, desarrolladas a diferente temperatura, se construyeron los gráficos de la Figura 19, correspondientes al modelo integrado de la reacción de cementación, presentado en la ecuación (10). Comportamiento de las Muestras a Diferentes Temperaturas 1800 y = 44.062x - 66.527 R² = 0.9898 1600 Vlog(Mo/Mt) 1400 1200 1000 Muestra 55°C 800 Muestra 28°C 600 Lineal (Muestra 55°C) 400 Lineal (Muestra 28°C) y = 20.106x - 14.214 R² = 0.974 200 0 0 10 20 30 40 50 Tiempo (min) Figura 19. Gráfica Correspondiente al Término Vlog(M0/Mt) Vs Tiempo; a Temperatura de 55°C y 28°C. Con la pendiente obtenida en el ajuste de ambas gráficas, se puede obtener las constantes de velocidad, sustituyendo los datos en la ecuación siguiente: = (11) 2.303 dónde: m = La pendiente A= Área Despejando de la ecuación (11), se obtienen los valores de la constante de velocidad para ambas temperaturas (A= 55oC y B=28oC). k(A)= 0.026694506 cm/min k(B)= 0.01cm/min Para analizar el efecto de la temperatura sobre las constantes de velocidad, se utilizó la ecuación de Arrhenius: = , en términos de log =− + log . (12) Graficando log k Vs 1/T, (Figura 20), se obtiene una línea recta, donde la pendiente m adopta el valor: =− . 0.00 Log K -0.50 -1.00 y = -1.2471x + 2.2269 R² = 1 -1.50 -2.00 -2.50 3 3.05 3.1 3.15 1X103/T Figura 20. 3.2 3.25 3.3 3.35 (1/oK) Gráfico del Efecto de la Temperatura sobre la Velocidad de la Reacción de Cementación. Ecuación de Arrhenius. Sustituyendo el valor de R = 1.987 Kcal/mol°K, se obtiene un valor de la energía de activación, Ea= 5.71 Kcal. La energía de activación del proceso es importante para determinar la etapa controlante de la velocidad Control por difusión Ea < 6 Kcal/mol Control químico Ea > 10 Kcal/mol Control Mixto 6 Kcal/mol < Ea < 10 Kcal/mol En base al análisis anterior, determinado mediante los datos experimentales, se deduce que la reacción de cementación de cobre con chatarra de fierro, analizada en este estudio, es un proceso controlado por difusión. Por otro lado, con el comportamiento del gráfico de la Figura 20, se pueden interpolar, si así se requieren, valores de constantes de velocidad, a niveles de temperatura diferentes a los utilizados en las Corridas 1 y 2, de este trabajo. Por ejemplo, la Tabla VIII, muestra los valores de la constante de velocidad de la reacción de cementación para los valores de temperatura de 55oC y 28oC, obtenidos experimentalmente, así como el valor interpolado de la constante de velocidad a 40oC, obtenido con el gráfico de la Figura 20 (Log K40°C= -1.76, K40°C= 0.02 cm/min). Tabla VIII. Valores de Log K, para Diferentes Temperaturas. T (°C) Log K 1X103/T 55 -1.57 3.047386866 40 -1.76 3.193357816 28 -1.91 3.32060435 Una vez obtenida la energía de activación del proceso, se hace un análisis retrospectivo, a fin de encontrar los datos de porcentajes de cementación con respecto al tiempo, para la velocidad de reacción de cementación. Tabla IX. Aproximación de la k para Determinar el Porcentaje Reaccionado a Diferentes Condiciones de Operación Conc. Cu (M) Tiempo (min) [Cu ]0/[Cu ]t 0 30 60 90 120 150 180 210 240 1.000000 1.209289 1.462379 1.768438 2.138552 2.586127 3.127374 3.781897 4.573405 2+ 2+ 2+ [Cu ]t 0.062343 0.051553 0.042631 0.035253 0.029152 0.024107 0.019934 0.016484 0.013632 % Reaccionado 0 17.3067541 31.6182709 43.4529286 53.2393913 61.3321348 68.0242872 73.5582452 78.1344547 4.1.4 Simulación del Proceso de Cementación, Utilizando un Precipitador Individual Después de tener los antecedentes teóricos, experimentales y el análisis de la cinética del proceso de cementación de cobre con chatarra de fierro, se simuló una prueba escalada a nivel piloto para un proceso de cementación operando a 40°C, con un solo precipitador individual, en lugar del tren utilizado en la fase experimental, donde se encontraron las relaciones reales de consumo de chatarra de fierro, tiempo de residencia y eficiencia del proceso. En base a esta prueba, se proyecta el diseño de un precipitador de 14 m3 de capacidad, dónde el licor contaría con poco más de 2 horas de tiempo de residencia, en contacto con la chatarra de fierro, lo cual es más que suficiente para que la cementación alcance un 80% de eficiencia. Bajo estas condiciones de operación, se recuperan 10,100 Kg de Cu/mes, con un consumo de 21.5 Ton/mes de chatarra de fierro. Tabla X. Resultados de la Simulación de un Decantador Piloto. Figura 21. Precipitador en la Simulación de una Planta Piloto de Cementación. Figura 22. Precipitador para una Planta de Cementación. El mercado local, maneja un costo de chatarra de alrededor de $5.0 /kg de Fe, lo cual representaría un costo de 10.01 pesos/Kg Cu cemento. Teóricamente éste se relacionaría con los valores límites para el aumento en el costo de esta materia prima, ya que la depreciación se estima sea de alrededor de 2.86 pesos/Kg Cu para 5 años de recuperación. 4.1.5 Evaluación General del Proceso de Cementación En base a la investigación realizada del proceso de cementación de cobre con chatarra de fierro, se encontró que es una opción muy viable y rentable para la instalación de una planta, ya que las recuperaciones de cobre son bastante buenas y la operación de la planta muy sencilla. En este trabajo, se analizaron exhaustivamente todos los aspectos importantes, mismos que pueden influir en el desarrollo este proceso, de donde se destacan los factores relacionados con el área de contacto y los tiempos de residencia entre el licor y la chatarra fierro, como los dos puntos fundamentales para lograr una buena cantidad de cobre cemento; es por ello, que en tanto el sistema cuente con una agitación más eficiente, se alcanzará una mejor recuperación de cobre. Por lo que corresponde a la cinética de la reacción, se encontró que a mayor temperatura, la reacción se hace muy violenta e incontrolable (mayor a 50°C), por lo que es indispensable tener un control adecuado de este parámetro. Al principio de esta investigación, se pensaba que la acidez en el proceso de cementación de cobre era uno de los principales obstáculos para un desarrollo óptimo del proceso, debido a que la acidez del licor de PACC es extremadamente alta (aprox. 400 g/L), sin embargo, con el avance de la investigación de las pruebas preliminares, se encontró que la acidez en combinación con la temperatura, beneficia la rapidez de la reacción, pero afecta en buena medida la cantidad de fierro consumida por efecto de las reacciones secundarias. Los resultados de laboratorio, también revelan que la acidez prácticamente se mantiene constante en la cementación, teniendo solo una ligera disminución, lo cual es satisfactorio, ya que se quiere obtener al final del proceso, un residuo líquido con alta acidez para su posterior venta a clientes potenciales. En general, el desarrollo del proceso de cementación de cobre a partir de los licores de la PACC, resultó satisfactoria, si está se maneja bajo las condiciones de operación favorables, descritas anteriormente. 4.2 Evaluación del Proceso de Cristalización de Sulfato de Cobre A lo largo del proceso de cristalización descrito en la sección anterior, se fueron formando gradualmente los cristales de sulfato de cobre. En las figura 23 y 24 se muestra el avance de la cristalización a diferentes tiempos: Figura 23. Muestra 1 y Muestra 2 (Respectivamente) después de 3h de Reposo. Figura 24. Cristales Muestra 1 y Muestra 2 (Respectivamente) al Final del Proceso. La Tabla XI muestra la diferencia en peso, al final del proceso de cristalización de sulfato de cobre para las dos muestras analizadas (Muestra 1 y 2). Tabla XI. Pesos de los Cristales en las Muestras 1 y 2 Muestra 1 2 Peso (gr) 17.52 29.52 Mediante los pesos correspondientes a cada muestra, se puede apreciar que la diferencia en la formación de cristales de una muestra a otra es bastante apreciable, ya que la Muestra 2 es el 168.49% más grande que la Muestra 1. Cabe mencionar, que en la sección metodológica se enfatizó que ambas muestras contaban con la misma solución, solo que a la Muestra 2 se le evaporo el 20% de su volumen, experimentado ambas el mismo tiempo de reposo; por lo anterior se puede constatar que la eficiencia de formación de cristales, es directamente proporcional a la concentración de sulfato de cobre, vía la evaporación de un porcentaje de su volumen, incrementado la formación de estos cristales. En base a lo anterior, se pueden discutir los siguientes puntos con respecto a la cristalización de sulfato de cobre: • La ley de cobre que se maneja en los licores de la PACC, es muy baja para este proceso, por lo que se tiene que saturar de este material, para poder cristalizar sulfato de cobre. • El sulfato de cobre se vende a muy buen precio, por ser una sustancia pura. • Contar un sistema de enfriamiento drástico para la cristalización, aumenta la eficiencia del sistema, formando cristales grandes en un menor tiempo. El proceso de cristalización de sulfato de cobre es rentable, solo si se tiene un método previo para concentrar los licores “débiles” de cobre, ya que así lo requiere el proceso. Con el desarrollo de la investigación de los diferentes procesos de recuperación de cobre a partir de los licores de la PACC, se puede llegar a definiciones concretas de propuestas muy satisfactorias, debido a su alta rentabilidad, y con ello, implementar un nuevo proceso en MOLYMEX, S.A. de C.V., el cual aproveche al máximo su materia prima, haciendo eficiente su sistema de recuperación de metales y que además, genere un ingreso más a la compañía. 4.3 Análisis Global de las Propuestas para la Recuperación de Cobre de los Licores de la PACC La Figura 25 resume las condiciones, ventajas y desventajas de la implementación de los procesos propuestos para la recuperación de cobre a partir de los licores de la PACC, donde destaca el proceso de cementación, como la alternativa más adecuada. Recuperación de Cobre en el Electrolito del PACC Electrodeposición Cementación Cristalización Producto: Placas de Cobre Producto: Cobre Cemento Producto: Sulfato de Cobre Operación Óptima: - Área de Contacto y Tiempos de Residencia Proporcionales a la Cantidad de Cu y Fe Añadidos. - Temperaturas Relativamente Bajas (<50°C) - Saturación de Cu los licores. - Contar con un Sistema de Enfriamiento Operación Óptima: - 30-55 g/L de Cu en Sol. - Acidez de Alrededor de 150 g/L No Rentable: Debido a las Condiciones No Aptas del Electrolito, Generaría Altos Costos de Operación. Operación Óptima: Rentable: Debido a que la Operación es Sencilla y Controlable. Rentable Parcialmente: Debido a que se tiene que tener un Proceso previo de Concentración de Cu, sin embargo, el Producto es Bien Cotizado. Figura 25.Comparación de los Procesos de Propuestos, para la Recuperación de Cobre de los Licores de la PACC. 4.4 Equipos Propuestos para el Proceso de Cementación, Considerado como Opción más Adecuada para la Recuperación de Cobre a partir de los licores de la PACC Como ya se constató anteriormente, el proceso de cementación, resultó ser la mejor opción para la recuperación de cobre de los licores de la PACC, por lo que las propuestas del equipo implementado para su ejecución, estarían fundamentados en los diseños de los precipitadores que se presentan en las Figuras 26 y 27. La Figura 26, presenta el esquema de un Cono Kennecott, mismo que se utilizó como modelo de diseño básico, para la construcción de la planta piloto de este estudio. La Figura 27, presenta el esquema de un Precipitador Denver, el cual ofrece características de agitación y recolección del producto, diferentes a los de los conos. Ambos equipos presentan características especiales, para la cementación de cobre, ya que cada uno de ellos ofrecen alternativas de diseño, para resolver los problemas más significativos del proceso de cementación, tales como: área de contacto, flujos y tiempos de residencia; por lo cual, se tendría que evaluar la mejor opción, desde el punto de vista económico. Por otro lado, en conjunto con cualquiera de estos equipos, también se requeriría de intercambiadores de calor, con el objeto de acondicionar la temperatura de la solución, a los niveles propuestos en este trabajo. Figura 26. Cono Kennecott [10]. Figura 27. Precipitador Denver [10].