PDF - DFarmacia.com
Anuncio
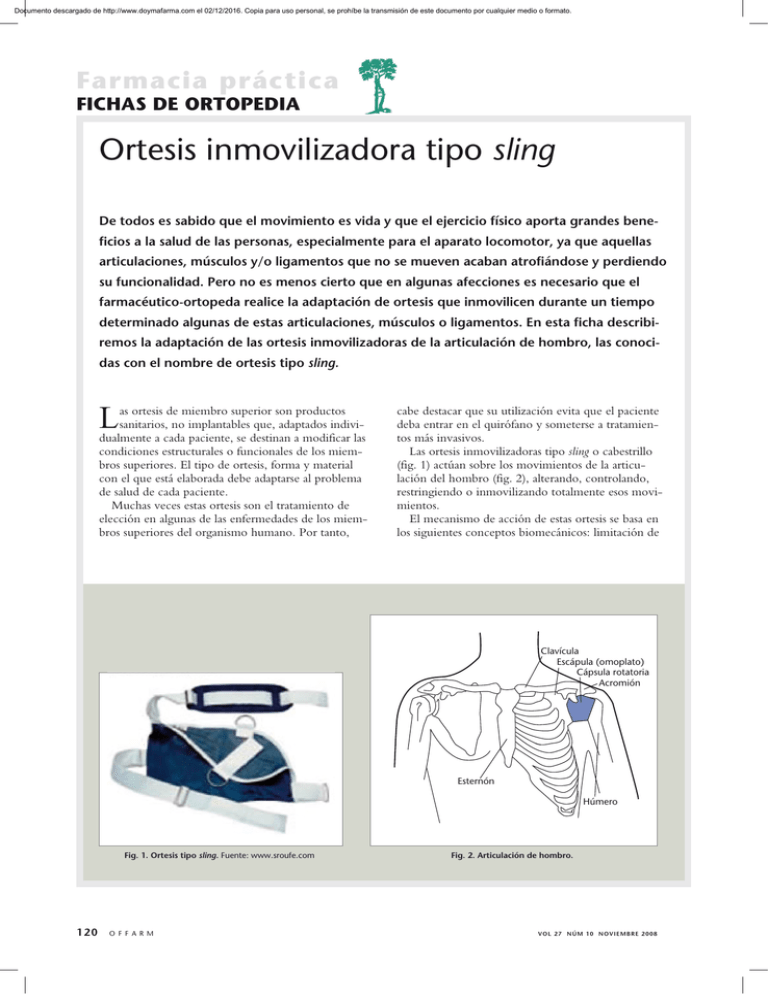
Documento descargado de http://www.doymafarma.com el 02/12/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Farmacia práctica Fichas de ortopedia Ortesis inmovilizadora tipo sling De todos es sabido que el movimiento es vida y que el ejercicio físico aporta grandes beneficios a la salud de las personas, especialmente para el aparato locomotor, ya que aquellas articulaciones, músculos y/o ligamentos que no se mueven acaban atrofiándose y perdiendo su funcionalidad. Pero no es menos cierto que en algunas afecciones es necesario que el farmacéutico-ortopeda realice la adaptación de ortesis que inmovilicen durante un tiempo determinado algunas de estas articulaciones, músculos o ligamentos. En esta ficha describiremos la adaptación de las ortesis inmovilizadoras de la articulación de hombro, las conocidas con el nombre de ortesis tipo sling. L as ortesis de miembro superior son productos sanitarios, no implantables que, adaptados individualmente a cada paciente, se destinan a modificar las condiciones estructurales o funcionales de los miembros superiores. El tipo de ortesis, forma y material con el que está elaborada debe adaptarse al problema de salud de cada paciente. Muchas veces estas ortesis son el tratamiento de elección en algunas de las enfermedades de los miembros superiores del organismo humano. Por tanto, cabe destacar que su utilización evita que el paciente deba entrar en el quirófano y someterse a tratamientos más invasivos. Las ortesis inmovilizadoras tipo sling o cabestrillo (fig. 1) actúan sobre los movimientos de la articulación del hombro (fig. 2), alterando, controlando, restringiendo o inmovilizando totalmente esos movimientos. El mecanismo de acción de estas ortesis se basa en los siguientes conceptos biomecánicos: limitación de Clavícula Escápula (omoplato) Cápsula rotatoria Acromión Esternón Húmero Fig. 1. Ortesis tipo sling. Fuente: www.sroufe.com 120 O ff a r m Fig. 2. Articulación de hombro. vol 27 nÚM 10 noviembre 2008 Documento descargado de http://www.doymafarma.com el 02/12/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. los movimientos rotacionales de la articulación del hombro, reducción de las fuerzas de cizalladura o los movimientos de traslación intraarticular producidos por esas fuerzas en el hombro y reducción de la carga axial generada por el peso corporal, que se transmite a través de las estructuras óseas y de los cartílagos articulares y mediante la fijación esquelética proximal y distal (fijación del brazo y del antebrazo). En definitiva, tal y como indica Viladot, nos interesa, con el uso de estas ortesis, soportar y fijar la extremidad superior en una posición determinada. Descripción y tipos de ortesis inmovilizadoras tipo sling Son ortesis confeccionadas en material textil, generalmente acolchado, que permite la adherencia del velcro en toda la superficie del soporte (fig. 3). Este sistema de sujeción por velcro hace que sea un soporte de fácil y rápida adaptación. La composición del material con el que están confeccionadas es, en su cara externa, de poliamida (65%) y en su cara interna, de poliéster (35%). Están constituidas por cuatro piezas: soporte de antebrazo, sistema de suspensión (cinta con anillas), cinta larga con dos velcros y cinta corta con dos velcros. En general, se fabrica una sola talla, universal, debido a que el material con el que está confeccionada permite una fácil adaptación. No obstante, algunos Fig. 3. Inmovilizador tipo sling. vol 27 nÚM 10 noviembre 2008 fabricantes confeccionan una versión pediátrica y también algunos modelos más ligeros y más confortables de llevar, en varias tallas (fig. 4). Indicaciones y mecanismo de acción El objetivo terapéutico de estas ortesis es la inmovilización del hombro en abducción, rotación y antepulsión. Por ello se utilizan en aquellos problemas en los que es necesario un reposo absoluto de la articulación glenohumeral (fig. 5). De esta manera, están indicadas en fracturas subcapitales de humero, fracturas de clavícula, luxaciones acromioclaviculares y tratamientos de traumatismos de hombro y brazo con inmovilización del hombro y soporte del peso del brazo. Adaptación y precauciones de uso Lo primero que hay que indicar es que estas ortesis se deben adaptar siguiendo estrictamente las indicaciones del médico prescriptor. Para adaptarlas correctamente se coloca el antebrazo sobre el soporte pasando la cinta sobre el hombro contrario y haciéndola atravesar por la anilla central del sistema de suspensión. Se adaptará la longitud del soporte de antebrazo doblando el extremo distal hacia el interior. Fig. 4. Inmovilizador tipo sling ligero y más confortable. O f f a r m 121 Documento descargado de http://www.doymafarma.com el 02/12/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Farmacia práctica fichas de ortopedia Clavícula Cabeza del húmero Vista superior Cabeza humeral Cavidad glenoide Húmero Fig. 5. Anatomía del hombro con detalle de la articulación glenohumeral. Para mantener la sujeción del codo, la cinta larga con los dos velcros se une al codo y rodeando la cintura se une a la anilla lateral del sistema de suspensión. Finalmente, la cinta corta que tiene dos velcros se utiliza para cerrar el soporte. Hay que evitar ejercer una presión excesiva en el ajuste de los velcros. No hay que exponer la prenda a una llama o fuente calorífica a temperaturas altas ya que se puede deteriorar. En cuanto a la limpieza, hay que hacerlo con agua fría y utilizando jabón neutro, no se debe utilizar lejía ni lavar en seco. Para secarla se extenderá la ortesis con la precaución de que no le dé directamente el sol o una fuente calorífica. Efectos secundarios El uso de este producto puede ocasionar en algunos pacientes la aparición de efectos secundarios, a saber: • Problemas cutáneos. • Erosiones en la piel como consecuencia de alteraciones de la sensibilidad cutánea. • Roce en bordes de las ortesis cuando no están bien adaptadas a los límites anatómicos (pliegues de flexión). • Dermatitis por contacto o exceso de sudoración. • Úlceras por presión debidas al apoyo sobre prominencias óseas no modeladas adecuadamente. • Lesiones por fricción en tejidos blandos. • Debilidad o atrofia muscular. • Retracción muscular o rigidez articular en la zona inmovilizada, sobre todo en el codo cuando no se utiliza correctamente • Dificultad en retorno venoso si la ortesis tiene cinchas muy apretadas. n Bibliografía general Baehler AR. Técnica ortopédica: Indicaciones. Tomo II. Extremidad superior. Columna vertebral. Miscelánea. Barcelona: Masson; 1999. Catálogo de EMO S.L. 2007 Cohí O, Viladot R, Clavell J. Ortesis de soporte. Capítulo 3. En: Ortesis y Prótesis del Aparato Locomotor. 3. Extremidad Superior. Barcelona: Masson; 1995. Consejo Interterritorial del Sistema Nacional de Salud. Guía descriptiva de ortoprótesis. Tomo 1. Sillas de ruedas, Prótesis especiales y Ortesis de columna vertebral. Madrid: Ministerio de Sanidad y Consumo; 2000. Flores J. Ortesis de miembro superior. Tipos. Indicaciones y chequeo. Disponible en: www.cofano.org (consultado en septiembre de 2008). healthcare.utah.eu/.../shoulder.htm (consultado en septiembre de 2008). Sling-Cabestrillo inmovilizador de hombro. Disponible en: http:// www.infoelder.com (consultado en septiembre de 2008). University of Utah. Health Sciences Center. Shoulder disponible en: Viosca E. Guía de uso y prescripción de productos ortoprotésicos a medida. Valencia: Instituto de Biomecánica;1999. JOSÉ GORGUES Farmacéutico coordinador del Área de Ortopedia del COF de Valencia ([email protected].) 122 O f f a r m vol 27 nÚM 10 noviembre 2008 Documento descargado de http://www.doymafarma.com el 02/12/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. QUETIAPINA ALTER 25 mg comprimidos recubiertos con película EFG QUETIAPINA ALTER 100 mg comprimidos recubiertos con película EFG QUETIAPINA ALTER 200 mg comprimidos recubiertos con película EFG QUETIAPINA ALTER 300 mg comprimidos recubiertos con película EFG COMPOSICIÓN. Cada comprimido recubierto con película contiene la cantidad nominal de quetiapina como quetiapina fumarato. Excipientes: Lactosa monohidrato, por comprimido: QUETIAPINA ALTER 25 mg, 41,18 mg. QUETIAPINA ALTER 100 mg, 164,72 mg. QUETIAPINA ALTER 200 mg, 329,44 mg. QUETIAPINA ALTER 300 mg, 494,16 mg. Para consultar el resto de excipientes, véase la sección Lista de Excipientes. FORMA FARMACÉUTICA. Comprimido recubierto con película, de color blanco, redondo biconvexo para QUETIAPINA ALTER 25 mg y QUETIAPINA ALTER 100 mg; oblongo para QUETIAPINA ALTER 200 mg y QUETIAPINA ALTER 300 mg. DATOS CLÍNICOS. Indicaciones Terapéuticas.- Tratamiento de la esquizofrenia. Tratamiento del episodio maníaco moderado a grave. Posología y Forma de Administración.- Quetiapina se administrará bid, con o sin alimentos. Adultos: Tratamiento de la esquizofrenia: 50 mg (día 1), 100 mg (día 2), 200 mg (día 3) y 300 mg (día 4). A partir del cuarto día, la dosis se ajustará a la dosis efectiva usual de 300-450 mg/día. Dependiendo de la respuesta clínica y tolerabilidad de cada paciente, la dosis se puede ajustar entre 150-750 mg/día. Tratamiento de los episodios maníacos asociados al trastorno bipolar: 100 mg (día 1), 200 mg (día 2), 300 mg (día 3) y 400 mg (día 4). Los ajustes posológicos posteriores hasta 800 mg/día en el día 6 deben realizarse mediante incrementos no superiores a 200 mg/día. La dosis puede ajustarse dependiendo de la respuesta clínica y tolerabilidad de cada paciente dentro del rango de 200-800 mg/día. Ancianos: Quetiapina deberá emplearse con precaución, especialmente durante el periodo inicial de tratamiento. Niños y adolescentes: La seguridad y eficacia de quetiapina no se han evaluado en niños y adolescentes. Alteración renal: No se requiere ajuste posológico. Alteración hepática: Quetiapina se metaboliza extensamente por el hígado. Los pacientes con alteración hepática conocida deberán iniciar el tratamiento con 25 mg/día. La dosis se aumentará diariamente en incrementos de 25-50 mg/día hasta una dosis efectiva, dependiendo de la respuesta clínica y tolerabilidad de cada paciente. Contraindicaciones.- Hipersensibilidad a alguno de los componentes. Está contraindicada la administración concomitante de inhibidores del citocromo P450 3A4,(inhibidores de las proteasas del VIH, antifúngicos de tipo azol, eritromicina, claritromicina y nefazodona). Advertencias y Precauciones Especiales de Empleo.- Cardiovascular: Quetiapina se empleará con precaución en pacientes con enfermedad cardiovascular, enfermedad cerebrovascular u otras condiciones que predispongan a hipotensión. Puede inducir hipotensión ortostática, especialmente durante el periodo inicial de titulación de dosis, más frecuente en pacientes ancianos que en jóvenes. Prolongación del intervalo QT: Quetiapina debe emplearse con precaución en pacientes con historial familiar de prolongación del intervalo QT. En estudios clínicos, y utilizada de acuerdo con la ficha técnica, quetiapina no se asoció a incrementos persistentes del intervalo absoluto QT. Sin embargo, en caso de sobredosis sí se observaron prolongaciones del intervalo QT. Ancianos con psicosis relacionada con demencia: No está aprobada la indicación. Quetiapina debe utilizarse con precaución en pacientes con factores de riesgo de accidentes cerebrovasculares. Convulsiones: Como con otros antipsicóticos, se recomienda precaución cuando se trate a pacientes con un historial convulsivo. Síntomas extrapiramidales: En ensayos clínicos controlados, la incidencia de síntomas extrapiramidales no fue diferente de la de placebo dentro del intervalo de dosis terapéutica recomendado. Discinesia tardía: Si aparecen signos y síntomas de discinesia tardía, se deberá considerar la reducción de la dosis o la interrupción del tratamiento con quetiapina.. Síndrome neuroléptico maligno: Se ha asociado al tratamiento con antipsicóticos, incluyendo quetiapina. Las manifestaciones clínicas incluyen hipertermia, estado mental alterado, rigidez muscular, inestabilidad autonómica y aumento de CPK. En tal caso, se interrumpirá la terapia con quetiapina y se administrará el tratamiento médico apropiado. Interacciones: El uso concomitante de quetiapina con un inductor de enzimas hepáticos, como carbamazepina o fenitoína, disminuye sustancialmente las concentraciones plasmáticas de quetiapina, lo que puede afectar a la eficacia del tratamiento. Debe evitarse el uso concomitante con neurolépticos. Hiperglucemia: Muy raramente, se han comunicado casos de hiperglucemia o exacerbación de la diabetes preexistente. Es aconsejable una monitorización apropiada en diabéticos y en pacientes con factores de riesgo para el desarrollo de diabetes mellitus. Información adicional: Los datos de quetiapina en combinación con valproato o litio en los episodios maníacos moderados a graves son limitados; sin embargo, el tratamiento en combinación fue bien tolerado. No se dispone de datos sobre el tratamiento en combinación más allá de la semana 6. Lactosa: Este medicamento contiene lactosa. Los pacientes con intolerancia hereditaria a galactosa, de insuficiencia de lactasa de Lapp o problemas de absorción de glucosa o galactosa no deben tomar este medicamento. Retirada: Se recomienda una retirada gradual del fármaco. Interacción con otros medicamentos y otras formas de interacción.- Estudios de interacción sólo han sido realizados en adultos. Interacciones con fármacos de acción central y alcohol: Quetiapina empleará con precaución en combinación con otros fármacos de acción central y alcohol. Fármacos responsables de la prolongación del intervalo QT e inhibidores metabólicos: Debe actuarse con precaución en caso de prescribir quetiapina junto con fármacos que provoquen prolongación del intervalo QT, fármacos causantes de desequilibrios electrolíticos y los inhibidores metabólicos (citocromo P450). El P450 (CYP) 3A4 es el principal enzima responsable del metabolismo de quetiapina. Por esto, está contraindicado el uso concomitante de quetiapina con inhibidores de CYP3A4. Zumo de pomelo: No se recomienda tomar quetiapina con zumo de pomelo. Inductores de enzimas hepáticos: Carbamazepina y Fenitoina incrementan significativamente el aclaramiento de quetiapina, lo que puede producir concentraciones plasmáticas menores, que pueden afectar a la eficacia del tratamiento con quetiapina. En pacientes tratados con un inductor de enzimas hepáticos, el tratamiento con quetiapina se deberá iniciar solamente si el médico considera que los beneficios de quetiapina superan los riesgos de retirar el inductor de enzimas hepáticos. Antidepresivos: La farmacocinética de quetiapina no se alteró significativamente por la co-administración de imipramina o fluoxetina. Antipsicóticos: La farmacocinética de quetiapina no se alteró significativamente por la co-administración de risperidona o haloperidol. El uso concomitante de quetiapina y tioridazina provocó un aumento en el aclaramiento de quetiapina de aproximadamente el 70%. Cimetidina, Litio: La farmacocinética de quetiapina no se alteró tras la co-administración con cimetidina o con litio. Valproato: La farmacocinética de valproato de sodio y de quetiapina no se alteró de forma clínicamente relevante cuando se administraron simultáneamente. Fármacos cardiovasculares: No se han realizado estudios formales de interacción con fármacos cardiovasculares. Embarazo y lactancia.Quetiapina solamente se utilizará durante el embarazo si los beneficios justifican los riesgos potenciales. Tras el empleo de quetiapina en el embarazo, se observaron síntomas de abstinencia neonatal. Se aconsejará a las mujeres en periodo de lactancia que eviten dicha lactancia durante el tratamiento. Efectos sobre la capacidad para conducir y utilizar máquinas.- Se deberá aconsejar a los pacientes que no conduzcan o utilicen maquinaria hasta que se conozca la susceptibilidad individual. Reacciones Adversas.Las incidencias de las RAs asociadas al tratamiento con quetiapina son: Investigaciones: Frecuentes (≥1/100, <1/10): Aumento de peso, elevación de las transaminasas séricas (ALT, AST). Poco frecuentes (≥1/1.000, <1/100): Elevación de los niveles de gamma-GT, elevación de los niveles de triglicéridos séricos en periodos de no ayuno, elevación del colesterol total. Cardíacas: Frecuentes: Taquicardia. Raras (≥1/10.000, <1/1.000): muerte súbita por motivos desconocidos, paro cardiaco, arritmias ventriculares (VF, VT), prolongación del intervalo QT, Torsades de pointes. Sistema sanguíneo y linfático: Frecuentes: Leucopenia. Poco frecuentes: Eosinofilia. Muy raras (<1/10.000): Neutropenia. Sistema nervioso: Muy frecuentes (≥1/10): Mareo, somnolencia, cefalea. Frecuentes: Síncope. Poco frecuentes: Convulsiones. Muy raros: Discinesia tardía. Respiratorias, torácicas y mediastínicas: Frecuentes: Rinitis. Gastrointestinales: Frecuentes: Sequedad de boca, estreñimiento, dispepsia. Cutáneas y del tejido subcutáneo: Muy raras: Angioedema, síndrome de Stevens-Johnson. Metabolismo y nutricionales: Muy raras: Hiperglucemia, diabetes mellitus. Vasculares: Frecuentes: Hipotensión ortostática. Generales: Frecuentes: Astenia leve, edema periférico. Raras: Síndrome neuroléptico maligno. Sistema inmunitario: Poco frecuentes: Hipersensibilidad. Hepato-biliares: Raras: Ictericia. Muy raras: Hepatitis. Aparato reproductor: Raras: Priapismo. Sobredosis.- Se han tomado dosis estimadas de hasta 20 g, sin desenlaces mortales. En la experiencia post-comercialización, se han producido notificaciones muy raras de sobredosis sólo con quetiapina que causaron fallecimiento o coma, o prolongación de QT. En general, los signos y síntomas comunicados fueron resultado de la exacerbación de los efectos farmacológicos conocidos del fármaco. No existe antídoto específico, recomendándose procedimientos de cuidados intensivos incluyendo el establecimiento y mantenimiento de una vía aérea abierta que asegure la oxigenación y ventilación adecuadas y la monitorización y apoyo del sistema cardiovascular. DATOS FARMACÉUTICOS. Lista de excipientes.- Lactosa monohidrato, celulosa microcristalina, fosfato cálcico dibásico dihidratado, povidona K30, carboximetilalmidón sódico de patata sin gluten, estearato cálcico, hipromelosa, E171 y triacetato de glicerol. Incompatibilidades.- No procede. Periodo de validez.- 2 años. Precauciones especiales de conservación.- No se precisan. Naturaleza y contenido del envase.Envase alveolar de PVC blanco opaco y aluminio. Quetiapina Alter 25 mg comprimidos recubiertos: 6 comprimidos. Quetiapina Alter 100 mg comprimidos recubiertos, Quetiapina Alter 200 mg comprimidos recubiertos y Quetiapina Alter 300 mg comprimidos recubiertos: 60 comprimidos. Precauciones especiales de eliminación y otras manipulaciones.- Ninguna especial. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN. LABORATORIOS ALTER, S.A. - Mateo Inurria, 30 - 28036 Madrid. Condiciones de dispensación: Con receta médica. Reembolsable por el Sistema Nacional de Salud. Aportación reducida. Presentaciones y PVP: QUETIAPINA ALTER 25 mg comprimidos recubiertos con película EFG, 6 comprimidos (PVP IVA 3,22 €). QUETIAPINA ALTER 100 mg comprimidos recubiertos con película EFG, 60 comprimidos (PVP IVA 61,65 €). QUETIAPINA ALTER 200 mg comprimidos recubiertos con película EFG, 60 comprimidos (PVP IVA 93,71 €). QUETIAPINA ALTER 300 mg comprimidos recubiertos con película EFG, 60 comprimidos (PVP IVA 146,16 €). Para más información, consulte la ficha técnica completa o al Departamento Médico de Laboratorios Alter, S.A. Tfno. 913 592 000. Diciembre 2007 (01a) enteras jano.indd 1 22/10/08 10:29:49









