View - Colegio Augusto Walte
Anuncio

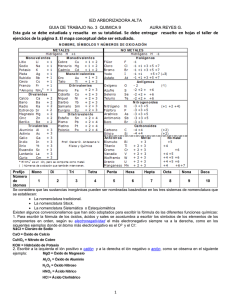
COLEGIO AUGUSTO WALTE. Materia: Química. Periodo II. Docente: Maricela de Morán. Primer Año de Bachillerato. CONTENIDO: NOMENCLATURA QUÍMICA DE LOS COMPUESTOS INORGÁNICOS. Estudiante: ____________________________________________________________________ Indicadores de logros: Indaga y explica con seguridad la nomenclatura de compuestos inorgánicos y describe las propiedades de los óxidos básicos, anhídridos u óxidos ácidos, hidruros no metálicos. Experimenta, identifica y explica las combinaciones químicas que dan como resultado compuestos ternarios: ácidos, bases y sales. Indaga y explica con seguridad la nomenclatura de compuestos inorgánicos y describe las propiedades de las sales haloideas e hidruros metálicos. Para nombrar compuestos inorgánicos, se aceptan 3 tipos de nomenclaturas: 1. Sistemática o estequiométrica. 2. Stock. 3. Tradicional. A continuación, se describen las características de cada una de las nomenclaturas referidas. Es importante señalar que para algunas funciones químicas las variantes son mínimas, por lo tanto, comprender las primeras familias es fundamental. Nomenclatura sistemática: para nombrar de este modo se usan prefijos numéricos excepto para indicar que el primer elemento de la fórmula sólo aparece una vez (mono) o cuando no puede haber confusión posible debido a que tenga un número de oxidación único. En adelante N.ss Prefijo griego Número Prefijo griego Número Mono 1 Hexa 6 Di 2 Hepta 7 Tri 3 Octa 8 Tetra 4 Nona o eneá 9 Penta 5 Deca 10 Ejemplos: CrBr3 tribromuro de cromo; CO monóxido de carbono Nomenclatura stock: En este caso, cuando el elemento que forma el compuesto tiene más de un número de oxidación, se indica en números romanos al final y entre paréntesis. Normalmente, a menos que se haya simplificado la fórmula, el número de oxidación puede verse en el subíndice del otro átomo (compuestos binarios). En adelante N.st Ejemplo: Fe2S3 Sulfuro de hierro (III) [se ve la valencia III en el subíndice del azufre] Nomenclatura tradicional: Aquí se indica el número de oxidación del elemento que forma el compuesto con una serie de prefijos y sufijos. En adelante N.tr. Número de oxidación Única Prefijos y Sufijos (de menor a mayor) Ico . Dos Oso e ico Tres Hipo - oso , oso e ico Cuatro Hipo - oso , oso, ico y Per - ico Cinco Hipo - oso , oso, ico, Per - ico e Hiper – ico 1 COMPUESTOS BINARIOS 1. FUNCIÓN ÓXIDOS Son compuestos químicos inorgánicos binarios formados por la unión del oxígeno con otro elemento diferente a los gases nobles. Según si este elemento es metal o no metal serán óxidos básicos u óxidos ácidos. El oxígeno siempre tiene número de oxidación 2-. Su grupo funcional es el ión oxigeno (O2). a) ÓXIDOS BÁSICOS Son aquellos óxidos que se producen entre el oxígeno y un metal. Fórmula: Metal2Ox si el número de oxidación del metal es par se simplifica. Ejemplo N ss Regla No se tienen en cuenta los números de oxidación sino que se menciona el prefijo de acuerdo al número que posea el oxígeno como subíndice K + O2 N st N tr El sufijo es de acuerdo El número romano es al número de igual al número de oxidación del elemento oxidación del elemento unido al oxígeno. unido al oxígeno K2O monóxido de dipotasio óxido de potasio óxido potásico Fe2O3 trióxido de dihierro óxido de hierro(III) óxido férrico Fe + O2 FeO monóxido de hierro óxido de hierro(II) óxido ferroso Sn + O2 SnO2 dióxido de estaño óxido de estaño (IV) óxido estánico Fe + O2 b) ÓXIDOS ÁCIDOS O ANHÍDRIDOS Son aquellos formados por la combinación del oxígeno con un no metal. Fórmula general: No Metal2Ox. Si se puede, se simplifica. En este caso, la nomenclatura tradicional. La nomenclatura sistemática es la más frecuente. Ejemplo N ss N st N tr No se tienen en cuenta los números de El número romano es Se emplea la palabra anhídrido en lugar oxidación sino que se igual al número de de óxido a excepción de un par de óxidos menciona el prefijo de oxidación del de nitrógeno como se muestran más acuerdo al número que elemento unido al adelante. posea el oxígeno como oxígeno. subíndice Regla S + O2 SO3 trióxido de azufre óxido de azufre(VI) anhídrido sulfúrico Cl2 + O2 Cl2O7 heptóxido de dicloro óxido de cloro(VII) anhídrido perclórico Los óxidos de nitrógeno, al igual que los óxidos del azufre son importantes por su participación en la lluvia ácida. Con el término óxido de nitrógeno se hace alusión a cualquiera de los siguientes: Óxido nítrico u Óxido de nitrógeno (II), de fórmula NO. Dióxido de nitrógeno, de fórmula NO2. Óxido nitroso o Monóxido de dinitrógeno, de fórmula N2O. Trióxido de dinitrógeno, de fórmula N2O3. Tetróxido de dinitrógeno, de fórmula N2O4. Pentóxido de dinitrógeno, de fórmula N2O5. 2- FUNCIÓN HIDRUROS Los hidruros son compuestos binarios que se originan de la combinación del hidrógeno con otro elemento. De acuerdo con el tipo de elemento con que se combine. Los hidruros se clasifican en: 2 a) HIDRUROS METÁLICOS Son compuestos binarios formados por hidrógeno con un metal. En estos compuestos, el hidrógeno siempre tiene número de oxidación -1. Se nombran con la palabra hidruro. Fórmula general: MH x (x=número de oxidación del metal) La nomenclatura stock es la más frecuente. Ejemplo N ss N st N tr KH monohidruro de potasio hidruro de potasio hidruro potásico NiH3 trihidruro de níquel hidruro de níquel(III) hidruro niquélico PbH4 tetrahidruro de plomo hidruro de plomo(IV) hidruro plúmbico b) HIDRUROS VOLATILES Son aquellos compuestos binarios constituidos por hidrógeno y un no metal. El hidrógeno siempre usa número de oxidación +1. Hay varios de ellos que tienen nombres especiales mucho más usados que los sistemáticos: Ejemplo Nombre más usado NH3 amoníaco o trihidruro de nitrógeno PH3 fosfina o trihidruro de fósforo BH3 borano o trihidruro de boro AsH3 arsina o trihidruro de arsénico SbH3 estibina o trihidruro de antimonio CH4 metano o tetrahidruro de carbono SiH4 silano o tetrahidruro de silicio 3- HIDRÁCIDOS Son aquellos hidruros no metálicos que forman disolución ácida en agua, se nombran de forma diferente según si están disueltos o en estado puro. Son los formados con S, Se, Te, F, Cl, Br, I. Si están puros se nombran de la forma -uro de hidrógeno y si están disueltos ácido -hídrico. Ejemplo en estado puro en disolución HF fluoruro de hidrógeno ácido fluorhídrico HCl cloruro de hidrógeno ácido clorhídrico HBr bromuro de hidrógeno ácido bromhídrico HI yoduro de hidrógeno ácido yodhídrico H2S sulfuro de hidrógeno ácido sulfhídrico H2Se seleniuro de hidrógeno ácido selenhídrico H2Te telururo de hidrógeno ácido telurhídrico 3 COMPUESTOS TERNARIOS. 4- FUNCIÓN HIDRÓXIDOS Son compuestos ternarios formados por la unión de un oxido básico con el agua. Para formularlo se coloca al metal y el grupo hidroxilo OH, que siempre tiene número de oxidación (-1). La fórmula general es M(OH)x siendo x el número de oxidación del metal. La nomenclatura stock es la más frecuente. Aquí la nomenclatura sistemática no antepone el prefijo mono cuando sólo hay un OH. Ejemplo N ss N st N tr No se tienen en cuenta los números de oxidación sino que se menciona el prefijo El número romano es de acuerdo al número que igual al número de posea el oxígeno como oxidación del elemento subíndice. unido al oxígeno. Se antepone el prefijo que Hidróxido de + metal + indique el numero de (número de oxidación) átomos de oxigeno +hidróxido de + metal. Regla Li + H2O El sufijo es de acuerdo al número de oxidación del elemento unido al oxígeno. Hidróxido de + metal + sufijo. LiOH hidróxido de litio hidróxido de litio hidróxido lítico Pb + H2O Pb(OH)2 dihidróxido de plomo hidróxido de plomo(II) hidróxido plumboso Al + H2O Al(OH)3 trihidróxido de aluminio hidróxido de aluminio hidróxido alumínico 5- FUNCIÓN OXIÁCIDOS O ÁCIDOS OXIGENADOS. Son compuestos ternarios formados por oxígeno, hidrógeno y un no metal, se obtienen al agregar una molécula de agua al correspondiente óxido ácido. Fórmula general H2O+N2Ox=HaNbOc (aquí N es un no metal). SO + H2O Ejemplo N ss N st N tr Regla Se denomina como ácido oxo-, dioxo-, trioxo(según nº de O)+ no metal terminado en -ico seguido del número de oxidación en nº romanos entre paréntesis. Si hay >1 átomo del no metal también lleva prefijo. Se denomina como oxo, dioxo- (según nº de oxígenos)+no metal terminado en -ato seguido de la valencia en números romanos entre paréntesis + "de hidrógeno". Si hay >1 átomo del no metal también lleva prefijo. No cambia con respecto a compuestos anteriores tan sólo que empieza por la palabra ácido. Ésta es la más frecuente. ácido dioxosulfúrico (II) dioxosulfato (II) de hidrógeno ácido hiposulfuroso H2SO2 Cl2O7 + H2O H2Cl2O8 SO3 + H2O H2SO4 HClO4 ácido tetraoxoclórico (VII) ácido tetraoxosulfúrico (VI) tetraoxoclorato (VII) de ácido perclórico hidrógeno tetraoxosulfato (VI) de hidrógeno ácido sulfúrico 4 El nitrógeno no forma oxiácidos con todos sus números de oxidación sino sólo con la 3 y la 5. Por otra parte, el fósforo, el arsénico y el antimonio forman ácidos especiales según se agregue 1, 2 ó 3 moléculas de agua llevando los prefijos meta-, piro- (o di-), y orto-, respectivamente, en la nomenclatura tradicional (se puede omitir el prefijo en el caso orto). Ejemplo P2O5 + H2O H2P2O6 Sb2O3 + 2H2O P2O5 + 3H2O HPO3 N ss N st N tr ácido trioxofosfórico (V) trioxofosfato (V) de hidrógeno ácido metafosfórico H4Sb2O5 ácido pentaoxodiestíbico (III) H6P2O8 H3PO4 pentaoxodiestibato (III) de ácido piroestiboso hidrógeno ácido tetraoxofosfórico (V) tetraoxofosfato (V) de hidrógeno ácido ortofosfórico o fosfórico Algunos metales también forman oxiácidos, como el cromo y el manganeso Ejemplo CrO3 + H2O Mn2O3 + H2O N tr Ejemplo N tr H2CrO4 ácido crómico MnO3 + H2O H2MnO4 ácido mangánico H2MnO3 ácido manganoso Mn2O7 + H2O HMnO4 ácido permangánico 6- FUNCIÓN SALES BINARIAS (SALES DE HIDRÁCIDOS O HALOIDEAS) Se obtienen sustituyendo los hidrógenos de los hidrácidos por un metal (que puede provenir de una base o directamente del catión). También hay otros no metales que forman sales iónicas como el boro, el silicio y el nitrógeno. Su nombre empieza por el no metal terminado en –uro, seguido del nombre del metal. La nomenclatura stock es la más frecuente. Ejemplo Ca(OH)2 + HF Fe + HCl CaF2 + FeCl3 + Co(OH)2 + H2S CoS + N ss N st N tr H2O difluoruro de calcio fluoruro de calcio fluoruro cálcico H2 tricloruro de hierro cloruro de hierro(III) cloruro férrico monosulfuro de cobalto sulfuro de cobalto(II) sulfuro cobaltoso H2O a) SALES DE OXOÁCIDOS (OXISALES U OXOSALES) Se trata de compuestos ternarios formados a partir de oxoácidos, sustituyendo los hidrógenos de este por un metal (que puede provenir de una base o directamente del catión). También se puede decir que son compuestos ternarios que resultan de la unión de un metal con un radical (un no-metal con oxígeno) Hay dos tipos: i) SALES NEUTRAS Son aquellas oxisales que han sustituido todos sus hidrógenos por un metal (que puede provenir de una base o directamente del catión). La nomenclatura stock y la sistemática coinciden. La tradicional es igual que las anteriores salvo en que los sufijos -oso e -ico se sustituyen por -ito y -ato respectivamente. La nomenclatura tradicional es la más frecuente. Ejemplo N ss y st N tr Zn2SiO4 tetraoxosilicato(IV) de zinc silicato de zinc Fe4(P2O7)3 heptaoxodifosfato(V) de hierro(III) pirofosfato férrico Al2(SO4)3 tetraoxosulfato(VI) de aluminio sulfato de aluminio o alumínico 5 ii) SALES ÁCIDAS Son aquellas sales en las que sólo se han sustituido parte de los hidrógenos. Se nombra anteponiendo al nombre hidrógeno-, dihidrógeno. En la nomenclatura tradicional también se puede indicar anteponiendo bi- si se ha quitado un hidrógeno. Ejemplo N ss y st N tr NaHSO4 hidrógenotetraoxosulfato(VI) de sodio hidrógenosulfato sódico o bisulfato sódico KH2PO4 dihidrógenotetraoxofosfato(V) de potasio dihidrógenofosfato(V) potásico o bifosfato potásico Ca(HCO3)2 hidrógenotrioxocarbonato(IV) de calcio hidrógeno carbonato o bicarbonato cálcico IONES CATIONES MONO Y POLIATÓMICOS Si son monoatómicos se nombran simplemente nombrando el elemento después de la palabra catión. Por ejemplo, Li + catión litio. Si el elemento tiene varios estados de oxidación, se usan números romanos (st) o los prefijos y sufijos hipo- oso, -oso, ico, per -ico (tr). Ejemplo Fe Nomenclatura st Nomenclatura tr 3+ catión hierro(III) catión férrico + catión cobre(I) catión cuproso Cu Cuando se trata de cationes poliatómicos, se distinguen dos casos: a) si proceden de oxoácidos se añade el sufijo -ilo al nombre del oxoácido correspondiente en nomenclaturas tradicional (éste puede indicar los números de oxidación en números romanos), también se puede nombrar en la stock. Es como el oxoácido sin moléculas de agua. Ejemplo Nomenclatura tr Nomenclatura st + catión nitroilo catión dioxonitrógeno(V) + catión nitrosilo catión monoxonitrógeno(III) 2+ catión sulfinilo o tionilo catión monoxoazufre(IV) 2+ catión sulfonilo o sulfurilo catión dioxoazufre(VI) + catión uranilo(V) catión dioxouranio(V) UO22+ catión uranilo(VI) catión dioxouranio(VI) 3+ catión vanadilo(V) catión monoxovanadio(V) + catión vanadilo (IV) catión dioxovanadio(IV) NO2 NO SO SO2 UO2 VO VO2 b) si proceden de hidruros, lleva el sufijo -onio. Ejemplo H 3O + NH4 + + PH4 SbH4 + Nombre hidronio u oxonio Ejemplo BiH4 fosfonio + Estibonio Arsonio + Bismutonio AsH4 Amonio H2S H2Cl Nombre + Sulfonio + Cloronio 6 ANIONES MONO Y POLIATÓMICOS a) Si son homoatómicos (todos los átomos son del mismo elemento) se añade el sufijo -uro a la raíz del nombre del elemento. Si hay varios átomos se usan prefijos cuantitativos y, si fuese necesario, la carga entre paréntesis. Ej. H - O 2- Nombre(s) Ej. - Hidruro O2 2- O2 - Cl óxido Br dióxido(2-), peróxido I - - Nombre(s) Ej. 2- Cloruro S Bromuro S22- Yoduro N Sulfuro ion disulfuro 3- Nitruro - dióxido(1-), superóxido Nombre(s) N3 trinitruro(1-), azida (nombre especial) b) si son heteroatómicos y proceden de oxiácidos, es decir, son los que intervienen en oxisales y similares se nombran como éstas, con sufijos ito y ato, sustituyendo las terminaciones oso e ico respectivamente. Ej. N. tr 2- SO4 SO3 ClO ClO2 ClO3 - ClO4 - BrO Hipoclorito Clorito Clorato Perclorato - BrO3 Hipobromito - Bromato - NO2 Nitrito - NO3 CrO4 Hipoyodito IO2 - Yodito IO3 - Yodato IO4 - IO Sulfito - Nitrato -2 Cromato 2- Dicromato Cr2O7 N. tr - Sulfato 2- - Ej. Peryodato 2- Manganato - Permanganato MnO4 MnO4 2- Carbonato 3- Borato PO3 3- Fosfito PO4 3- Fosfato 4- Silicato CO3 BO3 SiO4 c) si son heteroatómicos pero no proceden de oxisales o similares suelen terminar en -uro o en -oxido. Ejemplo Nombre(s) - Hidróxido - Cianuro NH2- Amiduro OH CN - HS hidrógenosulfuro(1-) HO2- hidrógenodióxido(1-), hidroperóxido NH 2- Imiduro 7 GUÍA DE TRABAJO. 1.- Complete el siguiente cuadro: Li + O2 Li2O Ba2+ BaO Nombre ss Monóxido de dilitio Nombre st Óxido de litio Nombre Tr Óxido lítico Ca2+ S6+ SO3 Fe3+ N3+ C4+ Cr3+ Se+4 2.- Escriba en los espacios correspondiente, el nombre de la sustancia obtenida cuando reacciona el elemento de la izquierda con el hidrógeno. H2 Hidrácido Hidruro metálico Hidruro volátil S P Si Na Se O2 Rb As N2 Cs 8 3- Copie los óxidos de la tabla 1 y escriba la formula y nombre, en las tres nomenclaturas, de las sustancias resultantes. H2O o OHLiOH Óxidos Li2O BaO Ba(OH)2 SO3 H2SO4 Nombre ss Hidróxido de litio Nombre st Hidróxido de litio Nombre Tr Hidróxido de lítico 4.- Escriba en los espacios en blanco, el nombre del ácido, la sal neutra que forman con el SODIO, y el nombre tradicional de esta sal. Fórmula del ácido Nombre ss Nombre st Nombre Tr H2CO3 HBrO3 H3PO3 HIO3 HClO4 H3PO4 H2Cr2O7 HNO3 H2SO4 HClO 9 5.- Escriba a la par de cada nombre, la fórmula correspondiente NOMBRE Oxido de aluminio FÓRMULA Anhídrido carbónico Anhídrido sulfuroso Cloruro de hidrógeno Acido perclórico Clorato de potasio Acido crómico Sulfato de bario Fosfato de sodio Cromato de litio Cloruro de plata Nitrato de cobalto (II) Acido bórico Hipoyodito de sodio Peryodato de potasio Acido nitroso Oxido de calcio Nitrato de plomo (II) Bicarbonato de sodio Permanganato de potasio Fosfato de calcio Hidróxido ferroso 10