Propiedades periódicas - SED | Colegio San Esteban Diácono
Anuncio

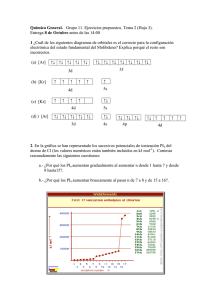
Colegio San Esteban Diácono Departamento de Ciencias Química – Iº Medio Prof. Juan Pastrián / Sofía Ponce de León GUÍA DE EJERCICIOS Nº4 “Propiedades periódicas” Objetivo: Comprender y analizar la variación de propiedades periódicas de tamaño y energía para diferentes elementos químicos en el sistema periódico. Habilidades: Comprender – Aplicar Instrucciones: A partir de lo trabajado en clases y con el apoyo de sus apuntes y texto de estudio (pág. 84 a 89), responda las siguientes preguntas: 1. ¿Qué es la carga nuclear efectiva? ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 2. Calcule la carga nuclear efectiva (Zef) para los elementos del período 3 del sistema periódico. Elemento 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar Configuración electrónica Carga nuclear efectiva (Zef = Z – a) 3. ¿Cómo varía la carga nuclear efectiva al desplazarse hacia la derecha por un período?. Fundamente. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 4. ¿Qué significa que el cloro tenga una mayor carga nuclear efectiva que el sodio? ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 5. Explique en qué consiste el efecto de apantallamiento. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 6. ¿Cómo podemos definir el radio atómico? Explique y represente su definición con una imagen y/o esquema. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 7. Respecto al radio atómico, explique: a) ¿Cómo varía al bajar por un grupo?, ¿por qué? …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… b) ¿Cómo varía al desplazarse hacia la derecha por un periodo?, ¿por qué? …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… 8. A partir del análisis del siguiente gráfico, ¿qué podemos concluir? ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 9. A partir del análisis del siguiente gráfico: a) ¿A qué periodo(s) pertenece(n) los elementos químicos cuyos radios atómicos se encuentran ahí graficados? …………………………………………………………………………………………………………… b) ¿Qué pasa con el Zef en la medida que aumenta el número atómico? …………………………………………………………………………………………………………… c) ¿Qué relación de proporcionalidad hay entre el radio atómico y la carga nuclear efectiva. Fundamemente. …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… 10. ¿Qué es el radio iónico? ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 11. ¿Cómo es el radio de un anión comparado con el radio de su átomo neutro?, ¿más grande o más pequeño? Fundamente. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 12. ¿Cómo es el radio de un catión comparado con el radio de su átomo neutro?, ¿más grande o más pequeño? Fundamente. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 13. Ordene, en base a su tamaño creciente, las siguientes secuencias de átomos e iones: a) 12Mg 2+ , 20Ca2+ y 20Ca …………………………………………………………………………………………………………… b) 2– 16S , 16S y 8O2– …………………………………………………………………………………………………………… 14. ¿Qué es la energía o potencial de ionización? ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 15. “Un átomo presenta una energía de ionización de 786 kJ/mol”. Explique el significado de la aseveración anterior. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 16. Si un átomo A presenta una mayor energía de ionización comparado con un átomo B, ¿podemos afirmar entonces que para extraer un electrón desde un átomo neutro de A en estado gaseoso se va a requerir mayor energía respecto a extraer un electrón desde un átomo neutro B en estado gaseoso? Explique ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 17. La primera energía de ionización del Be es 900 kJ/mol y la del B es 799 kJ/mol. Explique la diferencia entre estos dos valores. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 18. El siguiente gráfico representa la primera energía de ionización para los elementos del periodo 3. ¿Qué observa en el gráfico?, ¿qué podría inferir? 1521 1600 Energía / kJ mol-1 1400 1251 1200 1012 1000 600 786 738 800 1000 578 496 400 200 0 Na Mg Al Si P Elemento químico As Cl Ar ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 19. El siguiente gráfico representa las energías de ionización del fósforo (15P) 25000 Energía / kJ mol-1 20000 15000 10000 5000 0 I1 I2 I3 I4 I5 I6 Expliqué cada uno de sus valores y postule una posible explicación al aumento considerable en el valor de la sexta energía de ionización. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 20. Respecto a la energía de ionización, explique: a) ¿Cómo varía al bajar por un grupo?, ¿por qué? …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… b) ¿Cómo varía al desplazarse hacia la derecha por un periodo?, ¿por qué? …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… 21. ¿Qué es la afinidad electrónica o electroafinidad? ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 22. Respecto a la electroafinidad, explique: a) ¿Cómo varía al bajar por un grupo?, ¿por qué? …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… b) ¿Cómo varía al desplazarse hacia la derecha por un periodo?, ¿por qué? …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… 23. “La afinidad electrónica del flúor es -328 kJ/mol”. Explique el significado de la aseveración anterior. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 24. ¿Por qué la energía de ionización tiene un valor positivo y la electroafinidad tiene un valor negativo? Explique. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 25. ¿Qué es la electronegatividad? ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 26. Si un átomo P es más electronegativo que un átomo Q, ¿tiene mayor o menor tendencia a atraer los electrones compartidos en un enlace covalente? ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… 27. Respecto a la electronegatividad, explique: a) ¿Cómo varía al bajar por un grupo?, ¿por qué? …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… b) ¿Cómo varía al desplazarse hacia la derecha por un periodo?, ¿por qué? …………………………………………………………………………………………………………… …………………………………………………………………………………………………………… ……………………………………………………………………………………………………………