Les crioglobulines són immunoglobulines anormals que precipiten
Anuncio

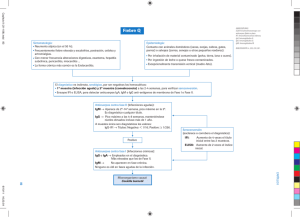
Laboratori de Referència de Catalunya S.A. Información Clínica INMUNOGLOBULINA G INTRODUCCIÓN Las Inmunoglobulinas (Ig) son un grupo de glucoproteínas sintetizadas por linfocitos B que tienen la propiedad de unirse, de forma especifica a otras moléculas, conocidas como antígenos. Las Ig tienen función de anticuerpo y su síntesis y excreción en la sangre y fluidos del cuerpo es el resultado de un proceso de activación antigénica en los órganos linfoides. La molécula de Ig esta constituida por dos tipos de cadenas polipeptídicas, las cadenas H o pesadas y las cadenas L o ligeras, que forman un conjunto simétrico (ver esquema) de cuatro cadenas unidas por puentes disulfuro. Las inmunoglobulinas se diferencian en cinco clases o isotipos dependiendo de la cadena pesada que las constituye: IgG (gamma, γ), IgA (alfa, α), IgM (mu, µ), IgD (delta, δ), e IgE ( epsilon, ε). Las cadenas ligeras son de dos tipos (kappa, κ y Lambda, λ) que se observan indistintamente en todos los isotipos. Las moléculas de IgG, IgD, e IgE estan formadas por monómeros de la unidad estructural H2L2, mientras que la IgM es una macromolécula, formada por un pentámero de esta unidad (H2L2)5, y la IgA puede presentarse en forma monomérica, dímérica o trimérica. Las cadenas pesadas H tienen una parte constante, constituida por los dominios C1,C2 y C3 y una parte variable (V). Las cadenas ligeras L presentan una región constante con un solo dominio el C1, y una región variable V, cuya estructura molecular coincide con la región variable de la cadena pesada. Dicha región variable esta constituida por 106 a 120 aminoácidos y a su vez presenta zonas de hipervariabilidad distintas en función de la especificidad que las ha activado. Las regiones hipervariables se denominan regiones determinantes de complementariedad (CDR), ubicadas en número de seis ( 3 y 3 por cadena) entre regiones de armazón llamadas regiones FR. Estas zonas de gran diversidad constituyen el sitio de unión al antígeno y determinan la especificidad antigénica de cada molécula. En un individuo puede existir mas de 106 moléculas de anticuerpo distintas. 07/06/2006 9:19 1 Laboratori de Referència de Catalunya S.A. Información Clínica La IgG: Es la inmunoglobulina mas abundante, comprende cerca del 80 % del total de inmunoglobulinas y esta igualmente distribuida en la sangre y líquido intersticial. Esta constituida por un monómero de dos cadenas pesadas y dos cadenas ligeras, lo que equivale a dos sitios de unión para el antígeno. La cadena pesada es la gamma (γ), y su peso molecular es de 150.000 daltons. Difunde bien a través de las membranas por ello se la encuentra en el liquido sinovial, liquido pleural, LCR, y en el humor acuoso. Pasa a través de la placenta y protege al feto en sus primeras semanas de vida. La IgG es la única Inmunoglobulina que da una efectiva inmunidad humoral en niños hasta los 7 a 9 meses de vida. Los anticuerpos IgG son los predominantes en las respuestas secundarias a un antígeno. Existen cuatro subclases conocidas como IgG1, IgG2, IgG3, e IgG4. Estas subclases se diferencian por el tamaño de la región bisagra y por el número de enlaces de disulfuro entre las cadenas pesadas. La IgG1 es la inmunoglobulina que predomina, mientras que la IgG4 es el mayor anticuerpo circulante libre entre tejidos. La IgG3 es la molécula mas efectiva como activadora de complemento seguida de la IgG1, y la IgG2. UTILIDAD CLÍNICA Concentraciones elevadas de IgG puede indicar infección crónica. Se halla incrementada en la hepatitis crónica, esclerosis múltiple, y algunas enfermedades autoinmunes, como el Lupus Eritematoso Sistémico y la tiroiditis de Hashimoto. Altos niveles de IgG pero de tipo monoclonal, a diferencia de los casos anteriores que se presentan de forma policlonal, están relacionados con presencia de mieloma múltiple. La síntesis de IgG está reducida en los síndromes de inmunodeficiencia congénita y adquirida y en deficiencias selectivas de subclase de IgG como la agammaglobulinemia o cuando hay una gammapatía monoclonal de otra inmunoglobulina que provoca la supresión de los clones que sintetizan IgG, como se da en la macroglobulinemia de Waldenström (IgM). La concentración disminuida de Ig en general, puede ser debida a una disminución de síntesis o a un aumento de su perdida. Si la función renal no está alterada, el cociente Albumina/Globulina nos ayuda a evaluar niveles bajos de Ig. Concentraciones disminuidas de IgG se observan en enteropatías con perdida proteica, en el síndrome nefrótico, y por quemaduras por perdida a traves de la piel. MÉTODO Inmunoturbidimetria. Test de medicion turbidimetrica de la aglutinación del complejo antigeno-anticuerpo. 07/06/2006 9:19 2 Laboratori de Referència de Catalunya S.A. Información Clínica INTERFERENCIAS Entre los factores que pueden interferir en la cuantificación de las Inmunoglobulinas. - Medicamentos: corticoides, hidralazina. - Tratamientos de cáncer quimioterapia y radioterapia. - Transfusiones de sangre en los 6 meses anteriores. - Vacunas en los 6 meses anteriores. - Uso de alcohol o drogas. - Contraste radioactivo practicado en menos de 3 días PROTOCOLO DE ANÁLISIS Es recomendable el estudio conjunto de la IgG (4150), la IgA (4160), y la IgM (4170). En el estudio de gammapatías también de cadenas kappa y lambda (4175). En infecciones recurrentes de vías respiratorias, se aconseja el estudio de las subclases de IgG (4153, 4154, 4155, 4156). BIBLIOGRAFIA - Birger Blombäck and Lars, A Hanson Plasma Proteins. 1979. Ed John Wiley and Sons. Interscience Publication. Farreras P y Rozman C. Medicina interna, Ed Doyma, 1995.Ed.13. Nissl J. Immunoglobulins. A-Z Health Guide from WebMD: Medical Test. 2004. 07/06/2006 9:19 3