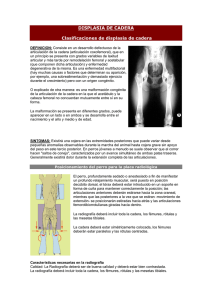
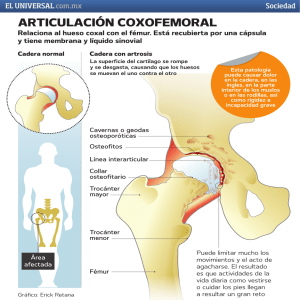
Cadera y Rodilla
Anuncio

Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT “Temas selectos de actualización en la Ortopedia Latinoamericana” Capítulo Cadera y Rodilla Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Pinzamiento Femoroacetabular Bernardo Aguilera B, M.D.*, Andrés F. Aranzazu Toro, M.D.**, José F. Castillo Sáenz, M.D.**. *Ortopedia y Traumatología – Coordinador Grupo de Cirugía de cadera y reemplazos articulares Clínica de preservación de la cadera del Instituto de Enfermedades Osteoarticulares del Centro Médico Imbanaco. **Ortopedia y Traumatología – Fellow Cirugía de Cadera y Rodilla – Pontificia Universidad Javeriana (Santiago de Cali) - Instituto de Enfermedades Osteoarticulares del Centro Médico Imbanaco Durante el último siglo múltiples autores sugieren que la etiología de la osteoartritis de la cadera se encuentra relacionada mas con la morfología que con la carga que esta recibe. (2,3,4,19) Recientemente un concepto de integración mecánica, el pinzamiento femoroacetabular (PFA), fue propuesto para ofrecer una explicación en el rol de las variaciones morfológicas de la cadera en el desarrollo de osteoartritis en pacientes jóvenes sin displasia. (7,21) Otras condiciones que pueden resultar en el contacto anormal entre el fémur proximal y el acetábulo incluyen fracturas del cuello femoral, osteotomías periacetabulares, retroversión acetabular y deslizamiento epifisiario de la cabeza femoral. (3,21,22,23) A pesar que todas estas condiciones pueden resultar en un pinzamiento femoroacetabular, la mayoría de estos paciente carecen de una historia clara de condiciones predisponentes. Sin embargo, la evidencia reciente muestra que en pacientes activos, las alteraciones morfológicas sutiles que afectan al fémur proximal o el acetábulo, son la causa más común de pinzamiento femoroacetabular. During the last century many authors suggest that the etiology of osteoarthritis of the hip is more related to the morphology of the burden this recibe. (2,3,4,19) Recently a concept of mechanical integration, the femoroacetabular impingement (FAI) was proposed to offer an explanation on the role of morphological changes in the development of hip osteoarthritis in young patients without displasia.(7, 21) Other conditions that can result in abnormal contact between the proximal femur and acetabulum include 73 “Temas selectos de actualización en la Ortopedia Latinoamericana” femoral neck fractures, periacetabular osteotomy, acetabular retroversion and sliding head epiphyseal femoral. (3,21,22,23) Although these conditions may result in FAI, most of these patients lack a clear history of predisposing conditions. However, recent evidence shows that active patients, subtle morphological changes affecting the acetabulum or proximal femur are the most common cause of femoroacetabular impingement.(7) FISIOPATOLOGÍA A Stulberg et al(3) se le atribuye la introducción del término “deformidad en mango de pistola” que describe la anormalidad morfológica de la cabeza y el cuello femoral en radiografías anteroposteriores de pacientes con osteoartritis temprana. Esto genera un contacto anormal durante los arcos de movilidad lo cual desarrolla lesiones en el labrum y en el cartílago acetabular adyacente. Esta lesión condral y labral temprana continúan hacia la progresión resultando en una enfermedad articular degenerativa. Ganz et al(7) describen 2 tipos distintos de pinzamiento femoroacetabular basados en el patrón de lesión condral y labral observados durante la luxación quirúrgica de la cadera: • Pinzamiento tipo cam • Pinzamiento tipo pincer Pinzamiento Tipo Cam Es más común en hombres jóvenes, ocurriendo en un promedio de edad de 32 años. Se presenta cuando la forma del cuello y la cabeza femoral es anormal. La anesfericidad de la cabeza femoral se produce por una prominencia ósea que produce una disminución “offset” de la cabeza y el cuello femoral. 74 El “offset” de la cabeza y el cuello femoral que se define como la distancia entre el diámetro más ancho de la cabeza femoral y la parte más prominente del cuello femoral, incrementando su radio lo cual produce un ingreso forzado en el acetábulo durante la movilidad normal, principalmente en la flexión de la cadera.(11,13,14). La irritación recurrente lleva a la abrasión del cartílago hasta romper la union del cartilago con el labrum (union condro-labral) y posteriormente la desinsercion del labrum acetabular.24 El área de cartílago acetabular comprometida en el pinzamiento tipo cam es mayor que en el pinzamiento pincer puro y puede asociarse con aéreas extensas de delaminación o fisura del cartílago. Sin embargo, en ambos mecanismos existe un daño preartrítico que es significativo e irreversible en el cartílago. No hay una pérdida del espacio articular ya que lo que se ve afectado es la calidad del cartílago y no su diámetro, en los estadios tempranos de la enfermedad. (25) La lesión labral y condral usualmente se observan en el área anterosuperior del acetábulo.(7,13,15) Imagenológicamente se describe mediante la medición del ángulo alfa tanto en proyección de Dunn/Rippstein a 45º y 90º y en cortes oblicuos axiales y radiales en la artroresonancia. Un ángulo alfa >50° es sugestivo de una deformidad tipo cam.(43) Este ángulo alfa se mide trazando una línea por el centro del cuello femoral hasta el centro de la cabeza y desde el centro de la cabeza femoral hasta el punto en el aspecto anterolateral donde el radio de la cabeza femoral se vuelve mayor que el radio de la circunferencia trazada con las plantillas de Mose.(42) (Fig. 6) Pinzamiento Tipo Pincer Es más común en mujeres de mediana edad, aproximadamente a los 40 años. Es el resultado del sobrecubrimiento global o focal de la cabeza femoral, causando un contacto entre el borde acetabular y la unión de la cabeza y el cuello femoral. En Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT contraste con el pinzamiento tipo cam, el daño del cartílago acetabular se ve restringido a la zona cercana al labrum comprometido.(8) En la fase crónica, el reborde acetabular puede osificarse ya sea local o globalmente. Esta osificación puede presentarse de 2 formas en la proyección AP de pelvis, el signo de la doble línea que se observa en caderas con una pared posterior prominente y en las cuales la osificación de la pared posterior se proyecta como un borde convexo que sobrepasa el centro de la cabeza femoral y el signo del receso que se observa como una brecha radiolúcida entre el reborde acetabular nativo y la extensión lateral de la osificación. En estos casos el labrum no se osifica sino que es desplazado por la osificación o cubierto por la misma hasta atrofiarlo.(55) Sobrecubrimiento Global Está relacionado con la profundidad radiológica de la fosa acetabular. Se describen 2 tipos de sobrecubrimiento global: la coxa profunda y el protrusio acetabular. La coxa profunda se produce cuando el piso de la fosa acetabular toca o sobrepasa la línea ilioisquiática medial.(25) El protrusio acetabular se produce cuando la cabeza femoral sobrepasa la línea ilioisquiática medial, 3mm o mas en hombres y 5mm o más en mujeres.(31) Cabe recordar que la configuración normal en una proyección AP de pelvis muestra el fondo de la fosa acetabular ubicada lateralmente a la línea ilioisquiática. Ambas formas se relacionan con un incremento de la profundidad acetabular, sin embargo en este momento no existe información clara sobre si las 2 entidades son la continuación una de la otra. (25) Generalmente un acetábulo profundo es asociado con una cobertura acetabular excesiva que puede ser cuantificada con el ángulo centro borde lateral o con el índice acetabular (Tönnis).(28) Un ángulo centro borde lateral < 20° se clasifica como displásico, entre 21° y 38° se clasifica como normal, de 39° a 44° se clasifica como coxa profunda y > 44° se clasifica como protrusio acetabular. Un ángulo centro borde >38° se considera suceptible a producir un pinzamiento tipo pincer.(29, 30) En las caderas con coxa profunda o protrusio acetabular el índice del techo acetabular (ángulo de Tönnis), es típicamente 0° o negativo.(30) Sobrecubrimiento Focal Puede ocurrir en la parte anterior del acetábulo. Sobrecubrimiento anterior es prodeucido por la “retroversión acetabular” que se define como como la perdida del la anteversion normal del acetabualo haciendo que el borde anterior se vuelva mas prominente por lo cual disminuye el rango de movilidad de la cadera en la flexion y esto lo podemos ver en rx cuando la línea del borde anterior se dispone lateral al borde posterior del acetábulo en la porción craneal y se entrecruza en la parte distal causando pinzamiento anterior que puede ser reproducido clínicamente con flexión y rotación interna dolorosa. Esta configuración en figura de 8 se conoce como el signo de “cross-over”.(30) (Fig. 5) Presentación Clínica Usualmente se presenta en adultos jóvenes (entre 20 y 40 años), con una prevalencia de 10% al 15%.(12) Durante los estadios iniciales de la enfermedad, el dolor es intermitente y puede exacerbarse con la demanda excesiva de la cadera. Puede presentarse además luego de sentarse por periodos prolongados y en las rotaciones de la cadera. Algunos pacientes describen dolor en región inguinal principalmente, aunque otros manifiestan dolor trocantérico que se puede irradiar a la cara lateral del muslo, dolor a nivel de la región glútea, en la porción interna del muslo y rodilla. Al examen físico estos pacientes frecuentemente no pueden definir el origen del dolor por lo cual abrazan la region trocanterica con la mano (signo de la “C”). (Fig. 1) 75 “Temas selectos de actualización en la Ortopedia Latinoamericana” • Prueba de Provocación de Pinzamiento • Prueba de Flexión-Aducción-Rotación Interna • Prueba de Flexión-Rotación Interna • Prueba de Flexión-Aducción-Compresión Axial • Prueba de Fitzgerald Figura 1. Signo de la “C” Prueba de provocación de pinzamiento Un signo positivo para pinzamiento anterior es cuando se logra reproducir el dolor con la cadera en flexión de 90° para posteriormente realizar aducción y rotación interna. Para pinzamiento posterior cuando se reproduce el dolor con extensión y rotación externa forzada.(7, 32) (Fig.3) Pueden presentar arcos de movilidad restringidos, principalmente, la rotación interna y externa.(7, 31) (Fig.2) Figura 3. Aducción/Rotación Interna y Abducción/Rotación Externa. Figura 2. Rotación Interna y Externa. Distintos autores han publicado pruebas clínicas para un diagnóstico más preciso del PFA y sus lesiones asociadas, pero siendo esta una patología tan compleja no podemos decir que una sola prueba es capaz de darnos el diagnóstico. Leibold et al realizó una revisión sistemática de las distintas pruebas clínicas para el diagnóstico de lesiones labrales encontrando una alta sensibilidad en las siguientes pruebas: 76 Un signo positivo de pinzamiento ha sido relacionado con alteraciones en la región antero superior ya sea a nivel del cartílago, unión condrolabral o del labrum mismo. Las cuales pueden ser visualizadas en un alto porcentaje en artroresonancias de la cadera.(33) Podemos considerar la prueba de flexión-aducción-rotación interna y la prueba de flexión-rotación interna como variaciones de la prueba de provocación de pinzamiento. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Prueba de Flexión Aducción y Compresión Axial Esta prueba consiste en realizar compresión axial sobre la cadera flexionada a 90° y leve aducción, si el paciente manifiesta dolor se considera la prueba positiva. Una prueba positiva se correlaciona con una lesión del labrum acetabular. Prueba de Fitzgerald Se utiliza para diagnosticar lesiones del labrum anterior o posterior. Para la evaluación del labrum anterior la posición inicial del paciente es con la cadera en flexión de 90°, rotación externa y abducción la cual se lleva a extensión completa, rotación interna y aducción. Para evaluar el labrum posterior la posición inicial del paciente es con la cadera en extensión, abducción y rotación externa la cual se lleva a una posición final de flexión, aducción y rotación Interna. pacientes con pinzamiento femoroacetabular y a la vez ayudarnos a diferenciarla de otras patología con clínica similar como la artritis, la necrosis avascular u otras alteraciones articulares, las cuales no se pueden descartar solamente con el examen físico. Las radiografías convencionales para pinzamiento femoroacetabular incluyen: • Proyección anteroposterior (AP) de pelvis. (7,41) Debe tomarse con el paciente en decúbito supino con ambas extremidades inferiores en rotación interna de 15° para una mejor visualización del cuello femoral y con una distancia del tubo de rayos x al chasis de 1.20m. (Fig. 4) Prueba Diagnóstica de la Xilocaína En muchos pacientes es difícil de establecer la etiología del dolor dado que las imágenes radiológicas pueden ser interpretadas como normales, aunque en algunos casos puede ser secundario a trauma. Una manera de diferenciar si la patología es de origen intra o extrarticular es la prueba diagnóstica de la xilocaína, la cual consiste en aplicar 5 cc de xilocaína sin epinefrina al 1 o 2% intra articular bajo visión fluoroscópica. Si los síntomas ceden luego de la infiltración se considera esta prueba como positiva y nos indica que la etiología del dolor es de origen intrarticular, de persistir los síntomas nos indica que la patología es de origen extrarticular y se considera una prueba negativa. IMÁGENES DIAGNÓSTICAS Radiología simple Debe enfocarse en evaluar las anormalidades de la cadera que se observan en los Figura 4. Esta proyección nos permite analizar: (Figura. 5) 1. Articulación sacroilíaca 2. Cuerpos vertebrales de L4, L5 y S1 3. Sínfisis púbica 4. Espacio articular coxo femoral 77 “Temas selectos de actualización en la Ortopedia Latinoamericana” 5. Orientación del acetábulo en sentido anteroposterior (pared anterior –pared posterior – espinas isquiáticas ) 6. Profundidad acetabular (línea ilioisquiática) 7. Orientación del acetábulo en sentido supero-inferior ( inclinación acetabular) Estas proyecciones nos permiten evaluar: 1. “Off set” anterior del cuello en la región anterosuperior. (Dunn 45°) (Fig. 7) 2. “Off set” anterior del cuello en la región anteroinferior. (Dunn 90°) (Fig. 9) 8. Fémur proximal (Angulo cervico diafisariorelación articulotrocantérica – “off set” superior del cuello femoral). 9. Índice de Extrusión de la cabeza Femoral. Figura 7. Dunn 45° /ángulo alfa. Figura 5. Proyección anteroposterior (AP) • Proyección de Dunn/Rippstein a 45° y 90° para valorar la morfología de la unión de la cabeza y el cuello femoral.(34) Con el paciente en decúbito supino se flexiona la cadera a 45° o 90° con 20° de abducción y neutro de rotación, con una distancia del tubo de rayos x al chasis de 102cm.(41) (Fig. 6 y 8) Figura 6. Dunn 45°. 78 Figura 8. Dunn 90° Figura 9. Dunn 90° /offset cuello femoral. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT • Proyección axial “cross-table” de cadera. (7,41) Con el paciente en decúbito supino con la cadera contralateral flexionada 80° y la extremidad sintomática con rotación interna de 15° para exponer la superficie anterolateral de la unión cabeza cuello femoral. El rayo debe ir paralelo a la mesa y orientado a 45° con la extremidad sintomática.(41) Esta proyección nos permite evaluar el “off set” anterior del cuello femoral en su porción anteroinferior. • Proyección de falso perfil ha sido utilizada para cuantificar el sobrecubrimiento anterior, el cual se calcula mediante el ángulo de Lequesne (ángulo centro borde anterior) y el mismo no debe ser menor de 20°.35 También puede ser utilizada para valorar el espacio articular en la parte medial e inferior que puede verse disminuido como causa del efecto de contragolpe. Es realizada con el paciente de pie con la cadera afectada contra el chasis y la pelvis rotada 65° en relación con el soporte de pared, el pie del mismo lado debe estar posicionado paralelo al chasis y el rayo se centra en la cabeza femoral a una distancia de 102cm.(41) (Figura. 10 y 11) Figura 10. Falso Perfil Figura 11. Falso perfil – Angulo de Lequesne. Esta proyección nos permite evaluar: 1. La pared posterior 2. Cobertura anterior de la articulación. 3. Alteraciones puntuales en la pared anterior 4. Perdida del espacio articular en la porción medial e inferior. Tomografía Axial Computarizada (TAC) Con la radiología simple se puede determinar el tipo de alteración morfológica, sin embargo mediante la TAC podemos valorar de forma más precisa la ubicación de la deformidad y las zonas de mayor contacto lo que nos permite realizar un planeamiento preoperatorio y determinar la cantidad de hueso que debemos resecar para corregirla. Es de utilidad en también en revisiones de artroscopias de cadera para determinar si se realizó una resección adecuada de la unión del cuello y la cabeza femoral. Las reconstrucciones 3D también facilitan la evaluación de estos casos. 79 “Temas selectos de actualización en la Ortopedia Latinoamericana” Resonancia magnética (RM) Se utiliza como complemento a la evaluación clínica y radiográfica para confirmar una impresion diagnóstico previa. Así como para evaluar estructuras no valorables con las radiografías simples tales como: • Labrum acetabular • Ligamento redondo • Cartílago articular (acetabular y cabeza femoral) • Cuerpos libres • Capsula articular • Tendón del Iliopsoas • Banda Iliotibial • Mecanismo abductor • Bursas La artroresonancia nos permite una mejor visualización de estructuras como el labrum acetabular y el cartílago articular valorando de manera más exacta la severidad y la extension de la lesión. De igual forma nos permite descartar patologías con clínica similar como la necrosis avascular de la cabeza femoral en fase temprana, tumoraciones, fracturas no desplazadas, entre otras. Sin embargo debemos tener en cuenta las siguientes consideraciones al momento de evaluar una RM: 6 meses sin tener resolución del problema. De persistir las molestias se debe considerar tratamiento quirúrgico. Tratamiento Quirúrgico El tratamiento quirúrgico está enfocado en corregir las alteraciones morfológicas, ya sea en la unión de la cabeza y el cuello femoral o en el reborde acetabular. Esto incluye básicamente la resección quirúrgica de la causa del pinzamiento mediante acetabuloplastia u osteocondroplastia de la unión cabeza y cuello femoral, la cual se puede realizar mediante una luxación quirúrgica controlada, (7,32,38) abordaje anterior limitado sin luxación (“mini open”), una artroscopia de cadera (39) o en casos con indicaciones especificas mediante la reorientación de un acetábulo retroverso con una osteotomía periacetabular reversa.(40) Luxación controlada de la cadera La luxación quirúrgica controlada, descrita por Ganz et al y enfocado hacia la preservación articular,(7) consiste en realizar una luxación de la cadera preservando la irrigación de la cabeza femoral y realizando una osteocondroplastia femoroacetabular. Se realiza mediante un abordaje lateral incidiendo la fascia lata hasta el trocánter mayor. Posteriormente se realiza una osteotomía del trocánter mayor en el borde lateral de la fosa piriforme en el tercio proximal y en el borde distal del vasto lateral (Fig. 12). • Resonador por encima 1.5 teslas. • Protocolo de PFA que incluya cortes axiales oblicuas y/o radiales para determinar el ángulo alfa.(36, 37) TRATAMIENTO Tratamiento No Quirúrgico Se indica inicialmente en pacientes con alteraciones morfológicas sutiles y con daño intrarticular mínimo. El mismo está enfocado al control del dolor con analgésicos (antiinflamatorios no esteroideos), infiltraciones y restricción de actividad deportiva. No debe sobrepasar los 80 Figura 12. Luxación controlada de cadera (Osteotomía de trocánter mayor) Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Durante este abordaje se preservan los músculos rotadores externos y la arteria circunfleja femoral medial es protegida por el musculo obturador externo que se mantiene intacto. El trocánter osteotomizado se retrae anteriormente y se realiza una capsulotomía anterior en forma de “S” para exponer la articulación de la cadera. Después de la separación del ligamento redondo se luxa la cadera luego de confirmar el pinzamiento femoroacetabular y el sitio específico de pinzamiento.(44) Cualquier lesión condral o labral puede ser identificada y desbridada. Las prominencias óseas en el cuello femoral pueden ser removidas fácilmente mediante una sierra oscilante o con el uso de osteótomos. La resección del reborde acetabular redundante o acetabuloplastia puede ser realizada y posteriormente reinsertar el labrum acetabular desprendido. Lesiones en el área posterior de la cabeza, cuello y acetábulo, también son accesibles con la manipulación de la extremidad.(45f) Beck et al, realizaron un estudio con un seguimiento promedio de 4.7 años y una media de edad de 36 años en 19 pacientes (14 hombres y 5 mujeres) utilizando la luxación controlada de la cadera. El seguimiento y la evaluación de estos pacientes se realizó con la escala de cadera de Merle d’Aubigné, obteniéndose resultados entre excelente y buena en 13 pacientes con una mejoría en la escala de 2.9 a 5.1 puntos en el ultimo seguimiento. En esta serie no se presentaron casos de necrosis avascular de la cabeza femoral. La luxación quirúrgica con corrección del PFA logró buenos resultados en pacientes con cambios degenerativos tempranos que no excedieran el Grado I de osteoartritis. Este procedimiento no es comparable con pacientes que presenten cambios degenerativos avanzados o daños extensos del cartílago articular.(24) Otros estudios como el de Peters et al con 30 caderas en 29 pacientes (16 hombres y 13 mujeres) quienes se les realizo luxación anterior de la cabeza femoral con osteotomía del trocánter. Seguimiento clínico y radiográfico a 32 meses utilizando la escala de cadera de Harris la cual mejoro de 70 puntos preoperatorio a 87 puntos al final del seguimiento (p<0.0001). Ningún paciente presento necrosis avascular ni no unión trocantérica. En 18 caderas se encontraba daño severo del cartílago acetabular el cual no se había apreciado en radiografías ni artroresonancia. En 8 de estos 18 pacientes presentaron evidencia radiográfica de la progresión de la osteoartritis, y 4 de estas están a la espera de un reemplazo total de cadera.(47) Espinosa et al, revisaron retrospectivamente los resultados clínicos y radiográficos de 52 pacientes (60 caderas) con PFA a quienes se les realizó artrotomía y luxación quirúrgica. En las primeras 25 caderas el labrum roto fue resecado (Grupo 1) y en las siguientes 35 caderas la porción intacta del labrum fue reinsertada al reborde acetabular (Grupo 2). Se dio un seguimiento a los 12 y 24 meses utilizando la escala de Merle d’Aubigné y el sistema de clasificación de artrosis de Tönnis para comparar ambos grupos. A los 12 meses ambos grupos mejoraron mejoría significativa en las escalas clínicas comparados con los valores preoperatorios, Grupo 1 (p=0.0003) y Grupo 2 (p<0.0001). A los 24 meses postoperatorios el 28% de las caderas del Grupo 1 tenían resultados excelentes, 48% buenos, 20% moderados y 4% pobres. En contraste con el Grupo 2 con 80% de excelentes resultados, 14% buenos y 6% moderados. Signos radiográficos de osteoartritis tuvieron mayor prevalencia en el Grupo 1 que en el Grupo 2 a un año (p=0.02) y a 2 años (p=0.009).(48) Abordaje anterior limitado sin luxación (“Mini-open”) Otra alternativa de tratamiento es el abordaje anterior de Smith-Petersen modificado que puede ser utilizado para realizar una artrotomía de la cadera. Bajo vi- 81 “Temas selectos de actualización en la Ortopedia Latinoamericana” sualización directa la prominencia en el cuello femoral puede ser resecada fácil y efectivamente. La reinserción de un labrum desprendido con suturas de anclaje también es posible mediante este abordaje. Los sistemas de tracción pueden ser utilizados para subluxar la cadera, examinar y resecar las lesiones condrales cuando es necesario.(44) Muchos autores complementan esta técnica con artroscopia para evaluar y manejar el compartimiento central de la cadera. Estudios como el de Clohisy et al, con 35 pacientes con un seguimiento a 2 años tratados con artroscopia y osteocondroplastia abierta limitada. Utilizando la escala de cadera de Harris se obtuvo una mejoría de 68.3 a 87.4 puntos en el último seguimiento, 83% de los pacientes presentaron una mejoría >10 puntos en la escala y un 71% presentaban puntajes superiores a 80.(49) Laude et al obtuvo resultados similares utilizando esta misma técnica al evaluar de forma retrospectiva 100 caderas en 97 pacientes con un seguimiento mínimo de 28.6 meses (promedio 58.3 meses). Utilizando la escala para caderas no artríticas (NAHS) se obtuvo un aumento en 29.1 puntos en promedio al último seguimiento. De estos 11 caderas desarrollaron osteoartritis por lo que requirieron un reemplazo total de cadera. Los mejores resultados se obtuvieron en pacientes menores de 40 años con Tönnis de 0.(50) Ribas et al evaluó 117 caderas tratadas con abordaje anterior “mini-open” con un seguimiento mínimo de 2 años divididos en 3 grupos: Grupo A (Tönnis 0) 32 caderas, Grupo B (Tönnis 1) 61 caderas y Grupo C (Tönnis 2) 24 caderas. Evaluó resultados utilizando el método combinado del Instituto Universitario Dexeus el cuál se aplicó preoperatorio y a los 3, 6 y 12 meses. A los 3 meses de seguimiento 30 caderas (94%) del Grupo A, 58 caderas (95%) del Grupo B y 14 caderas (58%) del Grupo C se obtuvieron resultados satisfactorios que se mantuvieron hasta el primer año. 82 Los puntajes de Merle D’Aubigné-Postel y WOMAC mostraron mejoría significativa en los Grupos A y B (p<0.001), no así el seguimiento del Grupo C el cual no mostro una mejoría significativa (p>0.05). Los resultados se encuentran altamente influenciados por los estadios degenerativos preoperatorios principalmente en estadio Tönnis 2 por lo cual es razonable realizar un procedimiento quirúrgico en los pacientes sintomáticos(54). Artroscopia de Cadera Actualmente la artroscopia de cadera se presenta dentro del armamentario para el diagnóstico y tratamiento de las patologías de la cadera.(46) La selección adecuada de los pacientes es la clave para un buen resultado post-quirúrgico. Para esto es importante conocer las indicaciones y contraindicaciones de la artroscopia de cadera. (Tabla 1.) Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Puede ser realizada con el paciente en posición decúbito lateral o en decúbito supino sobre una mesa de tracción y bajo visión fluoroscópica para evaluar la distracción de la articulación. Al colocar al paciente en posición decúbito supino es importante la aplicación de un vector de distracción oblicuo al eje del cuerpo del paciente, el cual se logra con el uso del poste perineal lateralizado hacia la cadera a operar (Fig. 13) Figura 13. Portales y distraccion articular. Para realizarla se utilizan distintos abordajes de los cuales los más importantes son: • Anterolateral • Anterior • Accesorio Inferior • Accesorio superior • Posterolateral Se hace una evaluación sistemática del compartimento central y periférico en busca de alteraciones en el labrum acetabular, superficies articulares tanto de la cabeza femoral como del acetábulo, región anterior del cuello femoral, repliegues sinoviales, ligamento redondo, unión condrolabral y una evaluación dinámica de la articulación para definir si se retiraran adecuadamente los topes que producían el pinzamiento. Sampson evaluó 120 caderas (118 pacientes) manejados mediante artroscopia de cadera en los cuales encontró que el signo de pinzamiento se eliminó en casi la totalidad de los pacientes. Los resultados más pobres ser observaron en los pacientes con mayor daño en la superficie articular visto en el momento de la artroscopia y que no se había detectado en los estudios imagenológicos. Se encontró que en el 50% de los pacientes el dolor había desaparecido entre 6 semanas y 3 meses, 75% a los 5 meses y 95% al año.(51) Otro estudio como el de Byrd et al, con 200 pacientes (207 caderas) y un seguimiento mínimo de 12 meses (promedio 16 meses). De estos 158 pacientes (163 caderas) se les realizó corrección del PFA tipo cam y a 42 (44 caderas) pacientes se les realizo una corrección concomitante del PFA tipo pincer. El promedio del aumento del puntaje de cadera de Harris fue de 20 puntos, 0.5% de los pacientes fueron convertidos a un reemplazo total de cadera. Los resultados a corto plazo del tratamiento artroscópico del PFA tipo cam son comparables con los reportes publicados para los métodos abiertos con la ventaja de tener un abordaje menos invasivo.(52) Phillipon et al realizaron manejo artroscópico para PFA en 112 pacientes (62 mujeres y 50 hombres) de estos 23 se les realizo osteoplastia para PFA tipo cam, 3 se le realizo solamente manejo del pincer y 86 se les realizó ambos procedimientos para PFA mixtos. Un seguimiento promedio de 2.3 años en donde se obtuvo una mejoría de 58 a 84 puntos con una media de 24 puntos (IC 95% 19 - 28) en el puntaje modificado para cadera de Harris. La media de satisfacción del paciente fue de 9 puntos (1 - 10). Luego de la artroscopia 10 pacientes requirieron de un reemplazo total de cadera en un promedio 83 “Temas selectos de actualización en la Ortopedia Latinoamericana” de 16 meses. Los predictores de mejores resultados fueron una escala modificada de Harris para cadera (p=0.018), disminución del espacio articular ≥ 2mm (p=0.005) y la reparación de la patología labral en lugar del desbridamiento (p=0.032). El manejo artroscópico del PFA acompañado de una adecuada rehabilitación brinda un buen resultado a corto plazo y una alta satisfacción del paciente.(53) Estudios más recientes con mayor volumen de pacientes como el de Byrd et al en donde evaluó a 200 atletas los cuales fueron sometidos a artroscopia de cadera por PFA y un seguimiento mínimo de 1 año. Pacientes con una media de edad de 28.6 años (11 – 60 años), 148 hombres y 52 mujeres con PFA tipo cam en 159 caderas, tipo pincer en 10 caderas y mixto en 31 caderas. De estos 23 eran atletas profesionales, 56 atletas universitarios, 24 atletas de secundaria y 97 atletas recreativos. Se dio seguimiento con el puntaje de cadera de Harris (HHS) el cual se aplicó en el preoperatorio y postoperatorio a los 3, 12, 24, 60 y 120 meses. La media del HHS preoperatorio fue de 72 puntos y postoperatorio de 96 con una media de mejoría en la escala de 20.5 puntos (p<0.001). El 95% de los atletas profesionales y el 85% de los atletas universitarios regresaron a su nivel de competición previo.(56) Otros estudios como el de Philippon et al donde evaluaron 153 pacientes de 50 años o mayores entre 2006 y 2008 tratados con artroscopia de cadera para PFA. El objetivo del estudio era observar la evolución de estos pacientes y determinar por cuánto tiempo se evitaba el reemplazo total de cadera. El 20% (31 pacientes) requirieron reemplazo total de cadera. A 3 años los pacientes con un espacio articular mayor de 2mm presentaban una sobrevida del 90%, contrario a los que presentaban un espacio de 2mm o menor quienes tenían una sobrevidad 57% (p=0.001). En los pacientes que no requirie- 84 ron reemplazo total de cadera presentaron una mejoría en el HHS Modificado de 58 a 84 puntos. En base a estos resultados los pacientes con espacio articular mayor de 2mm tienen mayor sobrevida con respecto al estado preoperatorio en dolor y función. Comentarios del autor El retomar el concepto del pinzamiento femoroacetabular donde se profundiza en la etiología, biomecánica y manejo de esta, de manera organizada, es un hito en la historia de la medicina. Pocas veces tenemos la oportunidad de evaluar y conocer una patología desde sus inicios observando la forma como evoluciona, los cambios en la manera de tratarlo y los resultados que se obtienen con los mismos. Debemos recordar que la finalidad de la cirugía en esta patología es preservar la articulación evitando la artrosis, algo muy ambicioso pero posible. Se logra limitar el daño por medio de la corrección de sus alteraciones morfológicas pero la misma no es capaz de revertir los daños ya sufridos en la articulación por lo que es muy importante el diagnóstico y el tratamiento temprano de esta patología. Esto debe ser de nuestro conocimiento y del conocimiento de nuestros pacientes para que tengan una percepción real de su problema y expectativas acorde con lo avanzado de su patología. Aunque se lleva muy poco tiempo decantando el proceso, es claro que es un evento que impacto de gran manera no solo la comunidad médica sino a la población general. Desde 2005 el número de publicaciones en la red y en las revistas médicas ha aumentado de manera exponecial, las técnicas quirúrgicas han evolucionado, haciéndose menos complejas, mas estandarizadas y obteniéndose resultados a mediano plazo muy alentadores. A pesar que el concepto de PFA se viene estudiando desde finales de los años 90, no Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT es sino a partir del año 2006 en donde se ha establecido un manejo moderno de esta patología al obtener resultados más predecibles en nuestra población mediante la estandarización de las técnicas quirúrgicas ya conocidas. Debido a esto actualmente podemos decir que existe un periodo de aproximadamente 5 a 6 años de seguimiento de técnicas quirúrgicas estandarizadas y estamos a la espera de un seguimiento mas prolongado de los pacientes tratados de esta forma. Sin embargo, consideramos que el mayor aporte de este proceso es haber logrado profundizar mas en los problemas de esta articulación, llevándonos a entender muchas cosas antes desconocidas y a cambiar conceptos errados que antes se daban como absolutamente ciertos. BIBLIOGRAFÍA 1. Bombelli R: Osteoarthritis of the Hip: Pathogenesis and Consequent Therapy. Berlin, Germany: Springer-Verlag, 1976. 2. Elmslie RC: Aetiological factors in osteoarthritis of the hip. BMJ 1933; 1: 1-3. 3. Stulberg SD, Cordell LD, Harris WH, Ramsey PL, MacEwen GD: Unrecognized childhood hip disease: A major cause of idiopathic osteoarthritis of the hip, in: The Hip: Proceedings of the Third Meeting of The Hip Society. St. Louis, MO, CV Mosby, 1975, pp 212-228. 4. Harris WH: Etiology of osteoarthritis of the hip. Clin Orthop Relat Res 1986; 213:20-33. 5. Reginster JY: The prevalence and burden of arthritis. Rheumatology (Oxford) 002; 41(suppl): 3-6. 6. Flores RH, Hochberg MC: Definition and classification of osteoarthritis, in Brandt KD, Doherty M, Lohmander LS (eds): Osteoarthritis. New York, NY: Oxford Medical Publication, Oxford Unipress, 1998, pp 1-12. 7. Ganz R, Parvizi J, Beck M, Leunig M, Nötzli H, Siebenrock KA. Femoroacetabular impingement: a cause for osteoarthritis of the hip. Clin Orthop Relat Res 2003; 417:1–9 8. Beck M, Kalhor M, Leunig M, Ganz R. Hip morphology influences the pattern of damage to the acetabular cartilage: femoroacetabular impingement as a cause of early osteoarthritis of the hip. J Bone Joint Surg Br 2005; 87:1012–1018. 9. Murphy SB, Tannast M, Kim YJ, Buly R, Millis MB. Débridement of the adult hip for femoroacetabular impingement: indications and preliminary clinical results. Clin Orthop Relat Res 2004; 429:178–181. 10.Tanzer M, Noiseux N. Osseous abnormalities and early osteoarthritis. Clin Orthop Relat Res 2004; 429:170–177. 11.Jäger M, Wild A, Westhoff B, Krauspe R. Femoroacetabular impingement caused by a femoral osseous head–neck bump deformity: clinical, radiological, and experimental results. J Orthop Sci 2004; 9:256–263. 12.Leunig M, Ganz R. Femoroacetabular impingement: a common cause of hip complaints leading to arthrosis. Unfallchirurg 2005; 108: 9-17. 85 “Temas selectos de actualización en la Ortopedia Latinoamericana” 13.Ito K, Minka MAII, Leunig M, Werlen S, Ganz R: Femoroacetabular impingement and the cameffect: A MRI-based quantitative anatomical study of the femoral head-neck offset. J Bone Joint Surg Br 2001; 83:171-176. 14.Nötzli HP, Wyss TF, Stoecklin CH, Schmid MR, Treiber K, Hodler J: The contour of the femoral head-neck junction as a predictor for the risk of anterior impingement. J Bone Joint Surg Br 2002; 84:556-560. 15.McCarthy JC, Noble PC, Schuck MR, Wright J, Lee J: The Otto E. Aufranc Award: The role of labral lesions to development of early degenerative hip disease. Clin Orthop Relat Res 2001; 393:25-37. 16.Reynolds D, Lucas J, Klaue K: Retroversion of the acetabulum: A cause of hip pain. J Bone Joint Surg Br 1999; 81:281-288. 17.Gekeler J: Coxarthrosis with a deep acetabulum. Z Orthop Ihre Grenzgeb 1978; 116:454-459. 18.Turgeon TR, Phillips W, Kantor SR, Santore RF. The role of acetabular and femoral osteotomies in reconstructive surgery of the hip: 2005 and beyond. Clin Orthop Relat Res 2005; 441: 188-199. 19.Smith-Petersen MN. Treatment of malum coxae senilis, old slipped upper capital femoral epiphysis, intrapelvic protrusion of the acetabulum, and coxae plana by means of acetabuloplasty. J Bone Joint Surg 1936; 18:869-80. 20.Ganz R, Leunig M, Leunig-Ganz K, Harris WH. The etiology of osteoarthritis of the hip: an integrated mechanical concept. Clin Orthop 2008; 466:264-72. 21.Rab GT: The geometry of slipped capital femoral epiphysis: Implications for movement, impingement and corrective osteotomy. J Pediatr Orthop 1999; 19:419-424. 22.Leunig M, Casillas M, Hamlet M, et al: Slipped capital femoral epiphysis: Early mechanical damage to the acetabular cartilage by a prominent femoral metaphysis. Acta Orthop Scand 2000; 71:370375. 23.Leunig M, Fraitzl CR, Ganz R: Early damage to the acetabular cartilage in slipped capital femoral epiphysis: Therapeutic consequences. Orthopade 2002; 31:894-899. 24.Beck M, Leunig M, Parvizi J, Boutier V, Wyss D, Ganz R. Anterior femoroacetabular impingement. Part II. Midterm results of surgical treatment. Clin Orthop Relat Res 2004; 418:67–73 25.Tannast M, Siebenrock KA, Anderson SE. Femoroacetabular impingement: radiographic diagnosis--what the radiologist should know. AJR Am J Roentgenol. 2007 Jun; 188(6): 1540-52. 26.Hotta Y, Matsui K, Nakada D, Azuma H. [The natural course of osteoarthritis of the hip. Indication of conservative treatment in relation to the osteophyte formation at the acetabular rim]. Nippon Seikeigeka Gakkai Zasshi. 1985; 59:1-15. [En Japonés]. 27.Ninomiya S, Shimabukuro A, Tanabe T, Kim YT, Tachibana Y. Ossification of the acetabular labrum. J Orthop Sci. 2000; 5:511-4. 28.Murphy SB, Kijewski PK, Millis MB, Harless A. Acetabular dysplasia in the adolescent and young adult. Clin Orthop Relat Res 1990; 261:214–223. 29.Murphy SB, Ganz R, Müller ME. The prognosis in untreated dysplasia of the hip. J Bone Joint Surg Am 1995; 77:985–989. 86 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 30.Tönnis D, Heinecke A. Acetabular and femoral anteversion: relationship with osteoarthritis of the hip. J Bone Joint Surg Am 1999; 81:1747–1770. 31.Armbuster TG, Guerra J Jr, Resnick D, Georgen TG, Feingold M, Niwayama G, et al. The adult hip: an anatomical study. Part 1: the bony landmarks. Radiology 1978; 128:1–10. 32.Ganz R, Gill TJ, Gautier E, Ganz K, Krügel N, Berlemann U. Surgical dislocation of the adult hip: a technique with full access to femoral head and acetabulum without the risk of avascular necrosis. J Bone Joint Surg Br 2001; 83:1119–1124. 33.MacDonald SJ, Garbuz D, Ganz R: Clinical evaluation of the symptomatic young adult hip. Semin Arthroplasty 1997;8:3-9. 34.Meyer DC, Beck M, Ellis T, Ganz R, Leunig M. Comparison of six radiographic projections to assess femoral head/neck asphericity. Clin Orthop Relat Res 2006; 445:181–185f. 35.Lequesne M, de Sèze S. False profile of the pelvis: a new radiographic incidence for the study of the hip—its use in dysplasias and different coxopathies [En Francés]. Rev Rhum Mal Osteoartic 1961; 28:643–652. 36.Leunig M, Werlen S, Ungersbock A, Ito K, Ganz R: Evaluation of the acetabular labrum by MR arthrography. J Bone Joint Surg Br 1997; 79:230-234. 37.Werlen S, Porcellini B, Ungersbock A: Magnetic resonance imaging of the hip joint. Semin Arthroplasty 1997; 8:20-26. 38.Lavigne M, Parvizi J, Beck M, Siebenrock KA, Ganz R, Leunig M. Anterior femoroacetabular impingement. Part I: Techniques of joint-preserving surgery. Clin Orthop Relat Res 2004; 418:61–66. 39.Wettstein M, Dienst M. Hip arthroscopy for femoroacetabular impingement [En Alemán]. Orthopäde 2006; 35:85–93. 40.Siebenrock KA, Schöniger R, Ganz R. Anterior femoro-acetabular impingement due to acetabular retroversion and its treatment by periacetabular osteotomy. J Bone Joint Surg Am 2003; 85:278– 286. 41.Clohisy JC, Carlisle JC, Beaulé PE, Kim YJ, Trousdale RT, Sierra RJ, Leunig M, Schoenecker PL, Millis MB. A Systematic approach to the plain radiographic evaluation of the young adult hip. J Bone Joint Surg Am. 2008; 90(Suppl 4):47-66. 42.Mose K. Methods of measuring in Legg-Calvé-Perthes disease with special regard to the prognosis. Clin Orthop Relat Res. 1980; 150:103-9. 43.Notzli H, Wyss T, Stoecklin C, Schmid M, Treiber K, Ho¬dler J. The contour of the femoral head-neck junction as a predictor for the risk of anterior impingement. J Bone Joint Surg (Br) 2002; 84B: 556-60. 44.Parvizi J, Leunig M, Ganz R. Femoroacetabular Impingement. J Am Acad Orthop Surg 2007 vol. 15 no. 9 561-570. 45.Shrader MW, Sucato DJ. Surgical dislocation with trochanteric osteotomy: a surgical approach for femoroacetabular impingement. Curr Opin Orthop 2005; 16:439-444. 46.Glick JM: Hip arthroscopy using the lateral approach. Instr Course Lect 1988; 37:223-231. 87 “Temas selectos de actualización en la Ortopedia Latinoamericana” 47.Peters CL, Erickson JA. Treatment of Femoro-Acetabular Impingement with Surgical Dislocation and Débridement in Young Adults. J Bone Joint Surg Am. 2006; 88:1735-1741 48.Espinosa N, Rothenfluh D, Beck M, Ganz R, Leuning M. Treatment of femoroacetabular impingement: Preliminary results of labral refixation. J Bone Joint Surg Am 2006; 88: 925-35. 49.Clohisy JC, Zebala LP, Nepple JJ, Pashos G. Combined hip arthroscopy and limited open os- teochondroplasty for anterior femoroacetabular impingement. J Bone Joint Surg Am. 2010 Jul 21;92(8):1697-706. 50.Laude F, Sariali E, Nogier A. Femoroacetabular impingement treatment using arthroscopy and anterior approach. Clin Orthop Relat Res. 2009 Mar; 467(3):747-52. 51.Sampson T. Arthroscopic treatment of femoroacetabular impingement. Techniques in Orthopaedics. 2005. 20(1):56-62. 52.Byrd J, Jones K. Arthroscopic femoroplasty in the management of camtype femoroacetabular impingement. Clin Orthop Rel Res 2009; 467(3): 739-46. 53.Philippon M, Briggs K, Yen Y, Kuppersmith D. Outcomes following hip arthroscopy for femoroa- cetabular impingement with associates chondrolabral dysfuntion: minimun two-year follow-up. J Bone Joint Surg Br 2009; 91: 16-23. 54.Ribas M, Ledesma R, Cardenas C, Marin-Peña O, Toro J, Caceres E. Clinical results after anterior mini-open approach for femoroacetabular impingement in early degenerative stage. Hip Int. 2010 May 27; 20 (Suppl 7) (S7):36-42. 55.Corten K, Ganz R, Chosa E, Leunig M. Bone apposition of the acetabular rim in deep hips. J Bone Joint Surg Am. 2011;93 Suppl 2:10-6. 56.Byrd J, Jones K. Arthroscopic management of femoroacetabular impingement in athletes. Am J Sports Med. 2011 Jul;39 Suppl:7S-13S. 57.Philippon M, Souza B, Briggs K. Hip Arthroscopy for Femoroacetabular Impingement in Patients Aged 50 Years or Older. Arthroscopy. 2011 Oct 7. 88 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Artroplastia no cementada de cadera Claudio Ángel Alonso, M. D. * Jefe del Servicio de Ortopedia y Traumatología del Hospital de Clínicas de la Universidad de Buenos Aires, Argentina. INTRODUCCIÓN Por definición, las prótesis no cementadas, son aquellas que están implantadas en la cadera “sin el uso de cemento”, y esta definición no da demasiada información de cómo estos implantes logran unirse al hueso, ni de los distintos tipos de mecanismos de fijación protésica. Para ello es bueno hacer una breve reseña de cómo se fueron desarrollando en el tiempo estos conceptos, como fueron variando a partir de la aparición y desarrollo de nuevas biotecnologías, las que han logrado resultados excelentes a largo plazo para las fijaciones no cementadas de las prótesis de cadera. En las ultimas décadas del siglo XVIII Temístocles Gluck en Berlín, es el primero en intentar una artroplastia de cadera en pacientes con articulaciones de cadera destruida por tuberculosis, demostrando que el organismo es capaz de tolerar un cuerpo extraño por largos periodos de tiempo (1). Marius Nygaard Smith-Petersen de Boston, influenciado por su odontólogo el Dr. John Cooke, introduce por primera vez en 1930, el uso de una aleación metálica de vitalium (2) en su copa de interposición (Figura 2 y 3), con resultados alentadores; que reemplazo a la que originalmente fuera de “pyrex”, un vidrio reforzado que tuvo roturas prematuras y fallas a corto plazo. El otro intento de la época fue la “hemiartroplastia” de los hermanos Judet, utilizando una cabeza protésica de acrílico con un vástago dentro del cuello femoral (Figura 1), la que mostró malos resultados a corto plazo debido al prematuro desgaste del acrílico. En esa misma época en Argentina, el Dr. Atilio Risolía, desarrolla una prótesis similar a la de Judet, de acrílico, a la que le agrega un vástago medular de acero para conseguir mas estabilidad del implante, pero observa también el desgaste rápido del acrílico de la cabeza, por lo que años después abandona el implante. 89 “Temas selectos de actualización en la Ortopedia Latinoamericana” Estos intentos dieron experiencia a los cirujanos en cirugía reconstructiva de cadera y estimularon nuevas ideas con el fin de obtener mejores técnicas y resultados. Figura 1. Prótesis acrílica de Judet Pero no fue sino hasta el año 1938, cuando Philip Wiles implanta la primera prótesis total de cadera (3), con ambos componentes de acero inoxidable, en 6 pacientes con enfermedad de Still. El Acetábulo era de acero inoxidable que no llegaba a ser una hemiesfera y se apoyaba dentro del acetábulo y se mantenía en posición gracias a un reborde metálico que evitaba su luxación y la cabeza y el vástago, estaban unidos a una placa lateral la que a su vez se fijaba con tornillos a la diáfisis femoral (Figura. 4). Figura 2. Copa de Smith-Petersen Figura 4. prótesis de Wiles Figura 3. Copa de Smith-Petersen 90 Fijación Biológica El primer implante en demostrar las potenciales ventajas del concepto de fijación biológica, fue diseñado por Austin Moore a principios de los 50’. El implante femoral tenía unas fenestraciones en el tallo (Figura. 5), que se rellenaban con hueso esponjoso obtenido de la cabeza femoral y de la esponjosa metafisaria, para que a través de la consolidación del injerto, el tallo se fijara por dentro del canal femoral y obtuviera así su estabilidad. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Figura 6. Granuloma de cotilo Figura 5. Prótesis de Austin Moore Con la introducción del cemento acrílico (4) por Sir John Charnley en 1957, casi la totalidad de los implantes de cadera que se realizaron a partir de esa época, fueron cementados. Esto permitió que los pacientes pudieran pararse y caminar en el postoperatorio inmediato, con las grandes ventajas que tiene para los pacientes, una rápida rehabilitación con carga inmediata del peso y la movilidad precoz, y mostrando resultados a mediano y largo plazo muy alentadores, con sobrevida protésica por arriba de 15 a 20 años antes de su falla mecánica por aflojamiento aséptico. Pero con el paso de los años, a fines de la década de los 70 comienzan a aparecer gran cantidad de aflojamientos mecánicos de las prótesis de cadera, atribuyéndose esto a fallas propias del cemento acrílico, por lo que a estos aflojamientos mecánicos se los denominó erróneamente como “enfermedad del cemento”; lo que años mas tarde sería cambiado por la “enfermedad de las partículas”, al comprenderse que la causa del aflojamiento mecánico no era por culpa del cemento, sino que se debía a la reacción del organismo a la acumulación de partículas del desgaste (fundamentalmente de polietileno) Figura 7. Desgaste del polietileno que generaban un “granuloma peri protésico” (Figura 6 y 7 ) que conducía al aflojamiento mecánico de la prótesis. A principios de los 70, se comienza a concebir la idea de desarrollar una superficie protésica distinta de la que se usaba en la cementación, con el objetivo de conseguir lo que se llamaría “fijación biológica”, a través de la obtención de crecimiento óseo dentro de la superficie porosa del implante; por lo tanto, esta unión biológica entre el hueso y el implante puede ser comparada al proceso de consolidación natural de una fractura. 91 “Temas selectos de actualización en la Ortopedia Latinoamericana” Este proceso de fijación biológica ocurre a través de la denominada “osteointegración”, que según lo describiera Bränemark (5) es la unión primaria entre implante y hueso, sin la fase de formación de tejido fibrocartilaginoso. Y para que esto se consiga es necesario crear 2 condiciones: 1. Generar a través del fresado un medio de contacto intimo entre hueso e implante. 2. Conseguir una fijación primaria del implante lo suficientemente sólida como para que no exista micromovilidad entre ellos. Esta fijación biológica genera un gran numero de puntos de unión con el hueso a lo largo del implante, que permite la transmisión de cargas de la prótesis al hueso, disminuyendo el estrés de la interfase hueso-cemento y cemento-implante, prolongando la supervivencia del implante y disminuyendo así la posibilidad del aflojamiento aséptico como ocurre en las prótesis cementadas. Es Robert Pillard, un Ingeniero metalúrgico de Ontario, Canadá, quien concibe a principio de los 70 la idea de fabricar una superficie porosa para fijación biológica en los implantes de cadera, en colaboración con los ortopedistas Ian Macnab del Wellesley Hospital y Hugh Cameron del Toronto General Hospital. Es en estos dos Hospitales donde se demostró y caracterizó la eficacia de la superficie porosa para conseguir una fijación mecánica sólida y duradera a través del llamado “crecimiento óseo”. nes clínicas de la superficie porosa en prótesis de cadera (Figura 8 9), ya que los implantes originalmente usados, eran solamente limitados al componente femoral y en un grupo limitado de pacientes a los que se los consideraba de alto riesgo de falla mecánica si se utilizaba un componente femoral cementado. El éxito de esta serie limitada de pacientes, llevó al Dr. Charles Engh desde 1977 (6) a extender sus indicaciones a todo tipo de pacientes y patologías sin limites de edad. En esta serie original de 500 pacientes, la mitad de los casos se utilizó un acetábulo cementado, dado que los acetábulos de superficie porosa, recién estuvieron disponibles para su aplicación clínica sin cemento a partir del año 1982. Este primer componente femoral de superficie microporosa, se llamo AML (Anatomic Medullary Locking) y que aun hoy día se continua utilizando. Figura 8. Superficie Microporosa. Estos primeros implantes de superficie porosa fueron utilizados por primera vez en Canadá en un grupo limitado de pacientes. Poco tiempo después, el Dr. P. Ring en Surrey, Inglaterra, implanta la primera prótesis de superficie porosa en ese país. En 1974, el bioingeniero canadiense Denis Bobyn se muestra interesado en las aplicacio- 92 Figura 9. Crecimiento óseo microporoso. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT (Figura 11), que tiene escamas a lo largo de todo el tallo, las que actuaban de interferencia y bloqueo contra el hueso, pero no conseguía una osteointegración, por lo que los resultados a largo plazo no fueron buenos y su uso se abandono en la década de los ’90. Otro tallo de macro fijación es el Spotorno (Figura 12), que tiene en el segmento metafisario 3 ranuras longitudinales que sirven de interferencia y consiguen un bloqueo del tallo en el hueso esponjoso metafisario. Figura 10. Microscopia del crecimiento óseo. La extraordinaria documentación e información que proveyó de esta serie de casos (7), permitió obtener muchas observaciones como el porcentaje de osteointegración (Figura 10), la osteoporosis localizada por desfuncionalización (stress shielding) y el dolor de muslo, conclusiones que sirvieron para el desarrollar y mejorar el diseño de este tipo de componentes no cementados. Aquí es importante hablar en forma separada de los implantes acetabulares y de los femorales, dado que por las características anatómicas de cada uno de ellos es diferente, y por lo tanto también son diferentes los tipos de fijación y sus conceptos. Es importante recordar que en el acetábulo, la interfase hueso-prótesis es sometida a fuerzas de compresión, mientras que en el fémur, la misma superficie es sometida a fuerzas de cizallamiento y de torsión, que influyen de distinta manera en la osteointegración. Figura 11. Tallo Parhoffer Tipos de fijación no Cementada Los tipos de fijación no cementada pueden dividirse en dos grandes grupos de acuerdo a su superficie de fijación primaria: a) Macrofijación y b) Microfijación. Las prótesis de “Macrofijación”, no han mostrado un buen desempeño a largo plazo, por lo que su uso ha sido prácticamente abandonado. Un clásico exponente de esta superficie fue el tallo femoral Parhoffer Figura 12. Escamas Tallo Parhoffer 93 “Temas selectos de actualización en la Ortopedia Latinoamericana” consecuente aflojamiento del implante, con una alta tasa de aflojamiento. Owen y col tuvieron 12% de revisiones de sus acetábulos con un 16% de granulomas a 6.5 años de seguimiento (10). Figura 13 Tallo Spotorno Los acetábulos de macrofijación (Zweymuller, Furlong, Lord) fueron muy difundidos en Europa, donde se intentaba la fijación primaria por medio de un cono truncado roscado, que fueron muy utilizados, pero también tuvieron un alto índice de fallas con aflojamientos precoces y generando una gran pérdida del capital óseo, terminado en muchas oportunidades en protrusiones acetabulares muy complejas. Los acetábulos mas difundidos son los que tienen una configuración hemiesférica, y cuya superficie exterior puede estar hecha con distintos tipos de recubrimiento. Los tallos de “Microfijación” tienen distintos tipos de superficie para fijación biológica: La relación entre tamaño del poro y osteointegración fue estudiado en modelos caninos por varios autores (8-9), donde se vio que el aumento del tamaño del poro va asociado aumento de la fijación ósea. La mayoría de los trabajos concluyen que el tamaño ideal del poro esta en un rango entre 175 μm y 350 μm, siendo este el tamaño seleccionado hoy por la mayoría de las compañías manufactureras. El tamaño del poro por debajo o por encima de estos valores, hace disminuir la capacidad de osteointegración o hacer fallar mecánicamente al implante por el desprendimiento exterior del recubrimiento. Figura 14 Desprendimiento de esferas prótesis PCA a) Red de fibras b)Microporosidad c)Macroporosidad d) Plasma spray e) Recubrimiento de Hidroxiapatita Tanto los acetábulos como los tallos con macroporo ( PCA, Howmedica) mostraron un buen resultado inicial obteniendo osteointegración, pero debido al tamaño del poro de mas de 500 μm, se producía el desprendimiento del recubrimiento (Figura 13) con el 94 Figura 15 Zona de desprendimiento Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT El material utilizado para la fabricación del microporo es de una aleación de cromo cobalto, el que es agregado luego del forjado del implante a través de un proceso de sinterizado, que lo fija sólidamente al sustrato metálico. Este recubrimiento microporoso ha mostrado excelente comportamiento tanto en el tallo como en los acetábulos con sobrevidas superiores al 96% a más de 15 años. Los acetábulos con sistema de fijación biológica a través de “red de fibras de titanio” (Harris-Galante), mostraron una buena capacidad de osteointegración, y si bien fallaron las primeras series por roturas del mecanismo de traba del inserto de polietileno (HG I), esto fue mejorado en los diseños posteriores (HG II) mostrando un muy buen resultado a largo plazo. Esta red de fibras de titanio también es utilizada en los tallos, donde se fija en parches alrededor de la metafisis protésica en su sector anterior, posterior, ventral y dorsal, a través de un proceso de sinterizado. Figura 16 Red de fibras y crecimiento . Tabla comparativa de seguimiento de acetábulos no cementados 95 “Temas selectos de actualización en la Ortopedia Latinoamericana” Consideramos hoy que el desarrollo de los biomateriales ha permitido lograr una fijación duradera en el tiempo, que asegure la solidez de la unión implante-hueso. El problema a resolver en los finales de los 90 y comienzos del 2000, fue conseguir evitar los problemas de las partículas del desgaste protésico, que en muchas ocasiones son las que provocan la formación de granulomas por detrás del acetábulo fijo, y que llevan a pérdidas masivas de hueso que conducen a la revisión de una copa fija. El desarrollo en este sentido se orientó a conseguir superficies de fricción con baja generación de partículas, con el fin de generar menor cantidad de granulomas, por lo que aparecieron las llamadas superficies de fricción duras como la metal-metal o la cerámica-cerámica, que tienen ventajas importantes aunque no totalmente exentas de problemas. Asegurada la fijación en el tiempo, si uno puede tener superficies que tengan un desgaste muy bajo o casi nulo, se podría considerar que los acetábulos de ultima generación con superficies de fricción de bajísimo desgaste, podrían teóricamente dar a esta combinación, una sobrevida alejada muy superior a las conocidas, por arriba de los 30 o 40 años, pero solo el paso del tiempo y el control alejado de estos implantes tienen la respuesta. Metal Trabecular Actualmente han aparecido en el mercado algunos acetábulos no cementados de características diferentes a los anteriormente descritos, dado que el metal utilizado para su fabricación tiene una estructura de tipo porosa, similar a la del hueso esponjoso. Esta estructura se denomina “metal trabecular” o “metal poroso”, y tiene un modulo de elasticidad de 3 GPa lo que lo ubica entre el hueso cortical que tiene 15 GPa y el hueso subcondral que tiene 1,5 GPa. Consiste en poros interconectados que generan una estructura de tipo porosa en un 80%, la que se fabrica a través de la deposición de vapor, de 96 la que resultan celdas que están interconectadas de la misma manera que ocurre en el hueso trabecular. Otra de las características de esta superficie, es que tiene un coeficiente de fricción mayor que la superficie microporosa, lo que permite conseguir al impactarlo dentro de la cavidad acetabular, un mayor “press-fit” o fijación primaria a presión más sólida que con las copas convencionales. Además por las características de la superficie, el porcentaje de crecimiento óseo dentro del metal trabecular es superior al 80%, por lo que es más segura la fijación ósea del cotilo. Estas características fueron estudiadas inicialmente por J. D. Bobyn en animales (18-19) y la aplicación clínica fue presentada por la Clínica Mayo (20). Figura 17 Copa de metal trabecular Figura 18 Metal trabecular Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Estas características excepcionales lo transforman en una alternativa interesante en aquellos pacientes con deficiencias óseas o en los que esta disminuída la capacidad de neoformación ósea. Estos acetábulos de metal trabecular pueden estar hechos con metales diferentes como el tantalio y el titanio, pero muy biocompatibles y combinables entre sí, con lo que se dispone de copas íntegramente de metal trabecular donde luego de realizada la fijación primaria impactada o con tornillos, se cementa un inserto de polietileno en su cavidad; o acetábulos de titanio donde se coloca un inserto dentro de su sistema de bloqueo que puede ser de polietileno o de cerámica en la forma clásica, pero que por fuera en lugar de estar recubiertos de superficie porosa, están cubiertos de metal trabecular. Este tipo de metal poroso representa un avance importante en el desarrollo de copas de ultima generación, ya que tienen características similares al hueso esponjoso, lo que asegura su rápida incorporación y fijación, pero aun no se cuenta con un seguimiento a largo plazo que permita superar los excelentes resultados de los acetábulos de superficie microporosa. Hidroxiapatita La hidroxiapatita (HA) está ubicada dentro del grupo de las cerámicas, y su etimología proviene del griego “keramikos” que significa material quemado, haciendo mención a una característica especial de estos compuestos, la que en algún momento del proceso de fabricación son necesarias altas temperaturas como un factor imprescindible para su generación. Este grupo de las cerámicas esta integrado por la hidroxiapatita junto con la alumina, zirconia, carbón y los vitrocerámicos, el que también puede ser definido como lo hiciera Krajewskien 1992, como una variedad de materiales sinterizados caracterizados por la interconexión de granos de cristales unidos entre si. La HA es parte fundamental de los huesos y dientes, siendo ella casi el 50% del contenido de los mismos. Es una sal doble de fosfato tricalcico e hidróxido de calcio que puede encontrarse en forma natural en huesos, dientes y algunos corales marinos y a su vez puede ser creada en forma sintética. Los estudios realizados originalmente por J.F. Osborn a principios de los 80, en los que adicionaba HA en fracturas conminutas consiguiendo una buena regeneración ósea, estimularon al ARTRO Group de Lyon en Francia liderado por JP Vidalain , a pensar en la idea de recubrir un tallo con HA para conseguir una fijación biológica y así evitar el uso del “cemento acrílico”, signado en esa época por Hungerford (21) en USA como el culpable de los aflojamientos mecánicos de los tallos. Este primer desarrollo se realizó entre 1984 y 1985 y los estudios realizados en perros, con bloques de titanio recubierto en HA con un espesor de 150 μm, mostraron una osteointegración completa sin la formación de membrana fibrosa, lo que concluyó con la creación de un tallo de titanio recubierto con una capa de HA de alrededor de 150 μm, denominado Corail, y que fuera implantado por primera vez en 1986. Figura 19 Tallo Corail recubierto con HA 97 “Temas selectos de actualización en la Ortopedia Latinoamericana” Se utilizó una aleación de titanio ya que es con el único metal en que la hidroxiapatita se fija sólidamente, además por tener el titanio un 50% menos de rigidez que las demás aleaciones de CR-Co (22) lo que asegura mejor distribución de la transmisión de cargas y menor estrés mecánico. El tallo tiene una configuración metafisaria en forma de tulipa de sección cuadrangular, con escalones horizontales y estrías longitudinales para el bloqueo de la movilidad tanto en hundimiento como en rotación y un segmento distal levemente cónico recto que minimiza la aparición de dolor de muslo postoperatorio y de “stress shielding” u osteoporosis por desfuncionalización. El recubrimiento de hidroxiapatita es un proceso de mucha precisión que debe tener algunas características especiales para que sea duradero en el tiempo y logre su osteointegración. La proporción de HA utilizada es una mezcla de las fases cristalina y amorfa, y esto influye en el proceso de remodelación alrededor del hueso. La HA de fase amorfa es la que se disuelve parcialmente en el proceso de remodelación y genera el crecimiento óseo. Esta disolución genera alrededor del tallo una solución sobresaturada que precipita sobre el recubrimiento, atrayendo a las células que formaran osteoide sobre la superficie de HA, 98 logrando así una osteointegración duradera en el tiempo como se muestra en esquema de la figura 20. El espesor del recubrimiento debe ser de 150 μm aproximadamente, ya que parte del mismo se disuelve en el proceso de osteointegración, si el mismo es más fino, se corre el riesgo de que el mismo desaparezca completamente al disolverse parcialmente, y si fuera muy grueso se correría el peligro de que por tener un espesor tan grande se produzca la delaminación y el desprendimiento del recubrimiento del tallo, cosa que ha ocurrido en otros implantes en los comienzos de la era de los recubrimientos de HA. Nuestra experiencia con este tallo realizada en el Hospital de Clínicas de la Universidad de Buenos Aires, comienza en agosto de 1991 con la implantación del primer tallo Corail en America, y cuya serie original de 117 casos tiene un seguimiento de 14 a 20 años. Esta serie mostró una tasa de supervivencia del tallo Corail a 16.7 años de promedio de mas del 97%. Los resultados publicados en todo el mundo sobre seguimiento a largo plazo del tallo Corail son coincidentes con nuestra casuística, por lo que nos ha llevado a considerar a este tallo como el nuevo “patrón de oro” en vástagos femorales. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT BIBLIOGRAFÍA 1. Gluck T. Die invaginationsmethode der osteo-und arthroplastik. Berlin Klin Wochenschr 1890; 28:732-736, 752-757. 2. Smith-Petersen MN. Arthroplasty for the hip: a new method. JBJS 1939;21:269-288. 3. Wiles P. The Surgery of the osteoarthritic hip joint. Br J Surg 1958;45:488-497. 4. Charnley J. Anchorage of the femoral head prosthesis to the Shaft of the fémur. J Bone Joint Surg 47 (Br):28,1960. 5. Bränemark P, Hansson H. Et al. Osseointegrated implants in the treatment of edentelous jaw, experience from a 10 year period. Scand J Plast Reconstr Surg. 1977. 6. Engh CA Jr, CulpepperWJ II, Engh CA. Long term results of the anatomic medullary locking prosthesis in total hip arthroplasty. J Bone Joint Surg Am 79:177-184, 1977. 7. Engh CA, Bobyn JD, Glassman AH. Porous-coated hip replacements. Factors governing bone ingrowth, stress shielding and clinical results. J Bone Joint Surg BR 69;45-55, 1987. 8. Weish RP, Pilliar RM, Macnab I. Surgical Implants. The role of surface porosity in fixation to bone and acrylic. J Bone Joint Surg Am 53;963. 1971. 9. Jasty M, Bragdon CR, Schulzer CS. Bone ingrowth into porous coated canine total hip repla- cements. Quantification by backscattered scannig electron microscopy and image analysis. Scanning Microsc. 1989;3:1061. 10.Owen TD, Moran GG, Smith SR. Results of uncemented porous-coated anatomic total hip replacement. J Bone Joint Surg. 1994;76B: 258-262. 11.Kim Y, Kim VEM. Cementless porous coated anatomic medullary locking total hip replacement. J Bone Joint Surg. 1993;75B:6-13. 12.Engh C, Griffin WL, Mark CL. Cementless acetabular components. J Bone Joint Surg. 1990;72B:53-59. 13.Davitt JS, Dunn HK. Porous-coated anatomic total hip arthroplasty long term radiographic and survivorship analysis. J Athroplasty. 1996. 14.Barrack RL, Folgueras A, Munn B y col. Pelvic lysis at 5-8 years with porous coated hemispherical screw fixed acetabular component. AAOS 1995;19:319. 15.Dorr L. Five-year experience with press-fit cementless acetabular component. 13th Annual hip and knee course. 1996. 16.Schmalzried TP, Harris WH. The Harris-Galante porous acetabular component press-fit without screw fixation. J Arthroplasty. 1994;8:235-242. 17.Morsher EW. Current status of acetabular fixation in total hip arthroplasty. Clin Orthop 1992;274:172-193. 99 “Temas selectos de actualización en la Ortopedia Latinoamericana” 18.Bobyn J, Toh K, Hacking S, Tanzer M, Krygier J. Tissue response to porous tantalum acetabular cups in a canine model. J Arthroplasty, 1999;14(3): 347-354 19.19. Bobyn J, Stackpool G, Hacking S, Tanzer M, Krygier J. Characteristics of bone in-growth and interface mechanics of a new porous tantalum biomaterial. J Bone Joint Surg, 1999;81B(5):907-914. 20.Hungenford DS, Jones LC. The rationale for cementless revision of cemented arthroplasty failure. J Clin. Orthop 235:12-24. 1988. 21.Huiskes R. The various stress patterns of press-fit ingrown, and cemented femoral stems. Clin Orthop Relat Res. 261:27-37. 1990. 100 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Planeamiento Preoperatorio de la Artroplastia Total de Cadera Zachary Post, M.D. Alvin Ong, M.D. Fabio Orozco, M.D. Miembro Capítulo Cadera y Rodilla - SCCOT La Artroplastia total de cadera (ATC) es uno de los procedimientos quirúrgicos más exitosos de la era moderna. La literatura ha demostrado que en comparación con otros procedimientos quirúrgicos, sólo el injerto de derivación coronaria es más exitoso, al permitir a los pacientes regresar a sus actividades y mejorar la calidad de vida (1). El abrumador éxito de la ATC ha permitido que cientos de miles de pacientes puedan volver a las actividades que alguna vez hicieron y que pensaron imposible el realizarlas de nuevo. El éxito de la ATC, por desgracia, también pueden haber convencido a algunos cirujanos que un buen resultado después de la artroplastia es una conclusión predeterminada. Hemos visto en numerosa literatura reciente, que la técnica quirúrgica descuidada puede dar lugar a resultados desalentadores (2). El abrumador éxito de la ATC como un procedimiento quirúrgico es probable que haya contribuido al aumento sin precedentes de su utilización en la última década (3). Este aumento de la demanda en combinación con los crecientes costos quirúrgicos amenaza con sobrepasar los presupuestos sanitarios de muchos gobiernos en todo el mundo; ahora es la responsabilidad de un buen cirujano, no sólo asegurar resultados exitosos para sus pacientes, sino también ayudar a reducir al mínimo los costos asociados con la ATC. Para asegurar el éxito de ambos objetivos, es crítico que la eficiencia sea la norma y las complicaciones se mantengan en un mínimo. La planificación preoperatoria es el primer paso para lograr resultados consistentemente exitosos para todos los pacientes; uno de los puntos claves de la planificación es adelantarse para evitar cualquier sorpresa en la sala de operaciones; resultados inesperados en la cirugía puede conducir a desenlaces menos que perfectos, así como al aumento de los tiempos operatorios. El cirujano que ha preparado adecuadamen- 101 “Temas selectos de actualización en la Ortopedia Latinoamericana” te cada caso planificándolo, finalizará cada procedimiento de manera expedita y óptima. Se ha demostrado que un acortamiento en los tiempos quirúrgicos, por sí solo, puede llevar a una disminución en la incidencia de la infección (4). La preparación adecuada también dará lugar a la restauración constante de la biomecánica apropiada de la cadera, afectando de manera favorable la longevidad de los componentes protésicos. La nueva economía de la salud exigirá que nosotros, como cirujanos, seamos mejores, más rápidos y eficientes con los recursos que tengamos asignados. La clave para lograr este objetivo en la ATC se encuentra en la planificación preoperatoria. HISTORIA Un enfoque exitoso en cada Artroplastia que realizamos, inicia tratando la operación como una experiencia que comienza la primera vez que el cirujano se encuentra con el paciente. Esta interacción se inicia con la historia y una adecuada anamnesis; recuerde que uno de los objetivos de la planificación es evitar sorpresas en el quirófano; si realizamos a cada uno de nuestros pacientes dos sencillas preguntas, sus respuestas nos ayudarán a evitar sorpresas. Pregunta 1: ¿Es el dolor del paciente consistente con los hallazgos de la historia y de los rayos X? Pregunta # 2: ¿Hay algo en la historia de nuestro paciente que podrían llevar a sospechar la existencia de verdaderos problemas en la sala de operaciones? Como dice el viejo refrán, “El paciente nos dirá lo que está mal con él, si sólo nos permitimos darle su tiempo y escuchar”. La mayoría de los cirujanos que realizan artroplastias, han evaluado cientos de historias de pacientes con dolor en la 102 cadera; la pregunta # 1 obliga al cirujano a comparar cada paciente con lo que ha visto en el pasado; la mayoría de los pacientes que presentan dolor en la cadera, tienen una historia que es consistente con el diagnóstico de enfermedad articular degenerativa de la cadera; ellos se quejan de un aumento gradual de los síntomas que se ha vuelto más grave. Cuando se interroga, los pacientes suelen recordar los episodios de dolor de meses e incluso años anteriores a la presentación a la oficina de un médico. El dolor asociado con la Artrosis de Cadera, es a menudo de tipo mecánico, aumenta con las actividades y se localiza en la región inguinal; anomalías sutiles en este modelo, pueden ayudar en el diagnóstico de otras patologías que de no diagnosticarse, podría dar lugar a complicaciones y/o resultados desfavorables después de un Reemplazo de Cadera. La paciente de la figura 1, se presentó con dolor de cadera que había estado presente durante varias semanas; curiosamente, ella negó una larga historia de dolor más que a lo sumo, unos pocos meses. Se hizo una Impresión diagnóstica de Necrosis Avascular avanzada con colapso articular y se empezó a discutir con ella la posibilidad de realizar una Artroplastia Total de Cadera como tratamiento. La paciente fue vista nuevamente antes de su Artroplastia, con incremento de la severidad del dolor; debido al cambio inesperado en la naturaleza de los síntomas, se ordenó repetir los estudios radiológicos; Las radiografías en la figura 2 fueron tomadas 4 semanas después de las expuestas en la figura 1. Estas radiografías más recientes, demuestran una pérdida completa de la cabeza femoral. Un posterior aspirado articular y cultivo, diagnosticaron una Artritis Séptica, causada por un germen identificado como PROTEUS MIRABELIS. En lugar de realizar entonces una Artroplastia primaria Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT los problemas médicos deben ser cuidadosamente revisados. Un problema común encontrado es una historia de malignidad que podría afectar la calidad del hueso. Los tumores más comunes que hacen metástasis al hueso incluyen el cáncer de mama, cáncer de próstata, cáncer de células renales o cáncer de pulmón. Figura 1. Figura 3. Figura 2. de rutina, este paciente se sometió a un procedimiento en dos tiempos, el primero con la colocación de un espaciador de cemento antibiótico seguido 10 semanas más tarde por su Artroplastia (figura 3). La naturaleza del dolor en esta situación no era coherente con lo que cabría esperar. La búsqueda de esta inconsistencia evitó un resultado negativo que pudo ser grave. La Pregunta # 2 requiere en primer lugar una revisión exhaustiva de toda la historia médica y quirúrgica, en busca de cualquier cosa que pueda afectar negativamente el resultado; en primer lugar, todos El aumento de la vascularización secundaria a enfermedad metastásica de cualquiera de estos tumores podría conducir a la pérdida de sangre extrema y al aumento de complicaciones potencialmente mortales dentro de la cirugía; en el contexto de enfrentarnos a un tumor metástásico que afecte la cadera, debe ser considerada una consulta con el oncólogo; la embolización preoperatoria de las lesiones óseas muy vascularizadas, puede permitir realizar con mayor seguridad la Artroplastia. De igual manera, una historia de radioterapia previa por enfermedad metastásica en la región de la cadera también pueden disminuir la probabilidad de éxito con el press-fit de nuestros componentes; en este caso parte del planeamiento es la utilización de componentes cementados, que se recomiendan en esta situación. 103 “Temas selectos de actualización en la Ortopedia Latinoamericana” Cualquier historia de enfermedad que pueda afectar la calidad del hueso también debe ser investigada a fondo; La artritis reumatoide (AR), enfermedad de Paget, o un historial de uso crónico de esteroides pueden debilitar el hueso cortical y aumentar el riesgo de fractura. La conciencia de este potencial aumento en el riesgo de fractura intraoperatoria, hace que se puede planificar una manipulación suave para evitar una fractura. Además de un mayor riesgo de fractura, muchos de los pacientes modernos con AR se encuentran bajo tratamiento con inhibidores del TNF para el manejo de su enfermedad. Estos fármacos se administran típicamente IV cada 4 a 8 semanas y suprimen la respuesta inmune a la infección; la mayoría de los cirujanos recomiendan que los pacientes que están tomando estos medicamentos tengan un período libre de medicación, entre 4 a 6 semanas antes de someterse a una Artroplastia, para reducir al mínimo el riesgo de infección. Una historia de cirugía previa en la región de la cadera o la pelvis puede determinar cuál será el enfoque que se utilizará para la realización de nuestro implante. En nuestra práctica utilizamos bien sea, el abordaje directo anterior o un abordaje lateral directo. Una historia de cirugía previa en la cadera a intervenir (cirugía de la cadera displásica en la infancia, fractura de cadera previa, biopsia, disección de los ganglios, o un procedimiento de derivación vascular) es una contraindicación para que usemos el abordaje anterior directo; una historia de fractura de la pelvis o de acetábulo, sobre todo con material de osteosíntesis en posición que podría pensar en retirarse, debería ser una indicación para utilizar un abordaje posterior. El abordaje lateral directo es más adecuado para la conversión a una ATC cuando haya un clavo intramedular retenido o una placa esté presente. Una vez que la historia está completa, deben hacerse notas especiales, con el fin 104 de alertar al cirujano y el personal de acompañamiento, sobre los retos particulares de cada caso; en nuestra práctica, es nuestra costumbre el tomar notas directamente sobre las radiografías, que acompañarán al paciente a la sala de operaciones. De esta manera todas las situaciones pertinentes y especiales serán revisadas varias veces antes de comenzar la operación (figura 4). Figura 4. EXAMEN FÍSICO Después de realizar una historia clínica detallada, el examen físico completo es una de las cosas a las que debemos dar la mayor importancia como cirujanos, para prepararse para la cirugía. Un buen examen debe comenzar con una detallada inspección, prestando especial atención a la zona donde se hará la incisión; en el contexto de existir cirugías anteriores, es crítico determinar si la incisión previa se puede utilizar para realizar nuestra Artroplastia. Si la incisión anterior no puede ser utilizada, debe planearse una incisión y por donde debe trascurrir; si existen incisiones múltiples debe ser planificada nuestra incisión de tal manera que evite los ángulos agudos entre las incisiones que podrían conducir a necrosis de la piel Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT y/o dehiscencia de la herida. Además de las cicatrices previas, lesiones dermatológicas locales, tales como erupciones o áreas de eritema, deben tenerse en cuenta. Estos hallazgos pueden tener implicaciones significativas en el enfoque y los resultados. En nuestra práctica la obesidad, que genera como resultado, la superposición de la piel en la ingle es una contraindicación para el uso de un abordaje anterior directo; las áreas de celulitis, escoriaciones o heridas abiertas pueden retrasar la cirugía y deben ser descubiertas y tratadas antes de encontrarlas por sorpresa en el quirófano. Una vez que el área quirúrgica inmediata ha sido evaluada, se debe hacer una inspección minuciosa de la pierna, así como de la extremidad contralateral. Llagas abiertas o zonas de celulitis activas son un riesgo para la infección y podría retrasar la cirugía; los pacientes con piel delgada o frágil, se deben identificar para evitar desgarros en la piel, bien sea durante el posicionamiento de la cirugía o durante la retirada de los apósitos quirúrgicos; la documentación de los pulsos disminuidos o hallazgos anormales neurológicos evitará la preocupación o realización de estudios diagnósticos costosos en el postoperatorio inmediato. Por último, una evaluación de la longitud de las piernas es fundamental en la planificación para la reconstrucción de la cadera. La mayoría de los pacientes tendrán un acortamiento de su extremidad en el lado a ser operado. La documentación de la cantidad de dicho acortamiento, puede ayudar a la hora de planificar la colocación de los componentes; Ocasionalmente, algunos pacientes pueden tener una extremidad más larga, en el lado en que la cirugía se va a realizar; tener conciencia de esto y documentarlo antes de la cirugía puede prevenir el acortamiento intencional de la sala de operaciones que podría conducir a generar inestabilidad. RADIOLOGIA X En nuestro servicio, los estudios solicitados estándar para todos los nuevos pacientes, son una Radiografía de pelvis AP y una lateral de rana. Una vez que la historia clínica y el Examen Físico estén completos, la revisión de estas radiografías, constituye la parte más importante de la planificación preoperatoria. Otros proyecciones especiales de rayos X se han descrito como útiles en la planificación preoperatoria pero la gran mayoría de los pacientes pueden ser evaluados adecuadamente con sólo estos dos. Las tradicionales películas duras en acetato se han utilizado durante décadas por los cirujanos ortopédicos para evaluar a los pacientes y la planificación de una Artroplastia. Estas películas tradicionales son tomadas a una distancia estándar del rayo hasta la placa, lo cual permite una magnificación predecible. El factor de ampliación permite una evaluación precisa y la planificación quirúrgica; en la última década se ha hecho cada vez más común que los consultorios de ortopedia empiecen a utilizar los formatos digitales de rayos x. La toma Digital de radiografías, requiere mucho menos trabajo y su revelado es más rápido que con una película tradicional. Estas nuevas máquinas también permiten el fácil registro y recuperación de películas, así como la eliminación de la necesidad de almacenar físicamente las radiografías; los beneficios de esta nueva tecnología tienen un costo en la reproducibilidad del factor de magnificación de la película tradicional. Para superar esta discrepancia de ampliación, la mayor parte de los sistemas digitales de rayos X, recomienda una calibración de cada película antes de la revisión clínica objetiva para la medición y utilización de plantillas especificas para el planeamiento; El proceso de calibración comienza por tomar la imagen del paciente con una bola metálica de alta densidad, colocada en el 105 “Temas selectos de actualización en la Ortopedia Latinoamericana” campo a visualizar, con un tamaño predeterminado de radio conocido (figura 5). La bola se coloca en el nivel del fémur en el plano anterior / posterior. Esto se hace típicamente de dos maneras: la primera consiste en colocar la bola en el nivel del trocánter mayor con el uso de un soporte que la sostiene, mientras se toma la imagen; el segundo utiliza una correa que va alrededor de la pierna del paciente y coloca dicha bola metálica en el centro de las piernas, presumiblemente en la porción media del muslo y por consiguiente, a nivel del hueso. Una vez que la imagen ha sido tomada debidamente, se realiza una calibración en la radiografía; La mayor parte de los sistemas digitales de rayos X son capaces de encontrar la bola de forma automática y ajustar el tamaño en consecuencia; algunos sistemas requieren que el usuario identifique la localización y el tamaño de la bola, así como asignar el diámetro conocido de la misma; la calibración se realiza entonces de acuerdo con el tamaño de entrada de la bola. En nuestra experiencia, la calibración de las películas digitales supone una empinada curva de aprendizaje para los técnicos de rayos X con el fin de conseguir colocar la bola correctamente. Para los pacientes delgados, es relativamente fácil, pero para los pacientes con sobrepeso, la colocación correcta puede ser un desafío. Hemos encontrado que la exactitud de las mediciones de tamaño es tan buena como la colocación de la bola de calibración. Aún tenemos que llegar a un punto donde se sienta que la precisión de nuestro sistema digital es tan buena como la del sistema de película analógica que sustituye. PLANTILLAS Una vez que tenemos buenas radiografías, con una calibración conocida podemos empezar a utilizar las plantillas para la reproducción de las mediciones anatómicas y escoger la posición y tamaño de los implantes para nuestro paciente. El primer 106 paso es identificar los puntos de referencia anatómicos reproducibles con las plantillas en las radiografías. La imagen en gota de lágrima es un hallazgo casi universal en la proyección AP; esta se forma por la confluencia de la cara medial inferior del acetábulo en su transición hacia el isquion y su nombre se debe al parecido con una gota de lágrima cayendo en la parte inferior del acetábulo. La segunda marca importante es la “Ceja”, que es el borde superior del acetábulo. La línea de Kohler es una línea vertical que se extiende desde el agujero obturador de la escotadura ciática, y es una aproximación de la cara medial del acetábulo en la proyección AP; finalmente, debe ser dibujada una línea horizontal que apenas toque el borde inferior de la gota de lágrima de ambas caderas (figura 5). Figura 5. Después de que los puntos de referencia anatómicos y las líneas se han trazado, puede identificarse y definirse la anatomía del paciente; La línea horizontal se debe utilizar para evaluar la discrepancia relativa longitud de las piernas. Esto se realiza mediante la identificación de un punto de referencia común a ambos fémures y midiendo su distancia de la línea horizontal. En nuestra Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT práctica, utilizamos típicamente la porción media del trocánter menor; La línea de Kohler se utiliza para identificar la protrusión. Cualquier penetración media de la cabeza femoral, más allá de esta línea se considera la protrusión. La línea de Kohler también se utiliza para evaluar el offset femoral; para tal fin, se traza una línea vertical por el centro de ambos fémures y se dibuja la distancia horizontal desde la línea en el lado normal (lado no quirúrgico) a la línea de Kohler, con lo que estamos midiendo el offset femoral. Por último, se identifica el centro de la cabeza femoral. Esto representa el centro actual de rotación de la cadera (figura 6). Figura 6. ACETÁBULO En nuestra práctica, comenzamos planificando el acetábulo con las plantillas; se elige una plantilla con el tamaño posible de la copa y se coloca en el acetábulo, colocando el borde inferior de la imagen del cotilo, en la parte inferior de la gota de lágrima. El ángulo de la copa se coloca en aproximadamente 40 a 45 grados con relación a la línea horizontal (figura 7). El tamaño de la plantilla se incrementa, mientras se mantiene la posición medial, hasta que la cara lateral de la copa toca la cara lateral del acetábulo, o la copa llena el espacio acetabular. Se selecciona la copa que mejor ajuste tenga, para garantizar el llenado adecuado del espacio acetabular sin la extracción excesiva del hueso; una vez que el tamaño de la copa se ha elegido, su posición e inclinación se han decidido, se identifica el nuevo centro de rotación de la cadera. El centro de esta copa representa la colocación prevista para el centro de rotación de la cadera; si se utiliza una plantilla digital, esta posición se guarda; si se utiliza la radiografía tradicional, el borde exterior de la copa se traza sobre la película, incluyendo el centro de la posición de la copa. (Figura 7). Figura 7. A menudo, cuando utilizamos las plantillas para planear nuestro acetábulo, podemos encontrar anomalías anatómicas, así como cambios estructurales en el hueso secundario a la enfermedad degenerativa; el más común de ellos es la lateralización del centro de rotación; cuando se pierde la forma esférica de la cadera por enfermedad degenerativa, los osteofitos hipertróficos puede comenzar a llenar el espacio medial del acetábulo; este proceso resulta en la extrusión de la cabeza femoral en dirección 107 “Temas selectos de actualización en la Ortopedia Latinoamericana” lateral. En este contexto, es fundamental identificar correctamente el verdadero centro de rotación de la cadera; La pared lateral de la lágrima es una guía reproducible que dirigirá la colocación correcta de la copa. Es importante ignorar el exceso de hueso y la posición lateral de la cabeza femoral y colocar el borde medial del cotilo contra la gota de lágrima. Otro hallazgo común anormal en la enfermedad degenerativa de la cadera es la displasia de cadera, con la migración superolateral de la cabeza femoral. Sea displasia o migración, el resultado final es a menudo ausencia de un borde lateral de soporte hueso, donde colocar la copa acetabulo. Varias opciones viables se encuentran disponibles en esta situación; La más sencilla es colocar la copa en una posición ligeramente más vertical, permitiendo que el mismo vaso para ocupar el defecto óseo. Este enfoque es mejor reservarlo para los casos de pérdida leve de masa ósea leve o displasia. Un método comúnmente utilizado, consiste en colocar la copa en la posición anatómica correcta dejando un defecto óseo que no puede ser llenado con el sólo acetabulo (figura 8). Figura 8. 108 Tradicionalmente, este defecto se ha llenado con un injerto de hueso de la misma cabeza femoral, asegurado en el margen superolateral del acetábulo con tornillos dirigidos en sentido de la carga; Una vez que el injerto de hueso esté en su lugar, la copa podría estar firmemente colocada en una posición anatómica correcta. Recientemente se ha hecho más común el uso de uno de varios dispositivos de aumentación con metales de alta fricción. Estos aumentos, oblongos que se consiguen simulando el defecto súpero/externo, esencialmente llenan el vacío óseo con el metal y están fijados en posición con tornillos. La mayoría de los fabricantes tienen plantillas de sus aumentos, que pueden ser colocados sobre la plantilla de copa, evaluando el tamaño requerido. Una vez que el aumento está en posición, la copa puede asegurarse de forma normal y luego unida al aumento, por lo general con una pequeña cantidad de cemento óseo, para evitar la fricción entre diferentes metales. En nuestra práctica hemos utilizado ambos enfoques, pero más recientemente se han preferido los suplementos metálicos por su facilidad de implantación, así como la reproducibilidad superior a la del injerto de hueso de la cabeza femoral. Otra opción para hacer frente a un cotilo descubierto, es colocar el implante en una posición relativamente medial. La profundización del acetábulo de esta manera, permite una mejor cobertura lateral de la copa por hueso fuerte dejado en el anillo periférico. En nuestra experiencia, el uso de los nuevos cotilos de metal trabecular de alta fricción hace que este enfoque sea más viable. Una combinación de una copa un poco más grande, colocada más medial y dejando una pequeña porción de la copa descubierta, puede ser muy eficaz para los casos de pérdida ósea moderada o displasia. La mayoría de los expertos coinciden en que hasta un 20% de la copa puede ser dejado al descubierto, sin aumentar el riesgo de fracaso y la utilización de este Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT hecho puede ayudar a evitar costosos aumentos de aloinjerto óseo estructural o metal trabecular. Por último, para los casos de displasia severa de cadera se podría utilizar un centro de rotación alto. Esta filosofía, preconiza colocar el acetabulo en una posición mucho más alta que el centro de rotación; el problema es que cuanto más alta se coloque la copa, el hueso de buena calidad disponible es mucho menor para asegurar su posición, ya que las paredes del ilíaco se estrechan y corticalizan. Además, los estabilizadores de la cadera son menos eficaces, entre más alejada esté la copa del centro de rotación original de la cadera, que se obtiene a partir de su posición correcta. Por estas razones, un centro rotacional de la cadera alto, sólo se utiliza si no hay otras opciones disponibles. El Protrusio es menos común que la lateralización del centro de la cadera, pero puede presentar dificultades durante la cirugía si no se planea de manera adecuada; se considera una protrusión de la cadera, cuando una parte de la cabeza femoral está medial a la línea de Kohler; este centro de rotación no anatómico debe evitarse. La gota de lágrima es de nuevo una valiosa guía para ayudar a colocar la copa en la posición correcta Al colocar el cotilo en el centro anatómico de rotación de la cadera en protrusión, habrá a menudo un defecto de la pared medial para corregir; esto puede hacerse con injerto de hueso morselizado o bien, mediante la colocación de un injerto estructural de cabeza femoral; en cualquiera de los casos, es importante aumentar el tamaño de la copa ligeramente para asegurar un buen ajuste periférico que soporte de manera adecuada la copa (Figura 9 y 10). FEMUR Una vez que la posición acetabular está completa y el nuevo centro de rotación identificado, el cirujano puede pasar al fémur. En nuestra práctica comenzamos dibujando Figura 9. Figura 10. el nivel anticipado de la resección en el cuello femoral; Esto se hace al trazar una línea desde donde la depresión de la fosa piriforme se encuentra con el borde medial del trocánter mayor a un punto de aproximadamente 1 cm proximal al borde superior del trocánter menor. Una plantilla de tamaño inicial del fémur se coloca entonces sobre el canal femoral, teniendo cuidado de asegurar que la plantilla está alineada con la línea central del fémur, evitando el posicionamiento del vástago en varo o valgo. Si se utiliza un implante de cobertura porosa 109 “Temas selectos de actualización en la Ortopedia Latinoamericana” proximal, el tamaño es elegido por encajar y llenar de la porción proximal del vástago en la metáfisis. Si se utiliza un implante totalmente recubierto, el tamaño se elige sobre la base de relleno del istmo, así como la porción proximal del canal. (Figura 11). Figura 11. Ha sido nuestra experiencia con el uso frecuente de tallos con cobertura proximal, que en ocasiones el mejor ajuste proximal no fije bien distal; encontramos esto con más frecuencia en hombres jóvenes sanos, donde el tallo de tamaño adecuado proximal, es demasiado grande distalmente. Hemos utilizado varias técnicas para compensar esto, que van desde broches personalizados distales a la utilización de fresas flexibles para crear espacio suficiente distalmente, que permitan un ajuste proximal adecuado. De vez en cuando, también utilizamos vástagosde diferentes fabricantes que tiene un menor perfil distal (figura 12); anticipar este problema es otra cualidad invaluable de una buena planificación preoperatoria. Una vez que ha sido elegido un tamaño de vástago inicial, el centro de rotación del componente femoral se coloca en el mismo nivel vertical que el centro de marcado previamente de rotación de la copa. En este punto se hacen ajustes al nivel de la resección del tallo. El nivel anticipado de la resección puede necesitar ser movido hacia proximal o distal, para colocar mejor el centro 110 Figura 12. de la cabeza femoral y que coincida con el nivel del centro previsto del componente acetabular. Para los pacientes con un cuello femoral corto, el nivel de la resección puede tener que ser movido distalmente a un nivel de resección baja. Los pacientes con un cuello más largo femoral puede requerir un mayor nivel de resección. Los fabricantes de implantes ortopédicos actuales, generalmente tienen 2 versiones de un mismo vástago femoral, una estándar y otra con offset aumentado; una vez que el nivel vertical de la rotación del vástago femoral esté colocado, se pueden hacer ajustes entre estas dos versiones con sus plantillas; la versión que mejor restaure el offset femoral el la que debe elegirse. (Figura 14). La medición de la distancia desde la línea de Kohler a una línea vertical por el centro del tallo y la comparación de esta distancia con el offste femoral de la cadera sana previamente medido desde el lado no quirúrgico determina el offset que se debe restaurar. Los pequeños ajustes del tamaño Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT una restauración casi perfecta del offset, el centro de rotación y longitud de las piernas en la mayoría de los casos (Figura 13). Figura 13. del tallo se pueden hacer para asegurar el mejor ajuste mientras se mantiene offset y centro de rotación. En general, la disminución del offset femoral, debe evitarse. Cuando la plantilla femoral seleccionada está bien adaptada a la anatomía del paciente, pasamos a realizar los ajustes para la restauración de longitud de las piernas. La mayoría de los pacientes con enfermedad degenerativa de la cadera tiene una extremidad acortada en su lado quirúrgico. La magnitud de este acortamiento se determina mediante la evaluación inicial de la longitud de la pierna. La mayor parte del acortamiento encontrado, se puede compensar con la correcta restauración del centro de la cadera. La distancia vertical desde el centro de la cabeza femoral hasta el centro de la copa acetabular es la cantidad de alargamiento que la restauración del centro rotacional de la cadera permitirá lograr. Si algún acortamiento está todavía presente, este se puede planear compensar mediante la utilización de cuellos con longitud adicional (large o extralarge). La variación de la longitud del cuello permitirá Una vez el planeamiento con las plantillas femorales está completo, es nuestra práctica de rutina, registrar todos los cambios previstos en la misma radiografía que será llevada al quirófano. Esto incluye un esquema general de la posición del vástago femoral, así como el nivel de resección planificada y la distancia desde ese nivel a la parte superior del trocánter menor. El vástago normal o con offsert extendido si se tiene previsto también se registra (lateralizado o estándar), el tamaño del tallo y la longitud del cuello previsto. Además, notas especiales, como anticipación de escariar o brochar distal, se hacen directamente sobre la misma radiografía. CONCLUSIÓN Benjamín Franklin es citado a menudo como diciendo, “Cuando usted no puede planear, usted planea fallar”. Esto nunca ha sido más cierto que cuando nos enfrentamos a cada Artroplastia Total de Cadera. Problemas adecuadamente previstos en la sala de operaciones son fáciles de superar; sin embargo, los problemas que no han sido previstos pueden conducir a un caos, el menor de los cuales es la ineficiencia en la sala de operaciones que pueden aumentar el Figura 14. 111 “Temas selectos de actualización en la Ortopedia Latinoamericana” costo, alargar el tiempo quirúrgico y aumentar la pérdida de sangre intraoperatoria. Fallas de planificación más graves puede ser peligroso para los pacientes y dar lugar a complicaciones que ponen en peligro el resultado del procedimiento. Un aforismo popular en ortopedia de formación es que el 80% de la operación se realiza antes de entrar al Quirófano. La aplicación sistemática de este principio dará lugar a un resultado exitoso para cada uno de nuestros pacientes y reproducible a través de una carrera de muchos reemplazos de cadera para el cirujano que juiciosamente la lleva a cabo. Figura 12. BIBLIOGRAFÍA 1. O’Shea, K, E Bale, y Murray P. “Análisis de costos de reemplazo total de cadera primaria.” Irlandés Medical Journal 95, no. 6 (junio de 2002): 177-180. 2. Hart, AJ, K Ilo, R Underwood, Cann P, Henckel J, Lewis A, Cobb J, J y Skinner. “La relación entre el ángulo de la versión y la tasa de desgaste de los metales recuperados-metal remodelaciones:. Un estudio prospectivo, CT-Estudio basado en” El Diario de Cirugía Ortopédica y Traumatología. Volumen británica 93, no. 3 (marzo de 2011): 315-320. 3. Salud y Costo del Proyecto de Utilización (HCUP). Nationwide Inpatient Sample (NIS). Agencia para la Investigación y Calidad; 1999-2008. 4. Willis, Owen, aire acondicionado, A Konyves y D K Martin. “Factores que afectan la incidencia de infección en el reemplazo de cadera y rodilla: un análisis de 5277 casos.” La Revista de Cirugía Ortopédica y Traumatología. Volumen británica 92, no. 8 (agosto 2010): 1128-1133. 112 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Complicaciones en Artroplastia Total de Cadera Everth Mérida Herrera, M. D. * Cirujano Ortopedista especializado en Cirugía de Cadera, adscrito al servicio de Endoprótesis del Hospital de Ortopedia Magdalena de las Salinas y en el Hospital Angeles Metropolitano, México. DF INTRODUCCIÓN La artroplastia total de cadera (ATC), es el procedimiento quirúrgico más exitoso de la ortopedia y de la medicina quirúrgica en general, a tal punto que la OMS la denominó como “..el procedimiento quirúrgico del siglo..”. Realmente sus resultados son bastante espectaculares y día a día hay un notable incremento de ésta cirugía protésica; sin embargo no está exento de problemas y complicaciones, por tanto también hay mayor número de re-intervenciones quirúrgicas de todo tipo. se que 19 de los eventos mayores son de cirugía ortopédica y 6 son los más relevantes en ATC, ocupando el primer lugar la discrepancia de las extremidades post quirúrgicas y como causa de re intervención la luxación protésica (2). Como bien podemos suponer, en nuestro medio latinoamericano no estamos nada alejados de éste importante reporte y es necesario realizar un análisis sobre los tipos de complicaciones, las circunstancias en que se pueden producir y sobretodo, buscar la manera de corregirlos o mejor prevenirlos. En los últimos años en la unión americana, Medicare recalcó “…un notable incremento de las reintervenciones quirúrgicas”, tanto que la Joint Commission on Accreditation of Healthcare Organizations, (JCAHO), realizó un profundo estudio al respecto y publicó en Junio de 2003 un reporte sobre las fallas y complicaciones quirúrgicas (1) encontrándo- Complicaciones más comunes en artroplastia total de cadera Es innumerable la cantidad de reportes que existen sobre complicaciones post Artroplastia; existen reportes desde lo más simple, hasta reportes con fracturas periprotésicas muy complejas. Sin embargo se puede realizar una compilación de todos ellos 113 “Temas selectos de actualización en la Ortopedia Latinoamericana” y agruparlos de manera que sea más fácil su revisión. De esta forma se puede tener una mejor idea de las diferentes complicaciones en ATC. Coincidiendo con el reporte de la JCAHO, la discrepancia post quirúrgica de las extremidades es sin duda la más frecuente de todas. Discrepancia de las extremidades Como se mencionó anteriormente, es la más claramente perceptible y común de todas. Su importancia no radica precisamente en la complicación por sí misma, sino por la percepción propia del paciente, ya que esta es la primera impresión que tiene el paciente sobre su cirugía y lo nota desde el momento en que inicia la deambulación. (fig.1) Es tan alto el número de casos que el Bureau of Healthcare of de United States se ha referido a él como “una complicación tan común que ha alcanzado ya niveles de iatrogenia”.Las consecuencias que pueden acarrear, van desde una lesión neurológica (generalmente parálisis isquiática, peronea y/o femoral) que puede llegar a ser muy grave, pasando por una carga anormal de la cadera ocasionando dolor bajo de espalda y cojera por desnivel. También se ha visto casos de luxación protésica por un notable acortamiento en el offset y el brazo de palanca de los aductores lo que condiciona el aflojamiento de las partes blandas con una incapacidad de contención de la cadera. La consecuencia más incómoda y molesta puede ser para el propio cirujano ya que puede terminar en un problema legal. El paciente se siente molesto, incómodo y no acepta fácilmente un zapato más alto, o un realce mediante plantilla. Edeen comprobó que casi la cuarta parte de los pacientes requieren de un aumento en el zapato (3). Como parte de las acciones que se deben seguir para evitar éstas molestias se recomienda en primer lugar una información detallada del tipo de cirugía, los riesgos que conlleva y sobretodo, las posibles complica- 114 Figura 1. Clara discrepancia de la longitud de las extremidades post artroplastia total de cadera ciones donde se debe incluir la posibilidad de una dismetría de las extremidades inferiores, muy especialmente en los pacientes donde ya se observa en el examen clínico inicial, una clara dismetría ya sea por defecto o deformidad de las extremidades (genu valgo o varo, secuelas de alguna fractura con alteración de la longitud de las extremidades, etc.) y asentarlo en el consentimiento informado, especialmente si no se tiene la capacidad de poder realizar la nivelación de las extremidades o estar seguro de poder asegurar la igualdad de las extremidades al término de la ATC. El segundo punto importante es la planificación preoperatoria, donde se debe realizar siempre basándonos en la cadera contralateral sana o ya operada seleccionando muy bien el tipo que requiere, altura de los cortes, etc. Un buen consejo es realizar una medición transoperatoria, Se puede colocar un clavo de Steinmann en la parte superior del acetábulo como punto fijo de medición y otro sobre la parte lateral del trocánter mayor (fig.2); se mide la distancia entre ambos antes de proceder a realizar la osteotomía y se realizan mediciones de prueba hasta llegar a la distancia previamente determinada en la planificación preoperatoria. Inclusive se pueden tomar controles radiográficos transquirúrgicos para medir distancias. Por último, el manejo fisiátrico para la recuperación muscular debe ser supervisado. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Figura 2. Se puede colocar intraoperatoriamente dos pines fijos tanto en trocánter mayor como en un punto fijo de iliaco y medir las distancias. Luxación protésica Actualmente es la primera causa de reoperación en cirugía protésica desplazando al aflojamiento protésico no séptico. La oficina de salud de la unión americana (Bureau of Healtcare of the United States) se refiere a ella como “una complicación tan común que ha alcanzado ya niveles de preocupación”. Se calcula que oscila entre el 3% al 5% (OKU, Hip and Knee Society. AAOS, 1995), hay reportes de series grandes como el de Woo y Morrey con 10.500 casos (1) con un porcentaje de 3.2%, No hay cifras claras al respecto y puede llegar hasta cifras tan altas como 10%, porque no existen datos fidedignos de la incidencia real, pues muchos casos no se reportan o se re-operan bajo otro diagnóstico. La incidencia es mucho mayor en los casos de revisión con recambio protésico de cadera elevándose a un 10 25 % (4) y más de la mitad de todas las luxaciones se presentan en los 3 primeros meses de postoperatorio y tres cuartas partes en el primer año (1,5). La luxación postquirúrgica es un problema altamente frustrante tanto para el cirujano como para el paciente que se vuelve muy temeroso de tener un nuevo episodio de luxación. Los factores atribuibles como causas de luxación se pueden dividir en dos grupos: factores atribuibles al paciente y factores propios de la cirugía (6). a. Entre los factores atribuibles al paciente, existen alteraciones neuromusculares y alteraciones del estado de la conciencia como bien la han reportado Fackler y Poss (7). Estas alteraciones como la parálisis cerebral, distrofia muscular, demencia, alcoholismo, drogadicción, etc. pueden ser responsables de hasta un 22% en casos de luxación simple y de un 75% en los casos de luxación recidivante. La debilidad o el imbalance muscular, junto con la incapacidad de poder razonar por parte del paciente la magnitud de la cirugía a la que fue sometido y los cuidados que deberá tener son los causantes de las luxaciones. También se reportan una mayor predominancia de luxaciones en mujeres de hasta dos veces más que en varones (2,5,8), inclusive el peso y la edad (1,9) porque a mayor aumento de volumen, las probabilidades de que se forme una palanca luxante es también mayor; de igual forma a mayor edad ya hay más descuido por parte del paciente. Como se podrá ver, es necesario seleccionar muy bien al paciente que es candidato a una ATC, especialmente si es una cirugía electiva (9). b. Por otro lado están los factores de riesgo de luxación protésica propios de la cirugía o el evento quirúrgico: 115 “Temas selectos de actualización en la Ortopedia Latinoamericana” El abordaje quirúrgico, siempre controversial, teóricamente aumenta la posibilidad de luxación por el compromiso de las estructuras musculares posteriores que dejarían inestable la articulación. Woo y Morrey (1) en un estudio muy serio mostraron una incidencia de casi el doble de luxaciones por vía posterior que un abordaje anterolateral. Un meta-anális publicado en el 2002 (10) donde se revisó 13. 203 ATC, mostró un 3.23% de luxaciones por vía posterior; 2.18% por vía antero-lateral; 1.27% después de un abordaje transtrocantérico y un escaso 0.55% en un abordaje lateral directo. Como se podrá apreciar, parece que el abordaje posterior sigue siendo desfavorecido al contrario que el lateral directo que no llega ni al 1%. (11). Manejo de partes blandas, donde se incluyen a la cápsula articular, rotadores externos cortos y músculo glúteos, son claramente un factor importante para la estabilidad de la cadera post ATC, su reconstrucción y reparación o más bien la reposición de la tensión, debe realizarse minuciosamente como fue demostrado por Pellici (11) y confirmado posteriormente en un estudio de 1000 pacientes (12), de lo contrario, existe una falta de tensión que no garantiza el soporte de la cadera dentro de la articulación. Cabe mencionar también que el acortamiento del offset es otro factor causante de luxación (7) por la falta de tensión de partes blandas al acercar el eje del fémur al acetábulo. El uso de copas lateralizadas o lateralizantes, puede solucionar éste problema al desplazar el centro de rotación de la cabeza protésica más externamente reponiendo el offset. También las fracturas del trocánter mayor o su avulsión pueden perder la tensión muscular y ser factor luxante. Posición de los componentes, sin lugar a dudas la mala orientación es el causante más importante de luxación y por lo tanto el primer sospechoso, especialmente del 116 componente acetabular (fig.3) donde una excesiva anteversión o retroversión o una inclinación muy vertical, puede originar una luxación. Es necesario conocer la “zona segura” (13) de 40º de inclinación y los 15º de anteversión que propuso Lewinnek. De igual forma la mala orientación del vástago, especialmente una exagerada anteversión, puede ser causante de luxación. Una correcta planificación preoperatoria y sobre todo el uso correcto de los orientadores junto con la posición exacta de la mesa y la perfecta fijación del paciente en la mesa quirúrgica evitará ésta mal posición de los implantes. Figura 3. Notable verticalización de la copa acetabular que condicionará una luxación protésica Puntos de fulcro (impingement), que se origina cuando dos superficies en movimiento se ponen en contacto originado un torque como si fuese una palanca de apoyo y produce la luxación. Puede ser de dos tipos: Uno cuando el cuello del vástago choca contra el liner o la copa acetabular (fig.4) y otro cuando el cuello choca contra un osteofito, hueso heterotópico o a veces cemento escurrido del acetábulo. Por ésta razón, se deben buscar y eliminar éstos puntos de contacto. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT de luxaciones que los más experimentados. Es fundamental que el cirujano nobel, tome nota de todas las recomendaciones de una ATC, conozca los implantes que va a utilizar, lleve a cabo una buena planificación preoperatoria y se asesore con un colega de mayor experiencia hasta adquirir más conocimiento sobre ATC. Figura 4. Es importante revisar puntos de palanca o fulcro El tamaño de la cabeza protésica disminuye el rango de movimiento (ROM) de la cadera. Cuanto más cerca está el diámetro de la cabeza con el del cuello del vástago, el arco de movimiento es menor, siendo un factor causante de luxación. Por lo tanto, se deben evitar utilizar cabezas pequeñas (en la actualidad ya prácticamente no existen las cabezas de diámetro 22) y con cuellos anchos (fig.5). Figura 5. El diámetro de la cabeza debe ser siempre mucho mas grande que del cuello de manera que la amplitud de movimiento sea mayor antes de chocar con el acetábulo Experiencia del cirujano. Hedlundth (14) demostró en un estudio de más de 4.000 ATC primarias, que los cirujanos con menos de 30 procedimientos por año tienen el doble Falsa vía y fractura periprotésica Más común en cirujanos con poca experiencia (fig.6) y se debe básicamente al desconocimiento de la calidad ósea del paciente quién puede tener corticales muy delgadas y a veces con casi nula resistencia como ocurre con la osteopenia ocasionada por la artritis reumática (AR). Figura 6. Una falsa vía lateral en un hueso con corticales delgadas y cemento óseo que quizás permitió libre deslizamiento del vástago A esto le podemos agregar una exposición insuficiente (muy común en nuestros tiempos en el afán de realizar abordajes más pequeños) que no permiten ver puntos de referencia con una consiguiente mala orientación entre el eje del canal femoral y el de la rima femoral o del implante al ser colocado definitivamente, amén de un rimado 117 “Temas selectos de actualización en la Ortopedia Latinoamericana” excesivo del canal femoral que adelgaza todavía más las corticales. Las fracturas suceden bajo las mismas circunstancias de la falsa vía y se añaden situaciones como utilizar implantes más grandes que las rimas o pretender realizar un mayor ajuste entre el implante y el endostio femoral. (15,16,17) En los casos cementados generalmente ocurre fractura por forzar la entrada del vástago en un cemento que fragua rápidamente. (fig.7). Hay casos excepcionales en los que se produce fractura distal (supracondílea) al realizar maniobras de reducción una vez terminada la colocación de los implantes o al pretender ofrecer mayor exposición con una rotación forzada de la pierna por parte del ayudante. Sea cual sea la situación, es preferible tener una buena exposición del campo operatorio que permita una visualización total, manejo gentil de la extremidad e inclusive uso profiláctico de un cerclaje con alambre. Lesión de vasos y nervios Aunque no es muy común pero puede suceder desde el posicionamiento del 118 paciente, donde se pueden comprimir vasos y nervios ya sea con la misma mesa quirúrgica o con los sistemas de sujeción; durante el acto quirúrgico por uso de los retractores, las maniobras para la luxación o reducción de la cadera o medios de sostén de la copa como el cemento y los tornillos. Pueden llegar a ser problemas muy serios y de gran magnitud (18). Lesión vascular, generalmente las más comprometidas son la arterias y vena Iliaca Externas, de las cuales la arteria es la más comprometida. Ambas discurren a lo largo del cuadrante anterior y superior del acetábulo, de modo que un retractor mal posicionado en la columna anterior del acetábulo puede lesionar éstos elementos. De la misma manera un rimado excesivo de la tabla interna puede lesionar la vena Iliaca Externa como la arteria al igual que la extrusión de cemento óseo ya sea por calor o compresión directa (18,19). La perforación para los tornillos de fijación o la colocación de los mismos, también puede lesionar la vena Iliaca Externa produciendo un hematoma retroperitoneal que no se observa en el campo quirúrgico. Los vasos femorales son los vasos extra pélvicos más comunes de lesionar y se pueden presentar por uso incorrecto de retractores especialmente en los abordajes antero laterales cuando se los coloca en el borde anterior e inferior del acetábulo (19). Los vasos obturadores discurren detrás de la superficie cuadrilátera y pueden ser lesionados por un retractor que se coloque debajo del ligamento transverso acetabular y se introduzca en el agujero obturador. Los vasos Glúteos, especialmente la superior se pueden lesionar por uso de retractores o pines fijados posteriormente pero con dirección a la escotadura y a veces los tornillos de sostén posteriores del acetábulo. Lesión neurológica, no es rara y su incidencia es de hasta el 3% (18) la causa Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT de su lesión es por compresión, tracción o isquemia. A veces es uno solo el factor causante pero otras veces es la suma de dos o los tres factores. La parálisis del nervio Ciático es la más común. Aunque la gran mayoría se recuperan favorablemente, hay un pequeño grupo que tarda mucho o no logra recuperarse quedando con secuelas y disfunciones. Las fibras del nervio Peroneo Común están más externamente (superficialmente) situadas en el cordón ciático por lo que son más susceptibles de ser dañadas. Se presentan por uso de retractores, tracción, rotación forzadas. Es mucho más común en cirugías de revisión. Se ha demostrado que el 50% de los casos se deben a alargamiento de la extremidad y a veces con lateralización agregada. 22% por lesión directa; 20% por sangrado compresivo (hematoma) y 10% por luxación post quirúrgica (18,19). La lesión del nervio femoral es muy rara y parece que la principal causa de su lesión es un retractor colocado anteriormente y a veces por tornillos en hemi acetábulo anterior (19). La mejor forma de evitar éstas lesiones es conocer muy bien la anatomía de la región, buscar las zonas seguras para el anclaje de los tornillos y planificar para evitar elongaciones innecesarias de la extremidad. Puede ser de utilidad el uso de Potenciales evocados para detectar lesiones neurológicas en forma temprana. Resumen Ninguna cirugía está exenta de complicaciones. La ATC no es una excepción, pero una causa general importante es el exceso de confianza por parte del cirujano que cada día tiene más acceso a publicaciones, revistas, congresos, cursos, etc. que aparentemente proporcionan una “facilidad técnica” y si a esto le agregamos la falta de familiaridad ya sea anatómica, del instrumental, de la biomecánica de la cadera, de los propios implantes, etc. se obtienen todos los elementos necesarios para una complicación. A veces es desconocimiento pleno de la magnitud de una ATC. Otras complicaciones son las infecciones periprotésicas y las enfermedades tromboembólicas, especialmente la embolia venosa y tromboembolia pulmonar que puede llegar a ser fatal, que no se mencionaron en el presente capítulo por considerarse de aparición menos inmediata y que requieren de estudio aparte. La mejor forma de evitar todo tipo de complicación, es la prevención que se obtendrá mediante una buena planificación preoperatoria donde básicamente se anticipan las posibles eventualidades que se presentarán y buscar la forma de corregirlas realizando una adecuada selección tanto del implante como del propio paciente, pero sin lugar a dudas, la actitud del cirujano es fundamental. Es un ser humano que puede cometer errores y tener ciertas limitaciones y debe saber reconocerlos para estudiarlos, meditarlos y luego corregirlos. BIBLIOGRAFÍA 1. Woo RY, Morrey BF: Dislocation after total hip arthroplasty. J Bone Joint Surg Am 1982; 64:12951306. 2. Improving America’s Hospitals The Joint Commission’s Annual Report on Quality and Safety - 2008 3. Edeen J, et al: Clinical significance of leg-length inequality after THA Am J Orthop 1995:24 4. Parvizi J, Morrey BF: Bipolar hip arthroplasty as a salvatage treatment for instability of the hip. J Bone Joint Surg Am 2000; 82: 1132-1139 119 “Temas selectos de actualización en la Ortopedia Latinoamericana” 5. Beaulé PE, Schmalzried TP, Udomkiat P, Amstutz HC: Jumbo femoral head for the treatment of recurrent dislocation following total hip replacement. J Bone Joint Surg Am 2002; 84: 256-263. 6. Soong M, Rubash HE, Macauly W: Dislocation after total hip Arthroplasty JAAOS 2004; Vol 12; 5: 314-321 7. Fackler CED, Poss R: Dislocation in total hip arthroplasties. Clin Orthop 1980; 151: 169-178. 8. Sanchez-Sotelo J, Berry DJ: Epidemiology of instability after total hip replacement. Orthop Clin North Am 2001; 32: 543-552. 9. Newington DP, Bannister GC, Fordyce M; Primary total hip replacement in patients over 80 years of age. J Bone Joint Surg Br 1990; 72: 450-452. 10.Masonis JL, Bourne RB: Surgical approach, Abductor function and total hip Arthroplasty dislocation. Clin Othop 2002; 405: 46-53. 11.Pellici PM, Bostrom M, Poss R: Posterior approach to total hip replacement using enhanced posterior soft tissue repair. Clin Ortho 1998; 355: 224-228. 12.Goldstein WM, Gleason TF, Kopplin M, Branson JJ: Prevalence of dislocation after total hip arthroplasty through a posterolateral approach with partial capsulotomy and capsulorrhaphy. J Bone Joint Surg Am 2001; 86: 2-7. 13.Lewinnek GE, Lewis JL, Tarr R, Compere CL, Zimmerman JR: Dislocations after total hip replacement arthroplasties. J Bone Joint Surg Am 1978; 60: 217-220. 14.Hedlundh U, Anhfelt L, Hybbinette CH, Weckström J, Fredin H: Surgical experience Related to dislocations after total hip arthroplasty. J Bone Joint Surg Br 1996; 78: 206-209. 15.Kavanagh Bf: Femoral Fractures Associated with total Hip Arthroplasty. Orthop Clin North Am 1992; 23: 249-257 16.Mont MA, Maar DC, Krackow KA, et al. Hoop-stress fractures of the proximal femur during Hip Arthroplasty. J Bone Joint Surg 1992; 74B: 257-260 17.Sharkey PF, Hozack Wj, Booth RE Jr. Intraoperative femoral fractures in cementless total hip arthroplasty. Orthop Rev 1992; 21: 337-342 18.Wasieleswski RC, Crossett LS, Rubash HE. Neural and vascular injury in total hip arthroplasty. Orthop Clin North Am 1992; 23: 219-235. 19.Schmelzried TP, Amstutz HC, Dorey FJ. Nerve palsy associated with total hip replacement: risk factors and prognosis. J Bone Joint Surg 1991; 73A: 1074-1080 120 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Biomateriales. Cómo Decidir la Tribología en una Artroplastia Total de Cadera. Felipe Gómez García, M. D. * Académico Titular de la Academia Mexicana de Cirugía, Director Médico de la Clínica de Cadera Hospital Ángeles Mocel, Cd. de México, Editor en Jefe de Acta Ortopédica Mexicana. INTRODUCCIÓN. La meta principal de un implante es lograr la máxima longevidad posible y la estabilidad es el punto cardinal para lograrlo. La estabilidad debe definirse como la serie de eventos que deben ocurrir entre el implante y en hueso para lograr una respuesta biológica equilibrada que permita la presencia de un cuerpo extraño sujeto a grandes esfuerzos generador de potenciales productos no deseables y permanecer largos periodos in situ sin que cause un detrimento significativo de las propiedades biológicas y mecánicas del receptor (1). Hay dos tipos de estabilidad claramente definidos por el tiempo y por los eventos que tienen que acontecer para obtenerla. La primera es la estabilidad primaria o mecánica que se logra en el momento mismo de la operación y se alcanza por el diseño del implante, los materiales con que se fabrica, los métodos alternos de fijación y la técnica quirúrgica. La estabilidad secundaria o biológica se logra con el paso del tiempo a través de adecuados fenómenos biológicos de remodelamiento óseo, preservación de la salud general y ósea y de ciertas contingencias que pueden estar relacionadas con los materiales implantados; la estabilidad biológica es la responsable del buen funcionamiento a largo plazo de la prótesis y es en este tipo de estabilidad donde ejerce mayor influencia la tribología (ciencia que estudia la fricción, el desgaste y la lubricación que tienen lugar durante el contacto entre superficies sólidas en movimiento) entre los pares endoprotésicos. La modificación a los diseños protésicos y a los materiales con los cuales se fabrican, han sido las estrategias preferida por los autores para obtener mejores resultados en estabilidad. Con este motivo han aparecido en el mercado una multitud de formas y tamaños de prótesis hechas con diferentes materiales; 121 “Temas selectos de actualización en la Ortopedia Latinoamericana” cada una de ellas con una filosofía propia y justificaciones racionales para su utilización. Esta efervescencia en investigación, ideas, conceptos y teorías ha traído como consecuencia, entre otras cosas, un cierto grado de confusión entre los médicos ortopedistas acerca de cuáles son los implantes que tentativamente ofrecen mejores ventajas para sus pacientes. La tribología forma parte activa en lo anterior por lo que es conveniente que los cirujanos estemos bien informados de los avances y retrocesos en este campo. OBJETIVO. Los avances en el diseño de componentes de artroplastias totales de cadera se han traducido en la producción de implantes con resultados clínicos más confiables, en especial en lo que respecta a la fijación estable de los mismos. Sin embargo, un desafío no completamente resuelto ha sido el rodamiento de las superficies articulares ya que deben resistir demandas de un cada vez mayor número de pacientes jóvenes y adultos mayores con expectativas de vida prolongadas y notable actividad. 122 Las alternativas actuales en cuanto a pares de fricción incluyen: Polietilenos de ultra alta densidad altamente entrelazados que se combinan con cerámica o metal; cerámica en cerámica; metal sobre metal, y otras combinaciones entre las que destacan los metales ceramizados. En este capítulo se revisará el estado actual de la tribología de cadera discutiendo cuales son las estrategias que se han seguido a lo largo del tiempo, sus resultados, problemas y el papel que desempeña el cirujano en la prescripción del par tribológico que mejor se adapte a las necesidades de cada paciente. POLIETILENO. Históricamente los plásticos han acompañado al desarrollo de la artroplastia de cadera y ha sufrido modificaciones en el paso del tiempo. La figura 1 lo resume. Se ha dicho que los productos de desecho del polietileno son la principal causa de osteolisis y masas pseudotumorales (a las que anteriormente dábamos el nombre genérico de Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT “granulomas” o “hamartomas”). Para minimizar lo anterior se han buscado diversas soluciones desarrollando “nuevos polietilenos”. Estas pretendidas soluciones arrancan del hecho que el principal factor responsable de la falla del polietileno es el deterioro de sus propiedades mecánicas desencadenadas por una degradación oxidativa (2), que ocasiona la disminución de la resistencia al desgaste abrasivo y conduce a la formación masiva de desechos. En respuesta a ello, se produce de manera reactiva una osteolisis con la consecuente falla del implante (3) (Figura 2). Ahora sabemos que una de las claves del problema es la oxidación del polietileno que se relaciona directamente con 2 factores principales: 1) El tipo o métodos de esterilización y 2) el grado de entrecruzamiento de enlaces entre las cadenas poliméricas. Figura 2.- En esta imagen se muestra un espécimen retirado por falla catastrófica del polietileno que ocasionó desgaste del titanio de la plataforma Metálica. 1. Los diferentes tipos o métodos de esterilización.- Sabemos que los componentes de polietileno esterilizados con óxido de etileno (O Et) no se oxidan en tanto no salgan de su paquete de envoltura (siempre y cuando hayan sido envasados al vacío), mientras que los esterilizados mediante radiaciones de alta energía en aire (radiación γ o con un haz de electrones a dosis de entre 25 – 450 kGy) muestran altos niveles de oxidación (4). La oxidación después del tratamiento con alta energía acontece de inmediato y da como resultado la escisión de las cadenas del polietileno, que hace que se disminuya la masa molecular y por lo tanto sus propiedades mecánicas de resistencia (5). Ya hemos dicho que los componentes de polietileno esterilizados con O Et no se oxidan, sin embargo ocurre una degradación oxidativa durante su permanencia in vivo (6-9). 2. El Grado de entrecruzamiento de enlaces entre las cadenas poliméricas.- Los Polietilenos que poseen un alto entrecruzamiento de enlaces reflejan una alta resistencia al desgaste en comparación con los convencionales (bajo o medio entrecruzamiento) (10, 11); sin embargo, para evitar la oxidación, el polietileno altamente cruzado requiere de un tratamiento térmico post-irradiación, que desafortunadamente reduce sus propiedades mecánicas 12. Recientemente, se ha introducido el uso de los antioxidantes como la vitamina E (alfatocoferol) para evitar la oxidación de los polietilenos con alto y medio entrecruzamiento (13). Es un hecho que el mayor entrecruzamiento de enlaces mejora la resistencia al desgaste, sin embrago debemos conocer que existen varias formas tecnológicas de fabricación para lograrlo. (Figura 3) y que hay en el mercado polietilenos con diversos tipos de métodos de esterilización con diferente entrecruzamiento de enlaces (7). La tabla 1 enlista las particularidades de varias marcas comerciales y las agrupa por sus características más relevantes. Debe recalcarse que NO TODOS LOS POLIETILENOS ALTAMENTE CRUZADOS SON IGUALES por lo que el cirujano debe conocer perfectamente el tipo de material que utiliza o analiza. 123 “Temas selectos de actualización en la Ortopedia Latinoamericana” Tabla 1. 124 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 125 “Temas selectos de actualización en la Ortopedia Latinoamericana” Figura 3. En esta figura se muestran diversas tecnologías para la fabricación de polietileno según la cantidad de radiación empleada para entrecruzar enlaces. Solo se muestran algunos polietilenos fabricados por extrusión forzada con resina GUR 1050. ( Adaptado de A.S., Bauer T.W., Ries. New polys for old: Contribution or caveat? J Bone Joint Surg Am 2001;83(suppl 2):27-31.) Es conveniente recordar que el uso clínico de los polietilenos con alto entrecruzamiento se inició en 1998 y por tanto la experiencia clínica es a mediano plazo es limitada. Los estudios disponibles hasta el momento son en su mayoría comparaciones (11, 14, 15), pruebas de materiales in vivo y en laboratorio (8-16) y seguimientos cortos (17-19). Debe comentarse que han empezado a aparecer artículos en los cuales se observa una disociación entre los resultados de los estudios en laboratorio y los resultados clínicos al analizar insertos de polietileno altamente entrecruzado que fueron retirados en revisiones por causas distintas a la fatiga de material (11, 18-20). En ellos se ha observado perdida del maquinado así como la presencia de defectos que sugieren patrones de desgaste mucho 126 mayores a los reportados en estudios con simuladores de cadera. Polietilenos medicados con vitamina E La incorporación más reciente para prevenir el riesgo de oxidación en los polietilenos altamente cruzados en especial por el problema que representan los radicales libres residuales después de irradiación (13, 20-21), es la adicción de vitamina E (alfa tocoferol) a la resina base del polietileno altamente cruzado. Esta alternativa se encuentra aún en fase de investigación; sin embargo los resultados preliminares en laboratorio y en vivo son altamente esperanzadores. Para incorporar este elemento se utilizan dosis de entre 0.1 - 0.3% del peso que se mezcla con la resina GUR 1050 que luego es irradiada. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Cuando este material se compara con el polietileno virgen que no contiene vitamina E, se encuentran tasas de oxidación entre 50 y 100 veces menores entre el UHMWPE medicado y el no tratado, mientras que el porcentaje de cristalinidad no varía entre uno y otro. Según Oral (21) la mejoría en la resistencia a la fatiga ha sido hasta de un 58%, lo que eliminaría la necesidad de tratamientos térmicos para eliminar radicales libres. Sin embargo no existen aún suficientes estudios prospectivos, comparativos, aleatorizados con tamaños de muestra suficientes y con seguimientos mayores a 10 años, por lo que debemos estar atentos a los resultados de estos estudios. Es conveniente tener cautela a la hora de abrazar estas innovaciones. Afortunadamente es cuestión de tiempo el que se culmine el seguimiento de numerosos estudios que están en curso tendientes a cumplir el propósito de evaluar realmente el lugar de debe ocupar esta nueva herramienta terapéutica. METAL-METAL. En los últimos años ha habido un renacimiento de la tribología metal-metal. Los investigadores en el comportamiento de los metales y sus efectos en seres vivos nos dicen que todos los metales que contactan con sistemas biológicos sufren de un proceso electroquímico llamado corrosión, que tiene como efecto generar iones metálicos que al interrelacionarse con proteínas endógenas pueden activar el sistema inmune y generar respuestas indeseables. Hoy sabemos que la tribología metal-metal genera iones y partículas. Esto está directamente relacionado con el tipo de aleación metálica, el diseño de los componentes y con el posicionamiento de los implantes. El Dr. Hans Georg Willert (22) publicó en 2005 un artículo en el que correlaciona las reacciones de hipersensibilidad con la liberación de iones en implantes me- tal-metal que ocasionaron cambios indeseables en los tejidos periprotéticos. Este autor acuño el término de “ALVAL”, que por sus siglas en inglés significa una vasculitis aséptica ligada a linfocitos asociada a otras lesiones. Las lesiones son; abundancia de fibrina, acúmulos de células macrofágicas y de eosinófilos con focos de necrosis. Actualmente entendemos el “ALVAL” como lesiones representadas por una histología dominada por linfocitos B y células plasmáticas; que sugieren una respuesta inmune, con un patrón histológico parecido, pero no igual al de una reacción de hipersensibilidad tardía grado IV. Desde la publicación del artículo de Willert (22), han aparecido una multitud de reportes que asocian la tribología metal-metal con diversos tipos de reacciones adversas, en especial la hipersensibilidad mediada por células y la formación de pseudotumores sólidos o con contenido líquido, algunos de ellos con necrosis granulomatosa. También se ha intentado explicar la patogénesis de las reacciones alérgicas asociándola a la presencia de ciertas inmunoglobulinas como la HLA DR+ CD8+ e interleucinas como la IL-8 y la IP-10, entre otras substancias. Llama la atención que no solo han aparecido alteraciones locales sino también efectos sistémicos caracterizados por linfopenia de células T. Por otra parte las características metalúrgicas (ej.: bajo contenido de carbono) y las de diseño (ej.: baja tolerancia de los implantes), al igual que el mal posicionamiento de los implantes (ej.: pinzamiento de bordes) han jugado un papel importante en el incremento de iones y partículas con la consecuente aparición de fenómenos alérgicos y otras reacciones adversas. Todas estas alteraciones se manifiestan por dolor disfuncional o aflojamiento protético que obligan a un recambio. Están bajo observación los posibles efectos teratogénicos y de carcinogénesis a largo plazo. 127 “Temas selectos de actualización en la Ortopedia Latinoamericana” Una situación que en cierta forma confunde es el hecho de que aunque hay suficientes evidencias de la relación entre iones y partículas metálicas con reacciones adversas, no todas las lesiones derivadas de ello presentan las mismas características clínico-patológicas ni el mismo patrón histológico. La confusión no solo se limita a las descripciones histológicas de las lesiones, sino que también a su nomenclatura, ya que las reacciones indeseables se describen con distintos nombres: Alergia, hipersensibilidad, pseudotumores, metalosis, “ALVAL” y generalizaciones tales como “reacciones adversas a metales”. En un intento para poner orden se han presentado propuestas para clasificar y calificar los hallazgos histológicos. Esto se ha hecho mediante un descripción fraccionada de los hallazgos relacionados con la membrana sinovial, el tipo de infiltrado inflamatorio y como se organizan los tejidos (23). No obstante estos avances aún quedan preguntas por responder por patólogos, inmunólogos y cirujanos interesados en el estudio de este campo; ¿son diferentes los mecanismos inmunológicos?; ¿son distintas fases de un mismo proceso?; ¿Son reacciones individuales a la misma noxa? y ¿qué falta hacer para uniformar los criterios histológicos? En fin, esta parte de historia es importante; sin embargo, algo que nos interesa de sobremanera a nosotros los cirujanos comunes y corrientes es saber: ¿Cuál es la importancia clínica? Para contestar esta pregunta primero debemos saber cuál es la magnitud del problema. Sabemos que la incidencia de hipersensibilidad a metales en seres humanos en población general puede llegar hasta un 15 %; en trabajadores metalúrgicos a un 10 % y en pacientes con implantes metálicos la nada despreciable cifra de 5.4% (24). 128 En cuanto a la incidencia de “ALVAL” es difícil saberlo; en parte por las dificultades de clasificación de tejidos ya anteriormente mencionada y por la escasez de patólogos bien calificados para identificarla, sin embargo en los peores reportes la incidencia no sobrepasa del 3 %. Con relación a la incidencia de pseudotumores tenemos el mismo problema. En una serie multicéntrica Canadiense que incluye 3232 caderas se pudo identificar solo un pseudotumor (25) y en la serie inglesa del Nuffiel Orthopaedic Centre de 1419 caderas se detectaron 22 de estas lesiones (26). Muy recientemente se ha publicado un estudio con pacientes “asintomáticos”, donde se evaluaron un total of 201 caderas con una media de seguimiento de 61 meses usando para la detección ultrasonido y resonancia magnética. En estos pacientes “asintomáticos” se encontró una frecuencia de 7 pseudotumores [4%] (27). Este estudio sugiere que la presencia de pseudotumores en pacientes aparentemente “normales” pude aumentar la cifra de incidencia general de este problema. Con las evidencias anteriores podemos decir hasta hoy, que son pocos los pacientes con prótesis Meta-Metal que desarrollan reacciones adversas que obliguen a efectuar un recambio. Es importante mencionar que NO TODOS LOS DISEÑOS METAL-METAL SON IGUALES. El Registro australiano de Artroplastias documenta que hay modelos con altas tasas de falla (28). Menciona a las prótesis de re-superficialización ASR®, Durom® y Cormet® como las de mayor incidencia de falla. El año pasado se agregó a esta lista a la prótesis Bionik®. La Cormet® ya fue retirada del mercado Australiano. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT En cuanto al diagnóstico no invasivo, los estudios de mayor utilidad son la radiología simple, el ultrasonido, la tomografía axial y la resonancia magnética. Debe mencionarse que las pruebas clásicas utilizadas para detectar hipersensibilidad o alergia por otras especialidades médicas (Pruebas sensibilidad de migración y parches dérmicos) no tienen la suficiente sensibilidad ni especificidad, por lo que hay un consenso entre ortopedistas que no deben utilizarse. Los estudios de laboratorio considerados como estándar de oro para el diagnóstico de hipersensibilidad inducida por metales son los ensayos de proliferación linfocítica, análisis de algunas citoquinas usando ELISA y de inhibición de migración linfocítica (29). Otras citoquinas como la IL-8 y la IP 10 (30) aún están bajo estudio pero podrían ser de futura utilidad. En fin, estamos aún lejos de tener una prueba única confiable para el diagnóstico de hipersensibilidad a metales en paciente con implantes ortopédicos, por lo que tendremos que utilizar diversos recursos para llegar al diagnóstico sobre todo en etapas tempranas. Mientras tanto, debemos estar muy atentos con pacientes que se consideren como de alto riesgo como son: portadores de componentes pequeños, género femenino de talla baja, prótesis colocadas en terreno de alteraciones anatómicas significativas (Ej. displasia acetabular), con posicionamiento inadecuado de los implantes y con antecedentes alérgicos a metales (31, 32). La Agencia Regulatoria de Medicamentos y Cuidados para la Salud del Reino Unido (33) ha emitido una serie de recomendaciones para pacientes que se han sometido a una artroplastia con tribología Metal-Metal. Como medidas generales recomienda: a)Un seguimiento anual mínimo de 5 años; o más frecuentemente si hay síntomas. b)Deben medirse niveles de metales y hacer estudios imagenológicos con resonancia magnética y ultrasonido en pacientes con mal posicionamiento de implantes; cuando son portadores de prótesis de recubrimiento de tamaño pequeño; en los casos donde hay preocupaciones del paciente y el cirujano acerca del comportamiento del metal-metal y en modelos con elevadas tasas de falla. c)Si los niveles de iones metálicos son elevados, reforzar la vigilancia y en caso necesario hacer estudios imagenológicos especiales. d)Si estos estudios revelan reacciones en tejidos blandos periprotéticos debe considerase la cirugía de revisión. Como comentario final diremos que las reacciones adversas a materiales protéticos en implantes son poco frecuentes, pero debemos vigilarlas y estar alertas a la evolución de su perspectiva histórica y al desarrollo de los métodos de diagnóstico temprano para esta entidad que parece estar dominada por implantes con tribología de Metal-Metal. CERAMICA –CERÁMICA Los pares cerámica-cerámica se han empleado desde los años setentas y han tenido una evolución histórica muy interesante donde las mejoras tecnológicas en la mezcla y fabricación de sus compuestos químicos y procesos termodinámicos (ej.: el sinterizado); el diseño, (Ej. diferencias entre las curvaturas cóncavas y convexas) y la mejor comprensión del funcionamiento de los sistemas “cono morse” (forma de los conos), han formado parte fundamental de su buen funcionamiento clínico (Figura 4). 129 “Temas selectos de actualización en la Ortopedia Latinoamericana” Figura 4.- En esta figura se esquematizan los rasgos históricos más importantes del desarrollo de las cerámicas de uso ortopédico de la marca Biolox® (CeramTec GmbH. Plochingen, Germany). Entre los pares de fricción actuales, la cerámica-cerámica posee el menor coeficiente de fricción de todas las tribologías existentes 34), ya que su pequeño tamaño de grano le permute tener una muy baja rugosidad en la superficie; su muy elevada dureza ofrece una mayor resistencia al rayado y su alta capacidad de hidrofílica le permite una excelente lubricación (35-37). Además de lo anterior, las superficies articulares de cerámica se asocian a bajos niveles de osteolisis; entre otras razones porque las cerámicas son bioinertes y porque las partículas de desecho que produce son de muy pequeño tamaño. Estas características hacen que en el ambiente articular se produzcan simples reacciones fibrosas en vez de inflamatorias como las observadas con el polietileno (37), es decir las cerámicas producen a una escasa respuesta biológica indeseable (34, 38). 130 Las mejoras antes mencionadas y otras características (tabla 2) han ocasionado que los resultados clínicos de las cerámicas sean cada vez mejores (36, 39). No obstante las ventajas antes mencionadas, las cerámicas actuales presentan 3 problemas que son: la fractura, el ruido al caminar y el despostillado sin ruptura. Fractura de cerámicas.- Aunque las cerámicas tienen una mucha mayor resistencia a las fuerzas compresivas que a la tensión (37) y poseen una muy baja ductilidad cuando se exponen a cargas o impactos tensiónales (39), el riesgo de fractura esta potencialmente presente en esta tribología. En un estudio de centros europeos (40) con cerca de 30 años de experiencia en el uso de cerámica-cerámica se presentaron 13 fracturas de cerámica en 5500 componentes implantados. La mayoría se atribuyó a un traumatismo aislado y en Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT los casos donde las fracturas ocurrieron sin trauma, la falla se atribuyó a deficiencias en la estructura de la cerámica o en el diseño del componente. Este estudio que incluye desde la primera a la tercera generación de cerámicas ilustra que a pesar de las mejoras tanto a los materiales como a los diseños, no se eliminó por completo el riesgo de fractura. Hoy por hoy se considera que el mayor riesgo de ruptura reside en el mal posicionamiento de los implantes. la fabricación de formas complejas ni para componentes muy delgados, y b) las hechas a base de Zirconia (Dióxido de zirconio [ZiO2]) que es más dura pero menos estable (Fuerte variabilidad a la degradación in vivo), sus resultados clínicos no han sido satisfactorios (presenta fallas tempranas en cabezas femorales [Prozyr ®]). Estos resultados han abierto una polémica sobre el futuro de Zirconia como biomaterial único en la fabricación de implantes (41). En la historia de la cerámicas se distinguen 2 tipos principales de este material: a) las que tienen como base Alúmina (Hidróxido de aluminio [Al2O3]) que ofrece alta estabilidad físico química y excelentes características tribológicas, sin embargo, presenta pobre dureza por lo que no se utiliza para Recientemente se ha obtenido un nuevo material compuesto por una matriz alúmina con inclusiones de Zirconia (Al2O3 + ZiO2) llamado Biolox Delta ® (CeramTec AG, Plochingen, Alemania), a fin de mezclar y mejorar las características positivas de ambos materiales (42). 131 “Temas selectos de actualización en la Ortopedia Latinoamericana” La composición química volumétrica de la cerámica compuesta Biolox delta® se muestra en la figura 6. Aunque son un verdadero alarde de tecnología debemos mencionar que esta combinación se encuentra en discusión por el problema que representa la degradación de los materiales, en especial de La Zirconia (envejecimiento). Figura 5. Microestructura de Cerámica Biolox Delta®. 1) Matriz de Alumina, 2) Partículas de Zirconia 3) Plaquetas de Oxido de Cromo. Recientemente Hamilton y Cols. (43) publicaron un estudio donde comparan articulaciones de cerámica delta sobre cerámica delta, contra cerámica delta sobre polietileno de ultra alta densidad con elevado entrecruzamiento de enlaces. Aunque el seguimiento fue corto (2 años mínimo con promedio de 31.2 meses y rango de 21 a 49 meses), 4 de los 177 pacientes a los que aplicó solo cerámicas, fueron revisados 4. En 2 de detectaron eventos relacionados con el inserto acetabular, (en uno se presentó un despostillamiento que ameritó revisión y en otro se detectaron fragmentos de cerámica Figura 6.- En esta figura se muestra la composición química volumétrica de la cerámica Biolox Delta® Observe que el 82 % está compuesta de Alúmina y solo el 17 % de Zirconia. 132 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT durante el seguimiento radiográfico pero no ha requerido revisión). No hubo ruidos en ningún caso. Debe mencionarse que se revisaron 3 pacientes con cerámica delta vs polietileno por causas ajenas a la cerámica. Ruidos articulares.- En un estudio hecho in vivo hecho por Glaser y cols. (44) en pacientes portadores de prótesis totales de cadera con diferentes tribologías, se pudo demostrar que TODOS los pares articulares son capaces de producir ruidos (Tabla 3). En cuanto a sus características, los ruidos pueden ser percibidos de diversas maneras y describirse como: “chasquidos”, “golpeteos” (sonoros o sordos), “aldabazos”, “rasquidos”, “rechinidos”, “crujidos”, “crepitaciones” y “chirridos” y pueden presentarse durante todo el ciclo de la marcha, en alguna fase de la misma o durante ciertas actividades específicas. Los ruidos pueden o no ser audibles y son comunes después de un reemplazo articular total convencional con una incidencia global que alcanza hasta el 96% (44); Sin embargo, no todos pueden oírse o “sentirse” por el paciente, pero en las superficies de “duro contra duro” puede llegar a ser audibles incluso a distancia (44-48) y en los últimos años se ha reconocido como una complicación de este tipo de pares articulares (44-55). En cuanto a su incidencia, se desconoce cuál es la real en ruidos de alta frecuencia (audibles) toda vez que diversos autores reportan una presencia clínica muy variada que va de menos del 1% hasta el 20% (46,47, 53, 55). La etiología de los ruidos es multifactorial y se encuentran implicados factores relacionados con el paciente (complexión, peso, estilos de vida, etc.), con la prótesis (tipo de 133 “Temas selectos de actualización en la Ortopedia Latinoamericana” implante, defectos en la fabricación, mala posición y combinaciones de diferentes diseños), con el cirujano (mal posicionamiento) y con la superficie de rodamiento, (micro separación, deficiencias en la lubricación, pinzamientos y terceros cuerpos intrarticulares) (45, 47, 49, 51, 55). monolíticas de cromo-cobalto, ya que comparativamente se reduce el desgaste del polietileno (57, 58) [Grafica 1] y pueden atender las necesidades de los pacientes que presentan hipersensibilidad a los metales (59, 60). Despostillamientos. Aunque es un accidente reportado en la literatura, es un evento sumamente raro que está relacionado principalmente con 2 factores. El primero es una deficiente manipulación transquirúrgica y el segundo a la colisión entre el cuello femoral y el borde del inserto de cerámica. Esto último puede evitarse colocando cabezas con el mayor diámetro posible y prescribiendo diseños que tengan protección contra colisiones entre los componentes. METALES CERAMIZADOS (OXINIUM®). La exigencia actual de mejores rendimientos para las artroplastias totales de cadera y rodilla, están impulsando el desarrollo de materiales tribológicos alternativos. En julio de 1995 Hunter (50) publicó estudios que introducen al oxido de zirconio (Oxinium® Smith & Nephew, Inc., Memphis,TN ) como parte articular de los implantes ortopédicos. Este material es una aleación metálica de Zirconio con una superficie de cerámica de Zirconia (Zirconio y Zirconia no son lo mismo; Zirconio es un metal y Zirconia una cerámica) que ofrece una sobresaliente resistencia al desgaste sin fragilidad, por lo que este material combina lo mejor del metal y la cerámica y no crea el riesgo de la fractura asociada a los componentes cerámicos monolíticos. La oxidación del zirconio a una alta temperatura en presencia de aire, transforma la superficie de la aleación metálica Zr-2.5Nb en una cerámica estable producto de una aleación entre zirconio, niobio y oxígeno (Zirconia) y se ha constituido en una esperanzadora alternativa para las aleaciones 134 Grafica 1. Esta grafica muestra el desgaste comparativo entre Oxinium y aleaciones de Cobalto-Cromo. Tomado de Long y cols.: Trans. Soc. Biomaterials, 21, 1998, p. 528. Aunque en el laboratorio el Oxinium® sufre 4900 veces menos desgaste volumétrico y 640 veces menos huellas de arañazos profundos cuando se le compara con las aleaciones de cromo cobalto tradicionales; el sustrato de Zirconio es relativamente suave (Hv= 285) en comparación con cabezas femorales de cromo cobalto (HV= ~ 420,), lo que lo hace muy riesgoso cuando existe un tercer cuerpo o bien ocurre una dislocación donde las cabezas protésicas pueden dañarse al entrar en contacto involuntario con los metales de las copas acetabulares. Kop y cols. (61) 61 analizaron tres casos de retiros de cabezas femorales y demostraron los serios daños que se produjeron durante la luxación al realizar maniobras Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT cerradas de reducción. Esto también se lo han podido demostrar otros autores (62, 63). En casos de eventos de luxación con este nuevo material es recomendable que las maniobras de reducción se ejecuten con mucha precaución para evitar daños significativos de cabeza y por ello llevar a un desgaste acelerado de polietileno. En el caso de una reducción cerrada exitosa, se recomienda el seguimiento estrecho del paciente. La reducción abierta con inspección de cabeza femoral y el intercambio de la misma puede ser preferible si se encuentran dificultades durante las maniobras de reducción cerrada o ha ocurrido una luxación recurrente. También deben vigilarse los pacientes en los que existe el riesgo o se sospecha la presencia de terceros cuerpos intrarticulares ya sea metálicos o de cemento. RECOMENDACIONES PRÁCTICAS PARA PRESCRIPCIÓN Y MANEJO DE PARES ARTICULARES EN ARTROPLASTIA TOTAL DE CADERA. La necesidad de tener diversas opciones para tratar a los pacientes jóvenes o viejos pero activos, ha hecho que tengamos que utilizar diversos recursos. En esta última parte del capítulo se hace un ejercicio en el que se sugieren algunas recomendaciones prácticas para la prescripción y manejo de los diferentes pares articulares. En las tablas 4 y 5 se resumen algunos conceptos que pueden ser útiles para facilitar la decisión de prescripción. 135 “Temas selectos de actualización en la Ortopedia Latinoamericana” Polietilenos. 1. Recomendaciones generales. 136 • Evitar insertos esterilizados con óxido de etileno (Se oxidan). • Preferir inserto con elevados enlaces cruzados esterilizados con radiaciones gamma, tratados con irradiación con electrones. • Prefiera la combinación de cerámica polietileno sobre la de metal – polietileno. • En polietilenos convencionales es mejor emplear cabezas de 28 mm. • • En polietilenos de ultra alta densidad con enlaces altamente cruzados es admisible usar cabezas de diámetro mayor a 28 mm. Recordar que NO TODOS LOS POLIETILENOS ALTAMENTE CRUZADOS SON IGUALES. • Tener Bajo observación los nuevos polietilenos en espacial los medicados con vitamina E. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Metal - Metal. 1. Los pacientes considerados como de alto riesgo para desarrollar reacciones adversas son: • Los portadores de componentes pequeños. • Género femenino y talla baja. • Pacientes con riesgo o insuficiencia renal ya desarrollada. • Pacientes con alteraciones anatómicas significativas (Ej. displasia acetabular). • Pacientes con antecedentes alérgicos a metales. • Pacientes con posicionamiento inadecuado de los implantes. resonancia magnética y ultrasonido en pacientes con mal posicionamiento de implantes, cuando son portadores de prótesis de recubrimiento de tamaño pequeño, en los casos donde hay preocupaciones del paciente y el cirujano acerca del comportamiento del metal-metal y en modelos con elevadas tasas de falla. • Si los niveles de iones metálicos son elevados, (> 7 partes por millón) reforzar la vigilancia y en caso necesario hacer estudios imagenológicos especiales. • Si estos estudios revelan reacciones en tejidos blandos periprotéticos debe considerase la cirugía de revisión aunque el implante esté radiológicamente estable. 2. Recomendaciones generales para pacientes que se someterán a una artroplastia con tribología metal-metal. Cerámica - Cerámica. 1. ¿Qué podemos hacer para disminuir las fracturas? • Preferir copas con radios de 180° con alto contenido de carbono. • Usar el tamaño de componentes lo más grande posible • Evitar su uso en pacientes que requieran copas menores de 50 -52 mm.). • Evitar cuellos cortos en especial los de 28 mm. de diámetro. • Evaluar la conveniencia de usarla en mujeres en edad de embarazo. • Recordar que el cono 12/14 no es universal: ¡hay muchas variaciones! • La técnica quirúrgica deberá ser muy exacta especialmente en el adecuado posicionamiento de la copa. La anteversión o apertura lateral excesivas pueden producir pinzamiento de bordes y causas desgaste metálico aumentado. • Asegurarse que los componentes cerámicos y los metálicos sean compatibles. 3. En pacientes con implantes Metal Metal ya instalados. • Hacer un seguimiento anual mínimo de 5 años; o más frecuentemente si hay síntomas. • Deben medirse niveles de metales y hacer estudios imagenológicos con • Revisar que los conos no estén dañados y acoplar los componentes correctamente. • Impactar los componentes con la fuerza necesaria para que no haya expulsiones durante las actividades de marcha. • Asegurarse de la compatibilidad entre la cabeza y el cono femoral. Nunca se deben de mesclar componentes de diferentes empresas. 137 “Temas selectos de actualización en la Ortopedia Latinoamericana” • Revisar que los conos no estén dañados y que los componentes se acoplen correctamente. • Si el cono metálico está dañado utilize cabezas especiales de recambio (Biolox® Option). 2. ¿Qué hacer en caso de que tenga que hacerse una revisión por una fractura de un componente cerámico? • No use cabeza de metal ni polietileno para sustituir los componentes dañados. Use cerámica nuevamente (Es muy resisite a los terceros cuerpos residuales de cerámica). • Irrigue abundantemente el área para eliminar las partículas pequeñas. • Haga una sinevectomia completa. • Revise meticulosamente los componentes dañados. 3. ¿Qué hacer cuando ocurre un despostillamiento intra-operatorio de los insertos? • Son causadas por falta de familiaridad con la cerámica. • Las conexiones cónicas tienen que ponerse en su posición final antes de impactarse. • Vigile que no haya colisión entre los implantes en las movilizaciones extremas de la cadera. Oxinium ®. 1. Recomendaciones generales. • Haga maniobras de reducción muy cuidadosas para evitar daños a la delgada capa de cerámica. • No prescribirla en pacientes con alto riesgo de luxación. • Es una buena alternativa para pacientes jóvenes o viejos activos con antecedentes alergias a metales y puede cubrir las necesidades de los pacientes que presentan hipersensibilidad a los mismos. • Deben vigilarse con mayor frecuencia a los pacientes en los que existe el riesgo o se sospecha la presencia de terceros cuerpos intrarticulares ya sea metálicos o de cemento. 2. ¿Qué se recomienda en casos de eventos de luxación? • Las maniobras de reducción se deben ejecutar con mucha precaución para evitar daños significativos de cabeza. • En el caso de una reducción cerrada exitosa, es recomendable seguir al paciente lo más estrechamente posible. • Prefiera una reducción abierta si se encuentran dificultades durante las maniobras de reducción cerrada o ha ocurrido una luxación recurrente. La finalidad es efectuar una cuidadosa inspección de cabeza femoral y si está dañada debe intercambiarse. BIBLIOGRAFÍA 1. Gómez G. F. Estado Actual de la prótesis femoral de cadera: SLA una consecuencia lógica en Artroplastia total de cadera. Ed. McGraw Hill Interamericana. (ISBN 970-10-2548-2). Año 2000. pag. 2. 2. Kurtz SM, Muratoglu OK, Evans M y cols. (1999) Advances in the processing, sterilization, and crosslinking of ultra-high molecular weight polyethylene for total joint arthroplasty. Biomaterials 20(18):1659–1688. 138 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 3. Besong AA, Tipper JL, Ingham E et al (1998) Quantitative comparison of wear debris from UHMWPE that has and has not been sterilised by gamma irradiation. J Bone Joint Surg Br 80-B(2):340–344. 4. McKellop H, Shen FW, Lu B et al (2000) Effect of sterilization method and other modifications on the wear resistance of acetabular cups made of ultra-high molecular weight polyethylene. A hip-simulator study. J Bone Joint Surg Am 82-A(12):1708–1725. [PubMed] 5. Harris WH (2001) Wear and periprosthetic osteolysis: the problem. Clin Orthop 393:66–70. 6. Takeuchi T, Lathi VK, Khan AM et al (1995) Patellofemoral contact pressures exceed the compres- sive yield strength of UHMWPE in total knee arthroplasties. J Arthroplasty 10(3):363–368. [PubMed] 7. Costa L, Jacobson K, Bracco P et al (2002) Oxidation of orthopaedic UHMWPE. Biomaterials 23(7):1613–1624. [PubMed] 8. Brach del Prever EM, Crova M, Costa L et al (1996) Unacceptable biodegradation of polyethylene in vivo. Biomaterials 17:873–878. [PubMed] 9. Costa L, Luda MP, Trossarelli L et al (1998) Oxidation in orthopaedic UHMWPE sterilised by gamma-radiation and ethylene oxide. Biomaterials 19(7–9):659–668. [PubMed] 10.Costa L, Luda MP, Trossarelli L et al (1998) In vivo UHMWPE biodegradation of retrieved prosthesis. Biomaterials 19(15):1371–1385. [PubMed] 11.Besong AA, Hailey JL, Ingham E et al (1997) A study of the combined effects of shelf ageing following irradiation in air and counterface roughness on the wear of UHMWPE. Biomed Mater Eng 7(1):59–65. [PubMed] 12.Harris WH, Muratoglu OK. A review of current cross-linked polyethylenes used in total joint arthroplasty. Clin Orthop Relat Res. Jan 2005(430):46-52. 13.Jasty M, Rubash HE, Muratoglu O. Highly cross-linked polyethylene: the debate is over--in the affirmative. J Arthroplasty. Jun 2005;20(4 Suppl 2):55-58. 14.Collier JP, Currier BH, Kennedy FE, et al. Comparison of cross-linked polyethylene materials for orthopaedic applications. Clin Orthop Relat Res. Sep 2003(414):289-304. 15.Harris WH. First Generation Highly Crosslinked Polyethylenes: Current Status. Paper presented at: 35th Annual Course Advances in Arthroplasty: Harvard Medical School; September 28 2005, 2005; Cambridge, Massachusetts. 16.Shen FW, McKellop H. Surface-gradient cross-linked polyethylene acetabular cups: oxidation resistance and wear against smooth and rough femoral balls. Clin Orthop Relat Res. Jan 2005(430):80-88. 17.Rohrl S, Nivbrant B, Mingguo L, Hewitt B. In vivo wear and migration of highly cross-linked polyethylene cups a radiostereometry analysis study. J Arthroplasty. Jun 2005;20(4):409-413. 18.Ries MD. Highly cross-linked polyethylene: the debate is over--in opposition. J Arthroplasty. Jun 2005;20(4 Suppl 2):59-62. 19.Krushell RJ, Fingeroth RJ, Cushing MC. Early Femoral Head Penetration of a Highly Cross-Linked Polyethylene Liner vs a Conventional Polyethylene Liner A Case-Controlled Study. J Arthroplasty. Oct 2005;20(6 Suppl 3):73-76. 139 “Temas selectos de actualización en la Ortopedia Latinoamericana” 20.Estok DM, 2nd, Bragdon CR, Plank GR, Huang A, Muratoglu OK, Harris WH. The measurement of creep in ultrahigh molecular weight polyethylene: a comparison of conventional versus highly cross-linked polyethylene. J Arthroplasty. Feb 2005;20(2):239-243. 21.Dorr LD, Wan Z, Shahrdar C, Sirianni L, Boutary M, Yun A. Clinical performance of a Durasul highly cross-linked polyethylene acetabular liner for total hip arthroplasty at five years. J Bone Joint Surg Am. Aug 2005;87(8):1816-1821. 22.Bragdon CR, Kwon YM, Geller JA et al (2007) Minimum 6-year follow-up of highly cross-linked polyethylene in THA. Clin Orthop Relat Res 465:122–127. 23.Mc Calden R.W, MacDonald S.J., Rorabeck C.H, Bourne R.B., Chess D.G., Charron K.D. Wear Rate of Highly Cross-Linked Polyethylene in Total Hip Arthroplasty: A Randomized Controlled Trial. The Journal of Bone & Joint Surgery, 2009 91 (4):773-82. 24.Bradford L. , Baker D., Ries M., Pruitt, L. A., Hanssen A. Fatigue Crack Propagation Resistance of Highly Crosslinked Polyethylene. Clinical Orthopaedics & Related Research: December 2004 Volume 429 - Issue - pp 68-72 25.Engh Ch.-E. Jr, Stepniewski A.S., Stuart D. Ginn S.D., Beykirch S.E., Sychterz-Terefenko C. Robert H. Hopper R.H. Jr. Charles A. Enghm Ch A. MD: A Randomized Prospective Evaluation of Outcomes After Total Hip Arthroplasty Using Cross-linked Marathon and Non–cross-linked Enduron Polyethylene Liners. Journal of Arthrop. Volume 21, Issue 6, Supplement, September 2006, Pages 17-25 26.Shibata N, Tomita N. The anti-oxidative properties of alpha-tocopherol in gamma-irradiated UHMWPE with respect to fatigue and oxidation resistance. Biomaterials. Oct 2005;26(29):5755-5762. 27.Oral E, Greenbaum ES, Malhi AS, Harris WH, Muratoglu OK. Characterization of irradiated blends of alpha-tocopherol and UHMWPE. Biomaterials. Nov 2005;26(33):6657-6663. 28.Oral E, Wannomae KK, Hawkins N, Harris WH, Muratoglu OK. Alpha-tocopherol-doped irradiated UHMWPE for high fatigue resistance and low wear. Biomaterials. Nov 2004;25(24):5515-5522. 29.Willert H-G, Buchhorn G H, Fayyazi A, Flury R, Windler M, Köster G, and Lohmann G H. Metal-on-Metal Bearings and Hypersensitivity in Patients with Artificial Hip Joints: A Clinical and Histomorphological Study. Journal of Bone and Joint Surg (A). 2005;87:28-36 30.Campbell P A, Nelson S, Tas T, et. al. The Immunopathology of ALVAL. AAOS 2011 Anual Meeting Scientififc Exhibit Number: SE01 31.Hallab N, Merrit K, Jacobs J. Metal Sensitivity in Patients with Orthopaedic Implants. Journakl of Bone and Joint Surg. 2001; 83-A; 3: 428-436. 32.Beaulé PE, Kim PR, Powell J, Mackenzie J, et. al. A survey on the prevalence of pseudotumors with metal-on-metal hip resurfacing in Canadian academic centers. J Bone Joint Surg Am. 2011 May;93 Suppl 2:118-21 33.Glyn-Jones S, Pandit H, Kwon YM, Doll H, Gill HS, Murray DW. Risk factors for inflammatory pseudotumour formation following hip resurfacing. J Bone Joint Surg Br. 2009 Dec;91(12):1566-74. 34.Kwon Y-M, Ostlere S.J., McLardy-Smith P., et. al. “Asymptomatic” Pseudotumors After Metal-on-Metal Hip Resurfacing Arthroplasty: Prevalence and Metal Ion Study. The Journal of Arthroplasty. Volume 26, Issue 4 , Pages 511-518, June 2011 140 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 35.Hallab N, Mikecz K, Jacobs J. A triple assay technique for the evaluation of metal-induced, delay-type hypersensitivity responses in patients with or receiving total joint arthroplasty. J Biomed Mater Res. 2000 sep; 53:480-489. 36.Ball S T: Inflammatory Cytokines are Elevated in Patients with Adverse Reactions to Metal-on-Metal THAs. AAOS, 2011 Meeting Podium No: 065 37.Haddad F,S. y cols. Metal-on-Metal Bearings: The Evidence so Far. JBJS (Br) May 2011;93B:572-9. 38.Gonzalez M.H., Carr R., Walton S., Mihalko W.M. The evolution and modern use of Metal-on.Metal Bearings in total Hip Arthroplasty. Inst Courses Lec 2011;60:247-255. 39.Medicines and Healthcare products Regulatory Agency UK. MDA/2010/033 Issued: 22 April 2010, Ref: 40.Hannouche D. et. Al. Ceramics in total hip replacement [report]. Clin Orthop Relat Res 2005;62 41.Hamadouche MB, Daussange P. Bolander J, et.al. Alumina on alumina total hip arthroplasty: a minimum 18.5-years follow-up study [Article]. J. Bone Joint Surg Am 2002;84-A:69. 42.Bierbaum BE, et.al. Ceramic on ceramic bearings in total hip arthroplasty. Clin Orthop Relat Res 1999;83. 43.Skinner HB.Ceramic Bearing surfaces. [Review] [50 refs] Clin Orthopo Rel Res 1999:83 44.Barrack RL. Burak C. Skinner HB. Concerns about ceramics in THA [Review] [30 refs]. Cl Orthop. Rel Res 2004 45.Yoo JJ, et al. Alumina on alumina total hip arthroplasty: a five years minimum follow-up study [Article] J. Bone and Joint Surg Am 2005;87-A:530. 46.Rosneck J. Klika A, Barsoum W. A rare complication of ceramic-on-ceramic Bearings in total Hip Arthoplasty. J Arthoplasty 2008; 23:311. 47.Chevalier J. What future for zirconia as a biomaterial? Biomaterials Volume 27, (4), February 2006, Pages 535-543 48.Dalla Pria P. Evolution and new application of the alumina ceramics in joint replacement. European Journal of Orthopaedic Surgery & Traumatology. Volume 17, Number 3, 253-256. 49.Hamilton WG, McAuley JP, Dennis DA, Murphy JA, Blumenfeld TJ, Politi J. THA with Delta ceramic on ceramic: results of a multicenter investigational device exemption trial. Clin Orthop Relat Res. 2010 Feb;468(2):358-66. 50.Glaser D, Komistek RD, Cates HE, Mahfouz MR. Clicking and squeaking: in vivo correlation of sound and separation for different bearing surfaces. J Bone Joint Surg Am. 2008;90 (Suppl 4):112–120. 51.Jarrett CA, Ranawat A, Bruzzone M, Rodriguez J, Ranawat C. The squeaking hip: an underreported phenomenon of ceramic-on-ceramic total hip arthroplasty. J Arthroplasty. 2007;22:302. 52.Restrepo C, Parvizi J, Kurtz SM, Sharkey PF, Hozack WJ, Rothman RH. The noisy ceramic hip: is component malpositioning the cause? J Arthroplasty. 2008;23:643–649. 141 “Temas selectos de actualización en la Ortopedia Latinoamericana” 53.Walter WL, O’Toole GC, Walter WK, Ellis A, Zicat BA. Squeaking in ceramic-on-ceramic hips: the importance of acetabular component orientation. J Arthroplasty. 2007;22:496–503. 54.Chevillotte C, Trousdale RT, Chen Q, Guyen O, An KN. The 2009 Frank Stinchfield Award: “Hip squeaking”: a biomechanical study of ceramic-on-ceramic bearing surfaces. Clin Orthop Relat Res. 2009 June 19. 55.Keurentjes JC, Kuipers RM, Wever DJ, Schreurs BW. High incidence of squeaking in THAs with alumina ceramic-on-ceramic bearings. Clin Orthop Relat Res. 2008;466:1438–1443. 56.Murphy SB, Ecker TM, Tannast M. Incidence of squeaking after alumina ceramic-ceramic total hip arthroplasty. J Arthroplasty. 2008;23:327. 57.18. Restrepo C, Post Z, Kai B, Hozack WJ. The effect of stem design on the incidence of squeaking in ceramic on ceramic bearing total hip arthroplasty. J Bone Joint Surg Am.. 2009. 58.Walter WL, Waters TS, Gillies M, Donohoo S, Kurtz SM, Ranawat AS, Hozack WJ, Tuke MA. Squeaking hips. J Bone Joint Surg Am. 2008;90(Suppl 4):102–111. 59.Capello WN, D’Antonio JA, Manley MT. Alumina-on-alumina bearings in total hip arthroplasty: clinical results, osteolysis, breakage, and noise. J Arthroplasty. 2007;22:311–311. 60.Jarrett CA, Ranawat A, Bruzzone M, Rodriguez J, Ranawat C. The squeaking hip: an underreported phenomenon of ceramic-on-ceramic total hip arthroplasty. J Arthroplasty. 2007;22:302. 61.Keurentjes JC, Kuipers RM, Wever DJ, Schreurs BW. High incidence of squeaking in THAs with alumina ceramic-on-ceramic bearings. Clin Orthop Relat Res. 2008;466:1438–1443. 62.Hunter, G., Dickinson, J., Herb, B., et al. Creation of oxidized zirconium orthopaedic implants. J. ATSM Int., 2 (7). July 2005 63.M. Long, L. Riester, and G. Hunter, Nano-hardness measurements of oxidized Zr-2.5Nb and various orthopaedic materials, Trans. Soc. Biomaterials, 21, 1998, p. 528 64.Good, V., Ries, M., Barrack, Rl, et al. (2003). Reduced wear with oxidized zirconium femoral heads. J. Bone Joint Surg., 85-A (suppl 4) 105-110. 65.Nasser, S., Mott, M., Wooley, P. (2006). A prospective comparison of ceramic and oxinium TKA components in metal hypersensitivity patients. Proceedings of the Annual Meeting of the American Academy of orthopaedic Surgeons, (pp. 194) San Diego, CA. 66.Lhotka, C., Szekerea, T., Steffan, T., Zhubar, K., and Zweymuller, K. 2003). Four year study of cobalt and chromium blood levels in patients managed with two different metal on metal total hip replacements. J. Ortho Research, 21 (2), 189-195. 67.Kop A.M., Colin Whitewood C., Johnston D.J.L. Damage of Oxinium Femoral Heads Subsequent to Hip Arthroplasty Dislocation: Three Retrieval Case StudiesThe Journal of Arthroplasty Volume 22, Issue 5, August 2007, Pages 775-779 68.Fulkerson E, Kummer F, Di Cesare PE. Surface damage to an Oxinium femoral head prosthesis after dislocation. Evangelista GT, J Bone Joint Surg Br. 2007 Apr;89(4):535-7. 69.McCalden RW, Charron KD, Davidson RD, Teeter MG, Holdsworth DW. Damage of an Oxinium femoral head and polyethylene liner following ‘routine’ total hip replacement. J Bone Joint Surg Br. 2011 Mar;93(3):409-13. 142 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Lesiones del aparato extensor en la Artroplastia de Rodilla. Perspectiva Latinoamericana Gustavo Adolfo García Rangel. M. D. * * Cirujano Ortopédico Adjunto al Post Grado de la Universidad Central de Venezuela Servicio de Traumatología y Ortopedia. Hospital Miguel Pérez Carreño. Caracas, Venezuela. INTRODUCCIÓN. En la década de los 80 y 90 se llegaron a observar altas tasas de complicaciones del aparato extensor de más del 10 %, entre ellas subluxación y fractura rotuliana, ruptura del aparato extensor, aflojamiento y desgaste, atribuibles según publicaciones a los primeros diseños modernos de la prótesis de rodilla. La mayoría de las complicaciones del mecanismo extensor han estado relacionadas con errores en la técnica quirúrgica y del diseño de los componentes femoral o rotuliano. Actualmente, a pesar de la modificación de los diseños, los sistemas de fijación e instrumentación, la incidencia de estas complicaciones ha disminuido como causas de fracasos del reemplazo de la rodilla primaria por debajo del 2-10%. Estas complicaciones van desde implicaciones menores como el “dolor rotuliano” que para algunos especialistas sólo afectan el grado de satisfacción del paciente, a otras complicaciones más catastróficas como “la fractura rotuliana o ruptura del aparato extensor” las cuales aunque infrecuente,s son más graves y de difícil solución, representando el 12% de la revisiones. El paciente con lesión del aparato extensor post artroplastia de rodilla, una vez intervenido , tiene un riesgo de 7% de ser nuevamente revisado dentro del primer año y de hasta 35,9% a los 10 años1. La rutina de reemplazar o no la rótula en artroplastia de rodilla, hoy en día sigue siendo muy controversial y será tema de revisión en otro capítulo. Debido al auge, difusión y aumento del número de artroplastias totales de rodilla, especialmente en pacientes cada día más jóvenes, activos y exigentes, encontraremos exponencialmente aumento de las complicaciones post artroplastia de rodilla, particularmente del aparato extensor. 143 “Temas selectos de actualización en la Ortopedia Latinoamericana” Las lesiones del aparato extensor van a representar una de las más comunes razones para revisar una artroplastia de rodilla y sus resultados van a ser menos favorables comparados con otras causas de revisión de artroplastia de rodilla y posiblemente 23 % de estos pacientes ameritarán una o más cirugias (2). La reconstrucción del mecanismo extensor es técnicamente demandante, con múltiples técnicas descritas y resultados inconsistentes. La prevención es el mejor tratamiento. Factores predisponentes En la literatura estos factores se ha relacionados como dependientes del paciente, de la técnica quirúrgica y del diseño de los componentes. (Ver Tabla 1). En relación a los pacientes, aquellos con enfermedades que implican mala 144 calidad ósea, que lo hacen predisponentes a fracturas de rotula. La obesidad(3) los traumatismos, actividades físicas excesivas con flexión mayor a los 115 grados. Antecedentes de intervenciones previas sobre el aparato extensor, (realineación rotuliana, osteotomías tíbiales)(4) producen acortamiento de este y mayor riesgo de lesión durante la cirugía primaria En lo que respecta a la técnica quirúrgica, el principal factor de supervivencia de una prótesis de rodilla primaria es la correcta alineación femorotibial; la mala colocación de los componentes predispone a fallo temprano. La rodilla valga con hipoplasia del cóndilo femoral externo o desgaste excesivos de los cóndilos posteriores puede conllevar a una incorrecta posición del componente femoral. Con los nuevos diseños protésicos más anatómicos o asimétricos, la liberación del alerón rotuliano externo ya muy poco se realiza, en el pasado se asoció a osteonecrosis rotuliana, pero no fue demostrable(5). Otros factores de riesgo se han relacionados con el diseño de los componentes femorales o rotulianos. A nivel del componente femoral no se ha encontrado diferencias entre los resultados funcionales o mecánicos de los diseños simétricos o asimétricos (anatómicos) existiendo además controversia con respecto a la eficacia o no de un surco troclear profundo o un alerón externo prominente(6). La literatura refleja que las complicaciones rotulianas son similares en ambos diseños (7). Aquellos diseños femorales amplios y cortos predisponen al llamado clunk patelar(8). En cuanto al diseño patelar, las de polietileno distribuyen irregularmente las fuerzas de compresión que las de bandeja metálica, pero estás se asocian a desgaste y aflojamiento precoces y por eso ya no se usan. La fijación cementada de la patela de polietileno da mucho mejor resultado que las de superficies porosas(3). Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Ruptura del Tendón Rotuliano (Avulsión del Tubérculo Tibial) sada. Es una complicación que debería ser prevenida más que tratada. Generalmente puede ocurrir cuando la exposición de las estructuras se hace difícil en rodillas rígidas y al momento de evertir la rótula hacia el lado externo, se ejerce una tracción importante sobre la inserción del tendón rotuliano. La avulsión del tubérculo durante las maniobras intra operatorias puede suceder con facilidad y si el periostio se desgarra transversalmente los resultados son desfavorables post reconstrucción. Su incidencia va desde el 0,17 -1,4 %. La ruptura del tendón rotuliano mucho más frecuente como avulsión del tubérculo tibial es una complicación seria ya que conlleva a un peor pronóstico en la recuperación de la extensión activa total con fuerza normal. La ruptura puede ocurrir bajo distintas circunstancias y hay diferencias en términos de pronóstico y tratamientos alternativos(9). (Fig. 1) Prevención El cirujano debe conocer desde el preoperatorio y en el trans operatorio cuan insuficiente puede ser la exposición de la rodilla sin exponer al daño del tendón rotuliano que es la parte más débil del aparato extensor en las rodillas primarias; en dado caso debe conocer alternativas para prevenir esta lesión. Tomaremos las tres consideraciones preventivas sugeridas por Insall & Scott10 Las lesiones del aparato extensor en la artroplastia total de rodilla pudiéramos clasificarlas arbitrariamente en dos grandes grupos 1. Lesiones del aparato extensor durante el acto quirúrgico y 2. Lesiones del aparato extensor que pudieran ocurrir después de la artroplastia. Revisaremos las entidades más frecuentes y nuestro enfoque particular. Figura 1.Avulsion intraoperatoria tendón rotuliano con prótesis ya colocada. La causa más común es una avulsión intra operatoria durante la cirugía primaria o en la revisión de una rodilla rígida o anquilo- 1. Incision capsular vertical sobre la tibia a 1 cm medialmente respecto al tuberculo tibial, tratando de dejar un manguito de periostio en continuidad con el tendón rotuliano, preservando así la integridad de las partes blandas en la región distal. Puede realizar de rutina la colocación de un clavo liso de Steinmann o Kirschner o pinza de campo en el tubérculo tibial; algunas casas comerciales han desarrollado aparatos especiales para esto, lo cual proporcionará un punto adicional de fijación – estabilización. Lo más importante es reconocer la insuficiencia del aparato extensor a tiempo. No confiarse de estos suplementos, debe revisarse secuencialmente la tensión sobre el tendón. Importante vigilar la tensión ejercida con los separadores en la exposición de la rodilla mientras se ejecuta el procedimiento quirúrgico. 2. En caso de ser una rodilla rígida puede realizarse un abordaje más complejo 145 “Temas selectos de actualización en la Ortopedia Latinoamericana” sobre la parte proximal del cuádriceps con una incisión adicional oblicua a 45 o recta desde su vértice hacia el vasto externo, hasta que el tendón del cuádriceps y la rótula pueden evertirse distal y externamente 3. En caso de no tener familiaridad con el abordaje sobre el cuádriceps, se puede realizar una osteotomía de la tuberosidad tibial anterior. Nosotros tratamos en la mayoría de los casos de no evertir la rótula, porque creemos que hay fuerzas tensionales adicionales con la eversión sobre la inserción del tendón tibial. Las causas de avulsión pueden ser como resultado de una manipulación externa post operatoria o una caída, o una avulsión espontanea durante la rehabilitación. Estamos de acuerdo con muchos autores que piensan que para que esto suceda, se debe haber interiorizado o comprometido la inserción del tendón durante la cirugía. Es muy frecuente la asociación de un hueso tibial osteoporótico. Actualmente no conocemos ningún método efectivo para reparar un tuberculo tibial avulsionado y más si hay un hueso osteoporótico. Varios escenarios podemos encontrarnos: 1. Avulsión intraoperatoria: la cual dependerá del manguito de periostio involucrado, si la avulsión es transversal completa, los resultados serán desfavorables post reconstrucción. Se puede realizar una tenodesis con fijación a hueso con sutura nylon no reabsorbible Etilón 1, con paso de varias suturas (referidas) a través del canal tibial antes de cementar el componente tibial. También puede usarse como complementos tornillos o grapas. 2. Avulsión post operatoria con fragmento de hueso tibial desplazado, debe realizarse fijación abierta mediante sutura, tornillos o grapas, luego inmovilización por 6 – 8 semanas. 3. 146 Avulsión post operatoria con fragmento de hueso tibial no desplazado y componente tibial fijo: inmovilización en extensión por 6 a 8 semanas. 4. Avulsión post operatoria con fragmento de hueso tibial desplazado o no con componente tibial flojo: revisión del componente tibial + reducción abierta y fijación interna de la fractura como mejor opción de tratamiento. Ruptura del Tendón Rotuliano o del tendón del cuádriceps Puede ocurrir como una complicación tardía post traumática. Con una incidencia de 0.17 % (14/8.288)(11) – 2,5 % (7/281)(12). Los factores de riesgos incluyen liberación retinacular lateral, cirugía previa de rodilla, sobre resección patelar, osteotomía previa del tuberculo tibial y manipulación cerrada por rodilla rígida en extension(13). (Fig. 2) La reparación de una ruptura de un tendón patelar siguiendo a reemplazo total de rodilla puede ser un procedimiento quirúrgico complejo con resultados inciertos; la causa es debido a que la re - ruptura es frecuente, entonces la reconstrucción del tendón es preferible(11). Figura 2. Lesiones tendinosas agudas de cuádriceps y rotuliano Opciones viables como el auto injerto del semitendinoso debe ser considerada; esta técnica consiste en aislar el tendón Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT desde su inserción distal y luego cortarlo en su parte proximal, para luego pasarlo a través de un orificio transversal perforado en el polo inferior de la rótula cara no articular, para luego fijarlo en el tuberculo tibial con una grapa, en el caso de que la longitud del semitendinoso sea insuficiente, puede sumarse el tendón gracilis. En el post operatorio la rodilla se inmoviliza en extensión por seis semanas y luego con un inmovilizador articulado se inician movimientos progresivos durante las siguientes seis a diez semanas. En los casos fallidos o crónicos, los aloinjertos de tendón de Aquiles o aparato extensor completo pueden ser una alternativa (13). Los casos de ruptura aguda del tendón del cuádriceps deben resolverse lo más rápido posible con técnicas estándar de reparación término – terminal, como cualquier reparación tendinosa no relacionada con reemplazos de rodilla. En los casos de ruptura crónica puede realizarse una reparación término – terminal, levantarse una solapa del cuádriceps para proteger la unión o utilizar un aloinjerto de Aquiles o aparato extensor completo, como mejor opcion (14). Como la mayoría de los resultados post reconstrucción no son tan alentadores se impone la Prevención. Complicaciones rotulianas Subluxación y Luxación Los problemas de recorrido fémoro rotuliano post ATR aparecen con una incidencia de 29% de los casos(9). La subluxación es más frecuente que la luxacion(15). Estas entidades van a depender de varios factores técnicos y de diseño protesico(8). Los más importantes factores involucrados: Profundidad de la tróclea femoral. El diseño del surco femoral siempre ha traído problemas con la rótula. Un surco poco profundo predispone a una inestabilidad rotuliana, pero uno excesivamente profundo permite una rotula demasiado constreñida, contribuyendo al aflojamiento del componente rotuliano y/o fractura de rotula. (Fig. 3) Colocación del componente femoral. La colocación del componente femoral en rotación interna aumenta la tensión de las partes blandas de la región externa cuando se flexiona la rodilla(16) . Preferimos cierto grado de rotación externa relativo a los cóndilos posteriores, verificamos con el eje epicondilar y el eje antero posterior o línea de Whitheside para establecer dicha rotación femoral.(Fig. 4). Por otro lado en nuestro medio latinoamericano, debido a la poca disponibilidad o ausencia de Banco de Tejidos, debemos tratar estas lesiones reparando en forma precoz, protegiendo y reforzando con malla de Marlex ®, dando una oportunidad al mejor resultado funcional. Debemos utilizar abordajes extensibles cuando sea necesario y evitar problemas intraoperatorios causados por imprudencia. Figura 3. Subluxacion patelar 147 “Temas selectos de actualización en la Ortopedia Latinoamericana” Retinacular o alerón externo tenso. Si este se encuentra tenso va a contribuir a una luxación rotuliana. El motivo de consulta de estos pacientes es dolor en la cara anterior de la rodilla o presentar una evidente subluxación o luxación, sintomática. En los casos de subluxación leve y un vasto medial débil, debe intentarse rehabilitación enérgica. El dolor se explica cuando hay una mala posición de los componentes o una mala alineación, y esto puede verificarse con una TAC antes de tomar una decisión quirúrgica; si esto es así, debe realizarse una cirugía de revisión. Figura 4. Mal posición componentes Rotación inadecuada del componente tibial. La rotación interna del componente tibial proporciona una localización externa del tuberculo tibial, aumentando el Angulo del cuádriceps y contribuyendo a la inestabilidad rotuliana. La causa más común, es una exposición insuficiente que no permite ver la superficie tibial completa y no apreciar así las referencias anatómicas para colocar en forma adecuada el componente tibial. El tuberculo tibial ha sido la referencia anatómica tradicional para establecer la rotación del componente tibial, podemos verificar con referencias anatómicas distales como eje transmaleolar del tobillo o el segundo Metatarsiano del pie (menos confiable por las variaciones anatómicas). Debe tenerse en cuenta que la alineación de un componente tibial simétrico con el margen posterior tibial, proporcionará cierta rotación interna de dicho componente, y esto debe evitarse. Alineación en valgo. La posición de la prótesis en valgo excesivo aumenta el Angulo del cuádriceps. La inestabilidad rotuliana suele aparecer en rodillas que tenían valgo patológico en el preoperatorio. 148 En la mayoría de los casos, siempre y cuando se determine una correcta orientación de los componentes, el tratamiento consiste en una liberación del alerón externo y se recomienda realizar una realineación proximal para obtener mejores resultados (17). Muchos autores no recomiendan la transposición del tuberculo tibial por la calidad del hueso subyacente que suma para el alto índice de complicaciones que esto representa (18). El mejor entendimiento de las técnicas quirúrgicas evita la inestabilidad patelofemoral; algunos factores técnicos atener en cuenta, incluyen: 1. Evitar la sobre resección de la patela 2. Quienes reemplazan la rótula, deben colocarla medial y superior 3. Posición rotacional correcta de los componentes femoral y tibial 4. Lateralización de los componentes femoral y tibial sin producir sobresalida de estos para evitar pinzamientos 5. Tratar de mantener la línea articular pre operatoria. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 6. Verificación del recorrido patelar en la tróclea femoral con la técnica de “no pulgar” 7. Asegurar bien el cierre de los planos de la artrotomia(19). Pinzamiento de partes blandas (Nódulo fibroso “ Clunk Patelar”) El pinzamiento de las partes blandas en la articulación patelofemoral ha sido descrito como causa de dolor y bloqueo. Un nódulo fibroso puede desarrollarse en la región suprapatelar del cuádriceps y producir un efecto de pinzamiento en la escotadura femoral intercondílea, cuando la rodilla es flexionada; a esto se le conoce como “Síndrome de clunk patelar” y se ha asociado con el uso de prótesis con estabilización posterior. Las mejoras en el diseño de la tróclea femoral ha reducido en forma importante la incidencia de este sindrome (8). En aquellos casos muy sintomáticos, cuando este síndrome de clunk patelar aparece, debe realizarse una exéresis del nódulo vía artroscopia. Las ventajas de la artroscopia incluyen simplicidad de la técnica, disminuye la recurrencia y el riesgo de infección, al mismo tiempo permite una rápida recuperación en el post operatorio (20). Fractura de la rótula La fractura de la rótula post artroplastia total de rodilla es infrecuente, pero puede ser una fuente de morbilidad significativa. La incidencia varía entre 1 al 4 % (21). En su etiología se ha involucrado muchas variables: compromiso vascular, factores bioquímicos, técnicos, térmicos y traumáticos (el remplazo patelar, liberación alerón externo, cirugía de revisión, reemplazo metálico, mala alineación post reemplazo de rodilla, sobre resección ósea El tratamiento depende del tipo de fractura, desplazada o no y de la estabilidad del componente patelar, flojo o no (Fig. 5). La mayoría de estas fracturas son hallazgos incidentales, son asintomáticas y evolucionan bien sin cirugía. Para fracturas desplazadas y componente patelar flojo se ofrecen varias opciones dependiendo de la continuidad o no del aparato extensor (Tabla 2). Figura 5. Fractura polo inferior rotula, componente flojo. Aflojamiento del componente patelar Un componente patelar flojo puede ser el resultado de una falla en la fijación, necrosis avascular de la patela, mal alineación o fractura. La causa de la falla debe ser identificada y verificada en el acto quirúrgico, donde el componente patelar debe ser removido con todos los restos de metilmetacrilato, el hueso patelar restante debe ser evaluado cuidadosamente, para determinar la reconstrucción ósea o el reimplante (22). Tratamiento Las consideraciones para el tratamiento dependerán de si la lesión es aguda o crónica, ya en los apartados anteriores comentábamos que la reparación aguda para cada caso debía ser oportuna y a tiempo, en ocasiones reforzar con aloinjertos y/o malla de Marlex ®. Opciones de tratamiento: 1. Manejo no quirúrgico 2. Reparación directa 3. Reparación directa con aumentación 4. Biológica 149 “Temas selectos de actualización en la Ortopedia Latinoamericana” 5. Sintética 6. Reconstrucción con aloinjertos 7. Artrodesis Manejo de la Disrupción Crónica del Aparato Extensor. La disponibilidad y calidad de los tejidos blandos, demandas funcionales y las condiciones médicas del paciente van a ser claves para la toma de decisiones (23). El tratamiento quirúrgico de la lesión del aparato extensor “es una reconstrucción y no una reparación”. Los resultados de la reparación aguda y de repetidos intentos de nueva reparación del mecanismo extensor son muy desfavorables y la fijación con suturas arrojan un porcentaje de falla > 90% usando una variedad de tecnicas (4-11), sumado a esto el riesgo de infección en esa búsqueda de restaurar la función del mecanismo extensor. En estas situaciones 150 la reconstrucción con aloinjertos es recomendada para restaurar la extensión activa de la rodilla. Debemos saber que el aloinjertos produce una reacción autoinmune, puede transmitir enfermedades, dependerá de su resistencia y de su incorporación. Opciones para las reconstrucciones con aloinjertos incluyen el uso de aloinjerto completo de aparato extensor o en casos de ruptura crónica del tendón rotuliano, uso de aloinjerto de Aquiles con su bloque óseo de calcáneo. Para cualquier caso siempre deben ser revisados los componentes protésicos antes de realizar la reconstrucción. Mientras los principios básicos son los mismos para ambas técnicas, hay algunas diferencias: • La principal ventaja del aloinjerto tendón de Aquiles es que la patela del paciente es retenida. • Sin embargo el aloinjerto completo de aparato extensor permite una fijación Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT proximal más firme y una cobertura mayor del tejido huésped, a diferencia del aloinjerto del tendón de Aquiles que queda debajo de la piel porque se coloca en forma superficial al aparato extensor remanente o huésped. De los resultados de la reconstrucción con aloinjerto de tendón de Aquiles Crossett y col(24). 9 pacientes con seguimiento de 28 meses, con retardo de extensión 44 grados en el preoperatorio a 3 grados en el post operatorio, con mejoría en la escala funcional, 2 casos fallidos en la fijación distal. (Fig. 6) • Extensión completa a medida que avanza el procedimiento • Quirúrgico, a veces es un poco difícil pero debe lograrse. • Se prefiere aloinjerto fresco congelado no irradiado del lado correcto que se va a reconstruir. (Fig. 7) Fig 7. Aparato extensor completo fresco congelado • Abordaje según la cicatriz anterior, preferible en la línea media Fig 6. Técnica quirúrgica para reconstrucción con Aloinjerto de Aquiles liofilizado y malla de Marlex. A) Preparación del aloinjerto. B) Fijación con tornillo en tibia proximal, previa preparación del lecho tibial C) Sutura con Vycril 1 de distal a proximal con hiperextensión de la pierna D) Refuerzo con malla sintética de Marlex® suturada con Vycril 1 sobre el tejido huésped y aloinjerto. • El bloque óseo tibial debería ser aproximadamente 5 cm en longitud x 2 cm de ancho x 2cm en profundidad para ser sembrado en la tibia proximal en un lecho (zona de inserción distal del tendón patelar) de iguales proporciones a la pastilla ósea del aloinjerto. • El aloinjerto completo del aparato extensor (tibia proximal, tendón. Previo tallado del bloque de hueso del aloinjerto, se realiza una fijación distal firme mediante un buen press fit de este dentro del lecho tibial elaborado, puede fijarse con alambre No. 16 o tornillos esponjosas 4.5 con arandelas. Si utiliza tornillo realizar la perforación del bloque de hueso del aloinjerto antes de prepararlo para el lecho, para evitar fracturarlo. • Patelar, patela y tendón del cuádriceps), debe ser colocado en • El aloinjerto es entonces tensionado en extensión completa. No debe relajarse Los principios básicos de la reconstrucción con aloinjerto completo del mecanismo extensor son tomados del Instituto Rush de Chicago (25, 26, 27,28) • 151 “Temas selectos de actualización en la Ortopedia Latinoamericana” la rodilla y se debe evitar evaluar la flexión intra operatoriamente. lidad, 5 infecciones profundas, 10 pacientes tenían un retardo de extensión en 30 grados. • La patela no se le debe realizarse resurperficialización. Recientemente Browne JA y Hanssen AD y col34. Del grupo de la Clínica Mayo – Minnesota, publicaron el desarrollo de una nueva técnica, una alternativa al uso del aloinjerto y además de su bajo costo. Ellos describieron la reconstrucción del aparato extensor con malla sintética de Marlex®. • El aloinjerto debería ser cubierto por tejidos blandos huésped. Protocolo Post operatorio: • Inmediato: colocación de férula de yeso en extensión completa. • 3er. día: evaluación de la herida operatoria, colocación de inmovilización inguino pédica con yeso. Descarga parcial de peso con muletas, puede realizar ejercicios isométricos de fortalecimiento de cuádriceps. • Un trozo de malla de 10 x 14 pulgadas es enrollada creando un tubo aproximadamente de 1 pulgada de ancho, el cual es cerrado con una sutura fuerte no reabsorbible. • El tubo de malla elaborado es fijado a) intramedularmente al momento que se coloca el nuevo componente tibial en caso de haber sido revisado. b) en el caso de haber sido retenido los componentes, se realiza un lecho en la tibia proximal similar al lecho cuando se inicia para la inserción de un clavo tibial endomedular. La malla es fijada dentro del lecho con cemento y un tornillo. • El aparato extensor remanente, es extensamente movilizado y liberado. • La patela se reduce a un adecuado nivel articular y el tejido blando huésped restante es reparado, suturado a la malla con sutura fuerte no reabsorbible. La meta es la cobertura completa de la malla con tejido huésped. • 3ra. semana: retiro de yeso, suturas o grapas y nueva inmovilización inguino pédica por tres semanas adicionales. • 6ta. semana: retiro de inmovilización y colocación de férula articulada con rango articular 0 – 30 grados, con incremento de la flexión de 10 grados por semanas. • Se permite la flexión activa solamente (no pasiva) con ejercicios continuos de fortalecimiento de cuádriceps. Los resultados generales de estos procedimientos reconstructivos es el recurrente retardo para la extensión completa más común que la falta de flexion (29, 30, 31, 32,33). Burnett y col.26 del Instituto Rush Chicago presentan sus resultados de 50 pacientes reconstruidos con aloinjerto completo de aparato extensor a un seguimiento de 56 meses (rango de 24 a 125 meses). 28 (56%) pacientes consiguieron extensión activa completa. 6 (12%) pacientes tuvieron fallas de la fijación del bloque óseo tibial y 3 pacientes tuvieron fracturas peri protésicas tardías de la tibia proximal. 19 (38%) fueron considerados fallas (4 inestabi- 152 En sus resultados reportaron 13 pacientes reconstruidos con mallas de Marlex® con seguimiento de 42 meses, 9 casos con retardo de extensión de 10 grados. 3(23%) pacientes fallaron. Método preferido por el Autor Dentro de todas las complicaciones, la lesión del aparato extensor es poco frecuente, pero cuando sucede pasa a ser muy devastadora, se desencadenan una Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT serie de eventos que aunque hagamos lo correcto, los resultados no siempre cubrirán las expectativas del paciente. Para nosotros una de las cosas más importante es informar al paciente antes de la cirugía, de todas las complicaciones existentes post artroplastia y sus desenlaces. Creemos que el mejor tratamiento es la PREVENCION y el reconocer a los pacientes en RIESGO. En nuestro medio latinoamericano, debemos depurar la técnica quirúrgica en los reemplazos de rodilla primario. Siempre tratamos de utilizar un marcador estéril para dibujar la Incision en piel y hacemos marcas transversales para orientar luego el cierre. Hacemos sobre la línea dibujada una Incision mediana de una longitud suficiente en la piel de la cara anterior de la rodilla de acuerdo. Utilizamos un abordaje para-patelar interno, sobre el intersticio entre musculo y tendón, realizamos un gesto sobre la esquina supero interna del borde superior de la rótula al momento de la artrotomía (Comunicación verbal - Dr. Claudio Alonso (Argentina) y lo hacemos para orientar el correcto cierre del aparato extensor. Casi nunca evertimos la rótula, solo la subluxamos externamente, se nos facilita más rotando externamente la pierna en flexión, en ocasiones si la rodilla es “muy apretada” le colocamos un pin en la inserción del tendón rotuliano, para protegerlo. Hacemos los cortes óseos correctos con una buena exposición articular de los reparos anatómicos. Importante proteger el tendón rotuliano sin desinsectarlo al momento de hacer el corte tibial, para evitar traumatismo repetido con la sierra que desvitalicen a mediano o corto plazo el tendón rotuliano. Revisamos la correcta posición de los componentes protésicos, insistimos en el balance de partes blandas. Desde que usamos prótesis anatómicas no liberamos casi nunca el alerón rotuliano externo. Por otro lado estas complicaciones son frecuentes en las rotulas reemplazadas, por eso desde hace varios años hacemos reemplazo selectivo de la rótula y preferimos el botón de polietileno con tres puntos de apoyo. Reemplazamos solo en pacientes con artritis reumatoide u otra enfermedad autoinmune, a todas las rotulas le hacemos exeresis parcial de la faceta lateral de rotula y no hacemos la supuesta denervación patelar periférica. Preferimos que la rodilla nos quede algo floja en la extensión, buscando el recurvatum fisiológico. Después de colocada la prótesis, liberamos el torniquete y practicamos “la regla no pulgar” para la excursión rotuliana. Realizamos el cierre de los planos profundos en flexión de la rodilla, afrontando proximalmente los planos del alerón interno a la altura de la mueca en el borde supero medial de la rótula y luego suturamos de distal a proximal para evitar el acortamiento del tendón rotuliano (Comunicación verbal Dr. Miguel Cabanela –USA). Es importante que antes de colocar la prótesis definitiva, se debe evaluar la integridad del tendón rotuliano y de su inserción tibial. En caso de tener una desinserción parcial del tendón rotuliano o sospechar de la debilidad de este, antes de cementar el componente patelar, perforamos con una mecha 2,5 mm y pasamos dos o tres suturas no reabsorbibles de dentro afuera del canal y viceversa, referimos estas suturas, colocamos y cementamos nuestro componente tibial, una vez colocado toda la prótesis, fijamos la desinserción del tendón rotuliano, si la desinserción fue parcial con bordes periosticos tendrá mejor resultado a diferencia de las desinserciones completas que terminan con malos resultados funcionales. Otro escenario es la desinserción del tendón patelar parcial o total después de colocado y cementado el componente tibial, ¿entonces tenemos un problema? que es la fijación deficiente y precaria al hueso, 153 “Temas selectos de actualización en la Ortopedia Latinoamericana” podemos usar suturas no reabsorbibles y alambre de por sí muy laborioso. Inmovilizamos por tres semanas de acuerdo a la lesión, luego férula articulada (0 extensión a 30 grados de flexión) x 3 semanas, movilidad progresiva semanal de 10 grados de flexión, se informa a los pacientes que puede haber una perdida funcional). Cuando nos enfrentamos a los casos crónicos de lesión de aparato extensor, muchos de estos pacientes han sido tratados en forma errónea e insuficiente y luego abandonados por su cirujano o institución tratante, al no tener buenos resultados. Por eso estos pacientes cuando llegan a la consulta, realizamos una exhaustiva historia clínica, tratamos de contactar a la institución o cirujano de origen para conocer las causas de la falla. Luego planificamos con extremo cuidado, se coordina con la Casa Comercial apropiada y nos mentalizamos para hacer una cirugía de revisión de rodilla, evaluamos la estabilidad de los componentes, si están flojos se cambian (en algunas oportunidades uno o los ambos componentes protésicos pueden aflojarse, debido a que estos pacientes desarrollan un recurvatum de adaptación para caminar provocando el aflojamiento por la inestabili- dad creada). De acuerdo a la disponibilidad de aloinjerto, preferimos en primer lugar el aloinjerto completo de aparato extensor fresco congelado, segundo lugar el aloinjerto de tendón de Aquiles fresco congelado. La técnica como se describió anteriormente. Todos los pacientes los reforzamos con malla de Marlex ® para crear un refuerzo adicional. Los resultados de nuestra experiencia de los 8 casos reconstruidos (4 aloinjertos completos, 3 aloinjertos de Aquiles, 1 aloinjerto hueso tendón hueso rotuliano) a un seguimiento de 5 años, 2 con retardo de extensión <5 grados, 2 con retardo de extensión <15 grados, 2 con retardo de extensión <30 grados, 1 infección profunda, 1 artrodesis. Como la literatura lo señala por ahora no hay un tratamiento definitivo y eficaz que ofrezca restitución de la función en estos casos, con el tiempo estas reconstrucciones van fallando por pérdida de las propiedades de los aloinjertos y los materiales sintéticos. Por ahora para nuestras comunidades latinoamericanas vemos el trabajo presentado por el grupo de Arlen Hassen (34) de la Clínica Mayo como la mejor alternativa practica y económica para estas reconstrucciones, en comparación con la disponibilidad escasa y costosa en los países que no tienen Banco de Hueso y Tejidos. BIBLIOGRAFÍA 1. Lizaur A. Complicaciones del aparato extensor en protesis total de rodilla, En Protesis de Rodilla Primaria. Estado actual ed por Rodriguez – Merchan, Medica Panamerica, Madrid, 2008, p197-211. 2. Griffin W. Extensor Mechanism Dysfunction. ICL # 202, Videos Techniques in Revision TKA. ICL #202, AAOS San Francisco 2012 3. Healy WL, Wasilewski SA, Takei R, Oberlander M. Patellofemoral complications following total knee arthroplasty: correlations, implants and design and patient risk factors. J Arthroplasty. 1995; 10 (2):197-201. 4. Rand JA. Extensor mechanism complications after total knee arthroplasty . Instr Course Lect. 2005; (54): 241-50. 5. Ritter MA, Campbell Ed. Postoperative patellar complications with or whihout lateral release during total knee arthroplasty. Clin Orthop Relat Res. 1987;(219):163-8. 154 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 6. Bindelglass DF, Dorr LD. Symmetry versus asymmetry in the design of total knee femoral components: an unresolved controversy. JArthroplasty. 1998; 13(8):939-44. 7. Ashraf T, Beard DJ, Newman JH. Symmetrical vs asymmetrical total knee replacement : a medium term compartive analysis. Knee.2003;10(1):61-6. 8. Clarke HD, Fuchs R, Scuderi GR, Mills EL, Scott WN, Insall JN. The influence of femoral component design in the elimination off patellar clunk in posterior – stabilized total arthroplasty. J Arthroplasty 2006;21(2):167-71. 9. Johanson NA: Extensor mechanism failure: Treatment of patella fracture, dislocation, and ligament rupture. In Lotke PA,ed. Master Techniques in Orthopedic Surgery, Knee Arthroplasty. New York Ravens Press, 1995, pp 219-240. 10.Insall & Scott. Surgery of the knee p 1833. Churchill/Livingstone, 2007. 11.Rand JA, Morrey BF, Bryan RS: Patellar tendon rupture after total knee arthroplasty. Clin Orthop 244: 233, 1989). 12.Lotke PA, Ecker MI: Influence of positioning of prosthesis in total knee replacement. J. Bone Joint Surg Am 59:77, 1977 . 13.Scuderi GR, DeMuth BC: Management of patella tendon disruption in total knee arthroplasty, In Surgical Techniques in Total Knee Arthroplasty ed by GR Scudery and AJ Tria, Springer, New York, 2002, 519-523. 14.Booth RE and Femino FP; Acute and cronic rupture of the cuadriceps tendon treated with direct repair. In Surgical Techniques in Total Knee Arthroplasty ed by Scuderi and AJ Tria, Springer, New York, 2002, 514-515. 15.Brick GW,Scott RD: The patellofemoral component of total knee arthroplasty. Clin Orthoped 231:163,1988. 16.Rhoads DD, Noble PC, Reuben JD, et al: The efect of femoral component position on patellar tracking after total knee arthroplasty. Clin Orthop 260:43,1990. 17.Grace JN, Rand JA: Patellar Instability after total knee arthroplasty.Clin Orthop 237:184, 1988. 18.Rand JA, Bryan RS: Results of revision total knee arthroplasties using total condylar prostheses: A review of fifty knees. J Bone Joint Surg Am 70:738,1988 19.Lee GC, Cushner FD, Scuderi GR, Insall JN: Optimizing patellofemoral tracking during total knee arthroplasty. J Knee Surgery 17(3): 144 -15, 2004. 20.Diduch DR, Scuderi GR, Scott WN, et al: The efficacy of arthroscopy following total knee replacement. Arthroscopy 13(2): 166-171,1997. 21.Keating EM, Hass G, Meding JB. Patella fractures after total knee replacement. Clin Orthop Relat Res. 2003; (416):93-7. 22.Lombardi AV, Mallory TH, Herrington JM: Revision of loose patellar components. In Surgical Techniques in Total Knee Arthroplasty ed by Scuderi and AJ Tria, Springer, New York, 2002, 514-515. 155 “Temas selectos de actualización en la Ortopedia Latinoamericana” 23.Griffin William L, Extensor Mechanism Dysfunction. ICL # 202 Videos Techniques in Revision TKA. San Francisco 2012. 24.Crossett LS, Sinha RK, Sechriest VF, Rubash HE. Reconstruction of a ruptured patellar tendon with achilles tendon allograft following total knee arthroplasty. J Bone Joint Surg Am. 2002;84:1354–61. 25.Craig J. Della Valle, MD. Managing the Extensor Mechanism. Let’s Do A Revision Total Knee Arthroplasty. ICL#263. 2012 AAOS Annual Meeting February 8th, 2012) 26.Burnett RS, Berger RA, Della Valle CJ, et al. Extensor mechanism allograft reconstruction after total knee arthroplasty—surgical technique. J Bone Joint Surg 2005;87:175–194. 27.Burnett RS, Berger RA, Paprosky WG, et al. Extensor mechanism allograft reconstruction after total knee arthroplasty—a comparison of two techniques. J Bone Joint Surg 2004;86:2694–2699. 28.Burnett RS, Berger RA, Paprosky WG, Della Valle CJ, Jacobs JJ, Rosenberg AG. Extensor mechanim allograft reconstrution after total knee arthroplasty. A comparison of two techniques. J Bone Joint Surg Am, 86: 2464-9, 2004. 29.Leopold SS, Greidanus N, Paprosky WG, Berger RA, Rosenberg AG. High rate of failure of allograft reconstruction of the extensor mechanism after total knee arthroplasty. J Bone Joint Surg Am. 1999;81:1574–9. 30.Emerson RH Jr, Head WC, Malinin TI. Reconstruction of patellar tendon rupture after total knee arthroplasty with an extensor mechanism allograft. Clin Orthop Relat Res. 1990;260:154–61. 31.Emerson RH Jr, Head WC, Malinin TI. Extensor mechanism reconstruction with an allograft after total knee arthroplasty. Clin Orthop Relat Res. 1994;303:79–85. 32.Nazarian DG, Booth RE Jr. Extensor mechanism allografts in total knee arthroplasty. Clin Orthop Relat Res. 1999;367:123–9 33.Burnett RS, Fornasier VL, Haydon CM, Wehrli BM, Whitewood CN, Bourne RB. Retrieval of a well-functioning extensor mechanism allograft from a total knee arthroplasty. Clinical and histological findings. J Bone Joint Surg Br. 2004;86:986–90. 34.Browne JA, Hanssen AD. Reconstruction of patellar tendon disruption after total knee arthroplasty: results of a new technique utilizing synthetic mesh. J Bone Joint Surg Am. 2011 Jun 15;93(12):1137-43. 156 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Luxación controlada de la cadera en el manejo del pinzamiento (atrapamiento) femoroacetabular Julio Cesar Palacio V, MD. Instituto de Enfermedades Osteoarticulares del Centro Médico Imbanaco El primer reporte de osteoplastia abierta del cuello femoral fue realizado por el doctor Whitman en 1909 cuando realizó este tipo de cirugía en uno de 11 pacientes con coxa vara (1). Unos años después en 1913 Vulpius y Stöffel hacen una breve referencia sobre un procedimiento de osteoplastia a nivel del cuello femoral (2). CITA “En febrero de 1935, un paciente de 55 años con marcado dolor en la cadera fue admitido en el pabellón de Ortopedia del Massachusetts General Hospital con diagnóstico de Protrusio acetabular bilateral. En ese momento el Dr. Smith Petersen planteo el concepto de pinzamiento entre dos superficies sensibles como la causa del dolor y pensó que el problema podía ser solucionado con una plastia en el acetábulo y/o en el cuello femoral. Consideró que realizar en este paciente una plastia a nivel del cuello femoral no era posible ya que tendría que sacrificar una porción importante del cuello por lo tanto decidió remover la porción an- terosuperior del anillo acetabular. Además, consideró importante remover una parte de la capsula anterior ya que con esto removería tejido inervado que para él, contribuía al síntoma de dolor. Enfatizó la importancia de revisar el arco de movimiento intraoperatoriamente asegurando la corrección del pinzamiento y recomendó que se debía ser cuidadoso en no resecar mucho hueso del aspecto superior del acetábulo para evitar el desplazamiento anterior de la cabeza femoral” (3, 4). CITA Realizó el procedimiento en 11 pacientes y según su reporte a todos les fue muy bien. “La mejoría del dolor fue dramática y la recuperación de movilidad fue importante pero no marcada” (3). Los doctores Heyman, Herndon y Strong en 1957 reportaron 20 pacientes, en caderas con pinzamiento secundario a deslizamiento epifisario de la cabeza femoral, a quienes les practicaron una plastia del cuello en vez 157 “Temas selectos de actualización en la Ortopedia Latinoamericana” de una osteotomía del fémur. La primera cirugía de este grupo fue realizada en el mismo año que la del Dr. Petersen en 1935, la segunda en 1942. Al momento del reporte en 1957, 14 de los 20 pacientes tenían un seguimiento entre 2 y 14 años y aunque todos según la descripción estaban funcionando bien, los autores hacen la siguiente advertencia: “Un verdadero resultado para este tipo de procedimientos no se puede dar si no hasta que las caderas sometidas a este tratamiento de conservación no sufran las cargas y estrés de muchos años de una vida físicamente activa” (5). Con esto dejaron planteada una premisa que es válida hasta la fecha en cuanto a que los procedimientos quirúrgicos considerados como de preservación de la cadera tendrán éxito siempre y cuando sean capaces de prevenir un deterioro de la articulación que en otras palabras no sería otra cosa que prevenir la osteoartritis (artrosis). Vemos cómo los primeros reportes sobre el concepto de pinzamiento o atrapamiento femoroacetabular y sus principios de tratamiento se remontan a cien años de antigüedad. Por alguna razón estos conceptos se olvidan en el resto del siglo XX y solo hasta finales de ese siglo en 1999 reaparece el concepto de pinzamiento femoroacetabular, con el reporte hecho por los doctores Myers y Ganz en cinco pacientes con dolor persistente de la cadera después de haber sido sometidos a Osteotomía periacetabular de Ganz (6, 7). En estos diez años se ha avanzado mucho en el entendimiento de esta redescubierta entidad. Se han definido claramente las alteraciones anatómicas existentes y causantes del pinzamiento o atrapamiento. Se acepta hoy que existen dos tipos de pinzamiento el primero de ellos el tipo Cam, caracterizado por la deformidad en cacha de revolver (Pistol Grip) del cuello femoral descrita desde 1965 por el doctor Murray, radiólogo (8) y posteriormente por los doctores Stulberg y Harris en 1975 y 1986 respectivamente (9, 10) y el segundo el tipo Pincer debido a sobrecobertura del acetábulo sobre la cabeza femoral. El pinzamiento o atrapamiento femoroacetabular por cualquiera de sus causas y que en un 80% de los casos tiene un comportamiento mixto (Cam - Pincer), (Figura 1) es una causa importante de dolor en la cadera en el adulto joven, por el daño del labrum acetabular y de su unión con el cartílago acetabular debido a la sobrecarga mecánica dada por la deformidad a través del tiempo. Al dañarse el labrum y la transición de este con el cartílago se origina una cascada de eventos que llevan al desarrollo de la osteoartritis (artrosis), al punto de que con la evidencia existente, esta entidad es catalogada hoy como el factor etiológico en la patogénesis de la mayoría de las mal llamadas artrosis idiopáticas de la cadera (11, 12, 13, 14, 15). El dolor de la cadera en el adulto joven plantea un reto grande en cuanto al diag- Figura 1. Tipos de pinzamiento: CAM, Mixto y Pincer. 158 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT nóstico etiológico del mismo ya que tenemos dolores de causa intraarticular, extraarticulares y referidos de las estructuras vecinas. Con un buen examen físico y con la ayuda de la radiología y la artrorresonancia de la cadera, en resonadores no menores a 1.5 teslas que nos permitan una mejor identificación y estado de la transición labrum-cartílago y el del estado del cartílago, el diagnóstico y estratificación del pinzamiento o atrapamiento femoroacetabular se ha facilitado mucho. (Figura 2) Las opciones de tratamiento para el pinzamiento o atrapamiento femoroacetabular se dividen en no quirúrgicas y las quirúrgicas. Aunque se plantea la posibilidad de tratatamiento no quirúrgico para el manejo del pinzamiento o atrapamiento femoroacetabular, con reposo, modificación de las actividades físicas, fisioterapia y el uso de antiinflamatorios no esteroideos e infiltración intraarticular de esteroides o condroprotectores. No creo que sea de utilidad este enfoque terapéutico en la resolución del problema ya que con esta medida se está atacando solo el síntoma y no el factor etiológico en la patogénesis mecánica de la entidad. El tratamiento quirúrgico es la única opción válida para el manejo del pinzamiento o atrapamiento femoroacetabular ya que actuamos sobre el factor etiológico. Creo que el buen resultado en cuanto al desenlace final en un paciente, depende más de la escogencia apropiada de la técnica para cada uno, dependiendo según el diagnóstico y el patrón de daño existente en la cadera, que de la técnica misma, suponiendo la adecuada idoneidad del profesional para realizar la técnica quirúrgica escogida. Dentro del manejo quirúrgico existen las técnicas conocidas como de preservación de la cadera y los reemplazos articulares como punto final en el manejo de esta patología. La decisión en cuanto a preservar o no, está dada básicamente por el grado de compromiso del cartílago articular. Caderas con compromiso menor a Tönnis Figura 2. Artrorresonancia como ayuda diagnostica. 159 “Temas selectos de actualización en la Ortopedia Latinoamericana” 2 son susceptibles a técnicas de preservación, ya que con compromisos mayores los resultados a corto plazo no son buenos. Uno de los aspectos que más ha evolucionado en estos últimos diez años son las técnicas quirúrgicas de preservación de la cadera, existiendo en la actualidad varias opciones con buenos resultados en la literatura en el corto y mediano plazo, creándose con esto una gran controversia en cuanto a cuál es la técnica quirúrgica más apropiada, para el manejo de esta entidad. Las técnicas conocidas como de preservación de la cadera son: 1. Luxación controlada de la cadera. 2. Osteotomía periacetabular reversa. 3. Artroscopia. 4. Mini abordaje anterior. 5. Mezclas entre ellas. Para poder comparar los resultados obtenidos con el tratamiento y que con esto podamos de forma objetiva definir cuál es la técnica quirúrgica de preservación más apropiada para cada caso, es muy importante el que nos planteemos unos objetivos claros en cuanto a lo que busca con el tratamiento del pinzamiento o atrapamiento femoroacetabular. Los objetivos se pueden dividir en corto, mediano y largo plazo así: Corto plazo 1. Corregir las alteraciones existentes en la anatomía de la articulación de la cadera tanto a nivel del fémur como del acetábulo, mejorando el espacio entre la unión cabeza-cuello del fémur y el acetábulo eliminando así el contacto anormal (pinzamiento o atrapamiento) entre el fémur proximal y el anillo acetabular. Con esto se elimina el factor etiológico en la patogénesis mecánica de esta entidad. (Figura 3) 2. Arreglar el daño del labrum acetabular preservándolo de forma ideal o sacrificando la parte que se encuentra muy deteriorada y que no sea susceptible de preservación. Existe hoy clara evidencia de la importancia en la preservación del labrum acetabular para el mantenimiento de la homeostasis articular (Figura 4). Figura 3. Corrección anatómica en fémur y en acetábulo. 160 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Mediano plazo 1. Mejorar la función articular. 2. Mejorar la calidad de vida del paciente. Largo plazo 1. Evitar la aparición del daño articular (osteoartritis) o la progresión del mismo si ya existía, para evitar tener que llegar a un reemplazo articular. Figura 4. Reparo desgarro labral. La luxación controlada de la cadera, publicada por el doctor Ganz en el 2001 (16) y doctor Lavigne en el 2004 (17), ha sido el estándar de oro para el manejo del pinzamiento o atrapamiento femoroacetabular hasta el día de hoy. Esta técnica quirúrgica, ha contribuido de forma significativa, al entendimiento de la fisiopatología de esta entidad. Es una técnica bien estandarizada y con un bajo índice de complicaciones. Figura 5. Desbridamiento de daño condral. 3. Desbridar el cartílago deteriorado o realizar perforaciones en el hueso subcondral en las zonas que no exista el mismo (Figura 5) Técnica Quirúrgica La técnica quirúrgica está claramente descrita por Ganz (16) y Lavigne (17), pero considero importante hacer unas recomendaciones sobre ciertos puntos de la técnica para evitar errores durante la misma. 4. Mejorar los síntomas sobre todo el dolor. El paciente se posiciona en decúbito lateral. (Figura 6) existentes, Figura 6. Abordaje y exposición de musculatura trocantérica. 161 “Temas selectos de actualización en la Ortopedia Latinoamericana” Se puede usar el abordaje de Gibson o el de Kocher-Langenbeck. En la mayoría de los casos se puede realizar el abordaje de Gibson, dejando el de Kocher-Langenbeck para los pacientes más obesos o musculosos. Se recomienda identificar bien el plano entre el glúteo máximo y el tensor de la fascia lata para ingresar preferiblemente por este intervalo y no transmúsculo con lo que se mejora la exposición y se consigue una disección menos traumática. Después se retira la bursa trocanteriana y se incide el vasto lateral sobre el tendón separando el músculo de la fascia hasta quedarse totalmente por fuera del periostio. Se continúa disecando anteriormente en el fémur rotando exteriormente la cadera todo el tiempo por fuera del periostio hasta encontrar la grasa del recto intermedio y se vean las ramas de la circunfleja lateral. Este es el borde inferior de la disección. Posteriormente se realiza la osteotomía del trocánter mayor de posterior a anterior (Figura 7). Antes de realizar la osteotomía se debe incidir la fascia del glúteo medio. El glúteo medio debe quedar adherido al trocánter con lo que protegemos la rama de la circunfleja medial. Recordemos que la arteria circunfleja medial femoral corre en el borde inferior del obturador y entra al cuello femoral por Figura 7. Osteotomía del Trocánter Mayor. 162 debajo del tendón del piriforme. Como regla, en este abordaje nunca se debe desinsertar el tendón del piriforme para no lesionar la arteria circunfleja. Después de realizar la osteotomía se coloca un retractor tipo Hohmann anteromedial y se rota la cadera externamente. En este momento se diseca el glúteo medio dejando algunas fibras del músculo adheridas al trocánter para asegurar la reinserción. Se encuentra la capsula adelante del piriforme y se diseca totalmente de forma extracapsular. Para asegurar una buena disección de la cápsula tenemos que disecar los músculos iliacos y superiormente el glúteo mínimo hasta encontrar la porción refleja del recto femoral en este momento se separa el borde anterior del acetábulo con un Hohmann ya sea por encima o por debajo de la porción refleja. En este punto, se tiene una buena exposición de la capsula y se procede a realizar la capsulotomía en z (Figura 8). Después se realiza la luxación de la cadera previa sección del ligamento redondo y a partir de este momento corregimos las deformidades existentes. Después de corregir las deformidades se realiza una capsulorrafia teniendo cuidado de no dejar la sutura ni el nudo intraarticular. Posteriormente, se hace la osteosíntesis del trocánter mayor con 2 tornillos corticales de 4,5 mm. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT corregir las deformidades se realiza una capsulorrafia teniendo cuidado de no dejar la sutura ni el nudo intraarticular. Posteriormente, se hace la osteosíntesis del trocánter mayor con 2 tornillos corticales de 4,5 mm. Figura 8. Capsulectomía y exposición cabeza femoral. Después se realiza la luxación de la cadera previa sección del ligamento redondo y a partir de este momento corregimos las deformidades existentes. Después de Al proteger el músculo obturador externo de la cadera y el piriforme durante el abordaje, la circulación de la cabeza femoral dada por la arteria circunfleja medial está a salvo (18). Este abordaje permite una visión de 360° de la cabeza femoral y del acetábulo, con lo que el cirujano puede hacer una evaluación de las alteraciones existentes de forma muy clara permitiéndole realizar una corrección adecuada de las mismas. (Figura 9). A través de este abordaje, se puede hacer una plastia de la transición del cuello cabeza y se puede restaurar de forma Figura 9. Exposición de 360°, únicamente con luxación quirúrgica 163 “Temas selectos de actualización en la Ortopedia Latinoamericana” adecuada el offset del cuello femoral en toda la extensión requerida dependiendo de la visualización directa de los puntos de pinzamiento con los movimientos de la articulación intraoperatoriamente hasta que quedar satisfecho con la corrección y el rango de movimiento obtenido. Es más fácil reconocer y tratar patrones inusuales de pinzamiento. El daño del cartílago en la cabeza y el acetábulo se puede manejar con condroplastia, perforaciones o microfracturas para promover una respuesta de fibrocartílago. El sobrecubrimiento del acetábulo se puede manejar con resección parcial del anillo acetabular desinsertando el labrum y reinsertándolo después de la resección. Es importante que no se exagere la resección del anillo acetabular ya que se puede inestabilizar la articulación. Lesiones del labrum acetabular pueden ser desbridadas o se pueden reinsertar si el tejido es sano y viable. Cuando se reinserte el labrum es importante que el punto y nudo de la sutura no queden intraarticular. Como se mencionó, la preservación del labrum acetabular es muy importante en la homeostasis de la articulación y hasta donde sea factible, este debe ser el enfoque que se debe seguir. y evitar el tener que llegar a un reemplazo articular. La artroscopia de la cadera se ha popularizado mucho en los últimos años en el manejo de esta entidad y aunque hay que reconocer sus avances, todavía tiene limitaciones sobre todo en el manejo apropiado de las deformidades óseas mayores tanto en el fémur como en el acetábulo, pues debido a que no se tiene una visualización tridimensional del defecto, no es posible llegar a todas las zonas de la articulación y no existe la certeza de haber corregido totalmente todos los puntos de pinzamiento existentes y aunque la mayor área de deformidad generalmente es anterior en el cuello, de fácil acceso con el artroscopio, su extensión siempre es variable. Lo mismo sucede a nivel del acetábulo. Cuando existe pinzamiento posterior, es imposible llegar con el artroscopio a esta región. Las fallas reportadas en el tratamiento con la artroscopia están descritas básicamente por no lograrse una osteoplastia del cuello femoral de forma apropiada (21). Los resultados de este procedimiento a corto y mediano plazo en la literatura son excelentes, siempre y cuando el procedimiento sea realizado en pacientes sin daño articular avanzado, pacientes con Tönnis < 2, ausencia de inestabilidad articular o displasia. Los resultados obtenidos cuando se preserva el labrum en vez de su resección asociado a este procedimiento son mejores como fue demostrado por Espinosa y McCarthy (19, 20). 1. Los detalles anatómicos se reconocen mejor. No existe claridad en la literatura en cuanto a cuál es la mejor técnica quirúrgica para conseguir el objetivo primario en el manejo del pinzamiento (atrapamiento) femoroacetabular que como hemos dicho, no es sino prevenir el daño de la articulación 164 Para el autor, la luxación controlada de la cadera es el método ideal de tratamiento del pinzamiento femoroacetabular en los casos de deformidad ósea mayor porque: 2. La patología existente se reconoce mejor. 3. La resección del anillo acetabular es más fácil. 4. El manejo de grandes deformidades es más fácil. 5. Se reconocen y manejan de forma más apropiada los patrones inusuales de pinzamiento. 6. Existe la posibilidad de resecar la parte anterior del trocánter que en muchos casos contribuye al pinzamiento. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 7. Se manejan mejor las causas de pinzamiento extra articular. 8. Es más fácil resecar la parte medial y la base del cuello femoral. 9. Es más fácil resecar la parte lateral de la cabeza femoral. Existe otro artículo de iguales características publicado en el 2007 por los doctores Sussman, Ranawat y Kelly que muestra que no hay diferencias en la osteoplastia hecha artroscopicamente vs con luxación abierta (23). 10.Se produce menor destrucción de la cápsula articular. Al analizar la literatura existente sobre el pinzamiento (atrapamiento) femoroacetabular encontramos: 11.Es más fácil definir la movilidad y las zonas de pinzamiento residual. 1. El 80% de los artículos son sobre histo-fisio-patologia y técnicas quirúrgicas. 12.Se pueden asociar osteotomías de fémur o acetabulares cuando sea necesario. Con lo anterior no se descalifica la artroscopia como técnica quirúrgica de preservación de la cadera; por el contrario, ella ha venido ganando terreno en el manejo de esta entidad y en el futuro, con el avance tecnológico de los instrumentos es probable que siga ganando espacio y por qué no, se convierta en el nuevo estándar de oro para el manejo del pinzamiento (atrapamiento) femoroacetabular. Hoy en día tiene una excelente indicación en el manejo de las lesiones cartilaginosas intraarticulares, en las lesiones aisladas del labrum o en deformidades óseas menores, en la remoción de cuerpos libres intraarticulares y en el manejo de la cadera en resalto, pinzamiento del psoas y algunas patologías inflamatorias que no mejoren al tratamiento médico. El trabajo realizado por el Doctor Mardones y su grupo publicado en 2009 (22) en el cual realizaron una comparación en cadáver entre luxación controlada versus artroscopia mostró que con la artroscopia no se apreciaba claramente el largo necesario de la osteoplastia del cuello femoral en el pinzamiento tipo CAM, además se observó que con la artroscopia la posición de la osteoplastia era más posterior y distal del lugar adecuado para realizarla. (24, 25) 2. Los resultados son a corto y mediano plazo (26, 27, 28, 29) 3. No hay unificación de criterios en cuanto al grado de lesión existente previa al tratamiento, para poder hacer una buena interpretación y comparación. (30, 31) 4. Los resultados se enfocan a mejoría clínica, satisfacción del paciente y regreso a la actividad deportiva. (32, 33, 34) 5. Los resultados son similares en los aspectos anteriores. (35) 6. Las fallas en el tratamiento artroscópico son por pinzamientos no detectados (36). 7. Malos resultados en artrosis (Tönnis >2) 8. El éxito del tratamiento radica en un buen diagnóstico.(33, 35, 37) El pinzamiento femoroacetabular es una patología que todavía está en proceso de entendimiento y definiciones, su historia en todos los aspectos se está escribiendo y hoy todavía son muchas las preguntas que no tienen una respuesta clara y que solo con el tiempo tendremos. 165 “Temas selectos de actualización en la Ortopedia Latinoamericana” BIBLIOGRAFÍA 1. Whitman R. Further observations on injuries of the neck of the femur in early life. Med Rec. 1909; 75:1-8. 2. Vulpius O, et al. Orthopadische Operationslehre. Suttgart, Germany: F. Enke; 1913. 3. Smith Petersen MN. Treatment of malum coxae senilis, old slipped upper femoral epiphysis, in- trapelvic protrusion of the acetabulum, and coxa plana by means of acetabuloplasty. J Bone Joint Surg Am. 1936; 18:869-880. 4. Brand RA. Femoroacetabular Impingement: Current Status of Diagnosis and Treatment. Marius Nygaard Smith-Petersen, 1886-1953. Clin Orthop Relat Res. 2009; 467:605-607. 5. Heyman CH, et ál. Slipped femoral epiphysis with severe displacement; a conservative operative treatment. J Bone Joint Surg Am. 1957; 39:293-303. 6. Myers SR, et ál. Anterior Femoroacetabular impingement after periacetabular osteotomy. Clin Orthop Relat Res. 1999; 363:93-99. 7. Beaulé PE. Femoroacetabular Impingement: Current Status of Diagnosis and Treatment. Clin Orthop Relat Res. 2009; 467:603-604. 8. Murray RO. The etiology of primary osteoarthritis of the hip. Br J Radiol. 1965;38:810 9. Harris WH. Etiology of osteoarthritis of the hip. Clin Orthop. 1986; 213:20-33. 10.StulbergSD, et ál. Unrecognized childhood hip disease: a major cause of idiopathic osteoarthritis of the hip. In: The Hip Proceedings of the Third Open Scientific Meeting of the Hip Society. St Louis: C.V. Mosby; 1975:212-220. 11.Ganz R, et ál. Femoroacetabular impingement: A cause for osteoarthritis of the hip. Clin Orthop Relat Res. 2003; 417:112-120. 12.Leuning M, et ál. The concept of femoroacetabular impingement: current status and future perspectives. Clin Orthop Relat Res.2009; 467:616-622. 13.Tibor LM, et ál. Differential diagnosis of pain around the hip joint. Arthroscopy. 2008; 12:1407-1421. 14.Beck M, et ál. Hip morphology influences the pattern of damage to the acetabular cartilage. Fe- moroacetabular impingement as a cause of early of osteoarthritis of the hip. J Bone Joint Surg Br. 2005; 87(7):1012-1018. 15.Ito K, et ál. Histopathological features of the acetabular labrum in femoroacetabular impingement. Clin Orthop Relat Res. 2004; 429:262-271. 16.Ganz R, et ál. Surgical dislocation of the adult hip: A technique with full access to the femoral head and acetabulum without the risk of avascular necrosis. J Bone Joint Surg Br. 2001; 83:1119-1124. 17.Lavigne M, et ál. Anterior femoroacetabular impingement. Part I. Techniques of Joint Preserving Surgery. Clin Orthop Relat Res. 2004; 418:61-66. 18.Gautier E, Ganz K, Ganz R, et ál. Anatomy of the medial femoral circumflex artery and its surgical implications. J Bone Joint Surg Br. 2000; 82(5): 679-683. 19.Espinosa N, et ál. Treatment of femoroacetabular impingement: preliminary results of labral refixation. J Bone Joint Surg Am. 2006; 88(5):925-935. 166 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 20.McCarthy J, et ál. Anatomy, pathologic features, and treatment of acetabular labral tears. Clin Orthop Relat Res. 2003; 406:38, 47. 21.Ilizaliturri VM Jr. Complications of arthroscopic femoroacetabular impingement treatment: a review. Clin Orthop Relat Res. 2009; 467(3):760-768. 22.Mardones R, et ál. Surgical correction of cam type femoroacetabular impingement: a cadaveric comparison of open versus arthroscopic debridement. Arthroscopy. 2009; 25(2): 175-182. 23.Sussmann PS, et ál. Arthroscopic versus open osteoplasty of the head neck junction: a cadaveric investigation. Arthroscopy. 2007;23(12): 1257-1264 24.Parvisi J, et ál. Management of arthritis of the hip in the young adult. J Bone Joint Surg Br. 2006; 88(10):1279-1285. 25.Peters CL, et ál. The etiology and treatment of hip pain in the young adult. J Bone Joint Surg Am. 2006; 88(10):20-26. 26.Khanduja V, et ál. Arthroscopic surgery of the hip. Current Concepts and recent advances. J Bone Joint Surg Br. 2006; 88(12):1557-1566. 27.Leuning BM, et ál. Anterior femoroacetabular impingement: part II. Midterm results of surgical treatment. Clin Orthop Relat Res. 2003; 406:38, 47. 28.Mardones RM, et ál. Surgical treatment of femoroacetabular impingement: Evaluation of the effect of the size of the resection. J Bone Joint Surg Am. 2006; 88: 84-91. 29.Tönnis D. Normal values of the hip joint for the evaluation of x-rays in children and adults. Clin Orthop. 1976; 119: 39-47. 30.Zebala LP, et ál. Anterior femoroacetabular impingement: A diverse disease with evolving treatment options. Iowa Orthop J. 2007; 27: 71-81. 31.Parvizi J, et ál. Femoroacetabular impingement. Journal of the American Academy of Orthop Surg. 2007; 15(9): 561-570. 32.Kim KC, et ál. Influence of femoroacetabular impingement on results of hip artrhroscopy in patients with early osteoarthritis. Clin Orthop Relat Res. 2007; 456:128-132. 33.Philippon MJ, et ál. Early outcomes after hip arthroscopy for femoroacetabular impingement in the athletic adolescent patient: A preliminary report. Journal of Pediatric Orthopaedics. 2008; 28(7): 705-710. 34.Philippon MJ, et ál. Arthroscopic Management of femoroacetabular impingement: Osteoplasty technique and literature review. American Journal of Sports Medicine. 2007; 35(9): 1571-1580. 35.Sariali LF, et ál. Femoroacetabular impingement treatment using arthroscopy and anterior approach. Clin Orthop Relat Res. 2009; 467(3):747-757. 36.Graves ML, et ál. Femoroacetabular impingement: do outcomes reliably improve with surgical dislocations? Clin Orthop Relat Res. 2009; 467(3):717-723. 37.Byrd JW, et ál. Arthroscopic femoroplasty in the management of cam type femoroacetabular impingement. Clin Orthop Relat Res. 2009; 467(3):739-746. 167 “Temas selectos de actualización en la Ortopedia Latinoamericana” 168 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Rehabilitación en Artroplastia Total de Cadera Leon Alberto Sardi M.D. Olga Cecilia Suarez F.T. Cali, Colombia INTRODUCCIÓN La intervención rehabilitadora por parte del personal de fisioterapia y Especialista en Actividad Física en los pacientes con reemplazo total de cadera (RTC) se ha fortalecido en los últimos años, sin embargo, persiste el desconocimiento general de las ventajas y desventajas de las técnicas y ejercicios empleados en el proceso rehabilitador. Ese desconocimiento por parte del personal de fisioterapia y actividad física se debe al poco interés manifestado por ellos en relación con el acto y técnica quirúrgica, cuyo conocimiento es de vital importancia para el posterior planeamiento de las actividades físicas a realizar. De igual manera en los cirujanos ortopedistas persiste el desconocimiento de los efectos terapéuticos de las diferentes modalidades físicas y de la gran variedad de técnicas empleadas por el personal de rehabilitación que es parte de un equipo interdisciplinario, cuyo trabajo esta enfocado en la recuperación exitosa de un paciente sometido a la artroplastia total de cadera. (1, 3, 4, 12, 24) Todo paciente al que se le va a realizar una artroplastia total de cadera debe tener un planeo preoperatorio, en el cual es tan importante el examen médico detallado, como la evaluación nutricional, la evaluación antropométrica, y de sus capacidades físicas(1), la educación para el paciente y sus familiares del procedimiento a realizar, y las terapias pre-quirúrgicas encaminadas al fortalecimiento muscular y al mejoramiento de la capacidad cardiopulmonar las cuales inciden en el momento quirúrgico y en la rehabilitación posterior. Todo esto con el fin de que el paciente retome a las diferentes actividades de la vida diaria, recupere su funcionalidad e independencia y de igual manera minimice los riesgos inherentes al procedimiento y evite las complicaciones postquirúrgicas. (3, 4, 12, 24) Por lo tanto es importante tener claro varios conceptos como: • El paciente debe ser atendido de manera individual al momento de realizar la evaluación, el diseño de las actividades físicas y la intervención. Muchos de los 169 “Temas selectos de actualización en la Ortopedia Latinoamericana” individuos que se someten a un RTC tienen una enfermedad de base, como artrosis, secuelas de luxación congénita de cadera, artritis reumatoidea, entre otras; y es en este tipo de pacientes en quienes la terapia se debe individualizar y no puede limitarse solamente a la cadera, sino que se hace indispensable extenderla a todo el aparato locomotor comprometido(7) y al sistema cardiopulmonar. • • 170 Al paciente hay que educarlo y prepararlo para el procedimiento y es fundamental conceder a la concientización y la rehabilitación del paciente, el mismo interés que se otorga a la técnica quirúrgica o al acto operatorio. APOYO: Si la prótesis es NO cementada, el inicio de la descarga de peso se permite en la cuarta semana postquirúrgica de manera progresiva y asistida por caminador o muletas (5,12) Si la prótesis es cementada se permite la descarga parcial de peso en forma progresiva al segundo día del postquirúrgico, asistida por el caminador o las muletas. • Los movimientos contraindicados en las articulaciones sometidos a artroplastia total de cadera varían según el abordaje quirúrgico. Si el abordaje es posterolateral están contraindicados la flexión de cadera mayor a 90 grados, la aducción y la rotación externa. Si el abordaje es anterior los movimientos contraindicados son la extensión forzada, la aducción y la rotación interna. • MODALIDADES: Está demostrado que el uso de la ESTIMULACION ELECTRICA es efectiva en la osteogénesis (25) Por lo tanto su aplicación permite acelerar el proceso de impactación de la prótesis; igualmente ayuda a la disminución del dolor y facilita la desinflamación por el efecto vasodilatador que presentan las corrientes (9, 11, 21) La utilización del ULTRASONIDO esta contraindicado sobre la cadera operada por el efecto vibratorio y térmico que posee. (9, 11, 12, 27) Sin embargo, el empleo de COMPRESAS CALIENTES en el postquirúrgico es permitido después de las primeras semanas. (9, 11, 22) La CRIOTERAPIA, por su efecto desinflamatorio y analgésico (12, 14, 30) es una herramienta empleada siempre en las etapas agudas de cualquier afección o procedimiento quirúrgico. Por ultimo se puede utilizar el LASER, como estimulador de la cicatrización y como vasodilatador, con el fin de acelerar el proceso de recuperación. Sin embargo la fortaleza de la intervención terapéutica esta en la realización de actividad física asistida. La actividad física asistida que se practica en el paciente durante el prequirúrgico va encaminada a mejorar la capacidad cardiopulmonar del individuo, al fortalecimiento de ambas extremidades, al mejoramiento de la flexibilidad y a la disminución de la inflamación y el dolor. Estos objetivos persisten en la fase postquirúrgica, en la cual además, se tiene especial cuidado y por tanto se hace énfasis, en las actividades que favorecen el proceso circulatorio (ejercicios de Buerguer Allen), en la realización de masaje cicatrizal (Técnica de Cyriax), en el fortalecimiento progresivo de toda la musculatura a través de: la autocarga, la resistencia manual, la utilización de theraband brazo de palanca corto, y de técnicas como William´s (trabajo de la región abdominal), Pilates y la gimnasia acuática, entre otras. La Técnica Pilates ha tenido gran acogida en los últimos años en el país y su aplicación en los pacientes sometidos a RTC se fundamenta en los beneficios que ella genera. “Las ventajas de la utilización del método Pilates en la recuperación funcional prequirurgica y postoperatoria, facilitando el retorno Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT rápido al ejercicio en el paciente ambulatorio y la promoción de la participación de todo el cuerpo en el proceso de rehabilitación.(6) Estos beneficios son: • La realización ordenada de una serie de ejercicios que trabajan el cuerpo de pies a cabeza • Alta efectividad por disminuir el total de repeticiones e incrementar el esfuerzo en cada movimiento permitiendo la obtención de resultados rápidos y duraderos. • En cada ejercicio el cuerpo se estira y fortalece, con posiciones que cambian de la postura supino a la sentada y la arrodillada. • La mente se activará durante el ejercicio, desarrollando y aumentando la conciencia del propio cuerpo • Finalmente la técnica Pilates basa su accionar en 6 principios que son: respiración, concentración, control, centro, precisión y fluidez.(35) Con relación a la gimnasia acuática los excelentes resultados obtenidos durante su aplicación en pacientes sometidos a cirugías de RTC tienen en cuentan los conceptos básicos necesarios para la programación de las actividades a realizar además del respeto por el tiempo de descarga, el proceso de cicatrización y los movimientos contraindicados según el abordaje quirúrgico. Además es necesario recordar que la terapia en agua, combina la acción térmica con el ejercicio terapéutico, siendo un método útil para el tratamiento de muchas enfermedades por proporcionar al paciente: relajación muscular, disminución del dolor y de los espasmos, aumento de la circulación, mantenimiento o incremento de la movilidad articular, reeducación muscular (desarrollo de la fuerza y resistencia), entrenamiento precoz de la marcha y la propiocepción, con disminución de la carga articular y muscular, mejorando el estado psicológico y emocional del paciente. (21) En relación con los conceptos básicos de la gimnasia acuática es importante recordar que la temperatura del agua debe ser de 36.5 ºC y el nivel de inmersión basándose en las características químicas, mecánicas y térmicas.(7,8) ya que en el agua el peso corporal presenta los siguientes valores: • 7.5% en inmersión hasta el cuello • 20% en inmersión hasta las axilas • 33% en inmersión hasta el pecho • 50% en inmersión a nivel umbilical • 66% en inmersión a nivel trocantérico • 90% en inmersión hasta las rodillas Teniendo el previo conocimiento por parte del terapeuta de la técnica quirúrgica y de la constante comunicación de éste con el cirujano ortopedista, para lograr una recuperación y funcionalidad mayor en el paciente, se inician los ejercicios de la cadera operada y sus articulaciones vecinas.(7) Recordando que estos ejercicios no sean causantes de dolor (8) y sin olvidar que la principal complicación en los abordajes posterior o posterolateral son las luxaciones de cadera. El propósito de este capitulo es compartir con ustedes la guía que se diseño, para la rehabilitación de los pacientes sometidos al reemplazo total de cadera(31) y con la cual desde hace trece años hemos tenido oportunidad de ayudar al paciente en su rehabilitación, en forma más rápida, efectiva y con la participación activa del individuo. Finalmente se incluirán las modificaciones realizadas con el transcurso del tiempo y las cuales tienen en cuenta los conceptos y actividades de técnicas como Pilates y Gimnasia acuática. 171 “Temas selectos de actualización en la Ortopedia Latinoamericana” 172 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 173 “Temas selectos de actualización en la Ortopedia Latinoamericana” 174 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Con relación a la Técnica PILATES se utiliza la siguiente secuencia de los ejercicios a partir de la segunda semana y se progresa paulatinamente. Es necesario recordar que la técnica se puede aplicar sin olvidar los movimientos contraindicados para un RTC, lo cual implica realizar algunas modificaciones a los ejercicios que se encuentran organizados en cuatro fases: (31) • Programa de Introducción • Programa para principiantes • Programa de nivel intermedio • Programa de avanzado -Los Cien: utiliza los glúteos para crear un sistema de soporte para la zona lumbar. 175 “Temas selectos de actualización en la Ortopedia Latinoamericana” • Círculos con una pierna: SIN realizar la aducción, parte de neutro hacia la abducción. • Estirar una pierna: Es importante recordar que la flexión de cadera solo se puede realizar hasta los 90 grados. • Estirar las piernas: donde el núcleo muscular será la base para que las extremidades se extiendan al mismo tiempo desde el centro del cuerpo. • Estirar la columna. • Pared: sirven para relajar y corrección de la alineación postural. Del programa intermedio se realizan: • Estiramiento de las piernas extendidas Finalmente se pueden realizar diferentes actividades con el aro mágico. Este aro es una herramienta portátil de resistencia compacta y ligera, utilizada para trabajar los músculos de los brazos, piernas y pecho además del núcleo muscular (musculo transverso del abdomen). Como sustituto del Aro, se puede utilizar una pelota de 30 o 40 centímetros de diámetro. De igual manera se especifican a continuación las diferentes actividades realizadas en la GIMNASIA ACUATICA las cuales se realizan de manera progresiva: Ganar Arcos de Movilidad Articular sin apoyo. (3 series de 8 repeticiones). Con una inmersión 75% del peso corporal y estando en posición bípeda realice: • Sierra • Dorsiflexión, plantiflexión, inversión y eversión del pie. • Círculos con el cuello • Flexión y Extensión de rodilla. • Patada con una pierna • Flexión de cadera 40 - 45 grados. • Patada con las piernas sin realizar la posición de descanso. • Abducción de cadera 40 - 45 grados. • Palanca del cuello • De lado se realiza todo las actividades de preparación • De lado al frente • De lado arriba-abajo sin exceder los arcos de movilidad articular permitidos. Del programa avanzado se practican: • De lado subir las piernas • De lado subir la pierna • Transición: taloneo • Natación • Estirar una pierna • La sirena 176 • Flexiones • Extensión de cadera 10 - 15 grados Ganar Fuerza Muscular. (Sostener de 5 a 8 segundos cada ejercicio). • Posición bípeda • Flexión de cadera 40 - 45 grados con rodilla en extensión. • Extensión de cadera 10 - 15 grados. • Abducción de cadera 40 - 45 grados. • Mejorar Propiocepción • Posición bípeda. • Ejercicios con los ojos abiertos y cerrados. • Desplazar con el pie un objeto de un lado a otro. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT • Agarrar objetos con los dedos del pie. Mejorar Flexibilidad • Estiramientos de miembro superior, Gastrosóleos, y cuádriceps. • Estiramientos de aductores en tierra. Isquiotibiales y Posteriormente se disminuye el porcentaje de inmersión, se aumentan los arcos de movilidad articular, las repeticiones, las series y finalmente se realizan ejercicios activos resistidos empleando flotadores y tablas. Por ultimo no se puede concluir este capitulo sin mencionar las diferentes RECOMENDACIONES dadas al paciente y sus acompañantes y las cuales son de vital importancia para la recuperación definitiva del paciente y realización de actividades deportivas de una manera guiada y correcta. El paciente en el postquirúrgico inmediato debe colocar hielo por 10 segundos cada dos horas en la zona operada, colocar una almohada gruesa entre las piernas, (12, 29) no debe rotar la pierna interna o externamente, no debe colocar almohada bajo la cadera y la rodilla operada, debe colocar almohada bajo el tobillo por periodos cortos. No puede apoyar la pierna hasta consultar con el médico tratante o con el terapeuta. No se pude acuclillar, (29) arrodillar (29) o flexionar la cadera por encima de los 90° (12, 29) Debe sentarse en sillas altas donde nunca su rodilla este más alta que la cadera, dormir en cama dura, boca arriba o de medio lado sobre la pierna NO operada y con almohada entre las piernas.(10) Evitar dormir o recostarse sobre la pierna operada. (12, 29) Utilizar calzado cómodo y de tacón bajo con suela antideslizante y sin cordones. No cruce las piernas. (12) Suba y baje las gradas, como le indique el fisioterapeuta. De igual manera debe retirar las alfombras, los cables de los diferentes equipos eléctricos, verificar que no halla líquido derramado a su paso, evitar la ingesta de alimentos grasosos o picantes. La herida SOLO debe ser revisada por la enfermera, terapeuta o el médico tratante. No por familiares o amigos. Las sugerencias hechas por personas ajenas a la salud debe omitirse o consultar con el médico tratante o el terapeuta. Realice los ejercicios indicados para su casa por el terapeuta tres 3 veces al día en series de tres 3 y veinte 20 repeticiones de cada ejercicio.(17) Cuando asista a terapias en consultorios no le deben colocar Ultrasonido ni Diatermia. De igual manera se recomienda al terapeuta físico consultar de manera previa a la intervención cualquier duda que tenga sobre la realización de las actividades y dialogar con el protesista sobre la cirugía realizada al paciente. BIBLIOGRAFÍA 1. Atkinson K, Coutts F, Hassenkamp A M: Physiotherapy in orthopaedics. A problem solving approach. Chapter 8, Pp 221 –226. Edinburgh Churchill Livingstone 1.999. 2. Barrett D, S. Cobb AG, Bentley G: Joint propiception in normal osteoarthritic and replaced knees, journal of bone and joint surgery. 73 B (1) 53- 56. 1.991. 3. Bentley, J.A: Physiotherapy following joint replacement. Cash´s textbook of orthopaedics and rheumatology for physiotherapists. Chapter 22 Pp. 435 – 439. Phyladelphia, American B. Lippincott company. 1.984 4. Bierbaum Benjamin E, Pomeroy Donald L, Berklacich Frank M: Complicaciones tardias del reemplazos totales de cadera. Capitulo 50. 177 “Temas selectos de actualización en la Ortopedia Latinoamericana” 5. Borden Lester S, Greenky Seth S: Reemplazo total de cadera primario dificultoso: Problemas acetabulares. Capitulo 47 PP 1106. 6. Bulletin of the NYU Hospital for Joint Diseases Rehabilitation after Total Hip and Knee Arthroplasty. A new Regimen Using Pilates Training.Volume 65. 2007 7. Case Leanne, Programa Fitness Aguagym. Editorial Hispano Europea. 2001. Capítulo 4; pp: 35-37, 40 – 44, capítulo 5; pp: 57-59 8. Cavicchioli Roberta. La gimnasia en el agua. Editorial del Vecchi, S.A, Barcelona, 1995. Capitulo 1; pp: 14,51 9. Clarke AK, Allard L, Braybrooks BA. Rehabilitation Techniques in Rheumatology. Williams & Wilkins. Philadelphia. pp;177. 1997 10.Corning C, P.T. Therapeutic exercises using resistive bands. Chapter 1 Pp. 83. Verthoud, Colorado 1.998 11. Cotta H, W Herpertz: Clinical handbooks in physical therapy management. Tomo 1 y 2 Pp. 51, 259, 276 Rockwille, Aspen Maryland. 1.987 12.Chandler H.P: Postoperative rehabilitation of the total hip patient. Stability of total hip replacement. Pp371, 401, Philadelphia Grune y Stratton, inc. 1.987 13.Chang, RW: Rehabilitation of the total hip patient. The art of total hip arthroplasty. Pp. 390, 395. Philadelphia, Grune y Stratton, inc. 1.997 14.DeLisa Joel A, Gans Bruce M: Rehabilitation medicine principles and practice rehabilitation of total hip and total knee replacements. Chapter 66 Pp. 1694 – 1689. Philadelphia, Lippincott raven publishers. 1.998 15.Evjenth Olaf, Hamberg Jern: Autostretching. The complete manual specific stretching. Pp. 91 135. Sweden, Alfta rehab forlag, 2nd edition. 1.988. 16.Fernández L de la Peña: Inflamación y dolor. Conceptos básicos de interés en medicina física. Manual de Medicina física. Capitulo 2 Pp. 2. 30. Madrid, Harcourt Brace 1.998. 17.Hyde, S.A: Physiotherapy in rheumatology surgical management of rheumatoid arthritis, Chapter 77 Pp.86. Oxford. Blackwell scientific publitations, 1.998. 18. Knott Margaret, Voss Dorothy E: Facilitación neuromuscular propioceptiva. Patrones y técnicas. Pp. 225, 240. Edición Medica Panamericana. 1.974 19.Lewis Carole B, Knortz Karen A, Kampa Kathy : Orthopedic assessment and treatment of geriatric patient. Chapter 17, Pp. 43 St. Louis, Mosby 1.997 20.Martínez M.(1998)Manual de Medicina Física, Primera edición, Editorial Harcourt Brace, Madrid – España, Capítulo 26; pp. 335 21.McGray B, Stuart M, Sim F: Participation in sports after hip and knee arthroplasty – review of literature and survey of surgeon preferences. Mayo Clinic Proceedings. 70(4): 342- 348. 1.995 22.Nickel, Vernon L, Botte Michael J: Orthopaedic rehabilitation. Chapter 55, Pp.779 Churchill Livingstone, New York. 1.998 23.Ochoa del Portillo G,: Principios generales en electroterapia. Pp. 5 – 100 Bogotá D. C. Boehringeer Ingelheim, Servicio médico de Post grados. 1.984 178 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 24.Pastor Vega J. M: Termoterapia. Manual de medicina fisica. Capitulo 6 y 7 Pp. 73 – 104. Madrid Harcourt Brace 1.998 25.Posner– Mayer Joanne: Swiss Ball aplitations for orthopedic and sports medicine First edition. Chapter 2, 3 Pp. 128, 131. Ball dinamics international. Colorado. 1.995. 26.Ranawat, Chitranjans, Figgie Mark P: Complicaciones tempranas del reemplazo total de cadera. Capitulo 49 PP. 1132 – 1134. 27.Rosenberg Aaron, Galante Jorge: Reemplazo total de cadera no cementada. La cadera : Diagnóstico y tratamiento de su patología. Capitulo 46 Pp. 1062. Steinberg, Edición Panamericana. 28. R. Grunig, E Morscher, P.E Ochsneer: Three to seven year results with the uncemented SL femoral revision prothesis. Arch orthop. Trauma surgeon. Chapter 116, Pp 187 – 197. Springer Verlag 1.997 29.Sánchez Oton C, Hernández Enrique, Sabaté Bel M: Ultrasonido terapeutico. Manual de medicina física. Capitulo 16, 17. Pp. 210, 231. Madrid. Harcourt Brace. 1.998 30.Sánchez J. Borrajo, Flórez C Rodríguez, López Rubio I, Sánchez Redondo E: Corrientes de alta frecuencia. Onda corta. Manual de medicina física. Capitulo 16, 17 Pp. 210- 231. Madrid. Harcourt Brace. 1.998 31.Sardi León. Suárez Olga. Rehabilitación en el Reemplazo Total de Cadera. Revista Colombiana de Ortopedia y Traumatologia. Volumen 18 Numero 2. 2004 32.Shankman, Gary A: Fundamental Orthopedic Management for the Physical Therapist Assistant. Chapter 14 Pp. 198, St Louis. Mosby. 1.997 33.Sierra Gabriel Ma del R: Fisioterapia y dolor. Fisioterapia en Traumatología, Ortopedia y Reumatología. Capitulo 1 Pp. 16, 18. Springer Verlag. Iberica S.A. Barcelona. 1.997. 34.Shankman, Gary A: Fundamental Orthopedic Management for the Physical Therapist Assistant. Chapter 14 Pp. 198. St. Louis. Mosby. 1.9 35.UNGARO. A. Pilates. Un programa de ejercicios para controlar todos los movimientos musculares. Ed. B. S. A. Barcelona 2002 179 “Temas selectos de actualización en la Ortopedia Latinoamericana” 180 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Artroplastia Total de Cadera en Pacientes con Displasia Residual y/o Luxación Inveterada de Cadera Nicolás Restrepo Giraldo M.D. Hospital Universitario Departamental de Nariño E.S.E. Clínica de Reemplazos Articulares, Clínica Los Andes Pasto Colombia INTRODUCCIÖN Desde los primeros albores de la Artroplastia, incluso mucho antes de que Sir John Charnley popularizara la técnica, este procedimiento fue destinado únicamente a pacientes mayores, generalmente con más de 60 años, con Artrosis, Artropatías Reumatoideas u ocasionalmente postraumáticas, dejando de lado por lo general, a pacientes jóvenes, frecuentemente con Displasias residuales severas del desarrollo de la Cadera y más aún, aquellos que nunca recibieron tratamiento, pues las complicaciones técnicas, según el mismo Charnley hacía que no fuera recomendada para este último tipo de pacientes. (1,2) Sin embargo y con el tiempo, la Artroplastia se ha convertido en uno de los procedimientos de la medicina más costo/ efectivos, lo cual ha hecho que sus indica- ciones hayan crecido, la industria se haya volcado a solucionar los problemas metalúrgicos y de diseño para mejorar la sobrevida; de igual manera los mismos pacientes, cada vez más informados por Internet, indagan, solicitan y ocasionalmente exigen una solución a su problema displásico, decididos a tener una mejor calidad de vida en su época más productiva; es así como pacientes jóvenes con Luxación inveterada o caderas altas producto de no haber recibido tratamiento oportuno en su infancia, consultan para lograr una mejor calidad de vida, disminuir la cojera, el acortamiento y su incapacidad funcional. Las condiciones socio/económicas de nuestro país, hace que encontrar pacientes jóvenes con Displasia residual o Luxación Inveterada sea algo muy frecuente en nuestra consulta, por lo que el Especialista de Cadera debe conocer 181 “Temas selectos de actualización en la Ortopedia Latinoamericana” y saber enfrentar este reto, definitivamente raro en países más desarrollados, que cuentan con mejor prevención de la displasia en el recién nacido; el entender el conjunto de cambios anatómicos derivados de su patología, realizar un adecuado planeamiento que incluya la escogencia del implante, de la técnica quirúrgica y de su perioperatorio, harán que los resultados puedan igualar a los desenlaces típicos del paciente añoso con patología artrósica. En 1975, Raymond G, Tronzo y Okin (3), publican en el Clinical Orthopedics and related research el resultado de 27 caderas en 19 pacientes, aquejados por displasia severa o luxación, siendo mucho más optimistas, pues todos sus pacientes mejoraron la marcha, la cojera de Trendelemburg, logrando ecualización en el 82% de los casos variando el alargamiento entre 2,5 y 6,0 centímetros y mejorando en la Escala de Harris de 20,2 a 94,6 (2). EVOLUCIÓN HISTÓRICA Uno de los primeros artículos que trata sobre el tema, es el publicado por Charnley y Feagin en 1973 (1) evaluando los resultados a 10 años de 6000 caderas de las cuales sólo 96, es decir el 1,5 % tuvieron diagnostico de displasia residual; en él refieren cómo estos pacientes presentan “profundos cambios anatómicos y biomecánicos que obligan a conservar el máximo de sustrato óseo, previniendo complicaciones futuras, que ameriten revisión”. Como política institucional en esa época el autor terminaba por recomendar “no intentar este tipo de intervención en caderas crónicamente dislocadas, ya que los riesgos son demasiado extremos para este tipo de cirugía, que dan más riesgos y dificultades técnicas que las que el grado de incapacidad garantiza”. Posteriormente en 1976, los Doctores. Harold Dunn y Wallace E. Hess (4), publican su experiencia en 16 pacientes con 22 caderas crónicamente luxadas y seguimiento promedio de 22 meses. El manejo que vale la pena resaltar de estos autores es el de realizar una osteotomía del trocánter mayor mas una osteotomía oblicua de la zona metafisaria para adaptar un tallo recto (Figura 1), aunado al concepto de medialización o técnica de seudoprotrusio para “aquellas caderas en que no exista buena cobertura acetabular, ya que la débil y delgada pared medial se rompe para permitir el desplazamiento hacia medial del componente”, para lo cual colocan injertos en el defecto y lo refuerzan con una malla de alambre y metilmetacrilato, dejando la periferia acetabular intacta, como se muestra en la figura. En sus Figura 1. Técnica femoral de Dunn & Hess 182 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT casos utilizaron prótesis hechas a medida y cabezas de 26 milímetros. En Septiembre de 1977, William H. Harris, Omar Crothers y Oh, (5) publican su clásico artículo donde muestran la técnica de aumentación de la porción supero/ externa deficiente en estos acetábulos con auto injerto de la misma cabeza femoral resecada. La cabeza femoral se talla para cubrir el defecto creado por el ascenso de la cabeza femoral en el iliaco, su superficie se escarifica y se coloca en esta posición para permitir un fresado aumentando la superficie de cobertura en la zona de carga del techo acetabular, como se aprecia en la (Figura 2). Figura 3. Técnica de artroplastia con medialización. Figura 2. Ejemplo de descenso más injerto súpero-externo en techo acetabular. En Octubre de 1978 es nuevamente el Dr. Hess, en compañía de James S. Umber, (6), quienes recopilan sus casos de artículos anteriores y estandarizan la técnica de fractura controlada de la pared acetabular y encaje del componente acetabular mediante medialización o seudoprotrusio y apoyo periférico de una copa tipo Aufranc/Turner, como podemos ver en la (Figura 3). Para finales de los 70, la literatura ortopédica tenía autores de renombre como Wagner, Efthekar o Stinchfield e incluso el mismo Charnley, que mostraban su preocupación e interés por el manejo de la cadera displásica, mediante la Artroplastia (7, 8, 9, 10, 11, 12). Para 1979, el Dr. Ranawat, junto con sus residentes (Crowe), publican su clasificación de las caderas congénitas que permitirá estandarizar diferentes artículos que muestran cómo va mejorando los desenlaces en pacientes jóvenes (13, 14, 15, 16, 17, 18, 19, 20, 21). En Febrero de 1988 los doctores Frank Linde, Jorn Jensen y Pilgaard, publican una larga serie seguida a lo largo de trece años, en total 124 Artroplastias en 99 pacientes, que permite demostrar una supervivencia acumulada a 5 años del 93%, a 10 del 89% y a 15 años del 80%, pero con una diferencia notoria y estadísticamente significativa entre aquellas caderas colocadas en el acetábulo original o muy cercanas al mismo (13%), comparado con aquellas colocadas proximales al techo del verdadero acetábulo (42%) (22). En ese mismo año, Hartofilakidis y Stamos, presentan su trabajos, así como su clasificación que será la que predomine en los siguientes trabajos, principalmente europeos (23, 24, 25, 26, 27, 28, 29) 183 “Temas selectos de actualización en la Ortopedia Latinoamericana” Ya empezando la década de los 90, el Dr. Paavilainen de Helsinki publica en el Journal Británico un estudio de 100 caderas utilizando la prótesis no cementada de cobertura madrepórica de Lord (30, 31), divididos en dos grupos dependiendo de si necesitan o no diafisectomía femoral de acortamiento. En el grupo donde no utilizaban diafisectomía preferían el abordaje posterior de Moore, mientras que si consideraban un avance del trocánter mayor y/o diafisectomía, preferían el abordaje de Hardinge. Salen a la luz, artículos con desenlaces a largo plazo en pacientes menores de 45 años con Displasia (32, 33, 34, 35, 36) El Doctor Daniel J. Berry habló sobre “Artroplastia Total de Cadera para Displasia y Subluxación: Indicaciones y Consideraciones técnicas” en el meeting de la Academia Americana de Ortopedistas en Dallas (2002). En su artículo (37), hace un recuento del estado del arte en lo que a este tópico se refiere; de igual manera, enumera los principios de tratamiento convencionales que son: • La reconstrucción acetabular en la posición original anatómica, de ser posible con un implante no cementado. • De ser necesario, utilizar auto-injerto en la porción antero lateral del acetábulo • Reservar el centro rotacional alto sólo con grandes erosiones laterales del acetábulo original, donde el acetábulo esté apoyado en su mayor parte en el injerto. En términos generales, habla poco acerca del manejo femoral, y considera necesario la osteotomía, tallos porosos totales o modulares, para corregir la severa anteversión que hace inestable el implante. La segunda parte a considerar, fue expuesta y su resumen escrito por Charles 184 Engh Jr., Titulado “Artroplastia Total de Cadera en pacientes con Luxación Alta”; (38). En cuanto a las indicaciones quirúrgicas, este autor las amplía, no reservándose únicamente a la severa limitación funcional y/o dolor, ya que considera pertinente su realización cuando existe: • Dolor, disfunción y falla de tratamientos no quirúrgicos. • Dolor más en nalgas, que en la ingle o región anterior. • Fatiga muscular dolorosa con la actividad, más que dolor agudo con la movilidad bien sea pasiva o activa. • Síntomas asociados en columna y/o rodilla. • Casos unilaterales que son más sintomáticos. Los casos bilaterales, a menudo pasan inadvertidos o con pocos síntomas, por lo que en términos generales, estos si requieren cirugía, con frecuencia es tardía. A partir de este siglo, podemos encontrar en la literatura, gran número de buenas series en las que, gracias a la metalurgia actual y los avances en la comprensión de la anatomía y biomecánica, muestran desenlaces similares a las cohortes de caderas artrósicas (39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60). Para ese mismo tiempo, la literatura nacional presenta los trabajos de las series iniciales del autor, con diseños de prótesis híbridas (61,62), al no contar con tallos no cementados pequeños, que manejen las pequeñas medidas comparativas de nuestros canales femorales, comparados con los canales displásicos americanos o europeos que se presentan en otras series (63, 64, 65, 66, 67, 68, 69, 70, 71, 72) Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT CAMBIOS ANATOMICOS EN LAS CADERAS DISPLASICAS CAMBIOS OSEOS En la medida que la cabeza femoral va migrando proximalmente hacia la subluxación en el acetábulo infantil, se van creando acetábulos oblongos, con rebordes que van estrechando el espacio libre articular; es así como encontramos un verdadero acetábulo muy plano, inclinado y poco profundo, casi vertical en ocasiones, que impide profundizar una copa protésica. Cuando la cabeza crea un falso acetábulo, con frecuencia existe un engrosamiento cortical entre los dos acetábulos, que de no resecarse, hará difícil la profundización acetabular al intentar usar como techo para la colocación del implante en el acetábulo original. Figura 4. Alteraciones femorales La cabeza femoral con frecuencia es pequeña, ovalada y deforme, tratando de adaptar su forma con la congruencia articular; con frecuencia encontramos osteofitos cervicales inferiores, o hipertrofia del trocánter menor, que tratan de servir de apoyo en esta cadera insuficiente y que debemos resecar, al ser causa de pinzamiento y luxación de nuestro implante durante la aducción. (2, 5, 11, 12) El cuello femoral con frecuencia es corto, ancho, de corticales engrosadas y generalmente con grados variables de anteversión; Tal vez la implicación anatómica más importante a nivel femoral sea su estrecho canal que en nuestro medio alcanza un promedio de 7 a 8 milímetros, cada vez más hipoplásico entre más alta sea la luxación y menos carga haya recibido esa cadera; características se ejemplifican en las (Figura 4 y 5). CAMBIOS EN TEJIDOS BLANDOS Con el ascenso y migración cráneo/ externa del fémur, todas sus inserciones musculares estarán acortadas y deformadas; es así como encontramos un mecanismo abductor corto, que ha migrado hacia posterior lo que lo hace muy débil, con una Figura 5. Cambios acetabulares. desventaja mecánica notoria. El ligamento redondo se puede encontrar elongado y es útil en las caderas ascendidas, donde nos puede servir como reparo y guía para encontrar el acetábulo original, como se aprecia en la (Figura 6). La cápsula articular, en la medida que la cadera se asciende, se va engrosando y crea recesos y adherencias a una amplia zona acetabular, que deben ser resecadas de manera cuidadosa para permitir el descenso en el momento de trabajar un implante y quererlo posicionar en el acetábulo original. (8, 12, 17, 18) 185 “Temas selectos de actualización en la Ortopedia Latinoamericana” 3. Arco De Shenton/Menard. En las caderas displásicas, este arco se ve afectado por el ascenso, lateralización y/o anteversión femoral. De igual manera nos permite evaluar el ascenso en milímetros desde el acetábulo original. Figura 6. Ligamento redondo elongado, guía al verdadero acetábulo. ANALISIS RADIOLOGICO DE LAS CADERAS DISPLASICAS Los estudios radiológicos simples nos brindan una ayuda invaluable, al mismo tiempo que nos permiten estandarizar los hallazgos al momento de realizar estudios comparativos y analizar resultados de una técnica específica; las medidas más utilizadas son (23, 26, 30): 1. Angulo Acetabular De Sharp. normalmente este ángulo, que en promedio es de 33º a 42º, se encuentra aumentado y en ocasiones es difícil de evaluar por la mala formación de la gota de lágrima y/o por la unión del falso con el verdadero acetábulo. Sin embargo es un reparo útil que nos indica la continencia y orientación de las paredes acetabulares. 2. Profundidad Acetabular. La medida promedio en las caderas normales es de 40 milímetros, mientras que en las caderas displásicas rara vez alcanza los 20 milímetros; esta medida nos da una indicación real de la insuficiencia acetabular a nivel del techo, siendo la norma el requerir algún tipo de aumento en aquellos acetábulos con profundidades menores a 20 milímetros, bien sea injertos cráneo/externos o medialización. 186 4. Diametro Del Canal Femoral Intramedular. Es la medida en milímetros, del canal medular en su zona más estrecha o istmo, tomada tanto AP como lateral; en los pacientes displásicos generalmente es menor de 12 milímetros y en nuestro medio el promedio es de 8 milímetros, haciendo imposible utilizar vástagos normales de las prótesis que generalmente tenemos en el mercado. 5. Indice Morfológico/Cortical. Sirve para evaluar la morfología del fémur proximal en relación con sus corticales; Lawrence Dorr lo ha simplificado dando a conocer tres tipos de canales femorales: el Tipo A o normal, que es infundibuliforme, el B o en copa de champaña que es más triangular y el C o cilíndrico (en tubo de chimenea), que permiten evaluar qué vástago se ajusta más a cada tipo de canal. 6. Acortamiento Radiográfico. Es la medida perpendicular tomada entre la línea Bi-isquiática y la parte más distal del trocánter menor; nos permite planear la compensación de la anisomelia y/o los recursos técnicos como osteotomías. 7. Angulo Cervico/Diafisario. Se relaciona aquí, pues es importante recordar que con frecuencia las caderas son muy anteversas, asociadas con varo o valgo, lo que agrega un factor más de inestabilidad, al enfrentarnos a este tipo de pacientes. Algunas de estas medidas, se pueden apreciar en la (Figura 7). Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT verdadera posición del acetábulo. La utilidad del TAC, radica en poder evaluar la continencia y suficiencia de las paredes, ya que en estos casos, por lo general, la pared anterior es insuficiente y si empezamos a fresar en esa posición, acabaremos por destruir el acetábulo original; la figura 8 muestra cómo debemos aprovechar un acetábulo displásico para obtener la mejor cobertura sin dañar la pared anterior. Figura 7. Profundidad acetabular, Shenton y otras medidas radiológicas OTROS ESTUDIOS Con frecuencia encontramos en nuestros pacientes algún tipo de sobre crecimiento compensatorio de la extremidad acortada que hace que incluso haciendo osteotomías de más de dos centímetros, se obtenga una ecualización de la anisomelia. Para este fin, es pertinente un test de farill o una goniometría radiológica o por TAC, para evaluar de manera real la diferencia de longitud en la extremidad afectada (32, 37, 38, 61, 62, 63). Cuando nos enfrentamos a un acetábulo muy plano o poco profundo, puede ser de utilidad una Tomografía Axial, pues nos permite evaluar la verdadera profundidad acetabular en cada pared, así como la A pesar de tener nuevos recursos como reconstrucción tridimensional por Tomografía o Resonancia, estos son procedimientos diagnósticos de exclusión, recomendados específicamente según el caso en particular (61, 62). EVALUACIÓN CLÍNICA Y PARACLÍNICA El paciente que consulta por una Luxación Inveterada de cadera alta, es generalmente un paciente muy joven, muchas veces con historia de innumerables procedimientos quirúrgicos fallidos en su infancia, o bien, un paciente más maduro, entre la cuarta a quinta década de su vida, que nunca tuvo tratamiento médico y que ahora, por su actividad, presenta dolor en su columna, rodillas y en la cadera afectada. Es muy importante tomarse su tiempo en la consulta con este tipo de pacientes pues deben tener muy claro al salir de la misma Figura 8. Acetábulo displásico y forma de fresar adecuada. 187 “Temas selectos de actualización en la Ortopedia Latinoamericana” que, de requerirse este tipo de cirugías, nunca debe realizarse por estética, prometiendo que sus extremidades se ecualizarán y que la cojera desaparecerá del todo; así mismo debe conocer y ser consciente de los mayores riesgos inherentes a las deformidades adquiridas que debemos solucionar en el momento de realizar esta artroplastia. Como se dijo anteriormente, ya en la anamnesis, es importante saber si el paciente fue sometido previamente a intervenciones quirúrgicas y de qué tipo; si aún tiene material de osteosíntesis que pueda hacer más difícil el procedimiento quirúrgico, ya que con frecuencia el material colocado y no retirado está cubierto por hueso, o el diseño del material ya no se utiliza, obligándonos a conseguir atornilladores o equipos especiales para lograr finalmente su extracción. De igual manera, es muy importante evaluar a la inspección las cicatrices quirúrgicas, qué abordajes se utilizaron para planear el nuestro. Debemos cuantificar de igual manera, la anisomelia real y planear según la conformación general femoral, si requerirá osteotomía de acortamiento o no, y de qué tipo (52, 63, 68). Con frecuencia en el primer examen puede pasar inadvertida la deformidad adaptativa que estos pacientes tienen en rotación externa y valgo de su pierna, ya que por el acortamiento su marcha es en punta de pie y con rotación externa; es muy importante mostrarle al paciente esta deformidad, y aclararle que es prequirúrgica, pues una vez restituida en el acetábulo original, el eje mecánico tiende a medializarse, haciendo mucho más evidente e incluso a veces, discapacitante, esta deformidad en valgo de su rodilla. CLASIFICACIÓN Y ESTADIAJE Siempre se ha dicho que una clasificación es útil, solamente si nos permite definir una 188 conducta terapéutica y da un valor pronóstico. Para tal fin, existen diferentes clasificaciones cuyo fin primordial es diferenciar si la cadera ocupa parcialmente el verdadero acetábulo, si está alojada en un falso neoacetabulo o si está tan alta, que está libre en los tejidos blandos del alerón iliaco. Las clasificaciones más utilizadas son las de Crowe y Ranawat, la de Hartofilakidis y la de Alan Gross; tienen en común el diferenciar si una cadera conserva algo de relación con el acetábulo original, o si por el contrario se aloja en otro acetábulo completamente formado diferente al real o incluso más alto, simplemente entre los tejidos blandos de la pelvis (13, 23, 30, 31, 32, 45, 62). CLASIFICACION DE CROWE De acuerdo con lo enunciado en su artículo de Enero de 1979, lo dividen en cuatro grupos (13), como se aprecia en la figura 9. Grupo I: Subluxación de menos del 50% Grupo II: 50 a 75% de la subluxación Grupo III: 75 a 100% de la luxación Grupo IV: Más del 100% de la luxación CLASIFICACION DE HARTOFILAKIDIS Publicada en Marzo de 1988 en el Journal Británico, divide en 3 grandes grupos las caderas displásicas (23): • Cadera Displásica: Contenida en el acetábulo original. • Luxación Baja: el borde inferior del falso acetábulo contacta el borde superior del verdadero acetábulo • Luxación alta: No hay contacto entre el verdadero ni el falso acetábulo CLASIFICACION DE ALAN GROSS A. Cadera en el verdadero acetábulo, displásico, elongado que generalmente Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT D. Luxaciones altas, localizadas en tejidos blandos (37, 61, 62, 63) Lo importante de estas clasificaciones es que nos permitan evaluar el verdadero daño y los cambios anatómicos que generan dificultad a la hora de realizar este procedimiento, al mismo tiempo que nos dan una idea de la necesidad o no de osteotomía femoral para logra el descenso al acetábulo original. Figura 9. Clasificación de Crowe. OPCIONES QUIRURGICAS EN EL MANEJO ACETABULAR Sea el abordaje escogido o preferido para manejar una cadera displásica o luxada, lo primero que se debe realizar es una completa y adecuada capsulectomía, que no sólo facilitará el descenso de la cadera al acetábulo original, sino que ampliará y mejorará la visualización de las paredes y la zona de carga. Al enfrentarse al acetábulo displásico, podemos encontrar diferentes escenarios que nos harán decidir entre las posibles opciones quirúrgicas, adecuadas para el manejo acetabular (4, 5, 6, 11, 32): Figura 10. Luxación baja y alta se comporta de manera similar a una cadera centrada al momento de ser trabajada. B. Cabeza femoral subluxada, con su centro compartiendo el acetábulo original; técnicamente es difícil ya que existe un acetábulo alargado, corto y deficiente con poca profundidad acetabular, y no es fácil evidenciar donde termina o comienza el verdadero y falso acetábulos C. Cabeza femoral luxada, que no comparte el acetábulo original; generalmente existe un engrosamiento entre los dos acetábulos, que resecandolo, facilita el posicionamiento. • Colocación del implante en el acetábulo original • Medializar nuestro implante (Seudoprotrusio) • Injertos de aumentación supero/externa • Utilizar un centro rotacional alto • Utilización de copas “Jumbo”. • Utilización de anillos y cajas 1. Reconstruccion En El Acetabulo Original. Aunque muchas veces, es la opción técnicamente más difícil de lograr, es la más anatómica, preserva la mayor cantidad de hueso periacetabular, y por consiguiente la que mejor ventaja biomecánica puede tener, obteniendo la mejor sobrevida 189 “Temas selectos de actualización en la Ortopedia Latinoamericana” en los estudios a largo plazo; Para tal fin, debemos ceñirnos a un estricto protocolo previamente comentado y común a todas estas caderas que incluirá: • Perfecta exposición • Resección capsular • Resección Osteofitos (central e inferior) • Identificar el ligamento trasverso • Identificar trasfondo • Evaluar paredes • Decidir dónde colocarlo Es importante en nuestro planeamiento pre quirúrgico, conocer medidas como la profundidad acetabular y la continencia de las paredes, ya que de acuerdo con estas mediciones, debemos ir preparados a complementar la colocación en el verdadero acetábulo con técnicas que mejoren la cobertura de la copa, como injerto supero externo o la misma medialización o sesudo Protrusio. Se evidencia un ejemplo de descenso al acetábulo original en la (Figura 11). algún Figura 11. Descenso al acetábulo original soporte óseo supero/externo, impiden que la copa de menor tamaño quede bien cubierta; para este tipo de casos se ideó la posibilidad de hacer una fractura controlada del acetábulo, de tal manera que permita hacer una técnica de seudo/protrusio, colocando la copa en el acetábulo original y quedando bien cubierta. La filosofía de la técnica se basa en el hecho de que podemos dejar descubierta una copa un 20% y de todas maneras obtener una adecuada fijación; sin embargo cuando existe un porcentaje mayor, la decisión está entre colocar una aumentación supero-externa con la misma cabeza femoral o profundizarla según la técnica clásica de Hess y Umber (6); en este tipo de pacientes, con relativa frecuencia encontramos una cabeza femoral tan pequeña y deforme que es insuficiente para ser utilizada como injerto de techo, lo cual nos obligaría a utilizar aloinjertos; sin embargo, para coberturas mínimas donde exista entre un 20 a un 40% de descubrimiento, si realizamos una pequeña medialización, podemos lograr una cobertura del 80% con un buen apoyo en el anillo periférico. En estos casos, trabajamos el trasfondo con reamers pequeños y progresivamente vamos debilitando la pared medial, vigilando cuidadosamente las paredes anterior y posterior. Una vez logramos fresar hasta logra el cubrimiento deseado, utilizamos esta papilla producto del fresado para colocarla en el defecto. Muchos autores, para evitar la fractura y protrusión intrapélvica de la copa, prefieren colocar dos tornillos de fijación a pesar de obtener adecuado press fit. Figura 11. Descenso al acetábulo original 2. Medializar Nuestro Implante. En ocasiones nos enfrentamos con acetábulos planos y poco profundos que incluso colocando 190 Es importante recalcar que medializaciones mayores, afectan el offset y la biomecánica de la cadera que vamos a implantar, llegando a producir desventaja mecánica y aumentar los riesgos de luxación por pinzamiento, cosas que se deben Figura 12. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Figura 12. Ejemplo de medialización. seguidores de esta técnica, tiene su filosofía básica el ser lo menos agresivos con una cadera joven y restituir el máximo de aporte óseo, necesario siempre en caso de una futura revisión; para los detractores, muchos de estos injertos realmente no cubren un gran porcentaje siendo innecesarios ya que una copa puede quedar descubierta el 20% del que hablamos anteriormente, mientras que en defectos grandes, corremos el riesgo de dejar apoyada la copa en una superficie mayor del 40% en el injerto, lo que puede determinar su resorción y posterior aflojamiento (Figura 13). Ejemplo de medialización. tener en cuenta al momento de planear nuestra cirugía. En la (Figura 12) apreciamos una medialización con cura y osificación del trasfondo sobre el implante. 3. Injertos de Aumentacion Supero/ Externa. Con Mucha frecuencia y una vez colocado el implante de prueba en el acetábulo original, nos damos cuenta que el cotilo final quedará descubierto en más de un 20%, lo cual a futuro, puede afectar la sobrevida de nuestro implante. Para mejorar este problema, si contamos con una cabeza de tamaño adecuado o bien un aloinjerto de cabeza femoral, se debe disecar y escarificar el borde superior y externo donde termina el acetábulo y se moldea la cabeza femoral, generalmente haciendo una típica forma de siete (7) invertido, que se coloca en dicha zona tratando de hacer coincidir la dirección trabecular y se fija provisionalmente con clavos de Kirschner siguiendo el eje de carga de la cadera, como lo recomendaba en su publicación William Harris y Crothers (5). Se procede a cambiar secuencialmente los Kirchner por dos tornillos de esponjosa que permitan compresión inter-fragmentaria o bien de cortical, labrando la porción proximal con broca mayor para permitir la compresión ínter fragmentaria según los principios y técnica de la A.O. Para los Figura 13. Injerto súpero-externo. 4. Centro Rotacional Alto. Descrito y defendido por Harris (27), que debe ser tenido en cuenta en nuestro armamentario sólo para aquellos pacientes con baja demanda, secuelas de luxo fractura y/o revisiones en pacientes que por su estado general, no toleren una adecuada reconstrucción. El centro rotacional alto, es decir, dejar la cadera alta, generalmente en el falso acetábulo, no corrige la desventaja biomecánica, la discrepancia de longitud de la extremidad, la cojera, ni los cambios que por estos problemas se generen en las articulaciones vecinas y la Columna Lumbosacra; de igual manera, la mayoría de las veces, las paredes del falso acetábulo son muy delgados y corticalizadas, lo que no permite 191 “Temas selectos de actualización en la Ortopedia Latinoamericana” una buena osteointegración de la copa. En la (Figura 14) mostramos dos caderas con centros rotacionales altos, leve y otro con la copa colocada en el falso acetábulo. Figura 14. Centro rotacional alto. 5. Copas Jumbo. Denominadas así por ser de un tamaño mucho mayor al habitual, son útiles para cubrir defectos producidos por acetábulos ovalados, elongados o neoacetábulos que comunican y prácticamente se continúan con el acetábulo original, como se aprecia en la figura 15. fresas grandes para unir las dos cavidades acetabulares, teniendo cuidado de mantener al máximo posible las paredes acetabulares, para lograr una adecuada continencia; en general, se prefiere colocar el producto del rimado en las zonas deficientes generadas por esta técnica, y dar una fijación inicial adicional mediante la colocación de tornillos (63). 6. Anillos y Jaulas. Es el método preferido por algunos autores, con severos detractores en su otra parte. Para su colocación debemos tener en cuenta las especificaciones de cada implante en particular, que obliga generalmente a fresar 4 o más milímetros para lograr su adecuado ajuste (32, 37, 38). De todas maneras, es importante tener en salas de cirugía implantes de este tipo, pues con frecuencia, a pesar de planear nuestra cirugía, la calidad ósea puede hacer que se presenten grandes pérdidas que obligan a contar con este método como un recurso útil en caso de que nosotros produzcamos lesiones importantes en la pared medial o parciales en alguna columna. La figura 16 muestra una solución artroplástica con injertos y el uso de un anillo tipo Müller. Figura 15. Copa “Jumbo” uniendo acetábulo elongado. En este caso, se prefiere resecar primero el hueso cortical duro que une los dos acetábulos y empezar a raspar el hueso con 192 Figura 16. Artroplastia con anillo. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT OPCIONES FEMORALES EN LAS CADERAS DISPLASICAS Con frecuencia, si el acetábulo representa un verdadero reto técnico, las alteraciones femorales producto de los cambios adaptativos que optimicen la carga, nos enfrentan a severas deformidades en pacientes con canales anteversos y estrechos. En los primeros años de utilización de las artroplastias, donde existían pocas opciones, el enfoque dado al problema era netamente Ortopédico, es decir, adaptando el fémur al implante disponible; para tal fin, destruíamos el fémur y sacrificábamos una parte importante del mismo, con tal de adaptarlo al implante disponible (1, 8, 10). Posteriormente, con los avances metalúrgicos, se empezaron a fabricar prótesis “A medida” o “custom made”, que pretendían dar un enfoque mecánico al problema, adaptando la prótesis a la conformación del canal femoral (14, 16, 18). Surgen así, diferentes tipos de tallos rectos, CDH para caderas displásicas y nace con ellos una nueva filosofía que es la que se maneja en la actualidad cuyo enfoque biológico pretende solucionar el problema en estos pacientes jóvenes que casi con seguridad requerirán una futura revisión, tratando de preservar el máximo de sustrato óseo. De acuerdo a la severidad de la lesión, su anisomelia y el tipo de canal, podemos en la actualidad intentar descender estas caderas al acetábulo original sin osteotomía, con osteotomía subtrocantérica proximal o con osteotomía supracondílea o distal (32, 37, 38, 61). 1. Descenso sin Osteotomía. Se puede realizar en aquellas caderas, generalmente Crowe II o III, que luego de colocar el acetábulo y trabajar el canal femoral, realizando la prueba reduce sin tensión y mantiene su estabilidad. Ocasionalmente existe tensión que con tenotomías se puede aliviar progresivamente hasta poder descender la cadera, por lo que se recomienda, de ser este el caso, el empezar realizando tenotomía del Psoas, posteriormente de glúteo máximo y ocasionalmente de los aductores, hasta lograr la reducción. En el post operatorio inmediato, se recomienda siempre dejar la cadera y rodilla en flexión, con el ánimo de disminuir la tensión del nervio ciático. Algunos autores, utilizan tallos rectos y van resecando fémur medial incluso por debajo del trocánter menor hasta lograr el descenso y reducción pero a costa de dejar un trocánter mayor muy alto, con relaciones artículo-trocantéricas muy negativas, que no mejoran la ventaja biomecánica y por ende, mantendrán la cojera. 2. Descenso Con Osteotomia Proximal Subtrocanterica. Considerada en la actualidad como estándar de oro, existen infinidad de osteotomías: trasversas, oblicuas, escalonadas, así como métodos de fijación, desde simples cerclajes hasta las nuevas placas LCP de agujeros combinados y tornillos unicorticales romos. La idea con este tipo de técnica, es medir y hacer una osteotomía subtrocantérica, prefiriendo tallos de cobertura porosa total o por lo menos fijación proximal metafisaria que alcance a tomar toda la parte proximal a la osteotomía. En ese punto se trabaja la porción proximal con las fresas, se hace una reducción provisional y colocando el fémur distal a ese nivel, se tracciona para evaluar la cantidad de hueso a resecar, así como la rotación y anteversión necesarias. Se realiza la resección, se marca el nivel para corregir la anteversión y se trabaja el fémur distal con las raspas necesarias para obtener la fijación. En ese punto se coloca el implante definitivo y se mantienen los dos fragmentos mientras el vástago pasa y toma las dos porciones del fémur osteotomizado. Las figuras 17 a 21, muestran los pasos relevantes de la técnica. 193 “Temas selectos de actualización en la Ortopedia Latinoamericana” Figura 17. Abordaje amplio, medición zona de osteotomía Figura 18. Trabajo con raspa de la porción proximal femoral Figura 19. Medición de la cantidad a resecar en foco de osteotomía. 194 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Figura 20. Trabajo con raspas del segmento distal de la osteotomía. Figura 21. Reducción de la osteotomía subtrocantérica con el vástago femoral. Ideales en tallos de configuración rectos, donde una resección no afectará de mayor forma la fijación de nuestro implante en las dos porciones, no así lo considera el autor con los canales normales o en champaña, debido a la notoria diferencia del diámetro endóstico al resecar un fragmento, lo que origina un cambio brusco en esta interfase de la osteotomía, donde ningún implante está diseñado para compensarlo, salvo un implante modular proximal tipo SROM. 3. Descenso Con Osteotomia Distal Supracondilea. tiene la ventaja de no afectar el fémur proximal, pues se realiza la artroplastia desde el punto de vista femoral, como se realizaría en cualquier primaria, incluso sin modificar la anteversión femoral proximal, lo que permite la colocación de cualquier tipo de implante al que estemos acostumbrados, cementado o no. Para tal fin, se utiliza el abordaje acostumbrado y del mismo tamaño que al realizar una primaria y se desciende al acetábulo original nuestro cotilo; el fémur se expone y trabaja como de costumbre y se coloca el tallo de nuestra preferencia con la cabeza planeada; una vez implantado y fijo, procedemos a realizar un abordaje lateral como el indicado para fracturas supracon- 195 “Temas selectos de actualización en la Ortopedia Latinoamericana” díleas, exponiendo la metáfisis femoral distal en donde realizamos la osteotomía lo suficientemente proximal a la región supracondílea que permita la colocación posterior de una placa DCP o LCP de 6 a 8 orificios según la contextura del paciente, para luego tomar el fragmento proximal ya osteotomizado con clamps que permitan traccionar, reducir y reorientar la prótesis en la versión adecuada según la técnica de Ranawatt; una vez lograda la reducción, se tracciona el fragmento distal para evaluar la cantidad de resección diafisaria que se realiza en el fragmento proximal y se procede a reducir la osteotomía en la anteversión deseada y completar la fijación con la placa; las figuras 23 a 28 nos muestran los pasos relevantes de la técnica. Figura 22. Problemas de fijación en la Osteotomía proximal. La filosofía de esta técnica, radica en la facilidad de manejar el fémur como en cualquier prótesis primaria, lo que nos deja un fémur intacto a futuro, sin materiales de osteosíntesis ni fijaciones deficientes en uno u otro segmento de la osteotomía, que termine por presentar grandes resorciones del fémur proximal. El realizar la osteotomía distal y hacer allí la resección necesaria para el descenso, así como la corrección de la anteversión hacen mucho más fácil este proceso que trabajar con dos segmentos muy móviles, donde al colocar el vástago tratando de fijar las dos partes, podemos cometer muchos errores en la anteversión requerida, máxime cuando nos enfrentamos a fémures de conformación no cilíndrica, donde existe mayor movilidad de alguno de los focos por la diferencia de diámetro endóstico, lo que puede dejar nuestro implante inestable; por otra parte, con los Figura 23. Colocación de implantes; se aprecia imposibilidad de reducción sin Osteotomía. 196 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Figura 24. Exposición de región supracondílea en fémur distal con el implante acetabular y femoral colocados mas no reducidos por lo alto e imposibilidad de reducción sin osteotomía. Figura 25. Se prueba placa y se demarca sitio de Osteotomía supracondílea. Figura 26. Se tracciona y reduce cadera; evaluación de cantidad de resección necesaria que se hará en el foco proximal 197 “Temas selectos de actualización en la Ortopedia Latinoamericana” Figura 27. Cantidad resecada y reducción en la anteversión deseada. Figura 28. Se completa Osteosíntesis. Se aprecia cadera reducida. actuales sistemas de fijación como placas LCP, el apoyo se puede realizar de manera mucho más precoz que anteriormente. En resumen, lo más importante en este tipo de pacientes, tanto para el manejo femoral, de tejidos blandos, como acetabular, es que debemos procurar hacer un manejo racional, escogiendo el mejor implante para cada tipo de paciente, dependiendo del déficit óseo acetabular y del tipo de canal femoral, así como de la discrepancia y grado de luxación, así como la técnica que nos lleve a colocar la prótesis escogida, pensando en el futuro de un paciente joven 198 y activo, que seguramente necesitará una futura revisión. COMPLICACIONES La artroplastia de cadera en el paciente displásico y/o con luxación no corregida, supone grandes retos y por ende presenta mayores complicaciones que una Artroplastia primaria sencilla; entre las más frecuentes podemos encontrar (52, 63, 64, 65): • Luxación: muestra incidencias mayores, generalmente por una combinación de factores, entre los que se haya una mala calidad y fuerza de la musculatura Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT abductora, el reducido tamaño que obliga a utilizar cabezas de 22 milímetros, menos estables que sus homólogas de 28 o 36 milímetros, así como la anteversión aumentada previa que tienen estos pacientes. Debemos ser estrictos en el momento de evaluar la anteversión que tiene el fémur y es por eso que el autor recomienda no colocar tanta anteversión acetabular, ya que la suma de estas anteversiones es la que puede inestabilizar la cadera; si por cualquier motivo esta es muy exagerada, debemos planear diferentes opciones como vástagos con modularidad metafisaria tipo SROM o incluso osteotomías correctoras. • Infección: presenta incidencias similares a las de las Artroplastias primarias, aunque hay algunos autores que reportan incidencias ligeramente mayores, aduciendo el mayor tiempo quirúrgico, gran exposición ósea y hematomas posteriores. Nuestra técnica debe ser depurada, la disección debe limitarse a lo necesario y siempre es importante una adecuada hemostasia. • Fracturas peri protésicas: son más frecuentes, por la mala calidad ósea principalmente la acetabular, lo que hace que debamos ir preparados a cirugía con anillos y/o cajas de refuerzo; de igual forma, lo delgado del canal medular hace importante planear el tipo y tamaño de tallo que se requiere pues con frecuencia no todas las casas dispones de tallos tan delgados. • Neurológicas: es una complicación frecuente, principalmente la del c Ciático, en caderas altas (Crowe III y IV), donde el descenso al acetábulo original supone un reto. Existen artículos en la literatura que señalan mayor incidencia por encima de descensos de 3 centímetros; sin embargo el autor ha descendido caderas hasta de 7 centímetros sin osteotomía y sin Neurapraxia mientras que ha tenido esta complicación en caderas con osteotomía y menos de 4 centímetros. La incidencia tiene mayor relación con elongaciones de más del 10% del tamaño femoral, si existen cicatrices y adherencias por cirugías previas y obviamente descensos en los que se debe realizar mucha fuerza. La recomendación es una vez colocado el implante, realizar una distracción normal y ver hasta donde se acerca la cabeza al cotilo; si está por lo menos en contacto, se puede hacer un mayor corte o bien tenotomizar progresivamente Psoas, glúteo máximo y aductores. Si a pesar de estas maniobras no se logra reducir, es mejor pensar en cualquier tipo de osteotomía. De igual forma, en el post-operatorio es recomendable dejar cadera y rodillas en ligera flexión para disminuir la tensión al Ciático. • Vasculares: la más temida de las lesiones es la vascular, que puede producirse por lesión directa secundaria a la distorsión de la anatomía propia de la región o por trombosis por tracción y lesión endotelial al lograr el descenso, llevando incluso a la isquemia y posterior amputación de la extremidad; para tal fin, debemos mantener nuestra vigilancia en el postoperatorio inmediato y consultar al cirujano vascular, ante la menor sospecha de lesión. REHABILITACION Y MANEJO POSTOPERATORIO Una vez acabado el acto quirúrgico, debemos procurar evitar todo riesgo innecesario que complique nuestro acto quirúrgico; Es preferible que el paciente quede de una vez en su cama y no en camilla, donde se coloca la rodilla en flexión y ligera abducción, para disminuir como habíamos dicho anteriormente la tensión del Ciático. En aquellos casos donde el paciente no comprenda bien su riesgo o por lo pequeño del acetábulo se 199 “Temas selectos de actualización en la Ortopedia Latinoamericana” requiera utilizar una cabeza de 22 milímetros, algunos autores prefieren proteger la cirugía colocando un brace abductor que restrinja la flexión. El post operatorio inmediato debe ser similar al de una cadera primaria, salvo la protección que debemos hacer del apoyo completo en caso de realizarse una osteotomía; se inicia movilidad precoz de tobillo y rodilla que mejora el bombeo muscular y se inicia marcha asistida con la ayuda externa que previamente se haya recomendado basado en su fuerza y equilibrio (57, 59, 60). En aquellos casos bilaterales donde aumentamos la anisomelia mientras se interviene la otra cadera, se recomienda el uso de un calzado con realce del lado no operado que evite la basculación y la deformidad en aducción, peligrosa para la estabilidad del implante. La profilaxis antibiótica y antitrombótica se debe realizar de manera similar a nuestro protocolo de primaria, así como el alta; una vez el paciente esté ambulatorio se debe estimular su actividad. En caso de existir Neurapraxia del ciático se debe iniciar medicación para evitar el dolor neuropático y estimular su actividad con soporte fisioterapéutico, que según protocolos puede incluir electrogimnasia y el uso o no de ortesis tipo férula en polipropileno para pie caído. METODO PREFERIDO DEL AUTOR Estas caderas suponen un reto que debe explicarse claramente desde la primera consulta tanto al paciente como a sus familiares; es muy importante esta anamnesis para comprender la motivación de cada paciente, ya que nunca debe realizarse esta cirugía por cosmética, buscando mejorar la marcha. Debe existir dolor y limitaciones funcionales claras que motiven la cirugía; de lo contrario, es mejor colocar a nuestro enfermo en un plan de manejo con analgésicos en caso de necesidad, compensación con algún tipo de realce y fortalecimiento fisioterapéu- 200 tico (61, 62). Algunos autores y la mayoría de los ortopedistas generales piensan que las caderas altas en tejidos blandos no ameritan cirugía; sin embargo, un análisis cuidadoso de las mismas puede mostrar el dolor, resalte y sensación de inestabilidad cuando la cabeza femoral choca con la tabla ilíaca y pasa de anterior a posterior y es en esos casos, donde sugiero también la Artroplastia. Al momento de decidir el procedimiento, nuestro paciente debe tener claro varios puntos que incluso deben darse por escrito, en folletos y representados claramente en el consentimiento informado, entre los cuales cabe destacar: • Es una cirugía mucho más compleja que una artroplastia de un paciente de edad con cadera artrósica. • Existe un riesgo REAL de Neurapraxia del Ciático, que será más frecuente en pacientes de baja talla, con cirugías previas y se le debe explicar las posibilidades quirúrgicas en caso de que no corrija. • La compensación, tanto de la anisomelia como de la cojera, puede llegar a no ser completa pues la musculatura abductora ha estado débil desde la infancia y con las osteotomías, la resección ósea puede dejar discrepancias generalmente menores a los dos centímetros, fácilmente compensables. • El cuidado para evitar la luxación debe extremarse; estos pacientes van a fisioterapia preoperatoria para conocer las posturas, uso de ayudas externas y cuidados con su desplazamiento. • Si la luxación es bilateral, a pesar de la existencia de complicaciones neurológicas o de otro tipo, se debe realizar la cirugía contra lateral, para corregir la discrepancia creada al operar la primera cadera. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT ¿Qué exámenes solicito? Los pre quirúrgicos necesarios para la edad y en cuanto a imágenes diagnosticas, únicamente una radiografía AP estándar de cadera; inicialmente solicitaba tomografías, cuando deseaba ver la continencia de las paredes acetabulares o se sospechaba una anteversión severa para planear su corrección, así como el manejo acetabular. En cuanto al planeamiento, lo realizo desde el mismo momento de la consulta para irle explicando al paciente algunos detalles técnicos; le doy especial valor a la profundidad acetabular, ya que la medida normal, generalmente es más de 40 milímetros, mientras que en la cadera displásica, esta medida es de alrededor de 20 milímetros. Por debajo de 20 milímetros, es imprescindible definir si se utiliza un injerto supero externo de acetábulo o se prefiere Medializar la copa; de igual manera, es importante evaluar la anisomelia y la forma más fácil de medirla es la discrepancia del Shenton, sabiendo que por encima de 4 centímetros, se debe decidir si se hace osteotomía proximal o distal. Hablando un poco acerca del tipo de implante preferido para estos casos, siempre utilizo vástagos cementados, bien sea de cobertura porosa proximal o bien porosidad total con recubrimiento de hidroxiapatita, que tienen excelente fijación y sobrevida; siempre se debe contar con implantes muy pequeños, del orden de 6 a 7 milímetros, que no siempre poseen las diferentes casas ortopédicas. En cuanto al cotilo, igualmente prefiero la fijación no cementada; respecto a la cabeza femoral, la idea es poder colocar la cabeza de mayor diámetro, siempre y cuando no sacrifiquemos hueso de manera indiscriminada. Con esto quiero decir que si podemos rimar uno o dos milímetros más sin dañar el anillo periférico y la reserva ósea para poder colocar una cabeza de 28 milímetros, prefiero hacerlo para evitar colocar una cabeza 22; en muy pocos casos ha sido posible llegar a colocar una copa de más de 52 milímetros que permite el uso de cabezas de 36 milímetros y diferentes pares de fricción como la cerámica. Trabajo Acetabular. Considero importante colocar la copa en el acetábulo original o lo más cerca posible, ya que tenemos allí la mejor reserva ósea, da más estabilidad, corrige mejor la anisomelia y tiene sobrevidas mucho mejores en todas las series que los centros rotacionales altos; al decidir Medializar o utilizar injerto, prefiero hacer una pequeña medialización, que puede alcanzar el 20%, con lo cual logramos una excelente cobertura de la copa, no violamos el anillo periférico y se coloca injerto suficiente en el trasfondo como para no violar la biomecánica articular, y agregar hueso creando un fuerte trasfondo que podrá ser utilizado a futuro en caso de una revisión. Con frecuencia es difícil localizar el verdadero acetábulo y mi sugerencia es realizar una adecuada capsulectomía, para llegar a encontrar el remanente de ligamento trasverso. Con frecuencia tenemos el ligamento redondo hipertrófico y lo podemos seguir hasta el trasfondo acetabular. Ya una vez allí, es importante evaluar la capacidad de cada pared para no fresar de manera indiscriminada y terminar produciendo una lesión mayor como se aprecia en la (Figura 29). Con frecuencia y antes de iniciar el fresado, reseco una porción superior y posterior con cincel de 2 centímetros, en la gruesa columna posterior y en la porción endurecida del techo que se encuentra entre el verdadero y falso acetábulo, lo que permite colocar en perfecta posición una canastilla de 36 milímetros y empezar a realizar el fresado hacia interno, llegando casi al trasfondo, para posteriormente reorientar la dirección del fresado y obtener un adecuado ajuste a presión de la copa, como lo esquematiza la (Figura 30). Trabajo femoral. Considero que cada fémur tiene su conformación, que puede 201 “Temas selectos de actualización en la Ortopedia Latinoamericana” Figura 29. Daño acetabular anterior si se fresa como está el acetábulo original. Figura 30. Resección de porción engrosada de columna posterior. ajustarse a los tipos de canal endóstico preconizados por L.Dorr y de acuerdo con su anatomía, es candidato ideal Figura 30. Resección de porción engrosada de columna posterior. para una diferente osteotomía. Los canales normales o tipo copa de Champaña (A y B según Dorr) tiene el problema de que al resecar un segmento metafisario proximal van a dejar una gran diferencia en el sitio de la osteotomía en cuanto al diámetro del canal endóstico, lo que haría que no se obtenga adecuada fijación en uno de los fragmentos, a menos de que se utilice un tallo tipo SROM, muy costoso en nuestro medio, caso 202 diferente al trabajar en un fémur cilíndrico tipo C; es por esto que ante los canales tipo A y B, mi preferencia es realizar una osteotomía distal supracondílea y corregir discrepancia y anteversión mediante esta incisión distal que se fija con una placa LCP, mientras que en los canales tipo C, realizo la osteotomía clásica subtrocantérica y de acuerdo con la calidad se fija con cerclajes interponiendo el fragmento resecado de hueso o bien con una placa LCP de tornillos romos unicorticales. Algunos fémures, sin importar el grado de discrepancia, no requieren de osteotomía femoral y eso se evalúa colocando el implante Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT e intentando una reducción de prueba. Si la cabeza alcanza a enfrentar el borde superior del cotilo, continúo con la idea de no realizar osteotomía y de acuerdo con la tensión, paso a realizar una tenotomía del psoas, posteriormente liberar el glúteo máximo y sólo en raras ocasiones los aductores. Si este parámetro no se alcanza, no intento la reducción y continúo el procedimiento realizando la osteotomía elegida. Rehabilitación. Mantengo en el postoperatorio una flexión de cadera y rodilla de aproximadamente 30° para relajar un poco el ciático y el esquema de manejo de dolor, antibioticoterapia y trombo profilaxis es similar al de una cadera primaria, salvo que la hospitalización y el catéter para manejo del dolor la dejo por dos días. En aquellos pacientes con osteotomía, el apoyo completo se debe diferir doce semanas o hasta que consolide la osteotomía; en pacientes bilaterales en los que se produce un alargamiento con discrepancias que pueden llegar a más de 5 centímetros, se le recomienda que utilice un calzado o zapato de tacón en la cadera no operada, mientras se opera la otra y se ecualiza. En resumen, la Artroplastia de Cadera en el paciente con Luxación inveterada, supone grandes retos quirúrgicos pero deja grandes satisfacciones, tanto en el cirujano como en el paciente. No está exenta de riesgos, sobre todo neurovascular y por eso, la explicación clara y conocer las expectativas individuales de cada paciente, debe realizarse como parte del planeamiento preoperatorio y el sano juicio, nos llevará a decidir si es candidato o no a este tipo de procedimientos. Ya en el intraoperatorio, una depurada técnica quirúrgica, planeando cada paso para no destruir la escasa reserva ósea, así como una adecuada escogencia del implante son claves para obtener el éxito a largo plazo; si mediante una tracción convencional no logramos reducir nuestra cadera de prueba, debemos pensar en realizar la osteotomía de nuestra preferencia, la cual modificará nuestro post-operatorio en cuanto a apoyo y actividad permitida. Vale la pena escoger el caso y enfrentar el reto. Artroplastia total de cadera en pacientes con displasia residual y/o luxacion inveterada de cadera. BIBLIOGRAFÍA 1. Charnley, J. And Feagin, J.A.: Low Friction Arthroplasty in Congenital Subluxation of the Hip. Clin. Orthop. 91: 98, 1973. 2. Harris,W.H. Traumatic Arthritis of the Hip after Dislocation and Acetabular Fractures: Treatment by mold Arthroplasty. An end-result study using a new method of result evaluation. J. Bone Joint Surg. 51(A): 4 June, 1960. 3. Tronzo, R.G., Okin, M. Anatomic restoration of Congenital Hip Dysplasia in adulthood by Total Hip Displacement. Clin. Orthop. (106): 1975, 94-98. 4. Dunn, H.k., Hess, W.E. Total Hip Reconstruction in Chronically Dislocated Hips. J. Bone Joint Surg., 58(A), Sept. 1976, 838-845. 5. Harris, W.H., Crothers, O et al. Total Hip replacement and femoral head bone grafting for severe acetabular deficiencies in adults. J. Bone Joi nt Surg. 59(A) Sept. 1977, 752-759. 6. Hess,W.E., and Umber, J.S.: Total Hip Arthroplasty in Chronically Dislocated Hips. Follow-up study on the Protrusio-socket technique. J. Bone Joint Surg. 60(A): 948-954, Oct., 1978. 7. De Lee, J.G., Cjarnley, J. Radiological demarcation of cemented sockets in Total Hip Replacement. Clin. Orthop. 121: 20-32, 1976. 203 “Temas selectos de actualización en la Ortopedia Latinoamericana” 8. Wedge, J.H., Wasilenko,M.J.; The natural History of Congenital Disease of the Hip. J. Bone Joint Surg. 61(B): 334-338, 1979. 9. Charnley, J. Artroplastia de Baja Fricción de la Cadera. Teoría y Práctica. Salvat Editores, S.A. Mallorca, 1981. 10.Eftekhar N.S. and Stinchfield, F.E.: Total Replacement of the Hip by Low Friction Arthroplasty. Orthop. Clin. North America, 4: 483-501, 1974. 11.Wagner, H. Osteotomies for Congenital Hip Dislocation. In: The Hip: Proceedings of the 4th Open scientific meeting of the Hip Society, Mosby, St. Louis, p.45, 1976. 691 12.Ponseti I.V.: Morphology of the Acetabulum in Congenital Dislocation of the Hip. Gross Histological and Roentgenographic studies. J. Bone Joint Surg. 60(A): 586-599, 1978 13.Crowe, J.F., Mani, V.J., Ranawat, C.S. Total Hip replacement in Congenital Dislocation and Dysplasia of the Hip. J. Bone Joint Surg. 61(A) Jan. 1979, 15-23 14.Dorr, L.D., Takei, G.K. and Conaty, J.P. Total Hip Arthroplasties in Patients less than 45 years Old. J. Bone Joint Surg. 65(A): 474-479, April 1983. 15.Incavo S.J., Difazio, F.A., Howe, J.G. Cement less hemispheric acetabular components: 2-4- years results. J. Arthroplasty, 1993; (8) 573-580. 16.Morscher,E.W. Current status of acetabular fixation in primary total hip Arthroplasty. Clin. Orthop. 1992; (274): 172-193. 17.Anwar, M.M., Sugano, N. et al. Total Hip Arthroplasty in the neglected congenital dislocation of the hip: A five to 14 year follow-up study. Clin. Orthop. 1993; (295) 127-134. 18.Woolson, S.T., Harris, W.H. Complex Total Hip replacement for Dysplastic or Hypo plastic hips using miniature or micro miniature components. J. Bone Joint Surg., 65(A), Oct. 1983, 1099-1108. 19.Harley, J.M., Wilkinson, J.A. Hip replacement for adults with unreduced congenital dislocation. A new surgical Technique. J. BONE joint Surg. 69(B), November, 1987, 752-755. 20.Mcqueary, F.G, Johnston, R.C. Coxarthrosis after congenital Dysplasia. Treatment by Total Hip Arthroplasty without acetabular bone grafting. J. Bone Joint Surg., 65(A) March 1983, 366-370. 21.Spector, M. Historical review of porous-coated implants. J. Arthroplasty 1987; (2): 163-177. 22.Linde, F., Jensen, J. Et al. Charnley Arthroplasty in Osteoarthritis secondary to Congenital Dislocation or Subluxation of the Hip. Clin. Orthop. (277) 1988, 164-171. 23.Hartofilakidis, G., Stamos, K. et al. Low friction Arthroplasty for old untreated congenital dislocation of the hip. J. Bone Joint Surg. 70(B), March, 1988, 182-186. A 24.Davlin, L.B., Amstutz, H.C. et al. Treatment of Osteoarthrosis secondary to congenital dislocation of the hip. Primary cemented surface replacement, compared with conventional total hip replacement. J. Bone Joint Surg. 72(A), August 1990, 1035-1042. 25.Fredin, H. Sanzen, L. et al. Total Hip Arthroplasty in high congenital dislocation. 21 hips with a minimum of five-year follow-up. J. Bone Joint Surg. 7 3(B), May, 1991. 430-433. 26.Garcia, C. E., Munuera, L. Low friction Arthroplasty in severe acetabular dysplasia. J. Arthroplasty, 1993, (8), 459-469. 204 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 27.Schultzer, S.F, Harris, W.H. high placement of porous coated acetabular components in complex total hip Arthroplasty. J. Arthroplasty, 9: 1994, 359-367. 28.Jasty, M. Anderson, M.J., Harris, W.H. Total Hip Replacement for developmental Dysplasia of the Hip. Clin. Orthop, 1995; (311), 40-51. 29.Silber, D.A. Engh, C.A. Cement less total hip Arthroplasty with femoral head bone grafting for Hip Dysplasia. J. Arthroplasty 5: 231-240, 1990. 30.PAAVILAINEN, T., HOIKKA, V. et al. Cement less Total replacement for severely Dysplastic or dislocated hips. J. Bone Joint Surg., 72(B), March 1990, 205-211. 31.Paavilainen, T. Hoikka, V. Paavolainen, P. Cementless Total Hip Arthroplasty for congenitally dislocated or dysplastic Hips. Techniques for replacement with a straight femoral component. Clin. Orthop. 297: 71-81, 1993. 32.Callaghan, J.J. Total Hip Arthroplasty: Clinical Perspectives. Clin. Orthop. 1992; (276): 33-40. 33.Greenwald, A.S. Alternative Bearing surface overview. Symposium of the 68th Annual Meeting of the A.A.O.S. San Francisco, 2001. 34.Hasegawa, Y. Iwata, H. Iwase, T. Et al. Cement less Total Hip Arthroplasty with autologous bone grafting for Hip Dysplasia. Clin. Orthop. 324: 179-186, 1996. 35.Becker, D.A., Gustilo R.B.: Double-chevron subtrochanteric femoral shortening osteotomy in Total Hip Arthroplasty for high-riding developmental dislocation of the Hip. J. Arthroplasty 12: 880-888, 1997. 36.Dorr, L.D., Tawakkol, S, Moorthy, M., Long, W. Wan, Z.: Medial Protrusio technique for placement of a porous-coated hemispherical acetabular component without cement in a total hip arthroplasty in patients who have acetabular dysplasia. J. Bone Joint Surg. 81(A): 83-92, 1999. 37.Berry, D.J. T.H.A. In Patients With Mild To Moderate Dysplasia/Subluxation. Proceedings, Annual meeting AAOS, Dallas Texas, 161-162, 2002. 38.Engh, C.A. Total Hip Arthroplasty in patients with High dislocation. Proceedings, Annual meeting, AAOS, Dallas, Texas, p. 163-164, 2002. 39.Mac Enzie, J.R., Kelley, S.S., Johnston, R.C. Total Hip Replacement for coxarthrosis secondary to congenital dysplasia and dislocation of the hip. Long-term results. J. Bone Joint Surg. 78(A): 55-61, 1996. 40.Haddad, F.S., Masri, B.A., Garbuz, D.S., Duncan, C.P.: Primary Total Replacement of the dysplastic hip. J. Bone Joint Surg. 81(A): 1462-1482, 1999. 41.Davies, J.P., Harris, W.H., In vivo and in vitro studies of pressurization of femoral cement in total Hip Arthroplasty. Arthroplasty; 8: 585-591, 1993. 42.Gill, T.J., Sledge, J.B., Muller, M.e.; Total Hip Arthroplasty with use of an acetabular reinforcement ring in patients who have congenital dysplasia of the hip. J. Bone Joint Surg. 80(A): 969-979, 1998. 43.Barrack, R.l., Mulroy, R.D.JR. Harris, W.H.; Improved cementing techniques and femoral component loosening in young patients with hip Arthroplasty: A 12 year radiographic review. J Bone Joint Surg. 74(B): 385-389, 1992. 205 “Temas selectos de actualización en la Ortopedia Latinoamericana” 44.Sochart, D.H., Porter, M.L.; The long term results of Charnley low-friction arthroplasty in young patients who have congenital dislocation, degenerative Osteoarthrosis or rheumatoid arthritis. L. Bone Joint Surg. 79(A): 1599-1617, 1997. 45.Jaroszynski, G. Woodgate, I., Saleh, K., Gross, A.E.: Total Hip Replacement for the dislocated Hip. J. Bone Joint Surg. 83(A): 272-282, 2001. 46.Yasgur, D.J., Stuchin, S.A., Adler, E.M., DI Cesare, P.E.; Subtrochanteric femoral shortening Osteotomy in Total Hip Arthroplasty for High riding developmental dislocation of the hip. J. Arthroplasty 12: 880-888, 1997. 47.Greenwald, A.S. Alternative Bearing surface overview. Symposium of the 68th Annual Meeting of the A.A.O.S. San Francisco, 2001. 48.Tachdjian, Mihran O. Pediatric Orthopaedics, Second Edition, Vol.1, p. 392-398. 1990. 49.Tachdjian, Mihran O. Pediatric Orthopaedics, Second Edition, Vol. 3, p. 1818-1821. 1990. 50.Hierholzer, G. And Müller, K.H. Corrective Osteotomies of the Lower Extremity after Trauma. Springer-Verlag, Berlin, 1985. 51.Gartland, J.J.: Orthopaedic clinical research: Deficiencies in experimental design and determinations of outcome. J. Bone Joint Surg. 70(A): 1357-1364, 1988. 52.Laupacis, A., Rorabeck, C.H., Bourne, R.B., et al: Randomized trials in Orthopaedics: Why, how and when? J. Bone Joint Surg. 71(A): 535-543, 1989. 53.Friedman, RJ. Black, J. Galante, J.O. et al: Current Concepts in Orthopaedic biomaterials and implant fixation. J. Bone Joint Surg. 75(A): 1 086-1109, 1993. 54.Noble, P.C., Alexander, J.W., Lindahl, L.J. et al: The anatomic basis of femoral component design. Clin. Orthop. 235: 148-165, 1988. 55.Callaghan, J.J., Fulghum, C.S., Glisson, R.R. et al: The effect of femoral stem geometry on interface motion in uncemented porous-coated total hip prostheses: Comparison of straight-stem and curved-stem designs. J. Bone Joint Surg. 74(A): 839-848, 1992. 56.Capello, W.N.: Technical aspects of Cementless total hip arthroplasty. Clin. Orthop: 261; 102-106, 1990. 57.Noble, P.C., Kamaric, E., Alexander, J.W.: Abstract: Distal stem centralization critically affects the acute fixation of Cementless femoral stems. Orth op. Trans. (13) 383, 1989. 58.Poss, R. Walker, P., Spector, M. et al: Strategies for improving fixation of femoral components in total hip arthroplasty. Clin. Orthop, 235; 181-194, 1988. 59.Schneider, E., Kinast, C., Eulenberger, J. Et al: A comparative study of the initial stability of Cementless hip prosthesis. Clin. Orthop. 248: 200-209, 1989. 60.Schmalzried, T.P., Jasty, M., Harris, K.W.: Periprosthetic bone loss in total hip arthroplasty: Polye- tilene wear debris and the concept of the effective joint space. J. Bone Joint Surg. 74(A): 849-863, 1992. 61.Restrepo, N. Evolución Histórica de la Artroplastia Total de Cadera en el tratamiento de la Luxación Congénita Inveterada. Revista Colombiana de Ortopedia y Traumatología, Vol. 13, (2), 135-144, Agosto, 1999. 206 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 62.Restrepo, N. Artroplastia Total Híbrida de Cadera en Luxación Congénita Inveterada. Estudio Prospectivo en Nariño. Revista Colombiana de Ortopedia y Traumatología, Vol. 13, (2), 145-154, Agosto, 1999. 63.Callaghan, J.J., Dennis, D.A., Paproski, W.G. And Rosenberg, A.G. Orthopaedic Knowledge Update. Hip and Knee Reconstruction. American Academy of Orthopaedic Surgeons. Chapter 16, p.127-138. 1995 64.Collier, J.P., Mayor, M.B., Jensen, R.E., et al: Mechanisms of failure of modular prostheses. Clin. Orthop. 285: 129-139, 1992. 65.Crowninshield, R.D., Brand, R.A., Johnston, R.C., et al: An analysis of femoral component stems design in total hip arthroplasty. J. Bone Joint Surg. 62(A): 68-78, 1980. 66.Barrack, R.L.: Modularity of prosthetic implants. J. Am. Acad. Orthop. Surg. (2) 16-25, 1994. 67.Ebramzadeh, E., Sarmiento, A., Mckellop, H.A., Llinas, A., Gogan, H.: The cement mantle in total hip arthroplasty, analysis of long-term radiographic results. J. Bone Joint Surg. 76 (A): 77-87, 1994. 68.Wroblewski, B.M., Siney, P.D.: Charnley low-friction arthroplasty in the young patient. Clin. Orthop. 285: 45-47, 1992. 69.Engh, C.A., Massin, P., Suthers, K.E.: Roentgenographic assessment of the biologic fixation of porous-surfaced femoral components. Clin. Orthop. 257: 107-128, 1990 70.Noble, C.P., Tullos, H.S., Landon, G.C. The optimum cement mantle for Total Hip 71.Replacement: Theory and practice. Instructional Course Lectures, Chapter 20, 145, 150. 72.71. Huddleston, H.D. Femoral Lysis after cemented hip Arthroplasty. 73.J. Anthrop, 1988, 3: 285-297. 74.72. Bocco, F., Langan, P., Charnley, J. Changes in the calcar femoris in relation to cement 75.technology in total hip replacement. Clin. Orthop. 128; 287-295, 1977. 76.697 207 “Temas selectos de actualización en la Ortopedia Latinoamericana” 208 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Lesiones Neurovasculares en Artroplastia Total de Cadera Nicolás Restrepo Giraldo M.D. Hospital Universitario Departamental de Nariño E.S.E. Clínica de Reemplazos Articulares, Clínica Los Andes Pasto Colombia INTRODUCCIÓN Las lesiones neurovasculares en la artroplastia total de cadera, a pesar de ser complicaciones poco frecuentes en las caderas sencillas, generan una carga emocional tanto para el paciente como para el cirujano y su grupo, pues llegan a ser devastadoras y muy limitantes; su incidencia ha aumentado notoriamente con la implementación de la técnica en casos difíciles como displasias con luxación inveterada, secuelas de fracturas de acetábulo, deformidades proximales severas, pacientes con cirugías previas y revisiones. Pueden existir además, lesiones neurológicas centrales, aún más raras, producto de embolia grasa principalmente durante el cementado, hipoxia prolongada y/o accidentes cerebro/ vasculares intraquirúrgicos (1, 2, 3, 4). Entre las lesiones periféricas, la lesión más frecuente sin duda es la neurapraxia del ciático, principalmente de su rama peronea; en menor frecuencia, se puede encontrar la lesión del nervio crural y por ultimo la del nervio obturador. Su prevalencia varía entre el 0,6 al 1,3% según diferentes series como las reportadas por Rubash o Salvati (5, 6, 7, 8). Evaluando las series de caderas displásicas con luxación alta no tratada, podemos ver que nos enfrentamos en estos casos a un problema frecuente, con incidencias que oscilan entre el 5,2 y el 32%. (5, 6, 9). La incapacidad generada por este tipo de lesión, que desde el post-operatorio inmediato presenta un dolor neuropático urente, además del déficit motor que dificulta la marcha, tiene una recuperación tan lenta que en muchas ocasiones puede sobrepasar el año, generando un alto costo al sistema de salud, así como una larga incapacidad laboral, máxime cuando un 15% de estos casos pueden tener una recuperación incompleta y/o dejar secuelas (9,10). Para el ortopedista que enfrenta esta lesión, supone una larga lucha contra una enfermedad discapacitante y dolorosa, aparte de una permanente actitud de acompañamiento y dialogo con el paciente y sus familiares, que de no estar informados previamente y muchas veces alentados por opiniones de otros colegas menos expertos en la materia, pueden pensar que existió iatrogenia, sección real inadvertida del nervio o complicaciones en 209 “Temas selectos de actualización en la Ortopedia Latinoamericana” la técnica quirúrgica no referidas, que fueron los causantes de dicha lesión. Este capítulo pretende mostrar al ortopedista general y subespecialista, los conceptos anatómicos, fisiológicos y patogenéticos que explican el por qué este tipo de lesiones se produce, por qué tarda tanto tiempo en recuperar, así como mostrar un abordaje diagnostico y terapéutico que le den más armamentarios en esta larga lucha para vencer esta complicación Conceptos Anátomo-fisiológicos del Nervio periférico. El nervio periférico es una fina estructura, encargada de trasmitir los impulsos eléctricos y/o potenciales de acción por largas distancias a lo largo del cuerpo, con fibras sensitivas o aferentes y/o motoras o eferentes, finalizando en las placas terminales pre sinápticas, estructuras que trasmiten la información a otras dendritas de la siguiente célula o bien a una unión neuro-muscular. El nervio periférico posee estructuras de colágeno y elastina que lo protegen más de las fuerzas tensiles y compresivas que los nervios espinales. La típica formación de endoneuro, que agrupa en fascículos las células de schwann, es el encargado de soportar el edema, que de presentarse a este nivel, es patognomónico de un daño irreversible; el perineuro, expansión de este tejido conectivo es el que soporta la mayor fuerza tensil contra el edema y el epineuro, que finalmente rodea al nervio, lo protege principalmente de las fuerzas compresivas. Una vez existe el daño nervioso, pueden existir según Seddon (11), quien las diferenció desde 1943, tres grados de lesión: • Neurapraxia: causada por una lesión menor, fisiológica mas no anatómica, que generalmente recupera por completo. • Axonotmesis: causada por una lesión más severa, que si produce un daño 210 anatómico de los axones, causando degeneración walleriana pero cuya cobertura tisular conectiva permanece íntegra, lo que permite servir de molde guía para reconstruir la disrupción aproximadamente a una velocidad de un milímetro día (1 mm/día); si el músculo se atrofia de manera severa, o pasados dos años la regeneración no alcanza la placa motora, puede no recuperarse la función. • Neurotmesis: causada por una lesión severa, supone el daño completo y la falta de regeneración del nervio periférico.; esta se produce por un daño vascular severo, causado por efectos únicos o combinados de compresión, distracción, isquemia y/o transección. Comportamiento ante la isquemia. Los nervios largos y grandes como el ciático, son más propensos a la lesión, debido a que poseen proporcionalmente más fascículos, firmemente empaquetados y menos tejido conectivo epineural, amortiguador de las fuerzas (12, 13). Los estudios clásicos de Lundborg en los que utiliza un torniquete productor de isquemia, muestra que la lesión es proporcional con el tiempo; con 2 horas o menos de isquemia, al desinflar el retorno sanguíneo ocurre en pocos segundos, mientras que si la isquemia persiste por 4 a 6 horas, la circulación demora en retornar a lo normal entre 2 y 3 minutos y al tenerla por más de 8 a 10 horas, se produce éstasis microvascular. (14, 15) Comportamiento ante la elongación. Cada nervio tolera la elongación de manera diferente e individual, teniendo relación con el grado de libertad en los tejidos blandos adyacentes, y se limita por las prominencias óseas, fascias inextensibles o cicatrices fibrosas post-operatorias; los estudios de Lundborg en conejos, muestran cómo elongando de 4 a 11%, ya se presentan cambios histológicos, ruptura de Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT fibras axonales con cambios tan pequeños como el 4 a 6%, la microcirculación se altera con valores por encima de 8% y se detiene al estirar un 15% de la longitud original y por último, la neuroconducción falla por completo al estirar un 25% de la longitud inicial. Comportamiento ante las cargas y/o agresión mecánica. Explicada por la Ley de Laplace, en la que se enuncia que la tensión es proporcional a la presión y al radio de una estructura cilíndrica, explica como nervios grandes, con axones mayores, son más susceptibles de dañarse (13); esta agresión mecánica, puede causar disrupción de las fibras por cuatro mecanismos: • Compresión/distracción • Aumento progresivo en la carga • Aumento en la duración de la carga • Aplicación desigual de la carga en los tejidos Comportamiento ante la transección. La sección parcial o total de un nervio, causada ocasionalmente durante un acto quirúrgico por separadores filosos, esquirlas óseas alambres de cerclajes o instrumentos cortantes, afectará específicamente las placas neuromusculares de los axones seccionados y su representación será una lesión parcial de ciertos grupos musculares o la lesión completa con pérdida de la función de los músculos por él inervados (14, 15, 16). Prevalencia. Las lesiones neurológicas en cadera primaria sencilla son relativamente infrecuentes, del orden del 0,6 a 1,3% (1, 5, 7, 10); sin embargo, esta cifra se incrementa en caderas complejas y cirugía de revisión; en esta última, encontramos publicaciones con más del 7,5% (1, 10, 17). La mayoría de las series nos muestran que el ciático alcanza más del 90% de las lesiones neurológicas (6, 7, 8), aunque la serie de Schmalzried (10) nos relata que se afectan con mayor frecuencia la rama peronea (52%), el ciático común (27%) y el nervio femoral (1,3%). Existen estudios de evaluación prospectiva, que muestran hasta un 70% de lesión subclínica en cualquier Artroplastia Total de Cadera, evaluada electromiográficamente en el postoperatorio (16). Luego de la lesión del ciático y el nervio femoral, existen con mucha menor frecuencia las lesiones del nervio obturador, el glúteo Superior y por último el fémorocutaneo. Factores de riesgo. Se han estudiado diferentes factores de riesgo sin encontrar una significancia estadística real, ya que muchos factores son coadyuvantes y alteran la verdadera incidencia. El trabajo de Schmalzried (10) muestra que de las 59 neurapraxias encontradas en 3126 artroplastias consecutivas, 28% de ese total eran por Displasia de Caderas o revisiones, pero esas dos patologías, sumaban el 63% del total de las lesiones. Mientras que el 1% ocurrían en el paciente osteoartrósico, lo que da significancia estadística como factor de riesgo a los pacientes con Displasia, con un riesgo proporcional a la severidad de la luxación y discrepancia de longitud corregida. En cuanto a los pacientes de revisión, la incidencia también se correlaciona con el tejido fibroso cicatricial y adherencias tisulares que no permiten la movilidad normal del nervio, así como la colocación de injertos y material de reconstrucción que favorece la lesión nerviosa directa; curiosamente, los datos de la revisión muestran una correlación proporcional con el grado de corrección de la discrepancia de longitud, pues retirando de su estudio aquellos pacientes de revisión que debieron alargarse más de 3,3 centímetros, la prevalencia de revisión, sólo fue 2,5 veces mayor que las presentadas por Osteoartrosis primaria. 211 “Temas selectos de actualización en la Ortopedia Latinoamericana” Se intentó evaluar la relación entre la altura del paciente y el porcentaje de alargamiento, pero existen muchas variables anatómicas individuales, que hace que algunos pacientes tengan menor tolerancia a la elongación. En este estudio, el 57% de los casos se desconoce la etiología, siendo el mayor grupo en hombres y las mujeres en quienes no se conoce la causa, proporcionalmente eran más altas y pesadas que en aquellas en las que se conoce; a pesar de que la elongación de más de tres centímetros en esta serie ocurrió en 6 de 9 pacientes, este parece ser un factor de riesgo pero no el único pues las alteraciones anatómicas y la necesidad de reconstrucciones complejas también favoreció el aumento en la incidencia en las caderas congénitas. En algunas series se encuentra como factor de riesgo el sexo femenino, con incidencias dos veces mayores que en el hombre; sin embargo en esta serie, a pesar de que si se presentó este mismo valor, es desestimable ya que el 66% de las cirugías era realizada en mujeres; sin embargo en aquellas mujeres de talla baja, extremidades cortas y discrepancias severas por luxaciones altas, era el grupo de más alto riesgo y mayor incidencia de lesión neurológica. La serie de Edwards mostró que 6 de sus 10 pacientes tuvieron alargamientos de más de 3 centímetros, pero alargamientos de menos de 3,8 centímetros produjeron sólo lesión de la rama peronea con mejor pronóstico, mientras que alargamientos mayores se asociaron con lesión de los troncos peroneo y tibial, con un peor pronóstico, concepto similar publicado en los estudios de la Clínica Mayo (18) y de Kennedy (19) con electromiografía y Nercessian (8) que establece como elongación segura un 10%. Etiología. En cualquier lesión neurológica podemos establecer como causas básicas las lesiones directas por objetos traumáticos en cirugía, tales como cerclajes, instrumental afilado, fresado sin protección, extrusión del cemento 212 o contacto durante las altas temperaturas del fraguado y lesiones indirectas por tracción, compresión o isquemia, evaluadas con detenimiento en apartes anteriores. Sin embargo, muchos factores potencian y coadyuvan a que se presente esta complicación y en la gran mayoría de los casos, esto genera que no se pueda esclarecer una causa determinante de la lesión. Lesiones del Nervio Glúteo Superior. Este nervio, proveniente de las raíces L4 a S1, que inerva los glúteos menor, medio, superior y Tensor de fascia Lata, afecta directamente la deambulación pues su alteración afecta la fuerza abductora causando una severa cojera de Trendelemburg. Se puede lesionar en el 77% de los abordajes transtrocantéricos y/o posteriores (20) y las fibras anteriores para la Fascia Lata, se lesionan en el abordaje antero/lateral de Hardinge, al divulsionar este músculo; de igual manera, si con este abordaje ascendemos más de 5 centímetros proximal a la punta del trocánter mayor, o 4 centímetros proximal al borde del techo acetabular, podemos lesionarlo de forma completa causando una cojera severa, dejando una insatisfacción marcada en nuestro paciente (21). Lesiones del Nervio Femoral. Originado de L2 a L4, pasa a través del psoas y discurre entre el psoas y el músculo ilíaco, descendiendo al muslo como la estructura más lateral del triangulo femoral, inervando la musculatura extensora de la rodilla (Quadriceps) y dar la sensibilidad a la cara medial de muslo y la pantorrilla; la hiperextensión de la cadera por tiempos prolongados, así como un hematoma iliaco, puede originar su compresión y posterior lesión, así como directo por separadores en el reborde anterior del acetábulo; su afectación en la Artroplastia de cadera es muy baja, del orden de 0,04 a 0,4% (8, 10, 16), y generalmente da poca sintomatología por ser una lesión leve e incompleta (22, 23). Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT La mayor serie reportada es la de Simmons (23), con un 2%, y todos habían recuperado a los 12 meses; el diagnostico clínico nos muestra dolor en el muslo, hipoestesia anteromedial en el muslo, medial en la pierna, asociado a debilidad en el Cuádriceps, que se manifiesta por dificultad para subir escaleras. Lesiones del Nervio Obturador. Este nervio, que nace de las raíces lumbares L2 a L4, en la parte posterior del psoas, emerge medial al ala sacra, para seguir a lo largo de la línea iliopectinea, dejando la pelvis en el aspecto superior del agujero obturatriz, inervando la musculatura aductora y dando sensibilidad a la cara antero interna del muslo; a pesar de ser una lesión infrecuente, hay que sospecharla cuando existe extrusión de cemento a la cavidad pélvica, paso de tornillos o de las fresas en el cuadrante anterior del acetábulo; se manifiesta por dolor crónico en la ingle o en la cara interna del muslo, debilidad de los aductores incluso con irradiación del dolor a la rodilla como ocurre típicamente en el dolor artrósico. Lesiones del Nervio Fémorocutaneo. A pesar de que parezca improbable su lesión, esta puede ocurrir por los posicionadores que causen presión sobre la espina iliaca ipsilateral, así como en abordajes mínimamente invasivos anteriores; más frecuentemente lesionados en osteotomías como la de Ganz, se manifiesta como hipoestesia en la cara antero lateral del muslo y con frecuencia puede producir neuromas cerca a la cresta iliaca, que molestan con vestimenta ajustada a dicho nivel. La recuperación generalmente como producto de la compresión por el posicionador, generalmente es rápida y completa. Lesiones del Nervio Ciático. Su ocurrencia varía, según las series reportadas, entre 0,5 y 2% en artroplastias normales (1, 5, 7, 10, 16); en las caderas dis- plásicas se encuentra alrededor del 5% (1, 10, 12,18) y en las revisiones entre 2 y 4,7% (8, 10, 12), llegando incluso hasta más de un 30% en caderas con luxación inveterada alta tipo Crowe IV (1, 5, 10). Esta complicación es dos veces más frecuente en mujeres (10), pero como se explicó anteriormente, existen diferentes hipótesis respecto a la mayor incidencia en el sexo femenino, que involucran la capacidad de distensión proporcional del nervio y que parecen estar más relacionadas con la baja talla y la capacidad limitada porcentual que tiene cualquier nervio de elongarse sin existir lesión fisiológica; sin embargo, la mayoría de las series son conscientes de que es mayor la incidencia de caderas displásicas operadas en mujeres, lo que hace que no se considere como un factor estadísticamente significativo. Etiopatogenia. Las fibras del nervio ciático vienen orientadas descendiendo longitudinalmente por la escotadura, estando en una situación más externa y superficial las fibras de la porción peronea, lo que aumenta el riesgo de lesionar el nervio de manera directa o indirecta (mediante compresión) dicha porción, bien sea con separadores utilizados en el procedimiento quirúrgico, o una vez se implanten tornillos y cajas tipo Bursch/Schneider, como se puede apreciar en la figura 1, que muestra su cercanía al trocánter mayor y su descenso en el fémur; por otro lado, estudios anatómicos muestran que la porción peroneal en menos extensible y está más fija entre la escotadura ciática y la cabeza del peroné, donde rodea su cuello (12). De igual manera, este nervio, al tener muchos fascículos y poco tejido conectivo que lo rodea proporcionalmente, es muy sensible a la distracción, lo cual hace que su lesión sea frecuente cuando se intenta corregir una anisomelia mayor de 4 centímetros (10, 16, 24). 213 “Temas selectos de actualización en la Ortopedia Latinoamericana” autonómica localizada en el primer espacio interdigital; desde el punto de vista motor, a nivel del muslo, sólo está inervada la porción corta del bíceps, mientras que en la pantorrilla, involucra la musculatura dorsiflexora; sin embargo, cuando hay un cuadro instaurado existe severo dolor de tipo neuropático, con disestesias en el territorio del nervio comprometido, un grado de paresia variable que puede llegar hasta el pie caído y signo de tinel, que permite evaluar el proceso de recuperación (7, 10, 12). Figura 1. Exposición del ciático en el abordaje posterior de cadera. Por otra parte, el nervio es vulnerable en su trayecto cuando se realiza una artroplastia, sobre todo en casos severos o en revisión, patologías en las cuales puede existir rigidez, cicatrización fibrosa y distorsión de la anatomía quirúrgica. No se ha comprobado una mayor incidencia con algún tipo de abordaje, pero sí se ha encontrado una relación con la presencia de un hematoma post-operatorio que produzca compresión (10, 12, 25, 26). En general, se puede decir que las principales causas de Neurapraxia son (1, 6, 8, 13, 27, 28, 29, 30): Posteriormente, se presentan cambios tróficos consistentes en alteraciones vasomotoras como frialdad, brillantez de la piel que toma un color violáceo, sudoración y, por último, atrofia muscular e incluso equino, como puede verse en la figura 2. • Alargamiento y/o lateralización (50% de los casos) • Lesión directa (20 a 22%) • Hematoma (18 a 20%) • Después de un episodio de luxación (10%) Cuadro clínico Todo paciente a quien se le realiza una elongación y/o lateralización apreciable puede presentar una sintomatología variable consistente en disestesias y debilidad muscular (1, 5, 7, 8); La distribución sensitiva de la rama peronea abarca el dorso del pie, con una zona 214 Figura 2. Cambios clínicos en neurapraxia de ciático instaurada. El daño de la porción tibial, que sólo llega al 2% (1, 10), produce debilidad de los flexores de rodilla (isquiotibiales), menos la porción corta del bíceps, así como debilidad variable de los plantiflexores y musculatura posterior del tobillo (12). Diagnóstico Inicialmente, el diagnóstico es eminentemente clínico, pues encontramos un paciente que en el post-operatorio presenta disestesias Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT mas debilidad en la musculatura planti y/o dorsiflexora, que según la severidad, alcanza la parálisis. Pasados 21 días, se pueden realizar estudios electrofisiológicos que muestran la ausencia de conducción del nervio afectado, mientras que el electromiograma evidencia fibrilación y ausencia de potenciales motores, similares a los encontrados en la Figura 3. (5, 7, 10, 11, 13). Figura 3. Silencio electromiográfico en lesión reciente. Con el paso del tiempo, los potenciales motores pueden ir mejorando y poco a poco se apreciará una conducción lenta, que tiende a normalizarse en la medida que el paciente mejora, o se mantiene estacionaria para incluso mostrar potenciales de denervación cuando empeora el pronóstico y no se espera mejoría (11, 13, 24). Clínicamente, es valioso identificar la progresión del tinel que a razón de un milímetro por día puede evidenciar si el paciente está mejorando o no (10, 12, 24). Tratamiento En general, lo principal es prevenir y tener cuidado con los pacientes que tienen un mayor riesgo (1, 5, 8, 10, 24, 30): • Displasias y luxaciones altas • Enfermedad lumbar previa • Defectos de pared y/o columna posterior • Pacientes que requieran cerclajes • Retiro de material de osteosíntesis cercano al nervio En estos pacientes, es muy importante el consentimiento informado, así como discutir y documentar con ellos las posibilidades de lesión, su manejo y pronóstico. En este tipo de pacientes, muchos autores recomiendan exponer el nervio e ir probando su tensión (1, 5, 10); incluso, algunos autores utilizan potenciales evocados, estudios fisiológicos intraoperatorios o algo similar a un test de despertar, pero cuando la lesión es por elongación en caderas displásicas se ha visto incluso una aparición lenta, progresiva e inexorable de la Neurapraxia en el posoperatorio inmediato (1, 10, 19, 24). Conviene ser diligentes con la exposición, evitar la colocación de separadores que puedan causar compresión y/o lesión directa, realizar una adecuada hemostasia para disminuir la presencia de hematomas y colocar la cadera y rodilla en flexión en el posoperatorio, para disminuir la tensión. La presencia de hematoma puede ser una causa importante de neurapraxia, principalmente en aquellos pacientes con mayor sangrado del habitual, que presenten dolor en la región glútea, con edema y pérdida progresiva rápida de la función motora más disestesias en el posoperatorio inmediato. Se trata de una verdadera urgencia si se sospecha, ya que la lesión se instaura en 12 horas, lo que amerita una descompresión, lavado y hemostasia de urgencia en caso de estar seguros del diagnostico; deben evaluarse y comentarse muy bien con el paciente los riesgos anestésicos, de resangrado y de aumento en los índices de infección si se explora la lesión. Por otra parte, no está muy bien definido y existe poca evidencia sobre lo que se debe hacer en estos casos, si la patología y la existencia real de un vaso sangrante es 215 “Temas selectos de actualización en la Ortopedia Latinoamericana” dudosa; algunos autores prefieren manejo médico con hielo local, compresión suave, valoración periódica y medicación específica, entre los que se incluye acido tranexámico (15, 26), mientras que otros, a pesar de los riesgos de infección prefieren hacer la exploración (10,26). De todas maneras, si se decide realizar alguna intervención, es mejor documentarlo para fines legales. Ya una vez presentada la Neurapraxia, para enfrentar este problema, debe tenerse una actitud optimista, positiva y de soporte, pero sobre todo, hay que tener mucha paciencia, pues algunas lesiones demoran hasta dos años en recuperarse, así sea de manera parcial. En estos casos, el uso de inmovilización y calzado especial y/o férulas en polipropileno para pie caído (figura 4), puede ser de mucha ayuda, siempre y cuando el paciente las tolere, ya que pueden ser incómodas y no ajustarse con el calzado habitual del paciente. • Carbamazepina (200 a 800 mg/día) • Oxcarbazepina (300 a 1200 mg/día) • Gabapentina (300 a 3200 mg/día) • Pregabalina (75 a 900 mg/día) Para este tipo de pacientes y su mejor acompañamiento, el manejo siempre debe ser interdisciplinario incluyendo fisiatría, ortopedia, clínica del dolor, fisioterapia y técnicos ortesistas para cubrir todos los aspectos básicos que garanticen su bienestar en el largo tiempo que demora su recuperación, a la vez que se discute e informa de manera natural y permanente sobre su mejoría. Pronóstico La gran mayoría de las lesiones del nervio femoral se recuperan; en cuanto a las lesiones del ciático, se puede decir que el 40% se recuperan por completo, el 45% se recuperan dejando algo de déficit funcional y el 15% tienen una recuperación mínima o no se recuperan pasados los dos años de evaluación (, 7, 8, 10, 24) El pronóstico es mejor en los pacientes que tienen pérdidas motoras parciales y/o en aquellos en los que existe alguna recuperación motora durante las dos primeras semanas (1, 6, 8, 9, 10, 17, 19). Figura 4. Férula para pie caído. La medicación analgésica de rutina debe estar encaminada a realizar titulación con diferentes componentes, centrales y periféricos, para controlar el dolor; debe acompañarse de drogas para el dolor neuropático tales como (1, 6, 19): 216 Corrección quirúrgica. Si pasado el tiempo esperado para la recuperación o de acuerdo con la evolución clínica, si la recuperación se detiene, es importante evaluar las posibilidades quirúrgicas en conjunto con el paciente; para tal fin, las dos propuestas son la Artrodesis o la transferencia tendinosa del Tibial Posterior; la Artrodesis de tobillo, es tal vez, la única opción válida si no existe ningún tipo de recuperación, pues para la transferencia, necesitamos poder plantiflexor, que al redirigir la fuerza muscular del tendón, permita Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT mantener el neutro del tobillo y lograr algo de dorsiflexión. TECNICA DE TRANSFERENCIA TENDINOSA DEL TIBIAL POSTERIOR. Debido a que la recuperación parcial es frecuente, el conocer la técnica ayuda a mejorar la marcha de un paciente que haya recuperado algo de poder plantiflexor; la técnica consiste en cosechar el tibial posterior de su inserción en el escafoides y redirigirlo a través de la membrana interósea para reinsertarlo en el dorso del pie. Toma del injerto. Se realiza una pequeña incisión siguiendo las líneas de Langerhans sobre el escafoides y se toma la porción tendinosa mayor en su inserción; se debe recordar que existen inserciones en los huesos vecinos, que deben retirarse, para obtener un tendón, grueso, fuerte y de la mejor calidad; una vez de tiene, del mismo se tracciona para encontrar su recorrido y se realiza la segunda incisión en el tercio distal, región posteromedial de la pierna (Figura 5) Reorientación del tendón al compartimento anterior. Una vez se toma el tendón, se realiza una incisión anterior, aproximadamente al mismo nivel de la segunda incisión, y se toma el tendón para redirigirlo al compartimento anterior, teniendo cuidado de no comprimir Figura 6. Paso del tendón al dorso del pie. a su paso el paquete neurovascular; un buen truco es tomar una pinza fuerte y curva, que se dirige subperióstica para poder tomar la sutura del tendón. Una vez se pasa el tendón, se escoge el sitio donde ha de insertarse en el dorso del pie, generalmente sobre la tercera cuña (Figura 6) Fijación de la trasferencia al dorso. Se escarifica la zona ósea receptora y se fija el tendón en dorsiflexión, de preferencia fijándolo con un tornillo con arandela dentada, que mantendrá fuertemente la fijación y permitirá menor tiempo de inmovilización (Figura 7) Se mantiene la corrección con una férula en leve dorsiflexión, que de acuerdo con el tipo Figura 5. Incisión y toma del Tendón del Tibial Posterior. 217 “Temas selectos de actualización en la Ortopedia Latinoamericana” presentarse un sangrado que puede poner en riesgo la vida del paciente; en ocasiones, algunas lesiones pueden pasar desapercibidas, pues se presenta un daño parcial o lesión endotelial, que a la postre producirá trombosis, eventos tromboembólicos o falsos aneurismas. Figura 7. Fijación de la trasferencia al dorso del pie. de fijación, se mantendrá hasta la adecuada fijación de la trasferencia y después se inicia protocolo de reeducación muscular. Esta fijación, sin ser lo mejor, ayuda notoriamente al marcha de un paciente que puede estar muy descontento por el resultado, si no se le han explicado previamente los riesgos y el pronóstico de la lesión. LESIONES VASCULARES. Durante una Artroplastia Total de Cadera, son muchas las estructuras vasculares que pueden lesionarse (31): • Arteria y vena femoral • Arteria obturatriz y sus ramas venosas adyacentes • Arteria ilíaca externa • Arteria Iliaca Común • Arteria y vena Glútea superior • Vasos femorales profundos De igual manera, existen diferentes formas de lesión, que pueden causar una hemorragia aguda masiva o bien, una vez se estabilicen los signos vitales en el postoperatorio inmediato, 218 PREVALENCIA. Resulta difícil evaluar la verdadera prevalencia de las lesiones vasculares, pues, afortunadamente son escasas; se sabe que es mucho más frecuente este tipo de lesiones en cirugía de revisión y en primarias complejas o aquellas realizadas con cirugías previas, donde alcanza un 0,25%, siendo las estructuras más lesionadas la Arteria Iliaca Externa y la Femoral común, tan cerca del borde acetabular anterior (32). ETIOLOGIA. Las lesiones pueden ser causadas de manera directa o indirecta; el daño directo a un vaso se puede producir fácilmente en el intraoperatorio, durante la disección con bisturí o electrocauterio, separando el borde anterior acetabular con retractores tipo Hohmann ( 33, 34, 35), donde se puede lesionar la arteria femoral, o bien al exponer el fémur colocando separadores en la pared medial, peritrocantéricos, donde pueden lesionarse las arterias circunflejas por lo que se debe preferir instrumental de punta roma para colocar en dichas zonas o bien, separar con retractores tipo Richardson; tampoco es infrecuente el encontrar en la literatura, lesiones con las fresas al violar el trasfondo acetabular, donde podemos lesionar los vasos ilíacos (36, 37, 38). Con el advenimiento de los acetábulos no cementados, el uso de tornillos para lograr su fijación inicial ha producido el que se presenten lesiones arteriales durante el proceso de perforación (7, 10, 37, 39,40, 41, 42). Desde 1990, los estudios anatómicos en cadáver realizados por Keating y Ritter, muestran la cercanía de los vasos ilíacos Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT externos al colocar los tornillos anterosuperiores, del paquete obturador en el trasfondo acetabular, así como de los plexos venosos en la porción inferomedial del acetábulo (42); en ese mismo año; Wasielewski y Rubash describieron un sistema de sectorizar en cuadrantes al acetábulo mediante las líneas que se cruzan perpendiculares partiendo de las espinas iliacas antero y posterosuperiores, donde recomiendan evitar los cuadrantes anteriores, por el paso de las estructuras nobles anteriormente descritas, como se aprecia en la figura 8. Figura 9. Tornillo intrapélvico y mala orientación De igual manera, es importante, durante las técnicas de medialización o seudoprotrusio, realizar la fractura de manera controlada, palpando las estructuras y evitando hacer un fresado excesivo, pues tanto por el mismo como por la migración intrapélvica del componente acetabular, pueden presentarse hemorragias incluso mortales (46). Figura 8. Zonas de seguridad para colocación de tornillos. La recomendación actual es colocarlas siempre en la zona de carga entre el huso horario de 11:00 a 1:00 y si se requiere utilizar en otros sitios por la calidad o reserva ósea, frecuentemente perdida en cirugía de revisión, utilizar el palpador previamente para confirmar la calidad de la superficie ósea escogida y una vez cerciorados, tratar de no violar la segunda cortical (7, 40, 42, 43, 44, 45). Ejemplos como el de la figura 9, donde vemos tornillos intrapélvicos, deben evitarse. Otra causa frecuente de lesión la constituyen la extracción de componentes generalmente cementados donde se hacían perforaciones mediales y migraba parte del cemento intrapélvico (10, 38, 39), que puede quedar adherido o en contacto con los vasos y desgarrar los mismos en el momento de la extracción completa de la copa, como se aprecia en la cadera derecha de la Figura 10. Algunas veces, no se presenta sangrado pero existe lesión vascular bien sea por trombosis, desgarro de la íntima durante elongaciones severas, compresión directa por los separadores o los mismos componentes o incluso por desprendimiento de placas atero 219 “Temas selectos de actualización en la Ortopedia Latinoamericana” zación acetabular, es preferible realizarla con una fresa de un tamaño similar al del tamaño acetabular y ni empezar con fresas muy pequeñas, que pueden violar con facilidad el trasfondo acetabular; si lo que se busca es una fractura controlada en técnicas de seudoprotrusio, el fresado debe ser mínimo, adelgazando el trasfondo y posteriormente perforándolo con un elemento romo, para continuar haciendo el fresado sin mucha presión hacia medial. Figura 10. Cemento intraabdominal. matosas en pacientes de edad con este tipo de patología; en todas ellas, la manifestación es tardía, con isquemia en el postoperatorio generalmente primer o segundo día, con consecuencias catastróficas que incluyen en algunas series hasta más de un 12% de amputación (7, 38, 39, 40, 42, 44, 46, 47, 48). En estos casos, el dolor desmedido, asociado a frialdad y paresia, deben alertar al cirujano para sospechar el diagnostico y lograr una exploración efectiva por parte de un cirujano vascular especializado. PREVENCIÓN Debe hacer parte de nuestro planeamiento preoperatorio una adecuada evaluación de las condiciones propias de cada paciente; en el caso de caderas primarias, debemos evaluar si existe diátesis hemorrágica o trombótica previa, patologías asociadas y/o material de osteosíntesis que amerite cambiar nuestro abordaje rutinario, o bien, entrar en compañía de un cirujano vascular. Siempre nuestra disección debe ser meticulosa, con incisiones que permitan la exposición y el trabajo adecuado en las zonas de riesgo, evitando el uso de separadores afilados tipo Hohmann, sobre todo eludiendo su colocación en la pared anterior acetabular, bajo el ligamento trasverso o peritrocantéricos mediales en el fémur. Al realizar la profundi- 220 En casos específicos de revisiones complejas como el de copas migradas, protruídas o con extravasación de cemento, una angiografía, angiotac o incluso exámenes más sofisticados con sustracción de imágenes metálicas, nos pueden dar una idea de la posición de las estructuras nobles, su cercanía a los implantes y la zona segura para su extracción; en estos casos no es infrecuente planear un abordaje ilioinguinal similar al utilizado en fracturas acetabulares de columna anterior, para extraer la copa por dicha ventana y posteriormente realizar el trabajo final por el abordaje de costumbre, como se aprecia en la figura 11. TRATAMIENTO. Como se ha dicho anteriormente, lo más importante es planear y anticiparse al evento, en aquellos casos complejos; siempre debemos realizar este tipo de cirugías en instituciones que cuenten con un adecuado banco de sangre, así como cirujano vascular o cirujano con experiencia en este tipo de casos. Una vez presentado el evento, se debe realizar el control del sangrado por parte del ortopedista, al tiempo que anestesia realiza la reanimación respectiva, con adecuada reposición de la volemia; a pesar de que ciertos vasos pequeños pueden solucionarse con electrocoagulación y/o ligadura, los vasos principales siempre deben ser reparados y/o de acuerdo con su importancia funcional, ligados. El empaquetamiento pélvico puede ser de utilidad como medida de control, Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT ralmente por displasia y quien tiene secuelas de fractura de acetábulo; es muy importante en este tipo de pacientes, informarle del mayor riesgo y en aquellos casos de caderas congénitas Crowe III y IV, de la casi certeza que el nervio sufra al momento de elongarse para lograr la ecualización de su extremidad. Durante el examen físico, doy mucha importancia a las retracciones visibles, producto de cirugías previas, así como a la prueba de distracción de la extremidad para ver que tanto se logra ecualizar realizando esta maniobra, ya que una vez esté relajado por el acto anestésico, seguramente podremos corregir discrepancias sin necesidad de osteotomías. Figura 11. Copa migrada, retiro mediante abordaje inguinal. mientras disponemos de un cirujano vascular en el quirófano, así como la presión intraabdominal sobre el trayecto más proximal de los vasos. Cuando por el contrario, sospechamos un evento trombótico en el postoperatorio inmediato, debemos realizar los estudios de rigor para descartarlos y buscar restablecer el flujo sanguíneo en las primeras 12, ojalá 6 horas posteriores al evento, lo cual con frecuencia no se puede lograr, debido al tipo de anestesia y/o analgesia postoperatoria que oscurece la sintomatología, siendo estos los casos de peor pronóstico; con frecuencia se deben utilizar injertos para retirar el segmento dañado y poder restablecer el flujo sanguíneo. MANEJO PREFERIDO DEL AUTOR. El paciente con mayor riesgo, es aquel con cirugías previas, anisomelia marcada, gene- Durante el acto quirúrgico, presto especial atención a evitar la tracción innecesaria del mismo; la liberación de tejidos blandos, dado por una completa capsulectomía para el caso de las caderas displásicas, es algo de primordial importancia; de igual manera, en casos de fracturas o deficiencias de la pared posterior, debemos utilizar el fresado articular con prudencia, tratando en lo posible de mantener separadas y lejos de las mismas las estructuras nobles; así mismo, se prefiere evitar retractores y separadores con punta, especialmente en la pared anterior, donde pueden causar una lesión neurovascular grave e incluso la muerte. En aquellos pacientes de riesgo, se deja en el post-operatorio la cadera y rodillas en ligera flexión (30 grados), lo cual ayuda a relajar la tracción excesiva y se incluye medicación para el dolor neuropático, amitriptilina 25 mg VO en la noche y/o Carbamazepina hasta 200 mg/ VO cada 12 horas ya que muchos pacientes con elongaciones mayores a los dos centímetros, a pesar de no presentar Neurapraxia, presentan disestesias y dolores severos, prueba de la elongación nerviosa. Una vez presentado el cuadro de Neurapraxia, la conducta instaurada debe ser agresiva y de soporte; estos pacientes tienen 221 “Temas selectos de actualización en la Ortopedia Latinoamericana” un seguimiento más periódico, se le instaura medicación para el dolor neuropático y se inicia un manejo interdisciplinario con la colaboración de fisiatría, clínica del dolor y fisioterapia. De rutina no se coloca férula en polipropileno para pie caído pero si un calzado suave, generalmente tipo bota, que ayude a soportar en algo la marcha; medidas locales para controlar los cambios neuropáticos y vasomotores, la atrofia progresiva y electrogimnasia facilitan el proceso de recuperación. Por regla general, sólo se ordena la primera electromiografía a los tres meses del post-operatorio, pues algunos pacientes recuperan antes su poder plantiflexor de manera parcial y se les explica que este primer reporte generalmente muestra un silencio absoluto y una línea de base plana, que servirá para evaluar la progresión en los subsecuentes estudios a realizar. En cuanto a las lesiones vasculares, es importante evaluar los factores de riesgo previos en cada paciente en particular; durante la exposición, prefiero no utilizar separadores de Hohmann para trabajar el acetábulo y buscar una medialización inicial dejando unos milímetros de trasfondo para reorientar en la posición deseada y evitar las fracturas; de igual manera, prefiero implantes con excelente Figura 12. Extracción copa intrapélvica por abordaje inguinal. press fit, y si debo colocar tornillos, siempre orientarlos en la zona de carga, dentro del huso horario de 11 a 1. En los casos de revisión por cemento intrapélvico o migración intraabdominal, prefiero un abordaje ilioinguinal en decúbito supino, separar los grandes vasos y posteriormente realizar el retiro de dichos componentes, como se aprecia en la figura 9; nunca debemos desestimar esta complicación por lo que debemos contar con un banco de sangre las 24 horas, así como un cirujano vascular o entrenado en este tipo de complicaciones dentro del staff del servicio. BIBLIOGRAFÍA 1. Lewallen, David, G. Instructional Course Lectures, The American Academy Of Orthopaedic Surgeons - Neurovascular Injury Associated With Hip Arthroplasty Journal. Bone Joint Surg79 (A):1870-80 (1997) 2. Ereth, M. H.; Weber, J. G.; Abel, M. D.; Lennon, R. L.; Lewallen, D. G. Et Al..: Cemented Versus Noncemented Total Hip Arthroplasty—Embolism, Hemodynamics, And Intrapulmonary Shunting. Mayo Clin. Proc., 67: 1066-1074, 1992. 3. Herndon, J. H.; Bechtol, C. O.; And Crickenberger, D. P.: Fat Embolism During Total Hip Replacement. A Prospective Study. J. Bone And Joint Surg., 56-A: 1350-1362, Oct. 1974. 4. Orsini, E. C.; Byrick, R. J.; Mullen, J. B. M.; Kay, J. C.; And Waddell, J. P.: Cardiopulmonary Function And Pulmonary Microemboli During Arthroplasty Using Cemented Or Non-Cemented Components. J. Bone And Joint Surg., 69-A: 822-832, July 1987. 5. Johanson, N. A.; Pellicci, P. M.; Tsairis, P.; And Salvati, E. A.: Nerve injury in total hip arthroplasty. Clin. Orthop. 179: 214-222, 1983. 222 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 6. Edwards, B. N.; Tullos, H. S.; And Noble, P. C.: Contributory Factors And Etiology Of Sciatic Nerve Palsy In Total Hip Arthroplasty. Clin. Orthop. 218: 136-141, 1987. 7. Wasielewski, R. C.; Crossett, L. S.; And Rubash, H. E.: Neural And Vascular Injury In Total Hip Arthroplasty. Orthop. Clin. North America, 23: 219-235, 1992. 8. Nercessian, O. A.; Macaulay, W.; And Stinchfield, F. E.: Peripheral Neuropathies Following Total Hip Arthroplasty. J. Arthroplasty, 9: 645-651, 1994. 9. Shaughnessy, W. J.; Kavanagh, B.; And Fitzgerald, R. H., Jr.: Long-Term Results Of Total Hip Ar- throplasty In Patients With High Congenital Dislocation Of The Hip. Orthop. Trans., 13: 510, 1989. 10.Schmalzried, T. P.; Amstutz, H. C.; And Dorey, F. J.: Nerve Palsy Associated With Total Hip Replacement. Risk Factors And Prognosis. J. Bone And Joint Surg., 73-A: 1074-1080, Aug. 1991. 11.Seddon, H. J.: Three Types Of Nerve Injury. Brain, 66: 237-288, 1943 12.De Hart, M.m., Ryley, Jr, L.h. Nerve Injuries In Total Hip Arthroplasty. Journal A.a.o.s. Vol 7. # 2March/April 1999. P. 101-111. 13.Bodine, S.c., Lieber, R.l: Peripheral Nerve Physiology, Anatomy, And Pathology, In Simon Sr (Ed): Orthopaedic Basic Science. Rosemont, Ill: American Academy Of Orthopaedic Surgeons, (Aaos) 1994, Pp 325-396. 14.Lundborg, G, Rydevik, B.: Effects Of Stretching The Tibial Nerve Of The Rabbit: A Preliminary Study Of The Intraneural Circulation And The Barrier Function Of The Perineurium. J Bone Joint Surg Br 1973; 55:390-401. 15.Lundborg, G: Structure And Function Of The Intraneural Microvessels As Related To Trauma, Edema Formation, And Nerve Function. J Bone Joint Surg (A) 1975; 57: P. 938-948. 16.Weber, E.r, Daube, J.r., Coventry, M.b: Peripheral Neuropathies Associated With Total Hip Arthroplasty. J Bone Joint Surg (A) 1976; 58: P. 66-69. 17.Navarro, R. A.; Schmalzried, T. P.; Amstutz, H. C.; And Dorey, F. J.: Surgical Approach And Nerve Palsy In Total Hip Arthroplasty. J. Arthroplasty, 10: 1-5, 1995 18.Hanssen, A.d, Mariani, E.m, Kavanagh, B.f, Coventry, M.b: Resection Arthroplasty (Girdlestone Procedure), Nerve Palsies, Limb Length Inequality, And Osteolysis Following Total Hip Arthroplasty, In Morrey Bf (Ed): Joint Replacement Arthroplasty. New York: Churchill Livingstone, 1991, Pp 897-905. 19.Kennedy Wf, Byrne Tf, Majid Ha, Pavlak Ll: Sciatic Nerve Monitoring During Revision Total Hip Arthroplasty. Clin.orthop. 1991; 264:223-227. 20.Jacobs, L.g., Buxton, R.a.: The Course Of The Superior Gluteal Nerve In The Lateral Approach To The Hip. J Bone Joint Surg. (A) 1989; 71: P.1239-1243. 21.ABITBOL, J.J, GENDRON, D., LAURIN, CA, BEAULIEU, M.A.: Gluteal nerve damage following total hip arthroplasty: A prospective analysis. J Arthroplasty 1990; 5: p. 319-322. 22.HARDINGE, K.: The direct lateral approach to the hip. J. Bone and Joint Surg., 64-B (1): 17-19, 1982. 23.SIMMONS, C., Jr.; IZANT, T. H.; ROTHMAN, R. H.; BOOTH, R. E., Jr.; and BALDERSTON, R. A.: Femoral neuropathy following total hip arthroplasty. Anatomic study, case reports, and literature review. J. Arthroplasty, 6 (Supplement): 57-S66, 1991. 223 “Temas selectos de actualización en la Ortopedia Latinoamericana” 224 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Osteotomías alrededor de la Cadera. Rodrigo Pesantez Reynoso M.D. Q. E. P. D. Hospital Universitario San José Alejandro López Cardona Nicolás Restrepo Giraldo. INTRODUCCIÓN La Displasia residual de cadera en el adulto joven, es una frecuente causa en nuestro medio, tanto de consulta como de discapacidad laboral; a pesar de que los controles en los primeros meses de vida se han convertido en una bandera institucional de salud, todavía seguimos viendo las secuelas de pacientes que nunca fueron tratados, o recibieron un tratamiento parcial, llevando a diferentes grados de descubrimiento de la cadera, anisomelia, cojera y dolor (1, 2, 3). nos enfrentamos a pacientes con este tipo de patología que informados por la tecnología moderna, buscan una solución no artroplástica a su problema; es nuestro deber conocer las diferentes opciones desde el punto de vista acetabular, para tratar de mejorar la biomecánica articular, impidiendo o por lo menos retardando la solución protésica final, en aquellos pacientes con caderas congruentes, no deformes, y que no aceptan un Reemplazo Total de Cadera. Por otra parte, a pesar de tener controles iniciales, somos conscientes de la existencia de la llamada “Displasia silente” (2), incluso en pacientes con radiografías normales al tercer o cuarto mes, que desarrollan un acetábulo plano y la cabeza femoral empieza a migrar supero/lateralmente. A pesar de que esta patología es manejada inicialmente por el Ortopedista Infantil, desde la adolescencia HISTORIA NATURAL. El paciente que llega a la vida adulta con una Displasia residual, tiene una desventaja biomecánica progresiva, que lentamente terminará por generar un proceso artrósico; en la medida que el paciente va creciendo y somete su cadera displásica a la carga diaria, va produciendo cambios anátomo-patológicos; las fuerzas supero-exter- 225 “Temas selectos de actualización en la Ortopedia Latinoamericana” Figura 1. Diferentes grados de displasia residual hasta franca luxación inveterada. nas vectoriales (4), van lateralizando la cabeza femoral, elongando el ligamento redondo la cápsula ligamentos y músculos periarticulares, aumentando la anteversión , aplanando la cabeza femoral y deformando el cuello femoral; en la medida que la subluxación aumenta, el apoyo se realiza en una pequeña parte de la región supero externa de la cabeza, disminuyendo el espacio articular en este nivel. De acuerdo con la severidad del problema, podemos encontrar displasias muy leves, moderadas, severas y francas luxaciones (Figura 1). Desde 1965, Murray demostró la relación entre la pérdida de la anatomía normal y el desarrollo de la Artrosis (5); para 1975, Stulberg y Harris (6) mostraban los cambios radiológicos incipientes, ahora conocidos como CAM, con su clásica deformidad en “cacha de revólver (Pistol Grip)”; para 1995, Murphy, Ganz y Müller (7), nos muestran cómo la posibilidad de desarrollar una Artrosis secundaria, está directamente relacionada con la severidad radiológica de la Displasia residual; mientras la cadera esté congruente y exista espacio articular, el paciente puede ser candidato para una Osteotomía que reoriente la superficie de 226 apoyo y por ende, distribuya mejor la carga, lo cual por lo menos teóricamente, detendría el proceso degenerativo; sin embargo, las Osteotomías, son parte del armamentario no artroplástico que podemos ofrecer en este tipo de pacientes, ya que a pesar de quedar algunas opciones en el olvido, también se puede realizar: • Osteotomías femorales • Artroscopia • Artrodesis • Artroplastia de resección Mientras la Artroscopia, cada vez tiene indicaciones y detalles técnicos más estandarizados (8), las otras opciones, por su morbilidad y secuelas inherentes, prácticamente no se ofrecen o ningún paciente las acepta en la actualidad. Tönnis (9) en 1999, publica su Clasificación de la Osteoartrosis, basada en los cambios radiológicos, dividiéndolo en 4 grupos desde el =, sin signos de artrosis, hasta el 3, con artrosis severa (Tabla1), en el que sólo serviría una Artroplastia Total. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Figura 2. Estadíos radiológicos de Tönnis de 0 a 3. hasta el punto de ser la conducta terapéutica de elección en ciertas instituciones ampliamente reconocidas (12, 15, 17, 18, 19). Tabla 1. Clasificación radiológica de la Artrosis según Tönnis. Esta clasificación también es importante, pues la literatura indica que los procedimientos quirúrgicos no artroplásticos realizados en pacientes con Artrosis radiológica moderada o severa (Tönnis 2 o 3) tienen un pobre desenlace y su pronóstico a corto plazo es malo (7, 8, 9, 10, 11); con el advenimiento de la Osteotomía “Bernesa”, popularizada desde 1988 por Reinhold Ganz (10), las diferentes variantes en la técnica quirúrgica nos han mostrado que este procedimiento es uno de los mejores para solucionar de manera efectiva y en el largo plazo, la Displasia residual de la cadera (11, 12, 13, 14, 15, 16), BIOMECÁNICA. Diferentes tipos de osteotomías fueron muy populares antes de la Artroplastia; sin embargo, con la mejoría en los desenlaces en pacientes con reemplazos articulares, comparativamente con resultados no tan alentadores a mediano plazo, este tipo de cirugía, principalmente las Osteotomías femorales, fueron disminuyendo en su utilización (20, 21, 22); sin embargo, la posibilidad potencial que tienen las Osteotomías de proveer una cadera durable, retardando o incluso en algunos casos evitando una Artroplastia Total, hace que estos procedimientos puedan ser atractivos para pacientes muy jóvenes con caderas moderadamente congruentes; la mayoría de los efectos benéficos de una Osteotomía, se pueden explicar desde el punto de vista biomecánico por disminución de la carga sobre la cadera, disminución del stress o ambas; teóricamente, la carga puede se puede disminuir de diferentes formas (4, 22, 23, 24, 25): • Aumentando el brazo de palanca de los músculos periarticulares • Relajando la cápsula tensa • Relajando la musculatura tensa 227 “Temas selectos de actualización en la Ortopedia Latinoamericana” • Desplazando parte de la carga de la cabeza femoral a otra porción del fémur proximal Por otro lado, si aumentamos la zona de carga, obviamente podremos disminuir el stress, incluso sin cambiar efectivamente la carga; mientras que las osteotomías femorales afectan directamente la transmisión de la fuerza mediante varo, valgo, anteversión y/o retroversión, relajando diferentes grupos musculares, las Osteotomías acetabulares pretenden aumentar la zona de carga después de una reorientación y/o aumentación acetabular para distribuir mejor la presión por una mayor área, como se puede apreciar en la Figura 3. Por otra parte, algunas Osteotomías acetabulares como el Chiari, pueden medializar el centro de rotación de la cadera, disminuyendo las fuerzas reactivas articulares (4, 12, 16); sin embargo, esta tipo de Osteotomías cuenta con una metaplasia del hueso supra-acetabular que soportará la cabeza, hacia una diferenciación a Fibrocartílago, que mecánicamente tiene propiedades inferiores en cuanto a soporte de carga (Figura 4). INDICACIONES Este tipo de procedimiento, debe limitarse a pacientes jóvenes con displasia residual de cadera sintomática (dolor, limitación funcional progresiva y cojera), sin excesiva migración proximal del centro de rotación, buenos Figura 3. Corrección biomecánica de la Osteotomía de Ganz Figura 4. Osteotomía de Chiari bilateral,15 años después. 228 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT arcos de movimiento (flexión mayor de 90°, abducción mayor de 30°) y pocos cambios degenerativos (Estadíos de Tönnis 0 o 1). Millis y Ganz, evaluando los resultados de su Osteotomía (10, 26, 27), refieren que se obtuvieron los peores resultados cuando se indicó este tipo de procedimientos en pacientes con: • Incongruencia articular severa • Tönnis 2 o más • Desgarro labral asociado • Edad mayor de 35 años En estos pacientes, la tasa de falla antes de 8 años era del 95%, por lo que se justifica ser estricto en los parámetros de inclusión para realizar una Osteotomía acetabular; por otro lado, como en muchas de las cirugías en articulaciones que soportan carga, el índice de masa corporal puede afectar los resultados a mediano y largo plazo. CONTRAINDICACIONES Este tipo de procedimientos se contraindica en Artrosis metabólicas, Artritis reumatoidea, severa incongruencia y/o deformidad articular, caderas rígidas, así como en pacientes obesos; en estos casos, es importante hablar con el paciente y escoger una alternativa artroplástica, de acuerdo con las expectativas, ajustadas a la tribología moderna. Es importante, a la hora de decidir una Osteotomía, hablar con el paciente y conocer sus expectativas, su edad no sólo real sino su edad ósea ajustada, su edad mental, función laboral, práctica de actividades deportivas y demás factores que pueden influir, de manera positiva o negativa en nuestros desenlaces; una cirugía ideal es aquella que es capaz de resolver un problema para el que está diseñada, sin generar más; igualmente que sea reproducible, tenga baja morbi/mortalidad y genere satisfacción tanto en el paciente como en el cirujano. Toda osteotomía supone de por sí, una técnica demandante, un excelente planeamiento y de parte de nuestro paciente una gran colaboración, de allí que sea importante que el candidato sea el ideal para este gran esfuerzo quirúrgico; debemos contar con un paciente comprometido en su rehabilitación, con sintomatología grave que estemos seguros ha de mejorar con el procedimiento, una anatomía corregible mediante la Osteotomía seleccionada específicamente para el caso en particular, y lo que se puede llamar un “Indice terapéutico favorable” dado por un adecuado arco de movimiento, masa muscular y congruencia, que permitan inferir un buen resultado; a mi juicio, si no se cumplen estas expectativas, a pesar de sonar radical, es mejor explicar al paciente la historia natural de la enfermedad y decidir un procedimiento artroplástico cuando el paciente, su dolor y discapacidad lo ameriten. En el momento actual, donde los pacientes están enterados de los desenlaces esperados, desean una recuperación pronta y no toleran un post-operatorio tortuoso, entender que una osteotomía genera un periodo de descarga mayor, una rehabilitación y desenlace más lento, hace que sea primordial la buena relación médico-paciente para estos procedimientos. EVALUACIÓN CLÍNICA. Una detallada anamnesis nos ayuda a comprender la patología, el grado de discapacidad, así como las expectativas que el paciente tiene respecto al manejo de su enfermedad; por lo general, el paciente que es candidato a una osteotomía, presenta dolor, limitación funcional y cojera que no es tan severa como el paciente artrósico, que requiere una artroplastia; es importante guiar el interrogatorio para descartar sintomatología causada por un pinzamiento fémoro-acetabular, donde los principios terapéuticos pueden variar (17, 19, 24, 26, 27, 28, 29). Por lo general, el paciente con secuelas de Displasia, puede presentar un 229 “Temas selectos de actualización en la Ortopedia Latinoamericana” Figura 5. Test de aprehensión anterior y de pinzamiento anterior. dolor mecánico, que aumenta proporcionalmente con la duración y/o tipo de actividad, cede con el reposo, asociado a un dolor trocantérico lateral, producto de la debilidad de la musculatura abductora, mientras que el paciente con pinzamiento, refiere un dolor inguinal, con la típica señalización de la “mano tomando toda la corva”. Típicamente, las displasias residuales que cursan sin artrosis, tienen buenos arcos de movimiento, no así los pacientes que presentan pinzamiento, donde pueden verse comprometidos la rotación interna en flexión y la abducción, o en aquellos con artrosis establecida, donde la cadera es francamente hipomóvil o rígida. En las caderas displásicas, dependiendo el grado de lateralización y/o subluxación, podemos encontrar acortamiento real e incluso un signo de Trendelemburg; en ellos, puede coexistir el llamado “Test de aprehensión anterior”, en el que se presenta dolor realizando extensión, adducción y rotación externa, diferente del Test de Pinzamiento, en el que el dolor se genera con flexión de 90°, adducción mas rotación interna, patognomónico de enfermedad labral y/o pinzamiento anterior (17, 29, 30), como lo muestra la figura 5. IMAGENOLOGÍA. Por lo general, las ayudas diagnósticas más útiles son las radiografías simples; una 230 verdadera AP de Pelvis y un falso perfil de Lequesne (31), permiten planear la mayoría de las Osteotomías; actualmente para descartar pinzamiento, se utilizan otras proyecciones diferentes como las de Dunn, la de Von Rosen, lateral Cross Table y otras, que no se mencionarán en este capítulo. Por lo general, la mejor forma de evaluar la lateralización de una cadera, es con el Angulo Centro-borde de Wiberg (32) que debe ser mayor de 20°, (Figura 6), mientras que el falso perfil permite evaluar el grado de descubrimiento posterior, para planear su cobertura. (31). Figura 6. Angulo CE, % descubrimiento y arco de Shenton. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT OSTEOTOMÍAS ACETABULARES. Como se ha dicho anteriormente, el objetivo de una cirugía de preservación articular es restaurar la estabilidad articular, disminuyendo la carga patológica sobre el borde acetabular, sin crear tampoco una incongruencia o por una reorientación exagerada, un pinzamiento; a pesar de que la gran mayoría de los cambios anatómicos son acetabulares y por ende, la corrección sería conveniente hacerla de ese lado articular, con la considerable ventaja de no crear una deformidad tridimensional compleja en el fémur proximal en caso de requerir una futura artroplastia; sin embargo, de existir alteraciones severas en el fémur proximal que puedan ser corregidas mediante osteotomía a ese nivel, o la deformidad sea mixta, podría requerirse una osteotomía en el fémur proximal o en los dos niveles, simultanea o estadiada (17, 19). Existen infinidad de osteotomías acetabulares, que podríamos dividir en dos grandes grupos: • Reconstructivas, cuyo objeto es lograr mediante un adecuado realineamiento, restaurar la biomecánica normal y la anatomía, lo cual a futuro generará una mejor función y retardará e incluso ocasionalmente, detendrá el proceso artrósico; de acuerdo con los sitios de resección pueden actuar sobre una, dos o las tres partes del iliaco, como el Salter, Pemberton, Sutherlan, Steel y Ganz entre otras. • De salvamento, en aquellos casos en los que la marcada deformidad y/o incongruencia articular, sólo permiten mejorar el área de carga, con lo que disminuye el stress y la sintomatología puede revertir, como es el caso de la Osteotomía de Chiari o el Staheli. (Figura 7) (1, 17, 19, 25, 26, 33, 34, 35, 36, 37, 38) Mientras que en el esqueleto inmaduro, podemos elegir entre un sinnúmero de Os- Figura 7. Osteotomías reconstructivas (Salter) y de salvamento (Chiari) cada una de 15 años de evolución. teotomías reconstructivas, pues la capacidad de remodelación con un cartílago trirradiado abierto, es buena, en los adultos jóvenes las osteotomías rotacionales tipo Wagner o las periacetabulares tipo Ganz, muestran los mejores resultados a largo plazo (17, 19, 26, 39, 40, 41, 42 ). En Colombia el precursor de esta técnica fue el Dr. Javier Pérez Torres, quien en la Revista Colombiana de Ortopedia de Julio de 1996, publica una modificación de la técnica original de Ganz, tratando 74 caderas en 62 pacientes, en la que se preserva la integridad de la columna posterior, entrando solo por la cara medial del ilíaco, lo que mejora la estabilidad y la vasculatura (43). Casi diez años después, los mismos autores principales, presentan su experiencia en menores de 14 años, con 22 caderas y buenos resultados (44). Para la fecha, el Dr. Pérez cuenta con más de 1000 casos y ha entrenado a la mayoría de los ortopedistas colombianos que realizamos este procedimiento; para la fecha, la Osteotomía de Ganz se ha popularizado, siendo posiblemente la Osteotomía más utilizada en el mundo para el tratamiento y corrección de la Displasia del adulto joven (1, 10, 13, 15, 19). Técnica de la Osteotomía de Ganz. La técnica original descrita utilizaba un abordaje de Smith – Petersen, para exponer la cara interna y externa del iliaco (10), desin- 231 “Temas selectos de actualización en la Ortopedia Latinoamericana” sertando el Sartorio, Tensor de la Fascia Lata y la porción anterior del glúteo medio. Una vez se llega a la cápsula, se hace una disección lateral y luego de una perfecta disección, se realizan los cortes en isquion, pubis y tabla iliaca de manera completa llegando a la columna posterior, para después rotar el fragmento en lo posición deseada y estabilizarlo con tornillos de cortical. Esta disección pronto mostró en la literatura una incidencia no despreciable de complicaciones inherentes al tamaño de la cirugía, así como a la inestabilidad generada, presentándose necrosis del acetábulo, pérdida de corrección, sobrecorrecciones y osificación heterotópica entre otros (10, 11, 12, 13, 14, 26). La técnica usada por el autor, es la misma modificada por Pérez y colaboradores, que se explica en detalle a continuación: Preparación: se coloca el paciente en decúbito supino, periné rasurado, y se lava toda la extremidad mas todo el iliaco (Figura 8). Una vez colocados los campos se trabaja con flexión de rodilla 20 a 30°. Incisión: Ilio-inguinal, ligeramente superior y proximal a la espina iliaca antero/superior, que permite ser cubierta por el interior femenino; una vez abierta la fascia, se procede a buscar, reparar y liberar el Nervio Fémorocutaneo (Figura 9); Exposición de tabla interna y rama púbica. Se diseca la musculatura de la tabla interna y se expone el tendón del psoas, que se retrae con una pinza tipo Rochester y se tenotomiza; inmediatamente queda expuesta la tabla interna (Figura 10); de Figura 8. Preparación y lavado Figura 9. Incisión y reparo del Nervio Fémorocutaneo. 232 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Figura 10. Exposición de tabla interna y psoas. manera rutinaria en la porción proximal de la herida se encuentra el agujero nutricio, que debe ser cauterizado, para evitar sangrado. Exposción ciega de rama isquio-púbica. Una vez disecado el periostio de la rama ilio-púbica, se desciende distal a la misma con ayuda de un elevador de periostio, tratando de llegar al agujero obturatriz y disecando la rama isquio-púbica; es importante disecar muy bien esta zona, porque la colocación del osteotomo angulado de Ganz es casi ciega, basándose en la prominencia infra-acetabular abajo del ligamento trasverso. En este punto si existe diuda, se puede tomar una proyección fluoroscópica para verificar tanto la posición como la orientación, para evitar un corte intraarticular (Figura 11). Osteotomía de la rama ilio-púbica. Se procede a realizar el segundo corte, en la rama ilio-púbica ya expuesta, cerca al acetábulo (Figura 12). Se debe comprobar que el corte esté completo, pues con frecuencia, de no ser así, puede haber dificultad posterior para rotar la Osteotomía. Figura 11. Posicionamiento del osteotomo y corte del isquion. Figura 12. Osteotomía rama púbica. 233 “Temas selectos de actualización en la Ortopedia Latinoamericana” Demarcación de la Osteotomía en tabla iliaca interna. Una vez se han realizado los dos cortes en las ramas del pubis, se procede a delinear la osteotomía, que asciende de la espina iliaca anteroinferior inclinada hacia la parte más delgada de la tabla ilíaca en la porción supra acetabular, aproximadamente a 120° se orienta trasversa hacia la columna posterior y a un centímetro aproximado de la misma, desciende paralela a la columna, para luego descender a tomar el corte de osteotomía incompleta de la rama isquio-púbica (Figura 13). Previo a realizar la Osteotomía, es conveniente realizar dos perforaciones a nivel de los ángulos (Figura 14), para evitar que durante el proceso de corte con los osteotomos, se pueda propagar como una fractura, de difícil resolución. Reorientación de la Osteotomía. Una vez realizados los cortes, se completan con osteotomo, tratando de llegar desde el corte paralelo a la columna posterior, al corte del isquion para completar la osteotomía (Figura 15) Una vez se siente que la osteotomía está completa, se puede colocar un clavo de scahnz paraleo al primer corte, que permitirá movilizar el fragmento en la posición deseada; generalmente. Se pretende lateralizar, anteriorizar por lo que la punta del hexágono Figura 13. Demarcación de corte en tabla iliaca interna. Figura 14. Perforaciones previas en tabla ilíaca interna. 234 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Figura 15. Reorientación de la Osteotomía. Figura 16. Colocación de clavo de Schanz para desplazamiento. osteotomizado se trata de colocar debajo del iliaco y algo hacia distal, lo que corregirá el Arco de Shenton (Figura 16). Fijación de la Osteotomía. Una vez se haya corroborado el desplazamiento, el cambio en la orientación de la “Ceja de Pauwels” y la corrección lograda (puede hacerse una verificación fluoroscópica), la osteotomía se fija con dos tornillos de cortical que van de proximal a la Espina Iliaca Antero-Superios (EIAS), uno hacia la columna anterior (Figura 17) y el otro hacia la columna posterior (Figura 18). 235 “Temas selectos de actualización en la Ortopedia Latinoamericana” Figura 17. Inclinación tornillo hacia anterior para fijación. Tornillo antirrotatorio. Aunque inicialmente se dejaba una pequeña porción de rama ilio-púbica unida al acetábulo y desde allí se dirigía un tornillo hacia posterior para hacer el cierre, en la actualidad, este tornillo se dirige retrógrado hacia la escotadura, tratando de hacer presa en el esponjoso de la tabla, con lo que podemos evitar una rotación exagerada o un desplazamiento de la fractura. Este no es un tornillo fácil de colocar, ya que con frecuencia se debe dirigir entre los dos tornillos y puede golpear e incluso romper la broca; un buen truco es colocarlo más proximal, con frecuencia utilizando el orificio dejado por el clavo se Schanz que se 236 utiliza para reorientar y mover la osteotomía (Figura 19). Una vez lograda esta fijación, se procede a realizar el lavado y cierre por planos. Esta Osteotomía puede sangrar moderadamente, sobre todo en el momento de hacer la disección ciega y empezar las osteotomías de las ramas, pero una vez reorientada y estabilizada con sus tornillos el sangrado cesa. El control radiológico mostrará la corrección (Figura 20) Manejo Post-operatorio. El primer día Post-operatorio se puede dar de alta con apoyo parcial de 10 kilogramos Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Figura 19. Colocación y orientación del tornillo anti/rotatorio. Figura 20. Pre y post-operatorio con dos muletas, analgésicos, anti-inflamatorios no esteroideos y plan de fisioterapia agresiva que incluya manejo de desensibilidad en la zona del Fémoro-cutaneo. En la medida que se logre la consolidación, el apoyo se incrementará semana a semana y generalmente al tercer mes, se da apoyo total sin ayudas externas. Osteotomías en el fémur proximal. Aunque las Osteotomías femorales han caído en desuso, tal vez, por la versatilidad y gran capacidad de corrección que ofrece la Osteotomía Periacetabular tipo Ganz, existen aún indicaciones claras para el manejo correctivo de la deformidad desde el lado femoral; aunque simplista, la filosofía de hace varias décadas donde se decía que la corrección se debe hacer donde existe el problema, es decir “ si la alteración es acetabular, el manejo debe hacerse en el acetábulo, mientras que si la deformidad está en el fémur, es allí donde debe corregirse” (4, 5, 6) no está reevaluada del todo; patologías como secuelas de Perthes, osteonecrosis y deslizamientos epifisarios femorales proximales, generan un daño tal en el fémur proximal, que ameritan muchas veces la corrección a este nivel. Las osteotomías correctoras en el fémur proximal tienen diversas técnicas y se pueden practicar a diferentes niveles: basicervicales, a nivel de cuello, inter o subtrocantéricas (20, 21, 25, 29); entre más proximal la osteotomía, más potencial tiene esta de corregir las defor- 237 “Temas selectos de actualización en la Ortopedia Latinoamericana” Figura 21. Reconstrucción mediante Tomografía. midades causadas en los deslizamientos epifisarios que con una osteotomía intertrocantérica, a costo de tener más riesgo de daño vascular y por ende, una mayor incidencia de necrosis avascular post-operatoria. Las Osteotomías intertrocantéricas, realizadas proximal al trocánter menor, permiten un sinfín de combinaciones para dar flexión, extensión, varo o valgo a la cadera enferma; de igual manera, existen autores que preconizan cuñas completas, hemicuñas e incluso cuñas abiertas para reorientar las cargas y hacerlas más congruentes con el acetábulo (4, 16, 17, 19); en estos casos, el clásico abordaje de “Smith- Petersen” o sus variaciones actuales, permiten exponer el fémur y de ser necesario, exponer la cápsula anterior y mediante artrotomía, la misma cabeza femoral; con los nuevos diseños de implantes, existen así mismo, placas LCP para correcciones específicas, que facilitan mucho este tipo de procedimientos; sin embargo, una de las partes más importantes de esta técnica es un adecuado planeamiento, basado en múltiples radiografías que nos permitan evaluar la cadera en diferentes posiciones y determinar con ello, cual es la mejor opción para lograr la cobertura ideal; ocasionalmente y aprovechando la tecnología moderna, recosntrucciones mediante Tomografía, nos dan una 238 excelente idea del grado de descubrimiento y nos pueden ayudar al planeamiento (Figura 21) Osteotomía Varizante. Es tal vez, la Osteotomía femoral más utilizada; su candidato ideal es aquel que presenta: • Cabeza esférica • Poca displasia mínimo de 15°) (Angulo de Wiberg • Ceja de Pauwels Súpero/externa • Angulo Cérvico-diafisario mayor de 135° En estos pacientes, las proyecciones en abducción, con diferentes grados de rotación, nos mostrarán si es o no el candidato ideal (Figura 22) Por lo general, el planeamiento nos indica, cortando los fragmentos en la zona de Osteotomía y posteriormente reorientándolos, cómo va a quedar el ángulo cérvico-diafisario, la relación artículo trocantérica, la cobertura final y otras medidas importantes (Figura 23). Debemos recordar que las Osteotomías varizantes, deben medializar la diáfisis, Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Figura 22. Centramiento al tomar proyección en abducción y rotación. Figura 23. Planeamiento de Osteotomía Varizante. para no alterar de manera notoria el eje mecánico y disminuir la fuerza de la musculatura adductora; los inconvenientes de esta osteotomía es que produce un acortamiento variable, por lo que en deformidades mayores se prefiere realizar una hemicuña, genera un trocánter mayor prominente que cambia la forma de la cadera y da una debilidad de la musculatura abductora que puede persistir incluso después de un año de post-operatorio. Osteotomía Valguizante. Osteotomía preconizada por Bombelli (4), útil en cabezas no esféricas, en las que se aprovechan los osteofitos ya formados, para ponerlos en contacto y que sirviendo de fulcro, puedan ampliar el espacio articular en la zona de carga súpero-externa; al mismo tiempo el valgo traccionará la porción supero-externa de la cápsula, favoreciendo su metaplasia y ayudando a formar un osteofito de techo que aumente la superficie de carga (4, 16, 19, 26). Teóricamente, se puede logra una mejoría a largo plazo, tanto de la superficie articular, como de la sintomatología dolorosa debido a: 239 “Temas selectos de actualización en la Ortopedia Latinoamericana” • Cambio del apoyo de una superficie dolorosa inervada a una de contacto Osteofito/osteofito que no está inervada • Mejorando la congruencia articular en una cadera incongruente, lo que aumenta la superficie de apoyo, distribuyendo mejor la presión • Reorientando las líneas de fuerza de los principales grupos musculares que actúan sobre la cadera • Desplazando medial el centro de rotación de la cadera, lo cual disminuye el brazo de palanca del peso corporal. Estas osteotomías, adicionando cortes en los otros planos de tal manera que podamos corregir contracturas fijas en flexión y o descubrimientos anteriores, mediante una osteotomía extensora, mejorando la anteversión mediante una osteotomía desrrotadora o mezclando a necesidad cada componente, buscando mejorar el área de carga, para distribuir mejor el apoyo. Osteotomías Mixtas. Existen casos severos, donde a pesar de nuestro planeamiento y la toma cuidadosa de proyecciones en diferentes posiciones, la cobertura perfecta no se logrará a no ser que se hagan osteotomías en ambos niveles; en estos complejos casos, debemos planear y decidir si es prudente hacerlas en uno o en dos tiempo y al mismo tiempo, se le debe explicar al paciente y su familia, las implica- ciones a futuro que esto puede generar en el momento de requerir una Artroplastia Total. Método preferido por los autores. Las Osteotomías alrededor de la cadera, suponen un gran reto, conocimiento profundo de la Anatomía y Biomecánica de la Cadera, así como un planeamiento meticuloso del procedimiento, que parte de la explicación clara y concisa de los alcances y limitaciones de este tipo de cirugías a nuestro paciente; con el paso de los años y la depuración de la técnica, la Osteotomía de Ganz ha opacado las diferentes técnicas, tanto acetabulares como femorales, siendo el procedimiento de elección en más del 90% de nuestros casos. En caso de pensar que el paciente se beneficiará de una Osteotomía femoral, es muy útil asistir al servicio de radiología y tomarnos unos minutos para evaluar la cadera con fluoroscopia, para determinar las mejores opciones posibles y una vez seleccionadas las posibles variantes, solicitar los estudios radiológicos en físico para poder planear mejorla posición ideal que generalmente se alcanza con una osteotomía multiplanar que incluya desrotación con flexo/extensión varo o valgo. Respecto al abordaje de rutina, se prefiere la variante recta del abordaje clásico de Smith- Petersen; la fijación se logra de manera mucho más fácil y expedita, con los nuevos diseños específicos de sistemas de agujero combinado, tipo L.C.P. BIBLIOGRAFÍA 1. Gurd, D..P. Late Presenting Developmental Dysplasia Of The Hip. O.k.o.orthopedic Knowledge On Line, 2. Raimann, A., Baar, A., Raimann, R., Morcuende, J.a.. Late Developmental Dislocation Of The Hip After Initial Normal Evaluation. J. Ped. Orthop. (27) 2007, P.32-36. 3. Schwend, R.m., Schoenecker, P., Richards, B.s. Et Al. Screening The Newborn For Developmental Dysplasia Of The Hip. Now What Do We Do. J. Ped. Orthop. (27) 2007, P. 607-610. 4. Bombelli, Renato. La Artrosis De La Cadera. Editorial Salvat Editores, 1985. 240 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 5. Murray, R.o.: The Aetiology Of Primary Osteoarthritis Of The Hip. Br J Radiol (38) 1965: P. 810-824. 6. Stulberg, S.d., Cordell, L.d, Harris, W.h., Ramsey, P.l., Macewen, G.d.: Unrecognized Childhood Hip Disease: A Major Cause Of Idiopathic Osteoarthritis Of The Hip, In Amstutz Hc (Ed): The Hip: Proceedings Of The Third Open Scientific Meeting Of The Hip Society. St.louis, Mo: Cv Mosby, 1975, Pp 212-228. 7. Murphy S.b., Ganz R, Muller, M.e.: The Prognosis In Untreated Dysplasia Of The Hip: A Study Of Radiographic Factors That Predict The Outcome. J Bone Joint Surg. 77 (A): 1995, P.985–989. 8. Mccarthy, J.c., Mason, J.b., Wardell, S.r.: Hip Arthroscopy For Acetabular Dysplasia: A Pipe Dream? Orthopedics 1998;21:977–979. 9. Tönnis, D, Heinecke, A: Acetabular And Femoral Anteversion: Relationship With Osteoarthritis Of The Hip. J. Bone Joint Surg 81 (A) 1999: P.1747–1770. 10.Ganz, R, Klaue, K., Vinh, T.s., Mast, J.w.: A New Periacetabular Osteotomy For The Treatment Of Hip Dysplasias: Technique And Preliminary Results. Clin Orthop (232):1988P.26–36. 11.Crockarell, J Jr., Trousdale, R.t., Cabanela, M.e., Berry, D.j.: Early Experience And Results With The Periacetabular Osteotomy: The Mayo Clinic Experience. Clin Orthop (363), 1999 P. 45–53. 12.Husell, J.g., Mast, J.w., Mayo, K.a., Howie, D.w., Ganz, R: A Comparison Of Different Surgical Approaches For The Periacetabular Osteotomy. Clin Orthop (363), 1999, P 64–72. 13.Matta, J.m., Stover, M.d., Siebenrock,K. Periacetabular Osteotomy Through The Smith Petersen Approach. Clin. Orthop. (363) 1999, P.21-32. 14.Siebenrock, K.a., Schöll, E., Lottenbach, M., Ganz, R. Bernese Periacetabular Osteotomy. Clin. Orthop. (363) 1999, P. 9-20. 15.Trumble, S.j., Mayo, K.a., Mast, J.w. The Periacetabular Osteotomy: Minimum 2 Year Follow-Up In More Than 100 Hips. Clin. Orthop. (363) 1999, P. 54-63. 16.Trousdale, R.t., Ekkernkamp, A., Ganz, R., Wallrichs,S.l. Periacetabular And Intertrochanteric Osteotomy For The Treatment Of Osteoarthritis In Dysplastic Hips. J. Bone Joint Surg 77(A): 1995, P. 73-85. 17.Clohisy, J.c., Beaule, P.e., O´Malley, A. Safran, M.r., Shoenecker, P. Aoa Symposium: Hip Disease In The Young Adult. Current Concepts Of Etiology And Surgical Treatment. J. Bone Joint Surg. 90(A) 10 2008, P. 2267-2281. 18.Kim, Y.j., Ganz, R., Murphy, S.b., Buly, R.i., Millis, M.b. Hip Joint Preserving Surgery: Beyond The Classic Osteotomy. Instr. Course Lect. (55) 2006, P. 145-158. 19.Sierra, R. J., Trousdale, R.t., Ganz, R., Leuning, M. Hip Disease In The Young Active Patient: Evaluation And Nonarthroplasty Surgical Options. J. Am. Acad. Orthop. Surg. J.a.a.o.s. 16 (12) 2008: P. 689-703. 20.Brand, R.a. Hip Osteotomies: A Biomechanical Consideration. J. Am. Acad. Orthop. Surg. (5) 1997: P. 282-291. 21.Maquet, P., Radin, E.l. Osteotomy As An Alternative In Total Hip Replacement In Young Adults. Clin. Orthop. (123) 1977: P. 138-142. 22.Sokoloff, L. Osteoarthritis As A Remodeling Process: J.reumathol. Suppl. 14 1987 P. 7-10. 241 “Temas selectos de actualización en la Ortopedia Latinoamericana” 23.Pauwels, F. Biomechanics Of The Normal And Diseased Hip: Theoretical Foundation, Technique And Results Of Treatment: An Atlas. Berlin: Springer-Verlag, 1976: P. 129.272. 24.Lloyd-Roberts, G.c. The Role Of Capsular Changes In Osteoarthritis Of The Hip Joint. J. Bone Joint Surg. 35(B) 1953: P. 627-642. 25.Fergusson, A.b. Jr. High Inter-Trochanteric Osteotomy For Osteo-Arthritis Of The Hip. A Procedure To Streamline The Defective Joint. J. Bone Joint Surg. 46 (A), 1964: P. 1159-1175. 26.Millis, M., Poss, R., Murphy, S.: Osteotomies Of The Hip In The Prevention And Treatment Of Osteoarthritis. En Instructional Course Lectures Volume 41 1992,: 145. 27.Millis, M, Murphy, S.b.: Use Of Computed Tomographic Reconstruction In Planning Osteotomies Of The Hip. Clin. Orthop, 274: 1992. P. 154-159. 28.Beaule, P.e., Allen, D.j.,Clohisy, J.c. Et Al. The Young Adult With Hip Impingement. Deciding On The Optimal Intervention. J. Bone Joint Surg 91(A) 1: 2009, P. 210-221. 29.Clohisy, J.c., Shoenecker, P.l.. Diagnosing The Young Adult With Hip Pain, In Beule, P.e., Amadio P.c. Editors: The Young Adult With Hip Pain. A.a.o.s. Rosemont, Il, 2007, P. 1-11. 30.Parvizi, J. , Leunig, M., Ganz, R. Femoroaceabular Impingement. J. Am. Acad. Orthop. Surg. Jaaos, 15 (9) 2007, P. 561-570. 31.Lequesne, M. De Seze,S. Le Faux Profile Du Basin. Nouvel Incidenc Radiographique Par Létude De La Hanche: Son Utilité Dans Les Dysplasies Et Les Diferentes Coxopathies. Rev. Rhum. Mal. Osteoartic. (28) 1961, P. 643. 32.Wiberg, G. Studies On Dysplasic Acetabular And Congenital Subluxation Of The Hip Joint With Special Reference To The Complications Of Osteoarthritis. Acta Chir Scand. 83 Suppl. 58, 1939, P. 5-135. 33.Salter, R.b. Role Of Innominate Osteotomy In The Treatment Of Congenital Dislocation And Subluxation Of The Hip In The Older Child. J. Bone Joint Surg. 48 (A) 7: 1966, P. 1413-1439. 34.Sutherland, D..H., Greenfield, R. Double Innominate Osteotomy. J. Bone Joint Surg 59(A) 1977, P. 1082- 1091. 35.Steel, H.h. Triple Osteotomy Of The Innominate Bone. J. Bone Joint Surg. 55(A), 1973, P. 343-350. 36.Wagner, H. Experiences With Spherical Acetabular Osteotomy For The Correction Of The Dysplastic Acetabulum. In Weil, U.h. Editor. Acetabular Dysplasia: Skeletal Dysplasiasin Childhood. Berlin, Springer-Verlag 1978, P. 131-145. 37.Böhm, P., Brzuske, A. Salter Innominate Osteotomy For The Treatment Of Developmental Dysplasia Of The Hip In Children: Results Of Seventy-Three Consecutive Osteotomies After Twenty-Six To Thirty Five Years Of Follow-Up. J. Bone Joint Surg. 84 (A) 2002, P. 178-186. 38.Chiari, K. Medial Displacement Osteotomy Of The Pelvis. Clin. Orthop. (98) 1974, P. 55-71. 39.Leuning, M., Siebenrock, K.a., Ganz, R. Rationale Of Periacetabular Osteotomý And Background Work. Inst. Course Lect. (50) 2001, P. 229-238. 40.Siebenrock, K.a., Leuning, M., Ganz, R. Periacetabular Osteotomy: The Bernese Experience. Instr. Course Lect. (50) 2001, P. 239-245. 242 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT 41.Santore, R. F., Turgeon, T.r., Phillips, W.f. Iii, Kantor, S.r. Pelvic And Femoral Osteotomy In The Treatment Of Hip Disease In The Young Adult. Inst. Course Lect. (55) 2006, P. 131-144- 42.Millis, M.b., Kaelin, A. Schulntz, K Et Al. Spherical Acetabular Osteotomy For Treatment Of Acetabular Dysplasia In Adolescents And Young Adults. J. Ped. Orthop. 1(B) 1994, P. 47-54. 43.Perez, J., Murcia, M.a. Resultados Del Tratamiento De La Displasia Acetabular De La Cadera Utilizando Una Modificación De La Osteotomía De Ganz. Rev. Col. Ort. (10) Julio #2, 1996, P. 44.Torres, F., Torres, H., Perez, J., Murcia, M.a. Descripción De Los Resultados De La Osteotomía Periacetabular Modificada De Ganz En Niños Y Adolescentes Con Displasia Residual. Rev. Col. Ort. (20) # 1. Marzo 2006, P. 53-59. 243 “Temas selectos de actualización en la Ortopedia Latinoamericana” 244 Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Revisão de artroplastia de joelho Rogério Fuchs M.D. Membro titular da Sociedade Brasileira de Ortopedia e Traumatologia / Sociedade Brasileira de Cirurgia do Joelho Médico voluntário do grupo Joelho-Quadril do Hospital de Clínicas da Universidade Federal do Paraná – Curitiba/Paraná/Brasil Thiago Fuchs M.D. Membro titular da Sociedade Brasileira de Ortopedia e Traumatologia Estagiário (R4) no grupo de Joelho-Quadril do Hospital de Clínicas da Universidade Federal do Paraná – Curitiba/Paraná/Brasil INTRODUÇÃO As artroplastias totais de joelho (ATJ) são realizadas com muita frequência nos dias atuais, com excelentes resultados em relação à sobrevida do implante acima de 15 anos (1-2). As taxas anuais de ATJ estão aumentando progressivamente, pois a população está vivendo mais e são realizadas cirurgias em pacientes cada dia mais jovens. Um estudo (3) mostra as projeções de revisões de ATJ nos Estados Unidos que irão duplicar até o ano de 2015 e terão aumento em torno de 600% até o ano de 2030. Em torno de 5% observam-se falhas da ATJ, representando um número substancial, onde os cirurgiões ortopedistas estão observando um aumento do número de pacientes que inicialmente tinham uma ATJ muito satisfatória e com o passar do tempo apresentam dor, evidências radiográficas de soltura de algum componente e/ou incapacidade funcional devido à falência da sua ATJ (4). Quando comparamos as cirurgias de ATJ primárias com as revisões, observamos que o procedimento é tecnicamente mais difícil com maiores riscos de complicações. Frente a isto, é necessária uma abordagem sistemática para melhor definição da etiologia da falha, diagnóstico correto e também fazer um planejamento mais preciso para que a cirurgia tenha maior chance de sucesso. Antes de realizarmos uma revisão, devemos tentar conhecer a causa da dor pós-ATJ, uma vez que cirurgias de revisão por dores inexplicáveis têm poucas chances de apresentar resultados satisfatórios (5). O cirurgião deve procurar identificar os implantes, bem como procurar por possíveis comorbidades para que o paciente apresente 245 “Temas selectos de actualización en la Ortopedia Latinoamericana” boas condições para a cirurgia de revisão. Uma boa cicatrização da ferida operatória é crítica após uma revisão de ATJ. Se existir alguma dúvida, deve-se pedir o auxílio de um cirurgião plástico para avaliar a necessidade de possível retalho musculo- cutâneo. AVALIAÇÃO DA DOR PÓS-ATJ A etiologia da dor e/ou incapacidade funcional pós-ATJ pode ser variada e numerosa, levando-nos a uma análise criteriosa e sistemática para melhor definir o diagnóstico (6-7-8). Uma boa abordagem deve levar em conta: história, exame físico, exames de imagem e laboratoriais para definição da possível causa de falha. As etiologias podem ser agrupadas em duas categorias: intrínsecas ou intra-articulares e extrínsecas ou extra-articulares (9). • Intrínsecas / intra-articulares: infecção, instabilidade, mau alinhamento, soltura asséptica, desgaste polietileno, osteólise, fratura do implante, artrofibrose, interposição de tecidos moles, “clunk” patelar, implantes muito grandes (“overhang”), alterações do aparelho extensor (instabilidade patelar, fratura da patela, dor patelar, patela baixa, excesso de espessura da patela/ implante e ruptura do tendão patelar ou quadricipital). • Extrínsecas / extra-articulares: patologia do quadril e/ou coluna, neuroma, algodistrofia, claudicação vascular, processo inflamatório dos tecidos moles (bursites, tendinites) e fratura periprotética (fêmur, tíbia, patela). HISTÓRIA E EXAME FÍSICO A história e o exame físico são os primeiros pontos críticos na avaliação dos pacientes com dor e/ou incapacidade funcional pós-ATJ. Com frequência, somente com esta avaliação inicial podemos identificar ou eliminar possível etiologia. Os sintomas ou sinais iniciais (dor, derrame articular, insta- 246 bilidade ou rigidez) devem ser bem esclarecidos, bem como quando surgem, quanto tempo de duração, qual a frequência e tipo de atividade que se manifestam. A dor que estava presente antes da cirurgia primária e que persiste sem modificação, sugere uma etiologia extrínseca. A dor que surge dentro do primeiro ano da cirurgia sugere infecção, má rotação dos componentes ou interposição de tecidos moles. A dor que aparece após o primeiro ano, sugere desgaste do polietileno, osteólise, soltura ou infecção (aguda hematogênica ou crônica). As comorbidades como, diabete, estenose lombar e doenças vasculares periféricas devem ser consideradas. O exame físico deve incluir a inspeção visual, a palpação cuidadosa de pontos dolorosos ou derrame articular, testes de estabilidade em extensão, média flexão e 90° de flexão e finalmente a avaliação da estabilidade femoropatelar com possíveis pontos dolorosos da patela ou retináculas. Neste exame deve-se: • ver / observar o paciente caminhar; • mensurar o arco de movimento ativo e passivo; • avaliar o “tracking” patelar; • examinar a força muscular do quadríceps e vasto medial, bem como as condições neuro-vasculares do membro inferior; • examinar as articulações adjacentes (coluna, quadril, tornozelo e pé, pois uma deformidade com pé plano-valgo pode levar à falência de prótese com retenção do ligamento cruzado posterior-LCP) (10). AVALIAÇÃO RADIOGRÁFICA O exame das radiografias simples podem revelar muitas causas intrínsecas de dor em pacientes pós-ATJ e avaliar as radiogra- Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT fias seriadas feitas com o passar do tempo, incluindo do pré-operatório podem ser muito úteis para o diagnóstico. As radiografias longas incluindo quadril e tornozelo com apoio, perfil do joelho, axial da patela e quadril ipsilateral devem ser realizadas e avaliadas. As radiografias anteroposteriores podem mostrar desgaste do polietileno; osteólise; linhas radioluscentes; “overhang”, subsidência ou mudança de posição do componente tibial. As radiografias em perfil podem definir o tamanho do componente femoral, “offset” posterior do fêmur, altura e espessura patelar, “slope” do componente tibial e possível subsidência. O axial da patela pode mostrar inclinação da patela, mau alinhamento, “overhang” femoral, impacto femoropatelar lateral e a espessura do componente patelar. As radiografias seriadas são muito importantes e inestimáveis para definir sinais súbitos de soltura, como progressão tardia de linhas radioluscentes, mudanças ou fraturas no manto de cimento, progressão de osteólise ou mudança súbita da posição dos componentes. O exame por fluoroscopia pode ser útil para avaliar a interface de próteses não cimentadas. A extensão da osteólise é melhor avaliada pela tomografia computadorizada(TAC) ou pela ressonância magnética (RNM) com supressão de artefatos metálicos, porém estes não estão universalmente disponíveis (11). A TAC e a RNM também podem ser usadas para avaliar a rotação dos componentes femoral e tibial; o componente femoral é comparado com o eixo transepicondilar e o componente tibial é comparado com o 1/3 médio do tuberosidade anterior tibial (TAT). A rotação interna excessiva dos componentes pode estar associada com a instabilidade patelar (12) e frouxidão lateral em flexão, levando a má função clínica do joelho. A avaliação por radionuclídeos (cintilografia óssea) pode ser útil para o diagnóstico de soltura asséptica, infecção, algodistrofia e fraturas periprotéticas por estresse. Estes exames não são específicos e podem levar a resultados falsos positivos nos primeiros anos de pós-operatório. A cintilografia com Tecnécio99 mostra hipercaptação em torno de 90% dos componentes tibiais e 65% dos femorais até um ano pós-ATJ (13). Os exames de cintilografia para o diagnóstico de infecção são inconclusivos, sejam eles com Tecnécio99 ou com Índio111, de acordo com estudos já publicados. O uso do Índio111 tem valor para a exclusão de infecção quando for negativo. Pela facilidade, acurácia e o baixo custo da aspiração articular para análise do líquido sinovial e cultura, estes exames avançados de imagem devem ser usados somente como “segunda linha”, quando não é possível obter líquido sinovial pela aspiração (4). EXAMES LABORATORIAIS (PRÉ-OPERATÓRIOS) Todos os pacientes com falha ou dor pós-ATJ devem ser avaliados para infecção profunda periprotética. Mesmo se a causa da falha estiver evidente, infecção concomitante pode estar presente e o tratamento neste caso será totalmente diferente daquele de falha asséptica. O histórico médico do paciente e a história da cirurgia primária pode sugerir infecção. Os riscos relacionados ao paciente incluem diabete, artrite inflamatória, obesidade, história de infecção prévia no joelho, problemas de pele, cirurgias anteriores no joelho, desnutrição, insuficiência renal (principalmente com diálise) e imunodepressão. Os pacientes devem ser questionados sobre possível dificuldade de cicatrização da ferida operatória na cirurgia primária, uso prolongado de antibióticos ou retorno à sala de cirurgia. Se não houve alívio da dor desde a cirurgia, principalmente se é diferente da dor do pré-operatório, aumentam as suspeitas de infecção. Alguma doença recente que pode levar à bacteremia, pode indicar uma infecção hematogênica. Na presença de soltura de algum componente da prótese dentro de dois a cinco anos de pós-operatório deve ser considerada a possibilidade de infecção. 247 “Temas selectos de actualización en la Ortopedia Latinoamericana” Os exames básicos são a velocidade de eritrosedimentação (VHS) e o nível da proteína-C-reativa (PCR) que são sensitivos para identificar infecção, e é improvável que ambos estejam em níveis normais se houver infecção (14). Em estudos recentes (14-15) foi mostrado que se o VHS for menor que 30 mm/h e a PCR for menor que 10 mg/ dL é improvável que haja infecção. Então, devemos avaliar cada paciente para identificar aqueles que necessitam de testes adicionais. Se só um dos testes é anormal ou a suspeita permanece alta, deve-se aspirar a articulação e fazer exame de Gram, cultura, contagem de células brancas e diferencial do líquido sinovial. O paciente não deve receber antibiótico por um mínimo de duas semanas antes da aspiração para “otimizar” os resultados da cultura. A aspiração deve ser repetida se existe alta suspeita clínica. A contagem de células brancas do líquido sinovial de uma ATJ entre 1100 e 3000 cel/mm3 é altamente sugestiva de infecção (16-17). A percentagem de neutrófilos no líquido aspirado também é um marcador sensível para infecção. Se a percentagem estiver entre 60 e 80%, infecção é muito provável. Quando a contagem de células brancas for menor que 1100 cel/mm3 e a percentagem de neutrófilos for menor que 64%, o valor preditivo negativo é de 98,2%; por outro lado, quando os valores estão acima que aqueles valores mencionados anteriormente, o valor preditivo positivo é de 98,6% para infecção(15). A determinação destes valores do líquido aspirado é de baixo custo, objetivo, pode ser realizado no pré ou no intraoperatório, com fácil acesso a qualquer cirurgião em qualquer parte do mundo. EXAMES LABORATORIAIS (INTRAOPERATÓRIOS) A aparência do local da cirurgia e a coloração pelo Gram mostraram ser pouco sensitivos para detectar possível infecção. O exame anatomopatológico de tecidos periprotéticos mostrou ser muito útil para o diagnóstico de infecção (18). Entretanto, para este exame ser acurado e sensitivo é necessário ter 248 disponível um patologista experiente. O critério histológico para diagnóstico de infecção é controverso, mas no geral é aceito que mais que 10 polimorfonucleares por campo de grande aumento, o diagnóstico é infecção. PLANEJAMENTO PRÉ-OPERATÓRIO A cirurgia de revisão normalmente é mais difícil que as cirurgias primárias, porém com um planejamento adequado muitos cirurgiões podem realizála de maneira adequada e efetiva. O planejamento deve fazer parte de qualquer cirurgia, porém nas cirurgias de revisão de ATJ isto se faz muito mais necessário, para que surpresas não surjam durante a cirurgia, e se elas surgirem, as soluções já estejam presentes em nossa mente. A avaliação da causa da dor (geralmente o sinal mais comum) após ATJ é crítica e fundamental para firmar um diagnóstico correto e planejar o tratamento mais adequado. Uma revisão de ATJ realizada sem diagnóstico preciso tem muita chance de levar a novo insucesso (19). Um dos primeiros passos, é determinar a causa da falência, se existe ou não infecção presente (fig.1), através de RX, ex. laboratoriais, Cintilografia, punção articular, ou outros exames necessários. Fig.1 – Nove meses pós-operatório (PO) – Soltura por infecção Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT As causas de falência asséptica (fig.2) podem ser divididas em três categorias: fatores do paciente / desenho dos implantes / técnica cirúrgica. implantes, a necessidade de hastes intramedulares, aumentos/calços, enxerto ósseo, etc. Devemos determinar que tipo de estabilidade (“constrição”) será necessária durante a cirurgia, ou seja, estabilização posterior, médio-lateral, articulada tipo “dobradiça”. A modularidade das próteses atuais nos permite uma customização adequada durante a cirurgia (fig.4). Fig.2 – Sete anos PO - Soltura asséptica O aparelho extensor deve ser visto com muito cuidado, pois muitas vezes as causas de falha são devidas a problemas da patela, componente patelar, mau alinhamento patelar, rotação dos componentes, etc. (fig.3) Fig.4 – Modularidade das próteses O - Soltura asséptica A seguir relatamos um “check list” que nos será muito útil para que a cirurgia seja realizada da maneira mais adequada possível. Cirurgia prévia • Que tipo de implante foi usado ? • Qual era o tamanho do implante ? • Tem história de calor local ou drenagem persistente na cirurgia primária ? Infecção Fig.3 – Ap. extensor – soltura do componente patelar As radiografias devem ser bem avaliadas com o uso das transparências (“templates”), para se determinar o possível tamanho dos • Os exames laboratoriais são sugestivos de infecção ? • As alterações radiográficas sugerem infecção ? • Cintilografia foi realizada ? É positiva ? Caso seja negativa = afasta infecção. 249 “Temas selectos de actualización en la Ortopedia Latinoamericana” • Punção e cultura do material foram realizadas ? • Se necessário, fazer biópsia de sinovial ou material articular para exame anatomo-patológico; • Será utilizado cimento com antibiótico na cirurgia ? Já vem misturado com o cimento de fábrica ou será adicionado ? Está disponível ? Exposição / Vias de acesso articular • Incisões prévias ? Cuidados para evitar necrose de pele (fig.5); Fig.6-B – Osteotomia da TAT • Osteotomia da tuberosidade tibial (TAT) será necessária ? (fig.6-A-B). Fios de aço e/ou parafusos estão disponíveis para fixação ? • A presença de um cirurgião plástico será necessária para possíveis coberturas e/ ou retalhos cutâneos ? Remoção dos implantes prévios (fig.7 / 8-A-B / 9-A-B) • Parafusos periarticulares – tipo de cabeça do parafuso ? Chave adequada disponível ? • Instrumentos para remoção dos implantes / cimento ósseo – serra de Gigli, osteótomos finos e flexíveis, brocas, curetas – material especial para remoção do cimento ? • Extratores dos presentes ? componentes Fig.5 – Problemas de pele Fig.6-A – Vias de acesso 250 Fig.7 – Esquema de retirada do componente femoral – serra de Gigle estão Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Implantes de revisão (fig.10-A-B) Fig.8-A – Esquema de retirada do componente femoral – osteótomos Fig.8-B – Retirada do componente femoral - cirurgia • Que tamanho de componente femoral e tibial será necessário ? Que tipo de estabilidade (“constrição”) será utilizada ? O material de revisão permite esta customização ? • Hastes / calços femorais e/ou tibiais serão necessários ? Diversos tamanhos disponíveis ? • Implantes e hastes “offset” serão necessários e estão disponíveis ? Fig.10-A – Implantes de revisão Fig.9-A – Esquema de retirada do componente tibial Fig.10-B – Implantes de revisão Enxerto ósseo Fig.9-B – Retirada do componente tibial - cirurgia • Defeitos ósseos foram previamente avaliados ? (fig.11-A-B-C). NÃO esquecer que na cirurgia, com frequência os defeitos são maiores que aqueles observados nas radiografias; 251 “Temas selectos de actualización en la Ortopedia Latinoamericana” • Tipo de enxerto necessário ? Estrutural – esponjoso ? • Enxerto autólogo – homólogo (banco de osso disponível) ? Diversos • Sangue – reposição / autotransfusão / etc ? • Imobilização pós-operatória (órtese / gesso) ? Quando avaliamos com cuidado as possíveis causas de falha da ATJ primária e planejamos corretamente nossa cirurgia de revisão, podemos ter uma grande chance de sucesso neste procedimento difícil e complexo, obtendo-se resultados satisfatórios ao paciente, que é nosso principal objetivo no tratamento. (fig.12-A-B) Fig.11-A – Esquema de defeito ósseo femoral Fig.12-A – Radiografia em AP - PO imediato Fig.11-B – Esquema de defeito ósseo tibial Fig.11-C – Defeitos ósseos cirurgia 252 Fig.12-B – Radiografia em perfil - PO imediato TÉCNICA CIRÚRGICA Princípios Os objetivos de uma revisão de ATJ incluem o alinhamento correto do membro inferior, posição e fixação adequada dos componentes, balanço ligamentar simétrico em flexão e extensão, mecanismo femoropatelar satisfatório e um aceitável arco de movimento final. Estes objetivos, em particular o balanço ligamentar e a fixação dos componentes da prótese dependem diretamente do correto manejo das perdas ósseas. A magnitude Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT das perdas ósseas tem total implicação na decisão quanto ao uso de enxerto ósseo e/ ou aumentos/calços nas próteses, escolha do tamanho dos componentes, necessidade de maior ou menor constrição e o uso ou não das hastes intramedulares. Se não for possível ter acesso às radiografias em perfil do pré-operatório da cirurgia primária, devemos fazer esta radiografia do joelho contralateral para determinar o provável tamanho dos componentes. A altura da interlinha articular está 2 cm abaixo da origem do ligamento colateral medial e 2,5 cm abaixo da proeminência do epicôndilo lateral. Este dado é importante, pois se houver elevação da interlinha articular é muito provável que teremos problema de arco de movimento, com perda de alguns graus de flexão. Exposição Uma adequada exposição é essencial para o sucesso da reconstrução. A exposição deve permitir total visualização dos implantes, possibilidade de desbridamento dos tecidos moles e dos focos de osteólise, avaliação do estoque ósseo e reimplantação dos componentes de revisão. A exposição pode ser mais difícil na presença de artrofibrose, osso osteoporótico, patela baixa e obesidade. O acesso e artrotomia parapatelar medial é mais comumente utilizado, entretanto, se houver acesso lateral prévio é recomendado repetí-lo para evitar possível osteonecrose da patela. Com frequência somente uma incisão foi usada previamente, e então esta incisão deve ser utilizada para a cirurgia de revisão. A incisão pode ser longitudinal anterior, medializada ou curvilínea. Se uma incisão transversa foi feita previamente, ela deve ser cruzada com ângulo mais aberto possível para minimizar complicações de pele dos bordos da incisão. Se existirem múltiplas incisões anteriores, normalmente a incisão mais lateral deve ser utilizada novamente, pois os vasos sanguíneos tem direção de medial para lateral ao joelho. Se não for possível refazer nenhuma das incisões antigas, devemos então deixar pelo menos 6 cm de pele entre a incisão antiga e a nova incisão. Durante a exposição devemos recriar as goteiras mediais e laterais, liberar o fundo de saco suprapatelar de possíveis tecidos fibróticos para facilitar a mobilização do aparelho extensor. Se existir artrofibrose, podemos realizar uma quadricepsplastia para liberar o aparelho extensor da face anterior do fêmur. Na presença de aderências na região anterior da tíbia e parte proximal do tendão patelar, também devemos fazer liberações para permitir uma mobilização patelar adequada. A subluxação patelar normalmente é suficiente para uma boa exposição do joelho, não sendo necessária a eversão da patela. O aparelho extensor deve ser protegido durante todo o procedimento para evitar a avulsão iatrogênica do tendão patelar, que é desastrosa e de difícil solução. Fazemos uma liberação extensa do canto posteromedial para permitir a rotação externa e subluxação anterior da tíbia para remover o polietileno tibial. Após esta remoção do polietileno teremos melhores condições de mobilizar os tecidos moles com consequente maior facilidade de exposição. Caso persista dificuldade de visualização e exposição dos componentes, podemos realizar um acesso tipo “quadríceps snip” (fig.13) que tornará mais fácil a exposição. Fig.-13 - Acesso tipo “quadríceps snip” 253 “Temas selectos de actualización en la Ortopedia Latinoamericana” Este acesso melhora a eversão da patela, flexão do joelho e a lateralização do aparelho extensor. O fechamento deste acesso é muito parecido com o acesso tradicional e não necessita mudanças no programa de reabilitação no PO (20). Se a exposição ainda persistir muito difícil e inadequada, podemos realizar uma osteotomia estendida da TAT conforme descrita por Whiteside (21). Esta osteotomia é muito útil na presença de patela baixa, na remoção de haste tibial cimentada e nos casos de mau funcionamento do aparelho extensor que necessitem de algum tipo de correção. É uma osteotomia longa (7-8 cm) onde devemos realizar um encaixe proximal para evitar a migração do fragmento (fig.14). suficiente para uma boa exposição articular e reimplantação dos novos componentes. Em casos mais difíceis, porém excepcionais, podemos utilizar acessos mais agressivos tipo “medial femoral peel”, osteotomia epicondilar medial ou “V-Y turndown” do quadríceps. Remoção dos componentes Após uma adequada exposição, as interfaces cimento-osso-implante devem ser expostas para facilitar a remoção dos implantes. Os componentes podem ser removidos com osteótomos delgados, serra de Gigli ou serra óssea com lâminas pequenas e finas, sempre tendo em mente que devemos retirar a menor quantidade de osso possível, isto é, procurar preservar o estoque ósseo. Todo o cimento ósseo deve ser removido, através de osteótomos especiais, brocas ou equipamentos de ultrassom. Após a retirada dos componentes e do cimento, deve-se realizar o desbridamento extenso das partes moles e tecidos fibrosos que estejam aderidos ao osso residual. A seguir utilizaremos as técnicas de reconstrução, com quatro principais procedimentos: reconstrução tibial, espaço em flexão, balanço em extensão e reconstrução femoropatelar. Fig.-14 – Osteotomia TAT Os tecidos moles da parte lateral da osteotomia são deixados intactos. A osteotomia é fixada com 2-3 cerclagens com fios de aço em orientação oblíqua. Se o paciente tiver um bom estoque ósseo, não há necessidade de mudanças no programa de reabilitação no PO. Na maioria dos casos de revisão de ATJ, a utilização dos acessos acima descritos é 254 Reconstrução tibial Nós devemos iniciar a reconstrução pela plataforma tibial que afetará diretamente os espaços em flexão e extensão. É mais comum o uso de guias de corte intramedulares nas cirurgias de revisão, caso não existam grandes deformidades da tíbia. Se for necessário, podemos utilizar os guias extramedulares nas deformidades tibiais mais acentuadas. O corte da parte proximal da tíbia é feito com o guia a 0° (fig.15-A-B). Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Fig.-15-A – Guia de corte tibial intramedular Fig.-15-B – Guia de corte a 0° As perdas ósseas são manejadas com cimento ósseo, enxertos ósseos autólogos ou homólogos (esponjoso ou estrutural), cunhas ou calços metálicos, hastes intramedulares ou implantes customizados (22). De maneira geral, as opções cirúrgicas devem minimizar a remoção adicional de osso. A classificação dos defeitos ósseos segundo o “Anderson Orthopaedic Research Institute” nos ajuda a definir a severidade da perda óssea durante a cirurgia e nos orienta sobre o tipo de reconstrução que será necessária (19). O tipo 1 é um defeito pequeno com osso metafisário intacto e não compromete a estabilidade do implante. O tipo 2 apresenta dano do osso metafisário sendo necessário fazer a reconstrução da fêmur e/ou da tíbia (com cimento, calços/cunhas ou enxerto ósseo); o tipo 2-A envolve um côndilo femoral ou tibial e o tipo 2-B envolve ambos os côndilos. O tipo 3 apresenta um defeito metafisário segmentar comprometendo uma porção maior do côndilo femoral ou do planalto tibial. Nos pacientes com defeitos cavitários na região proximal da tíbia podem ser tratados com cimento ósseo (mais idosos) ou enxerto ósseo impactado (mais jovens), promovendo um bom suporte da base tibial na periferia do osso (23-24). Os enxertos maciços homólogos ou calços/cunhas metálicos devem ser usados nos grandes defeitos estruturais do planalto tibial (25-26). No geral, os calços/cunhas metálicos têm sido utilizados em maior escala pela facilidade de customização durante a cirurgia, facilidade de colocação e ausência de absorção. As próteses tumorais são reservadas para os casos de perda óssea severa, em pacientes idosos e de baixa demanda. As hastes intramedulares de extensão devem ser utilizadas na maioria dos casos de reconstrução femoral ou tibial. As hastes transferem o estresse da parte deficiente para uma região diafisária mais distal (27). Elas também aumentam a área de superfície de fixação e podem orientar a direção do componente. No geral, o comprimento da haste deve ultrapassar o defeito metáfiso-diafisário. As hastes podem ser totalmente cimentadas (fig.16) ou ter uma fixação híbrida (fig.17), ou seja, a base tibial e a região metafisária são cimentadas e a extensão da haste é fixada de modo “press-fit” dentro do canal (28). A principal vantagem das hastes não cimentadas é a facilidade de remoção numa próxima cirurgia. As desvantagens das hastes não cimentadas incluem a dificuldade de uso nas tibiais com deformidades, dor potencial na extremidade da haste e a dificuldade de receber carga completa do planalto tibial. As hastes cimentadas aumentam a área para interdigitação, mas são mais difíceis de remoção. Elas não orientam o alinhamento, porém permitem alguns ajustes para melhor adaptação da superfície de corte do planalto tibial. As hastes com “offset” oferecem a vantagem adicional de melhor cobertura da tíbia e são comumente utilizadas não cimentadas. 255 “Temas selectos de actualización en la Ortopedia Latinoamericana” Fig.18 – Controle rotacional do fêmur após reconstrução da tíbia Fig.16 – Haste tibial cimentada Fig.17 – Haste tibial não cimentada. Cimentação da base tibial e região metafisária Também podemos usar o eixo transepicondilar para controle da rotação do componente, que nunca deve ficar em rotação interna. Nas revisões de ATJ o componente femoral deve ser entre 5-7° de valgo. As hastes femorais podem determinar o alinhamento no plano coronal. Na maioria dos casos de reconstrução femoral será necessário o uso de calços ou aumentos distais no fêmur para que a interlinha articular esteja em posição correta, ou seja, em torno de 25 mm do epicôndilo medial (29-30-31) (fig.19). Outra medida utilizada é em relação à patela (10 mm abaixo do polo inferior) (fig.20). Se não observarmos este detalhe, poderemos ter a elevação do interlinha, com consequente patela baixa e perda de mobilidade em flexão. Após a reconstrução da tíbia, devemos avaliar a altura da interlinha articular com uso de espaçadores/polietilenos de prova e a posição final é baseada no balanço ligamentar e na reconstrução femoral. Reconstrução femoral A reconstrução femoral deve iniciar após a reconstrução tibial que irá servir de guia ou parâmetro para a rotação do componente femoral (fig.18). 256 Fig.18 – Controle rotacional do fêmur após reconstrução da tíbia Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Fig.20 – Altura da interlinha articular -= 10 mm abaixo da patela As perdas ósseas são manejadas de maneira semelhante à reconstrução tibial, onde as perdas ósseas severas são reconstruídas com enxerto ósseo homólogo maciço ou com cunhas/calços metálicos (mesmos motivos da reconstrução tibial). O defeito ósseo tipo 3 com muita frequência está associado ao dano ou ausência dos ligamentos colaterais, necessitando implantes tipo dobradiça (“hinge”) para a reconstrução. Em muitas ocasiões utilizamos as hastes femorais com ou sem “offset” para permitir a melhor orientação e posicionamento do componente femoral, bem como evitar a perda do “offset” posterior do fêmur que levaria a um maior espaço (“gap”) em flexão e instabilidade residual. Para manter o “offset” posterior do fêmur (fig.21), necessitamos com frequência colocar enxerto ósseo ou calços posteriores e desta maneira utilizamos componentes femorais de tamanho adequado; ou seja, não devemos utilizar componentes pequenos (“undersize”). Fig.21 – Haste femoral sem “offset” e calços posteriores para manter o “offset” do fêmur Após a reconstrução com manutenção da altura da interlinha articular desejável é importante conseguir o balanço ligamentar correto em flexão e extensão através da espessura/tamanho mais adequado dos implantes. Reconstrução patelar O componente patelar deve ser bem exposto para melhor visualização da sua real situação. O implante deve ser mantido se estiver bem fixado, bem posicionado e ser compatível com os componentes da revisão. Se o implante estiver perdido (solto) deve ser retirado. Com o uso de serra óssea e lâmina de pouco espessura, retiramos a parte articular do componente patelar e com brocas de grande velocidade (“burrs”) removemos os “pegs” do componente e também o cimento ósseo residual. Se for possível e ainda existir estoque ósseo, deve-se fazer a colocação de novo componente patelar. Caso não seja possível a colocação de outro componente 257 “Temas selectos de actualización en la Ortopedia Latinoamericana” por falta de estoque ósseo (menor que 10 mm de espessura), a pateloplastia é realizada com regularização do osso remanescente (32). Muitas vezes, chega a ser surpreendente o bom resultado funcional no pós-operatório com a pateloplastia (fig.22). Fig. – 22 – Pós-operatório de revisão de ATJ – 12 anos e 6 meses - Pateloplastia Reconstrução das perdas ósseas Um ponto crítico nas revisões de ATJ é a determinação da extensão e localização da perda óssea. Após a remoção dos componentes é importante verificar se os defeitos são “contidos” ou “não contidos” (segmentares). A localização de osso de suporte e os arredores das perdas ósseas são essenciais para determinar que tipo e tamanho da reconstrução que será necessária (9). Os defeitos pequenos podem ser preenchidos com cimento e parafusos ou enxerto ósseo autólogo ou homólogo moído, particularmente nos pacientes mais idosos. Entretanto, nos defeitos maiores ou estruturais serão necessárias medidas reconstrutivas maiores, como blocos/calços modulares como aumentos, enxerto ósseo homólogo maciço, cones metálicos altamente porosos metafisários (“tantalum”) ou “sleeves” metafisários. Cimento ósseo e parafusos O uso do cimento com parafusos é simples, de baixo custo e eficiente. Este método é mais usado nos defeitos menores que 5 mm de profundidade. A armação com o uso adicional de parafusos aumenta as propriedades biomecânicas estruturais (fig.23). 258 Fig. – 23 – Armação de cimento ósseo com parafusos Enxerto ósseo moído Este método é utilizado em defeitos “contidos” e particularmente em pacientes mais jovens onde é importante preservar o estoque ósseo. Pode ser autólogo ou homólogo, com taxas similares de incorporação (fig.24-A,B) É importante que a superfície que irá receber o enxerto tenha boa vascularização para facilitar a incorporação. Caso o osso residual esteja corticalizado, podemos utilizar as brocas (“burrs”) para chegarmos ao osso esponjoso e com boa vascularização. Se isto não for possível, devemos então utilizar outros métodos para a reconstrução. Fig.-24-A – Esquema do uso de enxerto ósseo moído Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Fig.25-A – Esquema de reconstrução com enxerto ósseo estrutural Fig.24-B – Radiografia pós-operatória de revisão com enxerto ósseo moído no planalto tibial medial. Enxerto ósseo homólogo estrutural Os enxertos ósseos estruturais homólogos são comumente utilizados na reconstrução de grandes defeitos ósseos na intenção de promover suporte mecânico das reconstruções ósseas. Eles são indicações em defeitos acima de 15 mm de profundidade e que excedem as dimensões dos blocos/ calços metálicos. A vantagem deste enxerto é o seu potencial de reconstrução, principalmente em jovens. As desvantagens são o potencial de reabsorção do enxerto, colapso e a não incorporação ou união pelo hospedeiro. Quando indicamos este tipo de enxerto, devemos levar em consideração as condições de saúde geral do paciente, idade psicológica, qualidade óssea e nível de atividade (fig.25-A-B). Fig.25-B – Radiografia pós-reconstrução com enxerto ósseo estrutural Reconstrução com blocos/calços metálicos As reconstruções com blocos / calços metálicos são indicadas em defeitos femorais / tibiais pequenos ou moderados (fig.26-AB-C). Fig.26-A – Defeito moderado no fêmur e tíbia – pér-operatório Fig.26-B – Blocos metálicos na tíbia e fêmur – pér-operatório 259 “Temas selectos de actualización en la Ortopedia Latinoamericana” Fig.27-A – Cone de “tantalum” – Long e Scuderi (34) Fig.26-C – Radiografia pós-reconstrução com blocos metálicos no fêmur e tíbia Os blocos metálicos têm as vantagens de serem versáteis, eficientes, tecnicamente resistentes e não requerem osteointegração. São muito úteis em pacientes idosos e pouco ativos, porém tem a desvantagem de não restaurar o estoque ósseo. A maioria dos sistemas de revisões de ATJ tem um número grande de opções de tamanhos e formas que nos permitem restaurar com eficiência as perdas ósseas, a altura da interlinha articular e o correto balanço ligamentar. Reconstrução com cones metálicos altamente porosos e “sleeves” metáfisários Estes materiais foram desenvolvidos recentemente e indicados para os grandes defeitos no fêmur e/ou tíbia. Eles foram desenhados para evitar possível falhas na incorporação ou reabsorção dos enxertos estruturais homólogos, Os metais altamente porosos, em particular o ”tantalum” (fig.27A), são biomateriais com várias vantagens potenciais sobre os materiais tradicionais, incluindo baixa dureza, alta porosidade e alto coeficiente de fricção (9). Os desenhos destes cones metafisários foram desenvolvidos para preencher as diversas formas de perdas ósseas encontradas nas revisões de ATJ (fig.27-B) e providenciar suporte mecânico com integração biológica (33-34). 260 Fig.27-B – Perda óssea tibial tratada com “tantalum” e radiografia pós-operatória – Long e Scuderi (34) Uma outra alternativa é o uso dos “sleeves” metafisários (fig.28), que da mesma maneira são indicados para os defeitos grandes e sem possibilidade de reconstrução tradicional (35). Fig.28- “Sleeves” metafisários – Dennis (35) Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT Reconstrução com próteses “tumorais” Este tipo de reconstrução é de indicação excepcional, sendo considerada “cirurgia de salvação” (fig.29). A indicação seria nos casos extremamente graves, com instabilidade e perdas ósseas que são impossíveis de reconstrução através de todas as outras formas descritas acima. Elas são indicadas em pacientes idosos e de baixa demanda, pois há muita sobrecarga sobre o implante e o osso remanescente, com grande possibilidade de falha nos pacientes mais jovens e ativos. Fig.29 – Radiografia de prótese “tumoral”. Estabilidade final Após a inserção do componente femoral e tibial, o joelho deve ser avaliado em todo arco de movimento para que possamos avaliar a estabilidade da reconstrução. O joelho deve ter extensão completa e a patela deve excursionar bem centrada em todo arco de movimento. A estabilidade deve ser testada em extensão completa, flexão intermediária e flexão completa. A estabilidade deve ser adequada tanto no plano coronal como sagital e com frequência isto é obtido através de implantes que não necessitem constrição excessiva. Para as instabilidades unidirecionais ou com leve alteração na flexo-extensão, normalmente um “poste” mais alto para estabilização posterior é suficiente. Nós devemos utilizar implantes com a menor constrição possível, para evitar sobrecarga no manto de cimento. As extensões com hastes intramedulares devem ser consideradas sempre que o grau de constrição aumenta. As próteses mais constritas, tipo dobradiças (“hinge”) devem ser reservadas para os pacientes com marcada instabilidade em flexão e extensão, instabilidade global ou recurvato não controlado. Inserção dos componentes A técnica de inserção dos componentes depende do modo de fixação das hastes intramedulares. Se for utilizada uma haste cimentada, devemos usar um restritor de canal para boa pressurização do cimento e evitar o extravasamento distal no canal. O cimento deve ser aplicado na superfície dos componentes femoral e tibial, bem como ao longo da região metafisária dos ossos. Se houver osso cortical, devemos realizar perfurações para melhorar a penetração do cimento com melhor fixação. A rotação deve ser sempre observada durante todo o processo de fixação dos componentes, para se evitar qualquer rotação interna inadvertida. Método preferido pelos autores Dentro do que foi exposto anteriormente, nossa técnica cirúrgica é resumida nos seguintes passos: • Acesso anterior e artrotomia parapatelar medial; • Quando necessário utilizamos prolongamentos do acesso com “quadríceps snip” ou osteotomia da TAT; • Sinoviectomia extensa com exposição adequada dos componentes; • Retirada dos componentes com uso de serra de Gigli, osteótomos finos e flexíveis, serra óssea com lâmina delgada e impactores; 261 “Temas selectos de actualización en la Ortopedia Latinoamericana” • • 262 Colheita de 4-5 amostras de tecidos para cultura (líquido sinovial / tecido sinovial / tecido óoseo do fêmur / tíbia), após a retirada dos componentes; Reconstrução óssea tibial em primeiro lugar, que servirá como base para a reconstrução femoral (segundo lugar); • Uso de blocos/calços metálicos como preferência. Nas grandes perdas ósseas utilizamos enxerto ósseo homólogo associado; • As hastes são híbridas de preferência, cimentando a superfície do componente e a região metafisária, com fixação da haste tipo “press fit”; • Reconstrução patelar por último. Se não for possível a colocação de outro componente, fazemos somente a pateloplastia do osso remanescente; • Cimento com antibiótico já misturado de fábrica; • Limpeza extensa de todo sítio cirúrgico com “kit” de lavagem com pressão; • Sutura dos tecidos em flexão do joelho, para ganho de mobilidade no pós-operatório; • Dreno de sucção por 24 horas; • Antibiótico no pós-operatório até termos os resultados das culturas; • Profilaxia mecânica e medicamentosa contra tromboembolismo venoso por 14 dias; • Apoio parcial do membro operado em 24-48 horas com auxílio de andador ou muletas, se a reconstrução for satisfatória; • Início de reabilitação em clínica especializada após a retirada dos pontos, em torno de 14 dias. Discussão e conclusões As cirurgias de revisão de ATJ são desafiadoras para qualquer cirurgião e podem estar associadas a complicações, principalmente a infecção periprotética. Mas, através da avaliação sistemática que inclui uma boa história, um bom exame físico, radiografias adequadas e testes sorológicos, teremos a capacidade de identificar de maneira correta a etiologia da falha na maioria dos casos. Sempre devemos fazer o possível para identificar ou afastar qualquer possibilidade de infecção. A causa da falha com diagnóstico correto nos levará a um planejamento adequado para uma cirurgia bem sucedida. Todos os detalhes do procedimento, como uma exposição correta, liberação posteromedial extensa e associação de prolongamentos tipo “quadríceps snip” ou osteotomia da TAT são importantes para iniciar a reconstrução óssea e ligamentar. Devemos minimizar as perdas ósseas no momento da retirada dos componentes. O uso de blocos ou aumentos metálicos, bem como enxerto ósseo homólogo nos permitem reconstruções ósseas muito satisfatórias. Os implantes devem ter o mínimo de constrição possível, deixando para aumentar a constrição somente nos casos excepcionais com defeitos e instabilidade muito acentuada. Finalmente, devemos sempre ter em mente a possiblidade de infecção, uma vez que o procedimento padrão nestes casos será totalmente diferente, com a reconstrução devendo ser realizada em dois tempos. Sociedad Latinoamericana de Ortopedia y Traumatología - SLAOT BIBLIOGRAFÍA 1. Ranawat CS, Flynn WF Jr, Saddler S, Hansraj KK, Maynard MJ. Long-term results of the total condylar knee arthroplasty. A 15-year survivorship study. Clin Orthop Relat Res. 1993;286:94-102. 2. Ritter MA, Berend ME, Meding JB, Keating EM, 1993;286: 94-102. Faris PM, Crites BM. Long-term followup of anatomic graduated components posterior cruciate-retaining total knee replacement. Clin Orthop Relat Res. 2001;388:51-57. 3. Kurtz S, Ong K, Lau E, Mowat F, Halpern M: Projections of primary and revisions hip and knee arthroplasty in the United States from 2005 to 2030. J Bone Joint Surg Am 2007;89(4):780-785. 4. Jacofsky DJ, Della Valle CJ, Meneghini RM, Sporer SM, Cercek RM. Revision total knee arthroplas- ty: What the practicing orthopaedic surgeon needs to know. J Bone Joint Surg Am 2010;92(5):12821292. 5. Mont MA, Sema FK, Krackow KA, Hungerford DS. Exploration of radiographically normal total knee replacements for unexplained pain. Clin Orthop Relat Res.1996;331:216-220. 6. Fehring TK, Odum S, Griffin WL, Mason JB, Nadaud M. Early failures in total knee arthroplasty. Clin Orthop Relat Res. 2001;392:315-318. 7. Mulhall KJ, Ghomrawi HM, Scully S, Callaghan JJ, Saleh KJ. Current etiologies and modes of failure in total knee revision. Clin Orthop Relat Res. 2006;446:45-50. 8. Sharkey PF, Hozack WJ, Rothman RH, Shastri S, Jacoby SM. Insall Award paper: Why are total knee arthroplasty failing today? Clin Arthop Relat Res. 2002;404:7-13. 9. Meneghini RM. Revision total knee arthroplasty. In Orthopaedic Knowledge Update: Hip and Knee Reconstruction 4 - AAOS. 2011: 165-175 10.Meding JB, Keating EM, Ritter MA, Faris PM, Berend ME, Malinzak RA. The planovalgus foot: a harbinger of failure of posterior cruciate-retaining total knee arthroplasty. J Bone Joint Surg Am. 2005;87 Suppl 2:59-62. 11.Vessely MB, Frick MA, Oakes D, Wenger DE, Berry DJ. Magnetic resonance imaging with metal suppression for evaluation of periprosthetic osteolysis after total knee arthroplasty. J Arthroplasty. 2006;21:826-831. 12.Berger RA, Crossett LS, Jacobs JJ, Rubash HE. Malrotation causing patellofemoral complications after total knee arthroplasty. Clin Orthop Relat Res. 1998;356:144-153. 13.Hofmann AA, Wyatt RW, Daniels AU, Armstrong L, Alazraki N, Taylor A Jr. Bone scans after total knee arthroplasty in asymptomatic patients. Cemented versus cementless. Clin Orthop Relat Res. 1990;251:183-188. 14.Schinsky MF, Della Valle CJ, Sporer SM, Paprosky WG. Perioperative testing for joint infection in patients undergoing revision total hip arthroplasty. J Bone Joint Surg Am. 2008;90:1869-1875. 15.Ghanem E, Parvizi, Burnett RS et al. Cell count and differential of aspirated fluid in the diagnosis of infection at the site of total knee arthroplasty. J Bone Joint Surg Am. 2008;90(8):1637-1643. 16.Barrack RL, Jennings RW, Wolfe MW, Bertot AJ. The value of perioperative aspiration before total knee revision. Clin Orthop Relat Res. 1997;345:8-16. 17.Della Valle CJ, Sporer SM, Jacobs JJ, Berger RA, Rosenberg AG, Paprosky WG. Preoperative testing for sepsis before revision total knee arthroplasty. J Arthroplasty. 2007;22(6 Suppl 2):90-93. 263 “Temas selectos de actualización en la Ortopedia Latinoamericana” 18.Lonner JH, Desai P, Dicesare PE, Steiner G, Zuckerman JD. The reability of analisys of intraoperative frozen sections for identifying active infection during revision hip or knee arthroplasty. J Bone Joint Surg Am. 1996;78:1553-1558. 19.Engh GA et Rorabeck CH. Planning the revision surgery and Bone defect classification. In: Revision Total Knee Arthroplasty. Williams & Wilkins, 1997.63-182 20.Meek RM, Greidanus NV, McGraw RW, Masri BA. The extensile rectus snip exposure in revision of total knee arthroplasty. J Bone Joint Surg Br. 2003;85:1120-1122. 21.Whiteside LA. Exposure in difficult total knee arthroplasty using tibial tubercle osteotomy. Clin Orthop Relat Res. 1995;321:32-25. 22.Whittaker JP, Dharmarajan R, Toms AD. The management of bone loss in revision total knee replacement. J Bone Joint Surg Br. 2008;90:981-987. 23.Bush JL, Wilson JB, Vail TP. Management of bone loss in revision total knee arthroplasty. Clin Orthop Relat Res. 2006;452:186-192. 24.Lonner JH, Lotke PA, Kim J, Nelson C. Impaction grafting and wire mesh for uncontained defects in revision knee arthroplasty. Clin Orthop Relat Res. 2002;404:145-151. 25.Engh GA, Ammeen DJ. Use of structural allograft in revision total knee arthroplasty in knees with severe tibial bone loss. J Bone Joint Surg Am. 2007;89:2640-2647. 26.Long WJ. Scuderi GR. Porous tantalum cones for large metaphyseal tibial defects in revision total knee arthroplasty: a minimum 2-year follow-up. J Arthroplasty. 2009;24:1086-1092. 27.Bourne RB. Finlay JB. The influence of tibial component intramedullary stems and implant-cortex contact on the strain distribution of the proximal tibia following total knee arthroplasty. An in vitro study. Clin Orthop Relat Res. 1986;208:95-99. 28.Peters CL, Erickson J, Kloepper RG, Mohr RA. Revision total knee arthroplasty with modular components inserted with metaphyseal cement and stems without cement. J Arthroplasty. 2005;20:302-308. 29.Mahoney OM, Kinsey TL. Modular femoral offset stems facilitate joint line restoration in revision knee arthroplasty. Clin Orthop Relat Res. 2006;446:93-98. 30.Porteous AJ, Hassaballa MA,Newman JH. Does the joint line matter in revision total knee replacement ? J Bone Joint Surg Br. 2008;90:879-884. 31.Bottros J, Gad B, Krebs V, Barsoum WK. Gap balancing in total knee arthroplasty. J Arthroplasty. 2006.21(4 Suppl 1):11-15. 32.Rorabeck CH, Mehin R, Barrack RL. Patellar options in revision total knee arthroplasty. Clin Ortop Relat Res. 2003;41:84-92. 33.Meneghini RM, Lewallen DG, Hanssen AD. Use of porous tantalum metaphyseal cones for severe tibial bone loss during revision total knee replacement. J Bone Joint Surg Am. 2008;90(1):78-84. 34.Long WJ, Scuderi GR. Porous tantalum cones for large metaphyseal tibial defects in revision total knee arthroplasty. J Arthroplasty. 2009;24(7):1086-1092.. 35.35. Dennis DA. A stepwise approach to revision total knee arthroplasty. J Arthroplasty. 2007;22(4 Suppl):32-38. 264