Un modelo matemático para el diseño de quimioterapias con el uso
Anuncio

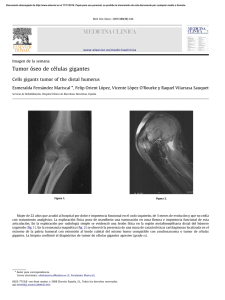
FARAUTE, Vol. 6, No. 1, 27-38, 2011 ISNN 1698-7418 Deposito Legal PP200402CA1617 Un modelo matematico para el diseño de quimioterapias con el uso de drogas citotoxicas y citoestaticas Soraya Aguilar1 *, Minaya Villasana 2 1 Universidad José Antonio Páez. Facultad de Ingenierı́a. Escuela de Ingenierı́a en Computación Simón Bolı́var . Departamento de Cómputo Cientı́fico y Estadı́stica *Autor de correspondencia: [email protected] 2 Universidad Resumen Se plantea una modificación a un modelo matemático previo, que simula la interacción entre las células cancerosas y las del sistema inmune con una droga citotóxica, que actúa en una fase especifica del ciclo celular. Aquı́ agregamos al modelo una droga citoestática, cuyo efecto es retener las células en una fase del ciclo, con el objetivo de maximizar la cantidad de células en una fase vulnerable para la droga citotóxica. El problema se plantea como uno de optimización, que se resuelve usando estrategias evolutivas, se plantea y se comparan ocho funciones objetivo. La mejor función objetivo se compara con un protocolo derivado de un problema similar que no incluye la nueva droga. Se confirma que la combinación con la nueva droga, mejora la efectividad de la droga citotóxica. Se argumenta, que el enfoque propuesto puede servir como una herramienta de apoyo al médico para diseñar un esquema tratamientos de quimioterapias. Palabras Claves: Citotóxica, Citoestática, Ecuaciones diferenciales con retardo, Ciclo celular, Control óptimo Abstract A modification of a previous mathematical model that simulates the interaction between cancerous cells and immune system cells and a cytotoxic drug, which acts upon a specific phase of the cell cycle is presented. Here we modify the model by incorporating a cytostatic drug, which arrests cells in a specific phase of its cycle. The rationale behind this is to maximize the amount of cells in the most vulnerable phase of their cycle with respect to the action of the cytotoxic drug. The problem is posed as an optimal control problem and is solved using an evolutionary strategy algorithm. Various objective functions are studied and compared against previously obtained chemotherapy schedules that only incorporated the cytotoxic drug. Results confirm that the inclusion of the cytostatic drug increases the cytotoxic’s effectivity. We argue that this approach may serve as a valuable tool for the medical community when designing chemotherapy treatments. Keywords: Cytotoxic, Cytostatic, Delay differential equations, Cell Cycle, Optimal Control 28 Un modelo matemático para el diseño de quimioterapias Introducción Cuando se diseñan esquemas de aplicación de tratamientos de quimioterapia a los pacientes de cáncer, el objetivo es eliminar las células cancerosas, afectando lo menos posible la salud del paciente. Se debe tomar en cuenta que las drogas citotóxicas usadas en estos tratamientos actúan no solo sobre las células cancerosas sino también sobre las células del sistema inmune y células normales, afectando la salud del paciente. Se han planteado diversos modelos matemáticos que simulen el comportamiento de las células ante distintas situaciones; como es el caso de la reacción de las células ante variedades de esquemas de aplicación de drogas antineoplásticas, y cómo estas afectan la salud del paciente. En (Villasana & Radunskaya, 2003) se plantea un modelo de ecuaciones diferenciales con retardo para la dinámica de las células cancerosas y del sistema inmune. El modelo contempla el efecto de una droga citotóxica en fases especı́ficas del ciclo celular y sobre el sistema inmune del paciente. De los resultados obtenidos en (Villasana, 2001), se desprende que la sincronización de las fases celulares podrı́a mejorar el desempeño de la droga citotóxica. Esta sincronización se podrı́a lograr con la inclusión de una droga citoestática en el modelo. La función principal de una droga cito-estática es atrapar las células en una fase particular del ciclo celular. Al disminuir los niveles de la droga citoestática, las células son liberadas para continuar su ciclo de celular. Este tipo de droga se utiliza para lograr una sincronización de células en el ciclo. La idea detrás de la sincronización es aumentar la cantidad de células que se encuentran en la fase de mitosis y en ese momento aplicar la droga cito-tóxica, maximizando el efecto de esta droga sobre el tumor. La suposición anterior se basa en los resultados obtenidos en (Villasana, 2001), donde se observó de forma empı́rica que la sincronización de las células en el ciclo celular aumentaba el volumen de la región de atracción del punto de equilibrio. Por otra parte, en la actualidad los métodos de optimización heurı́sticos se han usado para resolver problemas para los cuales no existe un método que lo resuelva en un tiempo razonable. Tal es el caso del problema de la búsqueda de protocolos de quimioterapias, que se puede plantear como un problema de control óptimo, en donde la idea es encontrar un Soraya Aguilar y Minaya Villasana esquema que maximice el efecto de las drogas sobre las células cancerosas, pero afectando lo menos posible la salud del paciente. En (Villasana & Ochoa, 2004), se plantea un problema de control óptimo para diseñar esquemas de aplicación de quimioterapias para una única droga cito-tóxica, y se comparan 3 métodos de optimización heurı́sticos (algoritmos genéticos, estrategias evolutivas y recocido simulado) para resolverlo; usando como base el modelo planteado en (Villasana & Radunskaya, 2003). La droga cito-tóxica que se considera en (Villasana & Radunskaya, 2003), ejerce su efecto sobre la fase de mitosis de la célula. Además, esta droga no sólo afecta las células cancerosas sino también las células del sistema inmune, las cuales son de vital importancia en la salud del paciente, por lo que se debe tomar en cuenta a la hora de diseñar un esquema de aplicación de tratamiento. Otros trabajos abordan el problema desde distintos puntos de vista. En (Tse et al, 2007) los autores presentan un modelo para simular la respuesta de las células cancerosas bajo el efecto de múltiples drogas. Su modelo toma en cuenta tres drogas en el tratamiento de quimioterapia, y considera la resistencia de las células a determinada droga, modelando la cantidad de células totales presentes que son resistentes a cada una de las drogas y a la combinación de ellas. Sin embargo, no hace una separación de las distintas fases celulares ni de la acción de las drogas sobre dichas fases. También se plantea un problema de control óptimo cuyo objetivo es minimizar el tamaño del tumor bajo un conjunto de restricciones, determinando que el controlador es de tipo “bang - bang” (soluciones que sólo pueden tomar valores máximos y mı́nimos) y usan un algoritmo memético para resolverlo. En (Liang & Leung, 2006) se plantea un modelo de ecuaciones diferenciales que toma en cuenta la cantidad de células malignas presentes, la concentración de la droga en el organismo y la toxicidad acumulada de la droga en el organismo. Allı́ también se plantea un problema de optimización con un control de tipo bang -bang, utilizando una técnica basada en algoritmos genéticos adaptativos con elitismo para resolverlo. En (Swierniak et al, 1996) los autores plantean un sistema de ecuaciones diferenciales para modelar la población de células cancerosas proliferativas bajo el efecto de drogas cito-tóxicas y cito-estáticas, basándose en el diseño de esquemas de aplicación de FARAUTE Ciens. y Tec., 6(1)2011 29 Un modelo matemático para el diseño de quimioterapias quimioterapias periódicos. Por otra parte plantean el problema de optimización en dos enfoques, uno es la minimización de la cantidad total de células malignas y a su vez la minimización de la acción de la droga en las células normales; el otro enfoque es la maximización de la cantidad de células normales y a su vez la maximización de la acción de la droga sobre las células malignas. El modelo planteado por (Swierniak et al, 1996) toma en cuenta las distintas fases celulares ası́ como también la acción de la droga sobre una fase celular especı́fica. Los autores resuelven el problema de control óptimo de forma analı́tica para el caso de una sola aplicación de la droga, obteniendo como solución óptima una en la que no se presenta un solapamiento en la aplicación de ambas drogas. En otras palabras, primero se aplica una droga (cito-estática) para luego aplicar la otra (cito-tóxica). Este resultado sugiere una sincronización previa con la droga cito-estática para luego aplicar una droga cito-tóxica. Sin embargo, los modelos utilizados son simples y no especifican la acción sobre las distintas etapas del ciclo celular como tampoco contemplan aplicaciones sucesivas de las drogas. En este estudio, se tomó el modelo planteado en (Villasana & Radunskaya, 2003) como base y se consideró una versión modificada para incluir una droga de tipo cito-estática. Para este nuevo modelo se plantearon distintas opciones para el problema de control óptimo, siempre teniendo como meta minimizar el número de células cancerosas y mantener el número de células del sistema inmune por encima de un nivel mı́nimo aceptable. El problema de control óptimo se formula empleando distintas funciones objetivo, con la finalidad de encontrar cuál es la que genera esquemas de quimioterapias más eficientes para el paciente. El planteamiento del problema en este trabajo, está basado en el estudio de (Villasana & Ochoa, 2004), modificando la representación de la solución para incluir la nueva droga. El artı́culo tiene la siguiente estructura: en la sección 2 se describen las bases biomédicas que soportan la investigación, que incluye el modelo matemático previo, en la sección 3 se presenta el modelo matemático modificado donde se incluye la dinámica para la droga citoestática y se describe el problema de optimización planteado. En la sección 4 se muestran los resultados y discusiones y finalmente la sección 5 presenta las conclusiones y las ideas que este trabajo aportó para otras investigaciones. Soraya Aguilar y Minaya Villasana Formulación del problema Bases Biomédicas El ciclo celular es el proceso mediante el cual una célula crece y se divide en dos células hijas. Todas las células se originan únicamente por la división de otra célula ya existente. Una célula puede encontrarse en dos fases en el ciclo celular, claramente diferenciadas: La fase de no división o interfase. Consta de 3 etapas: G1 es una etapa de descanso o fase pre-sintética, S es la segunda etapa del ciclo, también conocida como periodo sintético y G2 es otra etapa de descanso, también llamada etapa post-sintética La fase de división o mitosis. En ocasiones, una célula que se dice cancerosa, escapa a los controles normales de división y muerte celular y pierde la habilidad de autoregulación. En estos casos, se presenta el crecimiento descontrolado y diseminación de células anormales en el organismo, que invaden y dañan tejidos y órganos. La mayorı́a de las drogas usadas en los tratamientos de quimioterapias afectan las células en una fase del ciclo celular, tal es el caso de las drogas de tipo citotóxicas que atacan las células en alguna fase especı́fica y las drogas de tipo citoestáticas cuya función es atrapar las células en interfase. Con altas concentraciones de la droga cito-estática se provoca una sincronización en el ciclo celular puesto que, cuando la concentración disminuye las células son liberadas y continúan el ciclo. Modelo Matemático En el modelo matemático usado en (Villasana & Radunskaya, 2003) se considera la población de células del tumor durante la interfase en el tiempo, TI (t), la población de células del tumor en la fase de mitosis, TM (t), la población de células del sistema inmune, I(t), la cantidad de droga presente a tiempo t, u(t) y el tiempo de duración de las células en interfase, τ. Aquı́ se considera las células citotóxicas T en representación del sistema inmune por su importancia en el combate del cáncer. El modelo puede describirse mediante el siguiente sistema de ecuaciones: FARAUTE Ciens. y Tec., 6(1)2011 30 Un modelo matemático para el diseño de quimioterapias dT1 dt dTM dt dI dt du1 dt du2 dt u(t) = 2a4 TM − (c1 I + d2 )T1 − a1 T1 (t − τ) = a1 T1 (t − τ) − d3 TM − a4 TM − c3 TM I − k1 (1 − e−k2 u )TM = k+ = −λ1 u1 + c(t) = −λ2 u2 + c(t) = r1 u1 (t) + r2 u2 (t) ρI(T1 + TM )n − c2 IT1 − c4 TM I − k3 (1 − ek4 u )I α + (T1 + TM )n (1) = = = = = φ1 (t) φ2 (t) φ3 (t) 0 0 exponenciales separadas, donde cada una representa una tasa de eliminación distinta. Una representa una tasa de decaimiento rápida que se da mientras la droga se distribuye a través de la sangre a los tejidos, y la otra es una tasa de decaimiento más lenta de los tejidos periféricos. Esta función de decaimiento se expresa como decay(t) = r1 e−λ1t + r2 e−λ2t Con los datos iniciales dados por: TI (t) TM (t) I(t) u1 (0) u2 (0) Soraya Aguilar y Minaya Villasana para para para t ∈ [−τ, 0] t ∈ [−τ, 0] t ∈ [−τ, 0] Donde: d2 TI , d3 TM y d1 I. representan la proporción natural de muerte celular a1 y a4 son las tasas de reproducción del tumor ci representan las pérdidas de los encuentros de las células tumorales con las células inmunes. ρI(TI +TM )n α+(Ti +TM )n , representa el crecimiento no lineal de la población de células del sistema inmune debido a la presencia de células cancerosas. ρ y a representan la habilidad del organismo de producir ciertas citotoxinas y dependen del tipo de tumor a ser considerado y del sistema inmune k, representa la tasa constante de producción de células del sistema inmune τ, es el tiempo que reside la célula en la etapa de interfase TM I y TI I representan las pérdidas debidas a los encuentros entre los diferentes tipos de células −k1 (1 − e−k2 u )TM , representa las células del tumor que no proliferan al ser sacadas fuera del ciclo celular por la acción de la droga La droga citotóxica que se estudia en (Villasana & Radunskaya, 2003) es Paclitaxel, la cual tiene un decaimiento que puede ser modelado por dos curvas (2) donde r1 y r2 son constantes adimensionales. Sean u1 y u2 tales que, la concentración de la droga en cualquier tiempo está dada por una combinación lineal u(t) = r1 u1 (t) + r2 u2 (t). Las dos últimas ecuaciones del sistema de ecuaciones diferenciales (1) modelan la situación con múltiples aplicaciones de droga citotóxica durante el tiempo, y son identificadas con la función c(t), la cual es la concentración de Paclitaxel que entra al sistema a tiempo t. El sistema libre de droga puede tener hasta 5 puntos de equilibrio dependiendo de los valores de los parámetros libres del modelo. Uno de estos puntos es (0, 0, I0 ) con I0 = k/d1 > 0, el cual siempre está presente. Este punto representa un sistema libre de células cancerosas, con población del sistema inmune positiva, el cual es un escenario deseable. Cuenca de atracción En el punto de equilibrio (TI , TM , I) = (0, 0, I0 ), con I0 > 0 y u = 0, no hay células cancerosas presentes en el organismo y un número positivo (I0 ) de células del sistema inmune. Este es un escenario deseable y es el punto de equilibrio al cual se quiere que el sistema converja. En (Villasana & Radunskaya, 2003) se estudiaron las condiciones sobre el espacio de parámetros para garantizar la estabilidad del punto de equilibrio libre de tumor. En este trabajo se fijaron los parámetros libres a valores que garantizan la estabilidad del punto de equilibrio libre de tumor, tomando en consideración el rango fisiológicamente viable para cada parámetro, de modo que el punto es un atractor local de trayectorias vecinas. Los valores utilizados se resumen en la Tabla 1. La idea principal del estudio es llevar el sistema dentro de la cuenca de atracción de este punto. La cuenca de atracción del punto de equilibrio se define como el conjunto de funciones iniciales (historia) φ , para las cuales las trayectorias van hacia el FARAUTE Ciens. y Tec., 6(1)2011 31 Un modelo matemático para el diseño de quimioterapias Tabla 1. Valores de los Parámetros Parámetros τ a1 a4 d2 d3 c1 = c3 c2 = c4 k d1 n ρ α Valores Estimados 22 hr (0.9167 dia) 0.8470 dia−1 0.9159 dia−1 0.1145 dia−1 0.6641 dia−1 2,16x10−10 célula−1 dia−1 3,422x10−10 célula−1 dia−1 1,3x104 célula−1 dia−1 0.04 dia−1 3 0.2 dia−1 (0,3x106 célula)3 punto de equilibrio. Es difı́cil determinar analı́ticamente la cuenca de atracción de un punto de equilibrio. En este caso se presenta una aproximación numérica de la cuenca de atracción para el punto de equilibrio libre de tumor en la Fig 1, que aparece en (Villasana, 2001). Soraya Aguilar y Minaya Villasana librio libre de tumor. Se considera que el punto que representa a una función de historia converge a un punto de equilibrio si la distancia del punto final de la integración (luego de 500 dı́as) al punto de equilibrio disminuye con respecto a la distancia medida desde la posición inicial a tiempo 0. Tales funciones objetivos se dicen pertenecientes a la cuenca de atracción del punto libre de tumor. Modelo matemático incluyendo la droga citoestática en el modelo La función de una droga cito-estática es retener la célula en una fase del ciclo celular y en este caso, es de interés la retención en la fase G1, una de las etapas de la interfase. Es por esto que el término a modificar en el modelo es a1 T1 (t − τ) en la ecuación de dTdtM que representa la cantidad de células que entran a la fase de mitosis provenientes de interfase. La droga estudiada es Iressa, para la cual los fabricantes (Life Extensión Magazine, 2000) revelan que después de 3 dı́as de tratamiento el 100 % de las células es retenida en la fase G1. De acuerdo a nuestros estudios preliminares, la concentración de la droga en el organismo se satura a 333mg, considerando el suministro de 250mg diarios y la tasa de eliminación de la droga por el organismo. Esta concentración máxima se alcanza después de tres dı́as de administración de la droga. Asumiendo un efecto lineal se puede expresar el efecto de Iressa E(v) en función de los niveles de su concentración (v) de la siguiente forma E(v) = Figura 1. Región de Atracción del punto fijo (0, 0, I0 ). Los ejes TI y TM en la Fig 1 representan el número de células en interfase y en mitosis respectivamente, mientras que el eje z representa el número de células del sistema inmune. Cada punto en el espacio tridimensional representa una función inicial con valor constante en cada componente (TI , TM , I). Los puntos al interior de la región delimitada por la ‘cascada’ pertenecen al conjunto de funciones iniciales tales que usadas como funciones de historia al sistema libre de droga en (1), las órbitas convergen al punto de equi- 1 − 333 v+1 0 0 ≤ v ≤ 333 v > 333 (3) Tomando en cuenta estos datos, se puede decir que cuando la concentración de Iressa está en 333 mg, ninguna célula pasa de TI a TM , y cuando la concentración de la droga está en 0 no hay ningún efecto sobre el paso de las células entonces se puede modificar el término en la expresión original a1 T1 (t − 1 τ) a max(0, − 333 v + 1)a1 T1 (t − τ) También es necesario agregar al modelo la ecuación que simula la disminución de la nueva droga en el organismo. Para esto, asumimos un modelo exponencial para modelar el decaimiento de la concentración de Iressa y utilizando datos de vida media FARAUTE Ciens. y Tec., 6(1)2011 32 Un modelo matemático para el diseño de quimioterapias de la droga, se puede determinar que p decay v(t) = exp(ln( (2) ∗ t)) (4) El modelo planteado en el cual se incluye la droga cito-estática quedarı́a como: dT1 dt dTM dt dI dt = 2a4 TM − (c1 I + d2 )T1 − a1 T1 (t − τ) 1 v + 1)a1 T1 (t − τ) − d3 TM 333 −a4 TM − c3 TM I − k1 (1 − e−k2 u )TM ρI(T1 + TM )n − c2 IT1 − c4 TM I = k+ α + (T1 + TM )n = max(0, − −k3 (1 − ek4 u )I du1 dt du2 dt dv dt (5) = −λ1 u1 + c(t) Soraya Aguilar y Minaya Villasana está presente en la minimización de todas las funciones planteadas, ya que el objetivo del estudio se basa principalmente en la eliminación de las células cancerosas. TM (t f ) es el número de células en la fase de mitosis al final del tratamiento. Al igual que el caso anterior, está presente en todas las funciones planteadas, ya que las células cancerosas se componen de la cantidad de células en TI más la cantidad de células de TM . 1 tf R tf 0 TI (t) + TM (t) dt. es la cantidad promedio de células cancerosas a lo largo del tratamiento. Este factor está presente en algunas de las funciones objetivos planteadas. La idea detrás de este término es prevenir picos abruptos en los niveles del tumor a lo largo del tratamiento. PU es la cantidad de ciclos usados para la aplicación de la droga cito-tóxica. En general se desea minimizar la cantidad de droga utilizada lo cual podrı́a traducirse en una disminución de los ciclos de tratamiento. = −λ2 u2 + c(t) p = −ln( (2))v + cv (t) donde cv es una nueva variable de control, que representa la concentración de la droga cito-estática que entra al sistema en el tiempo t. El Problema de Control Óptimo En este estudio se plantea el problema del diseño de quimioterapias como un problema de control óptimo, donde el objetivo principal es minimizar el número de células cancerosas presentes en el sistema, manteniendo el nivel de células del sistema inmune sobre un nivel mı́nimo establecido. Dado que el tipo de solución es bang-bang, la variable a controlar es el tiempo de aplicación y descanso de las drogas cito-tóxicas y cito-estáticas, por lo cual cada solución estudiada plantea un posible esquema de aplicación y descanso de ambas drogas a lo largo del tiempo del tratamiento. En este trabajo se plantearon diversas funciones objetivos, para buscar cuál es la que genera mejores esquemas para la eliminación del tumor y sin perjudicar el sistema inmune del paciente. Se tomaron en cuenta distintos factores para cada función objetivo, los cuales se describen a continuación TI (t f ) es el número de células en interfase al final del tratamiento. Este es un factor que SDU es la suma de los tiempos de descanso en el esquema de la droga cito-tóxica. Se incluye la maximización de este término en algunas funciones para dar más tiempo al paciente de recuperarse entre aplicaciones de U. I − γImax ≥ 0, con I la cantidad de células del sistema inmune, y γImax el valor mı́nimo establecido para la cantidad de células del sistema inmune. Esta restricción controla que a lo largo del tratamiento la diferencia sea positiva para asegurar que el número de células no descienda por debajo de este mı́nimo. Si en algún momento se viola esta restricción se le impone una penalización a la función objetivo. Tomando en cuenta lo anterior se incluye en las funciones el término ζ (I − γImax ), donde ζ es la constante de penalización que se le impone cuando se viola la restricción del sistema inmune. Dada la importancia de este término, este fue incluido en todas las funciones estudiadas. Los términos:| TI (t f ) − 0,3 | y , | TM (t f ) − 0,3 | se incorporan con el fin de llevar el sistema al punto (0,3, 0,3, I0 ) que es un punto conocido dentro de la cuenca de atracción del punto fijo FARAUTE Ciens. y Tec., 6(1)2011 33 Un modelo matemático para el diseño de quimioterapias estable (0, 0, I0 ). Por ser este punto un atractor, si el sistema llega a un punto dentro de la cuenca se considera al paciente como curado. Las funciones objetivo analizadas son: F1 : TI (tt f ) + TM (t f ) + t1 f F2 : TI (tt f ) + TM (t f ) + R tf 0 TI (t) + TM (t) dt + ζ (I − γImax ) 1 R tf t f 0 TI (t) + TM (t) dt + PU + ζ (I − γImax ) F3 : TI (tt f ) + TM (t f ) + PU + ζ (I − γImax ) F4 : | TI (t f ) − 0,3 | + | TM (t f ) − 0,3 | + t1 f R tf 0 TI (t) + TM (t) dt + PU + ζ (I − γImax ) F5 : | TI (t f ) − 0,3 | + | TM (t f ) − 0,3 | +PU + ζ (I − γImax ) F6 : | TI (t f )−0,3 | + | TM (t f )−0,3 | +PU −SDU +ζ (I −γImax ) F7 : | TI (t f ) − 0,3 | + | TM (t f ) − 0,3 | −SDU + ζ (I − γImax ) F8 : | TI (t f ) − 0,3 | + | TM (t f ) − 0,3 | + t1 f R tf 0 TI (t) + TM (t) dt − SDU + ζ (I − γImax ) El método utilizado para resolver el problema de optimización asociado fue la Estrategia Evolutiva con matriz de covarianza adaptativa, que fue el que obtuvo mejores resultados en (Villasana & Ochoa, 2004). Los experimentos fueron realizados en la plataforma Matlab (Mathworks) y utilizamos una versión libre del método provista por el autor para esta plataforma. (Hansen, 1996). Para calcular los valor de TI , TM e I en (1), se resuelve el sistema de ecuaciones diferenciales con retardo usando la rutina dde23, el cual es la implementación propietaria del método publicado en (Shampine & Thompson, 2001), y que está incluida en la colección de métodos de Matlab. Los valores por defecto de los parámetros del paquete son: El número de hijos 3bb se calcula como λ = 4 + b3lnNc, donde N es la longitud de una solución, y el número de padres µ se calcula como µ = bλ /2c. Para este estudio N = 62 por lo tanto λ = 16 y µ = 8, y la población se calcula con la estrategia (µ, λ ) por lo que queda una población de 24 individuos. Los experimentos se hicieron con 100 iteraciones para alcanzar las 1600 evaluaciones de la función objetivo, la cual se determinó experimentalmente como suficientes iteraciones para la convergencia del método. Soraya Aguilar y Minaya Villasana En este trabajo la representación seleccionada para cada posible solución son duplas en la que la primera componente representa el tiempo de aplicación de una droga y la segunda componente representa el tiempo de descanso de la misma droga, cada dupla representa un ciclo dentro del esquema de aplicación. Se tomaron 15 ciclos como máximo para cada droga dentro de un protocolo. Este valor se estableció como un valor lo suficientemente grande como para obtener un protocolo de quimioterapia eficaz, tomando en cuenta que en (Villasana & Ochoa, 2004) se usaron 9 ciclos de aplicación. La estructura usada para almacenar una posible solución es un vector de 62 posiciones, en el cual las primeras 30 posiciones representan las 15 duplas del esquema de aplicación de la droga citotóxica (denominada U en este estudio), las 15 posteriores son las duplas del esquema de aplicación de la droga cito-estática (denominada V en este estudio), las dos últimas posiciones representan el número de ciclos de U (droga cito – tóxica) y de V (droga cito – estática) (denominadas PU y PV en este estudio), estos valores son calculados por el algoritmo. Resultados y discusión Para medir los resultados se tomaron algunos indicadores que ayuden a medir la eficiencia y eficacia de la solución, evaluando distintos aspectos. Estos indicadores son: 1. Interfase: Área bajo la curva para las células cancerosas en interfase y mitosis. 2. ISH: Immune System Health (Salud del Sistema Inmune). Mide el área bajo la curva de I − 0,9 que es el valor mı́nimo establecido para la cantidad de células del sistema inmune. 3. TD: Target Desviation. Mide la desviación del sistema a los valores objetivos al final del tratamiento. Para algunas funciones objetivo el valor objetivo final de la dupla (TI , TM ) es (0, 0); y para otras funciones es (0,3, 0,3). 4. SOLAP: Se mide el tiempo de aplicación en el cual se aplican ambas drogas U y V simultáneamente. 5. PU: Número de ciclos del esquema para U. FARAUTE Ciens. y Tec., 6(1)2011 34 Un modelo matemático para el diseño de quimioterapias La Tabla 2 muestra los resultados obtenidos para cada función objetivo planteada, mostrando los valores promedios los mejores valores obtenidos de 10 corridas por cada función. 6. También se observa que para el tiempo total de tratamiento, el tiempo de solapamiento es bastante corto, apenas alcanza en promedio para todas las funciones el 1.5 % del tiempo total de tratamiento. Lo que se puede concluir es que el algoritmo favorece el no solapamiento de ambas drogas, lo que va en concordancia con investigaciones de trabajos anteriores (Swierniak et al, 1996). Tabla 2. Resultados de mejor valor obtenido de 10 corridas para las funciones objetivo planteadas F.O. F1 F3 F4 F5 F6 F7 F8 Interfase 285,591 368,014 349,362 343,795 657,731 629,737 661,621 ISH 13,857 13,669 18,09 8,1412 25,763 25,732 25,73 TD 0,213 0,214 0,013 0,009 0,01 0,01 0,011 SOLAP 4,9242 11,3658 1,2039 4,8799 0,1999 0,1999 5,0755 PU 15 15 15 10 15 15 15 Algunas observaciones que se derivan de la tabla son: 1. La función objetivo en la cual se elimina la mayor cantidad de células del tumor es la correspondiente a la ecuación F1 . 2. la función objetivo que tiene mejores resultados con respecto al sistema inmune es la correspondiente a la ecuación F8 . En general se puede decir que las funciones que incluyen el punto (0,3, 0,3, I0 ) tienen mejores resultados con respecto a la salud del paciente. Soraya Aguilar y Minaya Villasana Dados los resultados de la Tabla 2, se puede decir que se ve una clara diferencia entre los resultados que incluyen el término SDU en la función objetivo y los que no en cuanto a que se tiene mayor cantidad de células cancerosas pero esto es producto de que al tener mayor tiempo de descanso entre las aplicaciones de la droga citotóxica se obtienen tratamientos más largos en el tiempo. Sin embargo estos son tratamientos que afectan menos la salud del paciente que es un escenario ideal. También se puede observar que se acerca al punto deseado al final del tratamiento, lo que se puede interpretar como un tratamiento efectivo. En la Fig 2 se puede observar un esquema de aplicación de quimioterapia obtenida con la función objetivo que no incluye la integral, y en la Fig 3 un esquema de aplicación de quimioterapias que incluye la integral. Se puede observar la diferencia en la aplicación de la droga cito-tóxica entre ambas funciones. De este estudio se desprende de forma empı́rica 3. La que más se acercó al punto objetivo son las correspondientes a la ecuaciones F6 y F7 (menor valor para TD), pero con resultados bastante duros para el sistema inmune. Dado que la mejorı́a en TD no fue significativa con respecto a las demás funciones, estas no parecieran balancear apropiadamente los diversos objetivos. 4. El término PU no pareciera ser relevante en la minimización. Figura 2. Esquema de tratamiento obtenido con la 5. La inclusión del término SDU en la función objetivo ofrece excelentes resultados sobre el sistema inmune, pero empeora el nivel de tumor durante el tratamiento. Sin embargo, el nivel de tumor al final del tratamiento es comparable con otras funciones. que la inclusión de la integral en la función objetivo obtiene esquemas que maximizan los tiempos de descanso y minimizan los tiempos de aplicación de la droga cito-tóxica al final del tratamiento, lo cual es un escenario ideal para el paciente. Comparación con resultados previos F7 FARAUTE Ciens. y Tec., 6(1)2011 35 Un modelo matemático para el diseño de quimioterapias Soraya Aguilar y Minaya Villasana que el tratamiento que incluye solo a U que sólo lleva el valor de TD a 0,4769 en el mismo tiempo. Conclusiones y Otros trabajos Figura 3. Esquema de tratamiento obtenido con la F8 Se consideraron algunas medidas para comparar los resultados actuales con los resultados en trabajos anteriores (Villasana & Ochoa, 2004), donde sólo se utilizaban drogas cito-tóxicas en el protocolo de quimioterapia. Solamente se realizó la comparación con la primera función objetivo ya que es la única que se repite en ambos trabajos. Dado que el tratamiento que incluye las drogas U y V es más largo en el tiempo y para hacer una justa comparación, se truncó la solución en función del tiempo del tratamiento que solo usa la droga U. Se consideró además en ambas funciones objetivos que el sistema debe aproximarse al punto fijo (0, 0, I0 ), obteniendo los resultados de la Tabla 3. Tabla 3. Comparación de esquemas hallados por la Estrategia Evolutiva incluyendo la droga citoestática y sin incluirla. Incluyendo U y V Sin Incluir V Interfase 13,857 13,669 ISH 0,213 0,214 TD 4,9242 11,3658 PU 15 15 En la Tabla 3, se puede observar la disminución de los valores de las células cancerosas, por lo que se puede decir que el tratamiento que incluye ambas drogas es más efectivo tomando en cuenta que tiene patrones de administración similares. Esto indica que la inclusión de la droga cito-tóxica aumenta la efectividad del tratamiento. También se observa una disminución en el número de células al final del tratamiento, y estas mejoras se obtienen sin mayor perjuicio a la salud del sistema inmune. También hay que tomar en cuenta que el tratamiento que incluye ambas drogas llega al valor de TD 0,2058 al final del tratamiento completo, lo que es mucho más efectivo Se observa una mejorı́a con respecto a los valores del tumor a lo largo y al final del tratamiento cuando se incluyen ambas drogas, por lo que se puede concluir que la inclusión de una droga cito-estática puede mejorar la efectividad de la droga cito-tóxica, sin que el sistema inmune se vea perjudicado. Por otra parte, el algoritmo encuentra tratamientos más largos que en el trabajo anterior (Villasana & Ochoa, 2004), lo que pudiese ser más molesto para el paciente, pero el valor del TD (Target Desviation) después de terminar el tratamiento completo presenta una mejora significativa con respecto a los resultados anteriores. La mejor función objetivo encontrada en nuestro estudio comparativo preliminar fue | TI (t f ) − 0,3 | + | TM (t f ) − 0,3 | + t1f TM (t) dt − SDU + ζ (I − γImax ) R tf 0 TI (t) + ya que consigue buenos resultados en cuanto a la eliminación del tumor a lo largo del tratamiento, y al final del mismo reporta una reducción tan buena como otras funciones en las cuales éste es el objetivo principal y único. Esta función objetivo arroja soluciones que representan un patrón ideal para el paciente, en el que al final del tratamiento se aplica muy poca droga U, lo que permite una recuperación del mismo. Este hecho se evidencia en los valores del sistema inmune en los que se ve una mejora significativa (dinámica no mostrada). Se pudo observar después de varios experimentos que el efecto que tiene el término de la integral sobre el esquema es la regularidad en los tiempos de descanso de U, que es un aspecto deseable dentro de la solución desde el punto de vista de la calidad de vida del paciente. La inclusión de PU no tiene ninguna influencia ya que el problema no minimiza esta cantidad y las soluciones tienden a considerar el máximo número de ciclos. La suma de los tiempos de descanso de U tiene un efecto positivo en la salud del sistema inmune aunque desmejora la cantidad de células cancerosas a lo largo del tratamiento. Sin embargo se puede observar que al final del tratamiento se logra el objetivo de llevar la dinámica del tumor dentro de la cuenca de atracción. La inclusión dentro FARAUTE Ciens. y Tec., 6(1)2011 36 Un modelo matemático para el diseño de quimioterapias de la función objetivo de minimizar hasta llegar a algún punto dentro de la cuenca de atracción (como por ejemplo al punto (0,3, 0,3, I0 )) hace que el sistema llegue muy cerca de estos valores al final del tratamiento, considerando al paciente curado. En las simulaciones realizadas se pudo ver que las mejores soluciones favorecen el no solapamiento en la aplicación de ambas drogas llegando a no superar el 1.5 % por ciento del tiempo total de aplicación, lo que va en concordancia con trabajos anteriores (Swierniak et al, 1996). Este trabajo sirvió como base para otros trabajos (Villasana et. al, 2010) donde se hacen entonaciones al modelo matemático en la identificación del sub-sistema de la droga cito-estática y se consideran aquellas funciones objetivos que produjeron resultados interesantes en este estudio preliminar del sistema F4 , F5 y F6 . Otro aspecto interesante explorado en profundidad es el efecto del solapamiento de la aplicación de ambas drogas en el tratamiento que se aborda considerando representaciones que permitan el solapamiento de ambas drogas y representaciones donde dicho solapamiento no esté permitido. Soraya Aguilar y Minaya Villasana Villasana M., (2001). A Delay Differential Equation Model for Tumor Growth. Dissertation for the degree of Doctor of Philosophy. Graduate Faculty of Mathematics. Claremont Graduate University. Claremont, California. USA Villasana M., Ochoa G. (2004). Heuristic Design of Cancer Chemotherapies. IEEE Transactions on Evolutionary Computation. 8(6): 513-521. Villasana M., Ochoa G., Aguilar S. (2010). Modeling and Optimization of Combined Cytostatic and Cytotoxic Cancer Chemotherapy. Artificial Intelligence in Medicine. 50(3): 163-173. Villasana M, Radunskaya A. (2003). A delay differential equation model for tumor growth. Journal of Mathematical Biology. 47: 270-294. Bibliografı́a Hansen N. (1996). The CMA evolution strategy. http://www.lri.frhansen/cmaesintro.html Liang Y, Leung K. (2006). A Novel Evolutionary Drug Scheduling Model in Cancer Chemotherapy. IEEE Transactions on information technology in biomedicine. 10: 237-245. Life Extensión Magazine. (2000). Suppressing cancer cell growth - a novel approach. www.lef.org/magazine/mag2000/dec2000 awsi2.html. Consultado en Mayo de 2007. Shampine L., Thompson S. (2001). Solving DDEs in MATLAB. Applied Numerical Mathematics. 37: 441-458 Swierniak A., Polanski A., Kimmel M. (1996). Optimal control problem arising in cell-cycle- specific cancer chemotherapy. Cell Proliferation. 29: 117139. Tse L, Liang Y, Leung K. (2007). A Memetic Algorithm for Multiple Drugs Cancer Chemotherapy Shedule Optimization. IEEE Transactions on System, Man and Cybernetics part B. 37: 84-91. FARAUTE Ciens. y Tec., 6(1)2011 37