Disnea: aspectos fisiopatológicos y aproximación diagnóstica
Anuncio

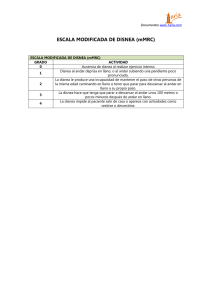
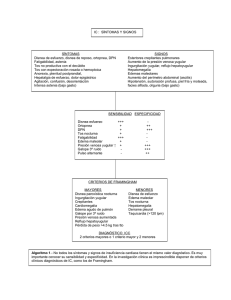
83 Módulo 7 – Fascículo Nº 1 – 2011 Disnea: aspectos fisiopatológicos y –aproximación diagnóstica Disnea: aspectos fisiopatológicos y aproximación diagnóstica Dra. Patricia Aruj, Dr. Edgardo Sobrino y Dr. Guillermo Semeniuk Contenidos – Mecanismos fisiopatológicos de la disnea –Quimiorreceptores –Mecanorreceptores – Receptores de la vía aérea – Receptores pulmonares – Receptores de la caja torácica – Músculos respiratorios – Fatiga muscular respiratoria – Patrón respiratorio – Disnea en diversas condiciones clínicas – Síndrome de hiperventilación – Métodos de evaluación – Diagnóstico –Evaluación clínica – Examen físico –Hallazgos clínicos que sugieren insuficiencia cardíaca – Hallazgos clínicos que sugieren enfermedad pulmonar obstructiva crónica –Estudios diagnósticos – Prueba de ejercicio cardiopulmonar – Fuerza de las recomendaciones –Referencias Abreviaturas ATS American Thoracic Society BNP Péptido natriurético cerebral o péptido natriurético tipo B CO2 Dióxido de carbono CRF Capacidad residual funcional EAV Escala analógica visual ECGElectrocardiograma EPOCEnfermedad pulmonar obstructiva crónica FD Fatiga diafragmática FMR Fatiga muscular respiratoria HTA Hipertensión arterial HTP Hipertensión pulmonar ICC Insuficiencia cardíaca congestiva LR Likelihood ratio (coeficiente de probabilidad) MRC Medical Research Council MV Murmullo vesicular O2Oxígeno Pdi Presión transdiafragmática PECPPrueba de ejercicio cardiopulmonar SH Síndrome de hiperventilación SNC Sistema nervioso central TEP Tromboembolia pulmonar Ti Tiempo inspiratorio Ttot Tiempo total o duración total de un ciclo respiratorio Servicio de Neumonología, Instituto de Investigaciones Médicas Alfredo Lanari 84 La disnea es un problema clínico de impacto similar al dolor, que compromete a un cuarto de la población general y a la mitad de los pacientes seriamente enfermos.(1, 2) Es una expresión subjetiva de la percepción de la intensidad del estímulo durante el acto de respirar o en asociación con él. Es un síntoma complejo, sujeto a diferentes mecanismos desencadenantes y cuya evaluación resulta dificultosa, sin que exista además un acuerdo unánime sobre cuáles son concretamente dichos mecanismos y cuáles los mejores métodos para su evaluación. La American Thoracic Society (ATS) la definió como una experiencia subjetiva de malestar respiratorio que consta de sensaciones cuantitativamente distintas que varían en intensidad.(3) Dicha experiencia deriva de interacciones entre factores fisiológicos, psicológicos, sociales y ambientales, que a su vez pueden inducir respuestas secundarias fisiológicas o conductuales. Esta sensación proviene de una serie de pasos que comprometen la activación de receptores sensoriales, la transmisión y el procesamiento de señales en centros cerebrales. En la práctica, el médico trata la enfermedad de base asociada con la disnea y, si el tratamiento es exitoso, la disnea desaparece. Si el tratamiento no es efectivo, el síntoma disnea es un problema en sí y poco se puede hacer en forma específica para aliviarlo. Generalmente se presta poca atención a los mecanismos por los cuales la enfermedad de base produce disnea o en qué medida cada uno de los procesos, diferentes en su fisiopatología, se acompañan por una misma o una diferente sensación de disnea. –––––––––––––––––––––––––––––––– La disnea es la experiencia subjetiva de malestar respiratorio. –––––––––––––––––––––––––––––––– La sensación de dificultad para respirar aumenta con una carga mayor de ejercicio aun en sujetos normales, pero en pacientes con enfermedades respiratorias, circulatorias y neuromusculares puede experimentarse con poco ejercicio o aun en reposo. El síntoma en sí mismo es una causa importante de padecimiento y discapacidad. Disnea de origen desconocido o no justificada es aquella cuya etiología no se puede explicar – Módulo 7 – Fascículo Nº 1 – 2011 mediante una historia clínica exhaustiva, una exploración física completa o pruebas diagnósticas de rutina [hemograma, gases en sangre arterial, radiografía de tórax, electrocardiograma (ECG) y espirometría].(4) Disnea crónica es la que se prolonga durante más de un mes. El diagnóstico diferencial de la disnea crónica es muy amplio y la causa subyacente a ella no se puede determinar en función de su duración o intensidad.(5) Aproximadamente las dos terceras partes de los casos de disnea son causados por enfermedades cardíacas o pulmonares.(6) Asma, insuficiencia cardíaca congestiva (ICC), enfermedad pulmonar obstructiva crónica (EPOC), neumonía, isquemia cardíaca, enfermedad pulmonar intersticial y condiciones psicógenas (p. ej., trastorno por ansiedad generalizada, crisis de pánico, síndrome de estrés postraumático) son la causa de disnea en un 85% de los pacientes.(5, 7) En la disnea crónica de origen desconocido, la prueba de ejercicio cardiopulmonar (PECP) es el instrumento más útil para llegar a un diagnóstico etiológico o dirigir las posteriores pruebas complementarias, lo que permite un ahorro en costos, tiempo y molestias a los pacientes. –––––––––––––––––––––––––––––––– Aproximadamente las dos terceras partes de los casos de disnea son causados por enfermedades cardíacas o pulmonares. –––––––––––––––––––––––––––––––– El concepto de que la disnea representa una única sensación que varía sólo en intensidad se está reemplazando por la idea de que, al igual que el dolor, es multidimensional(8) y, como el dolor, la sensación de respiración dificultosa puede ser producida o modulada por la estimulación de receptores específicos localizados a lo largo del sistema respiratorio, desde los quimiorreceptores centrales y periféricos hasta los mecanorreceptores de las vías aéreas superiores, los pulmones y la caja torácica. Sin embargo, el estudio aislado de estos receptores no permite un acabado conocimiento de la disnea, por lo que debe considerarse el papel de la sensación en relación con el comando neurológico central.(9) Disnea: aspectos fisiopatológicos y aproximación diagnóstica –––––––––––––––––––––––––––––––– La prueba de ejercicio cardiopulmonar es el instrumento más útil para establecer un diagnóstico etiológico o guiar estudios posteriores en la disnea crónica de origen desconocido. –––––––––––––––––––––––––––––––– En un intento de entender las bases de la disnea, cabe tener en cuenta que es una sensación consciente y debe investigarse tanto en términos neuroanatómicos como psicofísicos para relacionar el estímulo físico con la sensación evocada.(8, 10) Mecanismos fisiopatológicos de la disnea ___________ La disnea se asocia con condiciones en las cuales la actividad del centro respiratorio está incrementada o el sistema respiratorio está sometido a carga mecánica.(11-13) Estas condiciones se caracterizan por una sensación de “hambre de aire” o aumento del trabajo para respirar. Algunos trastornos se asocian con la estimulación de receptores en los pulmones; en estos casos, los pacientes pueden describir la sensación como de opresión torácica y constricción. Además de estos factores cualitativos, la intensidad de la disnea puede ser modificada por la correspondencia entre el comando motor respiratorio o señales originadas en el sistema nervioso central (SNC) Fig. 1. Mecanismos fisiopatológicos de la disnea. Señales eferentes y aferentes. 85 y la retroalimentación aferente de receptores en el sistema respiratorio. Una variedad de señales provenientes de quimiorreceptores en la sangre y el cerebro, mecanorreceptores en las vías aéreas, los pulmones, la pared torácica o los músculos respiratorios y comandos respiratorios motores centrales se consideran responsables de mediar la sensación de disnea (Figura 1). La sensación de esfuerzo muscular es un alerta consciente de la activación voluntaria de los músculos esqueléticos. Proviene de la activación simultánea de la corteza sensorial al tiempo que los músculos reciben la señal de contraerse.(13) En ciertas circunstancias, como debilidad muscular o fatiga, aun una pequeña tarea requiere un esfuerzo importante. La sensación de esfuerzo se relaciona con la presión generada por los músculos respiratorios en función de la máxima capacidad generadora de presión, se incrementa cuando la carga a los músculos respiratorios es elevada o éstos se encuentran debilitados por fatiga, parálisis o un aumento en el volumen pulmonar.(14, 15) Para un nivel dado de patrón ventilatorio, tanto los individuos normales como enfermos están más disneicos cuando se encuentran hipercápnicos que eucápnicos. Si se suprime la ventilación por debajo del nivel del drive químico, la sensación de disnea aumenta, aunque los índices de esfuerzo respiratorio (como la ventilación) disminuyen.(16) 86 Cuando se estudió la relación entre esfuerzo y disnea en sujetos normales manteniendo un nivel constante de ventilación, las dos sensaciones se hallaron disociadas: la disnea se incrementaba paralelamente al aumento teleespiratorio del CO2, aunque la sensación de esfuerzo fue en descenso.(17) Pese a que la evidencia sugiere que esfuerzo y disnea no son lo mismo, la sensación de esfuerzo puede ser el factor contribuyente predominante a la sensación de disnea cuando los músculos respiratorios están fatigados o debilitados, o cuando la carga está aumentada. La disnea involucra mecanismos centrales, periféricos y quimiorreceptores.(18-20) –––––––––––––––––––––––––––––––– En la disnea están involucrados: – Mecanismos centrales. – Mecanismos periféricos. – Quimiorreceptores. –––––––––––––––––––––––––––––––– – Módulo 7 – Fascículo Nº 1 – 2011 el SNC y, de esta manera, modular la ventilación y la sensación de esfuerzo respiratorio. Quimiorreceptores La idea de que los quimiorreceptores centrales y periféricos intervienen directamente en la generación de disnea ha estado presente en quienes estudiaron este tema. Cuando el impulso central aumenta como consecuencia de hipoxia o hipercapnia, la intensidad de la disnea aumenta, pero también aumenta el impulso motor a los centros respiratorios, receptores musculares, articulares e intrapulmonares. La evidencia sugiere que la hipercapnia puede producir sensación de dificultad respiratoria independientemente de los cambios en la ventilación total.(21) La actividad de los músculos respiratorios no parece necesaria, como lo sugieren trabajos en pacientes con lesiones medulares altas.(22) Receptores de la vía aérea Los receptores de la vía aérea superior regulan la deglución, el habla y la protección de la vía aérea. Su estimulación produce cambios en la ventilación y en el patrón respiratorio. La información aferente de estos receptores sigue la vía de los nervios trigémino, glosofaríngeo, hipogloso y vago, llegando a los centros respiratorios.(23, 24) Tales receptores pueden modular la sensación de dificultad respiratoria tanto por modificaciones en la ventilación como por acción directa sobre el SNC.(25-27) La mejoría de la disnea con la administración de O2 por cánula nasal puede deberse en parte a la estimulación de los receptores de las vías aéreas superiores. Algunos pacientes con disnea describen un alivio subjetivo cuando se aplica aire frío en la cara,(23) lo que sugiere que la estimulación de los receptores en el área del trigémino puede tener un efecto directo sobre la sensación de disnea. Los pacientes con EPOC refieren disminución de la disnea cuando respiran aumentando la resistencia espiratoria a nivel de la boca y se incrementa su dificultad cuando lo hacen a través de una pieza bucal. Cambios en la distribución de la ventilación con mejoría del intercambio gaseoso y traslado del punto de igual presión hacia la boca serían los responsables de este alivio.(28) El uso de presión positiva continua en la vía aérea podría disminuir la disnea al reducir la compresión dinámica de la vía aérea. Esto apoya la idea de que la pared de las vías aéreas tiene receptores sensibles al colapso dinámico o a cambios en la presión transmural y que la información proveniente de estos receptores modula la sensación de disnea. Mecanorreceptores Los receptores ubicados en las vías aéreas superiores e inferiores, parénquima pulmonar, caja torácica, responden a estímulos mecánicos como presión, estiramiento y variaciones en la temperatura ocasionados por el flujo aéreo. Su estimulación puede modificar la información aferente transmitida desde el sistema respiratorio hasta Receptores pulmonares La información proveniente de los receptores ubicados en el parénquima pulmonar es transmitida al SNC a través del nervio vago.(29) Los receptores pulmonares de estiramiento participan en la finalización de la inspiración, los irritantes en el epitelio responden a estímulos mecánicos y químicos mediante broncoconstricción y las Disnea: aspectos fisiopatológicos y aproximación diagnóstica fibras C localizadas en la pared alveolar y los vasos sanguíneos responden al edema intersticial. (30) Estos receptores podrían tener un papel en la modulación del patrón respiratorio y de la disnea en pacientes con enfermedad intersticial y con ICC, aunque hay estudios contradictorios, ya que la apreciación consciente de carga respiratoria se mantiene aun luego de bloqueo vagal.(29) Receptores de la caja torácica Receptores ubicados en las articulaciones, los tendones y los músculos de la caja torácica proveen información del movimiento del sistema respiratorio y del estado de los músculos respiratorios. Con una carga inspiratoria elástica o resistiva, la velocidad y la magnitud del acortamiento de los músculos respiratorios se modifica ante un impulso central dado. La sensación de dificultad respiratoria ocurre cuando el desplazamiento alcanzado por el sistema respiratorio es menor que el esperado. Cuando los centros respiratorios son estimulados y el impulso que de ellos proviene aumenta, la disnea parece que es mayor cuando el movimiento de la caja torácica se ve reducido. La falta de adecuación entre el signo eferente de los centros respiratorios y el aferente de la caja torácica que alcanza el SNC deriva en disnea. Este hecho puede referirse como disociación eferente-aferente.(31) La disociación entre el impulso químico para respirar y la ausencia de movimientos torácicos durante la apnea voluntaria intensifica la sensación de disnea. La hipercapnia por el agregado de CO2 al aire inspirado produce menos disnea si el patrón respiratorio consiste en grandes movimientos torácicos. A la inversa, la disnea aumenta si los movimientos torácicos se limitan voluntariamente por debajo de los que corresponderían a un patrón libre.(32) Si bien la disnea es una expresión de la sensación de esfuerzo respiratorio, la intensidad y la calidad de las experiencias subjetivas durante el acto de respirar también dependen de la retroalimentación aferente en los receptores de los músculos respiratorios. Estas aferencias pueden actuar ya sea cambiando el patrón de actividad motora o bien por efecto directo sobre los centros cerebrales superiores. 87 Músculos respiratorios La sensación de esfuerzo se refiere a la intensidad del comando motor. Éste puede medirse como la actividad de un músculo en porcentaje de la máxima. Si la actividad generada por un esfuerzo máximo representa el reclutamiento de todas las unidades motoras, la caracterización de la actividad real en relación con la máxima permite una medición del comando motor. La sensación de esfuerzo es traducida por pequeñas interneuronas y mediada por mecanismos de retroalimentación colateral alta en el SNC con destino final en la corteza sensitiva. La sensación de tensión está relacionada con la desarrollada por el músculo, traducida por los órganos tendinosos y mediada por el componente nervioso aferente. La sensación de desplazamiento se relaciona con la velocidad y la extensión de la contracción muscular. Es traducida por los husos neuromusculares, receptores articulares y cutáneos y mediada por nervios aferentes. La sensación de dolor se experimenta cuando los músculos son sometidos a un exceso de trabajo y se asocia con daño estructural que puede estimular terminaciones nerviosas libres. Las sensaciones musculares a nivel consciente no están limitadas a las mencionadas, ya que de ellas derivan otras. La impedancia a la acción del músculo se puede detectar independientemente de la de desplazamiento o tensión y puede originar sensaciones que integran fuerza y desplazamiento. La debilidad se puede detectar por la relación entre esfuerzo y fuerza desarrollada. Otra dimensión importante de las sensaciones musculares es la memoria consciente de las intensidades de todas estas sensaciones. En el caso de los músculos respiratorios, la tensión desarrollada por el diafragma puede evaluarse mediante la medición de la presión transdiafragmática; el desplazamiento está en relación con el flujo aéreo y el volumen corriente. La actividad muscular, el esfuerzo, la tensión, el desplazamiento, la resistencia y la debilidad son sólo algunas de las sensaciones que se pueden percibir. Aunque normalmente no somos conscientes de nuestra actividad respiratoria, en un amplio 88 rango de circunstancias el acto respiratorio alcanza niveles conscientes. En condiciones experimentales, la respiración con cargas inspiratorias resistivas o elásticas en aumento se asocia con un incremento progresivo de la sensación de la carga percibida. La estrecha correlación con la presión de la vía aérea sugiere que la intensidad de esta sensación está en relación con la magnitud y la duración de la fuerza generada por los músculos respiratorios. Existen dos determinantes de la sensación de fuerza respiratoria: la de tensión muscular mediada por una retroalimentación aferente desde los mecanorreceptores y la de esfuerzo, basada en signos del comando motor central y copia eferente. Las sensaciones de tensión y esfuerzo se pueden percibir independientemente. En gran parte, disnea es también una expresión de la sensación de esfuerzo respiratorio. Durante el ejercicio, la intensidad de la disnea aumenta conforme a la intensidad del ejercicio y la ventilación pulmonar. El agregado de una carga inspiratoria resistiva externa aumenta más la disnea, aun cuando la ventilación desciende por efecto de la carga. La intensidad de la disnea se correlaciona mejor con la presión de oclusión traqueal a los 100 mseg del inicio de la inspiración, una medida del impulso eferente de los centros a los músculos respiratorios. En las circunstancias clínicas en que la disnea se produce, su intensidad depende de las demandas metabólicas, de los mecanismos de control respiratorio, de la fuerza estática de los músculos respiratorios, de la velocidad de acortamiento, longitud y extensión de la contracción, de la coordinación entre diferentes grupos musculares, de la presión inspiratoria pico y del estado metabólico de los músculos.(33) Fatiga muscular respiratoria Para el sistema respiratorio, fatiga es la incapacidad de continuar generando la presión necesaria para mantener una ventilación alveolar adecuada. Es una causa de insuficiencia ventilatoria y la disnea que la acompaña puede originarse en los músculos respiratorios fatigados. La fatiga muscular respiratoria (FMR) ocurre cuando se excede la resistencia de los músculos – Módulo 7 – Fascículo Nº 1 – 2011 respiratorios. Bellemare y Grassino demostraron que hay un umbral por debajo del cual la fatiga diafragmática (FD) no ocurre.(34, 35) Este análisis se fundamenta en que el desarrollo de FD está relacionado con la fuerza y la duración de la contracción muscular. En el caso del diafragma, la fuerza de contracción puede expresarse como la presión transdiafragmática (Pdi) medida en cada contracción en relación con la fuerza máxima del diafragma desarrollada durante un esfuerzo estático a capacidad residual funcional (CRF) o Pdimáx. La duración de la contracción diafragmática puede expresarse como la relación entre la duración de la inspiración o tiempo inspiratorio (Ti) y la duración total de un ciclo respiratorio o tiempo total (Ttot). TTdi = Pdi/Pdimáx × Ti/Ttot donde: TTdi es el índice tensión-tiempo del diafragma que representa la integral de fuerza (o presión) y tiempo: TTdi = ∫ P × T Más que una Pdi crítica única, existe un único TTdi crítico de aproximadamente 0,15-0,20. Los individuos normales no llegan al umbral de fatiga, excepto durante ejercicios extremos y en los episodios de apneas obstructivas. En contraste, ciertas enfermedades, ya sea por la menor capacidad generadora de una fuerza máxima o por el aumento de la Pdi espontánea, están más cerca del umbral de FD. En este grupo pueden hallarse pacientes con obstrucción bronquial, enfermedades neuromusculares, obesos o con fibrosis pulmonar. El TTdi permite detectar patrones ventilatorios que pueden provocar FD al informar acerca de la reserva de fuerza en términos de fatigabilidad del diafragma.(36) La intensificación de la disnea durante el desarrollo de FMR no refleja la mayor activación o contracción del diafragma. El aumento de la sensación de esfuerzo inspiratorio registrado durante cargas inspiratorias resistivas fatigantes se correlaciona más con el nivel de activación de los músculos de la caja torácica y del cuello que con el nivel de activación del diafragma. Esto sugiere Disnea: aspectos fisiopatológicos y aproximación diagnóstica que para un nivel global de actividad respiratoria, la intensidad de la disnea parece que es mayor cuando la presión es generada predominantemente por los músculos intercostales y/o accesorios. Patrón respiratorio Para una ventilación alveolar dada y para determinadas propiedades mecánicas del sistema respiratorio hay una frecuencia respiratoria óptima que se asocia con un trabajo respiratorio mínimo. La debilidad de los músculos respiratorios contribuye a la percepción del esfuerzo respiratorio que se vincula más con los cambios de la presión intratorácica que con cambios en la Pdi. Durante carga resistiva, en sujetos conscientes se observa una prolongación del tiempo inspiratorio. Si un mismo volumen corriente ingresa en un período de tiempo mayor, el flujo aéreo y la presión pico de la vía aérea son menores. En contraste, la terminación prematura de la inspiración limita el volumen corriente y el flujo inspiratorio pico. La necesidad de minimizar la disnea mediante la adopción de patrones respiratorios alternativos puede ser un mecanismo aún más importante en pacientes con enfermedad pulmonar. En algunos pacientes con EPOC o fibrosis pulmonar, el tiempo inspiratorio es menor y, no obstante el aumento del impulso central, el volumen corriente también lo es. Este fenómeno puede conducir a retención crónica de CO2, que es el costo de evitar la FMR. Estos cambios en el patrón respiratorio que minimizan la fuerza desarrollada por los músculos respiratorios pueden significar además un intento para disminuir la sensación de disnea.(37) Para un nivel constante de estímulo químico, la sensación de dificultad respiratoria se intensifica cuando la ventilación aumenta o disminuye en forma voluntaria respecto del nivel espontáneamente adoptado, aun cuando la PO2 y la PCO2 no cambian. De manera similar, para una ventilación constante, los cambios en el patrón respiratorio intensifican la disnea. Todo esto sugiere que el patrón respiratorio adoptado es un intento de minimizar la sensación de esfuerzo respiratorio. Los ajustes en el patrón ventilatorio dependen, en parte, de la sensibilidad perceptual de 89 la sensación respiratoria. Sujetos normales y pacientes con EPOC sometidos a cargas inspiratorias o a un aumento de espacio muerto muestran exponentes para la percepción respiratoria que se correlacionan negativamente con el volumen corriente. Estos hallazgos sugieren que la mayor sensibilidad perceptual o, lo que es lo mismo, niveles altos de sensación llevan a una disminución del impulso central para reintegración central. La sensación de disnea parece proceder de dos sensores primarios periféricos: quimiorreceptores y fibras vagales. La información adicional aferente es provista por los mecanorreceptores de la pared torácica y los receptores de estiramiento. La información neural aferente converge en el núcleo del tracto solitario en la médula y, de allí, probablemente vía tálamo a la corteza insular, el sistema límbico y la corteza sensoriomotora. La disnea ocurre cuando hay un incremento mayor que lo habitual en los niveles de información aferente de los sensores periféricos, lo cual se procesa en la corteza insular y la red cortical y genera una salida neural al sistema respiratorio; la retroalimentación aferente de esta salida neural (cambio de volumen pulmonar, flujo de aire, ventilación) es provista por los receptores de estiramiento pulmonar y otros receptores inervados por nervios vagales y mecanorreceptores de la pared. Si la salida central no produce el resultado esperado (flujo de aire o ventilación), ya sea por falla del efector (debilidad o parálisis) o alteraciones mecánicas pulmonares (EPOC, enfermedades parenquimatosas), se produce la sensación de disnea. En el asma y en la EPOC, la relación entre el drive inspiratorio neural y el output ventilatorio y por lo tanto la disnea pueden empeorar (aumento de la capacidad residual funcional) en el ejercicio y mejorar con la broncodilatación. Esta afirmación presume que los centros corticales tienen una memoria preexistente de input aferente normal y respuesta eferente normal, en términos del esfuerzo requerido para lograr una ventilación o flujo aéreo dado. La extensión de esta desigualdad entre la nueva información aferente/eferente y la memoria preexistente (un cambio en la relación entre el drive respiratorio central y el output) determina la intensidad de la disnea.(21) 90 Los factores que regulan la calidad y la intensidad de la disnea son múltiples; la contribución cuantitativa de cada uno de ellos no está suficientemente aclarada.(38) Disnea en diversas condiciones clínicas ___________ Aproximadamente el 75% de las causas de disnea son respiratorias o cardiológicas.(5, 6) La disnea resulta de: – Un aumento en el drive respiratorio o esfuerzo necesario para superar una carga impuesta. – Un aumento en la proporción de la fuerza muscular respiratoria requerida para respirar (enfermedad neuromuscular o hiperinsuflación). – Un aumento en los requerimientos ventilatorios (consumo metabólico, anemia, hipoxemia, enfermedad vascular pulmonar). Algunos pacientes perciben más la disnea que otros a pesar de la misma limitación funcional. En el estudio de Burki, la percepción de una carga resistiva mayor en asmáticos fue similar a la de los sujetos normales y Hudgel encontró que el umbral de detección era mayor en pacientes ansiosos o dependientes.(39, 40) En contraste, la percepción de carga en pacientes con EPOC estaba bloqueada, probablemente por atenuación de la actividad mecanorreceptora como cambio adaptativo, o en el procesamiento central de la información.(41) Variaciones en el nivel de disnea para un grado determinado de deterioro funcional se relacionan con el hecho de que es una sensación subjetiva, dependiente del estímulo involucrado, del procesamiento central y de la integración de muchas aferencias motoras, del contexto situacional en el que ocurre y de la capacidad del paciente de describirla. Burns y Howell evaluaron dos grupos de pacientes con EPOC: un grupo grave (VEF1 0,67 litros), que calificaron su disnea como apropiada, y un grupo menos grave (VEF1 1,88 litros), que la calificaron como desproporcionada. En este último grupo, todos los pacientes fueron considerados psiquiátricamente enfermos (52% depresivos, 22% ansiosos, 26% con reacciones histéricas). La disnea del grupo que la refería como desproporcionada se relacionaba mal con el ejercicio, aumentaba en el – Módulo 7 – Fascículo Nº 1 – 2011 reposo, se asociaba con ataques de hiperventilación con pánico, presentaba fluctuaciones en su gravedad, despertaba al paciente por la noche, se asociaba con mayor dificultad en la inspiración que en la espiración y mejoraba con alcohol o sedantes.(42) –––––––––––––––––––––––––––––––– Mecanismos por los que se produce la disnea: –Aumento en el drive respiratorio o esfuerzo necesario para superar una carga impuesta. – Aumento en la proporción de la fuerza muscular respiratoria requerida para respirar (enfermedad neuromuscular o hiperinsuflación). –Aumento en los requerimientos ventilatorios (consumo metabólico, anemia, hipoxemia, enfermedad vascular pulmonar). –––––––––––––––––––––––––––––––– Síndrome de hiperventilación El síndrome de hiperventilación (SH) se asocia con trastornos orgánicos (neurológicos, tóxicos, hepáticos, dolor intenso y ocasionalmente con asma, enfermedad vascular o pulmonar intersticial) y psicógenos (ansiedad).(43, 44) Los mecanismos responsables de iniciar y sostener el SH se desconocen; situaciones estresantes causan alteraciones en el patrón respiratorio en individuos normales, por lo cual se postula que reflejaría una hiperrespuesta del sistema respiratorio al estrés.(45-47) La disnea se presenta en el 50-90% de los pacientes con SH como una sensación de incapacidad de hacer una respiración lo suficientemente profunda o una sensación de sofocación u opresión en el tórax.(48, 49) A diferencia de la disnea respiratoria o cardiovascular, en el SH hay escasa relación con el esfuerzo y su alivio con el reposo es menos probable. Suele asociarse con otros síntomas y signos, como dolor torácico o tetania.(50) Métodos de evaluación ___________ Se requiere una historia clínica detallada para evaluar la disnea (Cuadros 1 y 2). A diferencia de la disnea respiratoria o cardiovascular, en el SH hay escasa relación con el esfuerzo y su alivio con el reposo es menos probable. Suele asociarse con otros síntomas y signos, como dolor torácico o tetania. 91 Disnea: aspectos fisiopatológicos y aproximación diagnóstica Datos de la historia clínica – Circunstancias de aparición (reposo, ejercicio) – Posición (ortopnea, trepopnea, platipnea) – Otros factores precipitantes (ambientales, emocionales) – Cronología (duración, progresión, variaciones diurnas y estacionales, constante o intermitente) – Factores de alivio (reposo, medicamentos) – Factores predisponentes (tabaquismo, exposición ocupacional) – Condiciones médicas asociadas (pulmonares, cardíacas, neuromusculares) – Historia familiar Cuadro 1. Historia clínica detallada Evaluación de Escala MRC (Medical Research Council) disnea aguda Escala analógica visual (EAV) Escala de categorías de Borg Evaluación de Índices de disnea basal y de transición disnea crónica (IDB-IDT) Disnea en el cuestionario respiratorio crónico (CRC) Cuadro 2. Métodos para la evaluación de la disnea aguda y crónica –––––––––––––––––––––––––––––––– A diferencia de la disnea respiratoria o cardiovascular, en el SH hay escasa relación con el esfuerzo y su alivio con el reposo es menos probable. Suele asociarse con otros síntomas y signos, como dolor torácico o tetania. –––––––––––––––––––––––––––––––– La disnea sigue siendo una expresión clínica independientemente del ámbito donde se produzca (consulta ambulatoria, internación, servicio de urgencias). Con una actitud crítica y tendiente a cuantificar cualquier manifestación clínica, para luego evaluar sus modificaciones, existen cuestionarios estandarizados que pretenden medir y expresar numéricamente la magnitud del síntoma. Siempre existirá la subjetividad, pero al menos habrá una cifra para comparar y emitir un juicio más objetivo. Su validez, facilidad de uso, sensibilidad al cambio, etc., deben comprobarse en la misma población que va a utilizarse y, además, debe emplearse una escala validada al idioma y a la realidad sociocultural de la población en estudio. Hay dos tipos de escalas de medición, las indirectas, que miden el impacto de la disnea en las actividades de la vida diaria, que es lo que más le importa al paciente [entre ellas están la del Medical Research Council (MRC) , el Diagrama de Costo de Oxígeno, la escala de Mahler (BDI-TDI), que es multidimensional, y los cuestionarios de calidad de vida, como el St George]. El segundo tipo son las directas, que miden la tolerancia al ejercicio y son más objetivas, porque se le solicita al paciente que realice un ejercicio y se cuantifica la disnea (entre ellas están la escala de Borg y la escala analógica visual (EAV). La escala MRC (Medical Research Council), dentro de las escalas indirectas, se utilizó inicialmente para estudiar la neumoconiosis, se ha ido modificando y tiene valor pronóstico. La American Thoracic Society (ATS) recomienda una escala que mide la magnitud de la tarea que produce disnea en grados de 0 a 4 (Cuadro 3). Las desventajas de esta escala son que mide una sola dimensión (magnitud de la tarea que produce la disnea) y la poca sensibilidad para detectar cambios. Varios cuestionarios relacionan la disnea con la calidad de vida y algunos de ellos han establecido una correlación significativa con índices de ansiedad y depresión. Entre ellos están el SG (St George’s Respiratory Questionnaire), el CRQ (Chronic Respiratory Questionnaire y el HAD (Hospital Anxiety and Depression score). El índice de disnea basal de Mahler es una escala multidimensional que mide tres magnitudes de la disnea en un momento determinado: Grado 0 Disnea sólo con ejercicios extenuantes Grado 1 Disnea cuando camina rápido en superficie plana o sube una pendiente Grado 2 Camina más lento que los sujetos de su edad, por disnea, o tiene que detenerse para tomar aire cuando camina a su propio paso en superficie plana Grado 3 Se detiene para tomar aire después de caminar por pocos minutos en superficie plana Grado 4 Tiene demasiada disnea como para salir de la casa, vestirse o desvestirse Cuadro 3. Escala del MRC modificada - American Thoracic Society (ATS) 92 – Módulo 7 – Fascículo Nº 1 – 2011 la dificultad de la tarea, la intensidad del esfuerzo y el deterioro funcional.(51) Cada una de ellas se valora de 0 (nula) a 4 (muy intensa) y la suma total da una puntuación que oscila entre 0 y 12. Los cambios experimentados en el índice de disnea basal se miden con el índice de disnea transicional de Mahler, con un rango de entre –3 y +3 y 0 = sin cambios.(52, 53) Dentro de las mediciones directas, la escala de Borg es la que más se utiliza. Los cardiólogos la incorporaron en sus intervenciones y programas de rehabilitación, ya que es una forma directa de evaluar la disnea. Se ofrece la escala en una cartilla y debe calificarse con una nota la dificultad para respirar. Tiene la ventaja de que asocia descriptores con el valor numérico, lo que permite comparar distintos pacientes. La escala de Borg establece distintos grados de dificultad para respirar (Cuadro 4). –––––––––––––––––––––––––––––––– La escala de Borg es una forma directa de evaluar la disnea; tiene la ventaja de que asocia descriptores con el valor numérico, lo que permite comparar distintos pacientes. –––––––––––––––––––––––––––––––– La EAV es muy gráfica, pero la de Borg tiene mejor correlación entre un sujeto y otro. Es muy buena para un paciente antes y después; al mismo paciente se le pregunta qué dificultad tiene en este momento, se le pide que le ponga nota y él mismo dibuja el asterisco donde cree que está. 0Nada 1 Muy poco 2Poco 3Regular 4 Algo acentuado 5Acentuado 6 7 Muy acentuado 8 9 Muy acentuado, casi máximo 10Máximo Cuadro 4. Escala de Borg –––––––––––––––––––––––––––––––– Cuantificar la disnea con cuestionarios que midan su impacto en las actividades de la vida diaria es de vital importancia como primer paso diagnóstico. –––––––––––––––––––––––––––––––– Diagnóstico ___________ No hay una prueba diagnóstica perfecta, por lo que se requiere reflexionar en las probables implicaciones de una prueba normal o anormal. La interpretación de una prueba depende de sus características operativas (sensibilidad, especificidad) y de la probabilidad de enfermedad antes de la realización del estudio. Así, la probabilidad preprueba es la probabilidad de tener una patología por el hecho de pertenecer a una población (se estima con la prevalencia) y la probabilidad posprueba es la probabilidad de estar enfermo dado que pertenece a una población y además tiene un resultado de un método de diagnóstico. –––––––––––––––––––––––––––––––– No hay una prueba diagnóstica perfecta, por lo que se requiere reflexionar en las probables implicaciones de una prueba normal o anormal. Es recomendable utilizar algoritmos que se hayan mostrado eficientes. –––––––––––––––––––––––––––––––– Es recomendable la utilización de algoritmos diagnósticos que hayan mostrado eficacia y eficiencia (Figura 3). La utilización de algoritmos se basa en la existencia de un amplio rango de diagnósticos que abarcan la misma sintomatología y en el hecho de que enfocar el problema desde una subespecialidad suele ser menos eficiente que desde una perspectiva multidisciplinaria. Se suele reaccionar ante el resultado de un dato positivo indicando la realización de una prueba con alto costo o riesgo importante o el inicio de una terapia. La falta de “patrones oro” (gold standards) de diagnóstico en la mayoría de los casos obliga a realizar un seguimiento de la terapéutica empleada que permita identificar el método más útil. Debemos contestar dos preguntas claves: la primera es si la nueva información solicitada aumentará o disminuirá la chance de confirmar la hipótesis diagnóstica. La segunda es en qué 93 Disnea: aspectos fisiopatológicos y aproximación diagnóstica magnitud la cambiará. Esa información la provee la relación entre dos chances [coeficientes de probabilidad o likelihood ratio (LR)]. Estas relaciones van de 0 a infinito. Relaciones superiores a 1 indican aumento en la probabilidad de tener la enfermedad y las inferiores a 1 alejan la probabilidad de padecerla. Una relación de 1 implica que el resultado no provee información diagnóstica. En el Cuadro 5 se indican los LR de distintas maniobras del examen físico. Para mejorar la aplicación de los coeficientes de probabilidad a la práctica diaria sugerimos la regla de los cambios de la probabilidad después de la prueba. Para coeficientes de probabilidad de 2 o de 0,5, la probabilidad posprueba cambia el 15%, para coeficientes de 5 o de 0,2 el cambio será del 30% y finalmente para coeficientes de 10 o de 0,1 el cambio será del 45%. Así, si su preprueba para insuficiencia cardíaca es del 40% y en el examen físico encuentra el choque de punta desplazado hacia la izquierda de la línea hemiclavicular, signo que tiene una sensibilidad del 24-66% y una especificidad del 93-98% con un coeficiente de probabilidad positivo de 10,1, su probabilidad posprueba será del 85%, el cual, para su criterio clínico, podría llegar a ser el umbral terapéutico sin necesidad de realizar ninguna otra prueba diagnóstica. El primer paso en la evaluación es el examen del órgano o sistema comprometido: respiratorio, cardiovascular o ambos o ninguno, teniendo en Cuadro 5. Coeficientes de probabilidad o likelihood ratio (LR) de distintos parámetros para el diagnóstico de las causas de disnea cuenta que en hasta el 25% de los casos el origen puede ser multifactorial.(54) Con la historia clínica y el primer nivel de estudios solamente se puede orientar el diagnóstico en hasta el 80% de los pacientes y los diagnósticos más frecuentes son EPOC, ICC, enfermedad pulmonar parenquimatosa, desacondicionamiento y condiciones psicógenas.(5, 55, 56) Si en este punto hay una aproximación diagnóstica, se puede indicar tratamiento y en el caso de que la disnea remita se considera confirmatorio. Si los resultados del primer nivel de estudios no son orientadores, se continúa con el nivel 2, salvo que luego de realizados los estudios de primer nivel se requiera confirmar el diagnóstico con otros de mayor complejidad pertenecientes al tercer nivel. En esos casos se puede omitir la realización de la prueba de ejercicio cardiopulmonar (PECP). En el caso de llegar a la PECP, si confirma un diagnóstico y no se sospecha ninguna otra causa, no es necesario seguir avanzando; en caso contrario puede ser orientadora para estudios más específicos del nivel 3(57) (Figura 2). Evaluación clínica Según la GOLD (Global Initiative for Chronic Obstructive Lung Disease), la presencia de tos crónica con expectoración, disnea progresiva y persistente que se exacerba con infecciones respiratorias y la exposición a factores de riesgo (tabaquismo y polvo ambiental u ocupacional) Hallazgos de la historia clínica para el diagnóstico de causas de disnea(51-53) VPP VPN Tabaquismo 0,20 1,0 Sibilancias Historia previa de EPOC 0,45 LR (IC 95%) Prevalencia (%) 8 EPOC (14) 15 EPOC (14) 0,95 EPOC (14) Tos 0,42 0,81 Impresión clínica de EPOC moderada 9,9 (5,3-18) a grave EPOC (14) Historia previa de asma 0,48 0,76 Asma (29) Sibilancias 0,42 0,83 Asma (29) Disnea con ejercicio 0,52 1,0 1,3 (1,0-1,6) ICC (46) Ortopnea 0,63 0,72 2,2 (1,2-3,9) ICC (46) Disnea nocturna 0,62 0,63 1,9 (1,5-4,5) ICC (46) Edemas periféricos 0,58 0,60 2,3 (1,5-3,7) ICC (46) Historia previa de ICC 5,8 (4,1-8) Impresión clínica global de ICC 4,4 (1,8-10) 94 – Módulo 7 – Fascículo Nº 1 – 2011 son indicadores para considerar el diagnóstico de EPOC. La disnea en el ejercicio suele ser un síntoma precoz de ICC, aunque la disnea paroxística nocturna tiene mayor especificidad. Los hallazgos semiológicos más útiles para orientar a un diagnóstico probable en pacientes con disnea se encuentran detallados en el Cuadro 5. Dadas las prevalencias elevadas de los dos primeros diagnósticos (20% y 30%, respectivamente), la presencia de estos hallazgos incrementa su probabilidad hasta un valor cercano al 80%. Debido a que el examen físico para el diagnóstico de asma contribuye poco excepto en una crisis en el momento de la consulta, es de valor la historia de un patrón episódico de síntomas asociado con factores precipitantes. El diagnóstico se puede confirmar con la espirometría o excluir con prueba de broncoprovocación. En la mayoría de los pacientes con enfermedad parenquimatosa pulmonar difusa, la disnea con el ejercicio es un síntoma presente pero no específico. Los indicadores más útiles para el diagnóstico son la presencia de tos seca, estertores inspiratorios (audibles en el 80% de los pacientes) que no se modifican con la tos y opacidades reticulares en la radiografía de tórax asociadas con un patrón restrictivo. El clubbing (dedos en palillo de tambor o en maza) está presente en hasta un 50% de los pacientes con fibrosis pulmonar idiopática.(58) Con una capacidad vital inferior al 50% del teórico se pueden hallar signos de hipertensión pulmonar Fig. 2. Niveles de estudios. HC: Historia clínica. EF: Examen físico. Lab: Laboratorio. Hb: Hemoglobina. GSA: Gases en sangre arterial.TSH: Hormona tirotrófica estimulante. EFR: Examen funcional respiratorio. D l CO: Difusión pulmonar de monóxido de carbono. RxTx: Radiografía de tórax. ECG: Electrocardiograma. PECP: Prueba de esfuerzo cardiopulmonar. TAC: Tomografía axial computarizada. FBC: Fibrobroncoscopia. FEDA: Fibroendoscopia digestiva alta. VATS: Videotoracoscopia asistida. (HTP) secundaria, como aumento del segundo ruido y regurgitación tricuspídea. Examen físico Hallazgos clínicos que sugieren insuficiencia cardíaca La ICC es un síndrome que se caracteriza por deterioro de la función ventricular, presiones de llenado ventricular elevadas y disminución de la capacidad de ejercicio. Puede haber disminución de la fracción de eyección (disfunción sistólica) o fracción de eyección conservada (disfunción diastólica). La detección de presiones de llenado ventricular elevadas puede tener un alto grado de predicción clínica con el examen físico (Figura 3). Los hallazgos que más aportan al diagnóstico son: prueba abdominoyugular positiva (CP+ de 8), respuesta anormal a la maniobra de Valsalva (fase 4 ausente o respuesta en meseta) con un CP+ de 7,6, desplazamiento del latido apexiano (CP+ de 5,8), tercer ruido (CP+ de 5,7), taquicardia (CP+ de 5,5), presión venosa central elevada (CP+ de 3,9). Estos hallazgos son extremadamente útiles cuando son positivos, pero aportan poca información clínica cuando son negativos excepto en el caso de la maniobra de Valsalva y el reflejo abdominoyugular, cuyos valores negativos de 0,1 y 0,3, respectivamente, cambian la probabilidad posprueba en 45% y entre 15% y 30%. Estos signos son similares en cuanto a su coeficiente de probabilidad, así se trate de ICC por déficit de eyección o por aumento de presiones de llenado. 95 Disnea: aspectos fisiopatológicos y aproximación diagnóstica Fig. 3. Cambios de la probabilidad preprueba producidos en el examen físico para el diagnóstico de ICC. CP: Coeficiente de probabilidad. –––––––––––––––––––––––––––––––– Una prueba abdominoyugular positiva, la fase 4 de la maniobra de Valsalva ausente o en meseta, el desplazamiento del latido apexiano, el tercer ruido, la taquicardia y la PVC elevada aumentan la probabilidad de ICC, mientras que la respuesta normal a la maniobra de Valsalva y la prueba abdominoyugular negativa alejan la probabilidad de ICC. –––––––––––––––––––––––––––––––– Hemitórax Región del tórax Derecho Porción anterior y superior del tórax Área medioaxilar Base pulmonar Puntaje (1 a 4) Izquierdo Porción anterior y superior del tórax Área medioaxilar Base pulmonar Hallazgos clínicos que sugieren enfermedad pulmonar obstructiva crónica En el examen físico, algunos datos permiten sospechar EPOC. La longitud desde el cartílago cricoides hasta el mango esternal menor de 4 cm tiene en caso de que sea positivo un CP+ de 3,6, así como el signo de Hoover tiene un CP+ de 4,2. El único dato palpatorio es el latido cardíaco subxifoideo con un CP+ de 7,4. La hipersonoridad tiene un CP+ de 5,4 y la disminución de los ruidos cardíacos en la auscultación, un CP+ de 11,4. Los sonidos normales que se auscultan en el pulmón son el murmullo vesicular (MV) y las vibraciones vocales. De ellos, características importantes son la temporalidad y la intensidad. Con respecto a esta última, es proporcional al flujo de aire en la boca, el cual a su vez depende del esfuerzo y de la capacidad ventilatoria. Pardee desarrolló un sistema de puntaje de acuerdo con la intensidad del MV en seis áreas distintas del tórax (porción anterior y superior del tórax, área medioaxilar y ambas bases). El puntaje es de cero si se encuentra ausente, 1 difícilmente audible, 2 leve, 3 normal y 4 sonidos más fuertes que los normales (Cuadro 6). El rango es de 0 a 24. Si el paciente tiene < 9, el Cuadro 6. Puntaje de Pardee para el diagnóstico de EPOC CP+ es de 10,1 para el diagnóstico de EPOC y si es > 16, el CP– es de 0,1 para el mismo diagnóstico. La auscultación de estertores al inicio de la inspiración aumenta la probabilidad de tener EPOC con un CP+ de 14,6. La mayoría de los hallazgos del examen físico resultan de la hiperinsuflación torácica y del aumento del trabajo para espirar. Sólo dos signos en caso de que sean negativos disminuyen la probabilidad preprueba de la enfermedad: a) un puntaje de intensidad del MV > 16 (CP– de 0,1) y b) una capacidad ventilatoria forzada < 3 segundos (CP– de 0,2) (Figura 4). La longitud desde el cartílago cricoides hasta el mango esternal menor de 4 cm, el signo de Hoover, el latido cardíaco subxifoideo, la hipersonoridad, la disminución de los ruidos cardíacos y los estertores al inicio de la inspiración en la auscultación aumentan la probabilidad de EPOC. –––––––––––––––––––––––––––––––– Un puntaje de Pardee < 9 aumenta la probabilidad de EPOC, mientras que un puntaje > 16 la disminuye. –––––––––––––––––––––––––––––––– 96 – Módulo 7 – Fascículo Nº 1 – 2011 Fig. 4. Cambios de la probabilidad preprueba producidos en el examen físico para el diagnóstico de EPOC. CP: Coeficiente de probabilidad. Estudios diagnósticos La espirometría [examen funcional respiratorio (EFR)] es un estudio útil para el diagnóstico de enfermedad obstructiva. Un VEF1/CVF < 0,7 es criterio de obstrucción y la gravedad se cuantifica con el porcentaje de caída del VEF1 respecto del teórico. Puede ser reversible (respuesta a broncodilatadores positiva) o no reversible y progresiva, lo cual apunta al diagnóstico de EPOC.(55) Una enfermedad obstructiva con una difusión de monóxido disminuida aproxima el diagnóstico final hacia enfisema pulmonar, cuya confirmación se realiza con una tomografía computarizada de alta resolución. La radiografía de tórax es útil para orientar hacia enfermedad parenquimatosa pulmonar y patología pleural y de la caja torácica.(55) Para el diagnóstico de síndromes restrictivos, el patrón oro es el estudio de volúmenes pulmonares y el diagnóstico se justifica con una capacidad pulmonar total disminuida. Si ésta se asocia con aumento del volumen residual y de su relación con la capacidad pulmonar total, la orientación es hacia una enfermedad neuromuscular. En este último caso son útiles las presiones bucales (inspiratoria y espiratoria máxima) que pueden encontrarse disminuidas y si la restricción se asocia con difusión de monóxido disminuida, la orientación es hacia una enfermedad parenquimatosa, lo cual justifica una tomografía computarizada de alta resolución. Para el diagnóstico de enfermedad vascular pulmonar, el ecocardiograma con Doppler es de utilidad, ya que permite estimar la presión en la arteria pulmonar ante la presencia de regurgita- ción tricuspídea. Si se sospecha tromboembolia pulmonar (TEP), el centellograma V/Q, el eco Doppler de miembros inferiores, la angio-TAC o la arteriografía permiten aproximar y/o certificar el diagnóstico. El ecocardiograma bidimensional es de utilidad en el diagnóstico de ICC; sin embargo, hasta el 40% de los pacientes con evidencia clínica de ICC tienen disfunción diastólica con función sistólica preservada. En esos casos, el diagnóstico lo sugiere el hallazgo de hipertrofia ventricular izquierda, dilatación de la aurícula izquierda y reversión del patrón normal de velocidad de flujo a través de la válvula mitral. El BNP (péptido natriurético cerebral o péptido natriurético tipo B) es una neurohormona sintetizada por los miocitos ventriculares. Se libera ante la sobrecarga de presión/volumen telediastólica, lo que aumenta el estrés parietal. La magnitud de la elevación es proporcional a la gravedad de la falla cardíaca y se correlaciona con el pronóstico.(59, 60) Con un BNP > 150 pg/ml, la probabilidad de que un paciente con disnea tenga ICC es superior al 77% con un LR positivo de 5 (4,3-5,8).(61-63) En la radiografía de tórax, la presencia de congestión venosa pulmonar (distensión de las venas pulmonares y redistribución de flujo a los ápices) se asoció con un LR positivo de 12 (6,8-21), el hallazgo de cardiomegalia con un LR de 3,3 (2,4-4,7), el edema intersticial con un LR de 12 (5,2-27) y la presencia de derrame pleural con un LR de 4,6 (2,4-8,7). En el ECG, el hallazgo de FA en un paciente con disnea se asoció con un LR de 3,8 (1,7-8,8).(64) Disnea: aspectos fisiopatológicos y aproximación diagnóstica En algunos pacientes con enfermedad coronaria, la disnea puede representar un equivalente anginoso y debe evaluarse con los métodos diagnósticos menos invasivos hasta el cateterismo cardíaco. Prueba de ejercicio cardiopulmonar La intolerancia al ejercicio es el resultado del desequilibrio en uno o más componentes del transporte de oxígeno y se manifiesta con fatiga muscular, disnea, dolor en las extremidades o angina. La disnea de ejercicio es un problema común a muchas enfermedades, casi siempre debida a uno de los siguientes factores: hipoventilación, alteración hemodinámica, factores hematológicos, alteraciones en la difusión o desequilibrio de la relación ventilación/perfusión.(65) La PECP evalúa aspectos dinámicos de la fisiología cardiorrespiratoria; en contraste, las pruebas funcionales estáticas no reproducen la condición activa de un individuo. La capacidad de efectuar trabajo aeróbico requiere la integración respiratoria, hematológica, cardiovascular y muscular. La posibilidad de evaluar el consumo de oxígeno pico (VO2máx) aporta información diagnóstica y pronóstica en una amplia variedad de situaciones clínicas. –––––––––––––––––––––––––––––––– La capacidad de efectuar trabajo aeróbico requiere la integración respiratoria, hematológica, cardiovascular y muscular. –––––––––––––––––––––––––––––––– Las bases fisiológicas de la disnea han sido un tema ampliamente discutido en la literatura médica.(66, 67) La capacidad para el ejercicio puede caracterizarse según el consumo máximo de oxígeno (VO2 pico) y cualquier limitación puede categorizarse como respiratoria o circulatoria.(65) Un VO2/kg disminuido con un VO2 pico normal sin disfunción cardiorrespiratoria (estudios del nivel 1 normales) es orientador de disnea asociada con obesidad.(65, 70) Una PECP y pruebas de nivel 1 normales serían consistentes con disnea psicógena. Una PECP con VO2 pico disminuido en pacientes con escasa actividad son sugestivos de desacondicionamiento. En un trabajo se analizó específicamente la prueba de esfuerzo cardiopulmonar en la evaluación 97 de la disnea crónica de origen desconocido.(68) Fernández de Rota García y cols. analizaron el espectro y la frecuencia de causas de disnea crónica de origen desconocido mediante la realización de la prueba de esfuerzo cardiopulmonar en 178 pacientes (92 hombres; edad media 42,5 ± 16,7 años) que cumplieran con los siguientes criterios de inclusión: – disnea de más de un mes de evolución relacionada o no con el esfuerzo; – historia clínica, exploración física, laboratorio básico, radiografía de tórax, ECG, oximetría y gases en sangre arterial normales; – espirometría forzada normal; – prueba de broncodilatación negativa; – carecer de limitaciones físicas para realizar una prueba de ejercicio; – aceptar la realización de la prueba y firmar el consentimiento informado.(69) Por orden de frecuencia, los diagnósticos fueron: normal o disnea psicógena (71,9%), hiperreactividad bronquial (8,4%), limitación ventilatoria (6,7%), sobrepeso y sedentarismo (3,9%), crisis de hipertensión arterial (HTA) (3,9%), limitación cardiocirculatoria (3,4%) y alteración vascular pulmonar (1,7%). El diagnóstico de normalidad o de disnea de origen psicógeno, indistinguibles desde el punto de vista de la PECP, podría traducir el hecho de que es probable que estos pacientes con disnea psicógena no sean bien manejados desde la consulta, ya que una mejor historia insistiendo en los síntomas acompañantes (hiperventilación, ansiedad, adormecimiento de manos y cara, etc.) permitiría sospechar el diagnóstico y adoptar actitudes terapéuticas sin necesidad de otras pruebas. El segundo diagnóstico más frecuente fue hiperreactividad bronquial (8,4%). Esto pone de manifiesto la utilidad de la PECP como prueba de broncoprovocación en caso de que no se disponga de metacolina o histamina. Suele tratarse de pacientes con disnea casi siempre relacionada con el esfuerzo y que aunque por su historia se sospecha asma inducida por el ejercicio, no puede demostrarse con las pruebas de rutina. Pratter y cols. describieron su experiencia con pacientes de una consulta de Neumonología con disnea crónica, a los que no se les había realizado 98 ninguna prueba con anterioridad, por lo que al aplicar su protocolo diagnóstico sólo le realizaron la PECP al 18%, y concluyeron que su principal utilidad era para el diagnóstico de la disnea psicógena y la debida a la falta de entrenamiento.(55) De Paso y cols. informaron su experiencia con 72 sujetos con disnea no explicada mediante la historia, la exploración, la radiografía de tórax y la espirometría.(5) Utilizaron una gran cantidad de pruebas complementarias para llegar al diagnóstico, pero sólo solicitaron 15 PECP, de las cuales 11 resultaron normales (73,3%) y 4 patológicas y de éstas, 2 sirvieron para llegar al diagnóstico final y las otras 2 orientaron la evaluación posterior. Pese al escaso número, los resultados fueron similares a los de los estudios comentados previamente. Martínez y cols. evaluaron la utilidad de la PECP en el diagnóstico de la disnea de origen desconocido mediante la realización de la prueba a 50 pacientes en los que las pruebas iniciales eran normales o poco concluyentes.(68) El diagnóstico más frecuente fue el de sedentarismo o falta de entrenamiento en casi el 50% de los casos. El grupo de normales o con disnea psicógena representó el 26%, con trastornos cardiocirculatorios el 8%, con trastornos respiratorios el 10% y con alteraciones vasculares pulmonares el 2%. Uno de los principales problemas que refirieron fue la dificultad para distinguir entre algunos pacientes con patología cardíaca y aquellos con falta de entrenamiento, quedando finalmente todos integrados en este último grupo. Esto se debió a que en la mitad de los pacientes no monitorizaron el registro electrocardiográfico durante el esfuerzo, lo que les impidió encontrar cambios isquémicos típicos. – Módulo 7 – Fascículo Nº 1 – 2011 En los grupos comprendidos entre los 40 y los 59 años, el más numeroso, el 50% de los diagnósticos son normales o disnea psicógena y, a excepción de la hiperreactividad bronquial (más frecuente en menores de 40 años), es en este grupo donde se observan con mayor frecuencia los otros diagnósticos: procesos obstructivos, restrictivos, trastornos cardiocirculatorios, alteraciones vasculares pulmonares, HTA y sobrepeso. En el grupo de pacientes mayores, estos trastornos se diagnostican con menos frecuencia. En la mayoría de los estudios, una PECP normal permitió excluir la existencia de enfermedad significativa, lo cual hace que esto sea su mayor utilidad. En los pacientes en los que el resultado es patológico puede ser necesaria la realización de nuevas pruebas que confirmen este diagnóstico. –––––––––––––––––––––––––––––––– En la mayoría de los estudios, una PECP normal permitió excluir la existencia de enfermedad significativa, lo cual hace que esto sea su mayor utilidad. –––––––––––––––––––––––––––––––– La PECP, al orientar el diagnóstico, permite una selección más precisa de los estudios posteriores y, asimismo, es una prueba que se tolera bien y con buena reproducibilidad. La utilidad de esta prueba se pone de manifiesto en las primeras etapas del estudio de la disnea de origen poco claro, luego de una evaluación correcta, que incluya historia clínica, examen físico, radiografía de tórax, ECG, pruebas de laboratorio y pruebas funcionales respiratorias básicas.(57) Fuerza de las recomendaciones (evidencia C, consenso de expertos) Recomendación clínica El examen físico es útil en diferenciar etiologías de disnea con una precisión aproximada de 70%(71) Las respuestas positivas a la maniobra de Valsalva y el reflujo abdominoyugular son útiles para identificar disnea de origen cardíaco(71) En la evaluación inicial considerar los siguientes estudios en función de la anamnesis y el examen clínico: laboratorio, prueba de la función pulmonar, radiografía de tórax(6, 72) Si se sospecha HTP, el ecocardiograma es el estudio inicial de mayor utilidad(73) Si se sospecha ICC, deben solicitarse BNP y ecocardiograma(59, 61) La PECP debe considerarse ante disnea sin causa aparente luego del primer escalón diagnóstico(7) La TC de alta resolución/helicoidal es útil ante sospecha de enfermedad parenquimatosa pulmonar, enfisema o bronquiectasias/TEP(74) Disnea: aspectos fisiopatológicos y aproximación diagnóstica –––––––––––––––––––––––––––––––– – Primero: evaluación correcta, que incluya historia clínica, examen físico, radiografía de tórax, ECG, laboratorio y pruebas funcionales respiratorias básicas. – Segundo: PECP cuando el origen de la disnea queda poco claro, luego de lo anterior. –––––––––––––––––––––––––––––––– Referencias ___________ (La bibliografía en negrita es la que los autores destacan como lectura complementaria al texto. Se encuentra a su disposición en nuestra biblioteca o a través de www.sac. org.ar [tres sin cargo]). 1. Desbiens N, et al. The relationship of nausea and dyspnea to pain in seriously ill patients. Pain 1997;71:149-56. 2. Kroenke K, Arrington M, Mangelsdorff A. The prevalence of symptoms in medical outpatients and the adequacy of therapy. Arch Intern Med 1990;150:1685-9. 3. American Thoracic Society. Dyspnea. Mechanisms, assessments, and management: a consensus statement. Am J Respir Crit Care 1999;159:321-40. 4. Morgan W, Hodge H. Diagnostic evaluation of dyspnea. Am Fam Physician 1998;57:711-6. 5. De Paso W, et al. Chronic dyspnea unexplained by history, physical examination, chest roentgenogram, and spirometry. Analysis of sevenyear experience. Chest 1991;100:1293-9. 6. Gillespie D, Staats B. Unexplained dyspnea. Mayo Clin Proc 1994;69:657-63. 7. American Thoracic Society, ATS/ACCP Statement on cardiopulmonary exercise testing. Am J Respir Crit Care 2003;167:211-77. 8. Gracely R, Undem B, Banzett R. Cough, pain and dyspnoea: similarities and differences. Pulm Pharmacol Ther 2007;20(4). 9. Lansing R, Gracely R, Banzett R. The multiple dimensions of dyspnea: review and hypotheses. Respir Physiol Neurobiol 2009;167(1):53-60. 10. Tobin M. Dyspnea. Arch Intern Med 1990; 150:1604-13. 11. Campbell E, Guz A. Breathlessness. En: Hornbein TF, editor. Regulation of breathing. Part 2. Vol 17 of Lung biology in health and disease. New York: Marcel Dekker; 1981. p. 1181-95. 12. Elliott M, et al. The language of breathlessness: use of verbal descriptors by patients with cardiopulmonary disease. Am Rev Respir Dis 1991;144:826-32. 13. Mc Closkey D. Corollary discharges: motor commands and perception. En: Brookhart JM, Mountcastle VB, editors. Section 1: The Nervous System. Vol 2. Part 2 99 of Handbook of physiology. Bethesda, Md: American Physiological Society; 1981. p. 1415-47. 14. O’Connell J, Campbell A. Respiratory mechanics in airways obstruction associated with inspiratory dyspnoea. Thorax 1976;31:669-77. 15. Killian K, et al. Effect of increased lung volume on perception of breathlessness, effort, and tension. J Appl Physiol 1984;57:686-91. 16. Schwartzstein R, et al. Breathlessness induced by dissociation between ventilation and chemical drive. Am Rev Respir Dis 1989;139:1231-7. 17. Demediuk B, Manning H, Lilly J. Dissociation between dyspnea and respiratory effort. Am Rev Respir Dis 1992;146:1222-5. 18. Burki N. Breathlessness and mouth occlusion pressure in patients with chronic obstruction of the airways. Chest 1979;76(5):527-31. 19. Burki N. Dyspnea. Clin Chest Med 1980;1(1):47-55. 20. Buchanan G, Richerson G. Role of chemoreceptors in mediating dyspnea. Respir Physiol Neurobiol 2009;167(1):9-19. 21. Burki N, Lee L-Y. Mechanisms of dyspnea. Chest 2010;138(5):1196-201. 22. Banzett R, et al. ‘Air hunger’ arising from increased PCO2 in mechanically ventilated quadriplegics. Respir Physiol 1989;76:53-67. 23. Schwartzstein R, et al. Cold facial stimulation reduces breathlessness induced in normal subjects. Am Rev Respir Dis 1987;136:58-61. 24. Simon P, et al. Oral mucosal stimulation modulates intensity of breathlessness induced in normal subjects. Am Rev Respir Dis 1991;144:419-22. 25. Chaudhary B, Burki N. Effects of airway anesthesia on the ability to detect added inspiratory resistive loads. Clin Sci Mol Med 1978;44:621-26. 26. Chaudhary B, Burki N. The effects of airway anesthesia on detection of added inspiratory elastic loads. Am Rev Respir Dis 1980;122:635-9. 27. Burki N, et al. The effects of airway anesthesia on magnitude estimation of added inspiratory resistive and elastic loads. Am Rev Respir Dis 1983;127:2-4. 28. O’Donnell D, et al. Effect of dynamic airway compression on breathing pattern and respiratory sensation in severe chronic obstructive pulmonary disease. Am Rev Respir Dis 1987;135:912-8. 29. Guz A, et al. Experimental results of vagal block in cardiopulmonary disease. En: Porter R, editor. Breathing: Hering-Breuer Centenary Symposium. London: J & A Churchill; 1970. p. 315-29. 30. Murray J. The normal lung. 2nd ed. Philadelphia: WB Saunders; 1986. p. 69-80. 31. Campbell E, Howell J. The sensation of breathlessness. Br Med Bull 1963;19:36-40. 32. Manning H, Molinary E, Leiter J. Effect of inspiratory flow rate on respiratory sensation and pattern of breathing. Am J Respir Crit Care Med 1995;151:751-7. 100 33. Killian K, Jones N. Respiratory muscles and dyspnea. Clin Chest Med 1998;9:237-48. 34. Bellemare F, Grassino A. Effect of pressure and timing of contraction on human diaphragmatic fatigue. J Appl Physiol 1982;53:1190. 35. Bellemare F, Grassino A. Effect of pressure and timing of contraction on human diafragmatic fatigue during weaning from mechanical ventilation. Am Rev Respir Dis 1989;139:513-21. 36. De Vito E, Roncoroni A. Fatiga diafragmática en el shock hipovolémico. Medicina (Buenos Aires) 1990;50:35-42. 37. D’Negri C, Pessolano F, De Vito E. Variabilidad del patrón respiratorio durante la carga elástica inspiratoria. Medicina (Buenos Aires) 2009;69:311-17. 38. Manning H, Schwartzstein R. Pathophysiology of Dyspnea. N Engl J Med 1995;333(23):1547-53. 39. Burki N. Effects of bronchodilation on magnitude estimation of added resistive loads in asthmatic subjects. Am Rev Respir Dis 1984;129:225-9. 40. Hudgel D, Cooperson D, Kinsman R. Recognition of added resistive loads in asthma. Am Rev Respir Dis 1982;126:121-5. 41. Gottfried S, et al. Perception of changes in airflow resistance in obstructive pulmonary disorders. Am Rev Respir Dis 1981;124:566-70. 42. Burns B, Howell J. Disproportionately severe breathlessness in chronic bronchitis. Q J Med 1969;38:277-94. 43. Bass C, Gardner W. Respiratory and psychiatric abnormalities in chronic symptomatic hyperventilation. BMJ 1985;290:1387-90. 44. Bass C, Gardner W. Emotional influences on breathing and breathlessness. J Psychosom Res 1985;29:599-609. 45. Dudley D, Pitts-Poarch A. Psychophysiologic aspects of respiratory control. Clin Chest Med 1980;1:131-43. 46. Tobin M, Perez W, Guenther S. Breathing pattern and metabolic behavior during anticipation of exercise. J Appl Physiol 1986;60:1306-12. 47. Garssen B. Role of stress in the development of the hyperventilation syndrome. Psychother Psychosom 1980;33:214-25. 48. Brashear R. Hyperventilation syndrome. Lung 1983;161:257-73. 49. Magarian G. Hyperventilation syndromes: infrequently recognized common expressions of anxiety and stress. Medicine 1982;61:219-36. 50. Bass C, et al. Unexplained breathlessness and psychiatric morbidity in patients with normal and abnormal coronary arteries. Lancet 1983;1:605-9. 51. Mahler D, et al. The measurement of dyspnea: contents, interobserver agreement and physiologic correlates of two new clinical indexes. Chest 1984;85:751-8. 52. Mahler D, et al. Comparison of clinical dyspnea ratings and psychological measurements of respiratory – Módulo 7 – Fascículo Nº 1 – 2011 sensation in obstructive pulmonary disease. Am Rev Respir Dis 1987;135:1229-33. 53. Witek T, Mahler D. Minimal important difference of the transition dyspnoea index in a multinational clinical trial. Eur Respir J 2003;21:267-72. 54. Michelson E, Hollrah S. Evaluation of the patient with shortness of breath: an evidence based approach. Emerg Med Clin North Am 1999;17:221-37. 55. Pratter M, et al. Cause and evaluation of chronic dyspnea in a pulmonary disease clinic. Arch Intern Med 1989;149:2277-82. 56. Stein J. Internal Medicine. 5th ed. St Louis: Mosby; 1998. p. 401-6. 57. Pratter M, et al. An algorithmic approach to chronic dyspnea. Respiratory Medicine 2011;105:1014-1021. 58. American Thoracic Society. Idiopathic pulmonary fibrosis: diagnosis and treatment. International consensus statement. American Thoracic Society (ATS), and the European Respiratory Society (ERS). Am J Respir Crit Care Med 2000;161(2 pt 1):646-64. 59. Wieczorek S, et al. A rapid B-type natriuretic peptide assay accurately diagnoses left ventricular dysfunction and heart failure: a multicenter evaluation. Am Heart J 2002;144:834-9. 60. Harrison A, et al. B-type natriuretic peptide predicts future cardiac events in patients presenting to the emergency department with dyspnea. Ann Emerg Med 2002;39(2):131-8. 61. Maisel A, et al. Breathing Not Properly Multinational Study Investigators. Bedside B-type natriuretic peptide in the emergency diagnosis of heart failure with reduced or preserved ejection fraction. Results from the Breathing Not Properly Multinational Study. J Am Coll Cardiol 2003;41:2010-7. 62. Morrison L, et al. Utility of a rapid B-natriuretic peptide assay in differentiating congestive heart failure from lung disease in patients presenting with dyspnea. J Am Coll Cardiol 2002;39:202-9. 63. Hohl C, et al. Should emergency physicians use B-type natriuretic peptide testing in patients with uexplained dyspnea? Can J Emerg Med 2003;5(3):162-5. 64. Wang C, et al. Does this dyspneic patient in the emergency department have congestive heart failure? JAMA 2005;294(15):1944-56. 65. Wasserman K, Hansen J, Sue D. Principles of exercise testing and interpretation. 3 rd ed. Philadelphia: Lippincott Williams & Wilkins; 1999. p. 198-200. 66. Wright G, Branscomb B. Origin of the sensations of dyspnea. Trans Am Clin Climatol Assoc; 1966. p. 116-25. 67. Wasserman K, Casaburi R. Dyspnea: physiological Disnea: aspectos fisiopatológicos y aproximación diagnóstica and pathophysiological mechanisms. Am Rev Med 1988;39:503-15. 68. Martínez F, et al. Graded comprehensive cardiopulmonary exercise testing in the evaluation of dyspnea unexplained by routine evaluation. Chest 1994;105:168-74. 69. Fernández de Rota García B, et al. Papel de la prueba de esfuerzo cardiopulmonar en el diagnóstico de la disnea crónica de origen desconocido. Neumosur 2007;19(2):65-72. 70. Babb T, et al. Dyspnea on exertion in obese women: association with an increased oxygen cost of breathing. Am J Respir Crit Care Med 2008;178(2):116-23. 101 71. Mulrow C, Lucey C, Farnett L. Discriminating causes of dyspnea through clinical examination. Journal of General Internal Medicine 1993;8(7):383-92. 72. Swanney M, et al. FEV(6) is an acceptable surrogate for FVC in the spirometric diagnosis of airway obstruction and restriction. Am J Respir Crit Care Med 2000;162(3 (1)):917-9. 73. Nauser T, Stites S. Diagnosis and treatment of pulmonary hypertension. Am Fam Physician 2001; 63:1789-98. 74. Hunninghake G, et al. Radiologic findings are strongly associated with a pathologic diagnosis of usual interstitial pneumonia. Chest 2003;124:1215-23.