Fernando Armé star a,*, Alejandro Olivé Jordi Serra c y Napoleó n
Anuncio

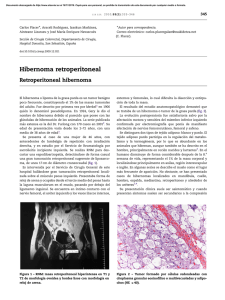
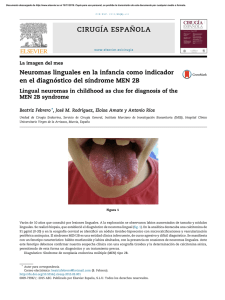
Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. 328 Cartas cientı´ficas / Med Clin (Barc). 2014;142(7):327–329 5. Langston JD, Wagman GF, Dickenman RC. Granulomatous myocarditis and myositis associated with thymoma. J Neurol Sci. 1973;18:1–9. Fernando Arméstara,*, Alejandro Olivéb, Jordi Serrac y Napoleón de la Ossad a Servicio de Medicina Intensiva, Hospital Universitari Germans Trias i Pujol, Badalona, Barcelona, España b Servicio de Reumatologı́a, Hospital Universitari Germans Trias i Pujol, Badalona, Barcelona, España c Servicio de Cardiologı´a, Hospital Universitari Germans Trias i Pujol, Badalona, Barcelona, España d Servicio de Anatomı´a Patológica, Hospital Universitari Germans Trias i Pujol, Badalona, Barcelona, España * Autor para correspondencia. Correo electrónico: [email protected] (F. Arméstar). http://dx.doi.org/10.1016/j.medcli.2013.04.003 Miocarditis de células gigantes fulminante Fulminant giant cell myocarditis Sr. Editor: La miocarditis de células gigantes (MCG) es una enfermedad rara, poco frecuente, de difı́cil diagnóstico y con una evolución rápida y grave1. Presentamos el caso de una mujer de 43 años con historia de hipotiroidismo primario en tratamiento sustitutivo y rinitis alérgica desde hace años. Consultó por astenia y deterioro progresivo de su grado funcional hasta hacerse III/IV de la New York Heart Association, de tres semanas de evolución. Destacaban un leve tinte ictérico y signos congestivos de predominio derecho; en el electrocardiograma, taquicardia sinusal y bloqueo de rama derecha; y en la radiolografı́a de tórax, cardiomegalia con derrame pleural bilateral. La ecocardiografı́a objetivó una dilatación y disfunción sistólica severa biventricular por hipocinesia global con insuficiencia mitral severa y tricuspı́dea moderada, ambas funcionales, y probable hipertensión pulmonar. Los estudios de laboratorio (incluidas serologı́as, proteı́na C reactiva y estudios de autoinmunidad) resultaron normales salvo importante alteración de las pruebas de función hepática. Se inició tratamiento diurético endovenoso a dosis altas más apoyo aminérgico. A pesar de una mejorı́a inicial, precisó la implantación de balón de contrapulsación intraórtico y posteriormente un sistema de asistencia biventricular por deterioro progresivo de la situación hemodinámica. Finalmente se realizó trasplante cardiaco ortotópico urgente con buena evolución clı́nica subsiguiente. El estudio histológico del órgano explantado arrojó como diagnóstico una miocarditis de células gigantes (fig. 1). Un año después del trasplante, la paciente ha permanecido asintomática y sin signos histológicos de recidiva en las biopsias endomiocárdicas (BEM) de control. La miocarditis es una enfermedad inflamatoria del miocardio, representando la MCG en torno al 1% de las miocarditis2 y siendo esta prevalencia similar en diferentes poblaciones3. La insuficiencia cardiaca es la forma más habitual de presentación (75%) pero se suele asociar con arritmias ventriculares y bloqueo auriculoventricular1. Se la ha relacionado con múltiples enfermedades autoinmunes y se la considera una miocarditis inmunomediada. Modelos experimentales murinos la han asociado con alteraciones de los linfocitos T CD4 y diversas citoquinas proinflamatorias4. El diagnóstico de certeza se realiza por estudio histológico, caracterizándose por la presencia en miocardio de un infiltrado inflamatorio compuesto por linfocitos, histiocitos, eosinófilos y células multinucleadas gigantes, con necrosis de extensión variable y sin evidencia de lesiones granulomatosas1. La baja prevalencia de la enfermedad asociado a la necesidad de la toma de muestras para el estudio histológico retrasa y dificulta el diagnóstico. Se ha desarrollado un documento de consenso con las indicaciones de BEM5, donde se considera un procedimiento seguro (0,5-1% de complicaciones graves) si se realiza por un equipo con experiencia, aunque situaciones como aumento de presiones y/o dilatación del ventrı́culo derecho o la presencia de diátesis hemorrágica, puede aumentar el porcentaje de complicaciones fatales5. El rendimiento diagnóstico muestra una baja sensibilidad (38-65%), que puede aumentarse si se realizan biopsias de forma dirigida con resonancia magnética cardiaca5, o bien repitiendo el procedimiento en varias ocasiones, llegando a alcanzarse sensibilidades de hasta el 93%6. Este teórico bajo rendimiento diagnóstico y/o la inestabilidad clı́nica de los pacientes son en ocasiones la causa de no realizar biopsias. De hecho, de los siete casos de MCG publicados en España hasta la fecha, el diagnóstico histológico fue realizado por necropsia en cinco casos y en órgano explantado en los dos restantes7. En nuestro caso, pese a las recomendaciones sobre la realización de BEM, esta no fue llevada a cabo por la precaria situación clı́nica de la paciente, siendo el estudio del órgano explantado el que facilitó el diagnóstico. En series clásicas, el 89% de los afectados fallecı́an o requerı́an trasplante cardiaco, con una mediana de supervivencia menor de seis meses desde el debut1. Sin embargo, actualmente el tratamiento inmunosupresor, principalmente ciclosporina, puede producir mejorı́a clı́nica y aumentar el tiempo hasta el trasplante cardiaco hasta en 5 años en el 52% de los pacientes6. Ası́ mismo, hay publicaciones con resultados favorables tras la utilización de Figura 1. Preparación histológica, tinción hematoxilina-eosina. 1 A) Músculo papilar cortado transvesalmente (10x). Se observa infiltrado inflamatorio difuso y células multinucleadas (flecha). 1 B) Misma preparación (40x). Infiltrado inflamatorio linfocitario (1). Células gigantes multinucleadas (2). Miocardiocitos con núcleos vacuolizados (3). Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Cartas cientı´ficas / Med Clin (Barc). 2014;142(7):327–329 anticuerpos monoclonales muromonab-CD34 o globulina antitimocı́tica8. La supervivencia postrasplante es similar a otras indicaciones, pudiendo presentar recurrencia en el injerto en un 20-25% de los casos9. En la fase aguda, los dispositivos de asistencia ventricular como estrategia puente al trasplante han mostrado resultados favorables10. Por tanto, teniendo en cuenta el aumento de sensibilidad diagnóstica de la biopsia endomiocárdica combinándola con otras técnicas de imagen o bien repitiendo la toma de muestra, la posibilidad de realizar un diagnóstico histológico precoz y el buen resultado mostrado por los regı́menes de tratamiento inmunosupresor debemos insistir en la necesidad de intentar alcanzar un diagnóstico de certeza de forma temprana ante un cuadro clı́nico compatible con miocarditis de células gigantes. Bibliografı́a 1. Cooper LT, Berry GJ, Shabetai R. Idiopathic giant cell myocarditis. Natural history and treatment. N England J Med. 1997;336:1860–6. 2. Hufnagal G, Pankuweit S, Richter A, Schonian U, Maisch B. The European Study of Epidemiology and Treatment of Cardiac Inflammatory Diseases (ESETCID). First epidemiologic results. Herz. 2000;25:279–85. 3. Vaideeswar P, Cooper LT. Giant cell myocarditis: clinical and pathological features in an Indian population. Cardiovasc Pathol. 2013;22:70–4. http://dx.doi.org/10.1016/j.medcli.2013.04.013 329 4. Suzuki J, Ogawa M, Watanabe R, Morishita R, Hirata Y, Nagai R, et al. Autoimmune giant cell myocarditis: clinical characteristics, experimental models and future treatments. Expert Opin Ther Targets. 2011;15:1163–72. 5. Cooper LT, Baughman KL, Feldman AM, Frustaci A, Jessup M, Kuhl U, et al. The role of endomyocardial biopsy in the management of cardiovascular disease. A Scientific statement from the American Heart Association, the American College of Cardiology and the European Society of Cardiology. European Heart Journal. 2007;28:3076–93. 6. Kandolin R, Lehtonen J, Salmenkivi K, Räisänen-Sokolowski A, Lommi J, Kupari M. Diagnosis Treatment, and Outcome of Giant Cell Myocarditis in the Era of Combined Immunosuppression. Circ Heart Fail. 2013;6:15–22. 7. Marquina MI, Garrido I, Avellanas ML, Escós J, Zamora M, Mallor T. Miocarditis de células gigantes de evolución fulminante. Med Intensiva. 2012;36:451–3. 8. Tayal U, Bell A, Mittal T, Banner NR. Giant cell myocarditis treated with antithymocyte globulin. Br J Hosp Med. 2011;72:474. 9. Cooper Jr LT, ElAmm C. Giant cell myocarditis. Diagnosis and treatment. Herz. 2012;37:632–6. 10. Murray LK, González-Costello J, Jonas SN, Sims DB, Morrison KA, Colombo PC, et al. Ventricular assist device support as a bridge to heart transplantation in patients with giant cell myocarditis. Eur J Heart Fail. 2012;14:312–8. Manuel Barreiro*, Alfredo Renilla, Irene Álvarez y Cecilia Corros Área del Corazón, Hospital Central de Asturias, Calle Celestino Villamil s/n, 33006, Oviedo, España * Autor para correspondencia. Correo electrónico: [email protected] (M. Barreiro).