Hematoma neuroaxial tras anestesia locorregional combinada
Anuncio

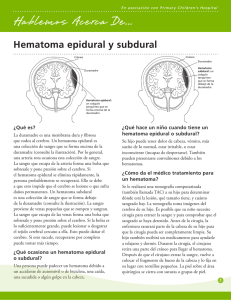
(Rev. Esp. Anestesiol. Reanim. 2005; 52: 433-437) CASO CLÍNICO Hematoma neuroaxial tras anestesia locorregional combinada resuelto de forma conservadora S. Martín*,a, A. Smaranda*,a, J. Archilla*,a, J. Gómez de Orellana*,a, F. Ramasco*,b, B. Muñoz*,a, A. Colmenero*,a, F. Simón*,a, A. Tabatabaian*,a Servicio de Anestesiología y Reanimación. aHospital Central de la Cruz Roja "San José y Santa Adela" Madrid. bHospital de La Princesa de Madrid. Resumen El hematoma epidural es una complicación neurológica infrecuente pero grave de la anestesia neuroaxial. Presentamos el caso de una mujer que fue intervenida de implante de prótesis de cadera y desarrolló esta complicación. Se realizó una anestesia combinada neuroaxial. La intervención transcurrió sin incidencias. En el postoperatorio se inició profilaxis tromboembólica y perfusión continua de ropivacaína por catéter epidural. El primer día del postoperatorio, apareció dolor lumbar y alteración sensitivomotora en miembros inferiores. Con la sospecha de hematoma epidural, se suspendió perfusión de anestésico local. Se realizó una tomografía computerizada (TC) que confirmó la existencia de un hematoma con límites mal definidos. Fue trasladada a centro de referencia para realización de resonancia magnética (RM) dorsolumbar, evidenciando un hematoma extenso. Rechazada para intervención quirúrgica se trató de forma conservadora. La evolución neurológica fue lentamente favorable en los días siguientes, siendo dada de alta a los 51 días de la cirugía con recuperación parcial. A los 6 meses de la intervención la recuperación era completa. Se comentan la prevalencia, la etiología y el tratamiento del hematoma neuroaxial asociado a anestesia locorregional. Palabras clave: Técnica anestésica: anestesia epidural, anestesia subaracnoidea. Heparina de bajo peso molecular. Complicaciones: hematoma epidural, hemorragia subaracnoidea Introducción La realización de técnicas anestésicas y analgésicas locorregionales es una práctica cada vez más extendida *Médico Adjunto Correspondencia: Sonsoles Martín Alcrudo C/Padilla, 56-6º Ext. Dcha. 28006 Madrid E-mail: [email protected] Aceptado para su publicación en abril de 2005. 59 Neuraxial hematoma after combined regional anesthesia: conservative resolution Summary Epidural hematoma is a rare but serious neurological complication of neuraxial anesthesia. We report the case of a woman in whom this complication presented after hip replacement surgery under combined neuraxial anesthesia. No adverse events occurred during surgery. In the early postoperative period thromboembolic prophylaxis and continuous perfusion of ropivacaine were started through the epidural catheter. Lumbar pain along with sensorimotor alterations in the lower limbs developed on the first day after surgery. Epidural hematoma was suspected and the perfusion of local anesthetic was suspended. A computed tomography scan confirmed the presence of a hematoma with poorly defined margins. The patient was transferred to another hospital for dorsolumbar magnetic resonance, which revealed an extensive hematoma. Surgery was ruled out in favor of conservative treatment. Neurological symptoms resolved slowly over the following days and the patient was discharged partially recovered 51 days after surgery and recovery was complete within 6 postoperative months. We discuss the prevalence, etiology, and treatment of neuraxial hematoma related to local or regional anesthesia. Key words: Anesthesia: epidural, subarachnoid. Low molecular weight heparin. Complications: epidural hematoma, subarachnoid hematoma. en los hospitales españoles y unidades de dolor por ser procedimientos seguros con una baja incidencia de complicaciones graves y secuelas. Presentan algunas ventajas en relación con la anestesia general como son una incidencia más baja de mortalidad, trombosis venosa profunda y tromboembolismo pulmonar, menor necesidad de transfusión perioperatoria y menor riesgo de depresión respiratoria y neumonía. Además son cada vez más demandadas por los pacientes que van a ser intervenidos1,2. Sin embargo no están exentas de complicaciones. El hematoma neuroaxial es una complicación extremadamente rara cuya incidencia actual se ha esti433 Rev. Esp. Anestesiol. Reanim. Vol. 52, Núm. 7, 2005 mado inferior a 1/150.000 en anestesias epidurales y menos de 1/220.000 en anestesias subaracnoideas3,4. Esta incidencia puede ser mayor ya que se desconoce el número real de procedimientos locorregionales que se realizan y por otro lado no se publican todas las complicaciones1. La intervención de pacientes más mayores tratados con anticoagulantes y/o antiagregantes como profilaxis tromboembólica, favorece el riesgo hemorrágico5. Los bloqueos neuroaxiales constituyen la décima causa de hematoma epidural de todos los hematomas publicados, aumentando a la quinta causa en caso pacientes con profilaxis tromboembólica6. La gravedad del sangrado peridural se debe a su localización en un espacio poco distensible, provocando la compresión e isquemia medular y, en casos extremadamente raros, incluso la muerte del paciente por difusión del sangrado intracraneal7,8. En cuanto a la etiología, es multifactorial a veces no del todo explicable. En casi un 30% de los hematomas espinales espontáneos no se pueden identificar factores predisponentes. El diagnóstico debe ser lo más precoz posible, ya que determinará la actitud terapéutica, quirúrgica de elección y, por tanto, el pronóstico. Caso clínico Presentamos el caso de una paciente de 76 años programada para artroplastia total de rodilla derecha que desarrolló un hematoma neuroaxial tras anestesia regional combinada. Entre sus antecedentes destacaban: hipertensión arterial, hipercolesterolemia, hemorragia digestiva alta por AINE, pérdida de la memoria reciente de meses de evolución que sugiere una demencia incipiente; lumbalgia tratada con AINE hasta dos días previos a la intervención. Las pruebas preoperatorias habituales, incluyendo las pruebas de coagulación, fueron normales. Se inició profilaxis tromboembólica 18 h antes de la intervención con heparina de bajo peso molecular (HBPM), enoxaparina 40 mg sc. Para la realización de la anestesia neuroaxial combinada se utilizó el set Braun®, realizándose punción epidural lumbar L3L4 única y atraumática más colocación del catéter progresado 4 cm cefálico. Por vía subaracnoidea se inyectaron 2,9 mL de bupivacaína hiperbara al 0,5%. Fueron monitorizados el ECG continuo, saturación de oxígeno, tensión arterial no invasiva y diuresis horaria. La intervención se realizó sin complicaciones en 1 hora y 45 min. Dos horas después de su ingreso en la Unidad de Reanimación (14:00 h) tras desaparición completa del bloqueo motor se inició la analgesia epidural previa dosis test (bupivacaína al 0,5% 4 mL) con ropivacaína al 0,2% y fentanilo (0,75 µg mL -1) en perfusión contínua de 4mL h-1 y bolos de 4 mL en régimen de PCA. Ocho horas después de la punción (20:00 h) se continuó la profilaxis tromboembólica con HBPM (40 mg de enoxaparina sc.) siendo el estudio analítico postoperatorio normal. A las 15 horas del ingreso (5:00 h) comenzó con dolor lumbar bilateral intenso que no mejoró con cambio postural ni con 434 la administración de mórfico parenteral asociado a agitación y desorientación temporoespacial. A las 18 h del ingreso (8:00 h del 2º día) se registró por primera vez bloqueo motor completo de extremidades inferiores suspendiéndose la infusión epidural para valoración clínica. A las 6 horas después de suspender la perfusión y ante la creciente sospecha de una complicación neurológica por persistencia de hemiplejía izquierda e hipoestesia L1 izquierda, se realizó una TC helicoidal en la que se apreciaron: áreas mal definidas en el interior del saco dural compatibles con sangre reciente en la parte posterior de D12 a L1 y anterior a nivel L2, sin poder definirse con precisión límites y extensión. Ante estas alteraciones la paciente fue trasladada a su centro de referencia para valoración neuroquirúrgica urgente y realización de RM a las 21:00 h. En la RM (figuras 1 y 2) se observó hematoma epidural y subdural subagudo extenso, mielitis de D10 a cono, estenosis de canal de L3 a S1. Dado el tiempo trascurrido desde la aparición de la sintomatología neurológica, el neurocirujano descartó indicación quirúrgica, iniciándose tratamiento conservador. Durante las siguientes 12 horas de tratamiento corticoideo (dexametasona 6 mg/6 h i.v.) se apreció evidente mejoría de la sensibilidad y discreta mejoría en la fuerza, con mejoría del cuadro confusional. La evolución neurológica inicial de la paciente fue favorable presentando a los 8 días después de la intervención una recuperación parcial de la fuerza distal y proximal bilateral, permaneciendo la incontinencia doble. Durante la fase de rehabilitación presentó varias complicaciones asociadas incluyendo deterioro de la función renal en la primera semana después de la intervención, accidente cerebro vascular agudo a los 30 días, infección urinaria y síndrome depresivo reactivo. A los 51 días de la intervención es dada de alta caminando con bastón, con marcha discretamente inestable y precipitada, con recuperación parcial de la continencia urinaria y en fase de rehabilitación de la continencia fecal. A los 6 meses camina sin ayuda habiendo recuperado la continencia. Discusión La mayoría de los casos publicados de hematoma neuroaxial en relación con una técnica locorregional se asocian al menos con cierta dificultad en la realización de la técnica, punción hemática o bien a coagulopatía previa1. En otros casos la ingesta previa de ácido acetíl salicílico, otros AINE9,10 o la profilaxis tromboembólica con heparina de bajo peso molecular (HBPM) se asoció con la aparición de hematoma espinal3,6,9,11,12. Los mecanismos fisiopatológicos implicados en la neuropatía tras anestesia locorregional son: la isquemia, la compresión, el traumatismo, la neurotoxicidad de las sustancias anestésicas y la infección13-16. Otros factores de riesgo relacionados con un hematoma epidural son: la edad, las alteraciones de la coagulación primarias o secundarias17-20; la técnica regional, el tipo 60 S. MARTÍN ET AL– Hematoma neuroaxial tras anestesia locorregional combinada resuelto de forma conservadora Fig. 2. Resonancia magnética. Vista axial a nivel de L1. Hematoma subdural posterior -izquierdo con desplazamiento de la médula hacia la derecha (Flecha). Fig. 1. Resonancia magnética. Vista sagital de la columna torácica y lumbar: Hematoma epidural y subdural en servilletero de D11 a L5. Mielitis de D10 a cono. Estenosis de canal de L3 a S1. y tamaño de aguja empleada21,22, la retirada del catéter epidural y finalmente también anormalidades anatómicas del canal medular13,15,23,24. En nuestro caso la realización de una profilaxis tromboembólica perioperatoria y la ingesta de AINE en los días previos a la intervención pueden haber favorecido la aparición de sangrado junto a la movilización accidental del catéter epidural por agitación psicomotriz y la presencia de estenosis de canal. Actualmente existe numerosa literatura que apoya el uso de anestesia regional asociada a HBPM y se considera que estos pacientes no deberían tener mayor riesgo de complicaciones siempre que se cumplan las normas vigentes en relación a este fármaco9,25-27. Se debe seguir el margen de seguridad establecido para el manejo preoperatorio de los antiagregantes y AINE13,17,20. La clínica del hematoma neuroaxial causa signos y síntomas secundarios a la compresión medular o de las raíces nerviosas. Su presentación es brusca, con dolor dorsal irradiado a las extremidades inferiores de intensidad variable y no siempre presente, debilidad mus61 cular en diferentes grados, siendo la sintomatología más frecuente y manifestaciones sensitivas1,9,28-30. Se han descrito casos con déficit neurológico transitorio de evolución espontánea, síntomas radiculares de tipo irritativo que recuerdan a la aracnoiditis por anestésicos locales30. Hay autores que postulan la existencia, en algunos casos, de sangrados subclínicos que pasarían desapercibidos10,31. En nuestro caso, el dolor y el déficit motor fue la sintomatología más llamativa. El diagnóstico de este tipo de complicaciones exige un seguimiento adecuado de los pacientes en los que se realizan técnicas locorregionales, especialmente con catéter epidural. El diagnóstico precoz es fundamental ya que su retraso empeora el pronóstico y las posibilidades de recuperación. Sin embargo no siempre es posible debido a que la sintomatología es muy variable y el bloqueo residual por anestésicos locales enmascara la clínica neurológica. Además si el paciente no se encuentra en una unidad de vigilancia continua, el seguimiento del paciente será inadecuado. En el caso presente los antecedentes de dolor lumbar previo, la perfusión continua de analgesia epidural y el cuadro confusional añadido dificultaron la interpretación de la sintomatología. Ante la sospecha de este tipo de complicaciones, debe realizarse para su diagnóstico una RM. En muchos casos la realización de una TC no es concluyente29. El estudio con RM proporciona excelentes imágenes del eje espinal con una buena definición del espacio subaracnoideo y de hematomas extradurales y 435 Rev. Esp. Anestesiol. Reanim. Vol. 52, Núm. 7, 2005 subdurales permitiendo detectar lesiones vasculares asociadas7,28. El diagnóstico precoz en nuestra paciente se vio dificultado por el hecho de carecer de RM en nuestro centro y tener que ser trasladada a hospital de referencia para su realización. El tratamiento de elección es la laminectomía con evacuación del hematoma peridural. Se debe efectuar de manera urgente para evitar lesiones neurológicas permanentes. Los resultados neurológicos dependen de la rapidez en que se desarrolle la compresión, del tamaño y extensión del hematoma, del compromiso neurológico existente y del tiempo transcurrido desde el inicio de la sintomatología hasta el momento de la descompresión. Se recomienda no se demore más de 8 horas3,29,32. Aunque también están descritos casos en los que se realiza la descompresión quirúrgica pasadas 12 h e incluso a las 72 h con recuperación completa3,29. El tratamiento quirúrgico puede no ser necesario si la clínica mejora o se estabiliza al retirar el catéter epidural y en estos casos se debe observar la evolución clínica para replantear tratamiento quirúrgico más adelante en función de la respuesta al tratamiento médico y los hallazgos por resonancia33,34. Una revisión de 4 casos clínicos presentada por Duffill et al. el diagnóstico fue precoz y a pesar de disponer de servicio de neurocirugía, el tratamiento con corticoides dio buenos resultados, presentándose como una alternativa a la laminectomía . En España la casuística del tratamiento conservador es bastante alta según el trabajo de J. Castillo et al1. En nuestra paciente se confirmó la sospecha clínica tras realizarse una RM a las 31 horas de la punción; el tratamiento conservador en este caso tuvo una recuperación favorable progresiva y completa a pesar de las complicaciones añadidas que tuvo durante su ingreso. Como conclusión podemos señalar que, a pesar de haberse realizado una técnica sin incidencias, con profilaxis tromboembólica adecuada y pruebas de coagulación, número de plaquetas normales, se desarrolló un hematoma neuroaxial. Por tanto siempre debemos estar alerta para que el diagnóstico y tratamiento sean lo más precoces posibles y así garantizar la recuperación sin secuelas. Para ello una estricta vigilancia neurológica postoperatoria con especial alerta a los síntomas de dolor lumbar y bloqueo motor prolongado, especialmente en casos de perfusión continua y pacientes poco colaboradores, así como el cumplimiento de las normas consensuadas en la realización de la técnica, manejo de medicación anticoagulante o antiagregante, pueden minimizar las complicaciones asociadas. El tratamiento médico puede ser una alternativa en determinados casos siempre y cuando podamos disponer de un especialista en neurocirugía y seguimiento por resonancia magnética. 436 BIBLIOGRAFÍA 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. Castillo J, Santiveri X, Escolano F, Castaño J. Hematomas raquídeos con compresión medular relacionados con las anestesias neuroaxiales en España. Rev Esp Anestesiol Reanim 2003;50(10):504-509. Rodgers WN, Schug S, McKee A, Kehlet H, Van Zunder A, Sage D et al. Reduction of postoperative mortality and morbidity with epidural or spinal anaesthesia: results from overview of randomised trials. Br Med J 2000;321(7275):1493-1497. Sanchis C, Gimeno MJ, Díez P, Tarín C, Miranda JA. Hematoma epidural de instauración progresiva tras anestesia combinada. Rev Esp Anestesiol Reanim 2004;51(8):467-469. Horlocker T, Wedel DJ. Neurologic complications of spinal and epidural anesthesia Reg Anesth Pain Med 2000; 25(1): 83-98. Horlocker TT, Wedel DJ, Benzon H, Brown DL, Enneking FK, Heit JA et al. Regional Anesthesia in the Anticoagulated Patient: Defining the Risks (The Second ASRA Consensus Conference on Neuraxial Anesthesia and Anticoagulation). Reg Anesth Pain Med 2003;28(3):172-197. Kreppel D, Antoniadis G, Seeling W. Spinal hematoma: a literature survey with meta-analysis of 613 patients. Neurosurg Rev 2003; 26(1):1-49. Peiró CM, Caballe N, Errando C, Moliner S. Hematoma espinal y cerebral postpunción lumbar diagnóstica con evolución letal. Rev Esp Anestesiol Reanim 2003;50(9):481-485. Acharya R, Chhabra SS, Ratra M, Sehgal AD. Cranial subdural haematoma after spinal anaesthesia. Br J Anaesth Jun 2001; 86(6):893-895. Vandermeulen EP, Van Aken H, Vermylen J. Anticoagulants and spinal epidural anesthesia. Anesth Analg 1994;79(6):1165-1171. Gerancher JC, Watere R, Middleton J. Transient paraparesis after postdural puncture spinal hematoma in a patient receiving ketorolac. Anesthesiology 1997;86(2):490-494. Sandhu H, Morley-Forster P, Spadafora S. Epidural hematoma following epidural analgesia in a patient receiving unfractionated heparin for thromboprophylaxis. Reg Anesth Pain Med 2000; 25(1):72-75. Horlocker T, Wedel DJ. Spinal and Epidural Blockade and Perioperative Low Molecular Weight Heparin: Smooth Sailing on the Titanic. Anesth Analg 1998;86(6):1153-1156. Carrascosa AJ, Molina JA. Complicaciones neurológicas de los bloqueos perimedulares en anestesia regional. Rev Neurol 1999;29(6):572-579. Wilkinson PA, Valentine A, Gibbs JM. Intrinsic spinal cord lesions complicating epidural anaesthesia and analgesia: report of three cases J Neurol Neurosurg Psychiatry 2002;72:(4)537-539. Yuen EC, Layzer RB, Weitz SR, Olney RK. Neurologic complications of lumbar epidural anesthesia and analgesia. Neurology 1995; 45(10):1795-1801. Freedman JM, Li DK, Drassner K, Jaskela MC, Larsen B, Wi S. Transient neurologic symptoms after spinal anesthesia: An epidemiologic study of 1863 patients. Anesthesiology 1998; 89(3):663-641. Llau JV, de Andrés J, Gomar C, Hidalgo F, Sahagún J, Torres LM. Fármacos que alteran la hemostasia y técnicas regionales anestésicas: recomendaciones de seguridad. Foro de consenso. Rev Esp Anestesiol Reanim 2001;48(6):270-278. Guasch E, Suarez A. Recuento plaquetario y punción hemática con el bloqueo epidural en obstetricia. Rev Esp Anestesiol Reanim 2003;50(3):130-134. Litz RJ, Gottschlich B, Stehr SN. Spinal epidural hematoma after spinal anesthesia in a patient treated with clopidogrel and enoxaparin. Anesthesiology 2004;101(6):1467-1470. Broadman LM. Non-steroidal anti-inflammatory drugs, antiplatelet medications and spinal axis anesthesia. Best Practice & Research Clinical Anaesthesiology 2005;19(1):47-58. Reina MA, López García A, de Andrés Ibáñez, Dittmann M, Cascales MR, del Caño MC, et al. Microscopía electrónica de las lesiones producidas en la duramadre humana por las agujas de bisel Quincke y Whitacre. Rev Esp Anestesiol Reanim 1997;44(2):56-61. Absalom AR, Martinelli G, Scott NB. Spinal cord injury caused by direct damage by local anaesthetic infiltration needle. Br J Anaesth 2001;87(3):512-515. Esler MD, Durbridge J, Kirby S. Epidural Haematoma after dural puncture in a parturient with neurobromatosis. Br J Anaesth 2001;87 (6):932-934. 62 S. MARTÍN ET AL– Hematoma neuroaxial tras anestesia locorregional combinada resuelto de forma conservadora 24. Bromage PR. Neurological complications of subarachnoid and epidural anaesthesia. Acta Anaesthesiol Scand 1997;41(4):439-444. 25. Horlocker TT. Tromboprofilaxis y anestesia neuroaxial: mantener la vigilancia para evitar efectos adversos. Rev Esp Anestesiol Reanim 2001;48(6):255-257. 26. Gilbert A, Brian DO, Michael FM. Epidural hematoma after outpatient epidural anestesia. Anesth Analg 2002;94(1):77-78. 27. Llau JV, Hoyas L, Ezpeleta J, García Polit J, Barberá. M, Santes MJ. Heparinas de bajo peso molecular. Implicaciones en anestesia y reanimación. Rev Esp Anestesiol Reanim 1997;44(2):70-78. 28. Macías Pingarrón JP, Torrado Criado MD, Alfonso Sanz F, Robles Barragán J, Gallego Cordoba JM. Hematoma epidural tras anestesia regional combinada en una paciente sin trastornos de la coagulación. Rev Esp Anestesiol Reanim 2003;50(4):209-210. 29. Cabrera A, Ornaque I, López Obarriob L, Quintanilla M, Gabarrós A, Fuentes J et al. Hematoma epidural tras la retirada de un catéter a un paciente sin transtornos de la coagulación. Rev Esp Anestesiol Reanim 2002;49(5):272-275. 30. Duffill J, Sparrow O, Millar J, Baker C. Can spontaneos epidural haematoma be managed safely without operation? A report of four cases. Neurol Neurosurg Psychiatry 2000;69(6):816-819. 63 31. Inoue K, Yokoyama M, Nakatsuka H, Goto K. Spontaneous resolution of epidural hematoma after continuous epidural analgesia in a patient without bleeding tendency. Anesthesiology 2002;97(3):735734. 32. Blasi A, Fita G, Gomar C, Adelia R, Jiménez MJ. Hematoma epidural tras la retirada de un catéter epidural. Rev Esp Anestesiol Reanim 1998;45(7):294-297. 33. Herbstreit F, Kienbaum P, Merguet P, Peters J. Conservative treatment of paraplejia after removal of an epidural catheter during low molecular- weight heparin treatment. Anesthesiology 2002;97(3):733-734. 34. La Rosa G, d'Avella D, Conti A, Cardali S, La Torre D, Cacciola F et al. Magnetic resonance imaging-monitored conservative management of traumatic spinal epidural hematomas. J Neurosurg 1999; 91(suppl): 128–132. 35. Broadman LM. Non-steroidal anti-inflammatory drugs, antiplatelet medications and spinal axis anesthesia. Best Practice & Research Clinical Anaesthesiology 2005; 19(1):47–58. 36. Rodrigo Casanova MP, García Peña JM, Bedia del Rio E, Freijo Guerrero J, Aguilera Celorrio L. Hematoma subaracnoideo tras punción lumbar diagnóstica. Rev Esp Anestesiol Reanim 2005;52(2):120-121. 437