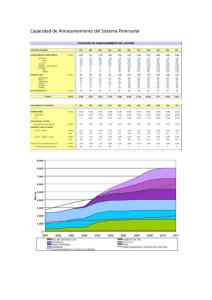
Comparación de los valores de referencia hematológicos en ratas
Anuncio

Comparación de los valores de referencia hematológicos en ratas wistar/UIS (Rattus norvergicus) con parámetros establecidos en laboratorios de altos estándares Comparison of hematology reference values of strain wistar/UIS (Rattus norvergicus) with parameters established in standards laboratories Víctor Hernán Arcila Quiceno MVZ, Esp.* * Docente-investigador. Comité de Investigación en Ciencias Animales (CICA). Grupo de investigación en ciencias animales, Universidad Cooperativa de Colombia. Correo electrónico: [email protected] Carlos Arturo Conde Cotes MD, Ph. D** ** Docente-investigador, Universidad Industrial de Santander. Director Bioterio UIS. Director Grupo de Neurociencias y Comportamiento UIS-UPB. Correo electrónico: [email protected] Javier Eduardo Nieto Pico MVZ*** *** Universidad Cooperativa de Colombia. Comité de Investigación en Ciencias Animales. Auxiliar de Investigación. Laboratorio de Neurociencias y Comportamiento UIS, Universidad Industrial de Santander. Correo electrónico: [email protected] Fredy Humberto García Prada MVZ**** **** Universidad Cooperativa de Colombia. Comité de Investigaciones en Ciencias Animales (CICA). Correo electrónico: [email protected] Recibido: 30 de septiembre del 2009 Aceptado: 30 de noviembre del 2009 Resumen: en el contexto mundial, muchos laboratorios y centros de investigación, tanto públicos como privados, han caracterizado totalmente las colonias de animales que mantienen, teniendo registrados datos que incluyen: el ambiente microbiológico de los bioterios, el peso de los órganos, la calidad microbiológica de los biomodelos, su condición genética, curvas de crecimiento, entre otros, lo que ha permitido obtener animales con características específicas para la necesidad de cada área de investigación. El objetivo de este trabajo fue determinar los valores de referencia hematológicos de la cepa wistar/UIS. Los resultados permiten observar diferencias en diferentes variables dentro de la cepa wistar/UIS, determinadas por sexo y edad, y también diferencias significativas con respecto a la cepa utilizada para comparación. Abstract: in the world, many research laboratories public and private, have totally characterized the colonies of animals maintained, this data recorded include: the microbiological environment of the animal facilities, the organs weight, microbiological quality of biomodels, genetic status, growth charts, among others, which has enabled researchers to produce animals with specific characteristics to the needs of each area of research. The aim of this study was to determine the hematology reference values for strain wistar/UIS, the results allow us to see differences in different variables, both within the wistar/UIS determined by sex and age, and also significant differences with the strain used for comparison. Keywords: animal housing facilities, strain, hematology, rat. Palabras clave: bioterio, cepas, hematología, ratones. VOLUMEN 6 / NÚMERO 12 / ENERO - JUNIO DEL 2010 / R07 SpeiDomus No 12.indd 45 R e v i s ta S p e i D o m u s 45 04/05/11 23:53 Comparación de los valores de referencia hematológicos en ratas wistar/UIS (Rattus norvergicus) con parámetros establecidos en laboratorios de altos estándares Introducción La hematología comprende el estudio del paquete celular, el perfil o el estado sanguíneo. Específicamente, los estudios de cambios hematológicos hacen parte de una primera aproximación para la caracterización de un biomodelo, determinando características morfológicas y químicas, permitiendo así establecer valores alrededor de las condiciones y el manejo de los animales de experimentación (1, 2), teniendo en cuenta: • Recuento de eritrocitos (y valor hematocrito) • Recuento de leucocitos • Determinación de hemoglobina • Fórmula leucocitaria (recuento diferencial de leucocitos) • Determinación de las plaquetas • Índices eritrocíticos de Wintrobe (VCM, HCM, CHCM) Los eritrocitos, también denominados hematíes o glóbulos rojos, son células redondeadas, bicóncavas y anucleadas (excepto en aves y reptiles). Están formados por un 60% de agua, 35% de hemoglobina y 5% de matriz orgánica; se caracterizan por ser altamente deformables, propiedad que les permite pasar a través de capilares estrechos. Son producidos en la médula ósea a nivel del compartimiento hematopoyético. La biometría hemática o hemograma es uno de los procedimientos de rutina a nivel de laboratorio con requerimientos mínimos de equipo y de mayor importancia, ya que la información obtenida proporciona una idea muy confiable del estado general de la salud del paciente (3, 4). La determinación de la fórmula roja se compone de los siguientes parámetros: • Conteo eritrocítico: consiste en la cuantificación del número de glóbulos rojos por volumen. El recuento de los eritrocitos se puede hacer mediante métodos manuales o automatizados (en la actualidad, los métodos manuales no son muy utilizados). Se realiza en un hemocitómetro o cámara de Neubaüer. Su variación en los resultados es alta (± 20%) y hay mayor gasto de tiempo. • Volumen corpuscular medio (VCM): (Hto. x 10/ eritrocitos): se trata del volumen promedio de una célula individual; es una forma de conocer el volumen ocupado por un eritrocito dentro del hematocrito. 46 • Concentración de hemoglobina corpuscular media (CHCM): (Hb. x 100 / Hto. %): es la cantidad de hemoglobina que está relacionada directamente con el eritrocito. Corresponde al índice más preciso, ya que no requiere del conteo total de eritrocitos circulantes. Esta ecuación indica cuál es la cantidad de hemoglobina presente en la masa globular, y se expresa en gr / dL. La CHCM estaría señalando si los glóbulos rojos poseen una cantidad adecuada de hemoglobina (normocrómicos), según la especie, o, por el contrario, si esta es baja (hipocrómicos) (5). • Hemoglobina corpuscular media (HCM): (Hb. x 10 / eritrocitos): señala cuál sería la cantidad de hemoglobina que contiene en promedio un eritrocito. Se expresa en picogramos (pg = 10-12 gr) y se obtiene al dividir la concentración de hemoglobina por el recuento de glóbulos rojos. La información obtenida con este índice es similar a la que entrega la CHCM, por lo que ofrece poca información adicional (5). La denominada “línea blanca” determina los parámetros relacionados con los leucocitos (también llamados glóbulos blancos), conjunto heterogéneo de células sanguíneas que son los efectores celulares de la respuesta inmune, de manera que intervienen en la defensa del organismo contra sustancias extrañas o agentes infecciosos (antígenos). Se originan en la médula ósea y en el tejido linfático. Son células con núcleo, mitocondrias y otros orgánulos celulares. Son capaces de moverse libremente mediante seudópodos. Su tamaño oscila entre los 8 y 20 μm (6). Materiales y métodos Para el desarrollo de este trabajo se tomaron muestras de sangre de 100 ratas wistar/UIS (Rattus norvegicus), 50 machos y 50 hembras mayores de 8 semanas, provenientes del bioterio de la Facultad de Salud de la Universidad Industrial de Santander. Los animales fueron mantenidos bajo ciclos de luz-oscuridad controlada (12 horas c/u, luz encendida a las 7 a.m. y apagada a las 7 p.m.) y en todos los casos se suministraron 15 gramos de alimento/ animal/día. Además, estuvieron bajo temperatura controlada (21 ± 2 ºC) y humedad relativa promedio de 65% a 75%. La toma de las muestras sanguíneas en todos los casos fue realizada entre las 6 a.m. R e v i s ta S p e i D o m u s / v o l u m e n 6 / N Ú M E R O 1 2 / E NE R O - J UN I O D E L 2 0 1 0 R07 SpeiDomus No 12.indd 46 04/05/11 23:53 V íc to r H . A rc i l a Q., C a r l o s A . C o nde C ., Ja vi e r E . N i e to P., Fredy H . García P. y las 8 a.m. por el método de punción de la vena lateral caudal. Todos los procedimientos llevados a cabo con los animales se hicieron con la aprobación del comité de bioética, y bajo los lineamientos para el uso y cuidado de animales de laboratorio (7, 8, 9, 10). Procesamiento de las muestras Para el recuento total de glóbulos rojos, se hizo una dilución 1/200 de la sangre. Posteriormente, se depositó la dilución en la cámara de Neubaüer, leyendo 5 de los 25 cuadrantes del centro (los 4 extremos y el centro). El conteo se realizó en un microscopio de luz con el objetivo de 40x y el resultado fue multiplicado por 10.000, lo que representa un número de eritrocitos por milímetro cúbico (106/mm3) de sangre. El hematocrito se determinó por el método de microhematocrito, que consiste en un tubo capilar de calibre estrecho, de aproximadamente 1 mm de diámetro y de 60 mm de longitud, que se llena casi completamente de sangre, cerrado en uno de sus extremos (para lo cual se usa con regularidad plastilina), y se centrífuga a 10.000 RPM durante 5 minutos. Transcurrido este tiempo, se hace la lectura en una tabla especial graduada de 0 a 100. La determinación de la hemoglobina se realizó por colorimetría, mediante el método de la cianometahemoglobina. El resultado se expresa en g/dl. Los índices de eritrocitos fueron determinados mediante cálculos matemáticos, por medio de los índices eritrocíticos de Wintrobe. El recuento total de glóbulos blancos se realizó utilizando un hemocitómetro de Neubaüer, la pipeta para dilución de leucocitos y la solución de Turk. El recuento diferencial se realizó por medio de un extendido de sangre en una lámina portaobjetos con tinción de Wright y se examinaron al microscopio de luz con el objetivo de 100x, usando aceite de inmersión y contando hasta 100 células, las cuales se clasificaban de acuerdo con sus características morfológicas. Para el recuento plaquetario se utilizó un hemocitómetro de Neubaüer, la pipeta para dilución y solución de oxalato. Análisis estadístico Para la elaboración del análisis de este estudio se dividieron los animales en 4 grupos, considerando sexo y edad. Esta división se realizó con base en el criterio de adultos jóvenes y adultos mayores, con el fin realizar la comparación con datos de otras publicaciones, como las de Charles River (11, 12). Tabla 1. Cuantificación del número de animales de acuerdo con los grupos de edad Grupo Hembras menores de 16 semanas Hembras mayores de 16 semanas Machos menores 16 semanas Machos mayores 16 semanas Fuente: los autores Para todos los sujetos de este estudio se registraron y analizaron las siguientes variables: • Sexo (machos-hembras), fecha de nacimiento y fecha de análisis, como criterio para precisar la edad en semanas. • Volumen y concentración de glóbulos rojos: hematocrito (Hto. %), hemoglobina (Hb gr/dL), recuento total de glóbulos rojos (RTGR 106/mm3), volumen corpuscular medio VCM fL (μm3), concentración de hemoglobina corpuscular media CHCM (g/dL), hemoglobina corpuscular media HCM (pg). • Valores relativos y absolutos respectivamente para los leucocitos: segmentados (%), segmentados (103/mm3), linfocitos (%), linfocitos (103/mm3), eosinófilos (%), eosinófilos (103/mm3), monocitos (%), monocitos (103/mm3), cayados (%), cayados (103/ mm3), basófilos (%), basófilos (103/mm3), recuento total de glóbulos blancos (RTGB 103/mm3). • Conteo total de plaquetas (103/mm3): para el análisis estadístico se realizó ANOVA de dos vías, tomando como factores el sexo y la edad, junto con comparaciones múltiples corregidas (Bonferroni test) para cada una de las variables. Posteriormente se utilizó la prueba de valor de hipótesis (hypothesis test) para hacer la comparación con los parámetros de referencia (mean vs. hipothesized value). El nivel de significancia fijado para las pruebas estadísticas utilizadas fue de P < 0,05. Se utilizaron los recursos de planillas de Excel (Microsoft Office) y el SigmaStat v. 3.5 para los análisis estadísticos. VOLUMEN 6 / NÚMERO 12 / ENERO - JUNIO DEL 2010 / R07 SpeiDomus No 12.indd 47 n 21 29 10 40 R e v i s ta S p e i D o m u s 47 04/05/11 23:53 Comparación de los valores de referencia hematológicos en ratas wistar/UIS (Rattus norvergicus) con parámetros establecidos en laboratorios de altos estándares Resultados 48 UIS 52 50 ** ** <=16S >16S ** * ** * CHARLES RIVER % 48 46 44 42 40 Hembras <=16S >16S Machos <=16S >16S <=16S Hembras - C >16S Machos - C Figura 1. Representa los promedios ± EEM de los valores de hematocrito (Hto. %) de los grupos de la muestra estudiada y de los valores reportados por Charles River. * Machos mayores que hembras dentro de la muestra UIS (ANOVA dos factores p < 0,05). ** Valores de la muestra UIS mayores que valores de Charles River (Prueba t, p < 0,05). Fuente: los autores RTGB 103/MM3 UIS 16 CHARLES RIVER 14 103/MM3 12 10 8 6 4 2 0 <=16S >16S Hembras <=16S >16S <=16S Machos >16S Hembras - C <=16S >16S Machos - C Figura 2. Representa los promedios ± EEM de los valores de Recuento total de glóbulos blancos (RTGB 103/mm3) de los grupos de la muestra estudiada y de los valores reportados por Charles River. * Mayor en los anímales menores de 16 semanas dentro de la muestra UIS (ANOVA dos factores p < 0,05). ** Valores de la muestra UIS mayores que valores de Charles River (Prueba t, p < 0,05). Fuente: los autores RTGB 103/MM3 9 CHARLES RIVER UIS 8,5 8 7,5 103/MM3 El primer análisis tenía como propósito evaluar si había diferencias significativas entre machos y hembras por grupos de edades en cada una de las variables. Un análisis con ANOVA de dos vías (sexo y edad) con cada una de las variables mostró los siguientes resultados: Las variables Hto. % (F 1,96 = 6,013 p = 0,016), Hb gr/dL (F 1,96 = 4,709 p = 0,032) y RTGR 106/mm3 (F 1,96 = 12,425 p = < 0,001) mostraron una diferencia significativa determinada por el sexo, siendo mayor en los machos que en las hembras la variable VCM fL, que también mostró una diferencia significativa por el sexo (F 1,96 = 4,092 p = 0,0459), pero que fue mayor en hembras que en machos. Las variables RTGR 103/mm3 (F 1,96 = 0,268 p = < 0,001), linfocitos % (F 1,96 = 0,451 p = < 0,001), plaquetas 103/mm3 (F 1,96 = 3,531 p = 0,008), linfocitos 103/mm3 (F 1,96 = 0,305 p = 8,60 E-05) y RTGR 106/mm3 (F 1,96 = 64,88 p = < 0,001) mostraron una diferencia significativa determinada por la edad, siendo mayor en los anímales menores de 16 semanas. Las variables segmentados % (F 1,96 = 0,531 p = < 0,001), HCM pg (F 1,96 = 0,464 p = 1,57 E-05) y VCM fL (F 1,96 = 4,092 p = 1,43 E-09) muestran también una diferencia significativa determinada por la edad, pero siendo mayores en los animales de más de 16 semanas. Con el tercer abordaje estadístico se pretendió realizar una comparación con los datos obtenidos para el mismo linaje de animales y los mismos intervalos de edades reportados en marzo del 2008 por Charles River Laboratories Preclinical Services, Raleigh, NC 26. El análisis de los datos mostró diferencias significativas para cada uno de los grupos, en algunas de las variables consideradas, esto es, valores de hematocrito, recuento total de glóbulos rojos, recuento total de glóbulos blancos y recuento plaquetario. Las figuras 1, 2, 3 y 4 muestran la comparación de los valores de hematocrito (Hto. %), recuento total de glóbulos blancos (TRGB 103/mm3), recuento total de glóbulos rojos (RTGR 106/mm3) y plaquetas (plaquetas 103/mm3), respectivamente, determinados tanto en machos como en hembras, en las diferentes edades, en ambos laboratorios (UIS - Charles River). Hto %54 7 6,5 6 5,5 5 <=16S >16S Hembras <=16S >16S Machos <=16S >16S Hembras - C <=16S >16S Machos - C Figura 3. Representa los promedios ± EEM de los valores de recuento total de glóbulos rojos (RTGB 106/mm3) de los grupos de la muestra estudiada y de los valores reportados por Charles River. * Machos mayores que hembras dentro de la muestra UIS (ANOVA dos factores p < 0,05). ** Valores de Charles River mayores que valores de la muestra UIS (prueba t, p < 0,05). *** Mayor en animales menores de 16 dentro de la muestra UIS (ANOVA dos factores p < 0,05) Fuente: los autores R e v i s ta S p e i D o m u s / v o l u m e n 6 / N Ú M E R O 1 2 / E NE R O - J UN I O D E L 2 0 1 0 R07 SpeiDomus No 12.indd 48 04/05/11 23:53 V íc to r H . A rc i l a Q., C a r l o s A . C o nde C ., Ja vi e r E . N i e to P., Fredy H . García P. Discusión Plaquetas 103/MM3 1000 900 800 103/MM3 700 600 500 400 300 200 100 0 <=16S >16S <=16S Hembras >16S <=16S Machos >16S Hembras - C <=16S >16S Machos - C Figura 4. Representa los promedios ± EEM de los valores de plaquetas (plaquetas 103/ mm3) de los grupos de la muestra estudiada y de los valores reportados por Charles River. * Mayor en animales menores de 16 semanas dentro de la muestra UIS (ANOVA dos factores p < 0,05). ** Valores de Charles River mayores que los valores de la muestra UIS (Prueba t, p < 0,05) Fuente: los autores Tabla 2. Valores de referencia hematológicos en ratas macho wistar/UIS Parámetro Hematocrito Hemoglobina Total glóbulos rojos Total glóbulos blancos Neutrófilos Linfocitos Monocitos Eosinófilos Basófilos Cayados VCM CHCM HCM Neutrófilos Linfocitos Monocitos Eosinófilos Basófilos Cayados Plaquetas Unidad SD Rango 51,3 15,24 1,42 1,32 49-54 13,20-17,10 49,80 14,72 3,60 2,44 40-55 10,22-23,52 106 /mm3 8,23 0,29 7,80-8,65 6,07 1,19 3,85-9,20 103/mm3 103/mm3 103/mm3 103/mm3 103/mm3 103/mm3 103/mm3 fL g/dL Pg % % % % % % 103/mm3 13,32 1,05 12,09 0,09 0,07 0 0,02 62,38 29,69 18,52 8,2 90,5 0,6 0,6 0 0,10 422,9 2,13 0,57 2,29 0,15 0,1 0 0,05 1,42 2,22 1,49 4,85 5,04 0,97 0,84 0 0,32 92,68 10,45-16,45 0,16-1,95 9,41-15,13 0-0,47 0-0,24 0,00 0-0,16 60-64,20 25,88-32,88 15,53-20,05 1 a 16 82-96 0-3 0 -2 0,00 0-1 270-584 10,50 1,45 8,82 0,10 0,12 0,00 0,01 84,67 29,72 25,28 13,90 83,88 0,95 1,18 0,00 0,08 361,80 2,18 0,77 2,02 0,19 0,14 0,03 0,03 15,14 5,63 7,88 6,27 7,30 1,41 1,36 0,00 0,27 181,25 7,30-15,6 0,11-3,74 5,93-12,96 0-1,09 0-0,67 0 0-0,14 58,4-117,52 20,86-52,27 17,04-61,09 1 a 29 64-99 0-7 0-7 0 0-1 102-662 % g/dL Promedio Machos menores de 16 semanas Promedio S.D. Rango Machos mayores de 16 semanas Fuente: los autores Tabla 3. Valores de referencia hematológicos en ratas hembra wistar/UIS Parámetro Hematocrito Hemoglobina Total glóbulos rojos Total glóbulos blancos Neutrófilos Linfocitos Monocitos Eosinófilos Basófilos Cayados VCM CHCM HCM Neutrófilos Linfocitos Monocitos Eosinófilos Basófilos Cayados Plaquetas Unidad % g/dL Promedio 48,38 13,90 106 /mm3 7,12 103/mm3 103/mm3 103/mm3 103/mm3 103/mm3 103/mm3 103/mm3 fL g/dL Pg % % % % % % 103/mm3 12,92 1,30 11,41 0,05 0,13 0,02 0,01 69,8 28,89 19,99 10,10 88,33 0,38 1,00 0,10 0,05 387,76 SD 3,47 1,02 Rango Promedio 37-53 46,21 12,5-15,8 13,98 Rango 40-52 10,40-18,50 1,20 5,12-8,50 5,53 0,74 4,44-7,27 3,09 0,58 2,79 0,10 0,11 0,09 0,03 13,2 2,98 3,08 4,17 4,66 0,67 0,77 0,44 0,22 121,22 9,25-19,55 0,39-2,58 7,96-17,40 0-0,37 0-0,39 0-0,39 0-0,13 57,8-92,1 24,53-36,22 15,29-25,39 4 a 20 77-96 0-2 0-2 0-2 0-1 228-656 10,11 1,24 8,69 0,05 0,12 0,01 0,05 90,0 28,61 25,68 14,03 84,00 0,66 1,14 0,10 0,03 279,59 4,81 0,46 4,74 0,10 0,13 0,03 0,10 14,9 4,32 5,37 7,33 7,41 1,23 1,19 0,03 0,19 74,46 5,55-26,50 0,45-2,13 3,72-24,65 0-41 0-0,54 0-0,13 0-0,41 63,02-114,86 21,76-36,27 17,48-41,01 5 a 30 67-94 0-5 0-4 0-1 0-1 176-460 Hembras menores de 16 semanas Fuente: los autores S.D. 3,33 2,37 Hembras mayores de 16 semanas Varios reportes han revelado que el sexo, la edad, la especie, la cepa, las condiciones ambientales, el estado sanitario, el estrés, la alimentación, la forma de obtención (13, 14) y el procesamiento de la muestra influyen en las grandes diferencias reportadas para estos parámetros. Ciertamente los valores reportados en cada una de estas investigaciones pueden ser limitados, ya que las variables aquí mencionadas pueden influenciar los resultados obtenidos. Así mismo, muchos datos han sido reportados en los trabajos citados, y existen diferencias significativas entre los reportados en cada uno de ellos. Todos estos resultados no son, desde luego, directamente comparables entre sí, ya que han sido producto del trabajo con diferentes cepas (15) y fueron obtenidos en laboratorios diferentes, con condiciones ambientales distintas, usando una variedad de técnicas, durante determinado número de años (16). Sin embargo, se han llevado a cabo discusiones en torno a los resultados de cada uno de estos trabajos (17), teniendo en cuenta, por ejemplo, que algunas de las variaciones en los diferentes parámetros pueden ser provocadas directamente por las diferencias genéticas de cada una de las cepas (18) y, por lo tanto, los datos allí reportados no pueden considerarse patológicos o anormales (19). Además, las diferencias en los parámetros para animales de la misma cepa mantenidos bajo las mismas condiciones pueden ser atribuibles a la fluctuación en el ambiente durante el curso del experimento (20). Como un primer abordaje a la discusión de los datos obtenidos en este trabajo, se pueden mencionar las grandes diferencias en los valores del hematocrito (Hto. %) de los sujetos de este estudio, comparados con los valores de la referencia, como se mostró en los resultados (figura 1), los cuales pueden ser influenciados por la altura sobre el nivel del mar y la presión parcial de O2 (21), teniendo en cuenta que hay una diferencia de ± 900 msnm entre la ubicación del bioterio del Laboratorio de Neurociencias y Comportamiento UIS y la ubicación del bioterio de la referencia. A pesar de que el recuento total de glóbulos rojos fue significativamente mayor en la referencia, una posible explicación de esta situación podría ser que el volumen corpuscular medio y la hemoglobina corpuscular media se encontraban elevados como respuesta compensatoria a los pocos glóbulos rojos en la sangre, sin VOLUMEN 6 / NÚMERO 12 / ENERO - JUNIO DEL 2010 / R07 SpeiDomus No 12.indd 49 R e v i s ta S p e i D o m u s 49 04/05/11 23:53 Comparación de los valores de referencia hematológicos en ratas wistar/UIS (Rattus norvergicus) con parámetros establecidos en laboratorios de altos estándares negar que estos resultados también pueden ser atribuibles a las características genéticas propias de cada cepa, como lo han discutido otros investigadores (20). Adicionalmente, se notó una diferencia significativa en el recuento total de glóbulos rojos entre los animales de este estudio. Los valores de este parámetro fueron significativamente mayores para animales menores de 16 semanas que para los mayores, hecho que podría ser atribuido a la disminución de la capacidad hematopoyética de la médula ósea del adulto, en la que la médula celular activa, conocida como médula roja, se convierte en médula inactiva infiltrada con grasa, que se conoce como médula amarilla. Por lo tanto, ya no hay tanta actividad hematopoyética en la médula de las cavidades de los huesos largos, excepto en la porción superior del húmero y del fémur. De igual forma, lo anteriormente mencionado puede explicar el hecho de que se haya encontrado este mismo comportamiento en el recuento de plaquetas y en el recuento total de glóbulos blancos (21). Con respecto a las diferencias encontradas para las variables hematocrito (Hto. %), hemoglobina (Hb gr/dL) y recuento total de glóbulos rojos (RTGR 106/mm3), que se muestran significativamente mayores en los machos que en las hembras de este estudio, cabría mencionar que se puede atribuir este efecto a la testosterona y los esteroides androgénicos relacionados (22), que demostraron poseer acciones eritropoyéticas (23). Ha sido postulado que su mecanismo de acción se relaciona con un incremento de la producción renal de eritropoyetina o con un efecto directo sobre los progenitores celulares eritroides, ya que todo parece indicar que la testosterona, al menos parcialmente, estimula la eritropoyesis vía incremento de la producción renal de eritropoyetina (24). Sin embargo, este no sería el único mecanismo en juego. Ha sido también demostrado que los esteroides androgénicos actúan, aparentemente en forma directa, sobre los progenitores eritroides medulares, estimulando su proliferación (25). Por otra parte, las grandes diferencias encontradas en otra variable como el recuento total de glóbulos blancos podrían ser atribuidas a las condiciones de las barreras sanitarias en las cuales son mantenidas las dos colonias (22), ya que en el bioterio donde se aloja la colonia objeto de este estudio no se cuenta con sistema de filtrado de alta eficiencia (filtros HEPA o 50 filtros ULPA); el tamo utilizado como cama para los animales y el alimento no son esterilizados, el agua de bebida no recibe un tratamiento dentro del bioterio y no se mantienen separadas las salas de lavado de jaulas de la zona de mantenimiento de los biomodelos, condiciones que hacen que en este bioterio las cargas microbiológicas de hongos y bacterias sean altas, como se pudo demostrar (25). En consecuencia, podría decirse que un recuento total de glóbulos blancos elevado es quizá producto de la exposición constante de los biomodelos de este estudio a factores de riesgo de enfermedad, como bacterias, hongos, virus, parásitos, entre otros, que mantienen en permanente actividad los mecanismos involucrados con la respuesta inmune. Con respecto a otra variable que mostró diferencias altamente significativas, como lo fue el recuento plaquetario, podemos mencionar que no se puede afirmar que los animales objeto de este estudio son trombocitopénicos de manera patológica, debido a que una de las manifestaciones clínicas de este estado patológico es el sangrado anormal, el cual no se ha reportado en la colonia hasta el momento. Generalmente, la trombocitopenia aparece como consecuencia de los cuatro mecanismos siguientes: a) producción insuficiente; b) destrucción o utilización; c) distribución o almacenamiento inadecuados en el organismo (secuestro plaquetario) y d) pérdida acelerada (1). Pero sería imposible decir que los resultados arrojados por este estudio con respecto a la variable en discusión son producto de alguno de estos mecanismos, ya que la metodología y los objetivos del trabajo no estuvieron encaminados a esto. Además, puede considerarse nuevamente que dichas diferencias pueden estar siendo influenciadas por las características genéticas propias de la cepa. Es importante resaltar también que ninguno de los artículos citados contiene una discusión sobre esta variable. De hecho, el valor del recuento de plaquetas fue reportado sólo en dos investigaciones, incluyendo la referencia utilizada para comparar los datos de este estudio. Agradecimientos Los autores quieren agradecer a la Facultad de Medicina Veterinaria y Zootecnia de la Universidad Cooperativa de Colombia, al Laboratorio de Neurociencias y R e v i s ta S p e i D o m u s / v o l u m e n 6 / N Ú M E R O 1 2 / E NE R O - J UN I O D E L 2 0 1 0 R07 SpeiDomus No 12.indd 50 04/05/11 23:53 V íc to r H . A rc i l a Q., C a r l o s A . C o nde C ., Ja vi e r E . N i e to P., Fredy H . García P. Comportamiento de la Facultad de Salud UIS y a los señores Jesús María Rodríguez Hernández y Jesús Octavio Mantilla (encargados del bioterio UIS). Referencias 1. Arcila VH. Patología y diagnostico clínico en pequeños y grandes animales. Bogotá: Universidad Cooperativa de Colombia; 2005. 2. Benjamín M. Manual de patología clínica en veterinaria. México D.F.: Editorial Limusa; 1991. 3. Coles E. Diagnóstico y patología en veterinaria. 4.ª ed. México D.F.: Interamericana, McGraw-Hill; 1989. 4. Doxey DL. Patología clínica y procedimientos de diagnóstico en veterinaria. México D.F.: Editorial Manual Moderno; 1987. 5. González VE. Determinación de la hemoglobina, integración de tecnologías de la información y la comunicación a la docencia. Universidad de Antioquia [sitio de internet] [acceso mayo del 2009]. Disponible en: http://aprendeenlinea.udea.edu.co/lms/moodle/mod/ resourceview.php 6. Schalm OW, Jain NC, Carroll EJ. Hematología veterinaria. 1.ª ed. Buenos Aires: Editorial Hemisferio Sur, S.A.; 1981. 7. Conybeare G et ál. An Improved Simple Technique for the Collection of Blood Samples from Rats and Mice. Laboratory Animals. 1988; 22: 177-182. 8. Diehl K et ál. A Good Practice Guide to the Administration of Substances and Removal of Blood, Including Routes and Volumes. Journal of Applied Toxicology. 2001; 21: 15-23. 9. Herck H et ál. Blood Sampling from the Retro-Orbital Plexus, The Saphenous Vein and The Tail Vein in Rats: Comparative Effects on Selected Behavioural and Blood Variables. Laboratory Animals. 2001; 35: 131139. 10. Luzzi MB et ál. Collecting Blood from Rodents: a Discussion by the Laboratory Animal Refinement and Enrichment Forum, Animal Technology and Welfare. 2005; 4(2): 99-102. 11. Turtoni JA, Hawkey CM, Hart MG, Wynne J, Hicks RM. Age-Related Changes in the Haematology of Female F344 Rats. Laboratory Animals. 1989; 23: 295-301. 12. Van H et ál. Orbital Sinus Blood Sampling in Rats as Performed by Different Animal Technicians: the Influence of Technique and Expertise. Lab Anim. 1998; 32: 377-386. 13. Aleman CL et ál. Reference Database of the Main Physiological Parameters in Sprague-Dawley Rats from 6 to 32 Months. Laboratory Animals. 1998; 32: 457-466. 14. Schnell MA, Hardy C, Hawley M, Propert KJ, Wilson JM. Effect of Blood Collection Technique in Mice on Clinical Pathology Parameters, Human Gene Therapy. 2002; 13(1): 155-161. 15. Aleman CL et ál. Reference Data for the Principal Physiological Indicators in Three Species of Laboratory Animals. Laboratory Animals. 2000; 34: 379385. 16. Matsuzawa T, Nomura M, Unno T. Clinical Pathology Reference Ranges of Laboratory Animals. J. Vet. Med. Sci. 1993; Jun, 55(3): 351-62. 17. Wolford ST et ál. Reference Range Data Base for Serum Chemistry and Hematology Values in Laboratory Animals. J. Toxicol. Environ Health. 1986; 18(2): 161-88. 18. Archer RK, Festing MF, Riley J. Haematology of Conventionally-Maintained Lac: P Outbreed Wistar Rats During the 1st Year of Life. Laboratory Animals. 1982; 16: 198-200. 19. Haley TJ. Retrospective Analysis of Control Animal Data - the Rat. Clin. Toxicol. 1978; Feb., 12(2): 2492-63. 20. Lovell DP, Archer RK, Riley J, Morgan RK. Variation in Haematological Parameters among Inbred Strains of Rat. Laboratory Animals. 1981; 15: 243-249. 21. Ganong WF. Fisiología médica. 20ª ed. México D.F.: Editorial Manual Moderno; 2006. 22. Malgor LA, Fisher JW. Effects of Testosterone on Erythropoietin Production in Isolated Perfused Kidneys. Am. J. Physiol. 1970; 218: 1732-1736. 23. Malgor LA, Barrios L, Blanc CC. Effects of Testosterone on Bone Marrow Erythroid Cells of Normal and Nephrectomized Rats. Acta Physiol. Latinoam. 1975; 25: 179-187. 24. Fisher JW, Samuels AI, Malgor LA. Androgens and Erythropoiesis. Israel J. Med. Sci. 1971; 7: 892-900. 25. Malgor LA, Valsecia ME. Farmacología de la hematopoyesis [sitio en Internet] [acceso abril del 2009]. Disponible en: http://med.unne.edu.ar 26. Charles River Laboratories. Baseline Hematology and Clinical Chemistry Values for Charles River Wistar Rats (CRL: (WI) BR) as a Function of Sex and Age. Technical Bulletin. 1998 [sitio en Internet] [acceso marzo del 2009]. Disponible en: http://info.criver. com/research_models_and_services/research_models/rats_a_c.html VOLUMEN 6 / NÚMERO 12 / ENERO - JUNIO DEL 2010 / R07 SpeiDomus No 12.indd 51 R e v i s ta S p e i D o m u s 51 04/05/11 23:53