FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD
Anuncio

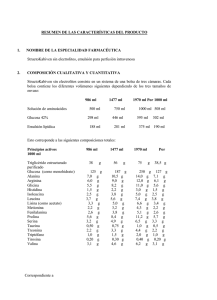
FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD FARMACÉUTICA StructoKabiven sin electrolitos, emulsión para perfusión intravenosa 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA StructoKabiven sin electrolitos consiste en un sistema de una bolsa de tres cámaras. Cada bolsa contiene los diferentes volúmenes siguientes dependiendo de los tres tamaños de envase: 986 ml 1477 ml 1970 ml Por 1000 ml Solución de aminoácidos 500 ml 750 ml 1000 ml 508 ml Glucosa 42% 298 ml 446 ml 595 ml 302 ml Emulsión lipídica 188 ml 281 ml 375 ml 190 ml Esto corresponde a las siguientes composiciones totales: Principios activos 986 ml 1477 ml 1970 ml Por 1000 ml Triglicérido estructurado purificado Glucosa (como monohidrato) Alanina Arginina Glicina Histidina Isoleucina Leucina Lisina (como acetato) Metionina Fenilalanina Prolina Serina Taurina Treonina Triptófano Tirosina Valina 38 g 56 g 75 g 38,5 g 125 7,0 6,0 5,5 1,5 2,5 3,7 3,3 2,2 2,6 5,6 3,2 0,50 2,2 1,0 0,20 3,1 g g g g g g g g g g g g g g g g g 187 10,5 9,0 8,2 2,2 3,8 5,6 5,0 3,2 3,8 8,4 4,9 0,75 3,3 1,5 0,30 4,6 g g g g g g g g g g g g g g g g g 250 14,0 12,0 11,0 3,0 5,0 7,4 6,6 4,3 5,1 11,2 6,5 1,0 4,4 2,0 0,40 6,2 g g g g g g g g g g g g g g g g g 127 7,1 6,1 5,6 1,5 2,5 3,8 3,4 2,2 2,6 5,7 3,3 0,5 2,2 1,0 0,20 3,1 Fresenius Kabi España, S.A. g g g g g g g g g g g g g g g g g www.fresenius-kabi.es Correspondiente a Acetato1) Fosfato2) Aminoácidos Nitrógeno Lípidos Carbohidratos - Glucosa (anhidra) • Contenido energético - total aprox. - no proteico aprox. • • • • • • 1 2 986 ml 1477 ml 73 mmol 110 mmol 2,8 mmol 4,2 mmol 50 g 75 g 8g 12 g 38 g 56 g 1970 ml 147 mmol 5,6 mmol 100 g 16 g 75 g Por 1000 ml 74,5 mmol 2,8 mmol 51 g 8 g 38 g 125 g 250 g 127 g 187 g 1100 kcal 870 kcal 1600 kcal 1300 kcal 2100 kcal 1735 kcal El aporte es procedente de la solución de aminoácidos El aporte es procedente de la emulsión lipídica Para consultar la lista completa de excipientes, ver la sección 6.1 “Lista de excipientes” 3. FORMA FARMACÉUTICA Emulsión para perfusión intravenosa Las soluciones de aminoácidos y de glucosa son transparentes, e incoloras o ligeramente amarillas y libres de partículas. La emulsión grasa es blanca y homogénea. • • • Osmolalidad aprox. 1610 mosmol/kg agua Osmolaridad aprox. 1340 mosmol/l pH aprox. 5,6 4. DATOS CLÍNICOS 4.1 Indicaciones terapéuticas Nutrición parenteral para pacientes adultos cuando la nutrición oral o enteral es imposible, insuficiente o está contraindicada. 4.2 Posología y método de administración La dosificación y velocidad de perfusión deberían establecerse en función de la capacidad para la eliminación de lípidos y para la metabolización de la glucosa. Ver la sección 4.4. “Advertencias y precauciones especiales de uso”. Dosificación La dosis debería ser individualizada teniendo en cuenta la situación clínica del paciente, peso corporal y requerimientos nutricionales. No se recomienda la utilización de StructoKabiven sin electrolitos en niños, ver la sección 4.4 “Advertencias y precauciones especiales de uso” Fresenius Kabi España, S.A. www.fresenius-kabi.es Los requerimientos de nitrógeno para el mantenimiento de la masa proteica corporal dependen de las condiciones del paciente (es decir, estado nutricional y grado de estrés catabólico). Los requerimientos son 0,10-0,15 g nitrógeno/kg peso corporal/día en un estado nutricional normal o en condiciones con un estrés metabólico leve. En pacientes con un estrés metabólico de moderado a alto, con o sin malnutrición, los requerimientos son del orden de 0,15-0,25 g nitrógeno/kg peso corporal/día (0,9-1,6 g aminoácidos/kg peso corporal/día). El rango de dosis de 0,10-0,25 g nitrógeno/kg peso corporal/día (0,6-1,6 g aminoácidos/kg peso corporal/día) cubre las necesidades de la mayoría de los pacientes y corresponde a 13 ml - 31 ml de StructoKabiven sin electrolitos/kg peso corporal/día. Para un paciente de 70 kg de peso corporal esto equivale a 910 ml – 2000 ml de StructoKabiven sin electrolitos por día. Los correspondientes requerimientos comúnmente aceptados son 2,0-6,0 g/kg peso corporal/día para la glucosa y 1,0-2,0 g/kg peso corporal/día para los lípidos. Los requerimientos de energía total, dependen de la situación clínica del paciente siendo lo más frecuente entre 20-30 kcal/kg peso corporal/día. En pacientes obesos la dosis debería basarse en el peso ideal estimado. StructoKabiven sin electrolitos está disponible en tres tamaños de envase dirigidos a pacientes con requerimientos nutricionales altos, moderadamente aumentados o basales. Para suministrar nutrición parenteral completa, adicionalmente deberían añadirse a StructoKabiven sin electrolitos, elementos traza, vitaminas y electrolitos. Velocidad de perfusión: La velocidad de perfusión máxima para la glucosa es 0,25 g/ kg / h, para los aminoácidos 0,1 g/ kg/ h y para los lípidos 0,15 g/ kg / h. La velocidad de perfusión no debe exceder 2,0 ml/ kg peso corporal/ h (correspondiente a 0,25 g de glucosa, 0,10 g de aminoácidos y 0,08 g de lípidos por kg peso corporal/hora). El período de perfusión recomendado es de 14-24 horas. Dosis máxima diaria: La dosis máxima diaria varía con la situación clínica del paciente e incluso puede cambiar día a día. La dosis máxima diaria recomendada es de 30 ml/ kg / día. Método y duración de la administración: Perfusión intravenosa en una vena central. 4.3 Contraindicaciones Hipersensibilidad a la proteína de huevo, de soja o de cacahuete, o a cualquiera de las sustancias activas o excipientes. Hiperlipemia grave Insuficiencia hepática grave Alteraciones graves de la coagulación sanguínea Defectos congénitos del metabolismo de los aminoácidos Insuficiencia renal grave sin posibilidad de hemofiltración o diálisis Shock agudo Hiperglicemia que requiere más de 6 unidades de insulina/h Contraindicaciones generales de una terapia de perfusión: edema pulmonar agudo, hiperhidratación, e insuficiencia cardíaca descompensada Deshidratación hipotónica Fresenius Kabi España, S.A. www.fresenius-kabi.es Síndrome hemofagocitótico. Condiciones inestables (por ejemplo, condiciones post-traumáticas graves, diabetes mellitus descompensada, infarto agudo de miocardio, acidosis metabólica, sepsis grave y coma hiperosmolar). 4.4 Advertencias y precauciones especiales de uso. La capacidad para la eliminación de lípidos debe ser monitorizada. Se recomienda que este control se realice mediante la determinación de los triglicéridos en suero, después de un período sin administrar lípidos de 5-6 horas. La concentración de triglicéridos en suero no debe exceder los 4 mmol/l cuando se inicie la perfusión. Para evitar riesgos asociados con velocidades de perfusión demasiado rápidas, se recomienda utilizar una perfusión continua y bien controlada, utilizando si es posible una bomba volumétrica. Las alteraciones del equilibrio de fluidos y electrolitos (por ejemplo, niveles séricos de electrolitos anormalmente elevados o bajos) deberían corregirse antes de iniciar la perfusión. Al comenzar una perfusión intravenosa debe realizarse una monitorización clínica especial. Si se produce cualquier signo anormal, debe detenerse la perfusión. Dado que el uso de una vena central está asociado a un elevado riesgo de infección, deben tomarse precauciones asépticas estrictas para evitar cualquier contaminación durante la inserción del catéter y la manipulación. StructoKabiven sin electrolitos debería administrarse con precaución en condiciones de metabolismo de lípidos alterado. Puede producirse hipertrigliceridemia en casos de insuficiencia renal, pancreatitis, alteración de la función hepática, hipotiroidismo y sepsis. Si se administra StructoKabiven sin electrolitos a pacientes en estas condiciones, es necesario monitorizar rigurosamente las concentraciones de los triglicéridos en suero. Cuando se administran lípidos durante un largo período de tiempo, deben monitorizarse el recuento sanguíneo celular y la coagulación. StructoKabiven sin electrolitos se fabrica prácticamente sin electrolitos para pacientes con unos requerimientos de electrolitos especiales y/o limitados. Se debe añadir sodio, potasio, calcio, magnesio y cantidades adicionales de fosfato en función de la situación clínica del paciente y de la monitorización constante de los niveles séricos. Deben monitorizarse la glucosa sérica, los electrolitos y la osmolaridad, así como el balance de fluidos, el equilibrio ácido-base y los tests de enzimas hepáticos (fosfatasa alcalina, ALT, AST). La nutrición parenteral debería administrarse con precaución en pacientes con acidosis láctica, aporte de oxígeno celular insuficiente y osmolaridad sérica incrementada. Ante cualquier signo o síntoma de reacción anafiláctica (como fiebre, escalofríos, erupción cutánea o disnea) debe interrumpirse inmediatamente la perfusión. Fresenius Kabi España, S.A. www.fresenius-kabi.es El contenido de lípidos de StructoKabiven sin electrolitos puede interferir con ciertas determinaciones de laboratorio (como bilirrubina, lactato deshidrogenasa, saturación de oxígeno, hemoglobina), si se toma la muestra de sangre antes de que los lípidos hayan sido adecuadamente eliminados del flujo sanguíneo. En la mayoría de los pacientes, los lípidos se eliminan después de un período de 5-6 horas sin administrar lípidos. Este producto contiene aceite de soja (que proviene de semillas de Glycine soja, Glycine max y Glycine hispida) y fosfolípidos de huevo, que muy raramente pueden causar reacciones alérgicas graves. Se han observado reacciones alérgicas cruzadas entre la soja y el cacahuete. La perfusión intravenosa de aminoácidos va acompañada de un aumento en la excreción urinaria de los elementos traza, particularmente cobre y zinc. Esto debería tenerse en cuenta en la dosificación de los elementos traza, especialmente durante una nutrición intravenosa de larga duración. En pacientes con malnutrición, el inicio de la nutrición parenteral puede ocasionar desplazamientos de fluidos dando lugar a edema pulmonar e insuficiencia cardíaca congestiva. Además, puede producirse una disminución en la concentración sérica de potasio, fósforo, magnesio y vitaminas hidrosolubles. Estos cambios pueden ocurrir en 24 a 48 horas, por lo tanto se recomienda iniciar la nutrición parenteral lentamente y con prudencia, junto con una rigurosa monitorización y con los ajustes apropiados de fluidos, electrolitos, minerales y vitaminas. StructoKabiven sin electrolitos no debería ser administrado simultáneamente con sangre en el mismo equipo de perfusión debido al riesgo de pseudoaglutinación En pacientes con hiperglicemia, podría ser necesaria la administración de insulina exógena. Debido a la composición de la solución de aminoácidos, StructoKabiven sin electrolitos no es adecuado para su utilización en recién nacidos o niños menores de 2 años. Hasta el momento no hay experiencia clínica sobre la utilización de StructoKabiven sin electrolitos en niños (de 2 a 11 años de edad). 4.5 Interacciones con otros medicamentos y otras formas de interacción Algunas especialidades farmacéuticas, como la insulina, pueden interaccionar en el organismo con la actividad de la lipasa. Sin embargo, esta interacción parece ser de limitada importancia clínica. La heparina administrada a dosis clínicas, produce una liberación transitoria de lipoproteinlipasa en la circulación. Esto provoca inicialmente un aumento de la lipolisis plasmática, seguida de una disminución transitoria en el aclaramiento de triglicéridos. Los triglicéridos estructurados purificados contienen aceite de soja que posee un componente natural, la vitamina K1. Sin embargo, la concentración en StructoKabiven sin electrolitos es tan baja que no se espera que tenga una influencia de consideración en el proceso de coagulación en pacientes que reciben derivados de la cumarina. Fresenius Kabi España, S.A. www.fresenius-kabi.es 4.6 Embarazo y lactancia No se dispone de datos clínicos sobre el uso de StructoKabiven sin electrolitos en mujeres embarazadas. No se han estudiado los efectos de StructoKabiven sin electrolitos sobre los fetos de animales más allá del periodo de organogénesis. La evaluación de los resultados en animales ha mostrado una toxicidad reproductiva después de la administración de Structolipid (ver la sección 5.3). La relevancia clínica de este dato no se conoce. StructoKabiven sin electrolitos se debe utilizar durante el embarazo sólo después de una especial consideración. No hay experiencia clínica disponible sobre su utilización durante el periodo de lactancia. Las mujeres tratadas con StructoKabiven sin electrolitos no deben estar en periodo de lactancia. 4.7 Efectos sobre la capacidad de conducir y utilizar máquinas. No aplicable 4.8 Reacciones adversas Poco frecuentes ≥ 1/1.000, < 1/100 Trastornos cardíacos Trastornos respiratorios y mediastínicos Trastornos gastrointestinales Trastornos del metabolismo y de la nutrición Trastornos vasculares Trastornos generales y alteraciones del lugar de administración Raras ≥1/10.000,<1/1.000 Taquicardia Muy raras < 1/ 10.000 Síntomas respiratorios Diarrea Niveles plasmáticos elevados de enzimas hepáticos, cuerpos cetónicos y triglicéridos Hipertensión Náuseas, cefalea, aumento de la temperatura corporal Erupción cutánea, dolor en la espalda, mareo Síndrome de sobrecarga lipídica Una alteración en la capacidad de eliminación de StructoKabiven sin electrolitos, puede dar lugar a un síndrome de sobrecarga lipídica como consecuencia de una sobredosificación, pero también puede ocurrir en casos de utilización a la velocidad de perfusión recomendada asociada con un cambio repentino de la situación clínica del paciente, como un deterioro grave de la función renal o infección. El síndrome de sobrecarga lipídica se caracteriza por hiperlipemia, fiebre, infiltración grasa, hepatomegalia, esplenomegalia, anemia, leucopenia, trombocitopenia, alteraciones de la coagulación y coma. Todos los síntomas son normalmente reversibles siempre que se interrumpa la perfusión. Fresenius Kabi España, S.A. www.fresenius-kabi.es Exceso de perfusión de aminoácidos Como con otras soluciones de aminoácidos, el contenido de aminoácidos en StructoKabiven sin electrolitos puede causar reacciones adversas cuando se excede la velocidad de perfusión recomendada. Estos efectos son náuseas, vómitos, escalofríos y sudoración. La perfusión de aminoácidos también puede causar un aumento de la temperatura corporal. Con una función renal alterada, pueden aumentar los niveles de productos que contienen nitrógeno (p.e. creatinina, urea). Exceso de perfusión de glucosa Si se excede la capacidad de eliminación de la glucosa del paciente, se desarrollará hiperglicemia. 4.9 Sobredosis Ver la sección 4.8 “Síndrome de sobrecarga lipídica”, “Exceso de perfusión de aminoácidos” y “Exceso de perfusión de glucosa”. Si se producen síntomas de sobredosis de lípidos o aminoácidos, la perfusión debe ser reducida o interrumpida. No hay un antídoto específico para la sobredosis. Los procedimientos de emergencia deben ser medidas de apoyo generales, con particular atención al sistema respiratorio y cardiovascular. Sería esencial una rigurosa monitorización bioquímica y un tratamiento adecuado de anomalías específicas. Si se produce hiperglicemia, se debe tratar de acuerdo a la situación clínica mediante una adecuada administración de insulina y/o ajuste de la velocidad de perfusión. Además, una sobredosis podría causar una sobrecarga de fluidos, desequilibrio electrolítico e hiperosmolalidad. En algunos casos aislados graves, puede ser necesaria la hemodiálisis, hemofiltración o hemo-diafiltración. 5. PROPIEDADES FARMACOLÓGICAS. 5.1 Propiedades farmacodinámicas Grupo farmacoterapéutico: Soluciones i.v. para nutrición parenteral Código ATC: B05BA10 Emulsión grasa Structolipid, emulsión grasa utilizada en StructoKabiven sin electrolitos, proporciona ácidos grasos esenciales y no-esenciales, de cadena larga y cadena media, importantes para el metabolismo energético y para la integridad estructural de las membranas celulares. Structolipid a las dosis recomendadas no produce cambios hemodinámicos. No se han descrito cambios clínicamente significativos en la función pulmonar, cuando se utiliza Structolipid correctamente. El aumento transitorio de los enzimas hepáticos observado en algunos pacientes con nutrición parenteral es reversible y desaparece cuando la nutrición parenteral se interrumpe. Se han detectado alteraciones similares en nutrición parenteral sin administración de emulsiones grasas. Fresenius Kabi España, S.A. www.fresenius-kabi.es Aminoácidos Los aminoácidos, constituyentes de las proteínas en la alimentación habitual, se utilizan para la síntesis de proteínas de los tejidos y algún excedente es canalizado hacia varias vías metabólicas. Diferentes estudios han mostrado un efecto termogénico de la perfusión de aminoácidos. Glucosa La glucosa no tiene efectos farmacodinámicos aparte de contribuir a completar o mantener el estado nutricional normal. 5.2 Propiedades farmacocinéticas Emulsión grasa Structolipid tiene propiedades biológicas similares a las de los quilomicrones endógenos. A diferencia de los quilomicrones, Structolipid no contiene ésteres de colesterol o apolipoproteínas, mientras que su contenido en fosfolípidos es significativamente más elevado. Structolipid es eliminado de la circulación por rutas similares a las de los quilomicrones endógenos. Las partículas lipídicas exógenas son primeramente hidrolizadas en la circulación y recogidas por los receptores LDL tanto periféricamente como en el hígado. La tasa de eliminación es determinada por la composición de las partículas lipídicas, el estado nutricional y clínico del paciente y la velocidad de perfusión. En voluntarios sanos, la tasa máxima de aclaramiento de Structolipid después del ayuno durante una noche es más rápida que en el caso de emulsiones que contienen sólo triglicéridos con ácidos grasos de cadena larga. Tanto las velocidades de eliminación como de oxidación son dependientes de las condiciones clínicas del paciente. La eliminación es más rápida y la utilización se aumenta en pacientes de postoperatorio y en traumas, mientras que los pacientes con insuficiencia renal e hipertrigliceridemia muestran una menor utilización de las emulsiones grasas exógenas. Aminoácidos Las principales propiedades farmacocinéticas de los aminoácidos perfundidos, son esencialmente las mismas que las de los aminoácidos que provienen de la alimentación habitual. Sin embargo, los aminoácidos de las proteínas de la dieta entran primero en la vena porta y después en el sistema circulatorio, mientras que los aminoácidos perfundidos intravenosamente alcanzan la circulación sistémica directamente. Glucosa Las propiedades farmacocinéticas de la glucosa infundida, son esencialmente las mismas que las de la glucosa que proviene de la alimentación habitual. 5.3 Datos de seguridad preclínica. No se han realizado estudios de seguridad preclínica con StructoKabiven sin electrolitos. Sin embargo, resultados preclínicos de Structolipid así como de soluciones de aminoácidos y glucosa de diferentes composiciones y concentraciones no demuestran un riesgo especial en humanos en base a estudios convencionales de seguridad farmacológica, toxicidad por dosis repetidas y genotoxicidad. Fresenius Kabi España, S.A. www.fresenius-kabi.es No se ha evaluado el potencial carcinogénico de Structolipid. No fue evidente una teratogenicidad o embriotoxicidad potencial en conejos después de la perfusión de Structolipid a dosis de 3 g/kg/día de triglicéridos (TG) (0,75 g TG/kg/h) durante 4 horas. A una dosis de 4,5 g TG/kg/día (1,12 g TG/kg/h) se observó un posible efecto embriotóxico debido a un ligero aumento en la pérdida embrionaria/fetal. La dosis y velocidad de perfusión fue 3 y 7 veces mayor, respectivamente, de la recomendada para el uso clínico. 6. DATOS FARMACÉUTICOS 6.1 Lista de excipientes Fosfolípidos purificados de huevo Glicerol Hidróxido sódico (para ajuste del pH) Ácido acético glacial (para ajuste del pH) Ácido clorhídrico 1M (para ajuste del pH) Agua para inyección 6.2 Incompatibilidades Este producto no debe ser mezclado con otros productos medicinales excepto aquellos mencionados en la sección 6.6. 6.3 Periodo de validez Caducidad del producto en el envase para la venta 2 años Ca d uc i da d de s pu é s d e m e zc la r Se ha demostrado una estabilidad química y física de la bolsa de tres cámaras mezclada lista para su uso durante 36 horas a 25°C. Desde un punto de vista microbiológico, el producto se debe utilizar inmediatamente. Si no se utiliza inmediatamente, el tiempo de conservación hasta su utilización y las condiciones previas a su uso son responsabilidad del usuario y normalmente no deberían ser superiores a 24 horas a 2 – 8º C. Ca d uc i da d de s pu é s d e la m e zc l a c on a d it i v o s Ver en la sección 6.6. ”Precauciones especiales para la eliminación y otras manipulaciones” la estabilidad química y física de la bolsa lista para su uso. Desde un punto de vista microbiológico, el producto se debe utilizar inmediatamente después de realizar las adiciones. Si no se utiliza inmediatamente, el tiempo de conservación hasta su utilización y las condiciones previas a su uso son responsabilidad del usuario y normalmente no deberían ser superiores a 24 horas a 2 – 8º C. 6.4 Precauciones especiales de almacenamiento No conservar por encima de 25ºC. No congelar. Mantener en la sobrebolsa. Para condiciones de almacenamiento del producto medicinal reconstituido, ver la sección 6.3. Fresenius Kabi España, S.A. www.fresenius-kabi.es 6.5 Naturaleza y contenido de los envases El envase consiste en una bolsa interna multicámara y una sobrebolsa. La bolsa interna está separada en tres cámaras por soldaduras tipo peel (de fácil apertura). Entre la bolsa interna y la sobrebolsa, se coloca un absorbente de oxígeno La bolsa interna está fabricada con un material polímero multicapa denominado Excel o alternativamente Biofine. El film de la bolsa interna Excel consta de tres capas. La capa interna está fabricada con un copolímero poli(propileno/etileno) y un elastómero termoplástico estireno/etileno/butileno/estireno (SEBS). La capa intermedia es de SEBS y la capa externa consiste en un copoliéster-éter. El port de infusión está equipado con una cápsula de poliolefina. El port de adición lleva un tapón de poli-isopreno sintético (libre de látex). El film de la bolsa interna Biofine está fabricado con poli(propileno-co-etileno), caucho sintético poli[estireno-block-(butileno-co-etileno)] (SEBS) y caucho sintético poli(estirenoblock-isopreno) (SIS). Los ports de infusión y adición están fabricados de polipropileno y caucho sintético poli [estireno-block-(butileno-co-etileno)] (SEBS), equipados con tapones de poli-isopreno sintético (libre de látex). El port sin salida, el cual sólo se utiliza durante la producción, está fabricado de polipropileno y lleva un tapón de poli-isopreno sintético (libre de látex). Presentaciones: 1 x 986 ml, 4 x 986 ml 1 x 1.477 ml, 4 x 1.477 ml 1 x 1.970 ml, 4 x 1.970 ml Puede que solamente estén comercializados algunos tamaños de envases. 6.6 ”Precauciones especiales para la eliminación y otras manipulaciones” No utilizar el envase si no está intacto. Utilizar sólo si las soluciones de aminoácidos y glucosa son transparentes, e incoloras o ligeramente amarillas y la emulsión grasa es blanca y homogénea. Antes de utilizar, debe mezclarse el contenido de las tres cámaras separadas. Después de la apertura de las soldaduras tipo peel (de fácil apertura), la bolsa debe ser invertida varias veces para asegurar una mezcla homogénea, que no muestre ninguna evidencia de una separación de las fases. Conservación después de la mezcla con aditivos Después de la apertura de las soldaduras tipo peel y de haber realizado la mezcla de las tres soluciones, las adiciones deben ser realizadas a través del port de adición. Com pat ibilidad Sólo pueden añadirse a StructoKabiven sin electrolitos, soluciones medicinales o nutricionales cuya compatibilidad haya sido comprobada. La compatibilidad para los diferentes aditivos y tiempos de conservación de diferentes mezclas puede facilitarse bajo petición. Fresenius Kabi España, S.A. www.fresenius-kabi.es Para un solo uso. Se debe realizar la adición asépticamente. Debe rechazarse cualquier mezcla sobrante después de la perfusión. 7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN FRESENIUS KABI AB Rapsgatan 7, 751 74 Uppsala Suecia 8. NÚMERO DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN 65.830 9. FECHA DE LA PRIMERA AUTORIZACIÓN/REVALIDACIÓN DE LA AUTORIZACIÓN Fecha de autorización: Enero 2004 Fecha de revalidación: 16 octubre 2007 Fresenius Kabi España, S.A. www.fresenius-kabi.es 10. FECHA DE REVISIÓN (PARCIAL) DEL TEXTO Mayo 2008 Fresenius Kabi España, S.A. www.fresenius-kabi.es