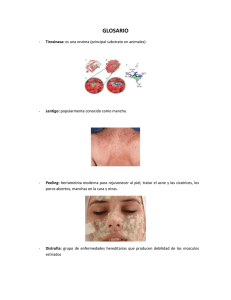
VERRUGAS GENITALES
Anuncio

Verrugas genitales EDUCACIÓN CONTINUA Prof. Dr. M. A. Allevato, Dra. L. Donatti Act Terap Dermatol 2005; 28: 302 VERRUGAS GENITALES Prof. Dr. Miguel Angel J. Allevato, Dra. Lucila B. Donatti Las verrugas genitales o anogenitales (condilomas acuminados, verruga venérea, papiloma venéreo) son lesiones benignas de la piel y de las mucosas, que resultan de la proliferación de queratinocitos infectados por el virus del papiloma humano, predominantemente HPV tipos 6 y 11. La prevalencia de las verrugas genitales se está incrementando globalmente y está estimada en cerca del 1% de la población sexualmente activa. Una variedad de opciones terapéuticas están disponibles pero muy pocas han sido evaluadas en estudios randomizados y controlados con placebo; no obstante los datos disponibles indican que muchos tratamientos resuelven las lesiones entre 1-6 meses pero las tasas de recurrencias son altas. EPIDEMIOLOGÍA La infección por HPV es muy frecuente en el mundo, sin distinción de razas ni grupos socioeconómicos. Según un estudio publicado en Dinamarca el 17% de las mujeres entre 20 y 29 años, que han tenido al menos una pareja sexual en el año previo, tiene verrugas genitales. En el Reino Unido de Gran Bretaña, en el 2002, fueron diagnosticados cerca de 70.000 nuevos casos , de los cuales el 53% fueron hombres.1 Un reporte de los EEUU señala 1,7 casos por cada 1000 personas/año, con predominio en las mujeres entre los 20 y 24 años (6,2/1000) y varones entre 25 y 29 años (5,0/1000). La tasa de nuevos casos aumentó de 117,8 en 1998 a 205,0 en 2001.2,3 Según un relevamiento realizado en Canadá, en los jóvenes es frecuente la infección incidental, llegándose a cifras de 25% entre los 15 y 19 años; las mujeres son las más afectadas: 1,4:1.4 La alta prevalencia de HPV en poblaciones asintomáticas de los Estados Unidos la señala como la enfermedad de transmisión sexual más frecuente. Un estudio llevado a cabo por el Instituto Nacional de Enfermedades Alérgicas e Infecciosas (NIAID) revela que el 50% de las mujeres infectadas no padecen síntomas4, a. La prevalencia es mayor aún entre los pacientes HIV+, alcanzando un 40% entre los varones homosexuales portadores.5 La Asociación Americana de Salud Socialb señala la existencia de, aproximadamente, 5,5 millones de nuevos casos cada año; reconociendo la existencia de al menos 20 millones de infectados. Un dato importante4 es que el ginecólogo/obstetra es el especialista a quien más consultan por verrugas genitales (67%) seguido por el dermatólogo (14%) y el urólogo (11%). ETIOPATOGENIA Hasta mediados del siglo XIX las verrugas genitales se consideraban una forma de sífilis o gonorrea. La etiología viral se estableció en 1907.6 Las verrugas anogenitales son el resultado de la infección por el virus del papiloma humano , predominando los HPV tipos 6 y 11 los cuales se consideran de bajo riesgo para la transformación maligna; no obstante es común la infección con múltiples tipos de HPV , de bajo y alto riesgo.7 El HPV invade las células de la capa basal de la epidermis y, tras un período de latencia variable de meses a años, produce las partículas virales desarrollándose la característica coilocitosis. Se estima que tres meses después del contacto con una persona infectada los dos tercios de las personas desarrollan lesiones. Las células blanco son los queratinocitos pero no tiene acción citolítica por lo cual el antígeno puede no ser expuesto a la acción de la célula presentadora de antígenos; tampoco tiene fase sistémica lo cual reduce el potencial antigénico.8 No existe inflamación asociada a la fase de replicación. El sistema inmunológico del huésped es poco estimulado y por ende la respuesta del sistema inmune celular, necesaria para eliminar las células infectadas, demora meses en desarrollarse; no obstante existe la regresión espontánea y el estudio histológico revela un infiltrado de linfocitos T CD4.9 remitir espontáneamente en 1 a 2 años confiriendo inmunidad duradera contra el subtipo específico.2,3 TRANSMISIÓN - Contacto sexual. - Sexo oral. - Vertical madre-hijo. - Auto inoculación. - Fomites. CLÍNICA Si bien se la considera una enfermedad de transmisión sexual, cualquier clase de contacto genito-genital puede implicar un riesgo de transmisión del virus. Las lesiones pueden verse, también, en laringe, orofaringe y tráquea. Son frecuentes las lesiones múltiples y el compromiso de más de un área. Las verrugas genitales o anogenitales o condilomas acuminados son proliferaciones epidérmicas que se observan como elementos papilomatosos, vegetantes, blandos, cuyo extremo libre presenta una serie de digitaciones que le han valido la denominación de "cresta de gallo"; estas prolongaciones filiformes en su conjunto recuerdan a una coliflor, son sésiles o pediculadas, tienen color rosado o rojo, secas o húmedas, si están en los pliegues; se reúnen en placas de tamaño considerable, que en la zona anogenital, por frote y maceración, desprenden olor fétido. La condición de infección latente y subclínica imposibilita la prevención. Tampoco existe un tratamiento erradicador efectivo, aunque la infección suele Usualmente se producen en superficies sujetas al trauma del coito tales como el frenillo, el surco de la corona del glande, el prepucio y en labios y TRANSMISIÓN Y CONTAGIO EDUCACIÓN CONTINUA horquilla de la vulva. Las anales y perianales suelen ser más frecuentes en hombres homosexuales. Estas lesiones son con frecuencia asintomáticas aunque pueden ocasionar disconfort,incluyendo inflamación, fisuras , prurito y dispareunia , o sangrado.1, 10,11 Son percibidas por el paciente como inaceptables cosméticamente y puede causar perturbación psicológica, ansiedad, miedo y pérdida de la autoestima.10 ASPECTO CLÍNICO • Lesiones únicas o múltiples. • Lesiones verruciformes o en placa • Superficie lisa, verrugosa o lobulada. • Eritema o hiperpigmentación. • Localización múltiple externas o internas: meato uretral, cuello uterino. blot) y la PCR. La diferencia entre dos tipos se define como, al menos, un 50% de diferencia en el ADN. Estos métodos también pueden detectar infección latente. Otros métodos incluyen el test de ELISA para detectar IgG contra el HPV16. También están disponibles pruebas de alta sensibilidad y especificidad como el Virapap, ThinPrep Pap y Hybrid capture II. Estudio histopatológico La biopsia se reserva para las lesiones pigmentadas, induradas o fijas de diagnóstico poco claro; y a los casos resistentes al tratamiento o que empeoran a pesar de él. Ambas situaciones implican la necesidad de descartar una displasia con riesgo de progresión a neoplasia maligna. Exámenes complementarios DIAGNÓSTICO El reconocimiento es clínico y no se requieren exámenes complementarios. Acido acético La prueba del ácido acético es sencilla y puede realizarse en el consultorio, con resultados inmediatos. Las lesiones visibles y la zona se cubren con una gasa embebida en ácido acético al 3-5%, durante 5 a 10 minutos, lo que facilita su detección, sobre todo con el colposcopio, aunque el diagnóstico no debe basarse exclusivamente en la observación de lesiones blancas, dado que pueden representar falsos positivos. Tipificación Los cultivos no proveen resultados consistentes. La tipificación es acorde al genotipo el cual se determina mediante pruebas de hibridización (Southern En las mujeres se recomienda realizar un Pap. Asimismo se sugiere investigar la presencia de otras ETS. Siempre examinar a la pareja sexual. DIAGNÓSTICOS DIFERENCIALES • Enfermedad de Darier • Enfermedad de Hailey-Hailey • Neoplasia • Nevo • Pápulas peneanas perladas • Neurofibromatosis vulvar • Papila vulvar vestibular • Papilomatosis laríngea (infantes y neonatos) TRATAMIENTO El objetivo terapéutico es eliminar las verrugas sintomáticas e inducir períodos libres de lesiones. No obstante, hasta el momento, no existen evidencias de que algún tratamiento logre erradicar el virus o modificar su historia natural. Además, eliminar las lesiones no reduce la infectividad. El tratamiento óptimo sería aquel capaz de inducir una respuesta inmunológica del huésped virus-específica a través de la producción de una reacción local inflamatoria con liberación de citoquinas. En lo que respecta al manejo de las verrugas genitales o anogenitales la modalidad seleccionada depende del caso en particular -tamaño, número, localización y morfología-, y es aconsejable cambiarla en caso de que no resulte eficaz al cabo de tres ciclos de tratamiento12. Libradas a su evolución natural, las verrugas suelen involucionar espontáneamente. Se ha sugerido una relación entre la remisión espontánea y una activación de la respuesta inmunitaria mediada por células5. Otras lesiones pueden aumentar de tamaño o número. Una amplia variedad de tratamientos están disponibles para las verrugas genitales; no obstante pocos han sido adecuadamente evaluados a través de estudios randomizados, controlados con pla- cebo; los comparativos entre diversas modalidades son también escasos al mismo tiempo que la eficacia relativa es dificil de determinar; las posibilidades de exito en la eliminación de lesiones así como la duración del tratamiento y los índices de recurrencia dependen de varios factores incluyendo el sitio, el tipo y la extensión de las verrugas, así como de la modalidad terapéutica empleada.1 La modalidad más apropiada para el tratamiento de las verrugas genitales variará de paciente en paciente y de acuerdo a la experiencia del profesional actuante y la disponibilidad de la terapéutica. Los tratamientos pueden ser clasificados como aquellos administrados por el profesional en su consultorio o los que se aplica el mismo paciente y hay que tener en consideración las preferencias del paciente al respecto, dado que algunos eligen la privacidad y conveniencia de la autoaplicación, mientras que otros pueden no sentirse a gusto o capaces de realizarse el tratamiento a sí mismo.1 TRATAMIENTO EN CONSULTORIO Acido tricloroacético El ácido tricloroacético (TCA) es un queratolítico con acción cáustica sobre la piel y las mucosas. Destruye las verrugas por coagulación química de las proteínas celulares lo que resulta en necrosis tisular.1 Se aplica en concentraciones que varían desde el 50 % a la saturación; se coloca sobre las lesiones con pincel o hisopo, en capas finas hasta que se forme una escara blanquecina. El ardor asociado se alivia con bicarbonato de sodio o agua fría.Puede colocarse sobre piel, semimucosas o mucosas variando la concentración de acuerdo con la zona. Las aplicaciones deben reiterarse, cada 1 a 2 semanas por un promedio de seis sesiones, aunque la ausencia de efecto visible en la 3º aplicación requiere un replanteamiento del diagnóstico y el tratamiento. Se obtiene una resolución entre el 60 al 80 % y son frecuentes las recurrencias (alrededor del 40%). Puede asociarse al podofilino, colocando primero el TCA, para mejorar los resultados. sionadas ni ulceradas y se desaconseja su uso en lesiones grandes. Se puede indicar en poblaciones pediátricas, pero se debe ser cauto. El uso de podofilina está contraindicado en embarazadas (es teratogénico), y en pacientes con hipersensibilidad, diabéticos, zonas con deterioro de la circulación, mucosas, ojos. Como secuelas, hipo/hiperpigmentación e incluso cicatrices siguiendo a erosiones y exulceraciones. Interferón No debe aplicarse sobre lesiones premalignas o malignas. El tratamiento con TCA es recomendable en embarazadas2 y en niños.13 potencial antiviral, antitumor y actividad inmunomoduladora. Se trata de un producto manufacturado empleando tecnología de recombinación de ADN. 2,3,a,b,c Podofilina La resina de podofilina sigue siendo de gran utilidad pese a algunas desventajas (irritación, necrosis). Se usa en concentraciones entre el 25-50% en etanol, que aumenta la penetración de la droga, o en tintura de benjui compuesta que mejora la permanencia del producto sobre la lesión.13 El agente activo, la podofilotoxina, actúa como citotóxico inhibiendo las mitosis en metafase. En sus lineamientos de 2002 el Centro de Control de Enfermedades (CDC) de Estados Unidos recomienda la podofilina aplicada en consultorio2, c Se aplica una pequeña cantidad sobre cada verruga, con la precaución de no contactar con piel sana, y se deja secar al aire. Unas 4 horas más tarde se enjuaga la zona con agua para evitar irritación local y efectos tóxicos por absorción sistémica. Se deben realizar 1 a 2 aplicaciones semanales por tres semanas y, solamente en caso de observarse respuesta positiva, continuar hasta la desaparición de las lesiones. La tasa de curación se reporta entre un 20 a 50% y las recurrencias oscilan entre el 20 al 60%. Únicamente debe aplicarse sobre lesiones intactas, no ero- El interferón (INF) es una proteína con La FDA ha aprobado las inyecciones intralesionales de INF-alfa-n3 para tratar las verrugas genitales refractarias al tratamiento convencional. El esquema terapéutico consiste en 250.000 UI (0,05 ml) en la base de cada verruga con una aguja de 30; dos veces a la semana hasta un máximo de 8 semanas, sin exceder los 2,5 millones UI por sesión de tratamiento. Otro de los esquemas sugiere inyectar 0,1 ml de un preparado de 10.000 U en 1 ml de diluyente, en cada lesión, tres veces por semana por 3 semanas. EDUCACIÓN CONTINUA En verrugas grandes puede aplicarse INF en varios puntos de la base hasta un total de 0,05 ml por verruga. La tasa de recurrencia alcanza el 20 a 40%. Entre sus desventajas se mencionan el costo y los efectos adversos sistémicos -fiebre, mialgias, síntomas gripales, dislipidemia, alteraciones de las series hematológicas-. No debe administrarse combinado con IL-2, teofilina, cimetidina, zidovudina y vinblastina por riesgo de toxicidad sistémica. dos, controlados con placebo, no obstante en un estudio comparativo ésta mostró mayores tasas de limpieza de lesiones que el podofilino (79% vs 41%) 14 ; en relación a la electrocirugía hay datos controversiales, Simmons y col no encontaron diferencias significativas mientras que Stone reportó un mayor éxito con la electrocirugía14,15; otros ensayos no mostraron diferencias significativas entre TCA y criocirugía después de 6 a 10 meses de tratamiento.16 Crioterapia Es efectiva en cualquier localización (aún periorificial), en lesiones de diversos tamaños y aún en niños y en embarazadas está contraindicada en vagina por el riesgo de perforación.2,13 Esta modalidad requiere un buen entrenamiento para lograr los mejores resultados sin secuelas. El criógeno más empleado es el nitrógeno líquido que se puede aplicar con la técnica de spray o con un hisopo de algodón . La metodología más efectiva es la de congelacióndescongelación-congelación. Se congelan las lesiones y unos pocos milímetros por fuera, por 15 a 20 segundos, a veces se requiere más tiempo, incluso hasta 1 minuto; las aplicaciones se pueden repetir cada 1 o 2 semanas pero la falta de respuesta en la 3º sesión requiere un replanteamiento del manejo diagnóstico- terapéutico. La crioterapia actuaría no sólo destruyendo las lesiones por criocitolisis sino estimulando la respuesta inmune en el área.13 La tasa de respuesta es alta (7090%), las secuelas escasas y las recidivas se dan en alrededor del 25%. Los resultados no son buenos cuando se tratan lesiones rectales. Entre las reacciones adversas se describe dolor, erosión, ulceraciones e hipopigmentación posinflamatoria. La eficacia de la criocirugía no ha sido evaluada en estudios randomiza- Cirugía La excisión quirúrgica usando bisturí, curetaje o tijeras remueve directamente las verrugas permitiendo además el estudio histopatológico de la pieza. Láser El láser de dióxido de carbono se indica para tratar lesiones extensas primarias o recurrentes; requiere anestesia local, regional o general. Se han reportado tasas de curación de hasta el 91%. Se lo recomienda como terapia de elección en embarazadas con lesiones extensas o que no responden al TCA. No obstante se han descrito casos de infectividad asociada al tratamiento habiéndose constatado la presencia de HPV en la pluma del láser. El láser pulsado se ha usado con tasas variables de éxito.2,12 TRATAMIENTO DOMICILIARIO Este procedimiento es muy útil para un número pequeño de lesiones queratinizadas de fácil acceso; pero en especial para las lesiones del canal anal e intrauretral; su efectividad es muy alta.1,13 Las recurrencias han sido estimadas en alrededor de un 20%. El tratamiento de las lesiones puede ser aplicado por el mismo paciente lo que facilita el cumplimiento y le evita la reiteración de visitas al consultorio. Pero se requiere una adecuada comprensión del esquema terapéutico. La mayor ventaja es que el paciente se libra de sus lesiones en una sola visita a su médico; y por ende es más satisfactoria que otras terapéuticas, aunque tiene algunos efectos adversos como posible cicatriz y sangrado; se hace con anestesia. Podofilotoxina Electrocirugía Si bien la electrodesecación puede ser usada, la técnica más común es la excisión eléctrica con asa por la cual la lesión es removida por la inserción de un pequeño electrodo en la dermis superficial. De acuerdo con algunas publicaciones los índices de eliminacion de lesiones son altos: 60-90% de los pacientes después de 3-6 semanas, y ha demostrado ser dos veces más efectiva que el podofilino y la criocirugía y similar al láser CO2.14,17 Consiste en un preparado de podofilina químicamente sintetizada o aislada y purificada de especies coníferas (Juniperus y Podophyllum), presentada al 0,15% en crema y al 0.5% en gel o solución, que se aplica con hisopo, dos veces al día durante tres días consecutivos con un período de descanso de 4 días; los ciclos deben reiterarse por 4 semanas.2 Se debe advertir al paciente que no tiene que aplicar el preparado sobre las lesiones ulceradas y no debe exceder los 0.5 ml/dl de solución ó 0,5 gramos de gel al día por área de 10 cm2 para evitar efectos sistémicos. Su efectividad ha sido demostrada en una variedad de estudios randomizados, doble ciego, contra placebo en los cuales las tasas de eliminación de lesiones han ido del 37 al 91% al final de por lo menos 4 ciclos; es en general considerada como más útil para verrugas blandas no queratinizadas.1 Hay pocos datos disponibles acerca de si la sustancia tiene algún efecto sobre la carga viral o la expresión génica viral.1 Los efectos adversos más frecuentes son sensación de quemazón, prurito, dolor, inflamación, erosión y sangrado. Imiquimod El imiquimod es una imidazoquinolina que actúa como modificador de la respuesta inmunológica estimulando la síntesis y liberación de citoquinas y quemoquinas (INF-alfa) y factor de necrosis tumoral (TNF) derivadas de macrófagos y monocitos, con activación de linfocitos Th1. Tiene actividad antiviral y antitumoral. Fue aprobado por la FDA en 1997 para tratar las verrugas genitales externas y perianales en pacientes inmunocompetentes.9,18 Se utiliza en crema al 5% que el paciente aplica por la noche, en una capa fina, tres veces por semana durante 16 semanas. Por la mañana, el remanente debe removerse con agua y jabón. 2 El beneficio del imiquimod comienza a hacerse aparente a partir de la 8º semana observándose tasas de aclaramiento completo del 37 a 70% (56% ).7,19. Y las recurrencias aproximadamente del 15% .La respuesta clínica se acompaña de disminución del ADN y el ARNm del HPV para E7 y L1.5, 9 quiera de estas complicaciones. No se recomienda su uso en mujeres gestantes ni para tratar lesiones internas (rectales, vaginales, uretrales)12. las lesiones en el 60% y una menor tasa de recurrencias, comparada con la electrocoagulación.21 Los efectos adversos reportados fueron dolor leve asociado a dermatitis erosiva. OTRAS OPCIONES El producto se aplica únicamente a lesiones externas y visibles, por 5 días consecutivos con una permanencia de 5 horas cada día, y remoción posterior con agua y jabón. Los ciclos se repiten con intervalos de 1 semana por un total de 18 semanas. 5- Fluorouracilo (5-FU) El 5- fluorouracilo se emplea en preparaciones de crema al 3-5% en 1 a 2 aplicaciones por semana, por 10 semanas o en crema al 1%, dos veces a la semana por 2 a 6 semanas; se debe remover luego de 8 hs de aplicado. Las tasas de curación son variables (1090%), con bajas recurrencias. Se lo menciona como alternativa para las verrugas vaginales con un aplicador, el cual debe llenarse hasta un tercio con una crema de 5-FU al 5%, 1 a 2 veces a la semana por 10 semanas consecutivas. La vulva y la uretra deben protegerse con vaselina y colocarse un tampón para evitar la irritación del introito. Es en general mal tolerado dada la frecuencia de efectos adversos locales (irritación, ardor, dolor, erosiones, edema). No obstante se emplea para prevenir las recurrencias en pacientes inmunocomprometidos durante las 4 semanas subsiguientes a la ablación de las lesiones.2,12 Está contraindicado en embarazadas. En un estudio reciente se lo ha encontrado útil en aplicación intralesional al 5% (administrado por el médico en consultorio).20 Interferones Pueden usarse en forma tópica pero son muy poco efectivos, la inyección intralesional da resultados variables y los estudios de su administración sistémica, no exenta de efectos indeseables, no son concluyentes.13 Retinoides La isotretinoína a 1 mg/kg/día se ha usado en casos muy severos asociada a otros tratamientos, en un intento de reducir el tamaño de las lesiones.13 Vacunas El desarrollo de una vacuna tendría un gran impacto contra la infección de HVP y los tumores asociados al virus. Terapia génica Hay en investigación tratamientos virales específicos como la técnica de la triple hélice y oligonucleótidos antisense.13 Cidofovir El cidofovir es un antiviral el cual ha También resulta eficaz para tratar la infección por HPV en pacientes HIV+, en quienes reduce el área de lesiones anogenitales.5 En particular resulta eficaz en pacientes que reciben HAART.18 resultado efectivo para tratar pacientes inmunocomprometidos con HPV anogenital recurrente severo y neoplasia intraepitelial cervical grado 3.21 Entre los efectos adversos del imiquimod, que son mínimos, se describen eritema, dolor, excoriaciones y hasta ulceraciones y se debe suspender ante cual- Se ha ensayado el cidofovir tópico al 1% en pacientes con lesiones perianales, comprobándose una tasa de curación del 32% con regresión parcial de ALGORITMO TERAPÉUTICO No es sencillo implementar un algoritmo terapéutico dado los numerosos factores a tener en cuenta en las verrugas genitales, localización, tamaño, características clínicas, número, factores propios del paciente (edad, inmunocompromiso, etc). Trascribimos adaptado12 uno que nos parece útil. (Figura I) EDUCACIÓN CONTINUA ALGORITMO TERAPÉUTICO12 T R A T A M I E N T O Tamaño, localización y morfología de las lesiones >10 lesiones, área >1.0 cm2 </= 10 lesiones; área 0,5 a 1.0 cm2 Verrugas grandes queratinizadas, >10 mm de diámetro Lesiones vaginales, anales o cervicales Selección en función de las recomendaciones y las preferencias del médico y el paciente: Selección en función de las preferencias del médico y el paciente: • Lesiones no queratinizadas sobre superficies húmedas: Selección en función de las preferencias del médico y el paciente: ✓ crioterapia. ✓ autotratamiento con ✓ autotratamiento con ✓ escisión quirúrgica ✓ TCA. ✓ podofilina o TCA para ✓ Posibilidad de podofilox o imiquimod ✓ crioterapia. Podofilina, TCA, láser, cirugía en lesiones no respondedores a lo anterior. podofilox o imiquimod las que no responden. • Lesiones queratinizadas sobre superficies secas: como 1º opción. pretratamiento con imiquimod para reducir el tamaño. ✓ procedimientos ablativos: crioterapia, cirugía. CONSIDERACIONES ESPECIALES Verrugas grandes Las lesiones de más de 10 mm diámetro requieren escisión quirúrgica. Previamente puede intentarse reducir el tamaño de la lesión aplicando tres ciclos de imiquimod, en caso de que la respuesta sea ampliamente favorable -reducción del tamaño > 50%- se recomienda continuar con el imiquimod. Verrugas subclínicas Se consideran subclínicas las lesiones que pueden identificarse en la colposcopía, biopsia, tinción con ácido acético o serología. No se considera su investigación dado que el tratamiento no reduce la transmisión ni evita recurrencias. Únicamente debe mantenerse una vigilancia relacionada con el riesgo de neoplasia. Embarazo En las gestantes, las infecciones latentes pueden reactivarse, las verrugas grandes pueden dificultar la micción y, en caso de lesiones internas disminuir la elasticidad y causar obstrucción durante el parto, además existe una tendencia al sangrado. Aunque poco frecuente, los niños pueden adquirir el virus al pasar por el canal de parto y desarrollar lesiones en la garganta y laringe, una condición denominada Papilomatosis respiratoria Recurrente de Inicio Juvenil.22 La incidencia puede alcanzar el 50%, en particular para los subtipos HPV 6 y 11. La incidencia de infección neonatal genital es del 4% pero, aún así, la Asociación Americana de Obstetricia y Ginecología considera que la presencia de HPV no es indicación de cesárea. En embarazadas se aconseja el uso de TCA, escisión quirúrgica, crioterapia y electrocauterio. El objetivo del tratamiento es minimizar el riesgo de infección neonatal. Están contraindicados el 5-FU, podofilina y podofilox. El uso de imiquimod no está aprobado en mujeres gestantes. Inmunocomprometidos En pacientes con inmunodeficiencia la tasa de recurrencia posterior a las terapias destructivas, la magnitud clínica de las verrugas y el potencial oncogénico, suele ser mayor al observado en pacientes con inmunidad conservada. Los pacientes con lesiones perianales, HIV+ o con relaciones anales frecuentes tienen la probabilidad aumentada de desarrollar lesiones intraepiteliales de alto riesgo. Mientras que en pacientes HIV+ la terapia antirretroviral mejora la tasa de infección por otros gérmenes oportunistas, no sucede lo mismo con el HPV.19 Recurrencias En todos los casos es necesario advertir a los pacientes del riesgo de recurrencia. La recurrencia se atribuye a reinfección, período de incubación de HPV, localización del virus en las capas superficiales de la piel, persistencia del virus en lesiones profundas, subclínicas o no tratadas, en la piel sana o en el folículo piloso; inmunosupresión. COMPLICACIONES Carcinoma anogenital El HPV induce una amplia variedad de lesiones hiperproliferativas en el epitelio cutáneo mucoso y, existen evidencias epidemiológicas que sustentan una asociación entre infección por HPV y carcinogénesis anogenital, en especial el cáncer de cuello uterino, además de pene, vulva, vagina y ano. En más del 90% de las mujeres con cáncer de cuello la prueba de PCR detecta HPV de alto riesgo, el cual se ha propuesto como causa directa de la neoplasia. El período de latencia puede superar los 10 años. El HPV codifica los genes E6 y E7 los cuales comprometen las funciones del p53 y la proteína supresora del retinoblastoma, respectivamente, interfiriendo con la replicación del ADN en las células escamosas diferenciadas de la capa mucosa intermedia.6 Las verrugas genitales por HPV se clasifican en función del riesgo asociado de cáncer cervical. Son más frecuentes (90%) las infecciones por HPV de bajo riesgo (HPV 6 y 11, 53 y 54). En el 10 a 15% de los casos se aísla más de un subtipo. tes sobre la evolución natural de las verrugas genitales que en su mayoría resuelven espontáneamente y confieren inmunidad duradera contra el subtipo específico. EL FUTURO Se ha postulado una relación del HPV con otras neoplasias malignas epiteliales incluyendo carcinomas basocelular y espinocelular, de cavidad oral, lengua, hipofaringe, laringe, esófago, vejiga y uretra. El riesgo de cáncer asociado el HPV y la relevancia de la respuesta inmunológica del huésped, en especial la inmunidad celular, en la patogénesis de estas lesiones, justifica el desarrollo de vacunas con poder de profilaxis y terapéutica. Para desarrollar una vacuna se requiere comprender la biología básica e inmunología del HPV. La presencia de anticuerpos neutralizantes contra las proteínas de la cápside ha motivado el diseño de partículas virus-like conteniendo la proteína L1 o la L1 y L2. La latencia entre la infección y el desarrollo de la neoplasia implica que las vacunas deberían aplicarse a niñas prepúberes y esperarse un período de 10 años para confirmar una potencial reducción del cáncer cervical.23 Se estima que un 10% de los carcinomas del mundo se encuentran, de alguna manera, vinculados al HPV.6 Sin embargo, hasta el momento, solamente se ha podido constatar con seguridad la relación del HPV con el cáncer de cuello uterino. Una profilaxis efectiva depende de la presencia de anticuerpos en la mucosa, hasta el momento se han detectado IgA e IgG contra el HPV-16 en pacientes infectados con HPV-16 y otros con neoplasia intraepitelial del cuello uterino asociada al mismo virus. Se ha demostrado una interacción entre el virus y la radiación ultravioleta, las proteínas celulares como p53 y la pro apoptótica de Bak y citoquinas del huésped. En función de estas investigaciones se afirma una contribución del HPV a la transformación maligna de los queratinocitos. En cuanto a los blancos antigénicos contra los cuales dirigir la terapia inmunológica, se sabe que es necesaria la replicación de las proteínas E2 y E1 para que se establezca una infección genital. También se han individualizado las proteínas E4 y E5. Las oncoproteínas E6 y E7 consideradas como el blanco más adecuado dada su elevada expresión en las neoplasias en estadios avanzados. En cambio las proteínas L1 y L2 no siempre están presentes en estas etapas avanzadas de la enfermedad lo cual limita sus aplicaciones.23 Los tipos de riesgo moderado de conversión neoplásica son 33, 35, 39, 40, 43, 45, 51-56, 58 y, los subtipos 16 y 18 se consideran de alto riesgo de anomalía en el Pap y conllevan peligro de neoplasia intraepitelial vulvar, lesiones escamosas intraepiteliales en el cuello uterino y cáncer cervical. Neoplasias extragenitales PREVENCIÓN El uso de preservativos masculinos no resulta eficaz para prevenir la transmisión del HPV dado que no resultan suficientes para evitar el contacto piel-piel de los genitales externos.23 Se recomienda advertir a los pacien- Las estrategias de prevención se dirigen a lograr una respuesta humoral con- EDUCACIÓN CONTINUA tra las infecciones futuras y,han resultado exitosas experiencias en ratones inmunizados con partículas virus-like. tivo de tratar lesiones anogenitales intraepiteliales de alto grado, sugiere una actividad importante contra el HPV. El tratamiento de lesiones preexistentes pretende estimular una respuesta inmunológica celular mejorando el reconocimiento antigénico. Para ello se está trabajando con las proteínas E6 y E7 del HPV16 y 18.24 Se ha ensayado, en una población de mujeres adolescentes, una vacuna con un 75% de probabilidad de inmunizar contra las infecciones por HPV de alto riesgo. La ganancia en expectativa de vida no resultó muy elevada pero, a nivel poblacional el beneficio es notable. En base a los resultados obtenidos se especula que vacunar a todas las niñas de 12 años evitaría 1.300 muertes por cáncer cervical.27 El beneficio podría ser mayor aún si se incluyen en el análisis otros carcinomas relacionados. No obstante disponer de una vacuna en el mercado demandará 4 a 5 años. A partir de la expresión de la proteína fusión HPV 16 L1E7, se ha logrado generar partículas virus like basadas en la fusión de las proteínas HPV-6 L2 y E7. Se trata de un preparado derivado de la fusión de la proteína Hsp65 del bacilo de Calmette Guerin con la proteína E7 del HPV-16. De este modo se combina la propiedad inmunoestimuladora del Hsp65 con un blanco antigénico del HPV.25 Estudios preclínicos han revelado que la administración subcutánea de este preparado en modelos de tumor de células escamosas asociados a HPV 16 desarrollados en ratones genera una respuesta inmunológica con inducción de anticuerpos neutralizantes y linfocitos T específicos. Además de la inmunización contra el HPV16 se ha observado efecto terapéutico sobre lesiones preexistentes.26 El análisis retrospectivo de las historias clínicas de pacientes con verrugas genitales a quienes se aplicó inmunoterapia específica con HspE7 con el obje- También se ha desarrollado experiencia con vacunas de HPV 16 preparada con partículas virus-like producidas por ensamble de la proteína L1 y el gen HPV-16L1. Administrada por vía intranasal se logró la producción de anticuerpos séricos IgG e IgA secretores vaginales. Se atribuye la reacción a la activación de linfocitos T CD4+ con capacidad de sintetizar INF gama, y subpoblaciones CD8+ citotóxicas.28 RELACIÓN MÉDICO PACIENTE Los pacientes quieren y deben ser informados acerca de su infección de modo claro y, para ello se han compilado las 10 preguntas más frecuentes recomendándose al médico dar respuestas adecuadas, comprensibles y comprensivas que ayuden a mitigar la ansiedad y el disconfort.22 Las 10 preguntas más frecuentes22 ¿Cómo, cuándo y de quién puede adquirirse la infección? ¿El HPV puede afectar el embarazo y al niño? ¿Puede una persona transmitir o adquirir el HPV por sexo oral o en sus manos? ¿Cómo se puede investigar la presencia de la infección? ¿La infección persiste por siempre? ¿Cómo se previene la transmisión o contagio? ¿Pueden las parejas sexuales reinfectarse mutuamente? ¿El HPV causa cáncer cervical? ¿Qué debo decirle a mi pareja sobre el HPV? ¿Cuál es el tratamiento más apropiado? BIBLIOGRAFÍA 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. Maw R.: Critical appraisal of commonly used treatment for genital warts. International Journal of STD and AIDS 2004;15: 357-364. Smith-McCune K.: Therapeutic Options for External Genital Warts Continuous Medical Education www.medscape.com Koshiol J., Laurent, S., Pimenta J.: Rate and Predictors of New Genital Warts Claims and Genital Warts-Related Healthcare Utilization Among Privately Insured Patients in the United States. Sexually Transmitted Diseases.2004 ; 31(12):748-752. Fleischer A., Parrish C., Glenn R. y col.: Condylomata Acuminata (Genital Warts): Patient Demographics and Treating Physicians. Sexually Transmitted Diseases. 2001 ;28(11):643-647. Gilson R., Shupack JL., Friedman-Kien A.E.: A randomised controlled, safety study using imiquimod for the topical treatment of anogenital warts in HIV-infected patients. AIDS 1999; 13:2397Harwood CA., Proby C.M. : Human papillomaviruses and nonmelanoma skin cancer. Curr Opin Infect Dis 2002; 15:101-114 Sobhani I., Vuagnat A y col : Prevalence of high-grade dysplasia and cancer in the canal in human papillomavirus-infected individuals . Gastroenterology 2001;120:857-858. Tyring S.: Immune-response modifiers: A new paradigm in the treatment of human papillomavirus. Curr Ther Res Clin Exp 2000; 61:584-596. Garland S.: Imiquimod. Current Opinion in Infectious Diseases. 2003; 16(2):85-89, Reitano M.: Counseling patients with genital warts . Am J Med 1997;102:38-43. Krogh G.: Clinical relevance and evaluation of genital papilloma virus infection in the male . Sem derm 1992;11:229. Kodner C., Nasraty S.: Management of Genital Warts. American Family Physician dic, 2004. 70:2335-42,2345-6. Marini M., Oxilia M.: Verrugas genitales (anogenitales) en Marini M , Oxilia M. : Las enfermedades de transmisión sexual en los tiempos del SIDA . Editorial Marymar, 1ª. ed. 1999, cap 10 , páginas 111 -126. Stone KM., Becker T y col: Treatment of external genital warts:a randomised clinical trial comparing podophyllin, cryotherapy, and electrodesiccation . Genitourin Med 1990; 66 :16-19. Simmons P., Langlet F y col : Cryotherapy versus electrocautery in the treatment of genital warts . Br J Vener Dis 1981 ; 57 :273-274. Abdullah A y col: Treatment of external genital warts comparing cryotherapy and TCA . Sex Transm Dis 1993;20:344. Ferenczy A y col: Treating vaginal and external anogenital condylomas with electrosurgery vs CO2 laser ablation. J Gynecol Surg 1995; 11:41-50. 18. Saiag P., Bourgault-Villada I.y cols. : Efficacy of imiquimod on external anogenital warts in HIV-infected patients previously treated by highly active antiretroviral therapy. AIDS. 2002; 16(10):1438-1440. 19. Manhart L., Koutsky L.: Do Condoms Prevent Genital HPV Infection, External Genital Warts, or Cervical Neoplasia?: A Meta-Analysis. Sexually Transmitted Diseases.2002; 29(11): 725-735. 20. Pall A., Mahajan B. y col.: Therapeutic Evaluation on Intralesional 5% 5-Fluorouracil in Condyloma Acuminata . The Journal of Dermatology 2004;31: 314-325. 21. Coremans G., Margaritis V., Snoeck R. y cols. :Topical Cidofovir (HPMPC) Is an Effective Adjuvant to Surgical Treatment of Anogenital Condylomata Acuminata. Diseases of the Colon & Rectum.2003; 46(8):1103-1108. 22. Gilbert L., Alexander L., y col.: Answering Frequently Asked Questions About HPV. Sexually Transmitted Diseases 2003;. 30(3):193-194. 23. Hagensee M. : Human Papillomavirus Vaccine. Infect Urol 1990; 12(1):11-19. 24. Murakami M., Gurski KJ., Steller M.A. : Human Papillomavirus Vaccines for Cervical Cancer. J Immunother 1999; May; 22(3):212-8. 25. Goldstone S., Palefsky J., y col : Activity of HspE7, a Novel Immunotherapy, in Patients with Anogenital Warts. Diseases of the Colon & Rectum.2002; 45(4):502-507. 26. Jochmus I., Schafer K., Faath S., Muller M., Gissmann L.: Chimeric Virus-Like Particles of the Human Papillomavirus Type 16 (HPV 16) as a Prophylactic and Therapeutic Vaccine. Arch Med Res 1999:Jul-Aug;30(4):269-74. 27. Sanders G. : Cost-Effectiveness of a Potential Vaccine for Human papillomavirus. Emerging Infectious Diseases. 28. Dupuy C., Buzoni-Gatel D., Touze A., Bout D., Coursaget P.: Nasal Immunization of Mice With Human Papillomavirus Type 16 (HPV-16) Virus-Like Particles or With the HPV-16 L1 Gene Elicits Specific Cytotoxic T Lymphocytes in Vaginal Draining Lymph Nodes. J Virol 1999;Nov:73(11):9063-71. Organizaciones a- bc- Office of Communications and Public Liaison, National Institute of Allergy and Infectious Diseases (NIAID), National Institutes of Health. http://www.niaid.nih.gov. American Social Health Association. http://www.ashastd.org Centers for Disease Control and Prevention. http://www.cdc.gov EDUCACIÓN CONTINUA Educación Continua Autoevaluación* Señale lo correcto 1. El ácido tricloroacético actúa en las verrugas anogenitales por: a) inmunomodulación b) antimitótico c) cáustico d) antiviral 2. La podofilina: a) se usa en solución alcohólica b) puede emplearse en tintura de benjui compuesta c) actúa como citotóxico d) está contraindicada en el embarazo e) todas son correctas 3. El interferón para las verrugas genitales: a) b) c) d) e) se puede emplear tópicamente se inyecta en la base de la verruga puede ser usado sistémicamente no debe combinarse con AZT todas son correctas 4. La criocirugía: a) es útil en localizaciones mucosas y cutáneas de verrugas anogenitales b) puede usarse en los niños c) se obtiene altas respuesta y bajas recidivas d) todas son correctas 5. La remoción quirúrgica a) es útil cuando las lesiones son escasas b) aporta la pieza para la histopatología c) su efectividad es muy alta d) está indicada en lesiones del canal anal e) todas son correctas 6. El imiquimod a) tiene actividad antiviral y antitumoral b) se usa en crema al 5% c) su efecto comienza a partir de la 8va. semana d) no se recomienda en la embarazada Señale lo incorrecto 7. El cidofovir: a) se lo ha ensayado en inmunocomprometidos con HPV recurrente y severo b) se lo usa al 1% tópico c) produce una dermatitis erosiva dolorosa d) el éxito se obtiene después de 1 o 2 semanas de tratamiento Señale falso/verdadero 8. Las verrugas anogenitales son producidas más frecuentemente por los HPV 1,3 y 4 F V 9. La transmisión puede ser por contacto sexual pero también por autoinoculación y por fomites F V 10.El 5 FU se lo menciona como alternativa para verrugas vaginales con un aplicador F V * Las respuestas serán publicadas en el próximo número RESPUESTAS CORRECTAS DEL NÚMERO ANTERIOR Lentigo solar Prof. Dr. Miguel Allevato Act. Terap. Dermatol., 2005; 28: 234 1. 2. 3. 4. e e e d 5. 6. 7. 8. d e d d