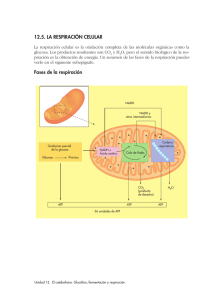
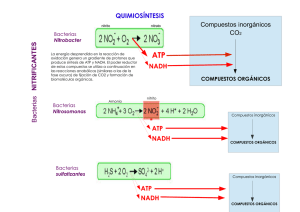
Tema IX METABOLISMO MICROBIANO Metabolismo Es el conjunto de transformaciones químicas que se efectúan en la célula. Movilidad, transporte de nutrientes, biosíntesis http://4.bp.blogspot.com/oiBXvE6GlSk/UPq5AqT7q5I/AAAAAAAAAPI/KxWsxyicHjQ/ s1600/resumen+metabolismo.jpg Transformaciones de materia y energía Los microorganismos necesitan: • Energía para el crecimiento y para el mantenimiento de la biomasa • “Materia prima” para síntesis de los compuestos celulares En la atmósfera la transformación de materia más importante es: Cgas, inorgánico = Corgánico Las transformaciones energéticas más importantes están relacionadas al H: la diferencia de potencial entre el H y el O es la fuente de energía para todos los organismos heterótrofos, aerobios y anaerobios. Transformación escalonada, la energía liberada: • Se pierde como calor • La célula la aprovecha para: -La síntesis química de moléculas grandes o complejas (crecimiento especialmente) -Transporte de sustancias iónicas y neutras hacia adentro y afuera de la célula o entre organelas - Trabajo mecánico para división celular y movimiento (flagelos) Recordar • Energía: Las reacciones químicas van acompañadas por cambios energéticos (H y G) • Catálisis: energía de activación, catalizador • Enzimas: son proteínas, catalizadores biológicos. Altamente específicos • Fuentes de energía: clasificación de los microorganismos • Composición de la célula • Nutrición microbiana Energía • Las reacciones químicas van acompañadas por cambios energéticos • Primera ley de la termodinámica: la energía se conserva (se convierte de una forma a otra) • Entalpía H > 0 reacciones endotérmicas < 0 reacciones exotérmicas • E. libre de Gibbs G > 0 procesos no espontáneos < 0 procesos espontáneos G0´: G en condiciones estándares: pH 7, 25ºC y todos los reactivos y productos inicialmente en una concentración 1M G = H – T S Catálisis y enzimas • Energía de activación: es la energía necesaria para llevar a las moléculas de los reactivos hasta un estado reactivo • Catalizador: es una sustancia que sirve para bajar la energía de activación de una reacción. Incrementa la velocidad de reacción sin sufrir cambios. Los catalizadores no afectan la energética o el equilibrio de una reacción • Enzimas: son proteínas, catalizadores biológicos. Altamente específicos E+S=E–S=E+P 1) Se forma un complejo: enzimasubstrato o substratos. 2) Se une la coenzima a este complejo. 3) Los restos de los aminoácidos que configuran el centro activo catalizan el proceso. Para ello debilitan los enlaces necesarios para que la reacción química se lleve a cabo a baja temperatura y no se necesite una elevada energía de activación. 4) Los productos de la reacción se separan del centro activo y la enzima se recupera intacta para nuevas catálisis. 5) Las coenzimas colaboran en el proceso; bien aportando energía (ATP), electrones (NADH/NADPH) o en otras funciones relacionadas con la Mecanismo de actuación enzimática productos sustrato Enzima inac Enzima tiva Centro activo Coenzima http://web.educastur.princast.es/proyectos/biog eo_ov/2BCH/B3_METABOLISMO/t31_METAB OL/animaciones.htm Oxidación-Reducción • La utilización de energía química en organismos vivos implica reacciones redox • Potenciales de reducción (E0´): tendencia de una sustancia a ceder e- y oxidarse, o aceptarlos y reducirse • En bioquímica las oxidaciones y reducciones involucran frecuentemente la transferencia de e- y de átomos completos de H (Brock) (Brock) Transportadores de electrones La transferencia de e- en reacciones de OR involucra intermediarios (transportadores) Hay tres etapas, cada una catalizada por una enzima diferente, que se une a su sustrato y a su coenzima específico: 1 Salida de los e- del donador primario o inicial 2 Transferencia de los e- a través de uno o varios transportadores intermediarios 3 Captura de los e- por el aceptor terminal o final Los transportadores de e- pueden: • Difundir libremente. Ej. coenzimas NAD+ y NADP+, que transportan dos átomos de H • Estar anclados firmemente a enzimas de la membrana citoplasmática e- ehttp://web.educastur.princast.es/proyectos/biogeo_ov/2BCH/B3_ METABOLISMO/t31_METABOL/animaciones.htm Compuestos de alta energía y almacenamiento de energía • La energía liberada en las reacciones de OR debe ser conservada para las reacciones biosintéticas y otras funciones celulares, cuidadosamente reguladas • Formación de compuestos de alta energía: enlaces fosfatos de alta energía (fosfoanhídridos) a partir de compuestos fosforilados. Ej.: ATP • Formación de compuestos de almacenamiento de energía: enlaces tioéster (sulfoanhídrido). Ej.: derivados de la coenzima A (acetil-CoA) (Brock) Adenosín trifosfato (ATP) Es el compuesto fosfatado de alta energía más importante en organismos vivos. Posee dos enlaces de alta energía de hidrólisis (enlaces anhídridos) Es una coenzima que interviene en las transferencias de energía de los procesos exotérmicos a los endotérmicos. E E Concentración en las células de crecimiento activo: 2 mM http://web.educastur.princast.es/proyectos/biogeo_ov/2BCH/B3_METABOLISMO/t31_METAB OL/animaciones.htm Coenzima A (HS-CoA) • Derivados del Coenzima A, por ej: acetil-CoA (enlaces sulfoanhídridos) Acetil-S-CoA + H2O + ADP + P- → acetato- + HS-CoA + ATP + H+ • Los derivados importantes para anaerobios, en energético implica de acetil-CoA son particularmente la energética de los microorganismos especial aquellos cuyo metabolismo la fermentación Unidad bioquímica de los seres vivos • Uniformidad de los componentes celulares, incluso las formas ópticas • Universalidad del código genético • Universalidad del ATP como unidad fundamental de la energía • Universalidad de las vías metabólicas glucólisis, del TCA y la cadena respiratoria • Las principales vías del metabolismo son casi idénticas, sólo hay pequeños cambios del esquema básico en algunas bacterias -------------------------------------------- Metabolismos productores de energía La respiración y la fermentación son mecanismos de conservación de energía. Desde el punto de vista de las reacciones redox, la respiración y la fermentación se diferencian en lo siguiente: -En la fermentación el proceso redox ocurre en ausencia de aceptores finales de electrones. -En la respiración el oxigeno celular o algún aceptor de electrones funciona como aceptor final de electrones. • Respiración aeróbica o Respiración: el O2 es aceptor final de e- (aceptor externo de e-) En la fermentación, la oxidación esta acoplada a la reducción de un compuesto que se genera a partir del propio sustrato inicial, por lo que no implica la intervención de un aceptor externo de electrones. • Respiración anaeróbica: otro elemento o grupo (externo) frecuentemente inorgánico o más raramente una molécula orgánica, distinto del O2 es aceptor final de e• Fermentación: una sustancia orgánica, en ausencia de O2, es receptor final de e- (esa sustancia se genera a partir del compuesto inicial, no es externo) Especies representativas Pseudomonas aeruginosa Escherichia coli Paracoccus denitrificans Pseudomonas stutzeri Desulfovibrio desulfuricans Desulmonema limicola Desulfuromonas acetoxidans Pyrodictuim occultum Acetobacterium woodii Clostridium aceticum Methanobacterium thermoautotrophicum Methanosarcina barkeri Wolinella succinogenes Escherichia coli Alteromonas putrefaciens -------------------------------------------- Mecanismos de producción/regeneración de ATP También difieren en el mecanismo por el cual se sintetiza el ATP. En la fermentación, el ATP se produce mediante un proceso de fosforilación a nivel de sustrato, donde el ATP se forma durante los pasos del catabolismo de un compuesto organico. Esto se diferencia de la fosforilación oxidativa que ocurre produceenATP la respiracion, a expensasque de la produce fuerza ATP a motriz expensas de protones. de la fuerza También motriz existe de protones. la fosforilación Tambiénque existe ocurre la en microorganismos fosforilación fotosintetica fotosintéticos, que ocurrecuyo en microorganismos mecanismo básico es similar a la fosforilación fotosintéticos, cuyo oxidativa, mecanismo solo que básico en es lugar similar de un a la compuesto fosforilación quimico, lasolo oxidativa, luz es quelaen que lugar inicia deelunproceso compuesto de oxidación-reduccion quimico, la luz es la que inicia el proceso de oxidación-reduccion 1. Fosforilación a nivel de sustrato: GLUCOLISIS 2. Fosforilación oxidativa: CADENA RESPIRATORIA 3. Fosforilación fotosintética: FOTOSINTESIS Sólo (1) y (2) son los mecanismos válidos para todos los seres vivos heterótrofos. Para los autótrofos (vegetales, algas, bacterias fotosintéticas) vale (3). Activación de metabolitos • Los metabolitos necesitan estar “activados” para que las reacciones enzimáticas ocurran • El ATP actúa como coenzima en la activación: hidrólisis del ATP y transferencia de grupos Glucosa + ATP →glucosafosfato + ADP Ribosa-5-fosfato + ATP → fosforribosildifosfato + AMP Ácido graso + ATP → acil-AMP + difosfato Aminoácido + ATP → aminoacil-AMP + difosfato Sulfato + ATP → AMP-sulfato + difosfato Vías de degradación de las hexosas Glucosa → compuestos de C3 (piruvato) 1. Vía más extendida, pasa por fructosa-1,6-bifosfato: FBP, o degradación glucolítica, glucólisis, o vía Embden-Meyerhof 2. Vía oxidativa de la pentosafosfato, vía de la hexosamonofosfato o esquema de Warburg-DickensHorecker (ciclo) 3. Vía de Entner-Doudoroff, parece limitada a las bacterias, también llamada vía KDPG (2-ceto-3-desoxi-6-fosfogluconato) En el balance energético las vías (2) y (3) producen 1 ATP. Ambas vías proveen intermediarios fosforilados para síntesis de compuestos de C3 a C7 Glucólisis o vía de Embden-Meyerhof Balance C6H12O6 + 2 ADP + 2 Pi + 2 NAD → 2 CH3COCOOH + 2 ATP + 2 NADH (glucosa) (ácido pirúvico) ADP/ATP: 4 – 2 = 2 • Ocurre en el citoplasma de las células (citosol) • Son 10 reacciones enzimáticas • Es la vía más común Vía de Entner-Doudoroff • Reemplaza la primera fase de la glucólisis • Bacterias del suelo y algunas Gram negativas, ej.: Rhizobium, Pseudomonas, Agrobacterium • Rendimiento: 1 ATP, 1 NADPH y 1 NADH -------------------------------------------Balance ATP: 1 molecula Piruvato: 2 moleculas (Prescott) (Prescott) -------------------------------------------- Vía de las Pentosas Fosfato Se generan moléculas importantes para la biosíntesis además del piruvato Etapas oxidativas • Puede operar aeróbica o anaeróbicamente • Es una vía anfibólica • Produce NADPH necesario para la biosíntesis (2 moléculas en crecimiento moderado y 12 bajo estrés oxidativo) http://bioados.blogspot.com.ar/2013_01_01_archive.html Degradación de los hidratos de carbono Respiración recursos.cnice.mec.es/.../contenidos4.htm http://recursostic.educacion.es/ciencias/biosfera/web/alumno/2bachillerato/Fisiologi a_celular/imagenes/oxidacion_completo.jpg Ciclo de Krebs -------------------------------------------Ciclo de los acidos tricarboxílicos Los compuestos involucrados son acidos organicos con tres grupos carboxílicos. Se produce la oxidación de estos compuestos, donde los electrones son tomados por los transportadores NAD+ y FAD+ y se produce la formación de ATP. Los electrones liberados que se encuentran en NADH y FADH deben ser transferidos al oxigeno que es el aceptor final, mediante la respiración. Algunos de los compuestos involucrados en el ciclo participan además en otras reacciones con otras funciones. Por lo que la celula para que continue el ciclo, produce estos compuestos mediante reacciones conocidas como anapleroticas. www.biologia.edu.ar/metabolismo/met5.htm Reacciones anapleróticas Degradación de los hidratos de carbono Respiración recursos.cnice.mec.es/.../contenidos4.htm Cadena respiratoria Sistema de transporte de electrones + Enzima ATP-sintasa. Regeneración del ATP www.stanford.edu/.../ treatmts/ebuffer/j1.html Sistemas transportadores de electrones • Los sistemas de transporte de e- están asociados a membranas: – Procariotas: en la membrana citoplasmática – Eucariotas: en la membrana mitocondrial interna Hay diferencias estructurales entre ambos aunque los principios operativos son los mismos • Funciones básicas: 1. Aceptar e- de un donador y transferirlos a un aceptor 2. Conservar parte de la energía liberada durante el transporte para la síntesis de ATP NADH -... ClJ e: NAO•+H• Í \ FAD Succinate Fumarate + 2 H+ ClJ ClJ ClJ 2 Hº ... - Complex 111 Cyt c , , -- i - QH, Q 2 Hº (ox) Cyt e (ox) ---,,< " l . Cyt e , , - - i - - ---,,< " l . Cyt e (red) (red) QH, QH, 2 Hº Complex IV 4 X Cyt c (red) + 4H 4x + 4H Componentes de los sistemas transportadores de e• Enzimas deshidrogenasas: transfieren H • Flavoproteínas: enzimas que usan FMN (NADH reductasa) o FAD (succinato deshidrogenasa) como grupos prostéticos. Aceptan H y ceden e-. • Proteínas sulfoférricas (con centros Fe-S): sistemas redox que transfieren e-. No pueden transportar H. Potenciales de reducción fuertemente negativos. • Quinonas: ubiquinona (CoQ) en bacterias Gram (-), naftoquinonas en Gram (+) y plastoquinona en cloroplastos. Aceptan H y ceden e-. • Citocromos: sistemas redox para el transporte de e-; no pueden transferir H. Contiene grupo Hemo como prostético: Citocromo - Fe+2 →Citocromo - Fe+3 + eLos distintos citocromos (b, c1, c, a y a3) se distinguen por sus espectros de absorción y sus potenciales redox. Son coloreados. La citocromo-oxidasa (citocromo a3) es la oxidasa terminal que reacciona con el O2. Electron Transport Chain inside Mit ochondria cyt c 1 cyt e Fes 1 111111 2e-1';l2 e -ft cyt b cyt b J1111 2ecyt a 3 c)t ª complex 3 complex 2 NADH + A 1 1 +Q NAO+ < z +1"11 :e 2 C. Ophardt, e. 2003 FADH2 FAD (enly used f er ene react ien in CAC) H::!O 3ADP + 3P Citric Ac id Cycle and Fat ty Acid Ox idation Occur 3ATP Balance La cadena respiratoria produce: ➢ 3 ATP/mol NADH2 ➢ 2 ATP/mol FADH2 C6H12O6 + 38 ADP + 38 Pi + 6 O2 → 6 CO2 + 6 H2O + 38 ATP Fermentación - El piruvato (o moléculas derivadas) • Disponible luego de la glucólisis • Muchas células los usan como aceptor terminal, creando productos de desecho que se excretan de la célula • Esos residuos se excretan en enormes cantidades dado que, en razón del bajo rendimiento, son necesarias muchas moléculas de glucosa para producir la energía que necesita la célula. Estos residuos todavía contienen energía aprovechable • Este sistema no es tan eficiente como la respiración pero permite que el catabolismo continúe. Fermentación alcohólica GLUCOLISIS Piruvato descarboxilasa Alcohol deshidrogenasa • Ocurre en levaduras (Saccharomyces cerevisiae, facultativa), otros hongos y algunas bacterias. • Es la base de numerosas aplicaciones en la alimentación humana: pan, cerveza, vino, etc. Fermentación láctica GLUCOLISIS Lactato deshidrogenasa • En muchas bacterias (bacterias lácticas), en algunos protozoos, en tejidos animales bajo condiciones limitadas de oxígeno • Obtención de productos lácteos acidificados: yogurt, quesos, cuajada, crema ácida, etc. • El ácido láctico tiene excelentes propiedades conservantes de los alimentos. Las bacterias homofermentativas: • Metabolizan la glucosa por vía de la fructosa-difosfato • Reducen el piruvato a lactato, producen lactato puro o casi puro • Ej.: Estreptococos (Lactococcus lactis, Enterococcus faecalis, Streptococcus salivarius, Streptococcus piogenes), Lactobacilos (Lactobacillus delbrueckii subsp lactis, bulgaricus, delbrueckii, L. helveticus), Estreptobacterias (Lactobacillus casei, L. alimentaris, L. coryniformis, L. plantarum) Las bacterias heterofermentativas: • Degradan las pentosas (xilosa) • Degradan la glucosa al comienzo por la vía de las pentosas y luego transforman el acetil-fosfato en etanol o acetato y el piruvato en lactato • Ej.: Estreptococos (Leuconostoc mesenteroides subsp. mesenteroides, dextranicum, cremoris, L. lactis), Lactobacilos (Lactobacillus brevis, L. bifermentans, L. fermentum, L. kandleri, L. viridescens) Eficiencia energética de la respiración Para la combustión (oxidación total) de la glucosa: C6H12O6 + 6 O2 → 6 CO2 + 6 H2O G0 = -686 Kcal/mol El rendimiento energético real de la respiración se puede calcular considerando los moles de ATP regenerados por mol de glucosa C6H12O6 + 38 ADP + 38 Pi + 6 O2 → 6 CO2 + 6 H2O + 38 ATP Para la hidrólisis ATP: G0 = -7.3 Kcal/mol Para la reacción: G = 38 (mol ATP/mol Glu) x (-7.3 Kcal/mol ATP) = -277 Kcal/mol Glu 19 veces más energía que la capturada por la célula durante la glucólisis: Respiración 38 ATP = = 19 Fermentación 2ATP Eficiencia energética de la respiración: 277 Kcal/mol Glu = 100 = 40% 686 Kcal/mol Glu Corrigiendo para las condiciones no estándares que ocurren en la célula la eficiencia resulta mayor que 60%. Hay una pérdida como calor, que se disipa para mantener la temperatura en el rango fisiológico adecuado. Fermentación propiónica • Formación de propionato • Especies de Propionibacterium se usan en la maduración de quesos tipo suizo. El piruvato proveniente de la ruta de la fructosa-difosfato o el lactato resultante de otras fermentaciones son reducidos vía mediante la de la metilmalonil-CoA • Clostridium propionicum y Bacteroides ruminicola (habitan el rumen y el intestino del ganado) siguen una ruta más simple, donde la lactil-CoA se reduce a propionil-CoA. Fermentación butírica - butanólica • En Clostridium se produce primero la transformación de azúcares en piruvato y una vez descarboxilado origina varios productos • En las primeras fases predominan los ácidos butírico y acético pero luego, al bajar el pH del medio comienzan a acumularse acetona y butanol que son neutros Fermentación fórmica o ácido mixta • Llevada a cabo por Escherichia coli (bacteria facultativa del intestino) y otras patógenas de animales, por ej. Salmonella spp., que excretan ácidos orgánicos y el pH desciende a 4,2, donde la solución de rojo de metilo tiene color rojo. • Los organismos coliformes se usan como indicadores de la contaminación fecal del agua • Ej.: Salmonella, Bacteroides, Bifidobacterium, Vibrio cholerae Incapacidad de formar acetoína (intermediario del 2-3 butanodiol) Fermentación butanodiólica o butilenglicólica • Bacterias que se encuentran en el agua y el suelo • Formación 2,3-butanodiol como producto principal. • La acetoína es un intermediario que da positiva la reacción de Voges-Proskauer con α-naftol en medio alcalino, útil para detectar algunos organismos con este tipo de fermentación • Ej. Enterobacter aerogenes, Bacillus cereus y la fitopatógena Erwinia Fermentaciones acéticas • Algunos clostridios, como C. thermoaceticum, fermentan la glucosa por la vía de la fructosadifosfato. Luego generan acetato por descarboxilación del piruvato. • La conversión del CO2 e hidrógeno en acetato es llevada a cabo por varios organismos, tales como Acetobacterium woodii y Clostridium aceticum (Prescott) En síntesis… Productos naturales fermentables y no fermentables • La mayoría de los productos naturales formados por C, H, O y/o N pueden ser fermentados bajo condiciones anaeróbicas • Condición necesaria para la fermentación: posibilidad de oxidar parcialmente el sustrato mediante una reacción exotérmica • Son fermentables: polisacáridos, hexosas, pentosas, tetrosas, polioles, ácidos orgánicos (gluconato, malato, tartrato, etc), aminoácidos (excepto los aromáticos que sólo son fermentables en condiciones específicas); purinas y pirimidinas. • No fermentables en condiciones anaeróbicas: hidruros alifáticos saturados y aromáticos, esteroides, carotenoides, terpenos y porfirinas. • La estabilidad de estos compuestos (que pueden degradarse en condiciones aeróbicas) se debe a: 1) La mayoría contienen exclusivamente átomos de C e H (no se obtiene energía) 2) Los hidrocarburos saturados y los polisoprenoides son atacados en presencia de O2 (primer paso es oxidación) Los productos sintéticos son degradables? Asimilación de nitrógeno: principales vías ADP + Pi Glutamina ATP NH4+ Glutamato 1 NO3N2 5 4 2 3 NH4+ 6 Glutamato Glutamato aminoácidos 2-oxoglutarato + 2 [H] aminoácidos 2-oxoglutarato + 2 [H] 7 Alanina aminoácidos piruvato + 2 [H] 1: asimilación directa del NH4+ 2: reducción del NO3- (nitrato reducción asimilatoria) 3: fijación del nitrógeno molecular 4: glutamino sintetasa 5: glutamato sintasa 6: L-glutamato deshidrogenasa 7: L-alanina deshidrogenasa Biosíntesis de aminoácidos Bibliografía recomendada: • • • • Biología de los microorganismos. Brock. M.T. Madigan, J.M. Martinko, J. Parker. 10th Edition. Pearson Prentice Hall, Madrid, 2004. Microbiology. Prescott, Harley, and Klein´s. J.M. Willey, L.M. Sherwood, C.J. Woolverton. Seventh Edition. Mc Graw Hill, New York, 2008. General Microbiology. H.G. Schlegel. Sixth Edition. University Press, Cambridge, 1987. Microbiology. An Introduction. G.J. Tortora, B.R. Funke, C.L. Case. Tenth Edition. Pearson Education, San Francisco, 2010. Videos sugeridos: http://www.uic.edu/classes/bios/bios100/lectures/resp_summary.html https://www.youtube.com/watch?v=rumUBQPykHA http://slideplayer.es/slide/27484/