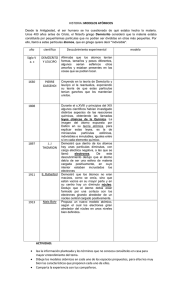
“Comprendemos la evolución de los modelos atómicos a través de la historia” ¿Cómo se elaboraron los conocimientos científicos? ¿Los conocimientos científicos en el pasado y en la actualidad serán los mismos? “A través de la historia todos los conocimientos científicos han ido cambiando y evolucionando, eso gracias al aporte de cada investigación, que es tomada con mucho respeto y valor por otros científicos para mejorar el conocimiento en favor del desarrollo de la humanidad. Es importante resaltar que no todos los contextos han sido favorables para el desarrollo de la ciencia, antiguamente se pensaba que las mujeres no eran capaces de estudiar o de realizar alguna investigación, lo cual era una discriminación; otro ejemplo claro es que las personas que experimentaban con sustancias se les consideraban hechiceros y eran perseguidos, lo que es un ejemplo de arraigo cultural de la época antigua, y de esa manera podemos citar muchos ejemplos más”. ¿Cómo pensaban que era el átomo en el siglo pasado? ¿cómo definirías al átomo ahora? ¿a qué factores se debe la evolución de este conocimiento? - - Los átomos son la fracción más pequeña en la que se divide la materia, la mínima porción en la que todavía se mantienen sus propiedades tanto químicas como físicas. El estudio del átomo comienza en Grecia, unos 400 años a.C., cuando Demócrito propuso que la materia estaba formada por partículas pequeñísimas a las que llamó átomos, que en griego significa “indivisible”. Fue necesario esperar más de 20 siglos para que Jhon Dalton propusiera el primer modelo basado en la experimentación que, aunque explica algunas propiedades de la materia, no es correcto. Actualmente, sabemos que el átomo no es indivisible, sino que está formado por otras partículas más pequeñas: protones, neutrones y electrones. ¿Qué observan? ¿podrían decir a qué modelo atómico pertenece cada representación? - - Los átomos son la fracción más pequeña en la que se divide la materia, la mínima porción en la que todavía se mantienen sus propiedades tanto químicas como físicas. El estudio del átomo comienza en Grecia, unos 400 años a.C., cuando Demócrito propuso que la materia estaba formada por partículas pequeñísimas a las que llamó átomos, que en griego significa “indivisible”. Fue necesario esperar más de 20 siglos para que Jhon Dalton propusiera el primer modelo basado en la experimentación que, aunque explica algunas propiedades de la materia, no es correcto. Actualmente, sabemos que el átomo no es indivisible, sino que está formado por otras partículas más pequeñas: protones, neutrones y electrones. John Dalton: “minúscula partícula esférica indivisible” Joseph John Thomson: “Budín con pasas” Ernest Rutherford: “El átomo tiene un núcleo pequeño cargado positivamente y alrededor giran los electrones cargados negativamente” Con este experimento, el científico llegó a las siguientes conclusiones: • El átomo está formado por una parte central o núcleo donde se concentra la carga positiva y la mayoría de la masa. Esto lo comprobó cuando unas cuantas partículas se desviaban y otras rebotaban. • El átomo es extremadamente vacío. Lo comprobó cuando casi la mayoría de partículas alfa atravesaban la lámina de oro. Estas conclusiones lo llevaron a proponer el modelo atómico nuclear, que explica que el átomo está formado por un núcleo pequeño cargado positivamente y alrededor giran los electrones cargados negativamente. Niels Bohr: “Modelo atómico de órbitas electrónicas” Modelo mecánico cuántico: Erwin Schrödinger Louis de Broglie Werner Heisenberg En este modelo, la materia a nivel subatómico empieza a comportarse de forma muy extraña e impredecible, y es capaz de producir efectos como hallarse en varios sitios a la vez. El electrón se comporta como una partícula o como una onda y se encuentra disperso por todo el átomo. Los electrones se encuentran distribuidos ocupando orbitales, lugar probable donde los podemos ubicar. Este modelo plantea que el átomo está constituido por el núcleo y la nube electrónica. www.educadocente.com 942 823 985 - 959 698 659