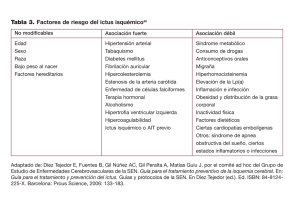
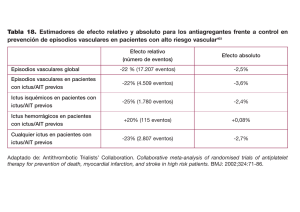
Fibrilación auricular detectada después de un ictus o ataque isquémico transitorio: un nuevo concepto clínico que desafía paradigmas actuales Sposato LA, Chaturvedi S, Hsieh CY, et al. Atrial Fibrillation Detected After Stroke and Transient Ischemic Attack: A Novel Clinical Concept Challenging Current Views. Stroke. 2022 Mar;53(3):e94-e103. Cerca del 20% al 30% de los pacientes con ictus isquémico y ataques isquémicos transitorios (TIA) tienen una fibrilación auricular conocida (KAF). Dentro de los 70% a 80% restantes sin arritmias conocidas, hasta el 24% puede ser diagnosticado con una fibrilación auricular (AF) de nueva aparición, teniendo un estimado de 1.3 a 1.5 nuevos casos de AF detectada después de un ictus o TIA (AFDAS) globalmente cada año. El rol de la AFDAS como un mecanismo causal está disputado en circunstancias específicas. La edad está consistentemente asociada con un riesgo incrementado para AFDAS. Las mujeres tienen un 49% más de probabilidades de ser diagnosticadas con AFDAS (OR 1.49, IC 95% 1.26-1.76). Nomenclatura La AFDAS fue introducida en 2017 como un nuevo término para reconocer un tipo específico de AF que es detectada después de un ictus o TIA, y que puede ser paroxística o permanente, prevalente o incidente, y que tiene características clínicas y pronósticas distintivas. Clasificación del ritmo cardíaco en pacientes con ictus o TIA El ritmo cardíaco en pacientes con ictus o TIA puede ser agrupado en tres categorías: (a) sin AF (incluyendo ritmo sinusal y otras arritmias que no son AF); (b) AF conocida (KAF)—AF diagnosticada antes de la aparición del ictus; y (c) AFDAS. Se define AFDAS como una AF detectada después de la aparición de un ictus isquémico o TIA en pacientes sin KAF. La distinción entre KAF y AFDAS se basa en diferentes marcos de tiempo de detección y características clínicas y pronósticas. Los pacientes con AFDAS tienen un puntaje CHA2DS2-VASc menor, menor prevalencia de comorbilidades vasculares, una fracción de eyección del ventrículo izquierdo (LEVF) más alta, y un menor diámetro auricular promedio comparado con aquellos con KAF. En promedio, los casos de AFDAS tienen menor sustrato cardíaco que KAF. El involucro de la corteza de la ínsula, un desencadenante de cambios cardíacos neurogénicos, se asocia con la detección de AFDAS, y es más frecuente en ADFAS que KAF. En comparación con KAF, la AFDAS puede ocurrir en pacientes con ictus o TIA con perfiles vasculares menos graves, corazones estructuralmente sanos ,y en algunas ocasiones, es desencadenada por fenómenos neurogénicos. Fisiopatología cardiogénica y neurogénica Conceptualmente, se considera que la AFDAS puede aparecer por la interacción de dos fuerzas: cardiogénica y neurogénica. Factores cardiogénicos y neurogénicos Los pacientes con factores de riesgo cardiogénico que llevan a AFDAS probablemente tenga un grado sustancial de cardiopatía atrial y factores de riesgo vascular. Pueden tener episodios de AF no diagnosticada antes de la aparición del ictus, continuando sin diagnosticarse hasta que los pacientes se someten a monitorización cardíaca prolongada (PCM) posterior al ictus. Los mecanismos neurogénicos han sido reconocidos como parte del recientemente descrito síndrome ictus-corazón. Los factores neurogénicos incluyen mecanismos autonómicos e inflamatorios que desencadenan focos ectópicos que envían descargas en el plexo ganglionar y, en etapas tardías, mecanismos de reentrada relacionados con lesión cardíaca inducida por ictus (SIHA). Modelos animales han demostrado el desarrollo de disfunción endotelial en la aurícula derecha, inflamación y fibrosis, de manera temprana después de la inducción de ictus isquémicos insulares. Por lo tanto, el desarrollo de AF neurogénica después de un ictus no solo tiene un componente fisiológico (disfunción autonómica e inflamación), sino que también pareces ser explicada por un incremento súbito de la gravedad del sustrato en la aurícula izquierda (inducido por el ictus), que ha sido descrito como SIHI. La AFDAS puede ocurrir en ausencia de enfermedad cardíaca clínica o ecocardiográficamente evidente, como consecuencia de mecanismos neurogénicos. Diagnóstico de la AFDAS Predictores de AFDAS Aún está por determinarse la mejor estrategia de tamizaje para AFDAS en pacientes con ictus isquémico y TIA. Los biomarcadores más consistentemente asociados con el diagnóstico de AFDAS son edad, dilatación de la aurícula izquierda, incremente de pépticos natriuréticos cardíacos, y complejos auriculares prematuros. La medición de troponinas se recomienda en las actuales guías de prevención de ictus y se realiza como parte del abordaje diagnóstico en la mayoría de los centros neurológicos. Una elevación de más del 20% en troponina cardíaca en los días después medida basal realizada al ingreso se ha descrito como un patrón de “incremento y caída”, que se asocia con involucro de la corteza de la ínsula. Este patrón constituye un biomarcador candidato prometedor para diferenciar las contribuciones cardiogénicas y neurogénicas de la AFDAS. Umbral mínimo de duración de la AF para el diagnóstico de AFDAS Las arritmias cardíacas con las características electrocardiográficas de AF deben durar más de 30 segundos para ser consideradas AF. Sin embargo, esto no ha sido suficientemente validado y no ha sido ampliamente aceptado por neurólogos vasculares. Los neurólogos vasculares son dos veces más propensos a aceptar un paroxismo de AF menor de 30 segundos como prueba de AF porque la detección de AF de muy corta duración puede no implicar el mismo riesgo de ictus como una FA de 30 segundos en la población general. La AFDAS con menos de 30 segundos de duración es altamente prevalente en pacientes con ictus, y componen el 52% (IC 95%, 36%-66%) de todas las AF diagnosticadas después de un ictus. AFDAS y riesgo de ictus recurrente, muerte y demencia Espectro de riesgo embólico de la AFDAS El riesgo embólico de la AFDAS puede ser entendido como un gradiente definido por la prevalencia de comorbilidades vasculares y la gravedad de la cardiopatía atrial. De hecho, la elevación de péptidos natriuréticos y la dilatación de la aurícula izquierda, marcadores confiables de cardiopatía auricular avanzada, son fuertes predictores de riesgo de ictus en pacientes con AF. La contribución de mecanismos no cardioembólicos, como la aterosclerosis carotídea o la enfermedad de pequeño vaso pueden jugar un rol en pacientes con AFDAS de alto riesgo que tienen un mayor conglomerado de factores de riesgo. Aunque algunas AFDAS pueden implicar un riesgo relativamente bajo de recurrencia de ictus, su detección requiere un seguimiento cercano y el manejo médico de los factores de riesgo para evitr su progresión a AF de mayor riesgo. AFDAS y riesgo de ictus recurrente La AFDAS tiene significativamente menor riesgo de ictus recurrente que la KAF. Sin embargo, la AFDAS se a asociado con riesgo doble de ictus recurrente comparado con pacientes que no tienen AF (HR 1.98, IC 95% 1.50–2.59). AFDAS y riesgo de muerte El riesgo de muerte en pacientes con AFDAS es similar a KAF. Se ha encontrado un 60% más rieso de muerte en AFDAS comparado con pacientes sin AF (HR 1.60, IC 95% 1.38-1.85). AFDAS y riesgo de demencia Comparado con pacientes sin AF, la AFDAS se ha asociado con un riesgo incrementado de demencia, independientemente si es diagnosticada durante la hospitalización por ictus (HR 1.78, IC 95% 1.512.10), o en el contexto ambulatorio (HR 1.74, IC 95% 1.47-2.05). El rol de la anticoagulación en pacientes con AFDAS Los anticoagulantes orales se han asociado con un 41% menor riesgo de ictus recurrente y un 29% menor riesgo de muerte en pacientes con AFDAS, sin diferencias en la incidencia de hemorragia intracerebral. También han sido asociados con un 40% menor riesgo de demencia incidente en pacientes con AFDAS e ictus isquémico de primera vez. Estos datos fueron obtenidos a partir de estudios en donde la AFDAS fue diagnosticada con una monitorización Holter de más de 48 horas. El rol de los anticoagulantes en la reducción del riesgo de ictus recurrente en AFDAS detectada por PCM es menos claro. Conclusiones La evidencia sugiere que la AFDAS es diferente de la KAF y posiblemente conlleva un menor riesgo de ictus, lo cual se explica por un gradiente de riesgo embólico determinado por la interacción de factores cardiogénicos y neurogénicos. El patrón de práctica clínica prevalente es que los pacientes con AFDAS reciban anticoagulantes orales a menos que esté contraindicado. Los pacientes con ictus embólicos de causa desconocida, especialmente aquellos con otros biomarcadores (dilatación de la aurícula izquierda, bloqueo auricular, alta carga de complejos auriculares prematuros) deben ser considerados para el tamizaje de AF. Elaboró: Dr. Emmanuel Solorza R2MI