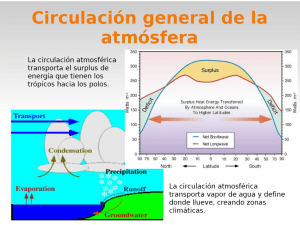
Resumen del Tema 1.1: La escala atómica de los materiales 1. Principales conceptos - Cristal – estructura ordenada, periódica y repetitiva de átomos, iones o moléculas (dependiendo del tipo de material) que se extiende en las tres direcciones del espacio (ordenamiento a corto y a largo alcance). Un material que presente una estructura 100% cristalina se denomina material cristalino, mientras que un material sin ningún tipo de ordenamiento (0% cristalino) se denomina material amorfo. Algunos materiales poliméricos pueden presentar un ordenamiento parcial, denominándose materiales semicristalinos (formados por una fracción desordenada amorfa y por una fracción ordenada cristalina). - Celda unidad – volumen repetitivo más pequeño que contiene el patrón de la estructura de un cristal (unidad mínima del material que representa su estructura ordenada cristalina, de tal manera que desplazando dicha estructura a través del material se sigue teniendo su estructura cristalina básica). La celda unidad está definida por sus constantes reticulares (parámetros reticulares o de red): 3 longitudes axiales y 3 ángulos axiales. Es común usar el término constante reticular para hacer referencia a la longitud de la arista en una estructura cúbica (parámetro “a”). A los 7 tipos distintos posibles de celdas unidad se les denomina sistemas cristalinos. La introducción de los componentes del material en dichos sistemas cristalinos (disposición de los átomos, iones o moléculas) da lugar a las 14 estructuras cristalinas posibles (redes de Bravais). - Alotropía/polimorfismo – Es la capacidad que poseen algunos materiales para existir en más de una forma cristalina en la misma fase o estado de la materia. Él termino alotropía se aplica a elementos puros (ejemplos: formas alotrópicas del carbono – diamante, grafito, nanotubos de carbono, etc.; formas alotrópicas del hierro (en función de la temperatura): hierro alfa (BCC), hierro gamma (FCC) e hierro delta (BCC)), mientras que el término polimorfismo se usa para compuestos. Resumen del Tema 1.1: La escala atómica de los materiales 2. Principales características de una estructura cristalina - Volumen de la celda unidad (Vc) - Número de átomos por celda unidad (n) - Fracción de empaquetado atómico (fv) – fracción de la celda unidad ocupada por átomos, iones o moléculas. Asumiendo un modelo de esferas rígidas en que el material está formado por un único elemento de radio r: ⎛4 ⎞ n ⎜ πr 3 ⎟ 3 ⎠ fv = ⎝ Vc [unidades – adimensional, multiplicando por 100 - %] - Densidad atómica lineal (ρ[u v w]) – número de átomos intersectados por su centro en la celda unidad por una dirección cristalográfica por longitud de dicha dirección en términos de la celda unidad. - Densidad atómica planar o superficial (ρ(u v w)) – número de átomos intersectados por su centro en la celda unidad por un plano cristalográfico por sección de dicho plano en términos de la celda unidad. - Densidad teórica (ρ) ρ= nA Vc N A [unidades típicas – g/cm3 o kg/m3] - Número o índice de coordinación – Es el número de vecinos más próximos que rodean a un componente dado (átomo/ión o molécula). Se tienen en cuenta en dicho cálculo las celdas unidad adyacentes. Resumen del Tema 1.1: La escala atómica de los materiales 3. Principales consideraciones sobre direcciones y planos cristalográficos - Direcciones cristalográficas – El origen del sistema debe coincidir con el origen de la dirección; se leen las proyecciones de dicha dirección en términos de las longitudes axiales de la celda unidad (en el caso de una celda unidad cúbica, a = b = c); reducción al mínimo valor entero de dichas proyecciones; colocación de los valores enteros entre corchetes sin comas (índices negativos – colocación del signo “–” sobre dicho índice). - Planos cristalográficos – OJO (diferencia con las direcciones): el origen del sistema no puede pertenecer al plano; se leen las intersecciones del plano con los ejes en términos de las longitudes axiales de la celda unidad (en el caso de una celda unidad cúbica, a = b = c); OJO (diferencia con las direcciones): obtener el valor recíproco (inverso) de dichas intersecciones; reducción al mínimo valor entero; colocación de los valores enteros entre paréntesis sin comas (índices negativos – colocación del signo “–” sobre el índice).