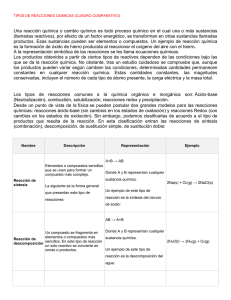
CONSULTA PREVIA 1. El sulfato de magnesio (MgSO4) se usa para fines terapéuticos. Es suministrado para desórdenes clínicos, entre los cuales podemos destacar: preclamsia, desórdenes cardiovasculares, procesos de isquemia cerebral, asma, migrañas, y síndrome Irukandji entre otros. Al ser administrado en las concentraciones consideradas como terapéuticas posee mínimos efectos tóxicos. Una empresa farmacéutica desea sintetizar este compuesto. Teniendo en cuenta la figura 1 del marco teórico realice las reacciones correspondientes para hacer la síntesis de este compuesto (tenga en cuenta tanto la formación del óxido básico, el hidróxido, la del óxido ácido y del oxácido), nombrar cada sustancia obtenida y balancear las reacciones. SÍNTESIS DE MgSO4 Mg+H2SO4 H2+MgSO4 2. Complete la siguiente tabla. (Las ecuaciones químicas deben estar balanceadas). PRODUCTO FUNCIÓN QUÍMICA DEL PRODUCTO NOMBRE DEL PRODUCTO (Nomenclatura tradicional) Ca(s) + O2(g) 2CaO+O2 Oxido Oxido de calcio P4(S) + 3O2(g) 2P O3 anhidrido Anhidrido de fosforo 2Na(OH) Hidróxido Hidróxidos sódicos H2SO4 CaSO4+2H2 O Acido Acido sulfúrico sal Sulfato de calcio REACTIVOS Na2O(g) + H2O(l) SO3(g) + H2O(l) H2SO4(l) + Ca(OH)2 (l) 3. Lea los siguientes enunciados y de acuerdo con la descripción de cada uno complete los recuadros que hacen faltan con los términos (según el numeral indicado) que corresponda y que se encuentra en la parte inferior. Una Reacción química es un proceso en el cual hay un cambio de las sustancias, donde a partir de las iniciales llamadas reactivos se da origen a productos. Dicho proceso se representa por medio de ecuaciones que deben estar balanceadas por Coeficientes que se anteponen a la fórmula y se relacionan con los Subíndices que 1. subíndices 5. combustión 9. sustitución simple indican la cantidad de átomos de un elemento, el cual a su vez presenta un Estado de oxidación y está representado por un Símbolo. Existen diferentes tipos de reacciones, por ejemplo, cuando dos reactivos intercambian sustituyentes generando nuevos productos es una doble sustitución 2. descomposición 6. símbolo 10. reacción química De igual forma cuando los átomos de un elemento reemplazan los de otro elemento es una sustitución simple, o cuando un compuesto se desintegra es una descomposición a diferencia de las sustancias que arden en presencia de O2 sufren una Combustión. 3. productos 7. reactivos 11. doble sustitución 4. coeficiente 8. ecuaciones 12. estado de oxidación 4. Cite las fuentes empleadas para responder las preguntas de la bibliografía. Use normas APA Grasselli, M, Colasurdo, V.( 2001). Reacciones http://revistas.unam.mx/index.php/req/article/view/66332. quimicas. [Blog]. Recuperado de