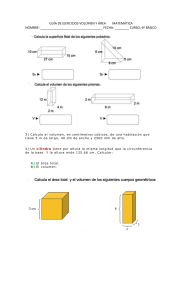
Cal or i me t r í a Rama de la termodinámica que mide la cantidad de energía generada en proces os de intercambio de calor C a lo r Es la trans ferencia de energía entre la materia como res u ltado de las diferencias en la temperatu ra . Energía T1 T2 T1 > T2 Unidad del Calor : Caloría (cal) ► Es la cantidad de calor necesaria para aumentar la temperatura de 1 gramo de agua de 14,5 °C a 15,5 °C a la presión de 1 atmósfera (Presión normal). Relación entre unidades Unidades de Cantidad de Calor Las unidades de cantidad de calor (Q) son las mismas unidades de trabajo (T). Sistema de Medida • Sis tema Técnico • Sis tema Internacional (S.I.) • Sis tema C.G.S. Unidad de Medida • Kilográmetro (Kgm) • Jou le (J) • Ergio (erg) 1 kgm = 9,8 J 1 cal = 4,186 J 1 J = 10 7 erg 1 kcal = 1000 (10 ³ ) cal 1 kgm = 9,8.10 7 erg 1 BTU = 252 cal Q Equivalente mecánico del calor W →Q El trabajoquerealizan laspaletas setransformaen calor 1 cal = 4,186 joule En el experimento de Joule se determina la relación entre la unidad de energía joule y la unidad de calor caloría. Capacidad calorífica y Calor es pecífico Capacidad calorífica (C) Esel calor quedeberecibir unasustanciaparaqueaumentesu temperatura1 ºC. Unidad : [c] = cal / °C Por lo tanto s i u na cantidad de calor Q produ ce u n cambio en la temperatu ra de u na s u s tancia s e tiene: Calor específico (c) Es la razón entre la capacidad calorífica (C) de un cuerpo y la masa (m) de dicho cuerpo. Unidad : [c] = cal / g °C •m es la masa de la sustancia en gramos. C agua = 1 cal/g.°C C hierro = 0,114 cal/g.°C C hielo = 0,5 cal/g.°C C latón = 0,094 cal/g.°C C aire = 0,24 cal/g.°C C mercurio = 0,033 cal/g.°C C aluminio = 0,217 cal/g.°C C cobre = 0,092 cal/g.°C C plomo = 0,03 cal/g.°C C plata = 0,056 cal/g.°C Conducción Formas de transformación del calor Convección Radiación Es típica en los sólidos. Es típica de líquidos y gases. Se presenta en todos los estados físicos. Es la transferencia de calor que tiene lugar por transmisión de Energía de unas partículas a otras, sin desplazamiento de éstas. Es la transferencia de calor que tiene lugar mediante el movimiento de las partículas de un fluido. El transporte es efectuado por moléculas de aire. Es la transferencia de calor mediante ondas electromagnéticas sin intervención de partículas que lo transporte. Efectos del Calor 1º.- Cambios de Estado Sublimación Fusión Vaporización Solidificación Licuefacción Sublimación Cambios progresivos () Cambios regresivos () Absorven Q Desprenden Q Fusión Vaporización Cambio de estado : Sólido a líquido Cambio de estado : Líquido a gas El calor absorbido por un cuerpo en la fus ión es igual al calor cedido por éste en la s olidificación. El calor absorbido por un cuerpo en la vaporización es igual al calor cedido por és te en la condens ación. Punto de fusión: Temperatura en la que se produce la fus ión (en el agua :0 ºC). Punto de ebullición: Temperatura en la que s e produce la ebullición (en el agua:100º C). Mientras s e produce el cambio de es tado, los puntos de fus ión y ebullición s on cte. Calor latente de fusión: Cantidad de Calor latente de vaporización : calor por unidad de mas a que Cantidad de calor por unidad de ha de s uministrars e a una mas a que ha de s uminis trars e a s ustancia a s u temperatura una sus tancia a s u temperatura de fus ión para convertirla de ebullición para convertirla completamente en líquido completamente en gas . Agua : Lf = 3.34 105 J/kg Lf = 79.6 cal/g Lv = 2.256 106 J/ kg L = 539 cal/g Q = mLf Q = mLv Calor latente Calor latente de cambio de estado L: Eslacantidad decalor quenecesitauna unidad demasadeunasustanciaparacambiar deestado. Semideen J/Kgo bien en cal/gr. Q= m x L T (°C) Fase gaseosa 100 Fase líquida Punto de fusión 0 -25 Punto de ebullición Fase sólida Tiempo El calor de fus ión y vaporización s olo s e emplean en el cambio de es tado, no en aumentar la Temperatura. 2º.- Dilatación Esel fenómenopor el queloscuerposexperimentan una variación devolumen al modificar su temperatura. Dilatación Lineal L = Longitud final Lo = Longitud inicial £ = Coeficiente de Dilatación Líneal At = incremento de temperatura = (tf - to) Coeficiente de dilatación lineal Dilatación Superficial S = Superficie final So = Superficie inicial ß = Coeficiente de Dilatación Superficial At = Incremento de temperatura = (tf - to) Coeficiente de dilatación s u perficial Dilatación Cúbica Coeficiente de dilatación cúbica V = Volumen final Vo = Volumen inicial y = Coeficiente de Dilatación Cúbica At = Incremento de temperatura = (tf - to) Te m p e r a tu ra 1 • Se define temperatu ra como la propiedad común a los cu erpos qu e s e encu entran en equilibrio térmico Equilibrio térmico •Sealatemperaturadel cuerpo calientet 1, su masam1 y su calor específicoc1 •Sealatemperaturadel cuerpofrío t 2, su masam2y su calor específico c2 •Seat mlatemperaturafinal de equilibrio Cua ndo dos cuerpos a dis tinta tempera tura , s e ponen en conta cto, a l ca bo decierto tiempo s e a ca ba n igua la ndo s us tempera tura s . Se dice que ha logra do el equilibrio térmico. Como Q cedido = Q absorbido m 1 · c 1 · (t 1 - t m) = m 2 · c 2 · (t m - t 2) 2• La temperatu ra es u na medida del calor o energía térmica de las partícu las en u na s u s tancia. 3• Se mide con los termómetros 4• El termómetro alcanza el equilibrio térmico con la mu es tra y nos indica la temperatura de la mis ma Escalas Termométricas Escala Celsius (ºC) • Es tablecido por Anders Celsius en 1741 • Utiliza dos temperaturas de referencia que s e llaman puntos fijos • Se divide el intervalo en 100 partes ( 1 ºC ) Escala Kelvin (ºK) • Propues ta por Lord Kelvin en 1854. Es la llamada es cala de temperaturas abs olutas . Sitúa el 0ºK en la temperatura a la que las moléculas de un cuerpo, no poseen Escala Fahrenheits (ºF) • Utilizada en el mundo anglos ajón y emplea los mis mos puntos fijos que la es cala centígrada pero los marca con los números 32 (fus ión) y 212 (ebullición), dividiendo el intervalo en 180 partes (1 ºF) Otra escala termométrica. Relación entre escalas • Escala Réaumur (º R) Establecida por René Antoine Réaumur, físico y naturalista francés que en 1730 popularizó el termómetro de alcohol con una escala 0 – 80, que dando la escala dividida en 80 partes ( 1 ºR ) • Relación entre escalas Calorímetro • Es un recipiente térmicamente aislado para evitar la fuga del calor • Se utiliza para determinar el calor especifico de un s olidó o liquido cualquiera Por el Principio de Regnault Sean: • Q1, el calor cedido por u n objeto • Q2 el calor abs orbido por otro objeto • Q3 el calor abs orbido por el calorímetro Se cu mple: Q1 = Q2 + Q3. Línea de Tiempo El Duque de Tos cana, cons truye el termómetro de bulbo de alcohol con capilar s ellado Cels ius , propus o los puntos de fus ión y ebullición del agua al nivel del mar (P=1 atm) como puntos fijos y una divis ión de la es cala en 1 00 partes (grados ). 1641 1592 Galileo dis eń a el primer termómetro 1740 1717 Fahrenheit cons truyó e introdujo el termómetro de mercurio con bulbo 1765 Jos eph Black introdujo los conceptos de calor es pecífico y de calor latente de cambio de estado. Con los concluyentes experimentos de Mayer y Joule, s e es tablece que el calor es una forma de energía. Es tablecen una corres pondencia entre la energía mecánica y el calor. Se as entaron las bas es para utilizar las máquinas de vapor para mover maquinaria indus trial, para el trans porte marítimo y terres tre. Watt ideó la s eparación entre el expans or y el condens ador y a partir de entonces empezó la fabricación a nivel indus trial. 1769 1842 1798 B. Thomps on (conde Rumford) rebatió la teoría del calórico de Black diciendo que s e podía generar continuamente calor por fricción, en contra de lo afirmado por dicha teoría. 1967 Se adopta la temperatura del punto triple del agua como único punto fijo para la definición de la es cala abs oluta de temperaturas y s e cons ervó la s eparación centígrada de la es cala Cels ius . Calor y Temperatura Objetos en contacto intercambiarán calor has ta alcanzar el equ ilibrio térmico (igu al temperatu ra) CALOR: Energía quefluyedeun cuerpoaotro TEMPERATURA: Esunamedida queindicadesdey haciadondefluiráel calor TERMÓMETROS: Están basadosen laspropiedadesfísicasdelosobjetosquepueden cambiar con latemperatura: •Volumen deun líquido •Longituddeun sólido •Presión deun gas •Resistenciaeléctricadeun sólido •Diferenciadepotencial eléctricoentredossólidos. Principios de la Calorimetría Primer Principio La cantidad de calor neces aria para elevar la temperatura de u n cu erpo es proporcional a s u mas a. Segundo Principio Q1 A B Q2 La cantidad de calor qu e s e neces ita para elevar la temperatura de u n cu erpo des de un valor A has ta un valor B es igual a la cantidad de calor qu e el cu erpo cede cuando s u temperatu ra desciende de B a A. Energía Térmica •Eslaformadeenergíaqueintervieneen losfenómenoscaloríficos. •Lacantidad deenergíatérmicarecibeel nombredecalor C a lo r y T r a b a jo CALOR TRABAJO Existe equilibrio cu ando la pres ión del gas s obre el embolo coincide con la pres ión del embolo s obre el gas Si la presión anterior aumenta, el émbolo s e elevará, obteniéndos e un trabajo de expans ión. Máquinas Térmicas Son dispositivos capaces de llevar a cabo la transformación del calor en trabajo mecánico . En todaslasmáquinastérmicasel sistema absorbecalor deun foco caliente; partedeél lo transformaen trabajo y el resto lo cedeal medio exterior queseencuentraamenor temperatura R e n d im ie n t o d e la s m á q u in a s El roza miento tra ns forma la energia cinética en ca lor. Suministrando calor al cuerpo no conseguimos que este se mueva. Sellamarendimiento deunamaquinatérmica al cocienteentreel trabajo realizado y el calor recibido del foco caliente. El rendimiento solo depende de las temperaturas T1 y T2. L e y f u n d a m e n t a l d e la c a lo r im e t r ía Un sistemaaislado compuesto por n cuerpos, adiferentestemperaturas, evolucionaespontáneamentehaciaun estado de equilibrio en el quetodoslos cuerpostienen lamisma temperatura. Los caloresintercambiadossumadoscon sus signosdan cero Σ Qi = 0 ¿De qué factores depende la cantidad de calor que puede transferirse a un cuerpo? ∆T , m, c • De la masa, • Del tipo de sustancia, • De la diferencia de temperaturas Ecuación fundamental de la calorimetría ∆ Q = mc ∆ T Q... cantidad de calor ► m... masa del cuerpo ► c... calor específico del cuerpo ► Δt... variación de temperatura ► ¿Quécantidad decalor necesitaabsorber un trozo decobrecuyamasaes 0.025gsi seencuentraaunatemperaturade8ºC y sedeseaquealcance unatemperaturafinal de20ºC? [ce = 0,093cal ] ∆ Q = mc ∆ T Q = 25gx 0.093cal x (20º - 8º ) 0.025 Kg. = 25 g Q = 25gx 0.093cal x 12º Q = 27,9calorías Latemperaturadelasuperficiedel Sol esdeunos6000ºK . Expréseseesa temperaturaen laescalaFahrenheit TC ( TF − 32) = 5 9 TC = 5 ( TF − 32) 9 TC = TK − 273,16 9 TF = ⋅ ( TK − 255,37 ) 5 = 10340,33 [ º F] Un trozo dehielo de10[gr] y temperatura–10[ºC] seintroducen en 1,5[Kg] deaguaa75[ºC]. Determinelatemperaturafinal delamezcla. c hielo = 0,45[ cal gr º C ] L fusión , hielo = 80[ cal gr ]. Q1 + Q2 +Q3 + Q4 = 0 mhielochielo( 0− (−10)) + mhielocagua (Te − 0) + mhieloLfusión + maguacagua ( Te − 75) T e= 73,94[ ºC ].