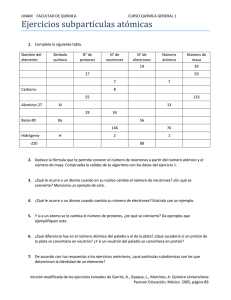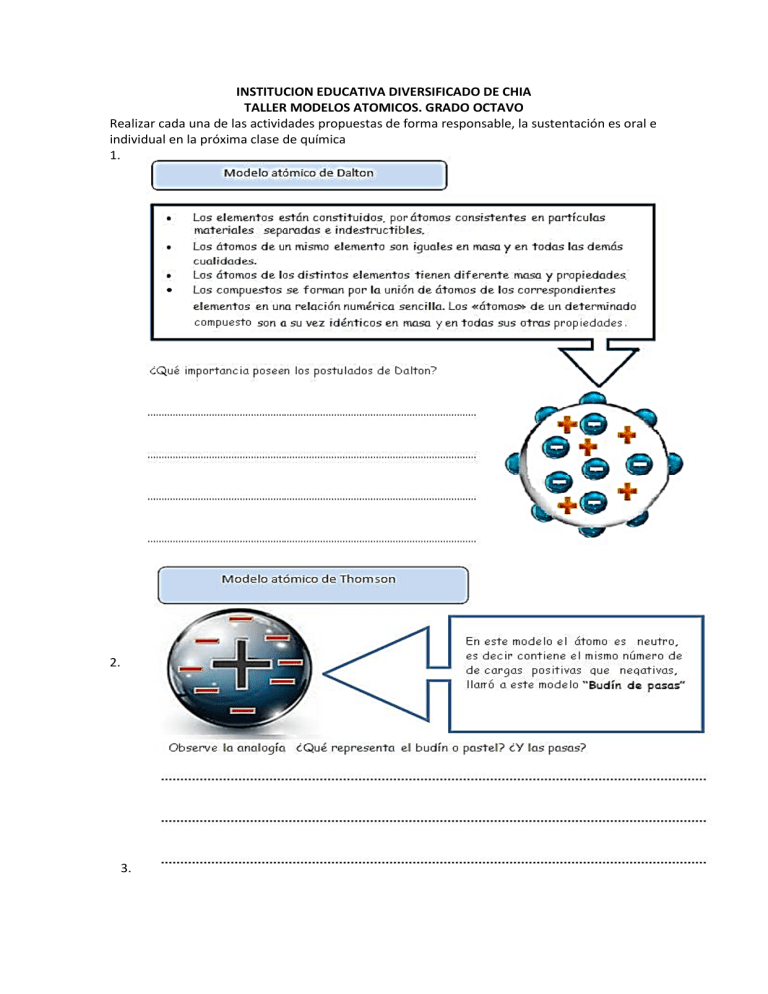
INSTITUCION EDUCATIVA DIVERSIFICADO DE CHIA TALLER MODELOS ATOMICOS. GRADO OCTAVO Realizar cada una de las actividades propuestas de forma responsable, la sustentación es oral e individual en la próxima clase de química 1. 2. 3. 4. 5. 5. ¿Qué significa que la energía del electrón esté cuantizada? ¿Qué significa que la energía del electrón esté cuantizada? ………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………… ………………..…................................................................................................................................. Si no comprendió está pregunta ¡¡¡Le ayudaremos!!! Una materia está cuantizada cuando se dispone de ella en cantidades específicas. Por ejemplo cuando compra leche está se encuentra en caja con una medida determinada, puede comprar una o dos o tres cajas, el volumen de leche está cuantizado en términos del número de cajas. Los peldaños de una escalera representarían los niveles de energía en un átomo, estos se van acercando entre ellos a medida que tienden a alejarse del núcleo. 6. Mirando los modelos atómicos de Dalton, Thomson, Rutherford, Chadwick y Bohr, haga una comparación entre ellos, siguiendo los pasos que se indican en la tabla. CRITERIOS CUALIDADES DALTON THOMPSON RUTHERFORD BOHR PARTICULA CHADWID descubrió el neutrón electrones, protones y neutrones ANALOGIA budín de pasas 7. ESCRIBE F O V DE ACUERDO AL ENUNCIADO. a) El número atómico está dado por el número de neutrones. ( ) b) El número másico está dado por la cantidad de protones. ( ) c) La palabra átomo significa indivisible. ( ) d) La suma de protones y electrones da el número másico. ( ) e) Los modelos atómicos son suposiciones de cómo se cree que son los átomos. ( ) f) El sabio griego Demócrito realizó sus afirmaciones a partir de observaciones y experiencias. ( ) g) Todos los átomos de carbono tienen número atómico 6. ( ) 8. Un átomo de carbono tiene 6 protones y 6 neutrones. Determina cuál es su: a) Número atómico (Z):……………….. b) Número másico (A):……………………….. 9. Si un átomo de potasio tiene Z=19 y A=39, calcula: a) ¿Cuántos protones tiene?:………………………………… b) ¿Cuántos electrones presenta?:…………………………… c) ¿Cuántos neutrones contiene?:…………………………… 7. COMPLETE EL SIGUIENTE CUADRO: Elemento Símbolo Z A Protones Electrones Neutrones Azufre 16 16 Berilio Be 8 4 Cobre 27 36 ELEMENTO SIMBOLO Z 16 A PROTONES 8 4 NEUTRONES 16 ELECTRONES 36 27 Be 9. Realizar el dibujo según Bohr de los elementos estudiados en el cuadro anterior( punto8) EVALUACION MODELOS ESTUDIADOS I. PREGUNTAS DE SELECCIÓN MULTIPLE CON UNICA RESPUESTA 1. Los electrones para el último nivel de energía de un elemento que tiene número atómico 35 es de: Justifica tu respuesta. A. 53 B. 7 C. 5 D. 4 JUSTIFICACION 2. El modelo atómico conocido como pastel de pasas, en el que se planteaba que los protones y electrones se encontraba distribuidos en todo el átomo fue propuesto por A. Niels Bohr B. Jhon Dalton C. Jhon Thomson D. Ernest Rutherford 3. Dos de los científicos que plantearon que el átomo era una partícula indivisible fueron: A. Thompson B. Rutherford C. Demócrito y Leucipo D. Dalton. 4. El elemento plomo tiene una masa atómica de 207 y un número atómico de 82. El número de protones es de _____________ y neutrones_______. Justifique su respuesta. A. 207 B. 120 C. 82 D. 125. JUSTIFICACION 5. Para el elemento indio de número atómico 49 y masa atómica 115, el número de electrones es de ________________ y en el último tiene posee electrones. Justifique su respuesta. A. 115 B. 66 C. 49 D. 3 JUSTIFICACION 6. Un átomo que tiene 11 protones en su núcleo: A. Cuál es su número atómico B. Cuál es su carga nuclear C. A que elemento pertenece D. Cuál es su carga nuclear II. Completa el siguiente cuadro con ayuda de la tabla periódica: SUSTANCIA NUMERO NUMERO No DE No DE MASICO ATOMICO PROTONES NEUTRONES AZUFRE CARBONO SILICIO CALCIO HIERRO ALUMINIO SODIO No DE ELECTRONES III. Halle la configuración electrónica indicando grupo y periodo para los siguientes elementos químicos: 1) ¿En cuál grupo y periodo se ubicará el elemento con número atómico Z=17? 2) ¿En cuál grupo y periodo se ubicará el elemento con número atómico Z= 35? 3) ¿En cuál grupo y periodo se ubicará el elemento con número atómico Z=47? 11) ¿En cuál grupo y periodo se ubicará el elemento con número atómico Z=55? IV Interpreta Taller presentado por: Lic. Nydia Sánchez R. V Argumenta Taller presentado por: Lic. Nydia Sánchez R. Taller presentado por: Lic. Nydia Sánchez R.