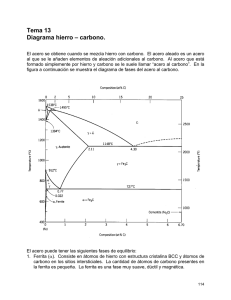
5.1 Introducción En el diagrama de equilibrio o de fases, Fe-C se representan las transformaciones que sufren los aceros al carbono con la temperatura, admitiendo que el calentamiento (o enfriamiento) de la mezcla se realiza muy lentamente de modo que los procesos de difusión (homogeneización) tienen tiempo para completarse. Uno de los materiales de fabricación y construcción más versátil, más adaptable y más ampliamente usado es el ACERO. A un precio relativamente bajo, el acero combina la resistencia y la posibilidad de ser trabajado, lo que se presta para fabricaciones mediante muchos métodos. Además, sus propiedades pueden ser manejadas de acuerdo a las necesidades específicas mediante tratamientos con calor, trabajo mecánico, o mediante aleaciones.Los materiales No Ferrosos no contienen hierro. Estos incluyen el aluminio, magnesio, zinc, cobre, plomo y otros elementos metálicos. Las aleaciones el latón y el bronce, son una combinación de algunos de estos metales No Ferrosos y se les denomina Aleaciones No Ferrosas. El Acero es básicamente una aleación o combinación de hierro y carbono (alrededor de 0,05% hasta menos de un 2%). Algunas veces otros elementos de aleación específicos tales como el Cr (Cromo) o Ni (Níquel) se agregan con propósitos determinados. Si la aleación posee una concentración de carbono mayor al 2,0% se producen fundiciones que, en oposición al acero, son quebradizas y no es posible forjarlas sino que deben ser moldeadas. 5.2 Definiciones Austenita:Fase γ, una solución solida intersticial de carbono en hierro FCC. La máxima solubilidad en estado del carbono en la austenita es del 2%. [1] Austenización: Calentamiento de un acero dentro de un rango de temperatura de la austenita para que su composición se convierta en austenita. La temperatura de la austenización varia dependiendo de la composición del acero. [1] Ferrita: Fase α, una solución solida intersticial de carbono en hierro BCC. La máxima solubilidad solida de carbono en hierro BCC es del 0,02%. [1] Cementita: El compuesto intermetálico Fe3C; una sustancia dura y quebradiza. [1] Perlita: Una mezcla de fases ferrita y cementita en laminas paralelas producida por la descomposición eutectoide de la austenita. [1] Eutectoide: Acero con un 0,8% C. [1] Hipoeutectoide: Acero con menos de 0,8% C. [1] Hipereutectoide: Acero con un 0,8% C a un 2% C. [1] Alotropía del Hierro: Muchos elementos y compuestos existen en más de una forma cristalina, bajo diferentes condiciones de temperatura y presión. Este fenómeno es determinado como polimorfismo o alotropía. Muchos metales industrialmente importantes como el hierro, titanio y cobalto experimentan transformaciones alotrópicas a elevadas temperaturas y a presión atmosférica. [1] Acero: Es toda aleación Fe-C entre 0,008% y 1,76% de Carbono. 5.3 Diagrama Hierro Carbono (Fe-C) En el diagrama de fase del Fe se observa las formas alotrópicas del hierro sólido, BCC y FCC, a distintas temperaturas: Hierro alfa (α): Cristaliza a 768 ºC. Su estructura cristalina es BCC con una distancia interatómica de 2.86 Å. Prácticamente no disuelve en carbono. Hierro gamma (γ): Se presenta de 910ºC a 1400ºC. Cristaliza en la estructura cristalina FCC con mayor volumen que la estructura cristalina de hierro alfa. Disuelve fácilmente en carbono y es una variedad de Fe amagnético. Hierro delta (δ): Se inicia a los 1400ºC y presenta una reducción en la distancia interatómica que la hace retornar a una estructura cristalina BCC. Su máxima solubilidad de carbono es 0.007% a 1487ºC. No posee una importancia industrial relevante. A partir de 1537ºC se inicia la fusión del Fe puro. Según el porcentaje de carbono las aleaciones Hierro-Carbono puede clasificarse en: Aceros %C ≤1.76%. Fundiciones %C≥1.76% – 6.667%C El carbono puede presentarse en tres formas distintas en las aleaciones Fe-C: En solución intersticial. Como carburo de hierro. Como carbono libre o grafito. Figura 5.1 Diagrama Hierro Carbono. [3] El estado actual del diagrama de equilibrio de las aleaciones hierro−carbono fue establecido como resultado de las investigaciones hechas por varios científicos. La elaboración de este diagrama fue empezada por D. Chernov, quien estableció en 1968 los puntos críticos del acero. Más tarde volvió a estudiar reiteradamente este diagrama. N. Gutovski, M. Wittorft, Roberts Austen, Roozebom hicieron una gran aportación al estudio de este diagrama. Los últimos datos acerca del diagrama están expuestos en las obras de I. Kornilov. Las aleaciones hierro−carbono pertenecen al tipo de aleaciones que forman una composición química. El carbono se puede encontrar en las aleaciones hierro−carbono, tanto en estado ligado (Fe3C), como en estado libre (C, es decir, grafito), por eso, el diagrama comprende dos sistemas: Fe−Fe3C (metaestable); este sistema está representado en el diagrama con líneas llenas gruesas y comprende aceros y fundiciones blancas, o sea, las aleaciones con el carbono ligado, sin carbono libre (grafito). Fe−C (estable); en el diagrama se representa con líneas punteadas; este sistema expone el esquema de formación de las estructuras en las fundiciones grises y atruchadas donde el carbono se encuentra total o parcialmente en estado libre (grafito). Para estudiar las transformaciones que tienen lugar en aceros y fundiciones blancas se emplea el diagrama Fe−Fe3C, y para estudiar fundiciones grises, ambos diagramas (Fe−Fe3C y Fe−C). Temperatura a que tienen lugar los cambios alotrópicos en el hierro está influida por elementos de aleación, de los cuales el más importante es el carbono. Muestra la porción de interés del sistema de aleación hierro − carbono. Esta la parte entre hierro puro y un compuesto intersticial, carburo de hierro, Fe3C, que contiene 6.67 % de carbono por peso; por tanto, esta porción se llamará diagrama de equilibrio hierro − carburo de hierro. Este no es un verdadero diagrama de equilibrio, pues el equilibrio implica que no hay cambio de fase con el tiempo; sin embargo, es un hecho que el compuesto carburo de hierro se descompondrá en hierro y carbono (grafito). Figura 5.2 Diagrama Hierro- Carbono [21] El diagrama hierro carbono tiene los siguientes puntos críticos. Figura 5.3 Puntos críticos en Diagrama Fe-C [21] Figura 5.4 Diagrama Fe-C. [4] Con el fin de brindar los datos exactos de la cantidad de cada uno de los componentes en un punto determinado del diagrama, se puede ingresar al siguiente link http://www.steeluniversity.org/content/html/spa/phase-diagram.asp, donde encontrara una aplicación, que permite establecer con toda exactitud las temperaturas exactas de los puntos así como el porcentaje de hierro y carbono. 5.4 Fases Del Diagrama Hierro Carbono 5.4.1 Fase Austenítica (0 hasta 2,1% C) La austenita es el constituyente más denso de los aceros y está formado por una solución sólida por inserción de carbono en hierro gamma, como lo muestra la Figura 5.3 La cantidad de carbono disuelto, varía de 0 a 2.1 % C que es la máxima solubilidad a la temperatura de 1130 °C. La austenita presenta las siguientes características: Baja temperatura de fusión. Baja tenacidad. Excelente soldabilidad. No es magnética. La austenita está formada por cristales cúbicos centrados en las caras estructura (FCC). Figura 5.5 Microestructura interna de la austenita. [6] 5.4.2 Fase Ferrítica 5.4.2.1 Ferrita alfa α (0 hasta 0,022%C) Es el nombre dado a la solución sólida α. Su estructura cristalina es BCC con una distancia interatómica de 2.86 Å. Prácticamente no disuelve en carbono, como se puede observar en la Figura 5.4, donde se tiene un acero con bajo porcentaje de carbono. La máxima solubilidad es 0,022% de C a 727°C, y disuelve sólo 0,008% de C a temperatura ambiente. Figura 5.6 Microestructura interna de la ferrita. [7] 5.4.2.2 Ferrita delta δ (0 hasta 0,09%C) Se inicia a los 1400ºC y presenta una reducción en la distancia interatómica que la hace retornar a una estructura cristalina BCC. Su máxima solubilidad de carbono es 0.007% a 1487ºC. Las características de la ferrita δ son: Muy blanda. Estructura cristalina BCC Es magnética. Muy poca posibilidad de disolución del carbono. La ferrita experimenta a 912°C una transformación polimórfica a austenita FCC o hierro γ. No posee una importancia industrial relevante. A partir de 1537ºC se inicia la fusión del Fe puro. La ferrita δ es como la ferrita α, y sólo se diferencian en el tramo de temperaturas en el cual existen. 5.4.3 Fase Cementita (0,022% a 6,67%C) Se forma cementita (Fe3C) cuando se excede el límite de solubilidad del carbono en ferrita α por debajo de 727°C (la composición está comprendida en la región de fases α+Fe3C). La cementita, desde el punto de vista mecánico, es dura y frágil, y su presencia aumenta considerablemente la resistencia de algunos aceros. La cementita se presenta de forma oscura al ser observada al microscopio como se puede ver en la Figura 5.5, Estrictamente hablando, la cementita es sólo metaestable; esto es, permanece como compuesto a temperatura ambiente indefinidamente. Pero si se calienta entre 650 y 700°C durante varios años, cambia gradualmente o se transforma en hierro α y carbono, en forma de grafito, que permanece al enfriar hasta temperatura ambiente. Es decir, el diagrama de fases no está verdaderamente en equilibrio porque la cementita no es un compuesto estable. Sin embargo, teniendo en cuenta que la velocidad de descomposición de la cementita es extraordinariamente lenta, en la práctica todo el carbono del acero aparece como Fe3C en lugar de grafito y el diagrama de fases hierro-carburo de hierro es, en la práctica, válido. Figura 5.7 Microestructura interna de la cementita[8] Las zonas oscuras corresponde a cementita que es el mayor constituyente en la fundición blanca, las zonas claras corresponden a perlita La cementita posee las siguientes propiedades: Alta dureza. Muy frágil. Alta resistencia al desgaste. 5.4.4 Fase Ledeburita La ledeburita no es un constituyente de los aceros, sino de las fundiciones. Se encuentra en las aleaciones Fe-C cuando el porcentaje de carbono en hierro aleado es superior al 25%, es decir, un contenido total de 1.76% de carbono. La ledeburita se forma al enfriar una fundición líquida de carbono (de composición alrededor del 4.3% de C) desde 1130ºC, siendo estable hasta 723ºC, descomponiéndose a partir de esta temperatura en ferrita y cementita. Está formada por 52% de cementita y 48% de austenita. La ledeburita no existe a temperatura ambiente en las fundiciones ordinarias debido a que en el enfriamiento se transforma en cementita y perlita; sin embargo en las fundiciones se puede conocer las zonas donde existió la ledeburita por el aspecto eutéctico con que quedan las agrupaciones de perlita y cementita. Figura 5.8 Microestructura interna de la ledeburita [8] 5.4.5 Fase Perlita Es la mezcla eutectoide que contiene 0,77 % de C y se forma a 727°C a un enfriamiento muy lento. Es una mezcla muy fina, tipo placa o laminar de ferrita y cementita. Se le da este nombre porque tiene la apariencia de una perla al observarse microscópicamente a pocos aumentos. Cuando esta estructura laminar es muy fina (las láminas son muy delgadas) la perlita se ve al microscopio óptico como negra. Sin embargo ambas fases, ferrita y cementita en condiciones normales de ataque son blancas. El color oscuro o negro lo producen el gran número de límites de grano existentes entre la matriz ferrítica y las láminas de cementita. Se comprende que cuanto más anchas sean las láminas (se habla entonces de perlita abierta o basta) la tonalidad se irá aclarando hasta poder distinguirse las distintas láminas, no por ello la perlita pierde su carácter de microconstituyente. Hay dos tipos de perlita: Perlita fina: dura y resistente. Perlita gruesa: menos dura y más dúctil. La perlita gruesa es más dúctil que la perlita fina a consecuencia de la mayor restricción de la perlita fina a la deformación plástica. Mecánicamente las perlitas tienen las propiedades intermedias entre la blanda y dúctil ferrita y la dura y quebradiza cementita. Figura 5.9 Micro-estructura interna de la perlita [9] 5.2.6 Fase Grafito Cuando las aleaciones hierro carbono, exceden el 2% de carbono se tiende a formar grafito, en la matriz de la aleación. Es especialmente cierto en la fundición gris, donde el grafito aparece en forma de escamas y es una característica predominante de la microestructura. En la Figura 5.8 se observa la una forma típica del grafito, la cual muestra la formación de este en forma de esferas. Figura 5.10 Microestructura interna del grafito [8] Es bastante duro, por lo que una cantidad elevada de grafito hace que la aleación sea muy dura pero a la vez, muy frágil, además los copos de grafito imparten una buena maquinabilidad actuando como rompe virutas, y también presentan una buena capacidad de amortiguación. El grafito se puede clasificar en varios tipos: El grafito tipo A: Es obtenido cuando son utilizadas bajas velocidades de solidificación. Una fundición que presente este tipo de grafito adquiere propiedades como superficie mejor acabadas, respuesta rápida a algunos tratamientos térmicos, baja dureza, alta tenacidad y alta ductilidad. El grafito tipo B: Se presenta en una fundición que presenta una composición casi eutéctica. El grafito tipo C: Aparece en hierros hipereutécticos, preferiblemente con altos contenidos de carbono. Los grafitos tipo D y E: S forman cuando las velocidades de enfriamiento son altas pero no tan altas como para formar carburos. Sus propiedades son alta dureza y resistencia a la tracción, baja ductilidad y baja tenacidad. 5.5 Aceros Acero es la denominación que comúnmente se le da, en ingeniería metalúrgica, a una aleación de hierro con una cantidad de carbono variable entre el 0,08% y el 1,76% en peso de su composición, dependiendo del grado. No se debe confundir el acero con el hierro, que es un metal relativamente duro y tenaz, con temperatura de fusión de 1.535 °C y punto de ebullición 2.740 °C. El acero conserva las características metálicas del hierro en estado puro, pero la adición de carbono y de otros elementos tanto metálicos como no metálicos mejora sus propiedades físico-químicas. Existen muchos tipos de acero en función del o los elementos aleantes que estén presentes. La definición en porcentaje de carbono corresponde a los aceros al carbono, en los cuales este no metal es el único aleante, o hay otros pero en menores concentraciones. [5] El acero es actualmente la más importante aleación mecánica empleándose de forma intensiva en numerosas aplicaciones como bienes de equipo (máquina-herramienta), construcción, etc. 5.5.1 Nota Histórica: Hierro y Acero El hierro se descubrió en algún momento de la edad del bronce. Probablemente se sacó de entre las cenizas de fuegos encendidos cerca de los depósitos de minerales de hierro. La ubicación del metal creció, sobrepasando finalmente al bronce en importancia. La edad del hierro se ubica generalmente alrededor del año 1200 a.C . Mediante hallazgos de artefactos hechos de hierro en la gran pirámide de Gizeh en Egipto, que data del 2900 a.C. En Israel se han descubierto hornos para el beneficio del hierro que datan del 1300a.C. en Asiria ( al norte de Irak ) se fabricaron por el año 1000 a. C. carros de hierro, espadas y herramientas. Los romanos heredaron el trabajo del hierro de sus provincias.; principalmente de Grecia, y desarrollaron la tecnología a nuevas alturas y la difundieron a través de Europa. Las antiguas civilizaciones aprendieron que el hierro era más duro que el bronce y que adquiría un mejor filo y más fuerte. La invención del cañón en Europa durante la Edad Media creó la primera demanda real del hierro: sólo hasta entonces el uso del hierro sobrepasó finalmente del cobre y del bronce. También la estufa de fundición de hierro, como artículo doméstico de los siglos XVII y XVIII. Contribuyó a incrementar significativamente la demanda de hierro. Durante el siglo XIX, industrias como la construcción, los ferrocarriles, la construcción de barcos, la maquinaria y la industria militar, crearon un dramático crecimiento en la demanda de hierro y acero en Europa y en América. No obstante que fue posible producir grandes cantidades de arrabio (crudo) en los altos hornos, los procesos subsiguientes para producir hierro forjado y acero eran lentos. La necesidad de incrementar la productividad de estos metales básicos fue la “madre invención”. Henry Bessemer desarrolló en Inglaterra el proceso para soplar aire a través del hierro fundido que condujo a la invención del convertidor Bessemer (patentado en 1856). Los hermanos Pierre y Emile Martin construyeron en Francia el primer horno de hogar abierto en 1864. Estos métodos permitieron producir hasta 15 toneladas de acero en un solo lote (hornada), un adelanto significativo sobre los métodos anteriores. La expansión de los ferrocarriles en Estados Unidos después de la Guerra Civil creó una enorme demanda de acero. Entre 1880 1890 se empezaron a usar las vigas de acero para la construcción en cantidades significativas la construcción en cantidades significativas. Las construcción de rascacielos empezó a depender de este acero estructural. Hacia el final del siglo XIX. Fue posible disponer de electricidad en cantidades suficientes, se usó esta fuente de energía para producir acero. El primer horno eléctrico comercial para la producción de acero se puso en operación en Francia en 1899. Para 1920, éste se había convertido en el principal proceso para fabricar acero de aleación. El uso de oxígeno puro en la producción de acero se inició un poco antes de la Segunda Guerra Mundial en varios países europeos y en Estados Unidos. Los trabajos en Austria después de la guerra culminaron con el desarrollo del horno básico de oxígeno (BOF, por sus siglas en inglés de basic oxygen furnace).Éste se ha convertido en la tecnología moderna para producir acero. Alrededor de 1970 sobrepasó al método de hogar abierto. El convertidor Bessemer había sido superado en 1920 por el método de hogar abierto, y dejó de ser un método de producción comercial de acero 1971. Figura 5.11 [22] 5.5.2 Acero Eutectoide Presentan una fase austenítica sólida a un composición de 0.89% C con granos orientados al azar. Al enfriar desde esta fase, se desarrollan las fases ferrita y cementita en láminas, formando una microestructura única llamada “perlita”, como se observa en la Figura 5.9, la cual, en relación con las propiedades mecánicas posee características intermedias de las fases que la componen, entre blanda y dúctil y dura y quebradiza. Figura 5.12 Transformación y microestructura de un acero eutectoide [6] La microestructura del acero eutectoide enfriado lentamente a través de la temperatura eutectoide es análoga a la de una aleación de composición eutéctica; es decir, se forman capas o láminas alternas de las dos fases (α y Fe3C) durante la transformación. 5.5.3 Acero Hipoeutectoide Se denomina acero hipoeutectoide a las aleaciones entre 0,008% y 0,89% de carbono según el diagrama hierro-carbono. El acero hipoeutectoide está formado por una mezcla de ferrita más perlita. Presentan una fase austenítica sólida a una composición inferior a 0.89% C con granos orientados al azar. Al enfriar comienza a desarrollarse la ferrita y se entra en la región bifásica α + γ donde la ferrita sufre una segregación formándose en los límites de grano de la fase γ. Al sobrepasar en enfriamiento a la línea A1 la austenita se transforma en perlita y se forma el acero. Los aceros hipoeutectoides pueden ser usados en elementos de máquinas (Elementos de sujeción y transmisión de potencia) y tienen las siguientes características: Al carbono y también aleados. Son plásticos y poseen buena resistencia mecánica. Bajo carbono hasta 0.2 % C, medio carbono 0.2%-0.5% C y alto carbono 0.5 %C. Figura 5.13 Transformación y microestructura de un acero hipoeutectoide [6] Los aceros hipoeutectoides se pueden dividir en tres tipos: Acero bajo en carbono: El porcentaje de carbono estos aceros no supera el 0,2%, se llaman aceros ferríticos, son muy suaves, dúctiles, deformables y de baja resistencia. Acero al carbono medio: A este grupo pertenecen la mayoría del acero comercial que se produce, su porcentaje de carbono está comprendida entre el 0,2% y el 0,5%. Sus propiedades dependen de la cantidad de ferrita y perlita que tienen y varían sus prestaciones en un rango muy amplio. Aceros de alto carbono: Estos aceros tienen un porcentaje de carbono comprendido entre el 0,5% y el 0,77%, se denominan aceros perlíticos. Se resistencia y dureza son elevadas pero su ductilidad y tencidad son bajas. 5.5.4 Acero hipereutectoide Se denomina acero hipereutectoide a aquellos aceros que en su composición y de acuerdo con el diagrama hierro-carbono tienen un porcentaje de carbono entre 0,89% y 1,76%. Su constituyente principal es la cementita (Carburo de hierro (Fe3C)). Es un material duro y de difícil mecanización. Presentan una fase austenítica a una composición superior a 0.89% C pero inferior a 1.76 %C con granos orientados al azar. Al enfriar comienza a formarse la cementita y se entra en la región bifásica γ+cem donde la cementita comienza a formarse en los límites de grano de la austenita. Al sobrepasar en enfriamiento a la línea A1 la austenita remanente se transforma en perlita y se forma el acero. Al descender por debajo de la temperatura eutéctica, toda la austenita remanente de composición eutectoide se transforma en perlita; de este modo, la microestructura resultante consiste en perlita y cementita proeutectoide como micro constituyentes una forma de típica asi como el diagrama de transformación de observan en la Figura 5.11. Los aceros hipereuctectoides presentan las siguientes características: Generalmente aleados. Muy alta resistencia mecánica. Mayor módulo de Young, muy elásticos. Alta resistencia mecánica y muy alta dureza. Figura 5.14 Transformación y microestructura de un acero hipereutectoide. [6] 5.6 Clasificación De Los Aceros Existe una gran variedad en la forma de identificar y clasificar a los aceros. Sin embargo, la mayoría de los aceros utilizados industrialmente presentan una designación normalizada expresada por medio de cifras, letras y signos. Hay dos tipos de designaciones para cada tipo de material, una simbólica y otra numérica. La designación simbólica expresa normalmente las características físicas, químicas o tecnológicas del material y, en muchos casos, otras características suplementarias que permitan su identificación de una forma más precisa. Por otro lado, la designación numérica expresa una codificación alfanumérica que tiene un sentido de orden o de clasificación de elementos en grupos para facilitar su identificación. En este caso, la designación no tiene un sentido descriptivo de características del material. En general, cuando se acomete el tema de hacer una clasificación de los aceros, ésta dará resultados diferentes según el enfoque que se siga. Así, se puede realizar una clasificación según la composición química de los aceros, o bien, según su calidad. También se pueden clasificar los aceros atendiendo al uso a que estén destinados, o si se quiere, atendiendo al grado de soldabilidad que presenten. La alta variedad de aceros ha hecho surgir una alta gama de normatividad que puede cambiar de un país a otro algunas de estas son: ANSI (American National Standards Institute) ACI (American National Standards Institute), AWS (American Welding Society), ASME (American Society of Mechanical Engineers CENIM (Centro Nacional de Investigaciones Metalúrgicas) 5.6.1 La Norma AISI-SAE AISI es el acrónimo en inglés de American Iron and Steel Institute (Instituto americano del hierro y el acero), mientras que SAE es el acrónimo en inglés de Society of Automotive Engineers (Sociedad de Ingenieros Automotores) esta utiliza un esquema general para realizar la clasificación de los aceros de 4 dígitos (Y Z XX). También pueden incluir un prefijo mediante letras para indicar el tipo de proceso de manufactura. XX: Nos indica el porcentaje (%) contenido de carbono multiplicado por 100 Z: Para aceros de aleación simple indica el porcentaje aproximado del elemento predominante de aleación. Y: Nos indica el tipo de acero o de la aleación. Y Puede tomar valores de 1 a 8 para designar tipo de aceros o aleación a continuación veremos según el número que significa. Y=1: aceros al Carbono (corriente u ordinario); Y=2: aceros al Níquel; Y=3: aceros al Níquel-Cromo; Y=4: aceros al Molibdeno, Cr-Mo, Ni-Mo, Ni-Cr-Mo; Y=5: aceros al Cromo; Y=6: aceros al Cromo-Vanadio; Y=7: esta numeración indica que son aceros resistentes al calor, pero estos no se fabrican habitualmente. Y=8: al Ni-Cr-Mo; Figura 5.15 Esquema General Clasificación aceros. [10] Ejemplos de aplicación para la correcta interpretación de la norma AISI- SAE. Designar los siguientes tipos de aceros. AISI 1020: 1: Para indicar que se trata de un acero corriente u ordinario. 20: Contenido máximo de carbono del 0.20%C. AISI 1045: 1: acero corriente u ordinario. 0: no aleado. 45: 0.45 %C. AISI 3215: 3: acero al Níquel-Cromo; 2: contenido del 1.6% de Ni, 1.5% de Cr. 15: contenido del 0.15% de carbono (C). En la Tabla 5.1 podemos encontrar una completa comparación entre las normas AISI, SAE y UNS para la clasificación de aceros con aleantes, no obstante, la composición de los aceros no es exacta, sino que existe un rango de tolerancia aceptable en referencia a los valores indicados en normas o catálogo. Tabla 5.1 Clasificación de los aceros según diferentes tipos de normas [11] Viendo la gran variedad de aceros que existen en la industria las normas se vieron obligadas a crear nuevas formas de designar los aceros que iban sufriendo para dar una correcta información tanto de su composición química como el uso o la forma como debe ser tratada es así como en la Tabla 5.2 se pueden observar la designación o símbolo para cada tipo acero rápido según su aplicación. Tabla 5.2 Códigos para la designación de aceros rápidos según la norma AISI. [12] Tabla 5.3 Relación entre la nomenclatura AISI-SAE con las propiedades mecánicas del acero[12] En la Tabla 5.3 se puede observar como un acero con un porcentaje de carbono que va desde un 0.1%C hasta 0.8%C varía sus propiedades a la resistencia, esto nos permite en forma ordenada y clara seleccionar el material adecuado que deseamos utilizar. En la Tabla 5.4 se indican los principales aleantes para los aceros comerciales, los aceros aleados presentan un porcentaje de cada uno de los elementos de la tabla, mientras los simples comunes u ordinarios solo presentan dentro de su constitución dos o tres elementos aleantes como máximo. Tabla 5.4 Principales componentes de los aceros comerciales.[12] Los diferentes tipos de acero se pueden también clasificar de acuerdo a los elementos de aleación que producen distintos efectos en el Acero: 5.6.2 Aceros Al Carbono Más del 90% de todos los aceros son aceros al carbono. Estos aceros contienen diversas cantidades de carbono y menos del 1,65% de manganeso, el 0,60% de silicio y el 0,60% de cobre. Entre los productos fabricados con aceros al carbono figuran máquinas, carrocerías de automóvil, la mayor parte de las estructuras de construcción de acero, cascos de buques, somieres y horquillas. 5.6.3 Aceros Aleados Estos aceros contienen un proporción determinada de vanadio, molibdeno y otros elementos, además de cantidades mayores de manganeso, silicio y cobre que los aceros al carbono normales. Estos aceros de aleación se pueden subclasificar en: 5.6.3.1 Aceros Estructurales Es fundamentalmente una aleación de hierro (mínimo 98 %), con contenidos de carbono menores del 1 % y otras pequeñas cantidades de minerales como manganeso, para mejorar su resistencia. Y el fósforo, azufre, sílice y vanadio para mejorar su soldabilidad y resistencia a la intemperie. Es un material usado para la construcción de estructuras, de gran resistencia, producido a partir de materiales muy abundantes en la naturaleza. Entre sus ventajas está la gran resistencia a la tensión y compresión y el costo razonable. A pesar de la susceptibilidad al fuego y a la intemperie es el material estructural más usado, por su abundancia, facilidad de ensamblaje y costo razonable. La alta resistencia del acero por unidad de peso, permite estructuras relativamente livianas, lo cual es de gran importancia en la construcción de puentes, y edificios altos. Sus propiedades no se alteran con el tiempo, ni varían con la localización en los elementos estructurales. Es el material que más se acerca a un comportamiento linealmente elástico, hasta alcanzar esfuerzos considerables. Permite soportar grandes deformaciones sin falla, alcanzando altos esfuerzos en tensión, ayudando a que las fallas sean evidentes. Tiene la capacidad de absorber grandes cantidades de energía en deformación (elástica e inelástica) y de unirse fácilmente con otros miembros (en perfiles se puede conectar fácilmente a través de remaches, tornillos o soldadura). La resistencia del acero puede disminuir cuando se somete a un gran número de inversiones de carga o a cambios frecuentes de magnitud de esfuerzos a tensión (cargas pulsantes y alternativas). 5.6.3.2 Aceros para herramientas. En este grupo se incluyen todos los aceros que normalmente se emplean para la fabricación de útiles o herramientas destinados a modificar la forma, tamaño y dimensiones de los materiales por cortadura, por presión o por arranque de viruta. Son aquellos aceros de alta calidad que se emplean en herramientas para cortar y modelar metales y no-metales. Por lo tanto, son materiales empleados para cortar y construir herramientas tales como taladros, escariadores, fresas, terrajas y machos de roscar. Los aceros de herramientas tienen generalmente un contenido en carbono superior a 0.30%, aunque a veces también se usan para la fabricación de ciertas herramientas, aceros de bajo contenido en carbono (0.1 a 0.30%). La templabilidad de los aceros aumenta con el contenido en elementos de aleación, excepto en el caso del cobalto, el cual es único elemento que la hace disminuir. En el caso de los aceros de herramientas, el término tenacidad se refiere más a la capacidad de sufrir golpes sin rotura que a la facultad de absorber energía durante la deformación. Los aceros de herramientas con contenidos en carbono medios y bajos, son los que presentan mejor tenacidad y constituyen el material utilizado en la fabricación de herramientas resistentes al choque. El acero de herramienta que presenta mejor maquinabilidad tiene un índice aproximadamente igual al 30%, por lo tanto como referencia para comparar la maquinabilidad de los distintos aceros de herramientas. La maquinabilidad y facilidad de trabajo de los aceros de herramientas disminuye al aumentar el contenido de carbono y elementos de aleados. Los aceros para herramientas se pueden clasificar como: Aceros al carbono: Para la fabricación de herramientas para los usos más diversos, se emplean aceros sin elementos de aleación con porcentajes de carbono variables de 0.50 a 1.40%. Para herramientas que deban tener gran tenacidad como martillos y picas; se emplean medios contenidos en carbono 0.50 a 0.70%. Para herramientas de corte como brocas, cuchillas, y limas; calidades intermedias de 0.70 a 1%. Aceros rápidos: La característica fundamental de estos aceros es conservar su filo en caliente, pudiéndose trabajar con las herramientas casi al rojo (Temperatura = 600ºC) sin disminuir su rendimiento. Algunas composiciones típicas de los aceros rápidos son: C = 0.75%, W = 18%, Cr = 4% y V = 1% ; otra C = 0.75%, W = 18%, Co = 4% y V = 1.25%. Aceros indeformables: reciben este nombre los aceros que en el temple no sufren casi deformaciones y con frecuencia después del temple y revenido quedan con dimensiones prácticamente idénticas a las que tenían antes del tratamiento. Esto se consigue empleando principalmente el cromo y el manganeso como elementos de aleación. Estos aceros templan con un simple enfriamiento al aire o en aceite. Composiciones típicas: C = 2% y Cr = 12%; C = 1% y Cr = 5% y otra C = 1% y Mn = 1%. Aceros al corte no rápidos: se agrupan varios aceros aleados, principalmente con cromo y wolframio, muy empleados para la fabricación de herramientas de corte que no deben trabajar en condiciones muy forzadas. Pueden considerarse como unas calidades intermedias entre los aceros rápidos y los aceros al carbono, y la mayoría de herramientas fabricadas con ellos suelen quedar con durezas comprendidas entre 60 y 66 Rockwell-C. 5.7 Fundiciones. Al igual que los aceros, las fundiciones son básicamente aleaciones hierro- carbono, con una alto porcentaje de carbono mayor que los aceros. Su concentración esta entre 1.76% y 6.67% de carbono. La mayoría de las fundiciones que se manufacturan comercialmente están entre 2,5% y 4% de carbono. El máximo porcentaje de carbono que es posible obtener en las aleaciones ferrosas es 6.67%. El mejor método para clasificar las fundiciones es de acuerdo con su estructura metalográfica. Las variables para definir los tipos de fundiciones son: El porcentaje de carbono. El contenido de aleación y de impurezas. La velocidad de enfriamiento. El tratamiento térmico después de la fusión en donde es posible observar grandes diferencias en la microestructura la cual define su forma física. El carbono puede estar libre, es decir en forma de grafito o puede estar combinado en forma de carburo de hierro en la cementita. La distribución del carbono sin combinar influirá en gran medida en las propiedades físicas de las fundiciones. Las fundiciones dependiendo del proceso de fabricación se puede clasificar como fundición gris y fundición blanca. 5.7.1 Fundición Blanca. La fundición blanca son aleaciones hipoeutécticas y las transformaciones que tienen lugar durante su enfriamiento son análogas a las de la aleación de 2,5 % de carbono. Se forma al enfriar rápidamente la fundición de hierro desde el estado líquido, durante el enfriamiento la austenita solidifica a partir de la aleación fundida en forma de dendritas. Se distinguen por que al fracturarse presenta un color blanco brillante. Si la velocidad de extracción de calor durante el paso del líquido a sólido, en una fundición de hierro es alta a raíz de un enfriamiento rápido, la solidificación del material se completa con la formación de un eutéctico Fe – Fe3C llamado ledeburita. El producto final se denomina Fundición blanca; siendo éste un material que se caracteriza por su color blanco en la fractura y por ser bastante dura y resistente al desgaste, por su gran cantidad de cementita, sin embargo es extremadamente frágil y difícil de mecanizar. La Fundición blanca es la de menor uso industrial. Es usada en casos en que la resistencia al desgaste es lo más importante y la aplicación a la cual está destinada no requiere buena ductilidad ni maleabilidad como es el caso de las camisas para mezcladoras de cemento, bolas de trituración para acería, camisas interiores de las hormigoneras. Las áreas oscuras corresponden a perlita, las cuales son dentritas de austenita trasnformada en (perlita). La región blanca corresponde a una matriz de cementita. Figura 5.16 Microestructura fundición blanca. [ 13] 5.7.2 Fundición Maleable. Esta fundición apareció del afán de ablandar la fundición blanca y convertirla en un material tenaz. La fundición maleable se obtiene a partir de la fundición blanca por calentamiento prolongado en atmósfera inerte (para prevenir la oxidación) a temperaturas entre 800 y 900 °C. Bajo estas condiciones la cementita se descompone para dar grafito en forma de racimos o rosetas dentro de la matriz ferrítica o perlítica de modo similar a la de la fundición esferoidal. La fundición maleable se suele emplear en tubos de dirección y engranajes de transmisión, muelles tubulares y partes de válvulas, también se utiliza como accesorios para cañerías, transmisión y conducción de líquidos y gases, piezas pequeñas, o piezas de bajo espesor. Microestructura fundición maleable (Grafito oscuro en forma de rosetas sobre una matriz de ferrita). Figura 5.17 Microestructura fundición maleable [2] Existen dos procedimientos para fabricar fundición maleable: M. Europeo (Corazón Blanco) Se debe tener una fundición blanca de la siguiente composición química: %C %Si %Mn %P %S Características: 2,5 a 3.3 0,5 a 1,25 0,5 0,1 0,1 Alargamiento 1 a 12 % M. Americano (Corazón Negro) Resistencia a la tracción 350 Mpa Para obtener una fundición de este tipo se requiere de: %C 2 a 2,75 %Si 0,5 a 1,2 %Mn %P %S 0,5 0,1 0,2 Alargamiento 1 a 20 % Características: Resistencia a la tracción 380 Mpa 5.7.3 Fundición Gris. Es una aleación hierro-carbono hipoeutéctica con un porcentaje entre 2.5 y 4.0 % y de silicio entre 1 y 3 %. El grafito suele aparecer como hilos dentro de una matriz de ferrita o perlita. Desde un punto de vista mecánico las fundiciones grises son frágiles y poco resistentes a la tracción, su resistencia y ductilidad a los esfuerzos de compresión son mayores. El hierro gris es uno de los materiales ferrosos más empleados y su nombre se debe a la apariencia de su superficie al romperse. Estas fundiciones amortiguan de forma óptima las vibraciones y en un mayor grado que los aceros, por lo que en sistemas de transmisión de potencia y mecanismos son muy utilizadas. A la temperatura de colada tienen mucha fluidez por lo que permite moldear piezas de formas complejas. Es además, uno de los materiales metálicos más baratos. Se utiliza en bloque de motores, tambores de freno, cilindros y pistones de motores. Hilos de grafito sobre una matriz de ferrita Figura 5.18 Micro-estructura fundición gris [2] Corresponden de izquierda a derecha a: • Matriz de perlita con cementita esferoidizada para trabajo a altas temperaturas. • Gris aleada, y consta de grafito tipo A con carburos libres (zonas blancas). • Templada y revenida, su microestructura consta de grafito en una matriz de martensita revenida. Figura 5.19 Microestructura de las clases de fundiciones grises [2] Cuando no se requieren unas características mecánicas muy exigentes, las condiciones más interesantes que en general conviene que cumplan estas fundiciones son: Que tengan buena colabilidad. Facilidad de mecanizado. Que no queden poros, para ello la temperatura de fusión debe ser baja y el contenido de carbono debe ser alto, aproximadamente de 3 a 3,75% y los contenidos de silicio entre 1,25 y 2,5% de tal forma que el CE= 4,3%. Caracteristicas: Dureza Carga rotura Resistencia Resiliencia compresión Mas blandas 15 kg/mm2 Mayor que las Muy baja que las grises grises 5.7.4 Mecanizado Se puede mecanizar Resistencia química Baja Fundición Nodular. Es una aleación Fe-C y Si, cuya microestructura está conformada por una matriz metálica y una cantidad del 10 al 15% de grafito en forma de esferas. La presencia de grafito afecta ciertas propiedades entre ellas la disminución de la dureza y la resistencia mecánica, pero por otro lado, incrementa la maquinabilidad. Ferríticas: Posee maquinabilidad, ductilidad y límite elástico moderado. Perlíticas: Buen límite elástico y ductilidad pero baja maquinabilidad, se pueden templar superficialmente. Tratadas térmicamente: Con tratamientos térmicos como normalizados, templados y revenidos o austemperadas, presentan alta resistencia a la tracción y alto límite elástico. La fundición nodular presenta una mayor resistencia a la tracción que la fundición gris y se suele utilizar para la fabricación de válvulas y engranajes de alta resistencia, cuerpos de bomba, cigüeñales y pistones. Se diferencia de la maleable porque generalmente se obtiene como resultado de la solidificación y no requiere tratamiento térmico. Esferoides de grafito sobre una matriz de ferrita. Figura 5.20 Microestructura fundición nodular [2] Caracteristicas: Módulo Elasticidad elasticidad 17500 Kg/mm2 65 a 85% Resistencia tracción 70 kg/mm2 y 3% alargamiento 5.7.5 Otras Fundiciones. 5.7.5.1 Fundición grafito compacto. Presenta propiedades intermedias entre la gris y la nodular; el grafito dentro de la matriz se presenta tanto en nódulos como en láminas en forma interconectada. Su resistencia a la tracción varía entre 40 y 85Ksi y el límite elástico entre 30 y 60Ksi con alargamientos entre 1 y 5%. Fundición grafito compacto, las zonas oscuras corresponden a la gran presencia de grafito. Figura 5.21 Microestructura de una función grafito compacto. [2] 5.7.5.2 Fundiciones chiliadas. En fundiciones grises, nodulares y de grafito compacto, se pueden inducir durante la solidificación la formación de fundición blanca en la superficie de las piezas recibe el nombre de chill y la fundición recibe el nombre de fundición chiliada. 5.7.5.3 Fundición moteada. Una fundición que solidifique a velocidades intermedias entre blanca y gris contendrá en su estructura grafito y cementita y se denomina fundición moteada o atruchada. 5.8 Diferencias Entre Los Aceros y Las Fundiciones. La diferencia fundamental entre los aceros y las fundiciones de hierro, es que los aceros por su ductilidad son fácilmente deformables en caliente bien por forja, laminación o extrusión, mientras que las fundiciones se fabrican generalmente por moldeo. De hecho al acero también se le ha venido conociendo como “hierro forjable” y a la fundición “hierro colado”en virtud de la técnica más favorable para trabajar el material. Las fundiciones de hierro son más resistentes a la corrosión y a los cambios súbitos de temperatura que los aceros. Las fundiciones presentan mayor porcentaje de carbono y por tanto son más duras y frágiles que los aceros. Los aceros son usados generalmente para la fabricación de piezas mecánicas, elementos de transmisión de potencia y herramientas de trabajo. Las fundiciones son usadas generalmente para la fabricación de piezas de gran tamaño como carcasas y bancadas. Las fundiciones poseen una maleabilidad y ductilidad casi nula comparada con los aceros que pueden ser sometidos a procesos de forjado y laminado. Las fundiciones son más fáciles de maquinar que los aceros. Figura 5.22 Cuadro comparativo aceros y fundiciones. [10] 5.9 Créditos. Recopilación y edición realizada por Mauricio Montoya Henao y Daniel Felipe Dávila Blandón estudiantes de ingeniería Mecánica de la universidad Tecnológica de Pereira 2012. También, por Evelin Bedoya Ospina y Juan Esteban Bedoya Gomez estudiantes de ingeniería Mecánica de la universidad Tecnológica de Pereira 2013. 5.10 Bibliografía. [1] William F. Smith, FUNDAMENTOS DE LA CIENCIA E INGENIERÍA DE MATERIALES, Tercera Edición. [2]ASM Metals HandBook [3] http://html.rincondelvago.com/materiales_9.html [4] http://www.centralclubs.com/diagram-t67924.html [5] http://es.wikipedia.org/wiki/Acero [6] Tesis de grado influencia de microestructura sobre las propiedades mecánicas en varillas de cero. Allauca Pancho Fabián Roberto. Escuela Superior Politécnica de Chimborazo. Ecuador 2011 [7] Marshalls etch + HF, 300x. Courtesy of A.O.Benscoter, Lehigh University [8] A.O. Benscoter, Lehigh University. [9]ASM Metals HandBook. Vol 3. Alloy Phase Diagram. [10]Autores. [11] http://es.scribd.com/doc/40912911/Clasificacion-de-los-aceros [12] http://ingemecanica.com/tutorialsemanal/tutorialn101.html#seccion35 [13] http://materialesdos.blogspot.com/2011_02_01_archive.html [14]http://enciclopedia.us.es/index.php/Acero [15]http://www.infoacero.cl/acero/que_es.htm [16]http://es.scribd.com/doc/30595021/Compendio-de-normas-acero [17]http://ingemecanica.com/tutorialsemanal/tutorialn101.html [18]http://materialesdos.blogspot.com/2011_02_01_archive.html [19]ASKELAND, Donald R. Ciencia e Ingeniería de los Materiales. 3. Ed. United Stated: Thomson Editorial. 2004 [20]ASM, International. Hand Book Metals, Vol 3. [21] http://4.bp.blogspot.com/_ypQZyFOEyRA/SjKA7ekm8uI/AAAAAAAADbQ/Iu2eRKNQhw/s1600-h/Diagrama+Fe-C.JPG [22] http://www.infoacero.cl/catalogo/images_csh/500_Personas/500_012.jpg