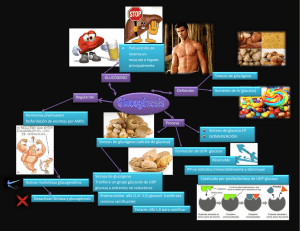
METABOLISMO DE LOS CARBOHIDRATOS Cap. 36 Integracion Metabolismo Lipidos y Carbohidratos. Lieberman, Michael (2013-0321T22:58:59). Mark. Bioquímica médica básica, 4.ª (Spanish Edition) Mblgo. Dr. Enrique Martin Alva Figura V.9. Principales vías del metabolismo de la glucosa Homeostasis de la glucosa. Acetil-CoA, acetil coenzima A DHAP, dihidroxiacetona fosfato AF, ácidos grasos OAA, oxaloacetato PEP, fosfoenolpiruvato ATC, ácidos tricarboxílicos TG, triacilgliceroles Metb. de AA y AG ESTAN INTERCONECADOS Hígado y Tej Adip. --------- Producción de glucosa I. REGULACIÓN DEL METABOLISMO DE CARBOHIDRATOS Y LÍPIDOS EN EL ESTADO DE ALIMENTACIÓN Luego de una comida, el hígado sintetiza glucógeno y triacilgliceroles. Después de un Ayuno Glucogeno ↑80 g a 200 a 300 g. Trigliceridos se empaquetan VLDL y se Almacena en tejido Adiposo glucogenogenesis y lipogénesis hepática , se regulan por enzimas clave en estas vías. Figura V.10. Vías reguladas por la liberación de glucagon ( Glucosa Sanguínea) e insulina ( Glucosa Sanguínea) Liberación de glucagón ← ↑ Glucogenolisis ↑ Gluconeogenesis ↑ Lipolisis ↓ Glucolisis hepática Glucosa Sanguínea Equilibrio intertisular Ayuno y Alimentación Cortisol, Epinefrina, Noradrenalina → Liberación de Insulina ↑ Glucogenogenesis ↑ Sintesis . Ac. Grasos ↑ Sintesis de Triacilglieridos ↑ Glucolisis hepática A. Mecanismos que afectan la síntesis de glucógeno y triacilglicerol en el hígado 1. GLUCOCINASA Glucose ATP ADP glucokinase high Km ⊕ Alimentacion = ↑[Insulina]= (Sintesis GK) Funcion hepática mantener niveles glucosa sérica ∴ hígado metaboliza glucosa sólo con azúcar altos Glucose-6-P Fructose-6-P phosphofructokinase-1 AMP + , F-2,6-BP ATP – , Citrate – +, Act. Alosterica (PFK-2 fosforilada.) Activa Act. Quinasa)), Fructose-1,6-BP Phosphoenolpyruvate pyruvate kinase Pyruvate – phosphorylation (cAMP-dependent) – Alanine + F-1,6-BP Reg. Desfosforilacion y ↑ Insulina/Glucagon 3. FOSFOFRUCTOCINASA-1 Y PIRUVATO CINASA Regulación de la glucógeno sintasa. Esta enzima se fosforila por una serie de cinasas, que se inician por la proteína cinasa AMPc dependiente, en condiciones de ayuno. Se desfosforila y está activa después de una comida y el glucógeno se almacena P, fosfato; ⊕, activado por 2. GLUCÓGENO SINTASA glycogen synthase– P (inactive) protein kinase A + Glucagon protein phosphatase ADP + Insulin ATP Pi glycogen synthase (active) Glycogen UDP-Glucose PPi UTP Glucose-1-P Glucose-6-P Glucose Activa desfosforilación ↑[insulina] ,↓ [glucagón] y ↑ [glucosa] 4. PIRUVATO DESHIDROGENASA Y PIRUVATO CARBOXILASA ∆(PDH) = desfosforilada ,↑sustratos y ↑(ADP) y la ↑insulina P Pyruvate dehydrogenase inactive ADP – kinase ADP + Ca2+ Phosphatase ATP Pi Pyruvate dehydrogenase active + Pyruvate – CoASH ⊕ PC Acetyl CoA CO2 NAD+ + – NADH ↑ NADH/NAD+ mitocondria – inhibe IDH, ⊕ PC piruvato convierte FIG. 36.3. Regulation of pyruvate dehydrogenase (PDH). A kinase associated with the en oxaloacetato. PDH complex phosphorylates and inactivates the enzyme. , activated by; , inhibited by. 5. CITRATO LIASA, ENZIMA MÁLICA Y G-6-PDH Se convierte en palmitoíl-CoA y se elonga y desatura para formar otras moléculas de acil-CoA, que son convertidas en triacilgliceroles,se empaquetan y se secretan en la sangre como VLDL (+ insulina) 7. COMPLEJO ÁCIDO GRASO SINTASA Bien alimentado =↑ Insulina/Glucagon = INDUCEN GENES ↑[FAS] VPP ↑ INDUCIDO Insulina Malato Dhasa Cito ACC VPP (+ insulina) FIG. 36.4. Regulation of citrate lyase, malic enzyme,G-6PDH, and FAS Lipogenesis y la síntesis del colesterol (+ insulina) Citrate lyase, which provides acetyl-CoA for fatty acid biosynthesis, the enzymes that provide NADPH (malic enzyme, G-6-P-D ), aswell as FAS are inducible ↑. FA, fatty acid 6. ACETIL-COA CARBOXILASA ACC Está activa en el estado de alimentación. Glucose Citrate Insulin B.+ Phosphatase Acetyl CoA Pi + Acetyl CoA carboxylase–P (inactive) Acetyl CoA carboxylase – ADP A.- ATP AMP-activated protein kinase Malonyl CoA + Low energy levels La ACC se regula por activación e inhibición, por A.- fosforilación (mediada por la proteína cinasa activada por AMP) y Palmitate Palmitoyl CoA B.- defosforilación (através de una fosfatasa insulino-estimulada) y por inducción y represión. Figura 36.5. Regulación de la acetil-CoA carboxilasa (ACC) B. Mecanismos que afectan el destino de quilomicrones y VLDL Quilomicrones y VLDL …………. AG y glicerol LPL ↑LP(POSTPRANDIAL) ↓LP(AYUNO ) Capilares Musculo(CARDIACO) ( Km Bajo) ). Capilars Tejido adiposo Km alto ESTADO DE ALIMENTACION Fed state C. Mecanismos que afectan el almacenamiento de triacilglicerol en el tejido adiposo TG Glucose ↑ insulina/glucagon Blood 2.- Glucose Insulin Chylomicrons Remnants 3.- ApoCII activa LPL VLDL LDL DHAP 1.+ TG IDL L P +L Glycerol 3phosphate LPL 3.- Glycerol 1.-↑Sintesis y secreción de LPL FACoA CII FA Liver 2.- ↑N° GLUT 4(Transporte) + FA Adipose cell NO Glicerol quinasa Figura 36.7. Regulación del almacenamiento de (TGs) en el tejido adiposo. II. REGULACIÓN DEL METABOLISMO DE CARBOHIDRATOS Y LÍPIDOS DURANTE EL AYUNO ↓insulina/glucagon A. Mecanismos en el hígado que sirven para mantener las concentraciones de glucosa sanguínea Figura 36.8. Regulación de las enzimas de la degradación de glucógeno en el hígado 1) El glucagon (o epinefrina) se une a su receptor de membrana celular, activando inicialmente una proteína G, que activa la adenil ciclasa. epinefrina) Ocurren en ayuno y producen glucosa para mantener homoestasis de glucosa sanguínea. 2) Como niveles de AMPc se elevan, las subunidades inhibitorias son retiradas de la proteína cinasa A, que ahora fosforila la fosforilasa cinasa . 3) 4) La proteína cinasa AMPcdependiente también fosforila la glucógeno sintasa, inactivando la enzima. 5) La fosforilasa cinasa fosforilada, fosforila la glucógeno fosforilasa (6) La glucógeno fosforilasa fosforilada cataliza la fosforólisis del glucógeno, produciendo glucosa 1fosfato. Estos eventos ocurren durante el ayuno y producen glucosa para mantener una concentración relativamente constante de glucosa sanguínea. Figura 36.9. Regulación de la gluconeogénesis (flechas rojas) y glucólisis (flechas negras) durante el ayuno 5.- La tasa de GK es baja ,por Km alto glucosa y ↓[glucosa] 1.- Las enzimas gluconeogénicas FEpiruvato carboxicinasa, F1,6-BPasa y G 6-Psa se inducen ↑PRECURSORES. 4.- La PFK-1 no muy activa porque su activador [F2,6-BP] es baja 3.-Enzimas de la glucólisis no muy activas. 6.-La piruvato cinasa es inactiva por fosforilación mediada por AMPc. F-2,6-BP, 2.- La F1,6-Basa está activa en el ayuno, el su inhibidor, F 2,6-BP, es baja. B. Mecanismos que afectan la lipólisis en el tejido adiposo en el ayuno HSL, TG Otras hormonas (por ej. la epinefrina, l [ACTH], la hormona del crecimiento) 4.- Hormonesensitive lipase (inactive) Fasted state 3.- Blood Protein kinase A Hormonesensitive lipase– P (active) + La gliceroneogénesis y la resíntesis de triacilgliceroles por el adipocito, regulan la tasa de liberación de los ácidos grasos durante el ayuno. 2.- cAMP + 1.- Low insulin/high glucagon ATP 5.Other lipases FA FA FA Glycerol Adipose cell FA FA FA Glycerol Figura 36.10. Regulación de la lipasa sensible a hormonas (HSL) en el tejido adiposo 1.-Durante el ayuno, la relación glucagon/insulina aumenta haciendo que los niveles de AMPc se eleven. 2.- La proteína cinasa A se activa y fosforila HSL, activando esta enzima. 3.-La HSL-P inicia la movilización del triacilglicerol adiposo retirando un ácido graso (AG). 4.5.- Actúan, entonces, otras lipasas, produciendo ácidos grasos y glicerol. La insulina estimula la fosfatasa que inactiva la HSL en el estado de alimentación. C. Mecanismos que afectan la producción de cuerpos cetónicos por el hígado + + Figura 36.6. Inhibición del transporte de ácidos grasos (AGs) a la mitocondria por la malonilCoA. Enel estado de alimentación, la concentración de malonil-CoA (el sustrato para la síntesis del ácido graso producido por la acetil-CoA carboxilasa) es elevada. Inhibe la carnitina palmitoíl transferasa I (CPTI), evitando el transporte de los ácidos grasos de cadena larga a la mitocondria. Por lo tanto, el sustrato no está disponible para la β-oxidación y la síntesis de los cuerpos cetónicos. Formación y exportación de Cuerpos Cetónicos desde el Hígado Diabetes no tratada dieta estricta ayuno Gluconeogénesis Ciclo de krebs Cetogénesis Acetoacetato y de D-3-Hidroxibutirato en sangre pH sanguíneo provoca ACIDOSIS ó CETOSIS D. Regulación del uso de glucosa y ácidos grasos por el músculo ∆(PDH) = desfosforila ,↑sustratos y ↑(ADP) y la ↑insulina P Pyruvate dehydrogenase inactive ADP – kinase ADP + Ca2+ Phosphatase ATP Pi Pyruvate dehydrogenase active + Pyruvate – CoASH ⊕ PC Acetyl CoA CO2 NAD+ + – NADH ↑ NADH/NAD+ mitocondria – inhibe ISDH, ⊕ PC piruvato convierte FIG. 36.3. Regulation of pyruvate dehydrogenase (PDH). A kinase associated with the en oxaloacetato. PDH complex phosphorylates and inactivates the enzyme. , activated by; , inhibited by. D. Regulación del uso de glucosa y ácidos grasos por el músculo Actividad intensa Glucogeno Muscular y glucosa sanguinea Actividad ligera o reposo Lactato ↓[Ins…= ↓[Glut 4 Acidos grasos Cuerpos cetonicos Glucosa en sangre ADP+Pi glucogenólisis y gluconeogénesis hepáticas ATP CO2 Fosfocreatina ATP Creatina Actividad intensa - CICLO DE CORI - CICLO GLU-ALA Contracción muscular Glicólisis III. LA IMPORTANCIA DE AMP Y FRUCTOSA 2,6-BISFOSFATO Liberación de glucagón ← ↑ Glucogenolisis ↑ Gluconeogenesis ↑ Lipolisis ↓ Glucolisis hepática Glucosa Sanguínea Equilibrio intertisular Ayuno y Alimentación Cortisol, Epinefrina, Noradrenalina ↓AMP (Alostéricos + PKB ) ↑AMP adenil cinasa (2 ADP→ ATP y AMP) (Alostéricos + PKA ) ↑Gluconeogénesis Vs ↓Glucolisis Hepatica PFK-1 ↓Gluconeogénesis Vs ↑Glucolisis Hepatica ▼ PFK-2 = fosforilada ↑[F2,6-BP] x PFK-2 + + F1,6-BPasa ↑ Glucogenogenesis ↑ Sintesis . Ac. Grasos ↑ Sintesis de Triacilglieridos ↑ Glucolisis hepática ANABOLISMO CATABOLISMO ↓[F2,6-BP] ▼ PFK-2 → Liberación de Insulina PFK-2 = No fosforilada PFK-1 F1,6-BPasa Figura 36.8. Regulación de las enzimas de la degradación de glucógeno en el hígado epinefrina) 1) El glucagon (o epinefrina) se une a su receptor de membrana celular, activando inicialmente una proteína G, que activa la adenil ciclasa. 2) Como niveles de AMPc se elevan, las subunidades inhibitorias son retiradas de la proteína cinasa A, que ahora fosforila la fosforilasa cinasa . 3) 4) La proteína cinasa AMPcdependiente también fosforila la glucógeno sintasa, inactivando la enzima. 5) La fosforilasa cinasa fosforilada, fosforila la glucógeno fosforilasa (6) La glucógeno fosforilasa fosforilada cataliza la fosforólisis del glucógeno, produciendo glucosa 1fosfato. Estos eventos ocurren durante el ayuno y producen glucosa para mantener una concentración relativamente constante de glucosa sanguínea. POSPRANDIAL ACTIVA GLUT2 INSULINA GLUCOLISIS GLUCOGENOGENESIS ACTIVA GLUT4 INSULINA GLUCOLISIS BIOSINTESIS DE TRIGLICERIDOS ACTIVA GLUT4 INSULINA GLUCOLISIS NO HAY G6Fasa NO HAY GLUCONEOGENESIS GLUCOGENOGENESIS